Просмотров: 5 784
Справочные материалы для ревматолога. Рекомендации по лечению острого коронарного синдрома. 2012 г.
РЕКОМЕНДАЦИИ ПО ЛЕЧЕНИЮ ОСТРОГОКОРОНАРНОГО СИНДРОМА БЕЗ СТОЙКОГОПОДЪЕМА СЕГМЕНТА ST
Ключевые слова: острый коронарный синдром, ангиопластика, аспирин, бивалирудин, шунтирование, отделение неотложной кардиологии, клопидогрел, диабет, эноксапарин, Европейское общество кардиологов, фондапаринукс, рекомендации, гепарин, инфаркт миокарда без подъема сегмента ST, прасугрел, стент, тикагрелор, тропонин, нестабильная стенокардия.
Таблица 1. Классы рекомендаций
 Таблица 2. Уровни доказательности
Таблица 2. Уровни доказательности
 Сердечно-сосудистые заболевания являются веду-щей причиной смертности в индустриально развитыхстранах. Ожидается, что к 2020 г. они займут первое ме-сто в структуре смертности в развивающихся странах [1].Среди сердечно-сосудистых заболеваний чаще всеговстречается ишемическая болезнь сердца (ИБС), кото-рая характеризуется высокой частотой осложнений, втом числе смерти. Клинические проявления ИБС вклю-чают в себя «немую» ишемию, стабильную стенокардию,нестабильную стенокардию, инфаркт миокарда (ИМ),сердечную недостаточность и внезапную смерть. Больв груди относится к числу основных причин неотлож-ных госпитализаций в Европе. Диагностика ОКС у па-циентов с болью в груди может быть достаточно труд-ной задачей, особенно при отсутствии характерныхсимптомов или электрокардиографических изменений.Несмотря на современное лечение, смертность, часто-та ИМ и повторных госпитализаций у пациентов сОКС остаются высокими.Установлено, что различные клинические вариантыОКС имеют общие механизмы развития. Результаты ауто-псийных и клинических исследований свидетель-ствуют о том, что в основе большинства случаев ОКС ле-жат разрыв или эрозия атеросклеротической бляшки,которые сопровождаются тромбообразованием и дис-тальной эмболизацией и приводят к ухудшению пер-фузии миокарда.ОКС — это угрожающее жизни атеротромботическоесостояние, поэтому разработаны критерии стратифи-кации риска, которые помогают врачам своевременновыбрать тактику индивидуализированного лечения, включающего в себя применение различных лекарст-венных средств, а также реваскуляризацию коронар-ных артерий. Ведущим симптомом является боль в гру-ди, однако ОКС классифицируют на основании изме-нений на ЭКГ. Выделают два варианта этого синдрома:1. Пациенты с острой болью в груди и персисти-рующим (>20 мин) подъемом сегмента ST — ОКС сподъемом сегмента SТ, который обычно отражает пол-ную окклюзию коронарной артерии. У большинства па-циентов формируется ИМ с подъемом сегмента ST. Пер-вичная цель лечения — быстрая, полная и стойкая ре-перфузия путем ангиопластики или тромболизиса.2. Пациенты с острой болью в груди без стойко-го подъема сегмента ST. У таких пациентов наблюдаютстойкую или преходящую депрессию сегмента ST, ин-версию зубца Т, сглаживание зубца Т, псевдонормали-зацию зубца Т, однако изменения на ЭКГ могут и отсут-ствовать. Тактика ведения пациентов предполагает ку-пирование ишемии и симптомов, мониторирование ЭКГи повторное определение маркеров некроза миокар-да. В зависимости от результатов измерения уровня тро-понинов выделяют ИМ без подъема сегмента ST и не-стабильную стенокардию (рис. 1). У части пациентовпроводимое исследование позволяет исключить ИБСкак причину боли в сердце.Ведение пациентов с ОКС с подъемом сегмента STрассматривается в соответствующих рекомендациях Ев-ропейского общества кардиологов [2]. В настоящем до-кументе обсуждается лечение пациентов с предпола-гаемым ОКС без подъема сегмента ST. Он заменяет до-кумент, впервые опубликованный в 2000 г. и изменен-ный в 2002 и 2007 гг. [3]. В рекомендации включенырезультаты всех исследований, опубликованных в ре-цензируемых журналах до мая 2011 г.Уровень доказательства А в настоящем документе —это результаты рандомизированных двойных слепых ис-следований адекватного размера, предполагавшихсовременную базовую терапию и анализ конечныхточек, не подверженных системной ошибке, таких каксмерть и ИМ. Результаты рандомизированных, но недвойных слепых исследований и/или исследований,предполагавших анализ менее «твердых» конечных то-чек (например, рефрактерной ишемии или необходи-мости в реваскуляризации), считали менее доказатель-ными. При наличии только небольших исследованийиспользовали результаты мета-анализа. Однако дажесамые крупные контролируемые исследования неохватывают все аспекты реальной жизни. В связи с этимнекоторые рекомендации основываются на результа-тах анализа подгрупп в более крупных исследованияхпри отсутствии соответствующих независимых иссле-дований, обладающих достаточной статистическойсилой.
Эпидемиология и естественное течение
Результаты регистров показали, что ОКС без подъе-ма сегмента ST встречается чаще, чем ОКС с подъемомсегмента ST [4]. Ежегодная заболеваемость составляет примерно 3 на 1000 населения, хотя она отличается вразных странах [5]. Госпитальная смертность у пациен-тов с ИМ с подъемом сегмента ST выше, чем у больныхОКС без подъема сегмента ST (7% и 3-5%, соответствен-но), однако через 6 мес смертность сопоставима придвух состояниях (12% и 13%, соответственно) [4,6,7].В отдаленном периоде смертность у пациентов с ОКСбез подъема сегмента ST превышала таковую у паци-ентов с ОКС с подъемом сегмента ST: например, через4 года она была в 2 раза выше [8]. Различия естествен-ного течения вариантов ОКС могут отражать особенно-сти пациентов: в частности, больные с ОКС без подъе-ма сегмента ST обычно старше, у них чаще встречают-ся сопутствующие заболевания, особенно сахарный диа-бет и почечная недостаточность.Результаты эпидемиологических исследований сви-детельствуют о том, что пациенты с ОКС без подъемасегмента ST нуждаются в интенсивном лечении нетолько в остром, но и в отдаленном периоде. Дополни-тельные данные об эпидемиологии и естественном тече-нии ОКС без подъема сегмента ST содержатся в преды-дущих рекомендациях [3] и учебнике Европейского об-щества кардиологов по сердечно-сосудистой медици-не [9].
Рис. 1. Спектр ОКС
Сердечно-сосудистые заболевания являются веду-щей причиной смертности в индустриально развитыхстранах. Ожидается, что к 2020 г. они займут первое ме-сто в структуре смертности в развивающихся странах [1].Среди сердечно-сосудистых заболеваний чаще всеговстречается ишемическая болезнь сердца (ИБС), кото-рая характеризуется высокой частотой осложнений, втом числе смерти. Клинические проявления ИБС вклю-чают в себя «немую» ишемию, стабильную стенокардию,нестабильную стенокардию, инфаркт миокарда (ИМ),сердечную недостаточность и внезапную смерть. Больв груди относится к числу основных причин неотлож-ных госпитализаций в Европе. Диагностика ОКС у па-циентов с болью в груди может быть достаточно труд-ной задачей, особенно при отсутствии характерныхсимптомов или электрокардиографических изменений.Несмотря на современное лечение, смертность, часто-та ИМ и повторных госпитализаций у пациентов сОКС остаются высокими.Установлено, что различные клинические вариантыОКС имеют общие механизмы развития. Результаты ауто-псийных и клинических исследований свидетель-ствуют о том, что в основе большинства случаев ОКС ле-жат разрыв или эрозия атеросклеротической бляшки,которые сопровождаются тромбообразованием и дис-тальной эмболизацией и приводят к ухудшению пер-фузии миокарда.ОКС — это угрожающее жизни атеротромботическоесостояние, поэтому разработаны критерии стратифи-кации риска, которые помогают врачам своевременновыбрать тактику индивидуализированного лечения, включающего в себя применение различных лекарст-венных средств, а также реваскуляризацию коронар-ных артерий. Ведущим симптомом является боль в гру-ди, однако ОКС классифицируют на основании изме-нений на ЭКГ. Выделают два варианта этого синдрома:1. Пациенты с острой болью в груди и персисти-рующим (>20 мин) подъемом сегмента ST — ОКС сподъемом сегмента SТ, который обычно отражает пол-ную окклюзию коронарной артерии. У большинства па-циентов формируется ИМ с подъемом сегмента ST. Пер-вичная цель лечения — быстрая, полная и стойкая ре-перфузия путем ангиопластики или тромболизиса.2. Пациенты с острой болью в груди без стойко-го подъема сегмента ST. У таких пациентов наблюдаютстойкую или преходящую депрессию сегмента ST, ин-версию зубца Т, сглаживание зубца Т, псевдонормали-зацию зубца Т, однако изменения на ЭКГ могут и отсут-ствовать. Тактика ведения пациентов предполагает ку-пирование ишемии и симптомов, мониторирование ЭКГи повторное определение маркеров некроза миокар-да. В зависимости от результатов измерения уровня тро-понинов выделяют ИМ без подъема сегмента ST и не-стабильную стенокардию (рис. 1). У части пациентовпроводимое исследование позволяет исключить ИБСкак причину боли в сердце.Ведение пациентов с ОКС с подъемом сегмента STрассматривается в соответствующих рекомендациях Ев-ропейского общества кардиологов [2]. В настоящем до-кументе обсуждается лечение пациентов с предпола-гаемым ОКС без подъема сегмента ST. Он заменяет до-кумент, впервые опубликованный в 2000 г. и изменен-ный в 2002 и 2007 гг. [3]. В рекомендации включенырезультаты всех исследований, опубликованных в ре-цензируемых журналах до мая 2011 г.Уровень доказательства А в настоящем документе —это результаты рандомизированных двойных слепых ис-следований адекватного размера, предполагавшихсовременную базовую терапию и анализ конечныхточек, не подверженных системной ошибке, таких каксмерть и ИМ. Результаты рандомизированных, но недвойных слепых исследований и/или исследований,предполагавших анализ менее «твердых» конечных то-чек (например, рефрактерной ишемии или необходи-мости в реваскуляризации), считали менее доказатель-ными. При наличии только небольших исследованийиспользовали результаты мета-анализа. Однако дажесамые крупные контролируемые исследования неохватывают все аспекты реальной жизни. В связи с этимнекоторые рекомендации основываются на результа-тах анализа подгрупп в более крупных исследованияхпри отсутствии соответствующих независимых иссле-дований, обладающих достаточной статистическойсилой.
Эпидемиология и естественное течение
Результаты регистров показали, что ОКС без подъе-ма сегмента ST встречается чаще, чем ОКС с подъемомсегмента ST [4]. Ежегодная заболеваемость составляет примерно 3 на 1000 населения, хотя она отличается вразных странах [5]. Госпитальная смертность у пациен-тов с ИМ с подъемом сегмента ST выше, чем у больныхОКС без подъема сегмента ST (7% и 3-5%, соответствен-но), однако через 6 мес смертность сопоставима придвух состояниях (12% и 13%, соответственно) [4,6,7].В отдаленном периоде смертность у пациентов с ОКСбез подъема сегмента ST превышала таковую у паци-ентов с ОКС с подъемом сегмента ST: например, через4 года она была в 2 раза выше [8]. Различия естествен-ного течения вариантов ОКС могут отражать особенно-сти пациентов: в частности, больные с ОКС без подъе-ма сегмента ST обычно старше, у них чаще встречают-ся сопутствующие заболевания, особенно сахарный диа-бет и почечная недостаточность.Результаты эпидемиологических исследований сви-детельствуют о том, что пациенты с ОКС без подъемасегмента ST нуждаются в интенсивном лечении нетолько в остром, но и в отдаленном периоде. Дополни-тельные данные об эпидемиологии и естественном тече-нии ОКС без подъема сегмента ST содержатся в преды-дущих рекомендациях [3] и учебнике Европейского об-щества кардиологов по сердечно-сосудистой медици-не [9].
Рис. 1. Спектр ОКС
 Патофизиология
ОКС — это угрожающее жизни проявление атеросклероза. Оно обычно развивается в результате острого тром-боза на фоне разрыва или эрозии атеросклеротическойбляшки в коронарной артерии±вазоконстрикции, ко-торые приводят к внезапному ухудшению коронарно-го кровотока. Ключевое значение в патогенезе разры-ва бляшки имеет воспаление. В редких случаях ОКС име-ет неатеросклеротическое происхождение и можетбыть обусловлен артериитом, травмой, расслоениемстенки артерии, тромбоэмболией, врожденными по-роками, употреблением кокаина или осложняет кате-теризацию сердца. Для адекватного лечения необхо-димо понимать ключевые концепции патогенеза ОКС,в том числе уязвимость бляшки, коронарный тромбоз,уязвимость пациента, эндотелиальную дисфункцию,ускоренный атеротромбоз, вторичные механизмы ОКСбез подъема сегмента ST и повреждение миокарда.Предсказать развитие ОКС позволяет наличие неболь-ших бляшек с тонкой оболочкой, крупных бляшек илизначительного сужения просвета сосуда [10]. Этот во-прос более подробно рассматривается в предыдущихрекомендациях [3] и учебнике Европейского обществакардиологов по сердечно-сосудистой медицине [9].
Диагноз
Ведущим симптомом ОКС обычно является боль вгруди. Наличие ОКС без подъема сегмента ST подтвер-ждается с помощью ЭКГ (отсутствие стойкого подъемасегмента ST). ИМ без подъема сегмента ST и нестабиль-ную стенокардию дифференцируют на основанииуровней биомаркеров (тропонинов). Эхокардиографиюи сцинтиграфию миокарда используют для исключениядругих заболеваний. Методы диагностики и стратифи-кации риска тесно связаны друг с другом.
Клиническая картина
Клинические проявления ОКС без подъема сегмента ST включают в себя различные симптомы. Тради-ционно выделяют несколько клинических вариантовОКС:
• длительная (≥20 мин) ангинозная боль в покое;
• впервые возникшая стенокардия II-III функциональ-ного класса по классификации Канадского сердечно-сосудистого общества [11];
• недавнее прогрессирование ранее стабильнойстенокардии, по крайней мере до III функционально-го класса (стенокардия crescendo);
• постинфарктная стенокардия.Длительный приступ боли в области сердца наблю-дается у 80% пациентов, а впервые возникшая стено-кардия или прогрессирующая стенокардия — у 20% [12].Типичный клинический симптом ОКС без подъемасегмента ST — боль или тяжесть за грудиной (груднаяжаба), иррадиирующая в левую руку, шею или челюсть,которая может быть интермиттирующей (обычно про-должается несколько мин) или стойкой. Боль может со-провождаться потливостью, тошнотой, болью в живо-те, одышкой и обмороком. Нередко отмечаются атипич-ные проявления ОКС, такие как боль в эпигастральнойобласти, диспепсия, кинжальная боль в груди, плевраль-ная боль или нарастающая одышка. Атипичные симп-томы чаще отмечаются у пациентов пожилого возрас-та (≥75 лет), больных сахарным диабетом, хроническойпочечной недостаточностью или деменцией [13,14]. Отсутствие боли в груди является причиной несвоевремен-ной диагностики и неадекватного лечения [15]. Труд-ности диагностики обычно возникают в тех случаях, ко-гда ЭКГ нормальная или практически нормальная,или, наоборот, если на исходной ЭКГ имеются измене-ния, связанные с нарушением внутрижелудочковой про-водимости или гипертрофией левого желудочка [16].Заподозрить диагноз ИБС помогают некоторые осо-бенности клинической картины. Появление симптомовпри физической нагрузке или их уменьшение в покоеили после приема нитратов подтверждает диагнозишемия миокарда. Важное значение имеет выявлениефакторов, провоцирующих развитие ОКС без подъе-ма сегмента ST, таких как анемия, инфекция, воспале-ние, лихорадка и метаболические или эндокринные за-болевания (особенно щитовидной железы).При наличии клинических симптомов некоторыефакторы риска повышают вероятность ИБС и, соответ-ственно, ОКС без подъема сегмента ST. К ним относят-ся пожилой возраст, мужской пол, отягощенный семей-ный анамнез, а также наличие атеросклероза некоро-нарных артерий, в частности периферических и сонных.Важное диагностическое значение имеет наличие дру-гих факторов риска, особенно сахарного диабета и по-чечной недостаточности, и проявлений ИБС в анамне-зе [перенесенный ИМ, чрескожное коронарное вмеша-тельство (ЧКВ) или коронарное шунтирование (КШ) ванамнезе).
Методы диагностики
Физическое обследование
При физическом обследовании изменения часто отсутствуют. Основанием для диагностики и лечениямогут быть симптомы сердечной недостаточности илинарушения гемодинамики. Важная цель физическогообследования — исключение несердечных причинболи в сердце и неишемических заболеваний сердца(например, тромбоэмболии легочной артерии, расслое-ния стенки аорты, перикардита, порока клапана серд-ца) или экстракардиальных причин, таких как остроезаболевание легких (пневмоторакс, пневмония илиплевральный выпот). Разница АД на верхних и нижнихконечностях, аритмичный пульс, шумы в сердце, шумтрения перикарда, боль при пальпации и пальпируе-мое образование в брюшной полости позволяют запо-дозрить другие диагнозы. Некоторые физические дан-ные, такие как бледность, потливость или тремор,указывают на анемию и тиреотоксикоз, которые могутспровоцировать развитие ОКС без подъема сегментаST.
Электрокардиография
ЭКГ в 12 отведениях — это первый метод диагности-ки, который используют при подозрении на ОКС безподъема сегмента ST. ЭКГ следует зарегистрировать втечение первых 10 мин после поступления в при-емное отделение или приезда машины скорой помо-щи. ЭКГ должен немедленно проанализировать опыт-ный врач [17]. Для ОКС без подъема сегмента ST харак-терны депрессия или преходящий подъем сегмента STи/или изменения зубца Т [6,18]. Наличие стойкогоподъема сегмента ST (≥20 мин) указывает на наличиеИМ с подъемом сегмента ST, тактика лечения которо-го отличается [2]. Если исходная ЭКГ нормальная илирезультаты ее неоднозначные, то необходимо регистри-ровать ЭКГ в динамике [18]. Важное значение имеетсравнение полученных данных с предыдущими ЭКГ, осо-бенно при наличии заболеваний сердца, таких как ги-пертрофия левого желудочка или перенесенный ИМ.ЭКГ следует зарегистрировать повторно по крайней меречерез 3 ч, 6-9 ч и 24 ч после обращения к врачу и не-медленно при рецидиве боли в груди или симптомов.Рекомендуется также зарегистрировать ЭКГ перед вы-пиской.Необходимо учитывать, что нормальная ЭКГ неисключает диагноз ОКС без подъема сегмента ST. В част-ности, при ишемии в бассейне огибающей артерии илиизолированной ишемии правого желудочка измененияна ЭКГ в 12 отведениях часто отсутствуют, однако онимогут быть выявлены в отведениях V7–V9 и отведенияхV3R и V4R, соответственно [18]. При эпизодах ишемиимиокарда иногда наблюдается преходящая блокада но-жек пучка Гиса.Стандартная ЭКГ в покое неадекватно отражает ди-намический характер коронарного тромбоза и ишемиимиокарда. Почти 2/3 эпизодов ишемии в нестабиль-ную фазу клинически бессимптомные и не регистри-руются с помощью стандартной ЭКГ. Соответственно,важное диагностическое значение имеет мониториро-вание ЭКГ в 12 отведениях.
Биомаркеры
Сердечные тропонины играют центральную роль вдиагностике и стратификации риска и позволяют так-же дифференцировать ИМ без подъема сегмента ST инестабильную стенокардию. По специфичности и чув-ствительности тропонины превосходят традиционныесердечные ферменты, такие как креатинкиназа (КК),МВ-фракция КК, и миоглобин. Повышение уровня сер-дечных тропонинов отражает повреждение кардиомио-цитов, которое при ОКС без подъема сегмента ST мо-жет быть связано с дистальной эмболизацией тромбо-цитарными тромбами, образующимися в области раз-рыва или эрозии бляшки. Соответственно, тропонинможно рассматривать как суррогатный маркер актив-ного тромбообразования [19]. При наличии ишемиимиокарда (боль в груди, изменения на ЭКГ и появле-ние асинергии стенки сердца) увеличение уровня тро-понина указывает на ИМ [18].У пациентов с ИМ уровень тропонина начинает уве-личиваться в течение примерно 4 ч после появлениясимптомов. Содержание тропонина может оставатьсяповышенным в течение 2 нед вследствие протеолизасократительного аппарата. При ОКС без подъема сег-мента ST уровень тропонина обычно нормализуется че-рез 48-72 ч. Тропонины T и I не имеют фундаменталь-ных отличий. Неоднозначные результаты исследованиймогут быть связаны с особенностями критериев включе-ния, вариабельностью сроков взятия крови и примене-ния различных методов исследования.В клинической практике необходимо использоватьметоды, позволяющие надежно исключить (предска-зательное значение отрицательного результата) и пра-вильно диагностировать ОКС (предсказательное значе-ние положительного результата). Диагноз ИМ устанав-ливают, если уровень сердечного тропонина превышает 99-й перцентиль нормального диапазона. Коэффи-циент вариации метода должен составлять ≤10% [18].Адекватность такого подхода была установлена в не-скольких исследованиях [20,21]. Первые методы ана-лиза тропонинов Т и I были недостаточно точными. Не-давно были разработаны высоко- или ультрачувстви-тельные методы (пороговый уровень в 10-100 разниже), обладающие необходимой точностью. Соответ-ственно, сегодня ИМ удается диагностировать чаще ираньше [20,21]. Преимущество новых методов анали-за, особенно в раннюю фазу, было установлено в про-спективных исследованиях [20,21]. Предсказатель-ное значение отрицательного результата при однократ-ном измерении при поступлении составляет ≥95% и покрайней мере такое же высокое как при анализе уров-ней тропонинов в динамике с помощью старых мето-дов. Уровень тропонина может быть нормальнымтолько на очень ранней стадии ИМ. Если провести по-вторное исследование в течение 3 ч после появлениясимптомов, то чувствительность диагностики ИМ при-ближается к 100% [22,23].Благодаря увеличению чувствительности анализанизкие уровни тропонина сегодня могут быть выявле-ны у многих пациентов со стабильной стенокардией[24,25] и здоровых людей [26]. Механизмы увеличе-ния уровня тропонина у таких пациентов не установле-ны, однако наличие тропонина в крови указывает на не-благоприятный прогноз [24]. Чтобы обеспечить специ-фичность диагностики ИМ, необходимо дифференци-ровать хроническое и острое повышение уровня тро-понина. Для этого имеет значение степень измененияпоказателя. Клинически значимое повышение уровнятропонина по сравнению с исходным показателемпродолжает дискутироваться. Пограничные измененияуровня тропонина должны превышать естественную ва-риабельность этого показателя, которую необходимоопределить для каждого метода [27].Другие угрожающие жизни состояния, сопровождаю-щиеся болью в груди, такие как расслаивающая анев-ризма аорты или тромбоэмболия легочной артерии, так-же могут привести к увеличению уровней тропонинов,поэтому их необходимо учитывать при проведении диф-ференциального диагноза. Увеличение концентрациисердечных тропонинов наблюдается также при повреж-дении миокарда некоронарного происхождения(табл. 3). Эти данные отражают чувствительность мар-кера в диагностике поражения кардиомиоцитов, поэто-му их не следует считать ложноположительными. Лож-ноположительные результаты анализа уровней тропо-нинов регистрировали при поражении скелетных мышцили хронической почечной недостаточности. Уровеньтропонинов часто повышается при концентрации сы-вороточного креатинина ≥2,5 мг/дл (221 мкмоль/л)при отсутствии доказанного ОКС; такое повышениетакже ассоциируется с неблагоприятным прогнозом[28,29].
Таблица 3. Возможные некоронарные причиныповышения уровня тропонина (полужирнымшрифтом выделены заболевания, которыеимеют важное значение с дифференци-ально-диагностической точки зрения)
Патофизиология
ОКС — это угрожающее жизни проявление атеросклероза. Оно обычно развивается в результате острого тром-боза на фоне разрыва или эрозии атеросклеротическойбляшки в коронарной артерии±вазоконстрикции, ко-торые приводят к внезапному ухудшению коронарно-го кровотока. Ключевое значение в патогенезе разры-ва бляшки имеет воспаление. В редких случаях ОКС име-ет неатеросклеротическое происхождение и можетбыть обусловлен артериитом, травмой, расслоениемстенки артерии, тромбоэмболией, врожденными по-роками, употреблением кокаина или осложняет кате-теризацию сердца. Для адекватного лечения необхо-димо понимать ключевые концепции патогенеза ОКС,в том числе уязвимость бляшки, коронарный тромбоз,уязвимость пациента, эндотелиальную дисфункцию,ускоренный атеротромбоз, вторичные механизмы ОКСбез подъема сегмента ST и повреждение миокарда.Предсказать развитие ОКС позволяет наличие неболь-ших бляшек с тонкой оболочкой, крупных бляшек илизначительного сужения просвета сосуда [10]. Этот во-прос более подробно рассматривается в предыдущихрекомендациях [3] и учебнике Европейского обществакардиологов по сердечно-сосудистой медицине [9].
Диагноз
Ведущим симптомом ОКС обычно является боль вгруди. Наличие ОКС без подъема сегмента ST подтвер-ждается с помощью ЭКГ (отсутствие стойкого подъемасегмента ST). ИМ без подъема сегмента ST и нестабиль-ную стенокардию дифференцируют на основанииуровней биомаркеров (тропонинов). Эхокардиографиюи сцинтиграфию миокарда используют для исключениядругих заболеваний. Методы диагностики и стратифи-кации риска тесно связаны друг с другом.
Клиническая картина
Клинические проявления ОКС без подъема сегмента ST включают в себя различные симптомы. Тради-ционно выделяют несколько клинических вариантовОКС:
• длительная (≥20 мин) ангинозная боль в покое;
• впервые возникшая стенокардия II-III функциональ-ного класса по классификации Канадского сердечно-сосудистого общества [11];
• недавнее прогрессирование ранее стабильнойстенокардии, по крайней мере до III функционально-го класса (стенокардия crescendo);
• постинфарктная стенокардия.Длительный приступ боли в области сердца наблю-дается у 80% пациентов, а впервые возникшая стено-кардия или прогрессирующая стенокардия — у 20% [12].Типичный клинический симптом ОКС без подъемасегмента ST — боль или тяжесть за грудиной (груднаяжаба), иррадиирующая в левую руку, шею или челюсть,которая может быть интермиттирующей (обычно про-должается несколько мин) или стойкой. Боль может со-провождаться потливостью, тошнотой, болью в живо-те, одышкой и обмороком. Нередко отмечаются атипич-ные проявления ОКС, такие как боль в эпигастральнойобласти, диспепсия, кинжальная боль в груди, плевраль-ная боль или нарастающая одышка. Атипичные симп-томы чаще отмечаются у пациентов пожилого возрас-та (≥75 лет), больных сахарным диабетом, хроническойпочечной недостаточностью или деменцией [13,14]. Отсутствие боли в груди является причиной несвоевремен-ной диагностики и неадекватного лечения [15]. Труд-ности диагностики обычно возникают в тех случаях, ко-гда ЭКГ нормальная или практически нормальная,или, наоборот, если на исходной ЭКГ имеются измене-ния, связанные с нарушением внутрижелудочковой про-водимости или гипертрофией левого желудочка [16].Заподозрить диагноз ИБС помогают некоторые осо-бенности клинической картины. Появление симптомовпри физической нагрузке или их уменьшение в покоеили после приема нитратов подтверждает диагнозишемия миокарда. Важное значение имеет выявлениефакторов, провоцирующих развитие ОКС без подъе-ма сегмента ST, таких как анемия, инфекция, воспале-ние, лихорадка и метаболические или эндокринные за-болевания (особенно щитовидной железы).При наличии клинических симптомов некоторыефакторы риска повышают вероятность ИБС и, соответ-ственно, ОКС без подъема сегмента ST. К ним относят-ся пожилой возраст, мужской пол, отягощенный семей-ный анамнез, а также наличие атеросклероза некоро-нарных артерий, в частности периферических и сонных.Важное диагностическое значение имеет наличие дру-гих факторов риска, особенно сахарного диабета и по-чечной недостаточности, и проявлений ИБС в анамне-зе [перенесенный ИМ, чрескожное коронарное вмеша-тельство (ЧКВ) или коронарное шунтирование (КШ) ванамнезе).
Методы диагностики
Физическое обследование
При физическом обследовании изменения часто отсутствуют. Основанием для диагностики и лечениямогут быть симптомы сердечной недостаточности илинарушения гемодинамики. Важная цель физическогообследования — исключение несердечных причинболи в сердце и неишемических заболеваний сердца(например, тромбоэмболии легочной артерии, расслое-ния стенки аорты, перикардита, порока клапана серд-ца) или экстракардиальных причин, таких как остроезаболевание легких (пневмоторакс, пневмония илиплевральный выпот). Разница АД на верхних и нижнихконечностях, аритмичный пульс, шумы в сердце, шумтрения перикарда, боль при пальпации и пальпируе-мое образование в брюшной полости позволяют запо-дозрить другие диагнозы. Некоторые физические дан-ные, такие как бледность, потливость или тремор,указывают на анемию и тиреотоксикоз, которые могутспровоцировать развитие ОКС без подъема сегментаST.
Электрокардиография
ЭКГ в 12 отведениях — это первый метод диагности-ки, который используют при подозрении на ОКС безподъема сегмента ST. ЭКГ следует зарегистрировать втечение первых 10 мин после поступления в при-емное отделение или приезда машины скорой помо-щи. ЭКГ должен немедленно проанализировать опыт-ный врач [17]. Для ОКС без подъема сегмента ST харак-терны депрессия или преходящий подъем сегмента STи/или изменения зубца Т [6,18]. Наличие стойкогоподъема сегмента ST (≥20 мин) указывает на наличиеИМ с подъемом сегмента ST, тактика лечения которо-го отличается [2]. Если исходная ЭКГ нормальная илирезультаты ее неоднозначные, то необходимо регистри-ровать ЭКГ в динамике [18]. Важное значение имеетсравнение полученных данных с предыдущими ЭКГ, осо-бенно при наличии заболеваний сердца, таких как ги-пертрофия левого желудочка или перенесенный ИМ.ЭКГ следует зарегистрировать повторно по крайней меречерез 3 ч, 6-9 ч и 24 ч после обращения к врачу и не-медленно при рецидиве боли в груди или симптомов.Рекомендуется также зарегистрировать ЭКГ перед вы-пиской.Необходимо учитывать, что нормальная ЭКГ неисключает диагноз ОКС без подъема сегмента ST. В част-ности, при ишемии в бассейне огибающей артерии илиизолированной ишемии правого желудочка измененияна ЭКГ в 12 отведениях часто отсутствуют, однако онимогут быть выявлены в отведениях V7–V9 и отведенияхV3R и V4R, соответственно [18]. При эпизодах ишемиимиокарда иногда наблюдается преходящая блокада но-жек пучка Гиса.Стандартная ЭКГ в покое неадекватно отражает ди-намический характер коронарного тромбоза и ишемиимиокарда. Почти 2/3 эпизодов ишемии в нестабиль-ную фазу клинически бессимптомные и не регистри-руются с помощью стандартной ЭКГ. Соответственно,важное диагностическое значение имеет мониториро-вание ЭКГ в 12 отведениях.
Биомаркеры
Сердечные тропонины играют центральную роль вдиагностике и стратификации риска и позволяют так-же дифференцировать ИМ без подъема сегмента ST инестабильную стенокардию. По специфичности и чув-ствительности тропонины превосходят традиционныесердечные ферменты, такие как креатинкиназа (КК),МВ-фракция КК, и миоглобин. Повышение уровня сер-дечных тропонинов отражает повреждение кардиомио-цитов, которое при ОКС без подъема сегмента ST мо-жет быть связано с дистальной эмболизацией тромбо-цитарными тромбами, образующимися в области раз-рыва или эрозии бляшки. Соответственно, тропонинможно рассматривать как суррогатный маркер актив-ного тромбообразования [19]. При наличии ишемиимиокарда (боль в груди, изменения на ЭКГ и появле-ние асинергии стенки сердца) увеличение уровня тро-понина указывает на ИМ [18].У пациентов с ИМ уровень тропонина начинает уве-личиваться в течение примерно 4 ч после появлениясимптомов. Содержание тропонина может оставатьсяповышенным в течение 2 нед вследствие протеолизасократительного аппарата. При ОКС без подъема сег-мента ST уровень тропонина обычно нормализуется че-рез 48-72 ч. Тропонины T и I не имеют фундаменталь-ных отличий. Неоднозначные результаты исследованиймогут быть связаны с особенностями критериев включе-ния, вариабельностью сроков взятия крови и примене-ния различных методов исследования.В клинической практике необходимо использоватьметоды, позволяющие надежно исключить (предска-зательное значение отрицательного результата) и пра-вильно диагностировать ОКС (предсказательное значе-ние положительного результата). Диагноз ИМ устанав-ливают, если уровень сердечного тропонина превышает 99-й перцентиль нормального диапазона. Коэффи-циент вариации метода должен составлять ≤10% [18].Адекватность такого подхода была установлена в не-скольких исследованиях [20,21]. Первые методы ана-лиза тропонинов Т и I были недостаточно точными. Не-давно были разработаны высоко- или ультрачувстви-тельные методы (пороговый уровень в 10-100 разниже), обладающие необходимой точностью. Соответ-ственно, сегодня ИМ удается диагностировать чаще ираньше [20,21]. Преимущество новых методов анали-за, особенно в раннюю фазу, было установлено в про-спективных исследованиях [20,21]. Предсказатель-ное значение отрицательного результата при однократ-ном измерении при поступлении составляет ≥95% и покрайней мере такое же высокое как при анализе уров-ней тропонинов в динамике с помощью старых мето-дов. Уровень тропонина может быть нормальнымтолько на очень ранней стадии ИМ. Если провести по-вторное исследование в течение 3 ч после появлениясимптомов, то чувствительность диагностики ИМ при-ближается к 100% [22,23].Благодаря увеличению чувствительности анализанизкие уровни тропонина сегодня могут быть выявле-ны у многих пациентов со стабильной стенокардией[24,25] и здоровых людей [26]. Механизмы увеличе-ния уровня тропонина у таких пациентов не установле-ны, однако наличие тропонина в крови указывает на не-благоприятный прогноз [24]. Чтобы обеспечить специ-фичность диагностики ИМ, необходимо дифференци-ровать хроническое и острое повышение уровня тро-понина. Для этого имеет значение степень измененияпоказателя. Клинически значимое повышение уровнятропонина по сравнению с исходным показателемпродолжает дискутироваться. Пограничные измененияуровня тропонина должны превышать естественную ва-риабельность этого показателя, которую необходимоопределить для каждого метода [27].Другие угрожающие жизни состояния, сопровождаю-щиеся болью в груди, такие как расслаивающая анев-ризма аорты или тромбоэмболия легочной артерии, так-же могут привести к увеличению уровней тропонинов,поэтому их необходимо учитывать при проведении диф-ференциального диагноза. Увеличение концентрациисердечных тропонинов наблюдается также при повреж-дении миокарда некоронарного происхождения(табл. 3). Эти данные отражают чувствительность мар-кера в диагностике поражения кардиомиоцитов, поэто-му их не следует считать ложноположительными. Лож-ноположительные результаты анализа уровней тропо-нинов регистрировали при поражении скелетных мышцили хронической почечной недостаточности. Уровеньтропонинов часто повышается при концентрации сы-вороточного креатинина ≥2,5 мг/дл (221 мкмоль/л)при отсутствии доказанного ОКС; такое повышениетакже ассоциируется с неблагоприятным прогнозом[28,29].
Таблица 3. Возможные некоронарные причиныповышения уровня тропонина (полужирнымшрифтом выделены заболевания, которыеимеют важное значение с дифференци-ально-диагностической точки зрения)
 Определение уровней биомаркеров у постели больногоДиагноз ОКС без подъема сегмента ST следует уста-новить как можно быстрее, чтобы назначить адекват-ное лечение. Экспресс-методы позволяют измеритьуровни биомаркеров в минимальные сроки [30]. Их сле-дует внедрять в тех случаях, когда в центральной лабо-ратории не удается выполнить это исследование втечение 60 мин [31]. Для интерпретации результатов те-ста не требуются специальные навыки или длительноеобучение. Соответственно, исследование могут вы-полнить различные медицинские работники. Однакорезультаты этих качественных тестов анализируются ви-зуально, что отражается на полученных данных. Суще-ствуют также оптические устройства, позволяющиепровести количественный анализ. Тесты обычно надеж-ны, если они положительные. Однако если диагноз не-стабильная ИБС остается вероятным, то исследованиеследует повторить в динамике, а также определить уров-ни тропонинов в сертифицированной лаборатории. Не-давно была показана возможность выделения пациентов низкого риска с помощью экспресс-алгоритма (2 ч),предполагающего применение экспресс-метода из-мерения уровня тропонинов, индекса риска и ЭКГ[32].
Визуализирующие методы
Неинвазивные методыСреди неинвазивных методов в острую фазу чащевсего проводят эхокардиографию в связи с доступностьюметода. Систолическая функция левого желудочка — этоважный прогностический показатель у пациентов сИБС, который можно легко и точно измерить с помо-щью эхокардиографии. Опытный специалист может вы-явить преходящую гипокинезию или акинезию сегмен-тов левого желудочка во время ишемии. Кроме того, ме-тод позволяет дифференцировать расслоение стенкиаорты, тромбоэмболию легочной артерии, аортальныйстеноз, гипертрофическую кардиомиопатию или пери-кардиальный выпот [33]. В связи с этим эхокардиогра-фию в отделениях интенсивной терапии следует про-водить всем пациентам.Если ЭКГ в 12 отведениях не информативна, ауровни сердечных биомаркеров у пациентов с предпо-лагаемым ОКС нормальные, может быть выполненасцинтиграфия миокарда с нагрузкой при условии от-сутствия боли в сердце. В различных исследованиях при-меняли также стресс-эхокардиографию, которая харак-теризовалась высоким предсказательным значениемотрицательного результата [34].Магнитно-резонансная томография (МРТ) сердцапозволяет одновременно оценить функцию и перфу-зию миокарда и выявить рубцовые изменения, одна-ко этот метод исследования пока малодоступен. В раз-личных исследованиях была показана информативностьМРТ в диагностике ОКС [35]. Кроме того, этот метод ис-пользуют для оценки жизнеспособности миокарда и ди-агностики миокардита.Показана также информативность перфузионнойсцинтиграфии миокарда, однако этот метод также не-достаточно широко доступен в круглосуточном режи-ме. Сцинтиграфия миокарда в покое была полезной наначальном этапе обследования пациентов с болью в гру-ди, у которых отсутствуют изменения на ЭКГ, или при-знаки сохраняющейся ишемии, или ИМ [36]. Проба снагрузкой имеет преимущество, так как она позволяетвыявить индуцируемую ишемию.Мультиспиральную компьютерную томографию(КТ) не применяют для диагностики ишемии, однакоэтот метод дает возможность прямо визуализироватькоронарные артерии. Теоретически с помощью муль-тиспиральной КТ можно исключить наличие ИБС. В раз-личных исследованиях было показано высокое пред-сказательное значение отрицательного результата ис-следования [37-41]. Для исключения ОКС или другихпричин боли в груди может быть полезной КТ-ангио-графия.
Инвазивные методы (коронарная ангиография)С помощью коронарной ангиографии получаютуникальную информацию о наличии и тяжести коро-нарного атеросклероза, поэтому данный метод по-преж-нему считают золотым стандартом. Ангиографию реко-мендуется проводить до и после интракоронарного вве-дения вазодилататоров (нитратов), чтобы уменьшитьвазоконстрикцию и устранить динамический компонентстеноза, который часто отмечается при ОКС. У пациен-тов с нарушением гемодинамики (отек легких, гипото-ния или тяжелые угрожающие жизни аритмии) целе-сообразно проводить исследования после введения ин-трааортального баллонного насоса.Ангиографию следует выполнять в неотложном по-рядке с диагностическими целями у пациентов высо-кого риска, а также в тех случаях, когда диагноз не ясен. Выявление острой тромботиче-ской окклюзии (например, огибающей артерии) име-ет особое значение у пациентов с сохраняющимисясимптомами или повышением уровня тропонинапри отсутствии диагностически значимых измене-ний на ЭКГ.В исследованиях TIMI-3B [42] и FRISC-2 [43] былопоказано, что у 30-38% пациентов с ОКС имеется по-ражение одной коронарной артерии, а у 44-49% — не-скольких (стеноз ≥50%). Частота стеноза левой глав-ной коронарной артерии составляет от 4-8%. У паци-ентов с поражением нескольких сосудов, а также ство-ла левой коронарной артерии имеется самый высокийриск развития серьезных неблагоприятных исходов. Ко-ронарная ангиография в сочетании с данными ЭКГ иасинергией стенки левого желудочка часто позволяетустановить, поражение какого сосуда стало причинойОКС. При ангиографии в типичном случае выявляют экс-центричный стеноз, неровные контуры, изъязвление идефекты наполнения, которые указывают на наличиеинтракоронарного тромба. Если трудно оценить тяжестьпоражения, то проводят внутрисосудистую эхографиюили измеряют фракционный резерв кровотока через >5дней после события [44]. Эти методы помогают выбратьстратегию лечения.Выбор сосудистого доступа зависит от опыта врача;этот выбор имеет важное значение, так как геморраги-ческие осложнения оказывают неблагоприятное влия-ние на клинические исходы. Лучевой доступ ассоции-ровался со снижением риска кровотечения по сравне-нию с таковым при феморальном доступе, поэтому пер-вый является предпочтительным при высоком риске ге-моррагических осложнений при условии, что врачимеет необходимый опыт. При лучевом доступе сни-жается риск образования крупной гематомы ценой более высокого облучения пациента и медицинских ра-ботников [45]. Феморальный доступ может быть пред-почтительным при нарушении гемодинамики, так какон облегчает проведение интрааортальной баллоннойконтрпульсации.
Дифференциальный диагноз
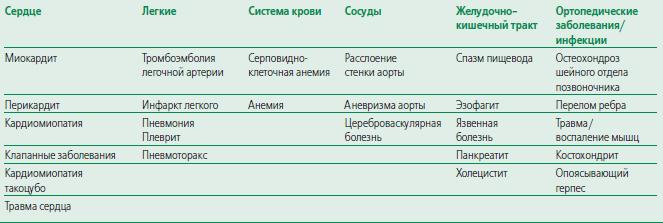
Некоторые заболевания сердца и других органов мо-гут имитировать ОКС без подъема сегмента ST (табл. 4).Гипертрофическая кардиомиопатия и пороки сердца(например, аортальный стеноз или аортальная недо-статочность) могут сопровождаться типичными симп-томами ОКС без подъема сегмента ST, повышеннымиуровнями биомаркеров или изменениями на ЭКГ [46].Иногда пароксизмальная фибрилляция предсердий(ФП) также имитирует ОКС. Некоторые такие пациен-ты страдают ИБС, что может быть причиной диагности-ческих трудностей. Миокардит, перикардит или мио-перикардит различной этиологии могут сопровож-даться болью в груди, сходной с типичной стенокарди-ей, и повышением уровней сердечных биомаркеров,изменениями ЭКГ и асинергией стенки левого желудоч-ка. Гриппоподобные симптомы, лихорадка и симпто-мы со стороны верхних дыхательных путей часто пред-шествуют развитию этих состояний или сопровож-дают их. Однако инфекции, особенно верхних отделовдыхательных путей, часто отмечают у пациентов с ОКСбез подъема сегмента ST. Установить диагноз миокар-дит или миоперикардит нередко удается только во вре-мя госпитализации.Необходимо также исключать угрожающие жизнизаболевания других органов. Например, тромбоэмбо-лия легочной артерии может сопровождаться одышкой,болью в груди и изменениями на ЭКГ, а также повышен-ными уровнями сердечных биомаркеров. Для диагно-стики тромбоэмболии легочной артерии определяютуровень Д-димера и проводят эхокардиографию иКТ. Альтернативный метод — МР-ангиография легочныхартерий, если этот метод доступен. Расслоение стенкиаорты — это еще одно заболевание, которое необходи-мо исключать при проведении дифференциального ди-агноза. ОКС без подъема сегмента ST может бытьосложнением расслоения стенки аорты, если оно рас-пространяется на коронарные артерии. Инсульт такжеможет сопровождаться изменениями на ЭКГ, асинер-гией стенки левого желудочка и повышением уровнейсердечных биомаркеров. Наоборот, атипичные симп-томы, такие как головная боль и головокружение, в ред-ких случаях могут быть единственным проявлением ише-мии миокарда.
4. Оценка прогнозаОКС без подъема сегмента ST — это нестабильное за-болевание, характеризующееся рецидивами ишемиии развитием других осложнений, которые могут при-вести к смерти или инфаркту миокарда в ближайшемили отдаленном периодах. Цели лечения, включающе-го в себя применение антиишемических и антитром-ботических лекарственных средств и различные стра-тегии реваскуляризации коронарных артерий, — пред-упредить или снизить риск таких осложнений и улуч-шить прогноз. Сроки и интенсивность вмешательствавыбирают с учетом индивидуального риска. Многие ме-тоды лечения повышают риск геморрагических ослож-нений, который необходимо тщательно взвешивать.Спектр риска, ассоциирующегося с ОКС без подъема сег-мента ST, широкий и особенно высокий в первыечасы, поэтому его необходимо тщательно оценивать не-медленно после первого контакта с врачом. Оценка рис-ка — это непрерывный процесс, который продолжает-ся до выписки пациента из стационара и может в лю-бые сроки оказать влияние на стратегию лечения. Гос-питализация пациентов в специальные отделения мо-жет улучшить результаты лечения больных с ОКС [47].У пациентов с ОКС без подъема сегмента ST риск оста-ется повышенным даже после выписки, поэтому они тре-буют особого внимания.
Таблица 4. Заболевания сердца и других органов, которые могут имитировать ОКС
Определение уровней биомаркеров у постели больногоДиагноз ОКС без подъема сегмента ST следует уста-новить как можно быстрее, чтобы назначить адекват-ное лечение. Экспресс-методы позволяют измеритьуровни биомаркеров в минимальные сроки [30]. Их сле-дует внедрять в тех случаях, когда в центральной лабо-ратории не удается выполнить это исследование втечение 60 мин [31]. Для интерпретации результатов те-ста не требуются специальные навыки или длительноеобучение. Соответственно, исследование могут вы-полнить различные медицинские работники. Однакорезультаты этих качественных тестов анализируются ви-зуально, что отражается на полученных данных. Суще-ствуют также оптические устройства, позволяющиепровести количественный анализ. Тесты обычно надеж-ны, если они положительные. Однако если диагноз не-стабильная ИБС остается вероятным, то исследованиеследует повторить в динамике, а также определить уров-ни тропонинов в сертифицированной лаборатории. Не-давно была показана возможность выделения пациентов низкого риска с помощью экспресс-алгоритма (2 ч),предполагающего применение экспресс-метода из-мерения уровня тропонинов, индекса риска и ЭКГ[32].
Визуализирующие методы
Неинвазивные методыСреди неинвазивных методов в острую фазу чащевсего проводят эхокардиографию в связи с доступностьюметода. Систолическая функция левого желудочка — этоважный прогностический показатель у пациентов сИБС, который можно легко и точно измерить с помо-щью эхокардиографии. Опытный специалист может вы-явить преходящую гипокинезию или акинезию сегмен-тов левого желудочка во время ишемии. Кроме того, ме-тод позволяет дифференцировать расслоение стенкиаорты, тромбоэмболию легочной артерии, аортальныйстеноз, гипертрофическую кардиомиопатию или пери-кардиальный выпот [33]. В связи с этим эхокардиогра-фию в отделениях интенсивной терапии следует про-водить всем пациентам.Если ЭКГ в 12 отведениях не информативна, ауровни сердечных биомаркеров у пациентов с предпо-лагаемым ОКС нормальные, может быть выполненасцинтиграфия миокарда с нагрузкой при условии от-сутствия боли в сердце. В различных исследованиях при-меняли также стресс-эхокардиографию, которая харак-теризовалась высоким предсказательным значениемотрицательного результата [34].Магнитно-резонансная томография (МРТ) сердцапозволяет одновременно оценить функцию и перфу-зию миокарда и выявить рубцовые изменения, одна-ко этот метод исследования пока малодоступен. В раз-личных исследованиях была показана информативностьМРТ в диагностике ОКС [35]. Кроме того, этот метод ис-пользуют для оценки жизнеспособности миокарда и ди-агностики миокардита.Показана также информативность перфузионнойсцинтиграфии миокарда, однако этот метод также не-достаточно широко доступен в круглосуточном режи-ме. Сцинтиграфия миокарда в покое была полезной наначальном этапе обследования пациентов с болью в гру-ди, у которых отсутствуют изменения на ЭКГ, или при-знаки сохраняющейся ишемии, или ИМ [36]. Проба снагрузкой имеет преимущество, так как она позволяетвыявить индуцируемую ишемию.Мультиспиральную компьютерную томографию(КТ) не применяют для диагностики ишемии, однакоэтот метод дает возможность прямо визуализироватькоронарные артерии. Теоретически с помощью муль-тиспиральной КТ можно исключить наличие ИБС. В раз-личных исследованиях было показано высокое пред-сказательное значение отрицательного результата ис-следования [37-41]. Для исключения ОКС или другихпричин боли в груди может быть полезной КТ-ангио-графия.
Инвазивные методы (коронарная ангиография)С помощью коронарной ангиографии получаютуникальную информацию о наличии и тяжести коро-нарного атеросклероза, поэтому данный метод по-преж-нему считают золотым стандартом. Ангиографию реко-мендуется проводить до и после интракоронарного вве-дения вазодилататоров (нитратов), чтобы уменьшитьвазоконстрикцию и устранить динамический компонентстеноза, который часто отмечается при ОКС. У пациен-тов с нарушением гемодинамики (отек легких, гипото-ния или тяжелые угрожающие жизни аритмии) целе-сообразно проводить исследования после введения ин-трааортального баллонного насоса.Ангиографию следует выполнять в неотложном по-рядке с диагностическими целями у пациентов высо-кого риска, а также в тех случаях, когда диагноз не ясен. Выявление острой тромботиче-ской окклюзии (например, огибающей артерии) име-ет особое значение у пациентов с сохраняющимисясимптомами или повышением уровня тропонинапри отсутствии диагностически значимых измене-ний на ЭКГ.В исследованиях TIMI-3B [42] и FRISC-2 [43] былопоказано, что у 30-38% пациентов с ОКС имеется по-ражение одной коронарной артерии, а у 44-49% — не-скольких (стеноз ≥50%). Частота стеноза левой глав-ной коронарной артерии составляет от 4-8%. У паци-ентов с поражением нескольких сосудов, а также ство-ла левой коронарной артерии имеется самый высокийриск развития серьезных неблагоприятных исходов. Ко-ронарная ангиография в сочетании с данными ЭКГ иасинергией стенки левого желудочка часто позволяетустановить, поражение какого сосуда стало причинойОКС. При ангиографии в типичном случае выявляют экс-центричный стеноз, неровные контуры, изъязвление идефекты наполнения, которые указывают на наличиеинтракоронарного тромба. Если трудно оценить тяжестьпоражения, то проводят внутрисосудистую эхографиюили измеряют фракционный резерв кровотока через >5дней после события [44]. Эти методы помогают выбратьстратегию лечения.Выбор сосудистого доступа зависит от опыта врача;этот выбор имеет важное значение, так как геморраги-ческие осложнения оказывают неблагоприятное влия-ние на клинические исходы. Лучевой доступ ассоции-ровался со снижением риска кровотечения по сравне-нию с таковым при феморальном доступе, поэтому пер-вый является предпочтительным при высоком риске ге-моррагических осложнений при условии, что врачимеет необходимый опыт. При лучевом доступе сни-жается риск образования крупной гематомы ценой более высокого облучения пациента и медицинских ра-ботников [45]. Феморальный доступ может быть пред-почтительным при нарушении гемодинамики, так какон облегчает проведение интрааортальной баллоннойконтрпульсации.
Дифференциальный диагноз
Некоторые заболевания сердца и других органов мо-гут имитировать ОКС без подъема сегмента ST (табл. 4).Гипертрофическая кардиомиопатия и пороки сердца(например, аортальный стеноз или аортальная недо-статочность) могут сопровождаться типичными симп-томами ОКС без подъема сегмента ST, повышеннымиуровнями биомаркеров или изменениями на ЭКГ [46].Иногда пароксизмальная фибрилляция предсердий(ФП) также имитирует ОКС. Некоторые такие пациен-ты страдают ИБС, что может быть причиной диагности-ческих трудностей. Миокардит, перикардит или мио-перикардит различной этиологии могут сопровож-даться болью в груди, сходной с типичной стенокарди-ей, и повышением уровней сердечных биомаркеров,изменениями ЭКГ и асинергией стенки левого желудоч-ка. Гриппоподобные симптомы, лихорадка и симпто-мы со стороны верхних дыхательных путей часто пред-шествуют развитию этих состояний или сопровож-дают их. Однако инфекции, особенно верхних отделовдыхательных путей, часто отмечают у пациентов с ОКСбез подъема сегмента ST. Установить диагноз миокар-дит или миоперикардит нередко удается только во вре-мя госпитализации.Необходимо также исключать угрожающие жизнизаболевания других органов. Например, тромбоэмбо-лия легочной артерии может сопровождаться одышкой,болью в груди и изменениями на ЭКГ, а также повышен-ными уровнями сердечных биомаркеров. Для диагно-стики тромбоэмболии легочной артерии определяютуровень Д-димера и проводят эхокардиографию иКТ. Альтернативный метод — МР-ангиография легочныхартерий, если этот метод доступен. Расслоение стенкиаорты — это еще одно заболевание, которое необходи-мо исключать при проведении дифференциального ди-агноза. ОКС без подъема сегмента ST может бытьосложнением расслоения стенки аорты, если оно рас-пространяется на коронарные артерии. Инсульт такжеможет сопровождаться изменениями на ЭКГ, асинер-гией стенки левого желудочка и повышением уровнейсердечных биомаркеров. Наоборот, атипичные симп-томы, такие как головная боль и головокружение, в ред-ких случаях могут быть единственным проявлением ише-мии миокарда.
4. Оценка прогнозаОКС без подъема сегмента ST — это нестабильное за-болевание, характеризующееся рецидивами ишемиии развитием других осложнений, которые могут при-вести к смерти или инфаркту миокарда в ближайшемили отдаленном периодах. Цели лечения, включающе-го в себя применение антиишемических и антитром-ботических лекарственных средств и различные стра-тегии реваскуляризации коронарных артерий, — пред-упредить или снизить риск таких осложнений и улуч-шить прогноз. Сроки и интенсивность вмешательствавыбирают с учетом индивидуального риска. Многие ме-тоды лечения повышают риск геморрагических ослож-нений, который необходимо тщательно взвешивать.Спектр риска, ассоциирующегося с ОКС без подъема сег-мента ST, широкий и особенно высокий в первыечасы, поэтому его необходимо тщательно оценивать не-медленно после первого контакта с врачом. Оценка рис-ка — это непрерывный процесс, который продолжает-ся до выписки пациента из стационара и может в лю-бые сроки оказать влияние на стратегию лечения. Гос-питализация пациентов в специальные отделения мо-жет улучшить результаты лечения больных с ОКС [47].У пациентов с ОКС без подъема сегмента ST риск оста-ется повышенным даже после выписки, поэтому они тре-буют особого внимания.
Таблица 4. Заболевания сердца и других органов, которые могут имитировать ОКС
 Клиническая оценка риска
Помимо некоторых универсальных факторов рис-ка, таких как пожилой возраст, сахарный диабет, почеч-ная недостаточность и другие состояния, важное значе-ние для оценки прогноза имеют первые клиническиепроявления. Например, симптомы в покое прогности-чески более неблагоприятны, чем симптомы, возникаю-щие при физической нагрузке. У пациентов с интермит-тирующими симптомами увеличение числа эпизодовишемии перед ОКС также оказывает влияние на про-гноз. Неблагоприятными прогностическими фактора-ми являются тахикардия, артериальная гипотония илисердечная недостаточность при поступлении; в таких слу-чаях необходимо быстро установить диагноз и назна-чить лечение [48-50]. У пациентов более молодого воз-раста с клиническими проявлениями ОКС необходимоисключать применение кокаина, которое сопровожда-ется более распространенным поражением миокардаи повышенным риском осложнений [51].
Электрокардиографические изменения
ЭКГ при поступлении позволяет предсказать риск вострую фазу. Если изменения на ЭКГ отсутствуют, то про-гноз более благоприятный, чем при наличии отрицатель-ных зубцов Т. У пациентов с депрессией сегмента ST про-гноз еще хуже и зависит от выраженности и распростра-ненности изменений на ЭКГ [52,53]. Число отведений,в которых определяются депрессия сегмента ST и степеньего депрессии, отражают распространенность и тяжестьишемии и коррелируют с прогнозом [52]. Депрессия сег-мента ST≥0,05 мВ в двух или более соседних отведенияхв сочетании с соответствующими клиническими проявле-ниями позволяет заподозрить ОКС без подъема сегмен-та ST и имеет прогностическое значение. Небольшую де-прессию сегмента ST (0,05 мВ) бывает трудно выявитьв клинической практике. Более важное клиническоезначение имеет депрессия сегмента ST≥0,1 мВ. В такихслучаях частота смерти и ИМ в течение ближайшего годасоставляет 11%. При депрессии сегмента ST≥0,2 мВ рисксмерти увеличивается примерно в 6 раз [53]. Депрессиясегмента ST в сочетании с преходящим его подъемом ука-зывает на еще более высокий риск.У пациентов с депрессией сегмента ST риск сердеч-но-сосудистых исходов выше, чем у пациентов с изо-лированной инверсией (≥0,1 мВ) зубца Т в отведенияхс преобладающим зубцом R, а у последних риск выше,чем у пациентов с нормальной ЭКГ при поступлении.Некоторые авторы высказывали сомнения по поводупрогностического значения изолированной инверсиизубцов Т, однако глубокие симметричные отрицатель-ные зубцы Т в передних грудных отведениях часто от-ражают выраженный стеноз проксимальной части ле-вой передней нисходящей коронарной артерии иствола левой коронарной артерии.Другие изменения, такие как подъем сегмента ST(≥0,1 мВ) в aVR, ассоциировались с высокой веро-ятностью стеноза левой основной коронарной артерииили трех коронарных артерий и неблагоприятнымпрогнозом [53].Пробы с нагрузкойПри сохранении типичной стенокардии покоя про-водить пробу с нагрузкой не следует. Однако проба с фи-зической нагрузкой позволяет сделать прогноз, поэто-му ее целесообразно выполнить перед выпиской приотсутствии диагностически значимых изменений на ЭКГ,а также боли, признаков сердечной недостаточности иповышенных уровней биомаркеров в динамике. Ран-няя проба с физической нагрузкой характеризуется вы-соким предсказательным значением отрицательного ре-зультата. Показатели, отражающие сократительнуюфункцию миокарда, имеют такое же прогностическоезначение, как показатели ишемии миокарда, а комби-нация таких показателей позволяет наиболее надежнооценить прогноз [54,55].Непрерывное мониторирование сегмента STВ нескольких исследованиях при непрерывном мо-ниторировании сегмента ST было показано, что у 15-30% пациентов с ОКС без подъема сегмента ST наблю-даются преходящие изменения сегмента ST, в основномего депрессия. У таких пациентов повышен риск раз-вития сердечно-сосудистых исходов, в том числе смер-ти [56]. Мониторирование сегмента ST дополняет про-гностическую информацию, полученную на основанииЭКГ в покое, уровней тропонинов и других клиническихпоказателей [56,57].
Биомаркеры
Биомаркеры отражают различные патофизиологи-ческие аспекты ОКС без подъема сегмента ST, такие какповреждение кардиомиоцитов, воспаление, активациятромбоцитов и нейрогуморальных систем. Для оценкириска развития ИМ и смерти в ближайшие 30 дн пред-почтительно использовать уровни тропонина Т или I[30,58]. Уровни тропонинов позволяли предсказать иотдаленный прогноз (1 год и более). У пациентов с ОКСбез подъема сегмента ST, у которых определяется по-вышенный уровень тропонина, но не изменена актив-ность МВ-фракции КК (доля их составляет около 28%от общего числа пациентов ОКС без подъема сегмен-та ST), отмечаются более высокий риск и пониженнаягоспитальная смертность по сравнению с пациентами,у которых повышены уровни обоих биомаркеров [59].Риск, связанный с повышенными уровнями тропони-на, не зависит от других факторов риска, таких как из-менения на ЭКГ в покое или при непрерывном мони-торировании и маркеры воспаления, и оказывает аддитивное действие на общий риск [60]. Выявление па-циентов с повышенными уровнями тропонина имеетзначение для выбора тактики ведения ОКС без подъе-ма сегмента ST. Однако при принятии решения не сле-дует учитывать только уровень тропонина, так как в опре-деленных группах пациентов высокого риска, у которыхуровень тропонина оставался нормальным, госпи-тальная летальность достигала 12,7% [61].Один отрицательный результат теста при первом ис-следовании может быть недостаточным для исключе-ния ОКС без подъема сегмента ST, так как у многих па-циентов уровень тропонина увеличивается в ближай-шие часы. В связи с этим рекомендуется повторный ана-лиз через 6-9 ч [27,30]. Разработанный недавно ульт-рачувствительный метод анализа тропонина позволяетнадежнее выделить пациентов группы риска и быстрооценить прогноз (дополнительную информацию см. вразделе 3.2.3. и на рис. 5).Хотя сердечные тропонины являются ключевымибиомаркерами при начальной стратификации риска,в клинических исследованиях изучалось прогностиче-ское значение многочисленных других биомаркеров.Среди них лучше всего изучены и используются вобычной практике высокочувствительный С-реактив-ный белок (вчСРБ) и мозговой натрийуретическийпептид (МНП). Натрийуретические пептиды, такиекак МНП и его N-терминальный фрагмент предшествен-ника МНП (NT-проМНП), — это высокочувствительныеи достаточно специфичные маркеры дисфункции ле-вого желудочка. Ретроспективные исследования пока-зали, что повышенные уровни МНП или NT-проМНПу пациентов с ОКС без подъема сегмента ST сопровож-даются увеличением смертности в 3-5 раз, а увеличе-ние риска не зависит от уровней тропонина или вчСРБ[62]. Риск смерти оставался повышенным даже послевнесения поправки на возраст, класс по Killip и фрак-цию выброса левого желудочка [60]. Уровни мозговыхнатрийуретических пептидов через несколько днейпосле появления симптомов позволяют предсказать про-гноз точнее, чем уровни при поступлении. Натрийуре-тические пептиды — это информативные маркеры в не-отложных ситуациях у пациентов с болью в груди илиодышкой, в частности они позволяли дифференциро-вать сердечные и несердечные причины одышки. Од-нако при оценке отдаленного прогноза они имеютограниченное значение при начальной стратификациириска и, соответственно, выбора тактики ведения па-циентов с ОКС без подъема сегмента ST [62].Среди многочисленных маркеров воспаления, ко-торые изучались на протяжении последнего десятиле-тия, СРБ, измеренный с помощью высокочувствитель-ного метода, лучше всего изучен и ассоциировался с не-желательными исходами. Установлено, что даже у па-циентов с тропонин-отрицательным ОКС без подъемасегмента ST повышенные уровни вчСРБ (≥10 мг/л) поз-воляют предсказать смертность в отдаленном периоде(от 6 мес до 4 лет) [60,63,64]. Исследование FRISC под-твердило, что повышенные уровни вчСРБ ассоциируют-ся с повышенной смертностью в раннем периоде и в от-даленные сроки (более 4 лет) [65]. Сходные результа-ты были получены в крупных когортах пациентов, ко-торых направляли на плановое ЧКВ. Самый высокийриск имели пациенты с персистирующим повышени-ем уровня вчСРБ [66]. Однако вчСРБ не имеет никако-го значения в диагностике ОКС.Гипергликемия при поступлении — это мощныйпредиктор смерти и сердечной недостаточности дажеу пациентов без диабета [67,68]. Недавно было пока-зано, что уровни гликемии натощак в начале госпита-лизации позволяют предсказать смертность лучше,чем уровни глюкозы при поступлении [68]. Крометого, изменения уровней гликемии натощак во времяпребывания в стационаре тесно ассоциируются с исхо-дами, а стойко нарушенная гликемия натощак указы-вает на неблагоприятный прогноз [67].Некоторые показатели общего анализа крови такжеявляются неблагоприятными прогностическими фак-торами. Риск неблагоприятных исходов повышается упациентов с анемией [69,70]. Увеличение числа лей-коцитов или снижение числа тромбоцитов в крови припоступлении также ассоциируется с неблагоприятнымпрогнозом [70].Нарушение функции почек — это независимыйпредиктор смертности в отдаленном периоде у паци-ентов с ОКС [60,71]. Сывороточная концентрациякреатинина — это менее надежный индикатор функциипочек, чем клиренс креатинина или расчетная скоростьклубочковой фильтрации (СКФ), так как она зависит отразличных факторов, включая возраст, массу тела,расу и прием различных лекарственных препаратов.Предложены несколько методов расчета СКФ на осно-вании сывороточного уровня креатинина, в частностиформулы Кокрофта-Голта и MDRD. Смертность в отда-ленном периоде экспоненциально увеличивается приснижении СКФ/клиренса креатинина.Новые биомаркерыВ клинических исследованиях изучались также дру-гие биомаркеры с целью более точной оценки риска,а также более раннего исключения диагноза ОКС.Наиболее перспективными считают биомаркеры, отра-жающие процессы сосудистого воспаления и оксида-тивного стресса. К ним, в частности, относят миелопе-роксидазу, фактор роста 15 и ассоциированную с ли-попротеином фосфолипазу А2 [72-75]. Для ранней ди-агностики ОКС могут быть использованы белок, связы-вающийся с жирными кислотами [76], или альбумин,модифицирующийся при ишемии [77], а также маркеры системного стресса (копептин) [78]. Однако их дополнительное значение, особенно по сравнению с вы-сокочувствительными методами измерения уровнятропонина, не изучалось, что не позволяет дать какие-либо практические рекомендации.
Индексы риска
Количественная оценка риска имеет важное значение для выбора метода лечения ОКС. Разработаны не-сколько индексов риска ишемических осложнений икровотечений, которые рассчитывают в различныесроки. В клинической практике предпочтительно при-менение простых показателей.Риск исходовДля оценки риска ишемических исходов в ближай-шие и средние сроки чаще всего используют индексыGRACE [50] или TIMI [49], которые несколько отличают-ся друг от друга (выборки пациентов, исходы, сроки,а также предикторы, которые оценивают на основанииисходных показателей, анамнеза, клинических проявле-ний, гемодинамических изменений, ЭКГ, лабораторныхпоказателей и лечения). По данным прямого сравне-ния [79,80], индекс GRACE позволяет точнее всегостратифицировать риск как при поступлении, так и пе-ред выпиской (табл. 5). Однако он предполагает слож-ные расчеты, требующие применения компьютера илиспециальных программ (расчеты могут быть выполне-ны online; http://www.outcomes.org/grace). Добавле-ние уровней биомаркеров (например, NT-проМНП) поз-воляет дополнительно повысить информативность ин-декса GRACE и улучшить оценку риска в отдаленном пе-риоде [81].Рассчитать индекс TIMI проще (учитываются только6 показателей), однако по точности он уступает индек-су GRACE [80]. Это связано с тем, что при расчете сум-марного индекса не учитываются ключевые факторыриска, такие как класс по Killip, частота сердечных со-кращений и систолическое АД [82].Риск кровотеченийКровотечение ухудшает прогноз у пациентов с ОКСбез подъема сегмента ST, поэтому необходимо пред-принимать все меры для профилактики геморрагиче-ских осложнений. Выделяют несколько факторов, ко-торые позволяют предсказать риск больших кровотече-ний во время госпитализации. На основании регистрови когортных исследований (ОКС и ЧКВ) разработаныиндексы риска кровотечения. Например, индексCRUSADE (www.crusadebleedingscore.org/) был пред-ложен на основании соответствующего регистра, в ко-торый были включены 71 277 пациентов. В последую-щем этот индекс был валидирован в когорте из 17 857пациентов из той же когорты (табл. 6) [83]. При увеличении индекса частота больших кровотечений посте-пенно увеличивалась (рис. 2). Этот индекс позволял до-статочно точно оценить риск кровотечений на основа-нии различных факторов, которые оценивали при по-ступлении и на фоне лечения. При расчете индекса неучитывается возраст, однако он используется при рас-чете клиренса креатинина [83].Другой индекс риска кровотечений был разработанна основании обследования 17 421 пациента, включен-ного в исследования ACUITY и HORIZONS [84]. Были вы-делены 6 независимых исходных предикторов (женскийпол, пожилой возраст, повышенный сывороточныйуровень креатинина, число лейкоцитов, анемия, ИМ сподъемом или без подъема сегмента ST) и 1 фактор,отражающий лечение (лечение гепарином или блока-тором гликопротеиновых IIb/IIIa рецепторов против при-менения только бивалирудина). Индекс позволяет вы-делить пациентов с повышенным риском кровотечений,не связанных с КШ, и смерти в течение 1 года, однакоон не был валидирован в независимом когортном ис-следовании.Оба индекса были предложены на основании обсле-дования пациентов, у которых применяли в основномили исключительно феморальный доступ для катетери-зации сердца. Их предсказательное значение может бытьниже при применении лучевого доступа. Любой индексне может заменить мнение врача, основывающееся наклинических данных, однако индексы представляют со-бой объективный инструмент, который используютдля оценки риска кровотечений у конкретного пациен-та или в определенной выборке.
Таблица 5. Смертность в стационаре и в течение 6 мес[50] в группах низкого, среднего и высокогориска, выделенных на основании индекса GRACE
Клиническая оценка риска
Помимо некоторых универсальных факторов рис-ка, таких как пожилой возраст, сахарный диабет, почеч-ная недостаточность и другие состояния, важное значе-ние для оценки прогноза имеют первые клиническиепроявления. Например, симптомы в покое прогности-чески более неблагоприятны, чем симптомы, возникаю-щие при физической нагрузке. У пациентов с интермит-тирующими симптомами увеличение числа эпизодовишемии перед ОКС также оказывает влияние на про-гноз. Неблагоприятными прогностическими фактора-ми являются тахикардия, артериальная гипотония илисердечная недостаточность при поступлении; в таких слу-чаях необходимо быстро установить диагноз и назна-чить лечение [48-50]. У пациентов более молодого воз-раста с клиническими проявлениями ОКС необходимоисключать применение кокаина, которое сопровожда-ется более распространенным поражением миокардаи повышенным риском осложнений [51].
Электрокардиографические изменения
ЭКГ при поступлении позволяет предсказать риск вострую фазу. Если изменения на ЭКГ отсутствуют, то про-гноз более благоприятный, чем при наличии отрицатель-ных зубцов Т. У пациентов с депрессией сегмента ST про-гноз еще хуже и зависит от выраженности и распростра-ненности изменений на ЭКГ [52,53]. Число отведений,в которых определяются депрессия сегмента ST и степеньего депрессии, отражают распространенность и тяжестьишемии и коррелируют с прогнозом [52]. Депрессия сег-мента ST≥0,05 мВ в двух или более соседних отведенияхв сочетании с соответствующими клиническими проявле-ниями позволяет заподозрить ОКС без подъема сегмен-та ST и имеет прогностическое значение. Небольшую де-прессию сегмента ST (0,05 мВ) бывает трудно выявитьв клинической практике. Более важное клиническоезначение имеет депрессия сегмента ST≥0,1 мВ. В такихслучаях частота смерти и ИМ в течение ближайшего годасоставляет 11%. При депрессии сегмента ST≥0,2 мВ рисксмерти увеличивается примерно в 6 раз [53]. Депрессиясегмента ST в сочетании с преходящим его подъемом ука-зывает на еще более высокий риск.У пациентов с депрессией сегмента ST риск сердеч-но-сосудистых исходов выше, чем у пациентов с изо-лированной инверсией (≥0,1 мВ) зубца Т в отведенияхс преобладающим зубцом R, а у последних риск выше,чем у пациентов с нормальной ЭКГ при поступлении.Некоторые авторы высказывали сомнения по поводупрогностического значения изолированной инверсиизубцов Т, однако глубокие симметричные отрицатель-ные зубцы Т в передних грудных отведениях часто от-ражают выраженный стеноз проксимальной части ле-вой передней нисходящей коронарной артерии иствола левой коронарной артерии.Другие изменения, такие как подъем сегмента ST(≥0,1 мВ) в aVR, ассоциировались с высокой веро-ятностью стеноза левой основной коронарной артерииили трех коронарных артерий и неблагоприятнымпрогнозом [53].Пробы с нагрузкойПри сохранении типичной стенокардии покоя про-водить пробу с нагрузкой не следует. Однако проба с фи-зической нагрузкой позволяет сделать прогноз, поэто-му ее целесообразно выполнить перед выпиской приотсутствии диагностически значимых изменений на ЭКГ,а также боли, признаков сердечной недостаточности иповышенных уровней биомаркеров в динамике. Ран-няя проба с физической нагрузкой характеризуется вы-соким предсказательным значением отрицательного ре-зультата. Показатели, отражающие сократительнуюфункцию миокарда, имеют такое же прогностическоезначение, как показатели ишемии миокарда, а комби-нация таких показателей позволяет наиболее надежнооценить прогноз [54,55].Непрерывное мониторирование сегмента STВ нескольких исследованиях при непрерывном мо-ниторировании сегмента ST было показано, что у 15-30% пациентов с ОКС без подъема сегмента ST наблю-даются преходящие изменения сегмента ST, в основномего депрессия. У таких пациентов повышен риск раз-вития сердечно-сосудистых исходов, в том числе смер-ти [56]. Мониторирование сегмента ST дополняет про-гностическую информацию, полученную на основанииЭКГ в покое, уровней тропонинов и других клиническихпоказателей [56,57].
Биомаркеры
Биомаркеры отражают различные патофизиологи-ческие аспекты ОКС без подъема сегмента ST, такие какповреждение кардиомиоцитов, воспаление, активациятромбоцитов и нейрогуморальных систем. Для оценкириска развития ИМ и смерти в ближайшие 30 дн пред-почтительно использовать уровни тропонина Т или I[30,58]. Уровни тропонинов позволяли предсказать иотдаленный прогноз (1 год и более). У пациентов с ОКСбез подъема сегмента ST, у которых определяется по-вышенный уровень тропонина, но не изменена актив-ность МВ-фракции КК (доля их составляет около 28%от общего числа пациентов ОКС без подъема сегмен-та ST), отмечаются более высокий риск и пониженнаягоспитальная смертность по сравнению с пациентами,у которых повышены уровни обоих биомаркеров [59].Риск, связанный с повышенными уровнями тропони-на, не зависит от других факторов риска, таких как из-менения на ЭКГ в покое или при непрерывном мони-торировании и маркеры воспаления, и оказывает аддитивное действие на общий риск [60]. Выявление па-циентов с повышенными уровнями тропонина имеетзначение для выбора тактики ведения ОКС без подъе-ма сегмента ST. Однако при принятии решения не сле-дует учитывать только уровень тропонина, так как в опре-деленных группах пациентов высокого риска, у которыхуровень тропонина оставался нормальным, госпи-тальная летальность достигала 12,7% [61].Один отрицательный результат теста при первом ис-следовании может быть недостаточным для исключе-ния ОКС без подъема сегмента ST, так как у многих па-циентов уровень тропонина увеличивается в ближай-шие часы. В связи с этим рекомендуется повторный ана-лиз через 6-9 ч [27,30]. Разработанный недавно ульт-рачувствительный метод анализа тропонина позволяетнадежнее выделить пациентов группы риска и быстрооценить прогноз (дополнительную информацию см. вразделе 3.2.3. и на рис. 5).Хотя сердечные тропонины являются ключевымибиомаркерами при начальной стратификации риска,в клинических исследованиях изучалось прогностиче-ское значение многочисленных других биомаркеров.Среди них лучше всего изучены и используются вобычной практике высокочувствительный С-реактив-ный белок (вчСРБ) и мозговой натрийуретическийпептид (МНП). Натрийуретические пептиды, такиекак МНП и его N-терминальный фрагмент предшествен-ника МНП (NT-проМНП), — это высокочувствительныеи достаточно специфичные маркеры дисфункции ле-вого желудочка. Ретроспективные исследования пока-зали, что повышенные уровни МНП или NT-проМНПу пациентов с ОКС без подъема сегмента ST сопровож-даются увеличением смертности в 3-5 раз, а увеличе-ние риска не зависит от уровней тропонина или вчСРБ[62]. Риск смерти оставался повышенным даже послевнесения поправки на возраст, класс по Killip и фрак-цию выброса левого желудочка [60]. Уровни мозговыхнатрийуретических пептидов через несколько днейпосле появления симптомов позволяют предсказать про-гноз точнее, чем уровни при поступлении. Натрийуре-тические пептиды — это информативные маркеры в не-отложных ситуациях у пациентов с болью в груди илиодышкой, в частности они позволяли дифференциро-вать сердечные и несердечные причины одышки. Од-нако при оценке отдаленного прогноза они имеютограниченное значение при начальной стратификациириска и, соответственно, выбора тактики ведения па-циентов с ОКС без подъема сегмента ST [62].Среди многочисленных маркеров воспаления, ко-торые изучались на протяжении последнего десятиле-тия, СРБ, измеренный с помощью высокочувствитель-ного метода, лучше всего изучен и ассоциировался с не-желательными исходами. Установлено, что даже у па-циентов с тропонин-отрицательным ОКС без подъемасегмента ST повышенные уровни вчСРБ (≥10 мг/л) поз-воляют предсказать смертность в отдаленном периоде(от 6 мес до 4 лет) [60,63,64]. Исследование FRISC под-твердило, что повышенные уровни вчСРБ ассоциируют-ся с повышенной смертностью в раннем периоде и в от-даленные сроки (более 4 лет) [65]. Сходные результа-ты были получены в крупных когортах пациентов, ко-торых направляли на плановое ЧКВ. Самый высокийриск имели пациенты с персистирующим повышени-ем уровня вчСРБ [66]. Однако вчСРБ не имеет никако-го значения в диагностике ОКС.Гипергликемия при поступлении — это мощныйпредиктор смерти и сердечной недостаточности дажеу пациентов без диабета [67,68]. Недавно было пока-зано, что уровни гликемии натощак в начале госпита-лизации позволяют предсказать смертность лучше,чем уровни глюкозы при поступлении [68]. Крометого, изменения уровней гликемии натощак во времяпребывания в стационаре тесно ассоциируются с исхо-дами, а стойко нарушенная гликемия натощак указы-вает на неблагоприятный прогноз [67].Некоторые показатели общего анализа крови такжеявляются неблагоприятными прогностическими фак-торами. Риск неблагоприятных исходов повышается упациентов с анемией [69,70]. Увеличение числа лей-коцитов или снижение числа тромбоцитов в крови припоступлении также ассоциируется с неблагоприятнымпрогнозом [70].Нарушение функции почек — это независимыйпредиктор смертности в отдаленном периоде у паци-ентов с ОКС [60,71]. Сывороточная концентрациякреатинина — это менее надежный индикатор функциипочек, чем клиренс креатинина или расчетная скоростьклубочковой фильтрации (СКФ), так как она зависит отразличных факторов, включая возраст, массу тела,расу и прием различных лекарственных препаратов.Предложены несколько методов расчета СКФ на осно-вании сывороточного уровня креатинина, в частностиформулы Кокрофта-Голта и MDRD. Смертность в отда-ленном периоде экспоненциально увеличивается приснижении СКФ/клиренса креатинина.Новые биомаркерыВ клинических исследованиях изучались также дру-гие биомаркеры с целью более точной оценки риска,а также более раннего исключения диагноза ОКС.Наиболее перспективными считают биомаркеры, отра-жающие процессы сосудистого воспаления и оксида-тивного стресса. К ним, в частности, относят миелопе-роксидазу, фактор роста 15 и ассоциированную с ли-попротеином фосфолипазу А2 [72-75]. Для ранней ди-агностики ОКС могут быть использованы белок, связы-вающийся с жирными кислотами [76], или альбумин,модифицирующийся при ишемии [77], а также маркеры системного стресса (копептин) [78]. Однако их дополнительное значение, особенно по сравнению с вы-сокочувствительными методами измерения уровнятропонина, не изучалось, что не позволяет дать какие-либо практические рекомендации.
Индексы риска
Количественная оценка риска имеет важное значение для выбора метода лечения ОКС. Разработаны не-сколько индексов риска ишемических осложнений икровотечений, которые рассчитывают в различныесроки. В клинической практике предпочтительно при-менение простых показателей.Риск исходовДля оценки риска ишемических исходов в ближай-шие и средние сроки чаще всего используют индексыGRACE [50] или TIMI [49], которые несколько отличают-ся друг от друга (выборки пациентов, исходы, сроки,а также предикторы, которые оценивают на основанииисходных показателей, анамнеза, клинических проявле-ний, гемодинамических изменений, ЭКГ, лабораторныхпоказателей и лечения). По данным прямого сравне-ния [79,80], индекс GRACE позволяет точнее всегостратифицировать риск как при поступлении, так и пе-ред выпиской (табл. 5). Однако он предполагает слож-ные расчеты, требующие применения компьютера илиспециальных программ (расчеты могут быть выполне-ны online; http://www.outcomes.org/grace). Добавле-ние уровней биомаркеров (например, NT-проМНП) поз-воляет дополнительно повысить информативность ин-декса GRACE и улучшить оценку риска в отдаленном пе-риоде [81].Рассчитать индекс TIMI проще (учитываются только6 показателей), однако по точности он уступает индек-су GRACE [80]. Это связано с тем, что при расчете сум-марного индекса не учитываются ключевые факторыриска, такие как класс по Killip, частота сердечных со-кращений и систолическое АД [82].Риск кровотеченийКровотечение ухудшает прогноз у пациентов с ОКСбез подъема сегмента ST, поэтому необходимо пред-принимать все меры для профилактики геморрагиче-ских осложнений. Выделяют несколько факторов, ко-торые позволяют предсказать риск больших кровотече-ний во время госпитализации. На основании регистрови когортных исследований (ОКС и ЧКВ) разработаныиндексы риска кровотечения. Например, индексCRUSADE (www.crusadebleedingscore.org/) был пред-ложен на основании соответствующего регистра, в ко-торый были включены 71 277 пациентов. В последую-щем этот индекс был валидирован в когорте из 17 857пациентов из той же когорты (табл. 6) [83]. При увеличении индекса частота больших кровотечений посте-пенно увеличивалась (рис. 2). Этот индекс позволял до-статочно точно оценить риск кровотечений на основа-нии различных факторов, которые оценивали при по-ступлении и на фоне лечения. При расчете индекса неучитывается возраст, однако он используется при рас-чете клиренса креатинина [83].Другой индекс риска кровотечений был разработанна основании обследования 17 421 пациента, включен-ного в исследования ACUITY и HORIZONS [84]. Были вы-делены 6 независимых исходных предикторов (женскийпол, пожилой возраст, повышенный сывороточныйуровень креатинина, число лейкоцитов, анемия, ИМ сподъемом или без подъема сегмента ST) и 1 фактор,отражающий лечение (лечение гепарином или блока-тором гликопротеиновых IIb/IIIa рецепторов против при-менения только бивалирудина). Индекс позволяет вы-делить пациентов с повышенным риском кровотечений,не связанных с КШ, и смерти в течение 1 года, однакоон не был валидирован в независимом когортном ис-следовании.Оба индекса были предложены на основании обсле-дования пациентов, у которых применяли в основномили исключительно феморальный доступ для катетери-зации сердца. Их предсказательное значение может бытьниже при применении лучевого доступа. Любой индексне может заменить мнение врача, основывающееся наклинических данных, однако индексы представляют со-бой объективный инструмент, который используютдля оценки риска кровотечений у конкретного пациен-та или в определенной выборке.
Таблица 5. Смертность в стационаре и в течение 6 мес[50] в группах низкого, среднего и высокогориска, выделенных на основании индекса GRACE
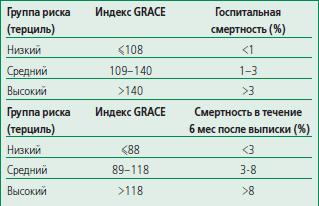 Таблица 6. Индекс риска кровотечений CRUSADE [83]
Таблица 6. Индекс риска кровотечений CRUSADE [83]
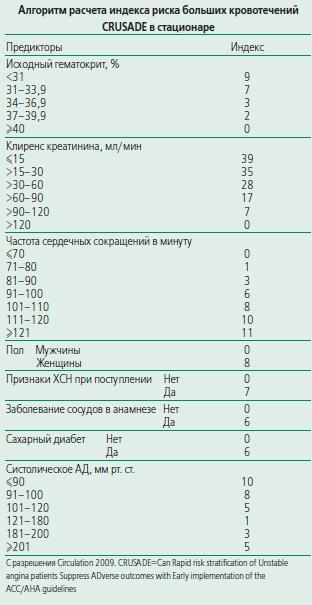 Рис. 2. Риск больших кровотечений в зависимостиот индекса CRUSADE(www.crusadebleedingscore.org/)
Рис. 2. Риск больших кровотечений в зависимостиот индекса CRUSADE(www.crusadebleedingscore.org/)
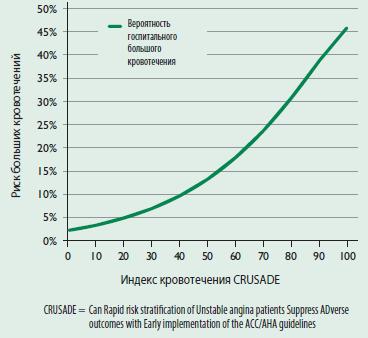 Рекомендации по диагностике и оценке риска
Рекомендации по диагностике и оценке риска
 Риск в отдаленном периоде
Помимо факторов, позволяющих предсказать бли-жайший прогноз, выделяют также предикторы риска вотдаленном периоде. Они имеют важное значениедля пересмотра риска и могут привести к интенсифи-кации начальной тактики лечения. К таким факторамотносят осложненное течение ОКС, систолическуюфункцию левого желудочка, тяжесть ИБС, наличиереваскуляризации и признаки резидуальной ишемиипо данным неинвазивных методов.
Лечение
Антиишемические препараты
Антиишемические препараты снижают потребностьмиокарда в кислороде (за счет уменьшения частоты сер-дечных сокращений, АД, преднагрузки или сократимо-сти миокарда) или увеличивают доставку кислорода кмиокарду (за счет дилатации коронарных артерий).Бета-адреноблокаторыБета-адреноблокаторы подавляют эффекты цирку-лирующих катехоламинов на миокард и уменьшают по-требность его в кислороде за счет снижения частоты сер-дечных сокращений, АД и сократимости. Благоприятныеэффекты бета-адреноблокаторов были установлены упациентов с ИМ с подъемом сегмента ST и стабильнойстенокардией [85,86]. В двух двойных слепых рандо-мизированных исследованиях бета-адреноблокаторысравнивали с плацебо у пациентов с нестабильнойстенокардией [87,88]. При мета-анализе было показа-но, что лечение бета-адреноблокатором вызывает сни-жение относительного риска прогрессирования и раз-вития ИМ с подъемом сегмента ST на 13% [89]. Хотя вэтих относительно небольших исследованиях не былоподтверждено снижение смертности у пациентов сОКС без подъема сегмента ST, тем не менее, можно экс-траполировать результаты более крупных рандомизи-рованных исследований бета-адреноблокаторов убольных ИМ [90]. В регистре CRUSADE, в которыйвключали пациентов с ИМ без подъема сегментаST/нестабильной стенокардией из 509 американскихбольниц с 2001 по 2004 гг., у больных, получавших бета-адреноблокаторы в острый период, выявили снижениескорректированного риска госпитальной летальности на34% (3,9% и 6,9%, соответственно; p<0,001) [91].При систематизированном обзоре литературы небыло убедительно подтверждено снижение госпи-тальной летальности при раннем применении бета-ад-реноблокаторов у пациентов с острым или предпола-гаемым ИМ. Был сделан вывод, что имеющиеся дан-ные не позволяют рекомендовать назначение бета-ад-реноблокаторов в первые 8 ч после развития ОКС[92]. В пользу данной рекомендации свидетельствуютрезультаты исследования COMMIT, в которое в основ-ном включали пациентов с ИМ с подъемом сегмента ST.У пациентов группы метопролола частота кардиогенно-го шока была значительно выше, чем в контрольнойгруппе (5,0% и 3,9%; p<0,0001) [93]. После исклю-чения результатов COMMIT из мета-анализа было вы-явлено изменение относительного риска (ОР) госпиталь-ной летальности [ОР 0,86; 95% доверительный интер-вал (ДИ) 0,77–0,96] в пользу бета-адреноблокатора[92].НитратыПрименение нитратов при нестабильной стенокар-дии преимущественно основывается на патофизиоло-гических данных и клиническом опыте. Терапевтическиеэффекты нитратов и сходных препаратов, таких как син-донимины, связано с действием на периферические икоронарные сосуды. В основном эффективность нит-ратов, вероятно, отражает дилатацию вен, котораяприводит к снижению преднагрузки миокарда и конеч-ного диастолического объема левого желудочка, в ре-зультате чего уменьшается потребление миокардом кис-лорода. Кроме того, нитраты расширяют нормаль-ные, а также атеросклеротически измененные коронар-ные артерии и увеличивают коронарный коллатераль-ный кровоток.Исследования нитратов у пациентов с нестабильнойстенокардией были небольшими и неконтролируе-мыми. Эффективность этих препаратов в профилакти-ке неблагоприятных сердечно-сосудистых исходов в ран-домизированных плацебо-контролируемых исследо-ваниях не изучалась. Хотя при анализе результатов ис-следования TIMI-7 не был подтвержден протективныйэффект хронической терапии нитратами в отношениинестабильной стенокардии или ИМ [94], в регистреGRACE применение нитратов ассоциировалось с изме-нением структуры ОКС в пользу развития ОКС безподъема сегмента ST, а не ИМ с подъемом сегмента ST,и с уменьшением уровней маркеров некроза миокар-да [95].У пациентов с ОКС без подъема сегмента ST, кото-рым необходима госпитализация, внутривенное вве-дение нитратов купирует симптомы и вызывает регрессдепрессии сегмента ST более эффективно, чем их суб-лингвальное применение [96]. Дозу следует постепен-но увеличивать, пока не будут купированы симптомы(стенокардия и/или одышка), при условии отсутствияпобочных эффектов (особенно головной боли илигипотонии). При постоянном приеме нитратов разви-вается привыкание, которое зависит как от дозы, так иот длительности лечения.Нитраты не следует назначать пациентам, принимаю-щим ингибиторы фосфодиэстеразы-5 (силденафил,варденафил или тадалафил), учитывая риск выражен-ной вазодилатации и критического снижения АД.
Рекомендации по применению антиишемических препаратов
Риск в отдаленном периоде
Помимо факторов, позволяющих предсказать бли-жайший прогноз, выделяют также предикторы риска вотдаленном периоде. Они имеют важное значениедля пересмотра риска и могут привести к интенсифи-кации начальной тактики лечения. К таким факторамотносят осложненное течение ОКС, систолическуюфункцию левого желудочка, тяжесть ИБС, наличиереваскуляризации и признаки резидуальной ишемиипо данным неинвазивных методов.
Лечение
Антиишемические препараты
Антиишемические препараты снижают потребностьмиокарда в кислороде (за счет уменьшения частоты сер-дечных сокращений, АД, преднагрузки или сократимо-сти миокарда) или увеличивают доставку кислорода кмиокарду (за счет дилатации коронарных артерий).Бета-адреноблокаторыБета-адреноблокаторы подавляют эффекты цирку-лирующих катехоламинов на миокард и уменьшают по-требность его в кислороде за счет снижения частоты сер-дечных сокращений, АД и сократимости. Благоприятныеэффекты бета-адреноблокаторов были установлены упациентов с ИМ с подъемом сегмента ST и стабильнойстенокардией [85,86]. В двух двойных слепых рандо-мизированных исследованиях бета-адреноблокаторысравнивали с плацебо у пациентов с нестабильнойстенокардией [87,88]. При мета-анализе было показа-но, что лечение бета-адреноблокатором вызывает сни-жение относительного риска прогрессирования и раз-вития ИМ с подъемом сегмента ST на 13% [89]. Хотя вэтих относительно небольших исследованиях не былоподтверждено снижение смертности у пациентов сОКС без подъема сегмента ST, тем не менее, можно экс-траполировать результаты более крупных рандомизи-рованных исследований бета-адреноблокаторов убольных ИМ [90]. В регистре CRUSADE, в которыйвключали пациентов с ИМ без подъема сегментаST/нестабильной стенокардией из 509 американскихбольниц с 2001 по 2004 гг., у больных, получавших бета-адреноблокаторы в острый период, выявили снижениескорректированного риска госпитальной летальности на34% (3,9% и 6,9%, соответственно; p<0,001) [91].При систематизированном обзоре литературы небыло убедительно подтверждено снижение госпи-тальной летальности при раннем применении бета-ад-реноблокаторов у пациентов с острым или предпола-гаемым ИМ. Был сделан вывод, что имеющиеся дан-ные не позволяют рекомендовать назначение бета-ад-реноблокаторов в первые 8 ч после развития ОКС[92]. В пользу данной рекомендации свидетельствуютрезультаты исследования COMMIT, в которое в основ-ном включали пациентов с ИМ с подъемом сегмента ST.У пациентов группы метопролола частота кардиогенно-го шока была значительно выше, чем в контрольнойгруппе (5,0% и 3,9%; p<0,0001) [93]. После исклю-чения результатов COMMIT из мета-анализа было вы-явлено изменение относительного риска (ОР) госпиталь-ной летальности [ОР 0,86; 95% доверительный интер-вал (ДИ) 0,77–0,96] в пользу бета-адреноблокатора[92].НитратыПрименение нитратов при нестабильной стенокар-дии преимущественно основывается на патофизиоло-гических данных и клиническом опыте. Терапевтическиеэффекты нитратов и сходных препаратов, таких как син-донимины, связано с действием на периферические икоронарные сосуды. В основном эффективность нит-ратов, вероятно, отражает дилатацию вен, котораяприводит к снижению преднагрузки миокарда и конеч-ного диастолического объема левого желудочка, в ре-зультате чего уменьшается потребление миокардом кис-лорода. Кроме того, нитраты расширяют нормаль-ные, а также атеросклеротически измененные коронар-ные артерии и увеличивают коронарный коллатераль-ный кровоток.Исследования нитратов у пациентов с нестабильнойстенокардией были небольшими и неконтролируе-мыми. Эффективность этих препаратов в профилакти-ке неблагоприятных сердечно-сосудистых исходов в ран-домизированных плацебо-контролируемых исследо-ваниях не изучалась. Хотя при анализе результатов ис-следования TIMI-7 не был подтвержден протективныйэффект хронической терапии нитратами в отношениинестабильной стенокардии или ИМ [94], в регистреGRACE применение нитратов ассоциировалось с изме-нением структуры ОКС в пользу развития ОКС безподъема сегмента ST, а не ИМ с подъемом сегмента ST,и с уменьшением уровней маркеров некроза миокар-да [95].У пациентов с ОКС без подъема сегмента ST, кото-рым необходима госпитализация, внутривенное вве-дение нитратов купирует симптомы и вызывает регрессдепрессии сегмента ST более эффективно, чем их суб-лингвальное применение [96]. Дозу следует постепен-но увеличивать, пока не будут купированы симптомы(стенокардия и/или одышка), при условии отсутствияпобочных эффектов (особенно головной боли илигипотонии). При постоянном приеме нитратов разви-вается привыкание, которое зависит как от дозы, так иот длительности лечения.Нитраты не следует назначать пациентам, принимаю-щим ингибиторы фосфодиэстеразы-5 (силденафил,варденафил или тадалафил), учитывая риск выражен-ной вазодилатации и критического снижения АД.
Рекомендации по применению антиишемических препаратов
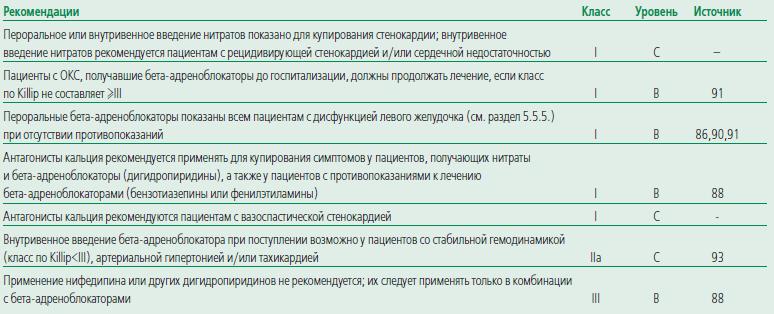 Антагонисты кальция
Антагонисты кальция — это вазодилататоры. Неко-торые из них оказывают также прямое действие на ат-риовентрикулярное проведение и частоту сердечныхсокращений. Выделяют три класса антагонистов каль-ция, которые отличаются друг от друга по химическо-му строению и фармакологическому действию: дигид-ропиридины (такие как нифедипин), бензотиазепины(дилтиазем) и фенилэтиламины (верапамил). Препа-раты этих классов отличаются по степени вазодилати-рующего действия, снижения сократимости миокардаи замедления атриовентрикулярной проводимости. Не-дигидропиридиновые антагонисты кальция могут вы-звать атриовентрикулярную блокаду. Нифедипин иамлодипин оказывают более выраженное расширяю-щее действие на периферические артерии, в то времякак дилтиазем дает менее выраженный вазодилатирую-щий эффект. Препараты всех классов оказывают сопо-ставимое расширяющее действие на коронарные ар-терии. Соответственно, антагонисты кальция — этопрепараты выбора при вазоспастической стенокар-дии. Дилтиазем и верапамил обладают сопоставимойсимптоматической эффективностью и эквивалентныбета-адреноблокаторам [97,98].Влияние антагонистов кальция на прогноз больныхОКС без подъема сегмента ST изучалось только в неболь-ших рандомизированных исследованиях. Среди дигид-ропиридинов в основном применяли нифедипин. Вовсех исследованиях лечение нифедипином было не-эффективным при ИМ или во вторичной профилакти-ке после ИМ, а исследование HINT было прекращенодосрочно в связи с более высокой частотой повторно-го ИМ в группе нифедипина по сравнению с группойметопролола [88]. Напротив, в исследованияхDAVIT-I и DAVIT-II применение верапамила привело кснижению риска внезапной смерти, повторного инфарк-та и смерти от любых причин; эффект препарата былнаиболее выраженным у пациентов с сохранной функ-цией левого желудочка [99]. Сходная тенденция былаотмечена в исследованиях дилтиазема [100]. В отли-чие от бета-адреноблокаторов антагонисты кальция, по-видимому, не обладают общими эффектами, характер-ными для всего класса.Другие антиангинальные препаратыНикорандил, открывающий калиевые каналы, сни-жал частоту комбинированной первичной конечной точ-ки у пациентов со стабильной стенокардией, однако онне изучался у пациентов с ОКС [101]. Ивабрадин, се-лективно ингибирующий If каналы синусового узла, мо-жет применяться у отдельных пациентов при наличиипротивопоказаний к лечению бета-адреноблокатора-ми [102]. Ранолазин оказывает антиангинальное дей-ствие за счет ингибирования позднего натриевоготока. Он не влиял на риск основных сердечно-сосуди-стых исходов в исследовании MERLIN-TIMI 36, носнижал частоту рецидивирующей ишемии [103].
Антитромбоцитарные препараты
Активация и последующая агрегация тромбоцитовиграют основную роль в развитии артериального тром-боза и, соответственно, рассматриваются как ключевыемишени при лечении ОКС. Антитромбоцитарную тера-пию следует начинать как можно раньше, чтобы сни-зить риск как острых ишемических осложнений, так иповторных атеротромботических событий. Для ингиби-рования тромбоцитов используют препараты 3 классов,которые отличаются по механизму действия.Аспирин (ацетилсалициловая кислота) ингибируетциклооксигеназу (ЦОГ-1), блокирует образованиетромбоксана А2 и вызывает необратимую блокадуфункции тромбоцитов. Однако для эффективного лечения и профилактики коронарного тромбоза необхо-димо ингибировать дополнительные пути агрегациитромбоцитов. Взаимодействие АДФ с P2Y12 рецепто-рами тромбоцитов играет важную роль в активации иагрегации тромбоцитов и усиливает начальный ответклеток на повреждение сосудов. Блокаторы P2Y12рецепторов широко применяют для лечения ОКС. Тие-нопиридины клопидогрел и прасугрел — это пролекарст-ва, которые превращаются в активные молекулы, не-обратимо связывающиеся с P2Y12 рецепторами. Новымпрепаратом является тикагрелор — производное пири-мидина, которое после биотрансформации необрати-мо связывается с P2Y12 рецепторами, блокирует сигналь-ную систему АДФ и активацию тромбоцитов. Блокато-ры GP IIb/IIIa рецепторов, предназначенные для внут-ривенного введения (абциксимаб, эптифибатид и ти-рофибан), оказывают действие на последний общийэтап агрегации тромбоцитов.
Аспирин
В исследованиях, проводившихся 30 лет назад, былопоказано, что аспирин снижает частоту повторногоИМ и смерти у пациентов с нестабильной стенокарди-ей [отношение шансов (ОШ) 0,47; 95% ДИ 0,37–0,61;р<0,001] [104–106]. Лечение рекомендуется начинатьс нагрузочной дозы обычного аспирина (150-300мг), который следует разжевать [107]. Альтернативныйпуть — внутривенное введение аспирина, однако этаформа препарата не изучалась в рандомизированныхконтролируемых исследованиях и не везде доступна.Суточная поддерживающая доза 75-100 мг по эффек-тивности сопоставима с более высокими дозами, нореже вызывает желудочно-кишечные расстройства[108]; последние служат причиной отмены препаратау 1% больных. Аллергические реакции на аспирин (ана-филактический шок, кожная сыпь и астматическиереакции) встречаются редко (<0,5%). У части пациен-тов возможно десенсибилизация.Аспирин надежно ингибирует ЦОГ-1, поэтому мо-ниторирование его эффектов при хорошей привержен-ности не требуется. Нестероидные противовоспалитель-ные препараты (НПВП), такие как ибупрофен, обрати-мо блокируют ЦОГ-1 и препятствуют ее необратимо-му ингибированию под действием аспирина, а такжемогут оказывать протромботическое действие вследствиеингибирования ЦОГ-2. Соответственно, НПВП повышаютриск ишемических осложнений, поэтому их примене-ния следует избегать [109].
Блокаторы
P2Y12 рецепторов5.2.2.1. КлопидогрелИнформация о блокаторах P2Y12 рецепторов при-ведена в табл. 7. Тиклопидин был первым тиенопири-дином, который изучался у пациентов с ОКС, однакопозднее он был заменен клопидогрелом в связи с по-бочными эффектами. Сегодня тиклопидин можноприменять у пациентов с аллергией на клопидогрел, хотявозможна перекрестная реактивность. В исследованииCURE лечение клопидогрелом в нагрузочной дозе 300мг, а затем по 75 мг/сут в течение 9-12 мес в сочета-нии с аспирином привело к снижению частоты сердеч-но-сосудистой смерти, нефатального ИМ или инсуль-та по сравнению с монотерапией аспирином (9,3% и11,4%; ОР 0,80; 95% ДИ 0,72–0,90; p<0,001) у па-циентов с ОКС без подъема сегмента ST, у которых былиповышены уровни сердечных биомаркеров или опре-делялась депрессия сегмента ST, а также у пациентов ввозрасте старше 60 лет без ИБС в анамнезе [110]. Сни-жение риска развития ИМ было достоверным. От-мечена тенденция к снижению сердечно-сосудистойсмертности и частоты инсульта. Благоприятный эффектбыл сопоставимым во всех подгруппах пациентов, от-личавшихся по уровню сердечно-сосудистого риска, атакже у пожилых людей, пациентов с отклонениями сег-мента ST от изолинии, больных с повышенными инормальными уровнями биомаркеров, перенесших ине перенесших ЧКВ, пациентов с диабетом. Эффект со-хранялся в течение первых 30 дн, а также в последую-щие 11 мес [111]. После отмены клопидогрела возмож-но увеличение риска неблагоприятных исходов, осо-бенно у пациентов, получавших консервативное лече-ние [112]. Однако польза продолжения терапии более12 мес не установлена.В группе клопидогрела выявили увеличение часто-ты больших кровотечений (3,7% и 2,7%; ОР 1,38; 95%ДИ 1,13–1,67; p=0,001), однако достоверное увеличе-ние частоты угрожающих жизни и фатальных кровотече-ний отсутствовало [110]. Во всей когорте, включаяпациентов, направленных на реваскуляризацию (ЧКВили КШ), польза клопидогрела перевешивала риск кро-вотечений. Лечение клопидогрелом у 1000 пациентовпозволяло избежать 21 случая сердечно-сосудистойсмерти, ИМ или инсульта ценой 7 дополнительных слу-чаев кровотечения, требующего трансфузии крови, и4 дополнительных случаев угрожающих жизни крово-течений [113].В нагрузочной дозе 600 мг клопидогрел оказываетболее быстрое и мощное действие, чем в дозе 300 мг[114,115]. В поддерживающей дозе 150 мг/сут клопи-догрел также давал несколько более выраженный и по-стоянный эффект, чем в дозе 75 мг/сут [116]. В иссле-довании CURRENT-OASIS [117] сравнивали эффек-тивность клопидогрела в нагрузочной дозе 600 мг, за-тем 150 мг/сут (в течение 7 дней) и 75 мг/сут и стан-дартных доз у пациентов с ИМ с подъемом сегмента STили ОКС без подъема сегмента ST. В исследованиевключали пациентов с признаками ишемии миокардаи повышенными уровнями сердечных биомаркеров. Коронарную ангиографию с целью выполнения ЧКВ про-водили как можно раньше, но не позднее, чем через72 ч после рандомизации. В целом клопидогрел в бо-лее высокой дозе не имел преимуществ перед обычнойсхемой. Частота сердечно-сосудистой смерти, ИМ илиинсульта через 30 дн была сопоставимой в двух груп-пах [4,2% и 4,4%, соответственно; ОШ 0,94; 0,83–1,06;p=0,30], однако было отмечено увеличение частотыбольших кровотечений, которые оценивали по крите-риям CURRENT (2,5% и 2,0%; ОШ 1,24; 1,05–1,46;p=0,01) или TIMI (1,7% и 1,3%; ОШ 1,26; 1,03–1,54;p=0,03), а также необходимости в гемотрансфузиях(2,2% и 1,7%; ОШ 1,28; 1,07–1,54; p=0,01). В вы-борке больных (17623 пациента; у 63,1% из нихимелся ОКС без подъема сегмента ST), которым выпол-нено ЧКВ, отмечено снижение риска комбинированнойпервичной конечной точки, включавшей в себя сердеч-но-сосудистую смерть, ИМ и инсульт (3,9% и 4,5%; ОШ0,86; 95% ДИ 0,74–0,99; p=0,039) за счет уменьше-ния частоты ИМ на фоне применения клопидогрела вболее высокой дозе (2,0% и 2,6%; ОШ 0,69; 95% ДИ0,56–0,87; p=0,001). Частота тромбоза стента [покритериям Academic Research Consortium (ARC)] значи-тельно снизилась независимо от типа стента, в том чис-ле частота определенного или вероятного тромбоза (ОШ0,69; 95% ДИ 0,56–0,87; p=0,001) и частота опреде-ленного тромбоза (ОШ 0,54; 95% ДИ 0,39–0,74;p=0,0001). Большие кровотечения, которые диагно-стировали в соответствии с критериями CURRENT, приприменении клопидогрела в двойной дозе встречалисьчаще, чем при лечении стандартной дозой (1,6% и1,1%; ОШ 1,41; 95% ДИ 1,09–1,83; p=0,009). Одна-ко частота больших кровотечений в соответствии скритериями TIMI достоверно не отличалась междугруппами (1,0% и 0,7%; ОШ 1,36; 95% ДИ 0,97–1,90;p=0,074). Значительного увеличения риска фатальныхили внутричерепных кровотечений или кровотече-ний, связанных с КШ, в основной группе не выявили.Результаты лечения существенно не отличались у паци-ентов с ИМ с подъемом сегмента ST и ОКС без подъе-ма сегмента ST. Снижение риска первичной комбини-рованной конечной точки было сопоставимым в этихдвух выборках пациентов (ИМ с подъемом сегмента ST:4,2% и 5,0%; ОШ 0,83; 95% ДИ 0,66–1,05; p=0,117;ОКС без подъема сегмента ST: 3,6% и 4,2%; ОШ0,87; 95% ДИ 0,72–1,06; p=0,167) [108].Фармакодинамический ответ на клопидогрел оченьвариабельный, что связано с несколькими факторами,включая генетический полиморфизм. Клопидогрелпревращается в активный метаболит в печени в два эта-па, которые опосредуются изоферментами цитохромаР450, включая CYP3A4 и CYP2C19. Кроме того, всасы-вание клопидогрела (и прасугрела) регулируется Р-гли-копротеином (кодируется ABCB1), который представ-ляет собой АТФ-зависимый эффлюксный насос итранспортирует различные молекулы через внекле-точные и внутриклеточные оболочки. В частности он экс-прессируется эпителиальными клетками кишечника, аповышенная экспрессия или функция Р-гликопротеи-на может отразиться на биодоступности лекарственныхвеществ, являющихся его субстратами. В результате эф-фективность образования активного метаболита кло-пидогрела значительно отличается у разных людей и за-висит (в числе других факторов, таких как возраст, на-личие диабета и функция почек) от генетических поли-морфизмов, определяющих функцию Р-гликопротеи-на и CYP2C19 [118]. Нуклеотидные полиморфизмыABCB1 и CYP2C19, сопровождающиеся частичной илиполной утратой функции ферментов, ассоциировалисьс уменьшением степени ингибирования агрегациитромбоцитов и увеличением риска сердечно-сосуди-стых исходов, хотя результаты исследований, посвящен-ных этому вопросу, были противоречивыми [119,120].Хотя генетические тесты не являются рутинными в кли-нической практике, предпринимались попытки иден-тификации пациентов, плохо отвечающих на клопидо-грел, на основании анализа функции тромбоцитов exvivo [121]. Сохранение высокой реактивности тромбо-цитов после начала лечения клопидогрелом ассоции-ровалось с повышенным риском тромбоза стента и дру-гих ишемических исходов [122,123]. Однако клиниче-ское значение тестирования функции тромбоцитовокончательно не установлено. В единственном рандо-мизированном исследовании, в котором дозу клопи-догрела адаптировали с учетом остаточной реактивно-сти тромбоцитов, не было отмечено клинических пре-имуществ увеличения дозы препарата, несмотря на уме-ренное усиление блокады функции тромбоцитов [124].В настоящее время проводятся несколько исследова-ний с целью изучения целесообразности модификацииантитромбоцитарной терапии на основании результа-тов анализа функции тромбоцитов, однако в настоящеевремя рекомендовать измерение агрегации тромбоци-тов при лечении клопидогрелом у больных ОК Снельзя.Ингибиторы протонной помпы, которые подав-ляют CYP2C19, особенно омепразол, снижают антитром-боцитарную активность клопидогрела ex vivo, однакоубедительных клинических данных, подтверждающихвозможность увеличения риска ишемических исходовпри сочетанном применении клопидогрела и ингиби-торов протонной помпы, нет [125,126]. В одном ран-домизированном исследовании (было прекращенодосрочно в связи с отсутствием спонсора) сравнивалирезультаты применения клопидогрела в сочетании с оме-празолом и одного клопидогрела в течение 12 мес у па-циентов, нуждавшихся в двойной антитромбоцитарнойтерапии, включая больных, перенесших ЧКВ, пациен
Таблица 7. Результаты исследований блокаторов P2Y12 рецепторов
Антагонисты кальция
Антагонисты кальция — это вазодилататоры. Неко-торые из них оказывают также прямое действие на ат-риовентрикулярное проведение и частоту сердечныхсокращений. Выделяют три класса антагонистов каль-ция, которые отличаются друг от друга по химическо-му строению и фармакологическому действию: дигид-ропиридины (такие как нифедипин), бензотиазепины(дилтиазем) и фенилэтиламины (верапамил). Препа-раты этих классов отличаются по степени вазодилати-рующего действия, снижения сократимости миокардаи замедления атриовентрикулярной проводимости. Не-дигидропиридиновые антагонисты кальция могут вы-звать атриовентрикулярную блокаду. Нифедипин иамлодипин оказывают более выраженное расширяю-щее действие на периферические артерии, в то времякак дилтиазем дает менее выраженный вазодилатирую-щий эффект. Препараты всех классов оказывают сопо-ставимое расширяющее действие на коронарные ар-терии. Соответственно, антагонисты кальция — этопрепараты выбора при вазоспастической стенокар-дии. Дилтиазем и верапамил обладают сопоставимойсимптоматической эффективностью и эквивалентныбета-адреноблокаторам [97,98].Влияние антагонистов кальция на прогноз больныхОКС без подъема сегмента ST изучалось только в неболь-ших рандомизированных исследованиях. Среди дигид-ропиридинов в основном применяли нифедипин. Вовсех исследованиях лечение нифедипином было не-эффективным при ИМ или во вторичной профилакти-ке после ИМ, а исследование HINT было прекращенодосрочно в связи с более высокой частотой повторно-го ИМ в группе нифедипина по сравнению с группойметопролола [88]. Напротив, в исследованияхDAVIT-I и DAVIT-II применение верапамила привело кснижению риска внезапной смерти, повторного инфарк-та и смерти от любых причин; эффект препарата былнаиболее выраженным у пациентов с сохранной функ-цией левого желудочка [99]. Сходная тенденция былаотмечена в исследованиях дилтиазема [100]. В отли-чие от бета-адреноблокаторов антагонисты кальция, по-видимому, не обладают общими эффектами, характер-ными для всего класса.Другие антиангинальные препаратыНикорандил, открывающий калиевые каналы, сни-жал частоту комбинированной первичной конечной точ-ки у пациентов со стабильной стенокардией, однако онне изучался у пациентов с ОКС [101]. Ивабрадин, се-лективно ингибирующий If каналы синусового узла, мо-жет применяться у отдельных пациентов при наличиипротивопоказаний к лечению бета-адреноблокатора-ми [102]. Ранолазин оказывает антиангинальное дей-ствие за счет ингибирования позднего натриевоготока. Он не влиял на риск основных сердечно-сосуди-стых исходов в исследовании MERLIN-TIMI 36, носнижал частоту рецидивирующей ишемии [103].
Антитромбоцитарные препараты
Активация и последующая агрегация тромбоцитовиграют основную роль в развитии артериального тром-боза и, соответственно, рассматриваются как ключевыемишени при лечении ОКС. Антитромбоцитарную тера-пию следует начинать как можно раньше, чтобы сни-зить риск как острых ишемических осложнений, так иповторных атеротромботических событий. Для ингиби-рования тромбоцитов используют препараты 3 классов,которые отличаются по механизму действия.Аспирин (ацетилсалициловая кислота) ингибируетциклооксигеназу (ЦОГ-1), блокирует образованиетромбоксана А2 и вызывает необратимую блокадуфункции тромбоцитов. Однако для эффективного лечения и профилактики коронарного тромбоза необхо-димо ингибировать дополнительные пути агрегациитромбоцитов. Взаимодействие АДФ с P2Y12 рецепто-рами тромбоцитов играет важную роль в активации иагрегации тромбоцитов и усиливает начальный ответклеток на повреждение сосудов. Блокаторы P2Y12рецепторов широко применяют для лечения ОКС. Тие-нопиридины клопидогрел и прасугрел — это пролекарст-ва, которые превращаются в активные молекулы, не-обратимо связывающиеся с P2Y12 рецепторами. Новымпрепаратом является тикагрелор — производное пири-мидина, которое после биотрансформации необрати-мо связывается с P2Y12 рецепторами, блокирует сигналь-ную систему АДФ и активацию тромбоцитов. Блокато-ры GP IIb/IIIa рецепторов, предназначенные для внут-ривенного введения (абциксимаб, эптифибатид и ти-рофибан), оказывают действие на последний общийэтап агрегации тромбоцитов.
Аспирин
В исследованиях, проводившихся 30 лет назад, былопоказано, что аспирин снижает частоту повторногоИМ и смерти у пациентов с нестабильной стенокарди-ей [отношение шансов (ОШ) 0,47; 95% ДИ 0,37–0,61;р<0,001] [104–106]. Лечение рекомендуется начинатьс нагрузочной дозы обычного аспирина (150-300мг), который следует разжевать [107]. Альтернативныйпуть — внутривенное введение аспирина, однако этаформа препарата не изучалась в рандомизированныхконтролируемых исследованиях и не везде доступна.Суточная поддерживающая доза 75-100 мг по эффек-тивности сопоставима с более высокими дозами, нореже вызывает желудочно-кишечные расстройства[108]; последние служат причиной отмены препаратау 1% больных. Аллергические реакции на аспирин (ана-филактический шок, кожная сыпь и астматическиереакции) встречаются редко (<0,5%). У части пациен-тов возможно десенсибилизация.Аспирин надежно ингибирует ЦОГ-1, поэтому мо-ниторирование его эффектов при хорошей привержен-ности не требуется. Нестероидные противовоспалитель-ные препараты (НПВП), такие как ибупрофен, обрати-мо блокируют ЦОГ-1 и препятствуют ее необратимо-му ингибированию под действием аспирина, а такжемогут оказывать протромботическое действие вследствиеингибирования ЦОГ-2. Соответственно, НПВП повышаютриск ишемических осложнений, поэтому их примене-ния следует избегать [109].
Блокаторы
P2Y12 рецепторов5.2.2.1. КлопидогрелИнформация о блокаторах P2Y12 рецепторов при-ведена в табл. 7. Тиклопидин был первым тиенопири-дином, который изучался у пациентов с ОКС, однакопозднее он был заменен клопидогрелом в связи с по-бочными эффектами. Сегодня тиклопидин можноприменять у пациентов с аллергией на клопидогрел, хотявозможна перекрестная реактивность. В исследованииCURE лечение клопидогрелом в нагрузочной дозе 300мг, а затем по 75 мг/сут в течение 9-12 мес в сочета-нии с аспирином привело к снижению частоты сердеч-но-сосудистой смерти, нефатального ИМ или инсуль-та по сравнению с монотерапией аспирином (9,3% и11,4%; ОР 0,80; 95% ДИ 0,72–0,90; p<0,001) у па-циентов с ОКС без подъема сегмента ST, у которых былиповышены уровни сердечных биомаркеров или опре-делялась депрессия сегмента ST, а также у пациентов ввозрасте старше 60 лет без ИБС в анамнезе [110]. Сни-жение риска развития ИМ было достоверным. От-мечена тенденция к снижению сердечно-сосудистойсмертности и частоты инсульта. Благоприятный эффектбыл сопоставимым во всех подгруппах пациентов, от-личавшихся по уровню сердечно-сосудистого риска, атакже у пожилых людей, пациентов с отклонениями сег-мента ST от изолинии, больных с повышенными инормальными уровнями биомаркеров, перенесших ине перенесших ЧКВ, пациентов с диабетом. Эффект со-хранялся в течение первых 30 дн, а также в последую-щие 11 мес [111]. После отмены клопидогрела возмож-но увеличение риска неблагоприятных исходов, осо-бенно у пациентов, получавших консервативное лече-ние [112]. Однако польза продолжения терапии более12 мес не установлена.В группе клопидогрела выявили увеличение часто-ты больших кровотечений (3,7% и 2,7%; ОР 1,38; 95%ДИ 1,13–1,67; p=0,001), однако достоверное увеличе-ние частоты угрожающих жизни и фатальных кровотече-ний отсутствовало [110]. Во всей когорте, включаяпациентов, направленных на реваскуляризацию (ЧКВили КШ), польза клопидогрела перевешивала риск кро-вотечений. Лечение клопидогрелом у 1000 пациентовпозволяло избежать 21 случая сердечно-сосудистойсмерти, ИМ или инсульта ценой 7 дополнительных слу-чаев кровотечения, требующего трансфузии крови, и4 дополнительных случаев угрожающих жизни крово-течений [113].В нагрузочной дозе 600 мг клопидогрел оказываетболее быстрое и мощное действие, чем в дозе 300 мг[114,115]. В поддерживающей дозе 150 мг/сут клопи-догрел также давал несколько более выраженный и по-стоянный эффект, чем в дозе 75 мг/сут [116]. В иссле-довании CURRENT-OASIS [117] сравнивали эффек-тивность клопидогрела в нагрузочной дозе 600 мг, за-тем 150 мг/сут (в течение 7 дней) и 75 мг/сут и стан-дартных доз у пациентов с ИМ с подъемом сегмента STили ОКС без подъема сегмента ST. В исследованиевключали пациентов с признаками ишемии миокардаи повышенными уровнями сердечных биомаркеров. Коронарную ангиографию с целью выполнения ЧКВ про-водили как можно раньше, но не позднее, чем через72 ч после рандомизации. В целом клопидогрел в бо-лее высокой дозе не имел преимуществ перед обычнойсхемой. Частота сердечно-сосудистой смерти, ИМ илиинсульта через 30 дн была сопоставимой в двух груп-пах [4,2% и 4,4%, соответственно; ОШ 0,94; 0,83–1,06;p=0,30], однако было отмечено увеличение частотыбольших кровотечений, которые оценивали по крите-риям CURRENT (2,5% и 2,0%; ОШ 1,24; 1,05–1,46;p=0,01) или TIMI (1,7% и 1,3%; ОШ 1,26; 1,03–1,54;p=0,03), а также необходимости в гемотрансфузиях(2,2% и 1,7%; ОШ 1,28; 1,07–1,54; p=0,01). В вы-борке больных (17623 пациента; у 63,1% из нихимелся ОКС без подъема сегмента ST), которым выпол-нено ЧКВ, отмечено снижение риска комбинированнойпервичной конечной точки, включавшей в себя сердеч-но-сосудистую смерть, ИМ и инсульт (3,9% и 4,5%; ОШ0,86; 95% ДИ 0,74–0,99; p=0,039) за счет уменьше-ния частоты ИМ на фоне применения клопидогрела вболее высокой дозе (2,0% и 2,6%; ОШ 0,69; 95% ДИ0,56–0,87; p=0,001). Частота тромбоза стента [покритериям Academic Research Consortium (ARC)] значи-тельно снизилась независимо от типа стента, в том чис-ле частота определенного или вероятного тромбоза (ОШ0,69; 95% ДИ 0,56–0,87; p=0,001) и частота опреде-ленного тромбоза (ОШ 0,54; 95% ДИ 0,39–0,74;p=0,0001). Большие кровотечения, которые диагно-стировали в соответствии с критериями CURRENT, приприменении клопидогрела в двойной дозе встречалисьчаще, чем при лечении стандартной дозой (1,6% и1,1%; ОШ 1,41; 95% ДИ 1,09–1,83; p=0,009). Одна-ко частота больших кровотечений в соответствии скритериями TIMI достоверно не отличалась междугруппами (1,0% и 0,7%; ОШ 1,36; 95% ДИ 0,97–1,90;p=0,074). Значительного увеличения риска фатальныхили внутричерепных кровотечений или кровотече-ний, связанных с КШ, в основной группе не выявили.Результаты лечения существенно не отличались у паци-ентов с ИМ с подъемом сегмента ST и ОКС без подъе-ма сегмента ST. Снижение риска первичной комбини-рованной конечной точки было сопоставимым в этихдвух выборках пациентов (ИМ с подъемом сегмента ST:4,2% и 5,0%; ОШ 0,83; 95% ДИ 0,66–1,05; p=0,117;ОКС без подъема сегмента ST: 3,6% и 4,2%; ОШ0,87; 95% ДИ 0,72–1,06; p=0,167) [108].Фармакодинамический ответ на клопидогрел оченьвариабельный, что связано с несколькими факторами,включая генетический полиморфизм. Клопидогрелпревращается в активный метаболит в печени в два эта-па, которые опосредуются изоферментами цитохромаР450, включая CYP3A4 и CYP2C19. Кроме того, всасы-вание клопидогрела (и прасугрела) регулируется Р-гли-копротеином (кодируется ABCB1), который представ-ляет собой АТФ-зависимый эффлюксный насос итранспортирует различные молекулы через внекле-точные и внутриклеточные оболочки. В частности он экс-прессируется эпителиальными клетками кишечника, аповышенная экспрессия или функция Р-гликопротеи-на может отразиться на биодоступности лекарственныхвеществ, являющихся его субстратами. В результате эф-фективность образования активного метаболита кло-пидогрела значительно отличается у разных людей и за-висит (в числе других факторов, таких как возраст, на-личие диабета и функция почек) от генетических поли-морфизмов, определяющих функцию Р-гликопротеи-на и CYP2C19 [118]. Нуклеотидные полиморфизмыABCB1 и CYP2C19, сопровождающиеся частичной илиполной утратой функции ферментов, ассоциировалисьс уменьшением степени ингибирования агрегациитромбоцитов и увеличением риска сердечно-сосуди-стых исходов, хотя результаты исследований, посвящен-ных этому вопросу, были противоречивыми [119,120].Хотя генетические тесты не являются рутинными в кли-нической практике, предпринимались попытки иден-тификации пациентов, плохо отвечающих на клопидо-грел, на основании анализа функции тромбоцитов exvivo [121]. Сохранение высокой реактивности тромбо-цитов после начала лечения клопидогрелом ассоции-ровалось с повышенным риском тромбоза стента и дру-гих ишемических исходов [122,123]. Однако клиниче-ское значение тестирования функции тромбоцитовокончательно не установлено. В единственном рандо-мизированном исследовании, в котором дозу клопи-догрела адаптировали с учетом остаточной реактивно-сти тромбоцитов, не было отмечено клинических пре-имуществ увеличения дозы препарата, несмотря на уме-ренное усиление блокады функции тромбоцитов [124].В настоящее время проводятся несколько исследова-ний с целью изучения целесообразности модификацииантитромбоцитарной терапии на основании результа-тов анализа функции тромбоцитов, однако в настоящеевремя рекомендовать измерение агрегации тромбоци-тов при лечении клопидогрелом у больных ОК Снельзя.Ингибиторы протонной помпы, которые подав-ляют CYP2C19, особенно омепразол, снижают антитром-боцитарную активность клопидогрела ex vivo, однакоубедительных клинических данных, подтверждающихвозможность увеличения риска ишемических исходовпри сочетанном применении клопидогрела и ингиби-торов протонной помпы, нет [125,126]. В одном ран-домизированном исследовании (было прекращенодосрочно в связи с отсутствием спонсора) сравнивалирезультаты применения клопидогрела в сочетании с оме-празолом и одного клопидогрела в течение 12 мес у па-циентов, нуждавшихся в двойной антитромбоцитарнойтерапии, включая больных, перенесших ЧКВ, пациен
Таблица 7. Результаты исследований блокаторов P2Y12 рецепторов
 тов с ОКС и др. Увеличения частоты ишемических ис-ходов отмечено не было, однако в группе омепразоланаблюдалось снижение риска кровотечений из верх-них отделов желудочно-кишечного тракта [127]. Часто-та ишемических событий была низкой, что не позволяетсделать вывод о влиянии омепразола на эффективностьклопидогрела у пациентов более высокого риска.Мощные ингибиторы (например, кетоконазол) или ин-дукторы (например, рифампицин) CYP3A4 могутзначительно снизить или усилить, соответственно, ин-гибирующий эффект клопидогрела, однако эти препа-раты редко применяют у пациентов с ОКС без подъе-ма сегмента ST.Нежелательные эффекты клопидогрела. Помимокровотечений при лечении клопидогрелом могут наблю-даться желудочно-кишечные расстройства (диарея,дискомфорт в животе) и сыпь. Тромботическая тром-боцитопеническая пурпура и дискразии крови встре-чаются редко. При аллергии на клопидогрел возмож-на десенсибилизация.5.2.2.2. ПрасугрелПрасугрел в два этапа превращается в активный ме-таболит, который по химическому строению сходен с ак-тивным метаболитом клопидогрела [119]. Первыйэтап биотрансформации происходит под действиемэстераз плазмы, а второй осуществляется в печени приучастии изоферментов CYP. Соответственно, прасу-грел оказывает более быстрое и постоянное ингибирую-щее действие на тромбоциты по сравнению с клопидо-грелом [128]. Ответ на прасугрел существенно не зави-сит от действия ингибиторов CYP, включая ингибиторыпротонной помпы, и полиморфизма гена CYP2C19, атакже функции ABCB1 [129].В исследовании TRITON-TIMI 38 сравнивали прасу-грел в нагрузочной дозе 60 мг, а затем 10 мг/сут и кло-пидогрел в нагрузочной дозе 300 мг, а затем 75 мг/сутпосле ЧКВ у пациентов, не получавших ранее клопидо-грел; показаниями к ЧКВ были острый ИМ с подъемомсегмента ST (первичное вмешательство) или недавноперенесенный ИМ с подъемом сегмента ST, а также ОКСбез подъема сегмента у пациентов среднего или высо-кого риска [130]. Пациентов с ОКС без подъема сегмен-та ST, которым проводилось консервативное лечение,в исследование не включали. Критериями включениябыли симптомы ишемии в течение 72 ч, индекс рискаTIMI≥3 и отклонение сегмента ST≥1 или повышенныеуровни сердечного биомаркера. В когорте пациентовс ОКС без подъема сегмента ST (n=10074) лечение ис-следуемым препаратом начинали в течение 1 ч послеангиографии, подтвердившей возможность ЧКВ. Ча-стота комбинированной первичной конечной точки (сер-дечно-сосудистая смерть, нефатальный ИМ или инсульт)составила 11,2% в группе клопидогрела и 9,3% в груп-пе прасугрела (ОШ 0,82; 95% ДИ 0,73–0,93; p=0,002);снижение ее частоты во второй группе в основном от-ражало достоверное снижение риска развития ИМ(с 9,2% до 7,1%; на 23,9%; 95% ДИ 12,7–33,7;p<0,001) [130]. Частота нефатального инсульта или сер-дечно-сосудистой смерти достоверно не отличаласьмежду группами. Во всей когорте частота определен-ного или вероятного тромбоза стента (ко критериямARC) в группе прасугрела значительно снизилась посравнению с группой клопидогрела (1,1% и 2,4%,соответственно; ОШ 0,48; 95% ДИ 0,36–0,64;p<0,001). Соответствующие показатели у пациентов сОКС без подъема сегмента SТ не известны.Во всей когорте в группе прасугрела отмечалосьзначительное увеличение частоты больших (по крите-риям TIMI) кровотечений, не связанных с КШ (2,4% и1,8%; ОШ 1,32; 95% ДИ 1,03–1,68; p=0,03), в основ-ном за счет спонтанных кровотечений (1,6% и 1,1%;ОШ 1,51; 95% ДИ 1,09–2,08; p=0,01), а не кровотече-ний, связанных с пункцией артерии (0,7% и 0,6%; ОШ1,18; 95% ДИ 0,77–1,82; p=0,45). В группе прасугре-ла значительно увеличился риск угрожающих жизникровотечений (1,4% и 0,9%; ОШ 1,52; 95% ДИ1,08–2,13; p=0,01), а также фатальных кровотечений(0,4% и 0,1%; ОШ 4,19; 95% ДИ 1,58–11,11;p=0,002). У пациентов с цереброваскулярными нару-шениями в анамнезе риск кровотечений при лечениипрасугрелом перевешивал его пользу [130]. Кроме того,не было отмечено «чистой» клинической пользы лече-ния у пациентов в возрасте ≥75 лет и больных с низкоймассой тела (≤60 кг). Более выраженный клиническийэффект без увеличения риска кровотечений наблюдал-ся у пациентов с диабетом. У пациентов с нарушениемфункции почек (клиренс креатинина≤60 мл/мин) и нор-мальной функцией почек (клиренс креатинина>60мл/мин) эффективность препарата не отличалась.Нежелательные эффекты прасугрела. Частота дру-гих нежелательных явлений в исследовании TRITONбыла сопоставимой в группах прасугрела и клопидо-грела. Тромбоцитопения встречалась в двух группах содинаковой частотой (0,3%), в то время как нейтропе-ния реже развивалась в группе прасугрела (<0,1% и0,2%; p=0,02).5.2.2.3. ТикагрелорТикагрелор принадлежит к новому химическомуклассу (циклопентилтриазолопиримидины) и являет-ся пероральным обратимым ингибитором P2Y12рецепторов с периодом полувыведения из плазмыоколо 12 ч. Степень блокады P2Y12 рецепторов зави-сит от уровня тикагрелора в плазме и в меньшей сте-пени его метаболита. Как и прасугрел, он оказывает бо-лее быстрое и постоянное действие, чем клопидо-грел. Кроме того, его действие прекращается быстрее, поэтому функция тромбоцитов также восстанавлива-ется в более короткие сроки (табл. 8) [131]. Тикагре-лор увеличивает уровни препаратов, которые метабо-лизируются под действием CYP3A, таких как симваста-тин, в то время как умеренные ингибиторы CYP3A, та-кие как дилтиазем, увеличивают уровни и снижают ско-рость прекращения действия тикагрелора.
Таблица 8. Блокаторы P2Y12 рецепторов
тов с ОКС и др. Увеличения частоты ишемических ис-ходов отмечено не было, однако в группе омепразоланаблюдалось снижение риска кровотечений из верх-них отделов желудочно-кишечного тракта [127]. Часто-та ишемических событий была низкой, что не позволяетсделать вывод о влиянии омепразола на эффективностьклопидогрела у пациентов более высокого риска.Мощные ингибиторы (например, кетоконазол) или ин-дукторы (например, рифампицин) CYP3A4 могутзначительно снизить или усилить, соответственно, ин-гибирующий эффект клопидогрела, однако эти препа-раты редко применяют у пациентов с ОКС без подъе-ма сегмента ST.Нежелательные эффекты клопидогрела. Помимокровотечений при лечении клопидогрелом могут наблю-даться желудочно-кишечные расстройства (диарея,дискомфорт в животе) и сыпь. Тромботическая тром-боцитопеническая пурпура и дискразии крови встре-чаются редко. При аллергии на клопидогрел возмож-на десенсибилизация.5.2.2.2. ПрасугрелПрасугрел в два этапа превращается в активный ме-таболит, который по химическому строению сходен с ак-тивным метаболитом клопидогрела [119]. Первыйэтап биотрансформации происходит под действиемэстераз плазмы, а второй осуществляется в печени приучастии изоферментов CYP. Соответственно, прасу-грел оказывает более быстрое и постоянное ингибирую-щее действие на тромбоциты по сравнению с клопидо-грелом [128]. Ответ на прасугрел существенно не зави-сит от действия ингибиторов CYP, включая ингибиторыпротонной помпы, и полиморфизма гена CYP2C19, атакже функции ABCB1 [129].В исследовании TRITON-TIMI 38 сравнивали прасу-грел в нагрузочной дозе 60 мг, а затем 10 мг/сут и кло-пидогрел в нагрузочной дозе 300 мг, а затем 75 мг/сутпосле ЧКВ у пациентов, не получавших ранее клопидо-грел; показаниями к ЧКВ были острый ИМ с подъемомсегмента ST (первичное вмешательство) или недавноперенесенный ИМ с подъемом сегмента ST, а также ОКСбез подъема сегмента у пациентов среднего или высо-кого риска [130]. Пациентов с ОКС без подъема сегмен-та ST, которым проводилось консервативное лечение,в исследование не включали. Критериями включениябыли симптомы ишемии в течение 72 ч, индекс рискаTIMI≥3 и отклонение сегмента ST≥1 или повышенныеуровни сердечного биомаркера. В когорте пациентовс ОКС без подъема сегмента ST (n=10074) лечение ис-следуемым препаратом начинали в течение 1 ч послеангиографии, подтвердившей возможность ЧКВ. Ча-стота комбинированной первичной конечной точки (сер-дечно-сосудистая смерть, нефатальный ИМ или инсульт)составила 11,2% в группе клопидогрела и 9,3% в груп-пе прасугрела (ОШ 0,82; 95% ДИ 0,73–0,93; p=0,002);снижение ее частоты во второй группе в основном от-ражало достоверное снижение риска развития ИМ(с 9,2% до 7,1%; на 23,9%; 95% ДИ 12,7–33,7;p<0,001) [130]. Частота нефатального инсульта или сер-дечно-сосудистой смерти достоверно не отличаласьмежду группами. Во всей когорте частота определен-ного или вероятного тромбоза стента (ко критериямARC) в группе прасугрела значительно снизилась посравнению с группой клопидогрела (1,1% и 2,4%,соответственно; ОШ 0,48; 95% ДИ 0,36–0,64;p<0,001). Соответствующие показатели у пациентов сОКС без подъема сегмента SТ не известны.Во всей когорте в группе прасугрела отмечалосьзначительное увеличение частоты больших (по крите-риям TIMI) кровотечений, не связанных с КШ (2,4% и1,8%; ОШ 1,32; 95% ДИ 1,03–1,68; p=0,03), в основ-ном за счет спонтанных кровотечений (1,6% и 1,1%;ОШ 1,51; 95% ДИ 1,09–2,08; p=0,01), а не кровотече-ний, связанных с пункцией артерии (0,7% и 0,6%; ОШ1,18; 95% ДИ 0,77–1,82; p=0,45). В группе прасугре-ла значительно увеличился риск угрожающих жизникровотечений (1,4% и 0,9%; ОШ 1,52; 95% ДИ1,08–2,13; p=0,01), а также фатальных кровотечений(0,4% и 0,1%; ОШ 4,19; 95% ДИ 1,58–11,11;p=0,002). У пациентов с цереброваскулярными нару-шениями в анамнезе риск кровотечений при лечениипрасугрелом перевешивал его пользу [130]. Кроме того,не было отмечено «чистой» клинической пользы лече-ния у пациентов в возрасте ≥75 лет и больных с низкоймассой тела (≤60 кг). Более выраженный клиническийэффект без увеличения риска кровотечений наблюдал-ся у пациентов с диабетом. У пациентов с нарушениемфункции почек (клиренс креатинина≤60 мл/мин) и нор-мальной функцией почек (клиренс креатинина>60мл/мин) эффективность препарата не отличалась.Нежелательные эффекты прасугрела. Частота дру-гих нежелательных явлений в исследовании TRITONбыла сопоставимой в группах прасугрела и клопидо-грела. Тромбоцитопения встречалась в двух группах содинаковой частотой (0,3%), в то время как нейтропе-ния реже развивалась в группе прасугрела (<0,1% и0,2%; p=0,02).5.2.2.3. ТикагрелорТикагрелор принадлежит к новому химическомуклассу (циклопентилтриазолопиримидины) и являет-ся пероральным обратимым ингибитором P2Y12рецепторов с периодом полувыведения из плазмыоколо 12 ч. Степень блокады P2Y12 рецепторов зави-сит от уровня тикагрелора в плазме и в меньшей сте-пени его метаболита. Как и прасугрел, он оказывает бо-лее быстрое и постоянное действие, чем клопидо-грел. Кроме того, его действие прекращается быстрее, поэтому функция тромбоцитов также восстанавлива-ется в более короткие сроки (табл. 8) [131]. Тикагре-лор увеличивает уровни препаратов, которые метабо-лизируются под действием CYP3A, таких как симваста-тин, в то время как умеренные ингибиторы CYP3A, та-кие как дилтиазем, увеличивают уровни и снижают ско-рость прекращения действия тикагрелора.
Таблица 8. Блокаторы P2Y12 рецепторов
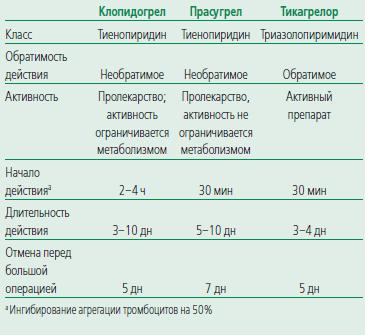 В исследовании PLATO рандомизировали пациен-тов с ОКС без подъема сегмента ST среднего или высо-кого риска (которым планировалось консервативное илиинвазивное лечение) или ИМ с подъемом сегмента ST(которым планировалось первичное ЧКВ). Пациентамназначали клопидогрел в нагрузочной дозе 300 мг, азатем по 75 мг/сут или тикагрелор в нагрузочной дозе180 мг, а затем 90 мг два раза в день [132]. При выпол-нении ЧКВ пациентам разрешалось ввести дополнитель-но нагрузочную дозу клопидогрела 300 мг (суммарнаянагрузочная доза 600 мг) или плацебо и рекомендо-валось ввести дополнительно 90 мг тикагрелора (илисоответствующего плацебо), если ЧКВ выполняли бо-лее чем через 24 ч после приема первой нагрузочнойдозы. Лечение продолжали в течение 12 мес (мини-мальная длительность составляла 6 мес, а медиана —9 мес) [132]. В целом в исследование были включены11 067 пациентов с ИМ без подъема сегмента ST илинестабильной стенокардией. Пациентов с ОКС в иссле-дование включали в течение 24 ч после появления симп-томов при наличии по крайней мере двух из следую-щих критериев: повышение биомаркеров некрозамиокарда; ишемические изменения сегмента ST; повы-шенный риск (возраст ≥60 лет, ИМ или КШ в анамне-зе, стеноз по крайней мере двух коронарных артерий≥50%, цереброваскулярная болезнь, сахарный диабет,заболевание периферических сосудов или хроническаядисфункция почек). Во всей когорте частота комбини-рованной первичной конечной точки снизилась с11,7% в группе клопидогрела до 9,8% в группе тика-грелора (ОШ 0,84; 95% ДИ 0,77–0,92; p<0,001).Смертность от сосудистых причин снизилась с 5,1% до4,0% (ОШ 0,79; 95% ДИ 0,69–0,91; p=0,001), а ча-стота ИМ — с 6,9% до 5,8% (ОШ 0,84; 95% ДИ0,75–0,95; p=0,005). Смертность от инсульта досто-верно не отличалась (1,3% и 1,5%; p=0,22). Частотаопределенного тромбоза стента снизилась с 1,9% до1,3% (p<0,01), а общая смертность — с 5,9% до4,5% (p<0,001).Частота больших кровотечений, которые диагности-ровали в соответствии с критериями PLATO, достовер-но не отличалась между группами клопидогрела и ти-кагрелора (11,2% и 11,6%, соответственно; p=0,43).Частота больших кровотечений, не связанных с КШ, уве-личилась с 3,8% в группе клопидогрела до 4,5% в груп-пе тикагрелора (ОШ 1,19; 95% ДИ 1,02–1,38; p=0,03).Частота больших кровотечений, связанных с КШ, быласопоставимой в группах тикагрелора и клопидогрела(7,4% и 7,9%, соответственно; p=0,32). Небольшиекровотечения в группе тикагрелора развивались чаще,чем в группе клопидогрела. Смертность от кровотече-ний в целом не отличалась между группами (0,3%), не-смотря на более высокую частоту фатальных внутриче-репных кровотечений в группе тикагрелора. У пациен-тов с положительным исходным тропонином частотапервичной конечной точки значительно снизилась вгруппе тикагрелора (10,3% и 12,3%; ОШ 0,85; 95%ДИ 0,77–0,94), в отличие от пациентов с нормальнымуровнем тропонина (7,0% и 7,0%). Значительноеснижение риска первичной конечной точки выявили так-же у пациентов с окончательным диагнозом ИМ безподъема сегмента ST (11,4% и 13,9%; ОШ 0,83;95% ДИ 0,73–0,94), в отличие от пациентов с оконча-тельным диагнозом нестабильной стенокардии (8,6%и 9,1%, соответственно; ОШ 0,96; 95% ДИ 0,75–1,22).Хотя снижение частоты тромбоза стента при лечении ти-кагрелором было отмечено в ранние сроки [133],благоприятный эффект на риск ИМ и смерти продол-жал нарастать в течение 12 мес [132].Тикагрелор снижал раннюю и позднюю смертностьпосле КШ. У 1 261 пациента, перенесшего КШ и полу-чавшего исследуемый препарат в течение <7 дн до опе-рации, частота комбинированной первичной конечнойточки составила 10,6% в группе тикагрелора и 13,1%в группе клопидогрела (ОШ 0,84; 95% ДИ 0,60–1,16;p=0,29). Общая смертность при лечении тикагрелоромснизилась с 9,7% до 4,7% (ОШ 0,49; ДИ 0,32–0,77;p<0,01), сердечно-сосудистая смертность — с 7,9% до4,1% (ОШ 0,52; 95% ДИ 0,32–0,85; p<0,01), смерт-ность от других причин — с 2,0% до 0,7% (p=0,07). Ча-стота больших кровотечений, связанных с КШ, досто-верно не отличалась между двумя группами. В соответствии с протоколом, лечение тикагрелором возобнов-ляли, когда его применение считалось безопасным с точ-ки зрения кровотечений (см. ниже) [134].Нежелательные эффекты тикагрелора. Помимо уве-личения частоты небольших и не связанных с КШбольших кровотечений нежелательные эффекты тика-грелора включали в себя одышку, увеличение частотыжелудочковых пауз и бессимптомной гиперурикемии[132,135,136]. Одышка, вызванная тикагрелором,чаще всего (до 15%) развивается в течение первой не-дели после начала лечения и может быть преходящейили сохраняется до прекращения лечения, однако онаобычно не требует прекращения лечения [132,137].Одышка, по-видимому, не связана с ухудшением функ-ции сердца или легких [137]. Желудочковые паузы приприменении тикагрелора в основном представляют со-бой бессимптомные эпизоды ночной синоатриаль-ной блокады. Рекомендуется соблюдать осторожностьу пациентов с выраженной синоатриальной блокадойили атриовентрикулярной блокадой II-III степени, еслипациенту не установлен постоянный водитель ритма. Ме-ханизмы развития одышки и желудочковых пауз не уста-новлены [137]. В исследовании PLATO в группе тика-грелора было выявлено несколько более выраженноеувеличение сывороточного уровня креатинина, од-нако разница между группами отсутствовала через 1 меспосле прекращения лечения [132]. Частота желудочно-кишечных расстройств и сыпи была сходной в двух груп-пах [136].5.2.2.4. Отмена блокаторов P2Y12 рецепторовперед операциейУ пациентов с ОКС без подъема сегмента ST двой-ную антитромбоцитарную терапию следует начинатьрано, так как польза перевешивает риск во всех случаях.Высказывалось предположение, что тиенопиридины сле-дует на время отменить перед ангиографией, учитываявозможную необходимость в КШ. В нескольких иссле-дованиях было отмечено увеличение риска большихкровотечений у пациентов, получавших клопидогрелперед КШ. В исследовании CURE медиана времени доКШ составила 26 дн; в среднем операцию проводиличерез 12 дн после госпитализации [113]. Решение оботмене препарата принимали лечащие врачи. Эф-фективность клопидогрела в профилактике ишемиче-ских исходов по сравнению с плацебо была отмеченаперед операцией (ОР 0,82; 95% ДИ 0,58–1,16) и от-сутствовала после нее (ОР 0,97; 95% ДИ 0,75–1,26).Частота больших кровотечений была выше в группе кло-пидогрела (ОР 1,27; 95% ДИ 0,96–1,69), однакоона снижалась в случае отмены клопидогрела за 5 дндо КШ. В последующих наблюдательных исследованияхбыло выявлено значительное увеличение частоты ге-мотрансфузий и повторных операций, но не смертно-сти в тех случаях, когда клопидогрел применяли в тече-ние 5 дн до КШ [138-140]. В исследовании ACUITY1 539 пациентов перенесли КШ, а 50,9% из них полу-чали клопидогрел до операции. У последних пациен-тов отмечалось увеличение длительности госпитализа-ции (12,0 и 8,9 дня, соответственно; p=0,0001), но сни-жение частоты ишемических осложнений (смерть,ИМ или внеплановая реваскуляризация) через 30 дн(12,7% и 17,3%; p<0,01), которое не сопровождалосьувеличением частоты больших кровотечений, не свя-занных с КШ (3,4% и 3,2%; p=0,87), или больших кро-вотечений после КШ (50,3% и 50,9%; p=0,83) посравнению с пациентами, не получавшими клопидогрелперед КШ. Прием клопидогрела перед операциейбыл независимым предиктором снижения частотыишемических исходов, но не влиял на риск кровотече-ний [141]. Причиной увеличения частоты кровотечениймогут быть не только сроки применения клопидогре-ла перед КШ, но и другие факторы. У 4 974 пациентов,которым проводилось плановое и внеплановое КШ, не-зависимыми предикторами кровотечений (повторноевмешательство по поводу кровотечения, трансфузияэритроцитарной массы или снижение гематокрита бо-лее чем на 15%) были исходный гематокрит(p<0,0001), искусственное кровообращение(p<0,0001), опыт сосудистого хирурга, выполнявше-го КШ (p=0,02), женский пол (p<0,0001), понижен-ный клиренс креатинина (p=0,0002), стенокардия(p=0,0003), введение блокаторов GP IIb/IIIa рецепто-ров перед КШ (p=0,0004) и число суженных сосудов(p=0,002) [142]. Лечение клопидогрелом в течение 5дн до операции не ассоциировалось с более высокимриском кровотечения после внесения поправки надругие факторы риска (ОР 1,23; 95% ДИ 0,52–2,10;p=0,45).Отменять клопидогрел у пациентов высокого рис-ка, например, с сохраняющейся ишемией миокарда всочетании со стенозом ствола левой коронарной арте-рии и тяжелым проксимальным стенозом несколькихартерий, не рекомендуется. Таким пациентам следуетпроводить КШ на фоне лечения клопидогрелом, одна-ко необходимо уделять особое внимание мерам, на-правленным на профилактику кровотечения [143].Если риск кровотечения очень высокий, например, приповторном КШ или сложном КШ в сочетании с опера-цией на клапане, оправдан перерыв в лечении клопи-догрелом на 3-5 дн перед операцией даже у пациен-тов с активной ишемией миокарда (см. ниже).В исследовании PLATO лечение клопидогрелом и ти-кагрелором рекомендовали на время прекратить за 5и 1-3 дн, соответственно, до КШ. У пациентов, получав-ших исследуемые препараты в течение 7 дн до КШ, ча-стота больших кровотечений, связанных с операцией,и гемотрансфузий, достоверно не отличалась между группами клопидогрела и тикагрелора [134]. Хотя ча-стота нефатального ИМ и инсульта в двух группахбыла сопоставимой в этой когорте, смертность была в2 раза ниже в группе тикагрелора (4,7% и 9,7%; ОШ0,49; 95% ДИ 0,32–0,77; p<0,01); в основном разни-ца была достигнута в ранние сроки после КШ. 36% па-циентов каждой группы возобновили лечение тикагре-лором или клопидогрелом в течение 7 дн после опе-рации, 26-27% — более чем через 7 дней и 37-38%— больше не принимали препарат [134]. Оптимальныесроки возобновления антитромботической терапиипосле КШ не установлены.5.2.2.5. Прекращение двойной антитромбоцитарнойтерапииОтмена антитромбоцитарных препаратов можетпривести к увеличению частоты рецидивирующихосложнений [112,144]. Прекращение двойной анти-тромбоцитарной терапии вскоре после имплантациистента повышает риск подострого его тромбоза, которыйхарактеризуется неблагоприятным прогнозом; смертностьчерез 1 мес достигает 15-45%. Временное прекраще-ние двойной антитромбоцитарной терапии перед хи-рургическим вмешательством более чем через 1 меспосле ОКС обоснованно у пациентов без стента, выде-ляющего лекарства. Если необходим перерыв в двой-ной антитромбоцитарной терапии, например, в случаенеотложного хирургического вмешательства (например,нейрохирургического) или развития большого крово-течения, которое не удается контролировать местнымисредствами, эффективных альтернативных методовлечения не существует. Обсуждалась возможность при-менения низкомолекулярных гепаринов (НМГ), одна-ко их эффективность не доказана [145].
Рекомендации по применению пероральных антитромбоцитарных препаратов
В исследовании PLATO рандомизировали пациен-тов с ОКС без подъема сегмента ST среднего или высо-кого риска (которым планировалось консервативное илиинвазивное лечение) или ИМ с подъемом сегмента ST(которым планировалось первичное ЧКВ). Пациентамназначали клопидогрел в нагрузочной дозе 300 мг, азатем по 75 мг/сут или тикагрелор в нагрузочной дозе180 мг, а затем 90 мг два раза в день [132]. При выпол-нении ЧКВ пациентам разрешалось ввести дополнитель-но нагрузочную дозу клопидогрела 300 мг (суммарнаянагрузочная доза 600 мг) или плацебо и рекомендо-валось ввести дополнительно 90 мг тикагрелора (илисоответствующего плацебо), если ЧКВ выполняли бо-лее чем через 24 ч после приема первой нагрузочнойдозы. Лечение продолжали в течение 12 мес (мини-мальная длительность составляла 6 мес, а медиана —9 мес) [132]. В целом в исследование были включены11 067 пациентов с ИМ без подъема сегмента ST илинестабильной стенокардией. Пациентов с ОКС в иссле-дование включали в течение 24 ч после появления симп-томов при наличии по крайней мере двух из следую-щих критериев: повышение биомаркеров некрозамиокарда; ишемические изменения сегмента ST; повы-шенный риск (возраст ≥60 лет, ИМ или КШ в анамне-зе, стеноз по крайней мере двух коронарных артерий≥50%, цереброваскулярная болезнь, сахарный диабет,заболевание периферических сосудов или хроническаядисфункция почек). Во всей когорте частота комбини-рованной первичной конечной точки снизилась с11,7% в группе клопидогрела до 9,8% в группе тика-грелора (ОШ 0,84; 95% ДИ 0,77–0,92; p<0,001).Смертность от сосудистых причин снизилась с 5,1% до4,0% (ОШ 0,79; 95% ДИ 0,69–0,91; p=0,001), а ча-стота ИМ — с 6,9% до 5,8% (ОШ 0,84; 95% ДИ0,75–0,95; p=0,005). Смертность от инсульта досто-верно не отличалась (1,3% и 1,5%; p=0,22). Частотаопределенного тромбоза стента снизилась с 1,9% до1,3% (p<0,01), а общая смертность — с 5,9% до4,5% (p<0,001).Частота больших кровотечений, которые диагности-ровали в соответствии с критериями PLATO, достовер-но не отличалась между группами клопидогрела и ти-кагрелора (11,2% и 11,6%, соответственно; p=0,43).Частота больших кровотечений, не связанных с КШ, уве-личилась с 3,8% в группе клопидогрела до 4,5% в груп-пе тикагрелора (ОШ 1,19; 95% ДИ 1,02–1,38; p=0,03).Частота больших кровотечений, связанных с КШ, быласопоставимой в группах тикагрелора и клопидогрела(7,4% и 7,9%, соответственно; p=0,32). Небольшиекровотечения в группе тикагрелора развивались чаще,чем в группе клопидогрела. Смертность от кровотече-ний в целом не отличалась между группами (0,3%), не-смотря на более высокую частоту фатальных внутриче-репных кровотечений в группе тикагрелора. У пациен-тов с положительным исходным тропонином частотапервичной конечной точки значительно снизилась вгруппе тикагрелора (10,3% и 12,3%; ОШ 0,85; 95%ДИ 0,77–0,94), в отличие от пациентов с нормальнымуровнем тропонина (7,0% и 7,0%). Значительноеснижение риска первичной конечной точки выявили так-же у пациентов с окончательным диагнозом ИМ безподъема сегмента ST (11,4% и 13,9%; ОШ 0,83;95% ДИ 0,73–0,94), в отличие от пациентов с оконча-тельным диагнозом нестабильной стенокардии (8,6%и 9,1%, соответственно; ОШ 0,96; 95% ДИ 0,75–1,22).Хотя снижение частоты тромбоза стента при лечении ти-кагрелором было отмечено в ранние сроки [133],благоприятный эффект на риск ИМ и смерти продол-жал нарастать в течение 12 мес [132].Тикагрелор снижал раннюю и позднюю смертностьпосле КШ. У 1 261 пациента, перенесшего КШ и полу-чавшего исследуемый препарат в течение <7 дн до опе-рации, частота комбинированной первичной конечнойточки составила 10,6% в группе тикагрелора и 13,1%в группе клопидогрела (ОШ 0,84; 95% ДИ 0,60–1,16;p=0,29). Общая смертность при лечении тикагрелоромснизилась с 9,7% до 4,7% (ОШ 0,49; ДИ 0,32–0,77;p<0,01), сердечно-сосудистая смертность — с 7,9% до4,1% (ОШ 0,52; 95% ДИ 0,32–0,85; p<0,01), смерт-ность от других причин — с 2,0% до 0,7% (p=0,07). Ча-стота больших кровотечений, связанных с КШ, досто-верно не отличалась между двумя группами. В соответствии с протоколом, лечение тикагрелором возобнов-ляли, когда его применение считалось безопасным с точ-ки зрения кровотечений (см. ниже) [134].Нежелательные эффекты тикагрелора. Помимо уве-личения частоты небольших и не связанных с КШбольших кровотечений нежелательные эффекты тика-грелора включали в себя одышку, увеличение частотыжелудочковых пауз и бессимптомной гиперурикемии[132,135,136]. Одышка, вызванная тикагрелором,чаще всего (до 15%) развивается в течение первой не-дели после начала лечения и может быть преходящейили сохраняется до прекращения лечения, однако онаобычно не требует прекращения лечения [132,137].Одышка, по-видимому, не связана с ухудшением функ-ции сердца или легких [137]. Желудочковые паузы приприменении тикагрелора в основном представляют со-бой бессимптомные эпизоды ночной синоатриаль-ной блокады. Рекомендуется соблюдать осторожностьу пациентов с выраженной синоатриальной блокадойили атриовентрикулярной блокадой II-III степени, еслипациенту не установлен постоянный водитель ритма. Ме-ханизмы развития одышки и желудочковых пауз не уста-новлены [137]. В исследовании PLATO в группе тика-грелора было выявлено несколько более выраженноеувеличение сывороточного уровня креатинина, од-нако разница между группами отсутствовала через 1 меспосле прекращения лечения [132]. Частота желудочно-кишечных расстройств и сыпи была сходной в двух груп-пах [136].5.2.2.4. Отмена блокаторов P2Y12 рецепторовперед операциейУ пациентов с ОКС без подъема сегмента ST двой-ную антитромбоцитарную терапию следует начинатьрано, так как польза перевешивает риск во всех случаях.Высказывалось предположение, что тиенопиридины сле-дует на время отменить перед ангиографией, учитываявозможную необходимость в КШ. В нескольких иссле-дованиях было отмечено увеличение риска большихкровотечений у пациентов, получавших клопидогрелперед КШ. В исследовании CURE медиана времени доКШ составила 26 дн; в среднем операцию проводиличерез 12 дн после госпитализации [113]. Решение оботмене препарата принимали лечащие врачи. Эф-фективность клопидогрела в профилактике ишемиче-ских исходов по сравнению с плацебо была отмеченаперед операцией (ОР 0,82; 95% ДИ 0,58–1,16) и от-сутствовала после нее (ОР 0,97; 95% ДИ 0,75–1,26).Частота больших кровотечений была выше в группе кло-пидогрела (ОР 1,27; 95% ДИ 0,96–1,69), однакоона снижалась в случае отмены клопидогрела за 5 дндо КШ. В последующих наблюдательных исследованияхбыло выявлено значительное увеличение частоты ге-мотрансфузий и повторных операций, но не смертно-сти в тех случаях, когда клопидогрел применяли в тече-ние 5 дн до КШ [138-140]. В исследовании ACUITY1 539 пациентов перенесли КШ, а 50,9% из них полу-чали клопидогрел до операции. У последних пациен-тов отмечалось увеличение длительности госпитализа-ции (12,0 и 8,9 дня, соответственно; p=0,0001), но сни-жение частоты ишемических осложнений (смерть,ИМ или внеплановая реваскуляризация) через 30 дн(12,7% и 17,3%; p<0,01), которое не сопровождалосьувеличением частоты больших кровотечений, не свя-занных с КШ (3,4% и 3,2%; p=0,87), или больших кро-вотечений после КШ (50,3% и 50,9%; p=0,83) посравнению с пациентами, не получавшими клопидогрелперед КШ. Прием клопидогрела перед операциейбыл независимым предиктором снижения частотыишемических исходов, но не влиял на риск кровотече-ний [141]. Причиной увеличения частоты кровотечениймогут быть не только сроки применения клопидогре-ла перед КШ, но и другие факторы. У 4 974 пациентов,которым проводилось плановое и внеплановое КШ, не-зависимыми предикторами кровотечений (повторноевмешательство по поводу кровотечения, трансфузияэритроцитарной массы или снижение гематокрита бо-лее чем на 15%) были исходный гематокрит(p<0,0001), искусственное кровообращение(p<0,0001), опыт сосудистого хирурга, выполнявше-го КШ (p=0,02), женский пол (p<0,0001), понижен-ный клиренс креатинина (p=0,0002), стенокардия(p=0,0003), введение блокаторов GP IIb/IIIa рецепто-ров перед КШ (p=0,0004) и число суженных сосудов(p=0,002) [142]. Лечение клопидогрелом в течение 5дн до операции не ассоциировалось с более высокимриском кровотечения после внесения поправки надругие факторы риска (ОР 1,23; 95% ДИ 0,52–2,10;p=0,45).Отменять клопидогрел у пациентов высокого рис-ка, например, с сохраняющейся ишемией миокарда всочетании со стенозом ствола левой коронарной арте-рии и тяжелым проксимальным стенозом несколькихартерий, не рекомендуется. Таким пациентам следуетпроводить КШ на фоне лечения клопидогрелом, одна-ко необходимо уделять особое внимание мерам, на-правленным на профилактику кровотечения [143].Если риск кровотечения очень высокий, например, приповторном КШ или сложном КШ в сочетании с опера-цией на клапане, оправдан перерыв в лечении клопи-догрелом на 3-5 дн перед операцией даже у пациен-тов с активной ишемией миокарда (см. ниже).В исследовании PLATO лечение клопидогрелом и ти-кагрелором рекомендовали на время прекратить за 5и 1-3 дн, соответственно, до КШ. У пациентов, получав-ших исследуемые препараты в течение 7 дн до КШ, ча-стота больших кровотечений, связанных с операцией,и гемотрансфузий, достоверно не отличалась между группами клопидогрела и тикагрелора [134]. Хотя ча-стота нефатального ИМ и инсульта в двух группахбыла сопоставимой в этой когорте, смертность была в2 раза ниже в группе тикагрелора (4,7% и 9,7%; ОШ0,49; 95% ДИ 0,32–0,77; p<0,01); в основном разни-ца была достигнута в ранние сроки после КШ. 36% па-циентов каждой группы возобновили лечение тикагре-лором или клопидогрелом в течение 7 дн после опе-рации, 26-27% — более чем через 7 дней и 37-38%— больше не принимали препарат [134]. Оптимальныесроки возобновления антитромботической терапиипосле КШ не установлены.5.2.2.5. Прекращение двойной антитромбоцитарнойтерапииОтмена антитромбоцитарных препаратов можетпривести к увеличению частоты рецидивирующихосложнений [112,144]. Прекращение двойной анти-тромбоцитарной терапии вскоре после имплантациистента повышает риск подострого его тромбоза, которыйхарактеризуется неблагоприятным прогнозом; смертностьчерез 1 мес достигает 15-45%. Временное прекраще-ние двойной антитромбоцитарной терапии перед хи-рургическим вмешательством более чем через 1 меспосле ОКС обоснованно у пациентов без стента, выде-ляющего лекарства. Если необходим перерыв в двой-ной антитромбоцитарной терапии, например, в случаенеотложного хирургического вмешательства (например,нейрохирургического) или развития большого крово-течения, которое не удается контролировать местнымисредствами, эффективных альтернативных методовлечения не существует. Обсуждалась возможность при-менения низкомолекулярных гепаринов (НМГ), одна-ко их эффективность не доказана [145].
Рекомендации по применению пероральных антитромбоцитарных препаратов
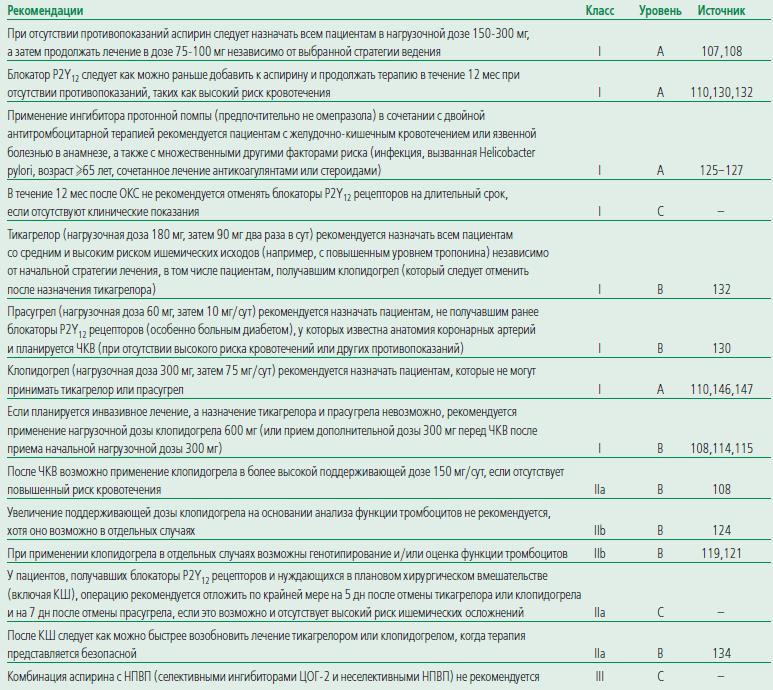 В инструкциях по применению всех трех ингибито-ров P2Y12 рецепторов указано, что их следует отменитьза 7 дн до операции. Однако тактика ведения пациен-тов, которых направляют на хирургическое вмеша-тельство на фоне двойной антитромбоцитарной тера-пии, зависит от степени неотложности операции, атакже индивидуального риска тромбообразования и кро-вотечения. Большинство хирургических вмешательствмогут выполнены на фоне двойной антитромбоцитар-ной терапии или по крайней мере монотерапии ацетил-салициловой кислотой; при этом риск кровотечений счи-тают приемлемым. Для оценки риска и выбора оптималь-ной стратегии необходим мультидисциплинарный под-ход (кардиолог, анестезиолог, гематолог и хирург).У пациентов с ОКС без подъема сегмента ST необхо-димо взвешивать риск кровотечений во время опера-ции и повторных ишемических осложнений, связанныхс прекращением антитромбоцитарной терапии. Приэтом следует учитывать характер операции, риск ише-мических исходов и тяжесть ИБС, срок, прошедшийпосле ОКС или ЧКВ (если оно было выполнено), нали-чие стента, выделяющего лекарства, и риск тромбозастента. При хирургических операциях, сопровождаю-щихся низким или средним риском кровотечения, це-лесообразно продолжать двойную антитромбоцитар-ную терапию. Если приемлемо умеренное подавлениеP2Y12 во время вмешательств, например при выполне-нии КШ в ранние сроки после ОКС, то препаратыможно отменить незадолго до операции. В таких слу-чаях целесообразно прекратить прием клопидогрелаза 5 дн до хирургического вмешательства или позднее,если валидированный метод оценки функции тромбо-цитов подтверждает низкий ответ на клопидогрел.Прасугрел отменяют за 7 дн до операции, а тикагрелор— за 5 дн. Если прекращение антитромбоцитарной те-рапии перед операцией сопровождается высокимриском (например, в первые недели после импланта-ции стента), некоторые авторы рекомендовали на-значить обратимый антитромбоцитарный препарат с ко-ротким периодом полувыведения, например, ингиби-торы GP IIb/IIIa рецепторов тирофибан или эптифиба-тид, однако эффективность такого подхода пока не до-казана. Двойную антитромбоцитарную терапию следу-ет возобновить, когда она представляется безопасной.
Блокаторы гликопротеиновых IIb/IIIa рецепторов
Три блокатора GP IIb/IIIa рецепторов предназначе-ны для внутривенного введения и принадлежат к раз-личным классам: абциксимаб — фрагмент моноклональ-ных антител, эптифибатид — циклический пептид, ти-рофибан — пептидомиметик. При мета-анализе 29 570пациентов, которым планировалось ЧКВ после первич-ного консервативного ведения, было выявлено сниже-ние относительного риска смерти или нефатального ИМпри лечении блокаторами GP IIb/IIIa рецепторов на 9%(10,7% и 11,5%; p=0,02) [149]. У пациентов, получав-ших только консервативное лечение, риск смерти илиИМ при применении блокаторов GP IIb/IIIa рецепторовне отличался от такового в группе плацебо. Лечение эти-ми препаратами было эффективным только во времяЧКВ (10,5% и 13,6%; ОШ 0,74; 95% ДИ 0,57–0,96;p=0,02). Применение блокаторов GP IIb/IIIa рецепто-ров сопровождалось увеличением частоты больших кро-вотечений, но не внутричерепных кровотечений. Пер-вые исследования этих препаратов проводились в тотпериод, когда отсутствовали клопидогрел или новыеблокаторы P2Y12 рецепторов.«Upstream» терапия или выборочное применениеблокаторов GP IIb/IIIa рецепторов при ЧКВВ исследовании ACUITY Timing сравнивали резуль-таты выборочного (только во время ЧКВ) и рутинногоприменения блокаторов GP IIb/IIIa рецепторов до вме-шательства (upstream) у 9 207 пациентов [150]. Впервой группе блокаторы GP IIb/IIIa рецепторов при-меняли у 55,7% пациентов в течение 13,1 ч, а во вто-рой группе — у 98,3% пациентов в течение 18,4 ч. В це-лом 64% пациентов получали тиенопиридины передангиографией или ЧКВ. Частота больших кровотечений,не связанных с КШ, в течение 30 дн была ниже на фоневыборочного применения блокаторов GP IIb/IIIa рецеп-торов (4,9% и 6,1%; ОР 0,80; 95% ДИ 0,67–0,95;p=0,009), в то время как частота ишемических исхо-дов достоверно не отличалась между двумя группами(7,9% и 7,1%; ОР 1,12; 95% ДИ 0,97–1,29; p=0,13).Суммарная частота ишемических исходов и большихкровотечений (чистый клинический эффект) через 30дн была сходной (11,7% и 11,7%; ОР 1,00; 95% ДИ0,89–1,11; p=0,93; значение р для сопоставимости<0,001).В исследовании EARLY-ACS были рандомизирова-ны 9 492 пациентов, которым планировалось инвазив-ное лечение. Пациентам вводили эптифибатид или пла-цебо в ранние сроки; кроме того, допускалось введе-ние эптифибатида после ангиографии перед ЧКВ[151]. Первичным критерием эффективности была сум-марная частота смерти, ИМ, неотложной реваскуляри-зации по поводу рецидивирующей ишемии или ост-рой или угрожающей тромботической окклюзии сосу-да через 96 ч. Среди 5 559 пациентов группы плаце-бо 38% получили эптифибатид после ангиографии.При раннем и отложенном введении эптифибатида ча-стота первичной конечной точки достоверно не отлича-лась (9,3% и 10,0%; ОШ 0,92; 95% ДИ 0,80–1,06;p=0,23). Частота вторичной конечной точки (смертьот любой причины или развитие ИМ в течение 30 дн)также была сопоставимой (11,2% и 12,3%; ОШ 0,89;95% ДИ 0,89–1,01; p=0,08). Частота той же конечной точки на фоне консервативного ведения (доЧКВ или КШ или в течение 30 дн у всех пациентов, ко-торые получали только медикаментозное лечение) так-же была сопоставимой (4,3% в группе эптифибатидаи 4,2% в группе плацебо). Это свидетельствует о том,что введение эптифибатида не приносит пользы паци-ентам, которым проводится консервативное лечение.Частота больших кровотечений на фоне раннего вве-дения эптифибатида была выше, чем при отложенномвведении препарата (частота больших кровотеченийпо критериям TIMI через 120 ч составила 2,6% и 1,8%,соответственно; ОР 1,42; 95% ДИ 1,97–1,89;p=0,015). Таким образом, это исследование не под-твердило преимуществ раннего (upstream) примене-ния эптифибатида перед современной стандартной так-тикой ведения, когда у части пациентов, которымпроводили ЧКВ, эптифибатид вводили в более позд-ние сроки.Во всех исследованиях отмечалось увеличение ча-стоты кровотечений на фоне раннего применения бло-каторов GP IIb/IIIa рецепторов. В связи с этим их не сле-дует вводить до ангиографии. При оценке целесообраз-ности введения блокаторов GP IIb/IIIa рецепторов передЧКВ следует учитывать результаты ангиографии (нали-чие тромба и распространенность атеросклероза), по-вышение уровня тропонина, предыдущую терапиюингибиторами P2Y12 рецепторов, возраст и другиефакторы, оказывающие влияние на риск серьезных кро-вотечений [2,152]. «Upstream» терапия блокаторамиGP IIb/IIIa рецепторов может быть обоснованной при со-хранении ишемии у пациентов группы высокого рискаили невозможности двойной антитромбоцитарной те-рапии. Пациентам, которым вводили эптифибатид илитирофибан перед ангиографией, следует продолжатьлечение тем же препаратом во время и после ЧКВ.ТромбоцитопенияПри применении всех трех зарегистрированныхблокаторов GP IIb/IIIa рецепторов может развиться тром-боцитопения (см. раздел 5.5.10.). Частота остройтромбоцитопении в клинических исследованиях парен-теральных блокаторов GP IIb/IIIa рецепторов составля-ла от 0,5 до 5,6% и была сопоставимой с таковой привведении одного нефракционированного гепарина(НФГ) [153,154]. Через 5-11 дн возможно развитиепоздней тромбоцитопении. Оба типа тромбоцитопениимогут быть следствием образования антител [155]. Прилечении абциксимабом частота тяжелой тромбоцито-пении была более чем в 2 раза выше, чем в группе пла-цебо. Риск ее ниже при введении эптифибатида (0,2%в исследовании PURSUIT) [156] и тирофибана. В иссле-довании TARGET развитие тромбоцитопении наблюда-ли у 2,4% пациентов группы абциксимаба и 0,5% —группы тирофибана (p<0,001) [157].Сравнительная эффективность блокаторовGP IIb/IIIa рецепторовАбциксимаб сравнивали с тирофибаном в исследо-вании TARGET, в котором у 2/3 пациентов имелсяОКС без подъема сегмента ST [158]. Абциксимаб пре-восходил тирофибан в стандартных дозах по эффектив-ности в профилактике смерти, ИМ и неотложной ревас-куляризации в течение 30 дн, однако через 6 мес раз-ница была недостоверной [159]. Дополнительные ис-следования, в которых тирофибан применяли в болеевысоких дозах в различных ситуациях, результатымета-анализа показали, что тирофибан в высокойдозе (25 мг/кг в виде болюса, а затем инфузия) по эф-фективности сопоставим с абциксимабом [160,161].Сравнительные исследования эптифибатида не прово-дились.Комбинация блокаторов GP IIb/IIIa рецепторовс аспирином и ингибиторами P2Y12Данные о пользе присоединения блокатораGP IIb/IIIa рецепторов к комбинированной терапии аспи-рином и блокатором P2Y12 рецепторов при ОКС безподъема сегмента ST ограниченны. В исследованииISAR-REACT-2 были рандомизированы 2 022 пациен-та высокого риска с ОКС без подъема сегмента ST, ко-торым после приема аспирина и клопидогрела в дозе600 мг вводили абциксимаб или плацебо во время ЧКВ.Доля пациентов с сахарным диабетом в двух группахбыла сопоставимой (в среднем 26,5%); у 52% боль-ных был повышен уровень тропонина, а у 24,1%имелся ИМ в анамнезе. Суммарная частота смерти, ИМили неотложной реваскуляризации целевого сосуда втечение 30 дн в группе абциксимаба была значитель-но ниже, чем в группе плацебо (8,9% и 11,9%; ОР 0,75;95% ДИ 0,58–0,97; p=0,03). Снижение риска про-изошло в основном за счет уменьшения риска смертии нефатального ИМ. Эффект препарата был болеевыраженным в некоторых подгруппах пациентов, в част-ности с повышенным уровнем тропонина (13,1% и18,3%; отношение рисков 0,71; 95% ДИ 0,54–0,95;p=0,02). Длительность терапии клопидогрелом передвведением блокатора GP IIb/IIIa рецепторов не оказы-вала влияния на исходы. У пациентов с нормальнымуровнем тропонина и сахарным диабетом лечениеабциксимабом оказалось неэффективным. Однакочисло пациентов с диабетом в этом исследованиибыло недостаточным для статистического анализа эф-фективности терапии.В исследованиях TRITON и PLATO частота примене-ния блокаторов GP IIb/IIIa рецепторов составила 55%и 27%, соответственно. У пациентов, получавших этипрепараты в исследовании TRITON, была выше часто-та больших и небольших кровотечений (по крите-риям TIMI), не связанных с КШ, однако применение блокаторов GP IIb/IIIa рецепторов не влияло на относитель-ный риск кровотечений, который сравнивали в группахпрасугрела и клопидогрела (значение Р для взаимодей-ствия 0,19) [162]. Лечение прасугрелом привело к сни-жению риска смерти, ИМ или инсульта по сравнениюс клопидогрелом как на фоне применения блокаторовGP IIb/IIIa рецепторов (6,5% и 8,5%; отношение рис-ков 0,76; 95% ДИ 0,64–0,90), так и без лечения эти-ми препаратами (4,8% и 6,1%; отношение рисков 0,78;95% ДИ 0,63–0,97). В исследовании PLATO тикагре-лор также снизил риск смерти, ИМ или инсульта посравнению с клопидогрелом у пациентов, получавших(10,0% и 11,1%; отношение рисков 0,90; 95% ДИ0,76–1,07) и не получавших (9,7% и 11,9%; отноше-ние рисков 0,82; 95% ДИ 0,74–0,92) блокатор GPIIb/IIIa рецепторов [132]. В целом применение блока-тора GP IIb/IIIa рецепторов в сочетании с аспирином иблокатором P2Y12 рецепторов оправданно при ЧКВ упациентов с ОКС без подъема сегмента, если риск раз-вития ИМ высокий, а риск кровотечений низкий.Блокаторы GP IIb/IIIa рецепторови антикоагулянтыВ большинстве исследований, показавших эффек-тивность блокаторов GP IIb/IIIa рецепторов, применя-лись антикоагулянты. В нескольких исследованиях у па-циентов с ОКС без подъема сегмента ST, а также в на-блюдательных исследованиях у пациентов, перенесшихЧКВ, было установлено, что НМГ, прежде всего энокса-парин, можно безопасно применять в сочетании сблокаторами GP IIb/IIIa рецепторов, хотя подкожное вве-дение эноксапарина не обеспечивает адекватную про-филактику катетерного тромбоза при первичном ЧКВ[163]. В исследовании OASIS-5 блокаторы GP IIb/IIIa ре-цепторов применяли в сочетании с аспирином и кло-пидогрелом, а также фондапаринуксом (n=1308) илиэноксапарином (n=1273) [164]. В целом частота кро-вотечений при лечении фондапаринуксом была ниже,чем при применении эноксапарина (см. раздел 5.3.).Бивалирудин и НФГ/НМГ характеризовались одинако-выми безопасностью и эффективностью в комбинациис аспирином, клопидогрелом и блокатором GP IIb/IIIaрецепторов в исследовании ACUITY [165]. Комбиниро-ванная терапия бивалирудином и блокаторомGP IIb/IIIa рецепторов привела к сходному снижениючастоты ишемических осложнений по сравнению содним бивалирудином, но сопровождалась более вы-сокой частотой больших кровотечений [166]. Эти дан-ные не позволяют рекомендовать широкое применениеданной комбинации.Выбор дозы блокаторов GP IIb/IIIa рецепторовЭффективность и безопасность блокаторовGP IIb/IIIa рецепторов в обычной клинической практи-ке изучалась в нескольких регистрах. Была отмечена вы-сокая частота больших кровотечений, которые были ча-стично связаны с назначением больших доз [167,168].Причинами передозировки были пожилой возраст, жен-ский пол, почечная недостаточность, низкая массатела, сахарный диабет и застойная сердечная недоста-точность. У пациентов, получавших слишком высокиедозы блокаторов GP IIb/IIIa рецепторов, скорректиро-ванная частота больших кровотечений была на 30%выше таковой при применении адекватных доз. Такимобразом, частота геморрагических осложнений в кли-нических исследований может быть заниженной посравнению с таковой в клинической практике, когда бло-каторы GP IIb/IIIa рецепторов применяют у пациентов,у которых чаще встречаются сопутствующие заболева-ния.Блокаторы GP IIb/IIIa рецепторови коронарное шунтированиеПри выполнении КШ у пациентов, получающихблокаторы GP IIb/IIIa рецепторов, необходимо обеспе-чить адекватный гемостаз и отменить блокаторGP IIb/IIIa рецепторов перед операцией или, если не-возможно, во время вмешательства. Эптифибатид и ти-рофибан обладают коротким периодом полувыведе-ния (около 2 ч), поэтому функция тромбоцитов при об-ратимом связывании рецепторов может восстановить-ся в конце КШ. Абциксимаб имеет короткий период по-лувыведения (10 мин), однако он медленно высвобож-дается из комплекса с рецептором с периодом полувы-ведения около 4 ч, поэтому восстановление нормаль-ной или близкой к норме агрегации тромбоцитовпроисходит в течение 48 ч после завершения инфузии(хотя абциксимаб, связанный с рецепторами, можетопределяться в течение более длительного времени).В случае значительного кровотечения возможна транс-фузия тромбоцитарной массы (см. раздел 5.5.9.). Длякупирования больших кровотечений при введениитирофибана и эптифибатида возможно применениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с тромбоци-тарной массой [169].
Антикоагулянты
Антикоагулянты применяют у пациентов с ОКС безподъема сегмента ST для ингибирования образованияи/или активности тромбина и для профилактики тром-бообразования. Установлена эффективность антикоа-гулянтов в сочетании с блокаторами функции тромбо-цитов, а комбинированная терапия была более эффек-тивной, чем монотерапия обоими средствами [171,172].У пациентов с ОКС без подъема сегмента ST изучалисьили изучаются несколько антикоагулянтов, действующихна различных уровнях каскада свертывания крови:
Рекомендации по применению блокаторов GP IIb/IIIa рецепторов
В инструкциях по применению всех трех ингибито-ров P2Y12 рецепторов указано, что их следует отменитьза 7 дн до операции. Однако тактика ведения пациен-тов, которых направляют на хирургическое вмеша-тельство на фоне двойной антитромбоцитарной тера-пии, зависит от степени неотложности операции, атакже индивидуального риска тромбообразования и кро-вотечения. Большинство хирургических вмешательствмогут выполнены на фоне двойной антитромбоцитар-ной терапии или по крайней мере монотерапии ацетил-салициловой кислотой; при этом риск кровотечений счи-тают приемлемым. Для оценки риска и выбора оптималь-ной стратегии необходим мультидисциплинарный под-ход (кардиолог, анестезиолог, гематолог и хирург).У пациентов с ОКС без подъема сегмента ST необхо-димо взвешивать риск кровотечений во время опера-ции и повторных ишемических осложнений, связанныхс прекращением антитромбоцитарной терапии. Приэтом следует учитывать характер операции, риск ише-мических исходов и тяжесть ИБС, срок, прошедшийпосле ОКС или ЧКВ (если оно было выполнено), нали-чие стента, выделяющего лекарства, и риск тромбозастента. При хирургических операциях, сопровождаю-щихся низким или средним риском кровотечения, це-лесообразно продолжать двойную антитромбоцитар-ную терапию. Если приемлемо умеренное подавлениеP2Y12 во время вмешательств, например при выполне-нии КШ в ранние сроки после ОКС, то препаратыможно отменить незадолго до операции. В таких слу-чаях целесообразно прекратить прием клопидогрелаза 5 дн до хирургического вмешательства или позднее,если валидированный метод оценки функции тромбо-цитов подтверждает низкий ответ на клопидогрел.Прасугрел отменяют за 7 дн до операции, а тикагрелор— за 5 дн. Если прекращение антитромбоцитарной те-рапии перед операцией сопровождается высокимриском (например, в первые недели после импланта-ции стента), некоторые авторы рекомендовали на-значить обратимый антитромбоцитарный препарат с ко-ротким периодом полувыведения, например, ингиби-торы GP IIb/IIIa рецепторов тирофибан или эптифиба-тид, однако эффективность такого подхода пока не до-казана. Двойную антитромбоцитарную терапию следу-ет возобновить, когда она представляется безопасной.
Блокаторы гликопротеиновых IIb/IIIa рецепторов
Три блокатора GP IIb/IIIa рецепторов предназначе-ны для внутривенного введения и принадлежат к раз-личным классам: абциксимаб — фрагмент моноклональ-ных антител, эптифибатид — циклический пептид, ти-рофибан — пептидомиметик. При мета-анализе 29 570пациентов, которым планировалось ЧКВ после первич-ного консервативного ведения, было выявлено сниже-ние относительного риска смерти или нефатального ИМпри лечении блокаторами GP IIb/IIIa рецепторов на 9%(10,7% и 11,5%; p=0,02) [149]. У пациентов, получав-ших только консервативное лечение, риск смерти илиИМ при применении блокаторов GP IIb/IIIa рецепторовне отличался от такового в группе плацебо. Лечение эти-ми препаратами было эффективным только во времяЧКВ (10,5% и 13,6%; ОШ 0,74; 95% ДИ 0,57–0,96;p=0,02). Применение блокаторов GP IIb/IIIa рецепто-ров сопровождалось увеличением частоты больших кро-вотечений, но не внутричерепных кровотечений. Пер-вые исследования этих препаратов проводились в тотпериод, когда отсутствовали клопидогрел или новыеблокаторы P2Y12 рецепторов.«Upstream» терапия или выборочное применениеблокаторов GP IIb/IIIa рецепторов при ЧКВВ исследовании ACUITY Timing сравнивали резуль-таты выборочного (только во время ЧКВ) и рутинногоприменения блокаторов GP IIb/IIIa рецепторов до вме-шательства (upstream) у 9 207 пациентов [150]. Впервой группе блокаторы GP IIb/IIIa рецепторов при-меняли у 55,7% пациентов в течение 13,1 ч, а во вто-рой группе — у 98,3% пациентов в течение 18,4 ч. В це-лом 64% пациентов получали тиенопиридины передангиографией или ЧКВ. Частота больших кровотечений,не связанных с КШ, в течение 30 дн была ниже на фоневыборочного применения блокаторов GP IIb/IIIa рецеп-торов (4,9% и 6,1%; ОР 0,80; 95% ДИ 0,67–0,95;p=0,009), в то время как частота ишемических исхо-дов достоверно не отличалась между двумя группами(7,9% и 7,1%; ОР 1,12; 95% ДИ 0,97–1,29; p=0,13).Суммарная частота ишемических исходов и большихкровотечений (чистый клинический эффект) через 30дн была сходной (11,7% и 11,7%; ОР 1,00; 95% ДИ0,89–1,11; p=0,93; значение р для сопоставимости<0,001).В исследовании EARLY-ACS были рандомизирова-ны 9 492 пациентов, которым планировалось инвазив-ное лечение. Пациентам вводили эптифибатид или пла-цебо в ранние сроки; кроме того, допускалось введе-ние эптифибатида после ангиографии перед ЧКВ[151]. Первичным критерием эффективности была сум-марная частота смерти, ИМ, неотложной реваскуляри-зации по поводу рецидивирующей ишемии или ост-рой или угрожающей тромботической окклюзии сосу-да через 96 ч. Среди 5 559 пациентов группы плаце-бо 38% получили эптифибатид после ангиографии.При раннем и отложенном введении эптифибатида ча-стота первичной конечной точки достоверно не отлича-лась (9,3% и 10,0%; ОШ 0,92; 95% ДИ 0,80–1,06;p=0,23). Частота вторичной конечной точки (смертьот любой причины или развитие ИМ в течение 30 дн)также была сопоставимой (11,2% и 12,3%; ОШ 0,89;95% ДИ 0,89–1,01; p=0,08). Частота той же конечной точки на фоне консервативного ведения (доЧКВ или КШ или в течение 30 дн у всех пациентов, ко-торые получали только медикаментозное лечение) так-же была сопоставимой (4,3% в группе эптифибатидаи 4,2% в группе плацебо). Это свидетельствует о том,что введение эптифибатида не приносит пользы паци-ентам, которым проводится консервативное лечение.Частота больших кровотечений на фоне раннего вве-дения эптифибатида была выше, чем при отложенномвведении препарата (частота больших кровотеченийпо критериям TIMI через 120 ч составила 2,6% и 1,8%,соответственно; ОР 1,42; 95% ДИ 1,97–1,89;p=0,015). Таким образом, это исследование не под-твердило преимуществ раннего (upstream) примене-ния эптифибатида перед современной стандартной так-тикой ведения, когда у части пациентов, которымпроводили ЧКВ, эптифибатид вводили в более позд-ние сроки.Во всех исследованиях отмечалось увеличение ча-стоты кровотечений на фоне раннего применения бло-каторов GP IIb/IIIa рецепторов. В связи с этим их не сле-дует вводить до ангиографии. При оценке целесообраз-ности введения блокаторов GP IIb/IIIa рецепторов передЧКВ следует учитывать результаты ангиографии (нали-чие тромба и распространенность атеросклероза), по-вышение уровня тропонина, предыдущую терапиюингибиторами P2Y12 рецепторов, возраст и другиефакторы, оказывающие влияние на риск серьезных кро-вотечений [2,152]. «Upstream» терапия блокаторамиGP IIb/IIIa рецепторов может быть обоснованной при со-хранении ишемии у пациентов группы высокого рискаили невозможности двойной антитромбоцитарной те-рапии. Пациентам, которым вводили эптифибатид илитирофибан перед ангиографией, следует продолжатьлечение тем же препаратом во время и после ЧКВ.ТромбоцитопенияПри применении всех трех зарегистрированныхблокаторов GP IIb/IIIa рецепторов может развиться тром-боцитопения (см. раздел 5.5.10.). Частота остройтромбоцитопении в клинических исследованиях парен-теральных блокаторов GP IIb/IIIa рецепторов составля-ла от 0,5 до 5,6% и была сопоставимой с таковой привведении одного нефракционированного гепарина(НФГ) [153,154]. Через 5-11 дн возможно развитиепоздней тромбоцитопении. Оба типа тромбоцитопениимогут быть следствием образования антител [155]. Прилечении абциксимабом частота тяжелой тромбоцито-пении была более чем в 2 раза выше, чем в группе пла-цебо. Риск ее ниже при введении эптифибатида (0,2%в исследовании PURSUIT) [156] и тирофибана. В иссле-довании TARGET развитие тромбоцитопении наблюда-ли у 2,4% пациентов группы абциксимаба и 0,5% —группы тирофибана (p<0,001) [157].Сравнительная эффективность блокаторовGP IIb/IIIa рецепторовАбциксимаб сравнивали с тирофибаном в исследо-вании TARGET, в котором у 2/3 пациентов имелсяОКС без подъема сегмента ST [158]. Абциксимаб пре-восходил тирофибан в стандартных дозах по эффектив-ности в профилактике смерти, ИМ и неотложной ревас-куляризации в течение 30 дн, однако через 6 мес раз-ница была недостоверной [159]. Дополнительные ис-следования, в которых тирофибан применяли в болеевысоких дозах в различных ситуациях, результатымета-анализа показали, что тирофибан в высокойдозе (25 мг/кг в виде болюса, а затем инфузия) по эф-фективности сопоставим с абциксимабом [160,161].Сравнительные исследования эптифибатида не прово-дились.Комбинация блокаторов GP IIb/IIIa рецепторовс аспирином и ингибиторами P2Y12Данные о пользе присоединения блокатораGP IIb/IIIa рецепторов к комбинированной терапии аспи-рином и блокатором P2Y12 рецепторов при ОКС безподъема сегмента ST ограниченны. В исследованииISAR-REACT-2 были рандомизированы 2 022 пациен-та высокого риска с ОКС без подъема сегмента ST, ко-торым после приема аспирина и клопидогрела в дозе600 мг вводили абциксимаб или плацебо во время ЧКВ.Доля пациентов с сахарным диабетом в двух группахбыла сопоставимой (в среднем 26,5%); у 52% боль-ных был повышен уровень тропонина, а у 24,1%имелся ИМ в анамнезе. Суммарная частота смерти, ИМили неотложной реваскуляризации целевого сосуда втечение 30 дн в группе абциксимаба была значитель-но ниже, чем в группе плацебо (8,9% и 11,9%; ОР 0,75;95% ДИ 0,58–0,97; p=0,03). Снижение риска про-изошло в основном за счет уменьшения риска смертии нефатального ИМ. Эффект препарата был болеевыраженным в некоторых подгруппах пациентов, в част-ности с повышенным уровнем тропонина (13,1% и18,3%; отношение рисков 0,71; 95% ДИ 0,54–0,95;p=0,02). Длительность терапии клопидогрелом передвведением блокатора GP IIb/IIIa рецепторов не оказы-вала влияния на исходы. У пациентов с нормальнымуровнем тропонина и сахарным диабетом лечениеабциксимабом оказалось неэффективным. Однакочисло пациентов с диабетом в этом исследованиибыло недостаточным для статистического анализа эф-фективности терапии.В исследованиях TRITON и PLATO частота примене-ния блокаторов GP IIb/IIIa рецепторов составила 55%и 27%, соответственно. У пациентов, получавших этипрепараты в исследовании TRITON, была выше часто-та больших и небольших кровотечений (по крите-риям TIMI), не связанных с КШ, однако применение блокаторов GP IIb/IIIa рецепторов не влияло на относитель-ный риск кровотечений, который сравнивали в группахпрасугрела и клопидогрела (значение Р для взаимодей-ствия 0,19) [162]. Лечение прасугрелом привело к сни-жению риска смерти, ИМ или инсульта по сравнениюс клопидогрелом как на фоне применения блокаторовGP IIb/IIIa рецепторов (6,5% и 8,5%; отношение рис-ков 0,76; 95% ДИ 0,64–0,90), так и без лечения эти-ми препаратами (4,8% и 6,1%; отношение рисков 0,78;95% ДИ 0,63–0,97). В исследовании PLATO тикагре-лор также снизил риск смерти, ИМ или инсульта посравнению с клопидогрелом у пациентов, получавших(10,0% и 11,1%; отношение рисков 0,90; 95% ДИ0,76–1,07) и не получавших (9,7% и 11,9%; отноше-ние рисков 0,82; 95% ДИ 0,74–0,92) блокатор GPIIb/IIIa рецепторов [132]. В целом применение блока-тора GP IIb/IIIa рецепторов в сочетании с аспирином иблокатором P2Y12 рецепторов оправданно при ЧКВ упациентов с ОКС без подъема сегмента, если риск раз-вития ИМ высокий, а риск кровотечений низкий.Блокаторы GP IIb/IIIa рецепторови антикоагулянтыВ большинстве исследований, показавших эффек-тивность блокаторов GP IIb/IIIa рецепторов, применя-лись антикоагулянты. В нескольких исследованиях у па-циентов с ОКС без подъема сегмента ST, а также в на-блюдательных исследованиях у пациентов, перенесшихЧКВ, было установлено, что НМГ, прежде всего энокса-парин, можно безопасно применять в сочетании сблокаторами GP IIb/IIIa рецепторов, хотя подкожное вве-дение эноксапарина не обеспечивает адекватную про-филактику катетерного тромбоза при первичном ЧКВ[163]. В исследовании OASIS-5 блокаторы GP IIb/IIIa ре-цепторов применяли в сочетании с аспирином и кло-пидогрелом, а также фондапаринуксом (n=1308) илиэноксапарином (n=1273) [164]. В целом частота кро-вотечений при лечении фондапаринуксом была ниже,чем при применении эноксапарина (см. раздел 5.3.).Бивалирудин и НФГ/НМГ характеризовались одинако-выми безопасностью и эффективностью в комбинациис аспирином, клопидогрелом и блокатором GP IIb/IIIaрецепторов в исследовании ACUITY [165]. Комбиниро-ванная терапия бивалирудином и блокаторомGP IIb/IIIa рецепторов привела к сходному снижениючастоты ишемических осложнений по сравнению содним бивалирудином, но сопровождалась более вы-сокой частотой больших кровотечений [166]. Эти дан-ные не позволяют рекомендовать широкое применениеданной комбинации.Выбор дозы блокаторов GP IIb/IIIa рецепторовЭффективность и безопасность блокаторовGP IIb/IIIa рецепторов в обычной клинической практи-ке изучалась в нескольких регистрах. Была отмечена вы-сокая частота больших кровотечений, которые были ча-стично связаны с назначением больших доз [167,168].Причинами передозировки были пожилой возраст, жен-ский пол, почечная недостаточность, низкая массатела, сахарный диабет и застойная сердечная недоста-точность. У пациентов, получавших слишком высокиедозы блокаторов GP IIb/IIIa рецепторов, скорректиро-ванная частота больших кровотечений была на 30%выше таковой при применении адекватных доз. Такимобразом, частота геморрагических осложнений в кли-нических исследований может быть заниженной посравнению с таковой в клинической практике, когда бло-каторы GP IIb/IIIa рецепторов применяют у пациентов,у которых чаще встречаются сопутствующие заболева-ния.Блокаторы GP IIb/IIIa рецепторови коронарное шунтированиеПри выполнении КШ у пациентов, получающихблокаторы GP IIb/IIIa рецепторов, необходимо обеспе-чить адекватный гемостаз и отменить блокаторGP IIb/IIIa рецепторов перед операцией или, если не-возможно, во время вмешательства. Эптифибатид и ти-рофибан обладают коротким периодом полувыведе-ния (около 2 ч), поэтому функция тромбоцитов при об-ратимом связывании рецепторов может восстановить-ся в конце КШ. Абциксимаб имеет короткий период по-лувыведения (10 мин), однако он медленно высвобож-дается из комплекса с рецептором с периодом полувы-ведения около 4 ч, поэтому восстановление нормаль-ной или близкой к норме агрегации тромбоцитовпроисходит в течение 48 ч после завершения инфузии(хотя абциксимаб, связанный с рецепторами, можетопределяться в течение более длительного времени).В случае значительного кровотечения возможна транс-фузия тромбоцитарной массы (см. раздел 5.5.9.). Длякупирования больших кровотечений при введениитирофибана и эптифибатида возможно применениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с тромбоци-тарной массой [169].
Антикоагулянты
Антикоагулянты применяют у пациентов с ОКС безподъема сегмента ST для ингибирования образованияи/или активности тромбина и для профилактики тром-бообразования. Установлена эффективность антикоа-гулянтов в сочетании с блокаторами функции тромбо-цитов, а комбинированная терапия была более эффек-тивной, чем монотерапия обоими средствами [171,172].У пациентов с ОКС без подъема сегмента ST изучалисьили изучаются несколько антикоагулянтов, действующихна различных уровнях каскада свертывания крови:
Рекомендации по применению блокаторов GP IIb/IIIa рецепторов
 Непрямые ингибиторы свертывания (для реализа-ции эффекта необходим антитромбин):Непрямые ингибиторы тромбина: НФГ НМГ. Непрямые ингибиторы Xa фактора: НМГ Фондапаринукс. Прямые ингибиторы свертывания. Прямые ингибиторы Ха фактора: апиксабан, ривароксабан, отамиксабан. Прямые ингибиторы тромбина: бивалирудин, дабигатран. Механизмы действия антикоагулянтов см. на рис. 3.Более подробную информацию можно найти в опуликованных обзорах [171].
Непрямые ингибиторы каскада коагуляции
Фондапаринукс. Единственным селективным ингибитором активиро-ванного фактора Х (фактора Ха) является фондапари-нукс — синтетический пентасахарид, который по строе-нию сходен с участком гепарина, связывающим анти-тромбин. Он ингибирует фактор Ха вследствие обрати-мого, высокоаффинного и неконвалентного связыванияс антитромбином. Фондапаринукс катализирует опосре-дованное антитромбином ингибирование фактора Хаи предупреждает образование тромбина. Препаратувеличивает способность к ингибированию фактора Хав 300 раз. Ингибирование 1 единицы фактора Ха по-давляет образование 50 единиц тромбина.Биодоступность фондапаринукса при подкожномвведении составляет 100%, а период полувыведения— 17 ч, поэтому его можно назначать один раз в день.Препарат выводится почками и противопоказан паци-ентам с клиренсом креатинина менее 20 мл/мин.Фондапаринукс не чувствителен к инактивирующемудействию белков, выделяющихся тромбоцитами инейтрализующих гепарин. При применении фондапа-ринукса не были описаны подтвержденные случаитромбоцитопении, индуцированной гепарином, дажепри широком его применении для профилактики и лече-ния венозных тромбоэмболических осложнений. Всвязи с этим мониторирование числа тромбоцитов нетребуется. При лечении фондапаринуксом нет не-обходимости в подборе дозы и контроле анти-Ха ак-тивности. Фондапаринукс не оказывает существенно-го влияния на стандартные показатели антикоагуляции,такие как активированное частичное тромбопластино-вое время (аЧТВ), активированное время свертывания(АВС), уровень протромбина и тромбиновое время.При ОКС фондапаринукс рекомендуется применятьв фиксированной дозе 2,5 мг/сут. Эта доза была вы-брана на основании результатов исследования PENTUA(дозо-определяющем исследовании фондапаринукса)и изучалась в двух крупных исследованиях III фазы(OASIS-5 и OASIS-6) [173–175]. В исследованииPENTUA доза 2,5 мг по эффективности и безопасностибыла по крайней мере сопоставима с более высокимидозами. Фондапаринукс применяли также в дозах2,5 и 5 мг внутривенно при плановых и неотложных ЧКВ.По эффективности и безопасности две дозы достовер-но не отличались друг от друга и от контроля (НФГ)[176]; однако в исследование были включены только350 пациентов, поэтому оно не обладало необходимойстатистической силой. Частота острой окклюзии сосу-да и тромбоза, выявленного при ангиографии, в двухгруппах фондапаринукса была несколько выше, чем вгруппе НФГ (фондапаринукс 2,5 мг — 2,5% и 5,1%,соответственно, фондапаринукс 5,0 мг — 0% и 4,3%,НФГ — 0,9% и 0,9%) [176].В исследовании OASIS-5 были рандомизированы20 078 пациентов с ОКС без подъема сегмента ST, ко-торым вводили фондапаринукс в дозе 2,5 мг один разв день подкожно или эноксапарин в дозе 1 мг/кг два раза в день подкожно в течение максимум 8 дн (в сред-нем 5,2 и 5,4 дн, соответственно) [175]. Частота пер-вичной конечной точки (смерть, ИМ или рефрактернаяишемия) через 9 дн составила 5,7% в группе энокса-парина и 5,8% в группе фондапаринукса (отноше-ние рисков 1,01; 95% ДИ 0,90–1,13), что подтвержда-ло сопоставимость эффектов двух препаратов. В то жевремя частота больших кровотечений была в 2 раза нижев группе фондапаринукса: 2,2% и 4,1%, соответ-ственно (отношение рисков 0,52; 95% ДИ 0,44–0,61;p<0,001). Большие кровотечения были независимымпредиктором смертности в отдаленном периоде, кото-рая значительно снизилась в группе фондапаринуксачерез 30 дн (2,9% и 3,5%; отношение рисков 0,83; 95%ДИ 0,71–0,97; p=0,02) и 6 мес (5,8% и 6,5%; отно-шение рисков 0,89; 95% ДИ 0,80–1,00; p=0,05). Че-рез 6 мес суммарная частота смерти, ИМ или инсуль-та в группе фондапаринукса была значительно ниже,чем в группе эноксапарина (11,3% и 12,5%; отноше-ние рисков 0,89; 95% ДИ 0,82–0,97; p=0,007). В вы-борке пациентов, которым проводили ЧКВ, частота боль-ших кровотечений (в том числе в области сосудистогодоступа) через 9 дн была значительно ниже в группефондапаринукса (2,4% и 5,1%; отношение рисков 0,46;95% ДИ 0,35–0,61; p<0,001). Интересно, что срок вме-шательства после введения последней дозы фондапа-ринукса не влиял на частоту больших кровотечений(1,6% и 1,3% — <6 ч и >6 ч, соответственно). Тромбозкатетера в группе фондапаринукса встречался чаще(0,9%), чем в группе эноксапарина (0,4%), однако егоудавалось ликвидировать путем введения эмпириче-ски подобранной болюсной дозы НФГ во время ЧКВ.Учитывая сопоставимую частоту ишемических исходовв группах фондапаринукса и гепарина через 9 дн, почистому клиническому эффекту (суммарной частотесмерти, ИМ, инсульта и больших кровотечений) фон-дапаринукс имел преимущества перед эноксапарином(8,2% и 10,4%; отношение рисков 0,78; 95% ДИ0,67–0,93; p=0,004).Предложено механистическое объяснение разницымежду фондапаринуксом и эноксапарином [177].Фондапаринукс в дозе 2,5 мг/сут по антикоагулянтнойактивности (анти-Ха активности) примерно в два разауступает эноксапарину в стандартной дозе. Степень ин-гибирования образования тромбина при примене-нии фондапаринукса также в два раза ниже. Это сви-детельствует о том, что низкий уровень антикоагуляциидостаточен для профилактики повторных ишемическихисходов в острую фазу ОКС без подъема сегмента ST упациентов, получающих полноценную антитромбо-цитарную терапию, в том числе аспирином и клопидо-грелом, а также блокатором GP IIb/IIIa рецепторов, учи-тывая отсутствие разницы частоты первичной конечнойточки через 9 дн между группами фондапаринукса иэноксапарина в исследовании OASIS-5 [175]. Низкийуровень антикоагуляции объясняет значительное сни-жение риска кровотечений. Однако подобная антикоа-гуляция недостаточна для профилактики тромбоза катетера во время ЧКВ. Это указывает на необходимостьвведения дополнительного болюса НФГ во время ЧКВу пациентов, получавших фондапаринукс.Оптимальная доза НФГ, которую следует вводить ввиде болюса во время ЧКВ пациентам, получающимфондапаринукс, изучалась в исследовании FUTURA/OASIS-8 [178]. В этом исследовании 2 026 пациентам,получавшим фондапаринукс и направленным на ЧКВв течение 72 ч после начала терапии, вводили НФГ ввиде болюса в низкой дозе (50 МЕ/кг) независимо отдозы блокатора GP IIb/IIIa рецепторов (если он приме-нялся) или в стандартной дозе 85 МЕ/кг (снижали до60 ЕД/кг в случае введения блокатора GP IIb/IIIa рецеп-торов), которую подбирали под контролем АВС. ЧКВбыло выполнено вскоре после введения последней дозыфондапаринукса (4 ч). Частота комбинированной пер-вичной конечной точки (большое кровотечение, неболь-шое кровотечение или большие кровотечения в обла-сти сосудистого доступа) через 48 ч после ЧКВ досто-верно не отличалась между двумя группами (4,7% и5,8%, соответственно; ОШ 0,80; 95% ДИ 0,54–1,19;p=0,27). Частота больших кровотечений была сходнойв двух группах (1,4% и 1,2%, соответственно) и сопо-ставимой с таковой у пациентов, направленных на ЧКВв группе фондапаринукса в исследовании OASIS-5(1,5% через 48 ч; те же критерии оценки кровотечений).Частота небольших кровотечений была ниже при вве-дении гепарина в низкой дозе (0,7% и 1,7%; ОШ 0,40;95% ДИ 0,16–0,97; p=0,04). По чистому клиническо-му эффекту (большое кровотечение через 48 ч или ре-васкуляризация целевого сосуда через 30 дн) преиму-щество имел гепарин в стандартной дозе (5,8% и3,9% — низкая и стандартная дозы, соответственно; ОШ1,51; 95% ДИ 1,00–2,28; p=0,05). Частота вторичнойконечной точки, включавшей в себя смерть, ИМ или ре-васкуляризацию целевого сосуда, также была ниже привведении гепарина в стандартной дозе (4,5% и 2,9%— низкая и стандартная дозы, соответственно; ОШ1,58; 95% ДИ 0,98–2,53; p=0,06). Тромбоз катетеравстречался редко (0,5% — низкая доза, 0,1% — стан-дартная доза; p=0,15). Полученные данные свидетель-ствуют о том, что пациентам, получавшим фондапари-нукс, во время ЧКВ обычный гепарин следует вводитьв стандартной дозе с учетом более выраженного чисто-го клинического эффекта и пониженного риска тром-боза катетера.
Рис. 3. Мишени действия антитромботических препаратов. АТ — антитромбин, GP — гликопротеин
Непрямые ингибиторы свертывания (для реализа-ции эффекта необходим антитромбин):Непрямые ингибиторы тромбина: НФГ НМГ. Непрямые ингибиторы Xa фактора: НМГ Фондапаринукс. Прямые ингибиторы свертывания. Прямые ингибиторы Ха фактора: апиксабан, ривароксабан, отамиксабан. Прямые ингибиторы тромбина: бивалирудин, дабигатран. Механизмы действия антикоагулянтов см. на рис. 3.Более подробную информацию можно найти в опуликованных обзорах [171].
Непрямые ингибиторы каскада коагуляции
Фондапаринукс. Единственным селективным ингибитором активиро-ванного фактора Х (фактора Ха) является фондапари-нукс — синтетический пентасахарид, который по строе-нию сходен с участком гепарина, связывающим анти-тромбин. Он ингибирует фактор Ха вследствие обрати-мого, высокоаффинного и неконвалентного связыванияс антитромбином. Фондапаринукс катализирует опосре-дованное антитромбином ингибирование фактора Хаи предупреждает образование тромбина. Препаратувеличивает способность к ингибированию фактора Хав 300 раз. Ингибирование 1 единицы фактора Ха по-давляет образование 50 единиц тромбина.Биодоступность фондапаринукса при подкожномвведении составляет 100%, а период полувыведения— 17 ч, поэтому его можно назначать один раз в день.Препарат выводится почками и противопоказан паци-ентам с клиренсом креатинина менее 20 мл/мин.Фондапаринукс не чувствителен к инактивирующемудействию белков, выделяющихся тромбоцитами инейтрализующих гепарин. При применении фондапа-ринукса не были описаны подтвержденные случаитромбоцитопении, индуцированной гепарином, дажепри широком его применении для профилактики и лече-ния венозных тромбоэмболических осложнений. Всвязи с этим мониторирование числа тромбоцитов нетребуется. При лечении фондапаринуксом нет не-обходимости в подборе дозы и контроле анти-Ха ак-тивности. Фондапаринукс не оказывает существенно-го влияния на стандартные показатели антикоагуляции,такие как активированное частичное тромбопластино-вое время (аЧТВ), активированное время свертывания(АВС), уровень протромбина и тромбиновое время.При ОКС фондапаринукс рекомендуется применятьв фиксированной дозе 2,5 мг/сут. Эта доза была вы-брана на основании результатов исследования PENTUA(дозо-определяющем исследовании фондапаринукса)и изучалась в двух крупных исследованиях III фазы(OASIS-5 и OASIS-6) [173–175]. В исследованииPENTUA доза 2,5 мг по эффективности и безопасностибыла по крайней мере сопоставима с более высокимидозами. Фондапаринукс применяли также в дозах2,5 и 5 мг внутривенно при плановых и неотложных ЧКВ.По эффективности и безопасности две дозы достовер-но не отличались друг от друга и от контроля (НФГ)[176]; однако в исследование были включены только350 пациентов, поэтому оно не обладало необходимойстатистической силой. Частота острой окклюзии сосу-да и тромбоза, выявленного при ангиографии, в двухгруппах фондапаринукса была несколько выше, чем вгруппе НФГ (фондапаринукс 2,5 мг — 2,5% и 5,1%,соответственно, фондапаринукс 5,0 мг — 0% и 4,3%,НФГ — 0,9% и 0,9%) [176].В исследовании OASIS-5 были рандомизированы20 078 пациентов с ОКС без подъема сегмента ST, ко-торым вводили фондапаринукс в дозе 2,5 мг один разв день подкожно или эноксапарин в дозе 1 мг/кг два раза в день подкожно в течение максимум 8 дн (в сред-нем 5,2 и 5,4 дн, соответственно) [175]. Частота пер-вичной конечной точки (смерть, ИМ или рефрактернаяишемия) через 9 дн составила 5,7% в группе энокса-парина и 5,8% в группе фондапаринукса (отноше-ние рисков 1,01; 95% ДИ 0,90–1,13), что подтвержда-ло сопоставимость эффектов двух препаратов. В то жевремя частота больших кровотечений была в 2 раза нижев группе фондапаринукса: 2,2% и 4,1%, соответ-ственно (отношение рисков 0,52; 95% ДИ 0,44–0,61;p<0,001). Большие кровотечения были независимымпредиктором смертности в отдаленном периоде, кото-рая значительно снизилась в группе фондапаринуксачерез 30 дн (2,9% и 3,5%; отношение рисков 0,83; 95%ДИ 0,71–0,97; p=0,02) и 6 мес (5,8% и 6,5%; отно-шение рисков 0,89; 95% ДИ 0,80–1,00; p=0,05). Че-рез 6 мес суммарная частота смерти, ИМ или инсуль-та в группе фондапаринукса была значительно ниже,чем в группе эноксапарина (11,3% и 12,5%; отноше-ние рисков 0,89; 95% ДИ 0,82–0,97; p=0,007). В вы-борке пациентов, которым проводили ЧКВ, частота боль-ших кровотечений (в том числе в области сосудистогодоступа) через 9 дн была значительно ниже в группефондапаринукса (2,4% и 5,1%; отношение рисков 0,46;95% ДИ 0,35–0,61; p<0,001). Интересно, что срок вме-шательства после введения последней дозы фондапа-ринукса не влиял на частоту больших кровотечений(1,6% и 1,3% — <6 ч и >6 ч, соответственно). Тромбозкатетера в группе фондапаринукса встречался чаще(0,9%), чем в группе эноксапарина (0,4%), однако егоудавалось ликвидировать путем введения эмпириче-ски подобранной болюсной дозы НФГ во время ЧКВ.Учитывая сопоставимую частоту ишемических исходовв группах фондапаринукса и гепарина через 9 дн, почистому клиническому эффекту (суммарной частотесмерти, ИМ, инсульта и больших кровотечений) фон-дапаринукс имел преимущества перед эноксапарином(8,2% и 10,4%; отношение рисков 0,78; 95% ДИ0,67–0,93; p=0,004).Предложено механистическое объяснение разницымежду фондапаринуксом и эноксапарином [177].Фондапаринукс в дозе 2,5 мг/сут по антикоагулянтнойактивности (анти-Ха активности) примерно в два разауступает эноксапарину в стандартной дозе. Степень ин-гибирования образования тромбина при примене-нии фондапаринукса также в два раза ниже. Это сви-детельствует о том, что низкий уровень антикоагуляциидостаточен для профилактики повторных ишемическихисходов в острую фазу ОКС без подъема сегмента ST упациентов, получающих полноценную антитромбо-цитарную терапию, в том числе аспирином и клопидо-грелом, а также блокатором GP IIb/IIIa рецепторов, учи-тывая отсутствие разницы частоты первичной конечнойточки через 9 дн между группами фондапаринукса иэноксапарина в исследовании OASIS-5 [175]. Низкийуровень антикоагуляции объясняет значительное сни-жение риска кровотечений. Однако подобная антикоа-гуляция недостаточна для профилактики тромбоза катетера во время ЧКВ. Это указывает на необходимостьвведения дополнительного болюса НФГ во время ЧКВу пациентов, получавших фондапаринукс.Оптимальная доза НФГ, которую следует вводить ввиде болюса во время ЧКВ пациентам, получающимфондапаринукс, изучалась в исследовании FUTURA/OASIS-8 [178]. В этом исследовании 2 026 пациентам,получавшим фондапаринукс и направленным на ЧКВв течение 72 ч после начала терапии, вводили НФГ ввиде болюса в низкой дозе (50 МЕ/кг) независимо отдозы блокатора GP IIb/IIIa рецепторов (если он приме-нялся) или в стандартной дозе 85 МЕ/кг (снижали до60 ЕД/кг в случае введения блокатора GP IIb/IIIa рецеп-торов), которую подбирали под контролем АВС. ЧКВбыло выполнено вскоре после введения последней дозыфондапаринукса (4 ч). Частота комбинированной пер-вичной конечной точки (большое кровотечение, неболь-шое кровотечение или большие кровотечения в обла-сти сосудистого доступа) через 48 ч после ЧКВ досто-верно не отличалась между двумя группами (4,7% и5,8%, соответственно; ОШ 0,80; 95% ДИ 0,54–1,19;p=0,27). Частота больших кровотечений была сходнойв двух группах (1,4% и 1,2%, соответственно) и сопо-ставимой с таковой у пациентов, направленных на ЧКВв группе фондапаринукса в исследовании OASIS-5(1,5% через 48 ч; те же критерии оценки кровотечений).Частота небольших кровотечений была ниже при вве-дении гепарина в низкой дозе (0,7% и 1,7%; ОШ 0,40;95% ДИ 0,16–0,97; p=0,04). По чистому клиническо-му эффекту (большое кровотечение через 48 ч или ре-васкуляризация целевого сосуда через 30 дн) преиму-щество имел гепарин в стандартной дозе (5,8% и3,9% — низкая и стандартная дозы, соответственно; ОШ1,51; 95% ДИ 1,00–2,28; p=0,05). Частота вторичнойконечной точки, включавшей в себя смерть, ИМ или ре-васкуляризацию целевого сосуда, также была ниже привведении гепарина в стандартной дозе (4,5% и 2,9%— низкая и стандартная дозы, соответственно; ОШ1,58; 95% ДИ 0,98–2,53; p=0,06). Тромбоз катетеравстречался редко (0,5% — низкая доза, 0,1% — стан-дартная доза; p=0,15). Полученные данные свидетель-ствуют о том, что пациентам, получавшим фондапари-нукс, во время ЧКВ обычный гепарин следует вводитьв стандартной дозе с учетом более выраженного чисто-го клинического эффекта и пониженного риска тром-боза катетера.
Рис. 3. Мишени действия антитромботических препаратов. АТ — антитромбин, GP — гликопротеин
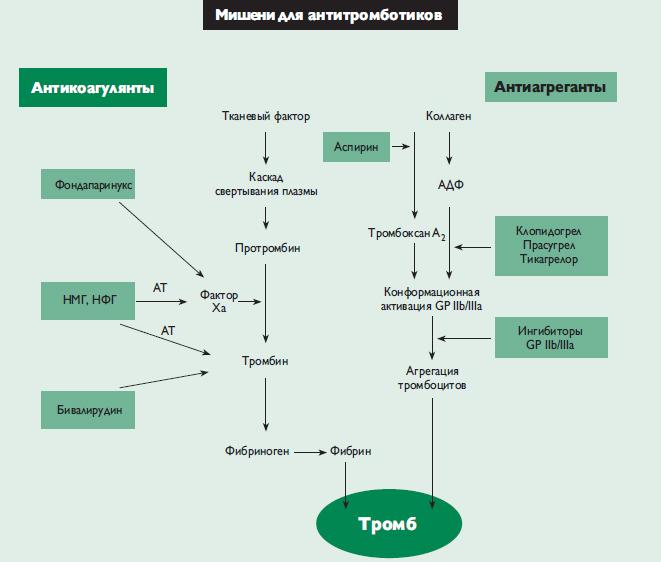 Низкомолекулярные гепарины
НМГ — это производные гепарина с молекулярноймассой от 2000 до 10000 Да. Они характеризуются сба-лансированной анти-Ха и анти-IIa активностью, кото-рая зависит от молекулярной массы препарата. При уве-личении последней повышается анти-IIa активность.НМГ отличаются по фармакокинетическим и анти-коагулянтным свойствам и, соответственно, не яв-ляются взаимозаменяемыми. НМГ имеют несколько пре-имуществ перед НФГ, включая более полное всасыва-ние после подкожного введения, меньшее связываниес белками, менее выраженную активацию тромбоци-тов и более предсказуемую зависимость эффекта от дозы[171]. При лечении НМГ риск развития тромбоцитопе-нии, индуцированной гепарином, ниже, чем при лече-нии НФГ; НМГ, по крайней мере частично, выводятсяпочками. Риск накопления увеличивается при сниже-нии функции почек, которое сопровождается повыше-нием риска кровотечения. Большинство НМГ противо-показаны пациентам с почечной недостаточностью(клиренс креатинина ниже 30 мл/мин). Однако дозуэноксапарина у пациентов с клиренсом креатинина ме-нее 30 мл/мин можно снизить (1 мг/кг один раз в день,а не два раза в день).НМГ при ОКС без подъема сегмента ST назначают вподобранной по массе тела и обычно вводят подкож-но два раза в день, хотя у пациентов высокого рискалечение можно начинать с внутривенного введения бо-люса [179-182]. При применении НМГ в стандартныхдозах мониторирование анти-Ха активности не требу-ется за исключением особых ситуаций, например у па-циентов с почечной недостаточностью или ожирением.Оптимальный уровень анти-Ха активности, который дол-жен быть достигнут у пациентов с ОКС без подъема сег-мента ST, не установлен. У пациентов с венозной тром-боэмболией (ВТЭ) терапевтический диапазон состав-ляет 0,6-1,0 МЕ/мл. Четкая связь между анти-Ха актив-ностью и клиническими исходами не установлена.Однако риск кровотечений увеличивается, когда анти-Ха активность превышает 1,0 МЕ/мл [183]. В дозоопре-деляющем исследовании у пациентов с ОКС без подъе-ма сегмента ST эноксапарин изучали в дозах 1,25 и 1,0мг/кг два раза в день. Максимальная анти-Ха активностьв двух группах составляла 1,5 и 1,0 МЕ/мл, соответ-ственно. При применении эноксапарина в дозе 1,25мг/кг частота больших кровотечений в течение 14 днравнялась 6,5% (в основном в области сосудистого до-ступа). В группе эноксапарина 1,0 мг/кг частота боль-ших кровотечений снизилась до 1,9%. У пациентов сбольшими кровотечениями анти-Ха активность нахо-дилась в диапазоне 1,8-2,0 МЕ/мл [184]. В крупной ко-горте пациентов с нестабильной стенокардией/ИМбез подъема сегмента ST низкая анти-Ха активность(<0,5 МЕ/мл) при лечении эноксапарином ассоции-ровалась с трехкратным увеличением смертности у па-циентов с анти-Ха активностью в целевом диапазоне0,5-1,2 МЕ/мл. Низкие уровни анти-Ха (<0,05 МЕ/мл)были независимым предиктором смертности в течение30 дн. Это свидетельствует о том, что при лечении энок-сапарином уровень анти-Ха активности по возможно-сти должен составлять по крайней мере 0,5 МЕ/мл [185]. В неконтролируемых исследованиях и неболь-ших контролируемых исследованиях у пациентов, ко-торым проводились ЧКВ, анти-Ха активность >0,5МЕ/мл ассоциировалась с низкой частотой ишемиче-ских и геморрагических осложнений [186,187].Опубликованы результаты нескольких мета-анали-зов исследований, в которых сравнивали эффективностьНМГ и НФГ у пациентов с ОКС без подъема сегмента ST.В первый мета-анализ были включены 12 клиническихисследований различных препаратов в целом у 17 157пациентов с ОКС без подъема сегмента ST, получавшихаспирин. Гепарины достоверно превосходили плаце-бо по эффективности в профилактике смерти или ИМ(ОШ 0,53; 95% ДИ 0,38–0,73; p=0,0001). НМГ неимели преимуществ перед НФГ по эффективностиили безопасности [172]. При мета-анализе всех иссле-дований, в которых изучались эноксапарин и НФГ, в це-лом у 21 946 пациентов достоверной разницы смерт-ности через 30 дн не выявлено (3,0% и 3,0%, соответ-ственно; ОШ 1,00; 95% ДИ 0,85–1,17; p=незначимый).При лечении эноксапарином выявлено дополнитель-ное снижение риска смерти или ИМ в течение 30 дн посравнению с гепарином (10,1% и 11,0%; ОШ 0,91;95% ДИ 0,83–0,99). При анализе post-hoc в подгруп-пе пациентов, не получавших НФГ перед рандомиза-цией, выявлено значительное снижение смертности иличастоты ИМ в течение 30 дн при лечении эноксапари-ном по сравнению с НФГ (8,0% и 9,4%, соответ-ственно; ОШ 0,81; 95% ДИ 0,70–0,94). Достовернойразницы частоты гемотрансфузий (7,2% и 7,5%;ОШ 1,01; 95% ДИ 0,89–1,14) или больших кровотече-ний (4,7% и 4,5%; ОШ 1,04; 95% ДИ 0,83–1,30) че-рез 7 дн после рандомизации отмечено не было как вовсей выборке, так и в выборке пациентов, не получав-ших антикоагулянты перед рандомизацией. При допол-нительном мета-анализе, в который были включены всеисследования эноксапарина у пациентов с ОКС (как безподъема сегмента ST, так и с подъемом сегмента ST),были получены сходные результаты [188].И, наконец, в небольших исследованиях сравнива-ли эффективность и безопасность НМГ и НФГ в комби-нации с блокаторами GP IIb/IIIa рецепторов. По безопас-ности две схемы лечения не отличались. Ни в одном ис-следовании не было выявлено разницы риска «твердых»конечных точек, за исключением исследованияINTERACT, в котором имелась достоверная разница меж-ду группами эноксапарина/эптифибатида и НФГ/эп-тифибатида в пользу первой схемы [189-191]. Одна-ко все эти исследования не обладали необходимойстатистической силой, чтобы сделать окончательныевыводы.Большинство исследований проводились в то вре-мя, когда инвазивная стратегия еще не была внедренав широкую практику, а в некоторых исследованиях при-менение инвазивных методов вообще не рекомендо-валось. В результате инвазивное лечение проводилосьтолько у небольшой части пациентов, поэтому любыевыводы, сделанные на основании этих исследований,сегодня будут устаревшими.Единственным исследованием, в котором эноксапа-рин сравнивали с НФГ на фоне высокой частоты ЧКВ,реваскуляризации, стентирования и активной антитром-боцитарной терапии аспирином, клопидогрелом иблокаторами GP IIb/IIIa, было SYNERGY [192]. В это ис-следование были включены 10 027 пациентов высо-кого риска, которым проводили инвазивное обследо-вание и реваскуляризацию. 76% пациентов получалиантикоагулянты перед рандомизацией. Достовернойразницы частоты смерти и ИМ через 30 дн между груп-пами эноксапарина и НФГ не выявили (14,0% и14,5%, соответственно; ОШ 0,96; 95% ДИ 0,86–1,06;p=незначимый) [193]. Частота кровотечений былавыше в группе эноксапарина, в частности было отмече-но достоверное увеличение частоты больших кровотече-ний в соответствии с критериями TIMI (9,1% и 7,6%;p=0,008), но недостоверное увеличение частоты тяже-лых кровотечений в соответствии с критериямиGUSTO (2,7% и 2,2%; p=0,08) и гемотрансфузий(17,0% и 16,0%; p=0,16). Повышенная частота кро-вотечений, вероятно, отражала частое применениеантикоагулянтов перед рандомизацией и, возможно,частую смену антикоагулянта после рандомизации.Тем не менее, НМГ, особенно эноксапарин, часто при-меняют при ЧКВ, хотя мониторировать антикоагуляциюнелегко. Фармакокинетические/фармакодинамиче-ские свойства эноксапарина отличаются при подкожноми внутривенном применении. При плановом ЧКВ энок-сапарин вводят в дозе 1 мг/кг внутривенно. Внутривен-ные дозы, которые изучались в клинических исследова-ниях, были ниже (обычно 0,5 мг/кг) и обеспечивали туже максимальную анти-Ха активность в течение 3 мин[194]. Эноксапарин при внутривенном введении даетбыстрый и предсказуемый антикоагулянтный эффект втечение 2 ч. Более низкие дозы изучались также в иссле-довании STEEPLE [195]. У пациентов без ОКС частота кро-вотечений в группе эноксапарина в дозах 0,5 и 0,75 мг/кгбыла ниже, чем в группе НФГ. Однако исследование необладало статистической силой, необходимой для вы-явления различий между группами эноксапарина.У пациентов с ОКС без подъема сегмента ST, полу-чавших эноксапарин, не рекомендуется дополнитель-ное введение эноксапарина во время ЧКВ, если послед-няя подкожная инъекция препарата была выполненаменее чем за 8 ч до вмешательства. Если эноксапаринвводили более чем за 8 ч до ЧКВ, то рекомендуется до-полнительное введение 0,3 мг/кг внутривенно в видеболюса. Переход с одного антикоагулянта на другой вовремя ЧКВ не рекомендуется.
Нефракционированный гепарин
НФГ — это неоднородная смесь полисахаридов с мо-лекулярной массой от 2 000 до 30 000 Да (в основном15 000-18 000 Да). Одна треть молекул, входящих всостав НФГ, содержит пентасахарид, который связыва-ется с антитромбином и увеличивает скорость ингиби-рования фактора Ха. Для подавления фактора IIa необхо-димо взаимодействие гепарина с тромбином и анти-тромбином с образованием связи между ними. НФГплохо всасывается после подкожного введения, поэто-му его предпочтительно вводить внутривенно. Препа-рат обладает узким терапевтическим окном, в связи счем необходимо частое мониторирование аЧТВ. Целе-вой его уровень составляет 50-75 с (в 1,5-2,5 раза вышеверхней границы нормы). При более высоких значенияхаЧТВ увеличивается риск геморрагических осложнений,а дополнительный антитромботический эффект отсут-ствует. При аЧТВ менее 50 с антитромботическое дей-ствие ограниченно. НФГ рекомендуется назначать в дозе,подобранной по массе тела. Лечение начинают с вве-дения болюса 60-70 ед/кг (максимум 5 000 ед) с после-дующей инфузией по 12-15 ед/кг/ч (максимум1 000 ед/ч). Такая схема чаще всего обеспечивает до-стижение целевых значений аЧТВ [171]. Антикоагулянт-ный эффект НФГ быстро прекращается (в течение не-скольких часов после прекращения введения). В пер-вые 24 ч после прекращения терапии существует рискреактивации процесса свертывания и, соответственно,преходящего повышения риска рецидивирующих ише-мических осложнений, несмотря на одновременную те-рапию аспирином.При мета-анализе 6 исследований было показано,что кратковременное введение НФГ приводит к сниже-нию риска смерти или ИМ на 33% по сравнению с пла-цебо или отсутствием антикоагуляции (ОШ 0,67; 95%ДИ 0,45–0,99; p=0,04) [172]. Благоприятный эф-фект препарата был связан со снижением риска разви-тия ИМ. В клинических исследованиях, в которыхсравнивали комбинированную терапию НФГ+аспирини монотерапию аспирином у пациентов с ОКС безподъема сегмента ST, было отмечено небольшое пре-имущество комбинированной терапии, но ценой уве-личения риска кровотечений. Рецидивы ишемическихосложнений после отмены НФГ объясняют, почему этотэффект не сохранялся в более поздние сроки, если па-циентам не проводили реваскуляризацию до прекра-щения введения НФГ.При ЧКВ стандартный гепарин вводят внутривеннов виде болюса под контролем АВС (250-350 с или200-250 с, если вводился блокатор GP IIb/IIIa рецеп-торов) или в дозе, подобранной пo массе тела (обыч-но 70-100 ед/кг или 50-60 ед/кг в комбинации с бло-каторами GP IIb/IIIa рецепторов) [171]. Учитываязначительную вариабельность биодоступности НФГ, егорекомендуется применять под контролем АВС, особен-но при длительных вмешательствах, когда может потре-боваться введение дополнительной дозы. Продолже-ние гепаринизации после завершения вмешательства(до или после удаления проводника) не рекомендуется.Если пациент поступает в ангиографическую лабо-раторию на фоне продолжающейся инфузии гепари-на, то введение дополнительного болюса НФГ не-обходимо адаптировать с учетом АВС и применения бло-каторов GP IIb/IIIa рецепторов.
Прямые ингибиторы тромбина (бивалирудин)
Хотя разрабатывались несколько прямых ингибито-ров тромбина, только бивалирудин был разрешен к кли-ническому применению при ЧКВ и ОКС. Бивалирудиннепосредственно связывается с тромбином (факторомIIa) и ингибирует индуцированное им превращениефибриногена в фибрин. Бивалирудин инактивируеттромбин, связанный с фибрином, а также находя-щийся в жидкой фазе. Он не связывается с белками плаз-мы, поэтому антикоагулянтное действие препаратаболее предсказуемое. Бивалирудин полностью выво-дится почками. Показатели свертывания (аЧТВ, АВС) тес-но коррелируют с концентрациями в плазме, поэтомуэти два теста можно использовать для мониторирова-ния антикоагулянтной активности бивалирудина.Бивалирудин первоначально изучали при ЧКВ. В ис-следовании REPLACE-2 бивалирудин±блокаторыGP IIb/IIIa рецепторов не уступали НФГ±блокаторыGP IIb/IIIa рецепторов по эффективности в профилак-тике ишемических осложнений при ЧКВ, но значитель-но реже вызывали большие кровотечения (2,4% и4,1%; p<0,001). Достоверной разницы частоты твер-дых конечных точек через 1 мес, 6 мес и 1 год не вы-явили. Бивалирудин в настоящее время разрешен к при-менению при неотложных и плановых ЧКВ в дозе0,75 мг/кг в виде болюса с последующей инфузией по1,75 мг/кг/ч. У пациентов с ОКС без подъема сегмен-та ST бивалирудин рекомендуется вводить в дозе0,1 мг/кг внутривенно в виде болюса, а затем по0,25 мг/кг/ч до ЧКВ.ACUITY было единственным исследованием, в ко-тором бивалирудин специально изучали у пациентовс ОКС без подъема сегмента ST [196]. В это рандоми-зированное открытое исследование были включены13 819 пациентов с ОКС без подъема сегмента ST вы-сокого риска, которым планировалось инвазивноелечение. Пациентов рандомизировали в три группы:стандартная комбинированная терапия НФГ или НМГв сочетании с блокатором GP IIb/IIIa рецепторов (конт-рольная группа) (n=4 603); бивалирудин в комбина-ции с блокатором GP IIb/IIIa рецепторов (n=4 604);только бивалирудин (n=4 612). Лечение бивалируди-ном начинали перед ангиографией с внутривенного введения болюса 0,1 мг/кг с последующей инфузиейпо 0,25 мг/кгч. Перед ЧКВ вводили дополнительно бо-люс 0,5 мг/кг внутривенно, а затем проводили инфу-зию по 1,75 мг/кг/ч. После ЧКВ введение препаратапрекращали. У пациентов, получавших НФН/НМГ в со-четании с блокатором GP IIb/IIIa рецепторов или бива-лирудин в комбинации с блокатором GP IIb/IIIa рецеп-торов, частота комбинированной конечной точки (ише-мические осложнения) через 30 дн (7,3% и 7,7%, со-ответственно; ОР 1,07; 95% ДИ 0,92–1,23; p=0,39) ибольших кровотечений (5,7% и 5,3%; ОР 0,93; 95%ДИ 0,78–1,10; p=0,38) достоверно не отличалась. Би-валирудин не уступал стандартной терапии по эффек-тивности в профилактике ишемических исходов (7,8%и 7,3%; ОР 1,08; 95% ДИ 0,93–1,24; p=0,32), но до-стоверно реже вызывал большие кровотечения (3,0%и 5,7%; ОР 0,53; 95% ДИ 0,43–0,65; p<0,001). Со-ответственно, через 30 дн он имел достоверные пре-имущества перед НФГ/НМГ в сочетании с блокаторомGP IIb/IIIa рецепторов по «чистому» клиническому эф-фекту (10,1% и 11,7%; ОР 0,86; 95% ДИ 0,77–0,94;p=0,02) [196]. Эффективность монотерапии бивали-рудином была сопоставимой в большинстве подгрупп,выделенных в соответствии с протоколом, за исключе-нием пациентов, получавших клопидогрел перед ЧКВ,у которых была отмечена более высокая частота ише-мических исходов в группе бивалирудина (9,1% и7,1%; ОР 1,29; 95% ДИ 1,03–1,63).В целом лечение бивалирудином±блокаторомGP IIb/IIIa рецепторов по эффективности было сопоста-вимым с терапией НФГ/НМГ в сочетании с системати-ческим применением блокаторов GP IIb/IIIa рецепто-ров, но сопровождалось значительным снижениемриска больших кровотечений [197]. Однако в исследо-вании ACUITY не было выявлено достоверной разни-цы исходов в ближайшем и отдаленном периоде присравнении двух стратегий антикоагулянтной терапии[198]. И наконец, полученные данные показали, что пе-реход с НФГ или НМГ на бивалирудин во время ЧКВ неприводит к увеличению риска кровотечений, а факти-чески способствует их предупреждению [199].
Новые антикоагулянты
В настоящее время изучаются эффективность и без-опасность новых антикоагулянтов у пациентов с ОКС. Боль-шинство из них предназначены, скорее, для вторичнойпрофилактики, а не для лечения в острую фазу заболе-вания. Ингибиторы фактора Ха изучались в исследова-ниях II фазы [200,201]. Прямые пероральные ингиби-торы фактора Ха апиксабан (APPRAISE) [202] и риварок-сабан (ATLAS ACS-TIMI) [201] в различных дозах приме-няли в течение 6 мес у пациентов, недавно перенесшихОКС, на фоне лечения аспирином или двойной антитром-боцитарной терапии ацетилсалициловой кислотой и кло-пидогрелом. В обоих исследованиях были выявлены до-зозависимое увеличение частоты кровотечений и тенден-ция к снижению риска ишемических осложнений, осо-бенно у пациентов, получавших один аспирин. На осно-вании полученных данных были начаты исследованияIII фазы (APPRAISE-2 и ATLAS-2). ИсследованиеAPPRAISE-2 было прекращено досрочно в связи с повы-шенным риском кровотечений в группе апиксабана.Прямой ингибитор тромбина дабигатран изучалсяв дозоопределяющем исследовании II фазы (RE-DEEM),результаты которого пока не опубликованы. Отамикса-бан, являющийся прямым ингибитором фактора Ха,предназначенным для внутривенного введения, такжеизучался в исследовании II фазы [203]; исследованиеIII фазы продолжается.
Комбинированная терапия антикоагулянтамии антитромбоцитарными препаратами
Антикоагуляцию и двойную антитромбоцитарнуютерапию аспирином и блокатором P2Y12 рецептороврекомендуется начинать сразу после развития ОКСбез подъема сегмента ST. Антикоагуляцию продолжаюттолько в острую фазу, а двойную антитромбоцитарнуютерапию рекомендуется проводить в течение 12 мес какпосле стентирования, так и без стентирования. У значи-тельной части пациентов (6-8%) с ОКС без подъема сег-мента ST имеются показания к длительной терапии пе-роральными антагонистами витамина К, в том числефибрилляция предсердий со средним или высоким рис-ком тромбоэмболических осложнений, протез клапа-на сердца или ВТЭ. Двойная антитромботическая тера-пия (аспирин или клопидогрел+антагонист витаминаК) или тройная терапия (аспирин, клопидогрел и ан-тагонист витамина К) сопровождается 3-4-кратным уве-личением частоты больших кровотечений. Ведениетаких пациентов представляет трудную задачу. Так, вострую фазу и в последующем необходимо поддержи-вать адекватный уровень антикоагуляции. Перерыв влечении антагонистами витамина К может привести кповышению риска тромбоэмболических осложнений.На фоне полной антикоагуляции антагонистами вита-мина К может быть затруднительным или невозмож-ным выполнение ангиографии, ЧКВ или КШ, а длитель-ная тройная терапия сопровождается высоким рискомкровотечений. В связи с этим необходимо соблюдатьмеры предосторожности, которые рассматриваются внедавно опубликованных рекомендациях по плановымвмешательствам на коронарных артериях и ведению па-циентов в острую фазу (ИМ с подъемом и без подъе-ма сегмента ST) [204]. Стенты, выделяющие лекарства,следует имплантировать только в тех клиническихи/или анатомических ситуациях (распространеннаябляшка, небольшие сосуды, диабет и т.д.), когда ониимеют значительные преимущества перед голометаллическими стентами. Если пациенту, получающемудвойную или тройную терапию, требуется повторная ан-гиография, предпочтительно применение лучевогодоступа с целью снижения риска кровотечений. Реко-мендовалось также проводить ЧКВ на фоне терапии ан-тагонистами витамина К.В острую фазу может быть оправданным прекраще-ние приема антагонистов витамина К и назначение ан-титромбоцитарных препаратов и антикоагулянтов приснижении МНО менее 2,0. Если необходима дли-тельная терапия антагонистами витамина К в сочетаниис клопидогрелом и/или аспирином в низкой дозе, сле-дует тщательно контролировать МНО (целевой диапа-зон 2,0-2,5). Длительность тройной терапии следуетограничивать с учетом клинической ситуации, им-плантации стента, выделяющего или не выделяющеголекарства, и риска ишемических и геморрагическихосложнений, который оценивают на основании индек-сов и/или исходных показателей (табл. 6). Около по-ловины спонтанных кровотечений являются желудоч-но-кишечными, поэтому следует назначать ингибито-ры протонной помпы с целью гастропротекции.
Рекомендации по применению антикоагулянтов
Низкомолекулярные гепарины
НМГ — это производные гепарина с молекулярноймассой от 2000 до 10000 Да. Они характеризуются сба-лансированной анти-Ха и анти-IIa активностью, кото-рая зависит от молекулярной массы препарата. При уве-личении последней повышается анти-IIa активность.НМГ отличаются по фармакокинетическим и анти-коагулянтным свойствам и, соответственно, не яв-ляются взаимозаменяемыми. НМГ имеют несколько пре-имуществ перед НФГ, включая более полное всасыва-ние после подкожного введения, меньшее связываниес белками, менее выраженную активацию тромбоци-тов и более предсказуемую зависимость эффекта от дозы[171]. При лечении НМГ риск развития тромбоцитопе-нии, индуцированной гепарином, ниже, чем при лече-нии НФГ; НМГ, по крайней мере частично, выводятсяпочками. Риск накопления увеличивается при сниже-нии функции почек, которое сопровождается повыше-нием риска кровотечения. Большинство НМГ противо-показаны пациентам с почечной недостаточностью(клиренс креатинина ниже 30 мл/мин). Однако дозуэноксапарина у пациентов с клиренсом креатинина ме-нее 30 мл/мин можно снизить (1 мг/кг один раз в день,а не два раза в день).НМГ при ОКС без подъема сегмента ST назначают вподобранной по массе тела и обычно вводят подкож-но два раза в день, хотя у пациентов высокого рискалечение можно начинать с внутривенного введения бо-люса [179-182]. При применении НМГ в стандартныхдозах мониторирование анти-Ха активности не требу-ется за исключением особых ситуаций, например у па-циентов с почечной недостаточностью или ожирением.Оптимальный уровень анти-Ха активности, который дол-жен быть достигнут у пациентов с ОКС без подъема сег-мента ST, не установлен. У пациентов с венозной тром-боэмболией (ВТЭ) терапевтический диапазон состав-ляет 0,6-1,0 МЕ/мл. Четкая связь между анти-Ха актив-ностью и клиническими исходами не установлена.Однако риск кровотечений увеличивается, когда анти-Ха активность превышает 1,0 МЕ/мл [183]. В дозоопре-деляющем исследовании у пациентов с ОКС без подъе-ма сегмента ST эноксапарин изучали в дозах 1,25 и 1,0мг/кг два раза в день. Максимальная анти-Ха активностьв двух группах составляла 1,5 и 1,0 МЕ/мл, соответ-ственно. При применении эноксапарина в дозе 1,25мг/кг частота больших кровотечений в течение 14 днравнялась 6,5% (в основном в области сосудистого до-ступа). В группе эноксапарина 1,0 мг/кг частота боль-ших кровотечений снизилась до 1,9%. У пациентов сбольшими кровотечениями анти-Ха активность нахо-дилась в диапазоне 1,8-2,0 МЕ/мл [184]. В крупной ко-горте пациентов с нестабильной стенокардией/ИМбез подъема сегмента ST низкая анти-Ха активность(<0,5 МЕ/мл) при лечении эноксапарином ассоции-ровалась с трехкратным увеличением смертности у па-циентов с анти-Ха активностью в целевом диапазоне0,5-1,2 МЕ/мл. Низкие уровни анти-Ха (<0,05 МЕ/мл)были независимым предиктором смертности в течение30 дн. Это свидетельствует о том, что при лечении энок-сапарином уровень анти-Ха активности по возможно-сти должен составлять по крайней мере 0,5 МЕ/мл [185]. В неконтролируемых исследованиях и неболь-ших контролируемых исследованиях у пациентов, ко-торым проводились ЧКВ, анти-Ха активность >0,5МЕ/мл ассоциировалась с низкой частотой ишемиче-ских и геморрагических осложнений [186,187].Опубликованы результаты нескольких мета-анали-зов исследований, в которых сравнивали эффективностьНМГ и НФГ у пациентов с ОКС без подъема сегмента ST.В первый мета-анализ были включены 12 клиническихисследований различных препаратов в целом у 17 157пациентов с ОКС без подъема сегмента ST, получавшихаспирин. Гепарины достоверно превосходили плаце-бо по эффективности в профилактике смерти или ИМ(ОШ 0,53; 95% ДИ 0,38–0,73; p=0,0001). НМГ неимели преимуществ перед НФГ по эффективностиили безопасности [172]. При мета-анализе всех иссле-дований, в которых изучались эноксапарин и НФГ, в це-лом у 21 946 пациентов достоверной разницы смерт-ности через 30 дн не выявлено (3,0% и 3,0%, соответ-ственно; ОШ 1,00; 95% ДИ 0,85–1,17; p=незначимый).При лечении эноксапарином выявлено дополнитель-ное снижение риска смерти или ИМ в течение 30 дн посравнению с гепарином (10,1% и 11,0%; ОШ 0,91;95% ДИ 0,83–0,99). При анализе post-hoc в подгруп-пе пациентов, не получавших НФГ перед рандомиза-цией, выявлено значительное снижение смертности иличастоты ИМ в течение 30 дн при лечении эноксапари-ном по сравнению с НФГ (8,0% и 9,4%, соответ-ственно; ОШ 0,81; 95% ДИ 0,70–0,94). Достовернойразницы частоты гемотрансфузий (7,2% и 7,5%;ОШ 1,01; 95% ДИ 0,89–1,14) или больших кровотече-ний (4,7% и 4,5%; ОШ 1,04; 95% ДИ 0,83–1,30) че-рез 7 дн после рандомизации отмечено не было как вовсей выборке, так и в выборке пациентов, не получав-ших антикоагулянты перед рандомизацией. При допол-нительном мета-анализе, в который были включены всеисследования эноксапарина у пациентов с ОКС (как безподъема сегмента ST, так и с подъемом сегмента ST),были получены сходные результаты [188].И, наконец, в небольших исследованиях сравнива-ли эффективность и безопасность НМГ и НФГ в комби-нации с блокаторами GP IIb/IIIa рецепторов. По безопас-ности две схемы лечения не отличались. Ни в одном ис-следовании не было выявлено разницы риска «твердых»конечных точек, за исключением исследованияINTERACT, в котором имелась достоверная разница меж-ду группами эноксапарина/эптифибатида и НФГ/эп-тифибатида в пользу первой схемы [189-191]. Одна-ко все эти исследования не обладали необходимойстатистической силой, чтобы сделать окончательныевыводы.Большинство исследований проводились в то вре-мя, когда инвазивная стратегия еще не была внедренав широкую практику, а в некоторых исследованиях при-менение инвазивных методов вообще не рекомендо-валось. В результате инвазивное лечение проводилосьтолько у небольшой части пациентов, поэтому любыевыводы, сделанные на основании этих исследований,сегодня будут устаревшими.Единственным исследованием, в котором эноксапа-рин сравнивали с НФГ на фоне высокой частоты ЧКВ,реваскуляризации, стентирования и активной антитром-боцитарной терапии аспирином, клопидогрелом иблокаторами GP IIb/IIIa, было SYNERGY [192]. В это ис-следование были включены 10 027 пациентов высо-кого риска, которым проводили инвазивное обследо-вание и реваскуляризацию. 76% пациентов получалиантикоагулянты перед рандомизацией. Достовернойразницы частоты смерти и ИМ через 30 дн между груп-пами эноксапарина и НФГ не выявили (14,0% и14,5%, соответственно; ОШ 0,96; 95% ДИ 0,86–1,06;p=незначимый) [193]. Частота кровотечений былавыше в группе эноксапарина, в частности было отмече-но достоверное увеличение частоты больших кровотече-ний в соответствии с критериями TIMI (9,1% и 7,6%;p=0,008), но недостоверное увеличение частоты тяже-лых кровотечений в соответствии с критериямиGUSTO (2,7% и 2,2%; p=0,08) и гемотрансфузий(17,0% и 16,0%; p=0,16). Повышенная частота кро-вотечений, вероятно, отражала частое применениеантикоагулянтов перед рандомизацией и, возможно,частую смену антикоагулянта после рандомизации.Тем не менее, НМГ, особенно эноксапарин, часто при-меняют при ЧКВ, хотя мониторировать антикоагуляциюнелегко. Фармакокинетические/фармакодинамиче-ские свойства эноксапарина отличаются при подкожноми внутривенном применении. При плановом ЧКВ энок-сапарин вводят в дозе 1 мг/кг внутривенно. Внутривен-ные дозы, которые изучались в клинических исследова-ниях, были ниже (обычно 0,5 мг/кг) и обеспечивали туже максимальную анти-Ха активность в течение 3 мин[194]. Эноксапарин при внутривенном введении даетбыстрый и предсказуемый антикоагулянтный эффект втечение 2 ч. Более низкие дозы изучались также в иссле-довании STEEPLE [195]. У пациентов без ОКС частота кро-вотечений в группе эноксапарина в дозах 0,5 и 0,75 мг/кгбыла ниже, чем в группе НФГ. Однако исследование необладало статистической силой, необходимой для вы-явления различий между группами эноксапарина.У пациентов с ОКС без подъема сегмента ST, полу-чавших эноксапарин, не рекомендуется дополнитель-ное введение эноксапарина во время ЧКВ, если послед-няя подкожная инъекция препарата была выполненаменее чем за 8 ч до вмешательства. Если эноксапаринвводили более чем за 8 ч до ЧКВ, то рекомендуется до-полнительное введение 0,3 мг/кг внутривенно в видеболюса. Переход с одного антикоагулянта на другой вовремя ЧКВ не рекомендуется.
Нефракционированный гепарин
НФГ — это неоднородная смесь полисахаридов с мо-лекулярной массой от 2 000 до 30 000 Да (в основном15 000-18 000 Да). Одна треть молекул, входящих всостав НФГ, содержит пентасахарид, который связыва-ется с антитромбином и увеличивает скорость ингиби-рования фактора Ха. Для подавления фактора IIa необхо-димо взаимодействие гепарина с тромбином и анти-тромбином с образованием связи между ними. НФГплохо всасывается после подкожного введения, поэто-му его предпочтительно вводить внутривенно. Препа-рат обладает узким терапевтическим окном, в связи счем необходимо частое мониторирование аЧТВ. Целе-вой его уровень составляет 50-75 с (в 1,5-2,5 раза вышеверхней границы нормы). При более высоких значенияхаЧТВ увеличивается риск геморрагических осложнений,а дополнительный антитромботический эффект отсут-ствует. При аЧТВ менее 50 с антитромботическое дей-ствие ограниченно. НФГ рекомендуется назначать в дозе,подобранной по массе тела. Лечение начинают с вве-дения болюса 60-70 ед/кг (максимум 5 000 ед) с после-дующей инфузией по 12-15 ед/кг/ч (максимум1 000 ед/ч). Такая схема чаще всего обеспечивает до-стижение целевых значений аЧТВ [171]. Антикоагулянт-ный эффект НФГ быстро прекращается (в течение не-скольких часов после прекращения введения). В пер-вые 24 ч после прекращения терапии существует рискреактивации процесса свертывания и, соответственно,преходящего повышения риска рецидивирующих ише-мических осложнений, несмотря на одновременную те-рапию аспирином.При мета-анализе 6 исследований было показано,что кратковременное введение НФГ приводит к сниже-нию риска смерти или ИМ на 33% по сравнению с пла-цебо или отсутствием антикоагуляции (ОШ 0,67; 95%ДИ 0,45–0,99; p=0,04) [172]. Благоприятный эф-фект препарата был связан со снижением риска разви-тия ИМ. В клинических исследованиях, в которыхсравнивали комбинированную терапию НФГ+аспирини монотерапию аспирином у пациентов с ОКС безподъема сегмента ST, было отмечено небольшое пре-имущество комбинированной терапии, но ценой уве-личения риска кровотечений. Рецидивы ишемическихосложнений после отмены НФГ объясняют, почему этотэффект не сохранялся в более поздние сроки, если па-циентам не проводили реваскуляризацию до прекра-щения введения НФГ.При ЧКВ стандартный гепарин вводят внутривеннов виде болюса под контролем АВС (250-350 с или200-250 с, если вводился блокатор GP IIb/IIIa рецеп-торов) или в дозе, подобранной пo массе тела (обыч-но 70-100 ед/кг или 50-60 ед/кг в комбинации с бло-каторами GP IIb/IIIa рецепторов) [171]. Учитываязначительную вариабельность биодоступности НФГ, егорекомендуется применять под контролем АВС, особен-но при длительных вмешательствах, когда может потре-боваться введение дополнительной дозы. Продолже-ние гепаринизации после завершения вмешательства(до или после удаления проводника) не рекомендуется.Если пациент поступает в ангиографическую лабо-раторию на фоне продолжающейся инфузии гепари-на, то введение дополнительного болюса НФГ не-обходимо адаптировать с учетом АВС и применения бло-каторов GP IIb/IIIa рецепторов.
Прямые ингибиторы тромбина (бивалирудин)
Хотя разрабатывались несколько прямых ингибито-ров тромбина, только бивалирудин был разрешен к кли-ническому применению при ЧКВ и ОКС. Бивалирудиннепосредственно связывается с тромбином (факторомIIa) и ингибирует индуцированное им превращениефибриногена в фибрин. Бивалирудин инактивируеттромбин, связанный с фибрином, а также находя-щийся в жидкой фазе. Он не связывается с белками плаз-мы, поэтому антикоагулянтное действие препаратаболее предсказуемое. Бивалирудин полностью выво-дится почками. Показатели свертывания (аЧТВ, АВС) тес-но коррелируют с концентрациями в плазме, поэтомуэти два теста можно использовать для мониторирова-ния антикоагулянтной активности бивалирудина.Бивалирудин первоначально изучали при ЧКВ. В ис-следовании REPLACE-2 бивалирудин±блокаторыGP IIb/IIIa рецепторов не уступали НФГ±блокаторыGP IIb/IIIa рецепторов по эффективности в профилак-тике ишемических осложнений при ЧКВ, но значитель-но реже вызывали большие кровотечения (2,4% и4,1%; p<0,001). Достоверной разницы частоты твер-дых конечных точек через 1 мес, 6 мес и 1 год не вы-явили. Бивалирудин в настоящее время разрешен к при-менению при неотложных и плановых ЧКВ в дозе0,75 мг/кг в виде болюса с последующей инфузией по1,75 мг/кг/ч. У пациентов с ОКС без подъема сегмен-та ST бивалирудин рекомендуется вводить в дозе0,1 мг/кг внутривенно в виде болюса, а затем по0,25 мг/кг/ч до ЧКВ.ACUITY было единственным исследованием, в ко-тором бивалирудин специально изучали у пациентовс ОКС без подъема сегмента ST [196]. В это рандоми-зированное открытое исследование были включены13 819 пациентов с ОКС без подъема сегмента ST вы-сокого риска, которым планировалось инвазивноелечение. Пациентов рандомизировали в три группы:стандартная комбинированная терапия НФГ или НМГв сочетании с блокатором GP IIb/IIIa рецепторов (конт-рольная группа) (n=4 603); бивалирудин в комбина-ции с блокатором GP IIb/IIIa рецепторов (n=4 604);только бивалирудин (n=4 612). Лечение бивалируди-ном начинали перед ангиографией с внутривенного введения болюса 0,1 мг/кг с последующей инфузиейпо 0,25 мг/кгч. Перед ЧКВ вводили дополнительно бо-люс 0,5 мг/кг внутривенно, а затем проводили инфу-зию по 1,75 мг/кг/ч. После ЧКВ введение препаратапрекращали. У пациентов, получавших НФН/НМГ в со-четании с блокатором GP IIb/IIIa рецепторов или бива-лирудин в комбинации с блокатором GP IIb/IIIa рецеп-торов, частота комбинированной конечной точки (ише-мические осложнения) через 30 дн (7,3% и 7,7%, со-ответственно; ОР 1,07; 95% ДИ 0,92–1,23; p=0,39) ибольших кровотечений (5,7% и 5,3%; ОР 0,93; 95%ДИ 0,78–1,10; p=0,38) достоверно не отличалась. Би-валирудин не уступал стандартной терапии по эффек-тивности в профилактике ишемических исходов (7,8%и 7,3%; ОР 1,08; 95% ДИ 0,93–1,24; p=0,32), но до-стоверно реже вызывал большие кровотечения (3,0%и 5,7%; ОР 0,53; 95% ДИ 0,43–0,65; p<0,001). Со-ответственно, через 30 дн он имел достоверные пре-имущества перед НФГ/НМГ в сочетании с блокаторомGP IIb/IIIa рецепторов по «чистому» клиническому эф-фекту (10,1% и 11,7%; ОР 0,86; 95% ДИ 0,77–0,94;p=0,02) [196]. Эффективность монотерапии бивали-рудином была сопоставимой в большинстве подгрупп,выделенных в соответствии с протоколом, за исключе-нием пациентов, получавших клопидогрел перед ЧКВ,у которых была отмечена более высокая частота ише-мических исходов в группе бивалирудина (9,1% и7,1%; ОР 1,29; 95% ДИ 1,03–1,63).В целом лечение бивалирудином±блокаторомGP IIb/IIIa рецепторов по эффективности было сопоста-вимым с терапией НФГ/НМГ в сочетании с системати-ческим применением блокаторов GP IIb/IIIa рецепто-ров, но сопровождалось значительным снижениемриска больших кровотечений [197]. Однако в исследо-вании ACUITY не было выявлено достоверной разни-цы исходов в ближайшем и отдаленном периоде присравнении двух стратегий антикоагулянтной терапии[198]. И наконец, полученные данные показали, что пе-реход с НФГ или НМГ на бивалирудин во время ЧКВ неприводит к увеличению риска кровотечений, а факти-чески способствует их предупреждению [199].
Новые антикоагулянты
В настоящее время изучаются эффективность и без-опасность новых антикоагулянтов у пациентов с ОКС. Боль-шинство из них предназначены, скорее, для вторичнойпрофилактики, а не для лечения в острую фазу заболе-вания. Ингибиторы фактора Ха изучались в исследова-ниях II фазы [200,201]. Прямые пероральные ингиби-торы фактора Ха апиксабан (APPRAISE) [202] и риварок-сабан (ATLAS ACS-TIMI) [201] в различных дозах приме-няли в течение 6 мес у пациентов, недавно перенесшихОКС, на фоне лечения аспирином или двойной антитром-боцитарной терапии ацетилсалициловой кислотой и кло-пидогрелом. В обоих исследованиях были выявлены до-зозависимое увеличение частоты кровотечений и тенден-ция к снижению риска ишемических осложнений, осо-бенно у пациентов, получавших один аспирин. На осно-вании полученных данных были начаты исследованияIII фазы (APPRAISE-2 и ATLAS-2). ИсследованиеAPPRAISE-2 было прекращено досрочно в связи с повы-шенным риском кровотечений в группе апиксабана.Прямой ингибитор тромбина дабигатран изучалсяв дозоопределяющем исследовании II фазы (RE-DEEM),результаты которого пока не опубликованы. Отамикса-бан, являющийся прямым ингибитором фактора Ха,предназначенным для внутривенного введения, такжеизучался в исследовании II фазы [203]; исследованиеIII фазы продолжается.
Комбинированная терапия антикоагулянтамии антитромбоцитарными препаратами
Антикоагуляцию и двойную антитромбоцитарнуютерапию аспирином и блокатором P2Y12 рецептороврекомендуется начинать сразу после развития ОКСбез подъема сегмента ST. Антикоагуляцию продолжаюттолько в острую фазу, а двойную антитромбоцитарнуютерапию рекомендуется проводить в течение 12 мес какпосле стентирования, так и без стентирования. У значи-тельной части пациентов (6-8%) с ОКС без подъема сег-мента ST имеются показания к длительной терапии пе-роральными антагонистами витамина К, в том числефибрилляция предсердий со средним или высоким рис-ком тромбоэмболических осложнений, протез клапа-на сердца или ВТЭ. Двойная антитромботическая тера-пия (аспирин или клопидогрел+антагонист витаминаК) или тройная терапия (аспирин, клопидогрел и ан-тагонист витамина К) сопровождается 3-4-кратным уве-личением частоты больших кровотечений. Ведениетаких пациентов представляет трудную задачу. Так, вострую фазу и в последующем необходимо поддержи-вать адекватный уровень антикоагуляции. Перерыв влечении антагонистами витамина К может привести кповышению риска тромбоэмболических осложнений.На фоне полной антикоагуляции антагонистами вита-мина К может быть затруднительным или невозмож-ным выполнение ангиографии, ЧКВ или КШ, а длитель-ная тройная терапия сопровождается высоким рискомкровотечений. В связи с этим необходимо соблюдатьмеры предосторожности, которые рассматриваются внедавно опубликованных рекомендациях по плановымвмешательствам на коронарных артериях и ведению па-циентов в острую фазу (ИМ с подъемом и без подъе-ма сегмента ST) [204]. Стенты, выделяющие лекарства,следует имплантировать только в тех клиническихи/или анатомических ситуациях (распространеннаябляшка, небольшие сосуды, диабет и т.д.), когда ониимеют значительные преимущества перед голометаллическими стентами. Если пациенту, получающемудвойную или тройную терапию, требуется повторная ан-гиография, предпочтительно применение лучевогодоступа с целью снижения риска кровотечений. Реко-мендовалось также проводить ЧКВ на фоне терапии ан-тагонистами витамина К.В острую фазу может быть оправданным прекраще-ние приема антагонистов витамина К и назначение ан-титромбоцитарных препаратов и антикоагулянтов приснижении МНО менее 2,0. Если необходима дли-тельная терапия антагонистами витамина К в сочетаниис клопидогрелом и/или аспирином в низкой дозе, сле-дует тщательно контролировать МНО (целевой диапа-зон 2,0-2,5). Длительность тройной терапии следуетограничивать с учетом клинической ситуации, им-плантации стента, выделяющего или не выделяющеголекарства, и риска ишемических и геморрагическихосложнений, который оценивают на основании индек-сов и/или исходных показателей (табл. 6). Около по-ловины спонтанных кровотечений являются желудоч-но-кишечными, поэтому следует назначать ингибито-ры протонной помпы с целью гастропротекции.
Рекомендации по применению антикоагулянтов
 Реваскуляризация коронарных артерийРеваскуляризация у пациентов с ОКС без подъемасегмента ST приводит к купированию симптомов, со-кращению длительности госпитализации и улучшениюпрогноза. Показания и сроки реваскуляризации мио-карда и выбор метода лечения (ЧКВ или КШ) зависятот многих факторов, включая состояние пациента, на-личие факторов риска и сопутствующих заболеванийи распространенность и тяжесть поражения коронар-ных артерий (по данным ангиографии).Стратификацию риска следует проводить как мож-но раньше, чтобы быстро выделить пациентов высоко-го риска и сократить срок до инвазивного лечения. Од-нако с точки зрения риска и прогноза пациенты с ОКСбез подъема сегмента ST представляют собой неодно-родную группу больных. Среди них могут быть паци-енты группы низкого риска, у которых возможны кон-сервативное лечение и выборочное инвазивное вме-шательство, и больные с высоким риском смерти и сер-дечно-сосудистых исходов, которых следует быстро на-правлять на ангиографию и реваскуляризацию. В свя-зи с этим стратификация риска имеет ключевое значе-ние для выбора оптимальной стратегии ведения. Рискоценивают на основании общепринятых факторовриска и/или с помощью специальных индексов, такихкак GRACE (см. раздел 4.4.) [205].
Инвазивное или консервативное ведение
В многочисленных рандомизированных контроли-руемых исследованиях и мета-анализах сравнивали эф-фективность инвазивного и консервативного или вы-борочного консервативного подходов к лечению ОКСв ближайшие и отдаленные сроки. Оценить пользу ре-васкуляризации в таких исследования трудно. Онаможет быть заниженной, учитывая разницу доли паци-ентов, которые переходят из одной группы в другую(консервативное лечение — инвазивное вмешательство;доля таких пациентов варьируется от 28% до 58%). Вцелом, польза реваскуляризации более выражена в техслучаях, когда разница частоты ее между двумя груп-пами высокая. Кроме того, возможно наличие си-стемной ошибки, связанной с отбором пациентов, таккак в некоторые исследования включали всех пациен тов подряд, в то время как из других исследований ис-ключали пациентов с тяжелыми нарушениями гемоди-намики.При мета-анализе 7 рандомизированных контро-лируемых исследований, в которых сравнивали рутин-ную ангиографию с последующей реваскуляризациейи выборочное инвазивное лечение, было выявлено не-достоверное снижение смертности и достоверноеснижение риска ИМ на фоне инвазивной стратегиилечения [206]. Однако было отмечено значительноеувеличение риска смерти, а также смерти и ИМ во вре-мя первичной госпитализации для инвазивного лече-ния. Тем не менее, 4 из 7 исследований, включенныхв мета-анализ, не соответствовали современной прак-тике, учитывая редкость имплантации стентов и при-менения блокаторов GP IIb/IIIa рецепторов. В другоммета-анализе 7 исследований, в которых вспомогатель-ная терапия была более современной, выявленозначительное снижение риска смерти от любых при-чин и нефатального ИМ в течение 2 лет после ранне-го инвазивного лечения, которое не сопровождалосьповышением риска смерти и нефатального ИМ втечение 1 мес [207]. В последнем мета-анализе 8 ран-домизированных исследований отмечено значитель-ное снижение риска смерти, ИМ или повторной гос-питализации через 1 год у пациентов с ОКС, которымпроводилось инвазивное лечение [208]. Однако бла-гоприятный эффект был достигнут в основном за счетулучшения исходов у пациентов с положительнымибиомаркерами (высокий риск). При этом результатылечения были сопоставимыми у женщин и мужчин сположительными биомаркерами. Важно отметить,что у женщин с отрицательными биомаркерами былавыявлена тенденция к увеличению частоты неблагопри-ятных исходов на фоне ранней инвазивной стратегии.Эти данные свидетельствуют о том, что ее следует из-бегать у женщин группы низкого риска, у которых неопределяется тропонин. По данным мета-анализа ин-дивидуальных результатов лечения пациентов в иссле-дованиях FRISC-2, ICTUS и RITA-3, в которых сравни-вали рутинную и выборочную инвазивную стратегиюлечения, было выявлено снижение смертности и ча-стоты нефатального ИМ в течение 5 лет; разницамежду группами была наиболее выраженной у паци-ентов с высоким риском [209]. Независимыми предик-торами смерти и нефатального ИМ были возраст, са-харный диабет, перенесенный ИМ, депрессия сегмен-та ST, артериальная гипертония, индекс массы тела (≥25или ≥35 кг/м2) и стратегия лечения [209]. В группахнизкого и среднего риска абсолютное снижение часто-ты смерти от сердечно-сосудистых причин и нефаталь-ного ИМ составило 2,0-3,8%, а в группе высокого рис-ка — 11,1%. Полученные данные обосновывают ши-рокое применение инвазивной стратегии, однако ониподчеркивают также роль стратификации риска при вы-боре метода лечения.Подгруппы пациентов высокого риска, у которых об-основанно раннее инвазивное лечение (пациенты с диа-бетом или почечной недостаточностью, пожилые люди)обсуждаются в соответствующих разделах.
Сроки ангиографии и вмешательства
Оптимальные сроки ангиографии и реваскуляриза-ции миокарда у пациентов с ОКС без подъема сегмен-та ST изучались в многочисленных исследованиях.Однако из рандомизированных контролируемых иссле-дований обычно исключали пациентов с очень высо-ким риском, например с рефрактерной стенокардией,тяжелой сердечной недостаточностью, угрожающи-ми жизни желудочковыми аритмиями или гемодина-мическими нарушениями, чтобы не отказывать им влечении, которое потенциально может сохранитьжизнь. У таких пациентов может иметься формирую-щийся ИМ, поэтому им следует проводить немедлен-ное (<2 ч) инвазивное обследование независимо от дан-ных ЭКГ и уровней биомаркеров.Ранее высказывались опасения по поводу того, чторанняя ангиография с последующей реваскуляризаци-ей могут сопровождаться увеличением риска осложне-ний в острую фазу [206]. В 5 проспективных рандоми-зированных исследованиях сравнивали очень ран-нюю (0,5-14 ч) и отсроченную (21-86 ч) стратегии ин-вазивного лечения; среди этих исследований было одноисследование адекватного размера — TIMACS (см. ре-комендации Европейского общества кардиологов по ре-васкуляризации [148]). По данным мета-анализа 3 ис-следований, в том числе ABOARD [210], ELISA [211] иISAR-COOL [170], и исследования TIMACS [212], ран-няя катетеризация с последующим коронарным вмеша-тельством в первый день госпитализации были безопас-ными и привели к снижению риска рецидивирующейишемии миокарда (–41%) и сокращению длительно-сти госпитализации (–28%) [213]. При анализе твер-дых конечных точек только в небольшом исследованииOPTIMA было выявлено увеличение частоты ИМ, свя-занного с вмешательством, у больных, которым ревас-куляризацию проводили немедленно (30 мин), а не вболее поздние сроки (25 ч) [214]. Напротив, исследо-вание ABOARD не подтвердило разницу частоты ИМ,который диагностировали на основании уровня тропо-нина, при немедленном ЧКВ (1,2 ч) или выполнениивмешательства на следующий рабочий день (в среднем21 ч) [210].Учитывая неоднородность профиля риска, оптималь-ные сроки инвазивного лечения могут отличаться в раз-личных когортах. Накапливаются данные о том, что ин-вазивная стратегия дает благоприятный эффект в тече-ние первых 24 ч у пациентов высокого риска. В исследовании TIMACS при раннем инвазивном лечении у па-циентов с высоким риском (индекс GRACE≥140) быловыявлено достоверное снижение частоты смерти, ИМили инсульта через 6 мес по сравнению с отсроченнымвмешательством (≥36 ч). У пациентов с низким илисредним риском (индекс GRACE≤140) достоверной раз-ницы исходов выявлено не было [212]. Важно отметить,что ранняя инвазивная стратегия в этом исследованиине сопровождалась какими-либо проблемами с точкизрения безопасности. В исследовании ACUITY выпол-нение ЧКВ более чем через 24 ч было независимым пре-диктором смертности в течение 30 дн и 1 года [215].Увеличение риска ишемических исходов было наибо-лее очевидным у пациентов со средним и высоким рис-ком (в соответствии с индексом TIMI).При выборе инвазивной стратегии важное значениеимеет оптимальная вспомогательная фармакотера-пия, однако она не должна задерживать ангиографиюи вмешательство [151]. Намеренная задержка инвазив-ного лечения с целью стабилизации пациентов передвмешательством, в том числе с помощью блокаторовGP IIb/IIIa рецепторов (стратегия «охлаждения»), не при-носит пользы [151,170].
Таблица 9. Критерии оценки высокого риска(показания к инвазивному лечению)
Реваскуляризация коронарных артерийРеваскуляризация у пациентов с ОКС без подъемасегмента ST приводит к купированию симптомов, со-кращению длительности госпитализации и улучшениюпрогноза. Показания и сроки реваскуляризации мио-карда и выбор метода лечения (ЧКВ или КШ) зависятот многих факторов, включая состояние пациента, на-личие факторов риска и сопутствующих заболеванийи распространенность и тяжесть поражения коронар-ных артерий (по данным ангиографии).Стратификацию риска следует проводить как мож-но раньше, чтобы быстро выделить пациентов высоко-го риска и сократить срок до инвазивного лечения. Од-нако с точки зрения риска и прогноза пациенты с ОКСбез подъема сегмента ST представляют собой неодно-родную группу больных. Среди них могут быть паци-енты группы низкого риска, у которых возможны кон-сервативное лечение и выборочное инвазивное вме-шательство, и больные с высоким риском смерти и сер-дечно-сосудистых исходов, которых следует быстро на-правлять на ангиографию и реваскуляризацию. В свя-зи с этим стратификация риска имеет ключевое значе-ние для выбора оптимальной стратегии ведения. Рискоценивают на основании общепринятых факторовриска и/или с помощью специальных индексов, такихкак GRACE (см. раздел 4.4.) [205].
Инвазивное или консервативное ведение
В многочисленных рандомизированных контроли-руемых исследованиях и мета-анализах сравнивали эф-фективность инвазивного и консервативного или вы-борочного консервативного подходов к лечению ОКСв ближайшие и отдаленные сроки. Оценить пользу ре-васкуляризации в таких исследования трудно. Онаможет быть заниженной, учитывая разницу доли паци-ентов, которые переходят из одной группы в другую(консервативное лечение — инвазивное вмешательство;доля таких пациентов варьируется от 28% до 58%). Вцелом, польза реваскуляризации более выражена в техслучаях, когда разница частоты ее между двумя груп-пами высокая. Кроме того, возможно наличие си-стемной ошибки, связанной с отбором пациентов, таккак в некоторые исследования включали всех пациен тов подряд, в то время как из других исследований ис-ключали пациентов с тяжелыми нарушениями гемоди-намики.При мета-анализе 7 рандомизированных контро-лируемых исследований, в которых сравнивали рутин-ную ангиографию с последующей реваскуляризациейи выборочное инвазивное лечение, было выявлено не-достоверное снижение смертности и достоверноеснижение риска ИМ на фоне инвазивной стратегиилечения [206]. Однако было отмечено значительноеувеличение риска смерти, а также смерти и ИМ во вре-мя первичной госпитализации для инвазивного лече-ния. Тем не менее, 4 из 7 исследований, включенныхв мета-анализ, не соответствовали современной прак-тике, учитывая редкость имплантации стентов и при-менения блокаторов GP IIb/IIIa рецепторов. В другоммета-анализе 7 исследований, в которых вспомогатель-ная терапия была более современной, выявленозначительное снижение риска смерти от любых при-чин и нефатального ИМ в течение 2 лет после ранне-го инвазивного лечения, которое не сопровождалосьповышением риска смерти и нефатального ИМ втечение 1 мес [207]. В последнем мета-анализе 8 ран-домизированных исследований отмечено значитель-ное снижение риска смерти, ИМ или повторной гос-питализации через 1 год у пациентов с ОКС, которымпроводилось инвазивное лечение [208]. Однако бла-гоприятный эффект был достигнут в основном за счетулучшения исходов у пациентов с положительнымибиомаркерами (высокий риск). При этом результатылечения были сопоставимыми у женщин и мужчин сположительными биомаркерами. Важно отметить,что у женщин с отрицательными биомаркерами былавыявлена тенденция к увеличению частоты неблагопри-ятных исходов на фоне ранней инвазивной стратегии.Эти данные свидетельствуют о том, что ее следует из-бегать у женщин группы низкого риска, у которых неопределяется тропонин. По данным мета-анализа ин-дивидуальных результатов лечения пациентов в иссле-дованиях FRISC-2, ICTUS и RITA-3, в которых сравни-вали рутинную и выборочную инвазивную стратегиюлечения, было выявлено снижение смертности и ча-стоты нефатального ИМ в течение 5 лет; разницамежду группами была наиболее выраженной у паци-ентов с высоким риском [209]. Независимыми предик-торами смерти и нефатального ИМ были возраст, са-харный диабет, перенесенный ИМ, депрессия сегмен-та ST, артериальная гипертония, индекс массы тела (≥25или ≥35 кг/м2) и стратегия лечения [209]. В группахнизкого и среднего риска абсолютное снижение часто-ты смерти от сердечно-сосудистых причин и нефаталь-ного ИМ составило 2,0-3,8%, а в группе высокого рис-ка — 11,1%. Полученные данные обосновывают ши-рокое применение инвазивной стратегии, однако ониподчеркивают также роль стратификации риска при вы-боре метода лечения.Подгруппы пациентов высокого риска, у которых об-основанно раннее инвазивное лечение (пациенты с диа-бетом или почечной недостаточностью, пожилые люди)обсуждаются в соответствующих разделах.
Сроки ангиографии и вмешательства
Оптимальные сроки ангиографии и реваскуляриза-ции миокарда у пациентов с ОКС без подъема сегмен-та ST изучались в многочисленных исследованиях.Однако из рандомизированных контролируемых иссле-дований обычно исключали пациентов с очень высо-ким риском, например с рефрактерной стенокардией,тяжелой сердечной недостаточностью, угрожающи-ми жизни желудочковыми аритмиями или гемодина-мическими нарушениями, чтобы не отказывать им влечении, которое потенциально может сохранитьжизнь. У таких пациентов может иметься формирую-щийся ИМ, поэтому им следует проводить немедлен-ное (<2 ч) инвазивное обследование независимо от дан-ных ЭКГ и уровней биомаркеров.Ранее высказывались опасения по поводу того, чторанняя ангиография с последующей реваскуляризаци-ей могут сопровождаться увеличением риска осложне-ний в острую фазу [206]. В 5 проспективных рандоми-зированных исследованиях сравнивали очень ран-нюю (0,5-14 ч) и отсроченную (21-86 ч) стратегии ин-вазивного лечения; среди этих исследований было одноисследование адекватного размера — TIMACS (см. ре-комендации Европейского общества кардиологов по ре-васкуляризации [148]). По данным мета-анализа 3 ис-следований, в том числе ABOARD [210], ELISA [211] иISAR-COOL [170], и исследования TIMACS [212], ран-няя катетеризация с последующим коронарным вмеша-тельством в первый день госпитализации были безопас-ными и привели к снижению риска рецидивирующейишемии миокарда (–41%) и сокращению длительно-сти госпитализации (–28%) [213]. При анализе твер-дых конечных точек только в небольшом исследованииOPTIMA было выявлено увеличение частоты ИМ, свя-занного с вмешательством, у больных, которым ревас-куляризацию проводили немедленно (30 мин), а не вболее поздние сроки (25 ч) [214]. Напротив, исследо-вание ABOARD не подтвердило разницу частоты ИМ,который диагностировали на основании уровня тропо-нина, при немедленном ЧКВ (1,2 ч) или выполнениивмешательства на следующий рабочий день (в среднем21 ч) [210].Учитывая неоднородность профиля риска, оптималь-ные сроки инвазивного лечения могут отличаться в раз-личных когортах. Накапливаются данные о том, что ин-вазивная стратегия дает благоприятный эффект в тече-ние первых 24 ч у пациентов высокого риска. В исследовании TIMACS при раннем инвазивном лечении у па-циентов с высоким риском (индекс GRACE≥140) быловыявлено достоверное снижение частоты смерти, ИМили инсульта через 6 мес по сравнению с отсроченнымвмешательством (≥36 ч). У пациентов с низким илисредним риском (индекс GRACE≤140) достоверной раз-ницы исходов выявлено не было [212]. Важно отметить,что ранняя инвазивная стратегия в этом исследованиине сопровождалась какими-либо проблемами с точкизрения безопасности. В исследовании ACUITY выпол-нение ЧКВ более чем через 24 ч было независимым пре-диктором смертности в течение 30 дн и 1 года [215].Увеличение риска ишемических исходов было наибо-лее очевидным у пациентов со средним и высоким рис-ком (в соответствии с индексом TIMI).При выборе инвазивной стратегии важное значениеимеет оптимальная вспомогательная фармакотера-пия, однако она не должна задерживать ангиографиюи вмешательство [151]. Намеренная задержка инвазив-ного лечения с целью стабилизации пациентов передвмешательством, в том числе с помощью блокаторовGP IIb/IIIa рецепторов (стратегия «охлаждения»), не при-носит пользы [151,170].
Таблица 9. Критерии оценки высокого риска(показания к инвазивному лечению)
 В целом, сроки ангиографии и реваскуляризации вы-бирают с учетом профиля риска пациентов. Пациентамс очень высоким риском (см. выше) показана не-отложная коронарная ангиография (<2 ч). У пациен-тов с высоким риском (индекс GRACE>140 и наличиепо крайней мере одного фактора высокого риска) об-основанна ранняя инвазивная стратегия в течениепервых 24 ч. Эта стратегия предполагает перевод па-циентов в лечебные учреждения, в которых может бытьвыполнена катетеризация. У пациентов с более низкимриском, у которых индекс GRACE составляет ≤140, од-нако, имеется по крайней мере один критерий высо-кого риска (табл. 9), инвазивное обследование можетбыть отложено, однако его следует провести во времягоспитализации, предпочтительно в течение 72 ч послепоступления. В таких случаях немедленный перевод па-циента не требуется, однако его следует организоватьв течение 72 ч (например, у пациентов с диабетом). Па-циентам с низким риском, у которых отсутствуют симп-томы ишемии, необходимо провести неинвазивнуюстресс-пробу перед выпиской. Если определяется об-ратимая ишемия миокарда, показана коронарная ан-гиография.
Чрескожное коронарное вмешательство
или коронарное шунтированиеВ рандомизированных контролируемых исследова-ниях ЧКВ и КШ у пациентов с ОКС без подъема сегмен-та ST специально не сравнивали. Во всех исследованиях,в которых сравнивали раннее или позднее лечение, атакже инвазивное или консервативное ведение, реше-ние о выборе вмешательства (КШ или ЧКВ) принима-ли исследователи.У стабильных пациентов, перенесших ОКС, метод ре-васкуляризации выбирают так же, как при стабильнойИБС [148]. Примерно у трети пациентов при ангиогра-фии выявляют стеноз одной коронарной артерии, чтопозволяет в большинстве случаев выполнить ЧКВ. У по-ловины пациентов наблюдается поражение несколькихкоронарных артерий [181,182]. В таких случаях выбратьтип вмешательства сложнее (ЧКВ на артерии, пораже-ние которой было причиной ОКС, ЧКВ на несколькихсосудах, КШ или комбинированная (гибридная) ревас-куляризация). Стратегию реваскуляризации выбираютс учетом клинического состояния, тяжести и распростра-ненности коронарного атеросклероза и особенностейатеросклеротической бляшки.У большинства пациентов с поражением несколькихартерий обычно начинают с ЧКВ на артерии, пораже-ние которой было причиной развития ОКС. Этот под-ход не сравнивали со стентированием нескольких со-судов в рандомизированных исследованиях. Однако прианализе крупной базы данных, включающей в себя105 866 пациентов с ОКС без подъема сегмента ST, у ко-торых имелось поражение нескольких коронарных ар-терий, были сопоставлены результаты ЧКВ на несколь-ких и одном сосуде [216]. Вмешательство на несколькихартериях реже было успешным, однако госпитальная ле-тальность и частота осложнений были сопоставимыми,хотя результаты длительного наблюдения отсутствуют.КШ сравнивали с ЧКВ у пациентов с поражениемнескольких коронарных артерий, которые быливключены в исследование ACUITY [217]. У пациентов,которым проводили ЧКВ, была ниже частота инсуль-та, ИМ, кровотечений и повреждения почек. Смерт-ность через 1 мес и 1 год была сходной в двух груп-пах, однако через 1 мес и 1 год после ЧКВ выявили значительное увеличение частоты внеплановой ревас-куляризации. Однако только 43% пациентов, перенес-ших КШ, были сопоставимы с пациентами группы ЧКВ.Кроме того, через 1 год выявили тенденцию к увеличе-нию риска основных сердечно-сосудистых событийпосле ЧКВ по сравнению с КШ (25,0% и 19,5%;р=0,05). Полученные данные согласуются с резуль-татами исследования SYNTAX, в котором 28,5% па-циентов перенесли ОКС [218]. Однако субанализэтих пациентов не проводился.В каждом лечебном учреждении необходимо иметьпротокол ведения пациентов, разработанный на осно-вании индекса SYNTAX. При этом следует выделить ана-томические и клинические критерии, позволяющиеопределить возможность выполнения ЧКВ после ангио-графии или целесообразность направления пациентана КШ [219]. После стентирования основного поражен-ного сосуда у пациентов с индексами SYNTAX, находя-щимися в двух верхних терцилях, следует оценить функ-циональное значение поражения других сосудов сучетом сопутствующих заболеваний и индивидуальныхособенностей пациента.
Коронарное шунтирование
Доля пациентов с ОКС без подъема сегмента ST, ко-торым проводится КШ во время первичной госпитали-зации, составляет около 10% [220]. Польза ЧКВ у та-ких пациентов отражает ранние сроки вмешательства,в то время как КШ дает наиболее выраженный эффект,если пациентов оперируют через несколько дней послестабилизации их состояния в зависимости от индиви-дуального риска. Результаты раннего и отсроченного КШв рандомизированном исследовании не сравнивали,поэтому после ЧКВ на основном пораженном сосуде упациентов с тяжелым коронарным атеросклерозомрекомендуется выждать 48-72 ч. По данным анализабольшого числа пациентов, госпитализированных с ОКС,раннее КШ, даже у пациентов с более высоким риском,сопровождалось очень низкой госпитальной смерт-ностью [221]. В регистрах CRUSADE и ACTION не быловыявлено достоверной разницы исходов у пациентов,которым КШ в проводили в течение ≤48 ч или >48 ч,хотя операцию чаще откладывали у пациентов с болеевысоким риском [222]. У пациентов, которым плани-руется КШ, сроки операции следует выбирать индиви-дуально с учетом симптомов, состояния гемодинами-ки, анатомии коронарных артерий, наличия ишемии ирезерва кровотока. Если сохраняется или рецидивиру-ет ишемия, имеются желудочковые аритмии или неста-бильность гемодинамики, КШ следует выполнить не-медленно. У пациентов со стенозом ствола левой коро-нарной артерии или стенозом трех коронарных арте-рий, включая проксимальную часть левой передней нис-ходящей артерии, операцию необходимо провестиво время первичной госпитализации. При принятии ре-шения следует учитывать риск геморрагических ослож-нений у пациентов, которым КШ проводят на фонеагрессивной антитромбоцитарной терапии[142,223,224]. Однако применение двух или трехантитромбоцитарных препаратов рассматривают толь-ко как относительное противопоказание к раннемуКШ, хотя в таких случаях во время операции следуетпринять меры, чтобы свести к минимуму риск крово-течения. Если неотложную операцию проводят до за-вершения отмывочного периода тиенопиридинов, тодля профилактики кровотечений рекомендуется выпол-нять КШ в режиме off-pump или свести к минимуму ис-кусственное кровообращение, а также использоватьтрансфузию тромбоцитарной массы.
5.4.5. Техника чрескожного коронарного вмешательстваРезультаты ЧКВ у пациентов с ОКС без стойкогоподъема сегмента ST значительно улучшились на фонестентирования коронарных артерий и применения со-временных антитромботических и антитромбоцитар-ных препаратов. Имплантация стента во время ЧКВ поз-воляет уменьшить угрозу внезапной окклюзии и ресте-ноза. Безопасность и эффективность стентов, выделяю-щих лекарства, в проспективных исследованиях в этойпопуляции пациентов специально не изучались, хотя вбольшинстве исследований, в которых изучались ре-зультаты ЧКВ, доля пациентов, недавно перенесших ОКСбез подъема сегмента ST, достигала 50%. Учитывая ак-тивацию тромбоцитов и воспалительные изменения упациентов с ОКС, результаты имплантации стентов, вы-деляющих лекарства, могут отличаться от таковых у ста-бильных пациентов. Однако в рандомизированном ис-следовании HORIZONS AMI, в котором сравнивалистенты, выделяющие лекарства, и голометаллическиестенты у пациентов с ИМ с подъемом сегмента ST, небыло выявлено каких-либо проблем с точки зрения без-опасности, в то время как после имплантации стентовс лекарственным покрытием было отмечено снижениечастоты рестеноза и внеплановых повторных реваску-ляризаций [225]. В связи с отсутствием рандомизиро-ванных исследований у больных с ОКС без подъема сег-мента ST выбирать тип стента следует на основании ин-дивидуальной оценки возможных пользы и риска[226]. Двойную антитромбоцитарную терапию следу-ет продолжать в течение 12 мес независимо от типа стен-та. При наличии обязательных показаний к длительнойантикоагуляции возможны имплантация голометалли-ческого стента, только баллонная ангиопластика или КШ,чтобы сократить длительность тройной терапии до 1 мес.При ИМ без подъема сегмента ST возможна аспира-ционная тромбоэктомия, однако ее пользу не изучалив проспективных рандомизированных исследованияху пациентов с ОКС без подъема сегмента ST [227]. Остается неясным, следует ли проводить вмешательства надругих умеренно суженных сегментах коронарных ар-терий при наличии уязвимых бляшек.
Рекомендации по инвазивному обследованию и реваскуляризации
В целом, сроки ангиографии и реваскуляризации вы-бирают с учетом профиля риска пациентов. Пациентамс очень высоким риском (см. выше) показана не-отложная коронарная ангиография (<2 ч). У пациен-тов с высоким риском (индекс GRACE>140 и наличиепо крайней мере одного фактора высокого риска) об-основанна ранняя инвазивная стратегия в течениепервых 24 ч. Эта стратегия предполагает перевод па-циентов в лечебные учреждения, в которых может бытьвыполнена катетеризация. У пациентов с более низкимриском, у которых индекс GRACE составляет ≤140, од-нако, имеется по крайней мере один критерий высо-кого риска (табл. 9), инвазивное обследование можетбыть отложено, однако его следует провести во времягоспитализации, предпочтительно в течение 72 ч послепоступления. В таких случаях немедленный перевод па-циента не требуется, однако его следует организоватьв течение 72 ч (например, у пациентов с диабетом). Па-циентам с низким риском, у которых отсутствуют симп-томы ишемии, необходимо провести неинвазивнуюстресс-пробу перед выпиской. Если определяется об-ратимая ишемия миокарда, показана коронарная ан-гиография.
Чрескожное коронарное вмешательство
или коронарное шунтированиеВ рандомизированных контролируемых исследова-ниях ЧКВ и КШ у пациентов с ОКС без подъема сегмен-та ST специально не сравнивали. Во всех исследованиях,в которых сравнивали раннее или позднее лечение, атакже инвазивное или консервативное ведение, реше-ние о выборе вмешательства (КШ или ЧКВ) принима-ли исследователи.У стабильных пациентов, перенесших ОКС, метод ре-васкуляризации выбирают так же, как при стабильнойИБС [148]. Примерно у трети пациентов при ангиогра-фии выявляют стеноз одной коронарной артерии, чтопозволяет в большинстве случаев выполнить ЧКВ. У по-ловины пациентов наблюдается поражение несколькихкоронарных артерий [181,182]. В таких случаях выбратьтип вмешательства сложнее (ЧКВ на артерии, пораже-ние которой было причиной ОКС, ЧКВ на несколькихсосудах, КШ или комбинированная (гибридная) ревас-куляризация). Стратегию реваскуляризации выбираютс учетом клинического состояния, тяжести и распростра-ненности коронарного атеросклероза и особенностейатеросклеротической бляшки.У большинства пациентов с поражением несколькихартерий обычно начинают с ЧКВ на артерии, пораже-ние которой было причиной развития ОКС. Этот под-ход не сравнивали со стентированием нескольких со-судов в рандомизированных исследованиях. Однако прианализе крупной базы данных, включающей в себя105 866 пациентов с ОКС без подъема сегмента ST, у ко-торых имелось поражение нескольких коронарных ар-терий, были сопоставлены результаты ЧКВ на несколь-ких и одном сосуде [216]. Вмешательство на несколькихартериях реже было успешным, однако госпитальная ле-тальность и частота осложнений были сопоставимыми,хотя результаты длительного наблюдения отсутствуют.КШ сравнивали с ЧКВ у пациентов с поражениемнескольких коронарных артерий, которые быливключены в исследование ACUITY [217]. У пациентов,которым проводили ЧКВ, была ниже частота инсуль-та, ИМ, кровотечений и повреждения почек. Смерт-ность через 1 мес и 1 год была сходной в двух груп-пах, однако через 1 мес и 1 год после ЧКВ выявили значительное увеличение частоты внеплановой ревас-куляризации. Однако только 43% пациентов, перенес-ших КШ, были сопоставимы с пациентами группы ЧКВ.Кроме того, через 1 год выявили тенденцию к увеличе-нию риска основных сердечно-сосудистых событийпосле ЧКВ по сравнению с КШ (25,0% и 19,5%;р=0,05). Полученные данные согласуются с резуль-татами исследования SYNTAX, в котором 28,5% па-циентов перенесли ОКС [218]. Однако субанализэтих пациентов не проводился.В каждом лечебном учреждении необходимо иметьпротокол ведения пациентов, разработанный на осно-вании индекса SYNTAX. При этом следует выделить ана-томические и клинические критерии, позволяющиеопределить возможность выполнения ЧКВ после ангио-графии или целесообразность направления пациентана КШ [219]. После стентирования основного поражен-ного сосуда у пациентов с индексами SYNTAX, находя-щимися в двух верхних терцилях, следует оценить функ-циональное значение поражения других сосудов сучетом сопутствующих заболеваний и индивидуальныхособенностей пациента.
Коронарное шунтирование
Доля пациентов с ОКС без подъема сегмента ST, ко-торым проводится КШ во время первичной госпитали-зации, составляет около 10% [220]. Польза ЧКВ у та-ких пациентов отражает ранние сроки вмешательства,в то время как КШ дает наиболее выраженный эффект,если пациентов оперируют через несколько дней послестабилизации их состояния в зависимости от индиви-дуального риска. Результаты раннего и отсроченного КШв рандомизированном исследовании не сравнивали,поэтому после ЧКВ на основном пораженном сосуде упациентов с тяжелым коронарным атеросклерозомрекомендуется выждать 48-72 ч. По данным анализабольшого числа пациентов, госпитализированных с ОКС,раннее КШ, даже у пациентов с более высоким риском,сопровождалось очень низкой госпитальной смерт-ностью [221]. В регистрах CRUSADE и ACTION не быловыявлено достоверной разницы исходов у пациентов,которым КШ в проводили в течение ≤48 ч или >48 ч,хотя операцию чаще откладывали у пациентов с болеевысоким риском [222]. У пациентов, которым плани-руется КШ, сроки операции следует выбирать индиви-дуально с учетом симптомов, состояния гемодинами-ки, анатомии коронарных артерий, наличия ишемии ирезерва кровотока. Если сохраняется или рецидивиру-ет ишемия, имеются желудочковые аритмии или неста-бильность гемодинамики, КШ следует выполнить не-медленно. У пациентов со стенозом ствола левой коро-нарной артерии или стенозом трех коронарных арте-рий, включая проксимальную часть левой передней нис-ходящей артерии, операцию необходимо провестиво время первичной госпитализации. При принятии ре-шения следует учитывать риск геморрагических ослож-нений у пациентов, которым КШ проводят на фонеагрессивной антитромбоцитарной терапии[142,223,224]. Однако применение двух или трехантитромбоцитарных препаратов рассматривают толь-ко как относительное противопоказание к раннемуКШ, хотя в таких случаях во время операции следуетпринять меры, чтобы свести к минимуму риск крово-течения. Если неотложную операцию проводят до за-вершения отмывочного периода тиенопиридинов, тодля профилактики кровотечений рекомендуется выпол-нять КШ в режиме off-pump или свести к минимуму ис-кусственное кровообращение, а также использоватьтрансфузию тромбоцитарной массы.
5.4.5. Техника чрескожного коронарного вмешательстваРезультаты ЧКВ у пациентов с ОКС без стойкогоподъема сегмента ST значительно улучшились на фонестентирования коронарных артерий и применения со-временных антитромботических и антитромбоцитар-ных препаратов. Имплантация стента во время ЧКВ поз-воляет уменьшить угрозу внезапной окклюзии и ресте-ноза. Безопасность и эффективность стентов, выделяю-щих лекарства, в проспективных исследованиях в этойпопуляции пациентов специально не изучались, хотя вбольшинстве исследований, в которых изучались ре-зультаты ЧКВ, доля пациентов, недавно перенесших ОКСбез подъема сегмента ST, достигала 50%. Учитывая ак-тивацию тромбоцитов и воспалительные изменения упациентов с ОКС, результаты имплантации стентов, вы-деляющих лекарства, могут отличаться от таковых у ста-бильных пациентов. Однако в рандомизированном ис-следовании HORIZONS AMI, в котором сравнивалистенты, выделяющие лекарства, и голометаллическиестенты у пациентов с ИМ с подъемом сегмента ST, небыло выявлено каких-либо проблем с точки зрения без-опасности, в то время как после имплантации стентовс лекарственным покрытием было отмечено снижениечастоты рестеноза и внеплановых повторных реваску-ляризаций [225]. В связи с отсутствием рандомизиро-ванных исследований у больных с ОКС без подъема сег-мента ST выбирать тип стента следует на основании ин-дивидуальной оценки возможных пользы и риска[226]. Двойную антитромбоцитарную терапию следу-ет продолжать в течение 12 мес независимо от типа стен-та. При наличии обязательных показаний к длительнойантикоагуляции возможны имплантация голометалли-ческого стента, только баллонная ангиопластика или КШ,чтобы сократить длительность тройной терапии до 1 мес.При ИМ без подъема сегмента ST возможна аспира-ционная тромбоэктомия, однако ее пользу не изучалив проспективных рандомизированных исследованияху пациентов с ОКС без подъема сегмента ST [227]. Остается неясным, следует ли проводить вмешательства надругих умеренно суженных сегментах коронарных ар-терий при наличии уязвимых бляшек.
Рекомендации по инвазивному обследованию и реваскуляризации
 Особые группы и состояния
Пожилые люди
Термином «пожилые» обозначают людей различно-го возраста. Традиционно к этой группе относят людейв возрасте старше 65 лет, хотя на фоне постарения на-селения более правильным было бы считать пожилы-ми людей в возрасте старше 75 или даже 80 лет. Поми-мо хронологического возраста следует учитывать состоя-ние пациента, когнитивные и функциональные расстрой-ства и наличие физической зависимости. В Европейскихрегистрах 27-34% пациентов с ОКС без подъема сег-мента ST были в возрасте старше 75 лет [228,229]. Темне менее, в последних клинических исследованиях доляпожилых людей (старше 75 лет) среди больных с ОКСбез подъема сегмента ST не превышала 20%. Даже еслипожилых людей включали в клинические исследова-ния, то у рандомизированных пациентов сопутствую-щие заболевания встречались реже, чем в обычной кли-нической практике [230]. В связи с этим возможностьэкстраполяции результатов клинических исследованийна всю выборку пожилых людей вызывает сомнения.Диагноз и стратификация риска у пожилых людейУ пожилых людей клинические проявления ОКС безподъема сегмента ST часто атипичные и нередко лег-ко выражены [15]. У пожилых людей с атипичнойклинической картиной ОКС без подъема сегмента ST ве-дущим симптомом является одышка, в то время как об-мороки, недомогание и дезориентация встречаютсяреже. На ЭКГ реже отмечают выраженные отклонениясегмента ST. У пожилых людей ОКС без подъема сегмен-та ST развивается чаще, чем ИМ с подъемом сегментаST. Одним из основных предикторов риска у пациентовс ОКС без подъема сегмента ST является возраст [50].У пациентов в возрасте старше 75 лет риск смерти покрайней мере в 2 раза выше, чем у пациентов в возрас-те до 75 лет. Частота осложнений ОКС, в том числе сер-дечной недостаточности, кровотечения, инсульта, по-чечной недостаточности и инфекций, значительно уве-личивается с возрастом.Терапевтические аспектыУ пожилых людей выше риск побочных эффектов ме-дикаментозной терапии. В частности это касается рис-ка кровотечений при лечении антитромбоцитарнымипрепаратами и антикоагулянтами, а также гипотонии,брадикардии и почечной недостаточности. Помимо бо-лее высокого риска кровотечений, характерного для по-жилых людей, у таких пациентов часто оказываютсячрезмерными дозы антитромботических препаратов,которые выводятся почками [231].У пожилых людей значительно увеличивается рискбольших кровотечений при лечении нефракциониро-ванным гепарином, эноксапарином, блокаторамиGP IIb/IIIa и P2Y12 рецепторов. В исследованииSYNERGY у пациентов в возрасте старше 75 лет не быловыявлено разницы частоты смерти или ИМ в течение30 дн, смертности в течение 30 дн и 1 года между груп-пами НФГ и эноксапарина. Однако частота больших кро-вотечений в соответствии с критериями TIMI и тяжелых кровотечений в соответствии с критериями GUSTOбыла значительно выше в группе эноксапарина. В свя-зи с этим следует осторожно применять эноксапарин упожилых людей и подбирать дозу с учетом функции по-чек. У пациентов в возрасте старше 75 лет целесообраз-но снизить дозу до 1 мг/кг один раз в день и монито-рировать анти-Ха активность [232]. В исследованииOASIS-5 риск кровотечений у пациентов в возрасте стар-ше 65 лет при лечении фондапаринуксом был значи-тельно ниже, чем при применении эноксапарина [175].У пожилых людей значительно ниже вероятность ин-вазивного лечения ОКС без подъема сегмента ST. Од-нако результаты отдельных исследований свидетель-ствуют о том, что польза инвазивной стратегии в основ-ном отмечается у пациентов в возрасте старше 65 лет[233,234]. По данным субанализа исследованияTACTICS-TIMI 18, у пациентов в возрасте старше 75 летс ОКС без подъема сегмента ST было отмечено наибо-лее значительное снижение относительного и абсолют-ного риска неблагоприятных исходов ценой увеличе-ния риска больших кровотечений и потребности втрансфузиях [235]. Это было недавно подтверждено примета-анализе [209].Тактику ведения пожилого пациента следует выби-рать индивидуально с учетом риска ишемическихосложнений и кровотечений, расчетной ожидаемой про-должительности жизни, сопутствующих заболеваний,качества жизни, желания пациента и расчетного рис-ка и пользы реваскуляризации.
Пол
Женщины с ОКС без подъема сегмента ST старшемужчин и чаще страдают сахарным диабетом, артери-альной гипертонией, сердечной недостаточностью и дру-гими сопутствующими заболеваниями [236-238]. У нихчаще отмечают атипичные проявления, включая одыш-ку и сердечную недостаточность [228,239]. Несмотряна разницу исходного риска, у женщин и мужчин с ОКСбез подъема сегмента ST прогноз сопоставимый, хотяв пожилом возрасте у женщин прогноз лучше, чем умужчин. Это может объясняться более высокой часто-той необструктивного коронарного атеросклероза, ко-торый обнаруживают при ангиографии у женщин[238]. С другой стороны, у женщин с ОКС без подъемасегмента ST риск кровотечений выше, чем у мужчин.Терапевтические аспектыХотя эффективность большинства лекарственныхсредств не зависела от пола, женщинам с ОКС безподъема сегмента по сравнению с мужчинами реже про-водят адекватное лечение, включая инвазивные диаг-ностические вмешательства и реваскуляризацию коро-нарных артерий [236,237,240]. Результаты изучениявлияния пола на эффективность инвазивной стратегиилечения ОКС без подъема сегмента ST оказались про-тиворечивыми. Хотя наблюдательные исследованиясвидетельствуют об улучшении отдаленного прогноза нафоне раннего инвазивного лечения у женщин, примета-анализе было показано, что инвазивные стратегиидают положительный эффект только у мужчин, в то вре-мя как у женщин какой-либо пользы в течение 1 года вы-явлено не было [241]. Более того, в ряде рандомизиро-ванных исследований [233,242] было выявлено увеличе-ние частоты смерти и нефатального ИМ у женщин с ОКСбез подъема сегмента ST, которым проводили раннее ин-вазивное лечение. В исследовании FRISC-2 в течение5 лет было выявлено достоверное взаимодействиемежду результатами лечения и полом. Инвазивнаястратегия привела к значительному снижению смертно-сти и частоты ИМ у мужчин, но не у женщин [234].При мета-анализе, выполненном экспертами CochraneCollaboration, было выявлено значительное снижениериска смерти или ИМ на фоне инвазивной стратегиилечения у женщин (ОР 0,73; 95% ДИ 0,59–0,91), хотяоно сопровождалось увеличением риска неблагопри-ятных исходов на раннем этапе [243]. Некоторые иссле-дования свидетельствуют о том, что ранняя инвазивнаястратегия оправданна только у женщин с высоким рис-ком, например с повышенным уровнем тропонина[244] или поражением нескольких коронарных артерий.Сходные данные были получены при изучении блока-торов GP IIb/IIIa у женщин [245]. В когорте из 35 128 па-циентов, которым проводили ангиографию в 11 иссле-дованиях, 30-дневная смертность с поправкой на тяжестьангиографических изменений достоверно не отличаласьот таковой у мужчин независимо от типа ОКС. Различия 30-дневной смертности, связанные с полом, у пациен-тов с ОКС значительно уменьшались после внесения по-правки на исходные показатели, ангиографическиеданные и стратегию лечения [246].Таким образом, имеющиеся данные свидетель-ствуют о том, что раннюю инвазивную стратегию сле-дует обсуждать у женщин на основании тех же принци-пов, что и у мужчин, т.е. тщательно взвешивая риск ише-мических исходов и кровотечений, включая клиниче-ское состояние и ЭКГ, уровни биомаркеров, сопутствую-щие заболевания и индексы риска.
Рекомендации по лечению пожилых людей
Особые группы и состояния
Пожилые люди
Термином «пожилые» обозначают людей различно-го возраста. Традиционно к этой группе относят людейв возрасте старше 65 лет, хотя на фоне постарения на-селения более правильным было бы считать пожилы-ми людей в возрасте старше 75 или даже 80 лет. Поми-мо хронологического возраста следует учитывать состоя-ние пациента, когнитивные и функциональные расстрой-ства и наличие физической зависимости. В Европейскихрегистрах 27-34% пациентов с ОКС без подъема сег-мента ST были в возрасте старше 75 лет [228,229]. Темне менее, в последних клинических исследованиях доляпожилых людей (старше 75 лет) среди больных с ОКСбез подъема сегмента ST не превышала 20%. Даже еслипожилых людей включали в клинические исследова-ния, то у рандомизированных пациентов сопутствую-щие заболевания встречались реже, чем в обычной кли-нической практике [230]. В связи с этим возможностьэкстраполяции результатов клинических исследованийна всю выборку пожилых людей вызывает сомнения.Диагноз и стратификация риска у пожилых людейУ пожилых людей клинические проявления ОКС безподъема сегмента ST часто атипичные и нередко лег-ко выражены [15]. У пожилых людей с атипичнойклинической картиной ОКС без подъема сегмента ST ве-дущим симптомом является одышка, в то время как об-мороки, недомогание и дезориентация встречаютсяреже. На ЭКГ реже отмечают выраженные отклонениясегмента ST. У пожилых людей ОКС без подъема сегмен-та ST развивается чаще, чем ИМ с подъемом сегментаST. Одним из основных предикторов риска у пациентовс ОКС без подъема сегмента ST является возраст [50].У пациентов в возрасте старше 75 лет риск смерти покрайней мере в 2 раза выше, чем у пациентов в возрас-те до 75 лет. Частота осложнений ОКС, в том числе сер-дечной недостаточности, кровотечения, инсульта, по-чечной недостаточности и инфекций, значительно уве-личивается с возрастом.Терапевтические аспектыУ пожилых людей выше риск побочных эффектов ме-дикаментозной терапии. В частности это касается рис-ка кровотечений при лечении антитромбоцитарнымипрепаратами и антикоагулянтами, а также гипотонии,брадикардии и почечной недостаточности. Помимо бо-лее высокого риска кровотечений, характерного для по-жилых людей, у таких пациентов часто оказываютсячрезмерными дозы антитромботических препаратов,которые выводятся почками [231].У пожилых людей значительно увеличивается рискбольших кровотечений при лечении нефракциониро-ванным гепарином, эноксапарином, блокаторамиGP IIb/IIIa и P2Y12 рецепторов. В исследованииSYNERGY у пациентов в возрасте старше 75 лет не быловыявлено разницы частоты смерти или ИМ в течение30 дн, смертности в течение 30 дн и 1 года между груп-пами НФГ и эноксапарина. Однако частота больших кро-вотечений в соответствии с критериями TIMI и тяжелых кровотечений в соответствии с критериями GUSTOбыла значительно выше в группе эноксапарина. В свя-зи с этим следует осторожно применять эноксапарин упожилых людей и подбирать дозу с учетом функции по-чек. У пациентов в возрасте старше 75 лет целесообраз-но снизить дозу до 1 мг/кг один раз в день и монито-рировать анти-Ха активность [232]. В исследованииOASIS-5 риск кровотечений у пациентов в возрасте стар-ше 65 лет при лечении фондапаринуксом был значи-тельно ниже, чем при применении эноксапарина [175].У пожилых людей значительно ниже вероятность ин-вазивного лечения ОКС без подъема сегмента ST. Од-нако результаты отдельных исследований свидетель-ствуют о том, что польза инвазивной стратегии в основ-ном отмечается у пациентов в возрасте старше 65 лет[233,234]. По данным субанализа исследованияTACTICS-TIMI 18, у пациентов в возрасте старше 75 летс ОКС без подъема сегмента ST было отмечено наибо-лее значительное снижение относительного и абсолют-ного риска неблагоприятных исходов ценой увеличе-ния риска больших кровотечений и потребности втрансфузиях [235]. Это было недавно подтверждено примета-анализе [209].Тактику ведения пожилого пациента следует выби-рать индивидуально с учетом риска ишемическихосложнений и кровотечений, расчетной ожидаемой про-должительности жизни, сопутствующих заболеваний,качества жизни, желания пациента и расчетного рис-ка и пользы реваскуляризации.
Пол
Женщины с ОКС без подъема сегмента ST старшемужчин и чаще страдают сахарным диабетом, артери-альной гипертонией, сердечной недостаточностью и дру-гими сопутствующими заболеваниями [236-238]. У нихчаще отмечают атипичные проявления, включая одыш-ку и сердечную недостаточность [228,239]. Несмотряна разницу исходного риска, у женщин и мужчин с ОКСбез подъема сегмента ST прогноз сопоставимый, хотяв пожилом возрасте у женщин прогноз лучше, чем умужчин. Это может объясняться более высокой часто-той необструктивного коронарного атеросклероза, ко-торый обнаруживают при ангиографии у женщин[238]. С другой стороны, у женщин с ОКС без подъемасегмента ST риск кровотечений выше, чем у мужчин.Терапевтические аспектыХотя эффективность большинства лекарственныхсредств не зависела от пола, женщинам с ОКС безподъема сегмента по сравнению с мужчинами реже про-водят адекватное лечение, включая инвазивные диаг-ностические вмешательства и реваскуляризацию коро-нарных артерий [236,237,240]. Результаты изучениявлияния пола на эффективность инвазивной стратегиилечения ОКС без подъема сегмента ST оказались про-тиворечивыми. Хотя наблюдательные исследованиясвидетельствуют об улучшении отдаленного прогноза нафоне раннего инвазивного лечения у женщин, примета-анализе было показано, что инвазивные стратегиидают положительный эффект только у мужчин, в то вре-мя как у женщин какой-либо пользы в течение 1 года вы-явлено не было [241]. Более того, в ряде рандомизиро-ванных исследований [233,242] было выявлено увеличе-ние частоты смерти и нефатального ИМ у женщин с ОКСбез подъема сегмента ST, которым проводили раннее ин-вазивное лечение. В исследовании FRISC-2 в течение5 лет было выявлено достоверное взаимодействиемежду результатами лечения и полом. Инвазивнаястратегия привела к значительному снижению смертно-сти и частоты ИМ у мужчин, но не у женщин [234].При мета-анализе, выполненном экспертами CochraneCollaboration, было выявлено значительное снижениериска смерти или ИМ на фоне инвазивной стратегиилечения у женщин (ОР 0,73; 95% ДИ 0,59–0,91), хотяоно сопровождалось увеличением риска неблагопри-ятных исходов на раннем этапе [243]. Некоторые иссле-дования свидетельствуют о том, что ранняя инвазивнаястратегия оправданна только у женщин с высоким рис-ком, например с повышенным уровнем тропонина[244] или поражением нескольких коронарных артерий.Сходные данные были получены при изучении блока-торов GP IIb/IIIa у женщин [245]. В когорте из 35 128 па-циентов, которым проводили ангиографию в 11 иссле-дованиях, 30-дневная смертность с поправкой на тяжестьангиографических изменений достоверно не отличаласьот таковой у мужчин независимо от типа ОКС. Различия 30-дневной смертности, связанные с полом, у пациен-тов с ОКС значительно уменьшались после внесения по-правки на исходные показатели, ангиографическиеданные и стратегию лечения [246].Таким образом, имеющиеся данные свидетель-ствуют о том, что раннюю инвазивную стратегию сле-дует обсуждать у женщин на основании тех же принци-пов, что и у мужчин, т.е. тщательно взвешивая риск ише-мических исходов и кровотечений, включая клиниче-ское состояние и ЭКГ, уровни биомаркеров, сопутствую-щие заболевания и индексы риска.
Рекомендации по лечению пожилых людей
 Рекомендации по лечению пациентов различного пола
Рекомендации по лечению пациентов различного пола
 5.5.3. Сахарный диабетПримерно 20-30% больных с ОКС без подъема сег-мента ST страдают сахарным диабетом. По крайней мере,у такого же процента пациентов имеются недиагности-рованный диабет или нарушение толерантности к глю-козе [247]. В исследовании Euro Heart Survey установ-ленный или вновь выявленный сахарный диабет имел-ся у 37% пациентов с ОКС без подъема сегмента ST [248].Пациенты с сахарным диабетом в целом старше, чащеявляются женщинами и чаще страдают сопутствующи-ми заболеваниями, такими как гипертония и почечнаянедостаточность. У них выше вероятность появления ати-пичных симптомов и развития осложнений, особенносердечной недостаточности и кровотечений [248].Сахарный диабет — это независимый предикторсмерти больных с ОКС без подъема сегмента ST. Рисксмерти у больных диабетом повышен в 2 раза [249,250].Кроме того, у пациентов с нарушением толерантностик глюкозе или нарушенной гликемией натощак прогнозхуже, чем у пациентов с нормальным метаболизмомглюкозы, однако лучше, чем у больных подтвержден-ным диабетом.Гипергликемия при поступлении или во время гос-питализации — это независимый неблагоприятныйпрогностический фактор при ОКС независимо от нали-чия сахарного диабета. Она может иметь даже большеенеблагоприятное прогностическое значение, чем уста-новленный диагноз диабета [251].Терапевтические аспектыРегистры показали, что у больных с ОКС без подъе-ма сегмента ST, сочетающимся с диабетом, выше рисксердечно-сосудистых исходов в ближайшем и отдален-ном периодах. При этом они получают субоптимальноелечение по сравнению с пациентами без диабета. В Ев-ропейских регистрах частота реваскуляризации (любо-го типа), применения тиенопиридинов и блокаторовGP IIb/IIIa рецепторов у больных диабетом была ниже,чем у пациентов без диабета, что сопровождалось чет-ким ухудшением госпитальной и отдаленной смертно-сти (5,9% и 3,2% через 1 мес и 15,2% и 7,6% через1 г). Кроме того, больным диабетом реперфузию илиреваскуляризацию проводят реже, чем у пациентам бездиабета [248,250].Пациенты с диабетом относятся к группе высокогориска, поэтому они нуждаются в более агрессивном ме-дикаментозном, а также инвазивном лечении. Крометого, им необходима адекватная вторичная профилак-тика, включающая медикаментозную терапию и моди-фикацию образа жизни [252].Результаты изучения эффективности жесткого конт-роля гликемии у пациентов с ИМ неоднозначные[251]. У пациентов с ИМ с подъемом сегмента STжесткий контроль гликемии путем внутривенного вве-дения инсулина в исследовании DIGAMI привел кснижению смертности в течение 1 года на 30%, одна-ко этот эффект не был подтвержден в исследованииDIGAMI-2. В последних исследованиях у стабильных па-циентов с диабетом, а также больных, находившихсяв отделениях интенсивной терапии, было выявлено улуч-шение исходов на фоне жесткого контроля гликемии,хотя он сопровождался увеличением частоты гипогли-кемических состояний [253]. Пока не будут полученыдополнительные данные, при сахароснижающей тера-пии следует добиваться отсутствия выраженной гипер-гликемии (>10-11 ммоль/л [180-200 мг/дл]), а так-же гипогликемии (<5 ммоль/л [90 мг/дл]). Эффектив-ность смеси глюкоза-инсулин-калий в профилактике ис-ходов не доказана; более того, она может даже даватьнежелательный эффект [254].Реваскуляризация у больных сахарным диабетом со-провождается особыми проблемами. У таких пациен-тов коронарный атеросклероз обычно диффузный и рас-пространенный и отмечается более высокая частота ре-стеноза, а также окклюзии после ЧКВ и КШ. После ЧКВповторную реваскуляризацию приходится проводитьчаще, чем после КШ. В этой группе пациентов с высо-ким риском установлена эффективность ранней инва-зивной стратегии, польза которой была более значитель-ной, чем у пациентов без диабета [255].У пациентов с сахарным диабетом и стенозом не-скольких сосудов КШ улучшало исходы по сравнениюс ЧКВ. По данным мета-анализа 7 812 пациентов, при-нимавших участие в 10 рандомизированных исследо-ваниях, смертность после КШ в течение 5,9 лет при на-личии сахарного диабета была значительно ниже, чемпосле ЧКВ [256]. В целом смертность в группах КШ иЧКВ не отличалась (15% и 16%; отношение рисков0,91; 95% ДИ 0,82–1,02; p=0,12), однако у 1 233 па-циентов было выявлено достоверное снижение смерт-ности после КШ [23% и 29%; отношение рисков 0,70; 95% 0,56–0,87; p=0,05; число больных, которых не-обходимо пролечить (NNT)=17]. В исследованииBARI-2D рандомизировали больных сахарным диабе-том и стабильной стенокардией, которым проводилиинтенсивную медикаментозную терапию или интенсив-ную медикаментозную терапию в сочетании с КШ илиЧКВ (по выбору врача). В течение 5 лет у пациентов, пе-ренесших КШ, по сравнению с группой больных, полу-чавших консервативную терапию, выявили снижениериска смерти и ИМ (21,1% и 29,2%; p<0,010), а так-же частоты сердечной смерти или ИМ (15,8% и 21,9%;p<0,03) и ИМ (10% и 17,6%; p<0,003). У пациентов,которым проводили ЧКВ, частота сердечно-сосудистыхисходов достоверно не отличалась от таковой на фонеконсервативной терапии [257,258]. В исследованииSYNTAX, в котором сравнивали результаты КШ и стен-тирования (применяли стенты, выделяющие лекарст-ва) у пациентов со стенозом ствола левой коронарнойартерии и нескольких коронарных артерий, разница ча-стоты нежелательных исходов в течение 1 года междугруппами КШ и ЧКВ удваивалась у пациентов с сахар-ным диабетом, в основном за счет повторной реваску-ляризации [259]. Однако достоверной разницы смерт-ности или частоты ИМ не выявили. И наконец, в NewYork Registry у пациентов с сахарным диабетом была вы-явлена тенденция к улучшению исходов после КШ посравнению с имплантацией стента, выделяющего ле-карства (ОШ смерти или ИМ в течение 18 мес 0,84; 95%ДИ 0,69–1,01) [260].Все эти исследования свидетельствуют о том, что КШимеет преимущества перед ЧКВ у больных сахарнымдиабетом. Однако следует отметить, что в большинствоперечисленных исследований включали только стабиль-ных пациентов с хронической ИБС, поэтому остается не-ясным, можно ли экстраполировать полученные дан-ные на пациентов с ОКС без подъема сегмента ST.По данным мета-анализа, имплантация стентов, вы-деляющих лекарства, по безопасности не уступалаимплантации голометаллических стентов, если двой-ную антитромбоцитарную терапию продолжали в тече-ние более 6 мес (подобная терапия в любом случае по-казана пациентам с ОКС) [261]. После установки стен-та, выделяющего лекарства, выявили значительноеснижение частоты повторной реваскуляризации целе-вого сосуда (ОШ 0,29 для стентов, выделяющих сиро-лимус и 0,38 — для стентов, выделяющих паклитаксел).Можно предположить, что у больных сахарным диабе-том будут получены сходные данные. Неконтролируе-мые исследования свидетельствуют о том, что артери-альные шунты имеют преимущества перед венозными.Влияние билатерального артериального шунтированияна риск отдаленных исходов и медиастинальных инфек-ций продолжает дискутироваться. У пациентов с ОКСспециальные исследования не проводились.Данных в пользу модификации схемы антитромбо-тической терапии у пациентов с сахарным диабетом нет.Однако в исследовании TRITON-TIMI 38 прасугрелпревосходил клопидогрел по эффективности в профи-лактике сердечно-сосудистой смерти, ИМ или инсуль-та и не вызывал увеличение риска кровотечений [262].В исследовании PLATO лечение тикагрелором посравнению с клопидогрелом привело к снижению ча-стоты ишемических исходов у пациентов с ОКС неза-висимо от наличия сахарного диабета и контроля гли-кемии и не сопровождалось увеличением частотыбольших кровотечений [263]. Применение тикагрело-ра привело к снижению общей смертности у пациен-тов с уровнем гемоглобина A1c выше медианы (>6%).Хотя при первом мета-анализе было установленоблагоприятное влияние блокаторов GP IIb/IIIa рецеп-торов (без сопутствующей терапии тиенопиридинами)на исходы у пациентов с сахарным диабетом [264], поль-за их широкого применения не была подтверждена висследовании EARLY-ACS [151]. Следовательно, нафоне современной терапии пероральными антитром-боцитарными препаратами дополнительно назначатьблокаторы GP IIb/IIIa рецепторов больным сахарнымдиабетом, по-видимому, не следует. У больных сахарным диабетом, которым проводят-ся ангиография и/или ЧКВ особое значение имеет про-филактика контрастной нефропатии.Откладывать ангиографию у пациентов, получающихметформин, не следует, так как риск развития лакта-цидоза минимальный [265]. После введения контраст-ных агентов следует тщательно контролировать функ-цию почек.
Рекомендации по лечению больных сахарным диабетом
5.5.3. Сахарный диабетПримерно 20-30% больных с ОКС без подъема сег-мента ST страдают сахарным диабетом. По крайней мере,у такого же процента пациентов имеются недиагности-рованный диабет или нарушение толерантности к глю-козе [247]. В исследовании Euro Heart Survey установ-ленный или вновь выявленный сахарный диабет имел-ся у 37% пациентов с ОКС без подъема сегмента ST [248].Пациенты с сахарным диабетом в целом старше, чащеявляются женщинами и чаще страдают сопутствующи-ми заболеваниями, такими как гипертония и почечнаянедостаточность. У них выше вероятность появления ати-пичных симптомов и развития осложнений, особенносердечной недостаточности и кровотечений [248].Сахарный диабет — это независимый предикторсмерти больных с ОКС без подъема сегмента ST. Рисксмерти у больных диабетом повышен в 2 раза [249,250].Кроме того, у пациентов с нарушением толерантностик глюкозе или нарушенной гликемией натощак прогнозхуже, чем у пациентов с нормальным метаболизмомглюкозы, однако лучше, чем у больных подтвержден-ным диабетом.Гипергликемия при поступлении или во время гос-питализации — это независимый неблагоприятныйпрогностический фактор при ОКС независимо от нали-чия сахарного диабета. Она может иметь даже большеенеблагоприятное прогностическое значение, чем уста-новленный диагноз диабета [251].Терапевтические аспектыРегистры показали, что у больных с ОКС без подъе-ма сегмента ST, сочетающимся с диабетом, выше рисксердечно-сосудистых исходов в ближайшем и отдален-ном периодах. При этом они получают субоптимальноелечение по сравнению с пациентами без диабета. В Ев-ропейских регистрах частота реваскуляризации (любо-го типа), применения тиенопиридинов и блокаторовGP IIb/IIIa рецепторов у больных диабетом была ниже,чем у пациентов без диабета, что сопровождалось чет-ким ухудшением госпитальной и отдаленной смертно-сти (5,9% и 3,2% через 1 мес и 15,2% и 7,6% через1 г). Кроме того, больным диабетом реперфузию илиреваскуляризацию проводят реже, чем у пациентам бездиабета [248,250].Пациенты с диабетом относятся к группе высокогориска, поэтому они нуждаются в более агрессивном ме-дикаментозном, а также инвазивном лечении. Крометого, им необходима адекватная вторичная профилак-тика, включающая медикаментозную терапию и моди-фикацию образа жизни [252].Результаты изучения эффективности жесткого конт-роля гликемии у пациентов с ИМ неоднозначные[251]. У пациентов с ИМ с подъемом сегмента STжесткий контроль гликемии путем внутривенного вве-дения инсулина в исследовании DIGAMI привел кснижению смертности в течение 1 года на 30%, одна-ко этот эффект не был подтвержден в исследованииDIGAMI-2. В последних исследованиях у стабильных па-циентов с диабетом, а также больных, находившихсяв отделениях интенсивной терапии, было выявлено улуч-шение исходов на фоне жесткого контроля гликемии,хотя он сопровождался увеличением частоты гипогли-кемических состояний [253]. Пока не будут полученыдополнительные данные, при сахароснижающей тера-пии следует добиваться отсутствия выраженной гипер-гликемии (>10-11 ммоль/л [180-200 мг/дл]), а так-же гипогликемии (<5 ммоль/л [90 мг/дл]). Эффектив-ность смеси глюкоза-инсулин-калий в профилактике ис-ходов не доказана; более того, она может даже даватьнежелательный эффект [254].Реваскуляризация у больных сахарным диабетом со-провождается особыми проблемами. У таких пациен-тов коронарный атеросклероз обычно диффузный и рас-пространенный и отмечается более высокая частота ре-стеноза, а также окклюзии после ЧКВ и КШ. После ЧКВповторную реваскуляризацию приходится проводитьчаще, чем после КШ. В этой группе пациентов с высо-ким риском установлена эффективность ранней инва-зивной стратегии, польза которой была более значитель-ной, чем у пациентов без диабета [255].У пациентов с сахарным диабетом и стенозом не-скольких сосудов КШ улучшало исходы по сравнениюс ЧКВ. По данным мета-анализа 7 812 пациентов, при-нимавших участие в 10 рандомизированных исследо-ваниях, смертность после КШ в течение 5,9 лет при на-личии сахарного диабета была значительно ниже, чемпосле ЧКВ [256]. В целом смертность в группах КШ иЧКВ не отличалась (15% и 16%; отношение рисков0,91; 95% ДИ 0,82–1,02; p=0,12), однако у 1 233 па-циентов было выявлено достоверное снижение смерт-ности после КШ [23% и 29%; отношение рисков 0,70; 95% 0,56–0,87; p=0,05; число больных, которых не-обходимо пролечить (NNT)=17]. В исследованииBARI-2D рандомизировали больных сахарным диабе-том и стабильной стенокардией, которым проводилиинтенсивную медикаментозную терапию или интенсив-ную медикаментозную терапию в сочетании с КШ илиЧКВ (по выбору врача). В течение 5 лет у пациентов, пе-ренесших КШ, по сравнению с группой больных, полу-чавших консервативную терапию, выявили снижениериска смерти и ИМ (21,1% и 29,2%; p<0,010), а так-же частоты сердечной смерти или ИМ (15,8% и 21,9%;p<0,03) и ИМ (10% и 17,6%; p<0,003). У пациентов,которым проводили ЧКВ, частота сердечно-сосудистыхисходов достоверно не отличалась от таковой на фонеконсервативной терапии [257,258]. В исследованииSYNTAX, в котором сравнивали результаты КШ и стен-тирования (применяли стенты, выделяющие лекарст-ва) у пациентов со стенозом ствола левой коронарнойартерии и нескольких коронарных артерий, разница ча-стоты нежелательных исходов в течение 1 года междугруппами КШ и ЧКВ удваивалась у пациентов с сахар-ным диабетом, в основном за счет повторной реваску-ляризации [259]. Однако достоверной разницы смерт-ности или частоты ИМ не выявили. И наконец, в NewYork Registry у пациентов с сахарным диабетом была вы-явлена тенденция к улучшению исходов после КШ посравнению с имплантацией стента, выделяющего ле-карства (ОШ смерти или ИМ в течение 18 мес 0,84; 95%ДИ 0,69–1,01) [260].Все эти исследования свидетельствуют о том, что КШимеет преимущества перед ЧКВ у больных сахарнымдиабетом. Однако следует отметить, что в большинствоперечисленных исследований включали только стабиль-ных пациентов с хронической ИБС, поэтому остается не-ясным, можно ли экстраполировать полученные дан-ные на пациентов с ОКС без подъема сегмента ST.По данным мета-анализа, имплантация стентов, вы-деляющих лекарства, по безопасности не уступалаимплантации голометаллических стентов, если двой-ную антитромбоцитарную терапию продолжали в тече-ние более 6 мес (подобная терапия в любом случае по-казана пациентам с ОКС) [261]. После установки стен-та, выделяющего лекарства, выявили значительноеснижение частоты повторной реваскуляризации целе-вого сосуда (ОШ 0,29 для стентов, выделяющих сиро-лимус и 0,38 — для стентов, выделяющих паклитаксел).Можно предположить, что у больных сахарным диабе-том будут получены сходные данные. Неконтролируе-мые исследования свидетельствуют о том, что артери-альные шунты имеют преимущества перед венозными.Влияние билатерального артериального шунтированияна риск отдаленных исходов и медиастинальных инфек-ций продолжает дискутироваться. У пациентов с ОКСспециальные исследования не проводились.Данных в пользу модификации схемы антитромбо-тической терапии у пациентов с сахарным диабетом нет.Однако в исследовании TRITON-TIMI 38 прасугрелпревосходил клопидогрел по эффективности в профи-лактике сердечно-сосудистой смерти, ИМ или инсуль-та и не вызывал увеличение риска кровотечений [262].В исследовании PLATO лечение тикагрелором посравнению с клопидогрелом привело к снижению ча-стоты ишемических исходов у пациентов с ОКС неза-висимо от наличия сахарного диабета и контроля гли-кемии и не сопровождалось увеличением частотыбольших кровотечений [263]. Применение тикагрело-ра привело к снижению общей смертности у пациен-тов с уровнем гемоглобина A1c выше медианы (>6%).Хотя при первом мета-анализе было установленоблагоприятное влияние блокаторов GP IIb/IIIa рецеп-торов (без сопутствующей терапии тиенопиридинами)на исходы у пациентов с сахарным диабетом [264], поль-за их широкого применения не была подтверждена висследовании EARLY-ACS [151]. Следовательно, нафоне современной терапии пероральными антитром-боцитарными препаратами дополнительно назначатьблокаторы GP IIb/IIIa рецепторов больным сахарнымдиабетом, по-видимому, не следует. У больных сахарным диабетом, которым проводят-ся ангиография и/или ЧКВ особое значение имеет про-филактика контрастной нефропатии.Откладывать ангиографию у пациентов, получающихметформин, не следует, так как риск развития лакта-цидоза минимальный [265]. После введения контраст-ных агентов следует тщательно контролировать функ-цию почек.
Рекомендации по лечению больных сахарным диабетом
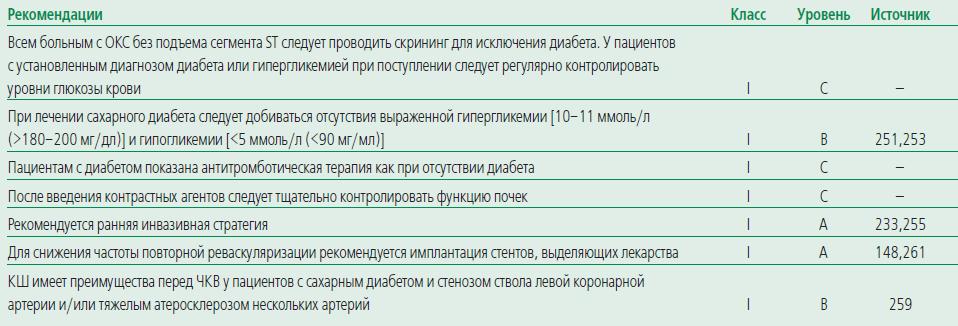 Таблица 10. Рекомендации по применениюантитромботических препаратов при ХБП
Таблица 10. Рекомендации по применениюантитромботических препаратов при ХБП
 Хроническая болезнь почек
Почечная дисфункция имеется у 30-40% пациен-тов с ОКС без подъема сегмента ST [266,267]. Оптималь-ным показателем функции почек является СКФ, кото-рую рассчитают с помощью уравнения MDRD с учетомэтнической принадлежности и пола. СКФ следует рас-считывать у всех пациентов с хронической болезнью по-чек (ХБП) или повышенным риском ее развития. В кли-нической практике можно рассчитывать также клиренскреатинина по формуле Кокрофта-Голта. КритерииХБП см. в предыдущих рекомендациях [3].У пациентов с ХБП часто развивается сердечная не-достаточность и отсутствует типичная боль в груди[268]. Пациенты с ОКС без подъема сегмента ST и ХБПнередко не получают адекватного лечения в соответствиис рекомендациями. ХБП ассоциируется с очень небла-гоприятным прогнозом [266,268] и является незави-симым предиктором смерти в ближайшем и отдален-ном периоде и больших кровотечений у больных с ОКСбез подъема сегмента ST [267].Терапевтические аспектыХотя доля пациентов с ОКС без подъема сегментаST и ХБП в клинических исследованиях была занижен-ной, это не может служить основанием для неадекват-ного лечения. Однако при применении антитромбо-тических препаратов необходимо соблюдать осто-рожность, учитывая риск геморрагических осложне-ний [168,269,270]. Данные регистров свидетель-ствуют о том, что у больных с ХБП часто отмечается пе-редозировка антитромботических препаратов, особен-но антикоагулянтов и блокаторов GP IIb/IIIa рецепто-ров, что повышает риск кровотечений. Многие препа-раты, которые исключительно или в значительнойстепени выводятся почками, следует назначать в по-ниженных дозах, а некоторые из них противопоказа-ны больным с ХБП, в том числе эноксапарин, фонда-паринукс, бивалирудин и низкомолекулярные блока-торы GP IIb/IIIa рецепторов (табл. 10). При тяжелой по-чечной недостаточности, когда противопоказаны фон-дапаринукс и эноксапарин, следует назначать НФГ. Од-нако в регистре GRACE применение НФГ не позволя-ло избежать геморрагических осложнений. При этомбыло отмечено постепенное нарастание риска крово-течений на фоне снижения функции почек, как и прилечении НМГ [269]. Преимущества НФГ перед други-ми антикоагулянтами у больных с ХБП связаны с лег-костью мониторирования антикоагулянтной актив-ности с помощью аЧТВ и возможностью быстрой ней-трализации активности препарата в случае крово-течения. Фондапаринукс по безопасности имел значи-тельные преимущества перед эноксапарином у боль-ных с ХБП. В исследовании OASIS-5 риск кровотече-ний при лечении фондапаринуксом был значительнониже, чем при применении эноксапарина. Тикагрелорв исследовании PLATO значительно снижал риск ише-мических осложнений и смерти по сравнению с кло-пидогрелом и не вызывал значительного увеличениячастоты больших кровотечений, хотя риск кровотече-ний, не связанных с вмешательствами, был недосто-верно выше в группе тикагрелора [271].
Систолическая дисфункция левого желудочкаи сердечная недостаточность
Сердечная недостаточность — это одно из самых ча-стых и тяжелых осложнений ОКС без подъема сегмен-та ST [274], хотя частота ее, по-видимому, снижается [50].Фракция выброса левого желудочка и сердечная недо-статочность — это независимые предикторы смерти идругих серьезных нежелательных исходов у пациентовс ОКС без подъема сегмента ST. Сердечная недостаточ-ность чаще встречается у пожилых людей и ассоцииру-ется с ухудшением прогноза, если нарушение функциисердца определяется при поступлении или во время гос-питализации [274]. У пациентов с сердечной недоста-точностью без боли в груди диагностировать ОКС бы-вает трудно, учитывая повышение уровня тропонинавследствие острой сердечной недостаточности. У такихпациентов иногда невозможно дифференцироватьострую сердечную недостаточность от ОКС без подъе-ма сегмента ST, осложнившегося сердечной недостаточ-ностью. Для дифференциальной диагностики двухсостояний может потребоваться ангиография.Терапевтические аспектыПациенты с ОКС без подъема сегмента ST, осложнив-шегося сердечной недостаточностью, реже получаютадекватное лечение в соответствии с рекомендациями,включая применение бета-адреноблокаторов и инги-биторов АПФ или блокаторов рецепторов ангиотензи-на II, коронарной ангиографии и реваскуляризации[50,274]. Все рекомендации, предложенные на осно-вании исследований у пациентов, перенесших ИМ, мож-но экстраполировать на пациентов с ОКС без подъемасегмента ST, осложнившимся сердечной недостаточ-ностью. Дополнительная информация содержится в со-ответствующих рекомендациях [275].
Низкая или высокая масса тела
Низкая масса тела ассоциируется с повышенным рис-ком смерти или ИМ и особенно кровотечений, которыечасто связаны с неадекватным выбором доз анти-тромботических препаратов [279]. У пациентов с низ-кой массой тела уровень креатинина может быть нормальным, несмотря на наличие почечной недостаточ-ности, особенно у пожилых людей. Нарушение функ-ции почек увеличивает риск токсических и вторичныхэффектов препаратов, которые выводятся почками. Всвязи с этим рекомендуется рассчитывать клиренскреатинина у пациентов с низкой массой тела и соот-ветствующим образом подбирать дозы препаратовдля внутривенного введения.Хотя ожирение сопровождается более высокимриском коронарных осложнений, у пациентов с ожи-рением и ОКС без подъема сегмента ST наблюдается па-радоксальное улучшение исходов во время пребыва-ния в стационаре и в течение 1 года, включая сниже-ние риска кровотечений [279,280]. У пациентов сожирением больше факторов риска, однако они моло-же. Таким пациентам чаще проводят адекватную тера-пию, что позволяет объяснить улучшение исходов[280].
Рекомендации по лечению пациентов с ХБП
Хроническая болезнь почек
Почечная дисфункция имеется у 30-40% пациен-тов с ОКС без подъема сегмента ST [266,267]. Оптималь-ным показателем функции почек является СКФ, кото-рую рассчитают с помощью уравнения MDRD с учетомэтнической принадлежности и пола. СКФ следует рас-считывать у всех пациентов с хронической болезнью по-чек (ХБП) или повышенным риском ее развития. В кли-нической практике можно рассчитывать также клиренскреатинина по формуле Кокрофта-Голта. КритерииХБП см. в предыдущих рекомендациях [3].У пациентов с ХБП часто развивается сердечная не-достаточность и отсутствует типичная боль в груди[268]. Пациенты с ОКС без подъема сегмента ST и ХБПнередко не получают адекватного лечения в соответствиис рекомендациями. ХБП ассоциируется с очень небла-гоприятным прогнозом [266,268] и является незави-симым предиктором смерти в ближайшем и отдален-ном периоде и больших кровотечений у больных с ОКСбез подъема сегмента ST [267].Терапевтические аспектыХотя доля пациентов с ОКС без подъема сегментаST и ХБП в клинических исследованиях была занижен-ной, это не может служить основанием для неадекват-ного лечения. Однако при применении антитромбо-тических препаратов необходимо соблюдать осто-рожность, учитывая риск геморрагических осложне-ний [168,269,270]. Данные регистров свидетель-ствуют о том, что у больных с ХБП часто отмечается пе-редозировка антитромботических препаратов, особен-но антикоагулянтов и блокаторов GP IIb/IIIa рецепто-ров, что повышает риск кровотечений. Многие препа-раты, которые исключительно или в значительнойстепени выводятся почками, следует назначать в по-ниженных дозах, а некоторые из них противопоказа-ны больным с ХБП, в том числе эноксапарин, фонда-паринукс, бивалирудин и низкомолекулярные блока-торы GP IIb/IIIa рецепторов (табл. 10). При тяжелой по-чечной недостаточности, когда противопоказаны фон-дапаринукс и эноксапарин, следует назначать НФГ. Од-нако в регистре GRACE применение НФГ не позволя-ло избежать геморрагических осложнений. При этомбыло отмечено постепенное нарастание риска крово-течений на фоне снижения функции почек, как и прилечении НМГ [269]. Преимущества НФГ перед други-ми антикоагулянтами у больных с ХБП связаны с лег-костью мониторирования антикоагулянтной актив-ности с помощью аЧТВ и возможностью быстрой ней-трализации активности препарата в случае крово-течения. Фондапаринукс по безопасности имел значи-тельные преимущества перед эноксапарином у боль-ных с ХБП. В исследовании OASIS-5 риск кровотече-ний при лечении фондапаринуксом был значительнониже, чем при применении эноксапарина. Тикагрелорв исследовании PLATO значительно снижал риск ише-мических осложнений и смерти по сравнению с кло-пидогрелом и не вызывал значительного увеличениячастоты больших кровотечений, хотя риск кровотече-ний, не связанных с вмешательствами, был недосто-верно выше в группе тикагрелора [271].
Систолическая дисфункция левого желудочкаи сердечная недостаточность
Сердечная недостаточность — это одно из самых ча-стых и тяжелых осложнений ОКС без подъема сегмен-та ST [274], хотя частота ее, по-видимому, снижается [50].Фракция выброса левого желудочка и сердечная недо-статочность — это независимые предикторы смерти идругих серьезных нежелательных исходов у пациентовс ОКС без подъема сегмента ST. Сердечная недостаточ-ность чаще встречается у пожилых людей и ассоцииру-ется с ухудшением прогноза, если нарушение функциисердца определяется при поступлении или во время гос-питализации [274]. У пациентов с сердечной недоста-точностью без боли в груди диагностировать ОКС бы-вает трудно, учитывая повышение уровня тропонинавследствие острой сердечной недостаточности. У такихпациентов иногда невозможно дифференцироватьострую сердечную недостаточность от ОКС без подъе-ма сегмента ST, осложнившегося сердечной недостаточ-ностью. Для дифференциальной диагностики двухсостояний может потребоваться ангиография.Терапевтические аспектыПациенты с ОКС без подъема сегмента ST, осложнив-шегося сердечной недостаточностью, реже получаютадекватное лечение в соответствии с рекомендациями,включая применение бета-адреноблокаторов и инги-биторов АПФ или блокаторов рецепторов ангиотензи-на II, коронарной ангиографии и реваскуляризации[50,274]. Все рекомендации, предложенные на осно-вании исследований у пациентов, перенесших ИМ, мож-но экстраполировать на пациентов с ОКС без подъемасегмента ST, осложнившимся сердечной недостаточ-ностью. Дополнительная информация содержится в со-ответствующих рекомендациях [275].
Низкая или высокая масса тела
Низкая масса тела ассоциируется с повышенным рис-ком смерти или ИМ и особенно кровотечений, которыечасто связаны с неадекватным выбором доз анти-тромботических препаратов [279]. У пациентов с низ-кой массой тела уровень креатинина может быть нормальным, несмотря на наличие почечной недостаточ-ности, особенно у пожилых людей. Нарушение функ-ции почек увеличивает риск токсических и вторичныхэффектов препаратов, которые выводятся почками. Всвязи с этим рекомендуется рассчитывать клиренскреатинина у пациентов с низкой массой тела и соот-ветствующим образом подбирать дозы препаратовдля внутривенного введения.Хотя ожирение сопровождается более высокимриском коронарных осложнений, у пациентов с ожи-рением и ОКС без подъема сегмента ST наблюдается па-радоксальное улучшение исходов во время пребыва-ния в стационаре и в течение 1 года, включая сниже-ние риска кровотечений [279,280]. У пациентов сожирением больше факторов риска, однако они моло-же. Таким пациентам чаще проводят адекватную тера-пию, что позволяет объяснить улучшение исходов[280].
Рекомендации по лечению пациентов с ХБП
 Рекомендации по лечению пациентов с сердечной недостаточностью
Рекомендации по лечению пациентов с сердечной недостаточностью
 Необструктивная коронарная болезнь сердца
У значительной части пациентов (около 15%) с ОКСбез подъема сегмента ST отсутствуют изменения коро-нарных артерий или имеется необструктивный коронар-ный атеросклероз. ОКС без подъема сегмента ST харак-теризуется неоднородным патогенезом, а возможныемеханизмы его развития включают в себя спазм коро-нарной артерии (стенокардия Принцметалла), ост-рый тромбоз на фоне интрамуральной бляшки с после-дующей реканализацией коронарной артерии, эмбо-лии в коронарные артерии и синдром Х. У пациентовс ОКС без подъема сегмента ST наличие неизмененныхили практически неизмененных коронарных артерийпри ангиографии позволяет усомниться в диагнозе. Од-нако изменения сегмента ST и выделение биомаркерову пациентов с типичной болью в груди и проходимы-ми коронарными артериями без выраженного стено-за могут быть следствием истинного некроза, а не от-ражать ложноположительные результаты. ОКС без из-менений коронарных артерий чаще встречается у жен-щин. Выраженные атеросклеротические изменениямогут наблюдаться даже при отсутствии ангиографиче-ского стеноза, так как диффузный атеросклероз приво-дит к ремоделированию стенки артерии. При этом утол-щение стенки сосуда происходит кнаружи, а просвет егоне суживается. Прогноз у таких пациентов более бла-гоприятный, чем при наличии выраженного коронар-ного атеросклероза, поэтому они нуждаются в оптималь-ной антитромботической терапии и вторичной профи-лактике антитромбоцитарными препаратами и стати-нами [281].Вариантная стенокардия Принцметалла часто оста-ется недиагностированной и характеризуется ишеми-ческой болью в груди, которая не связана с физическойнагрузкой или эмоциональным напряжением и сопро-вождается преходящим подъемом сегмента ST. Причи-ной стенокардии считают спазм эпикардиальной коро-нарной артерии, который может развиться в области тя-желого локального стеноза, однако в типичном случаеопределяется при минимальном атеросклеротическомпоражении. Пациенты с вариантной стенокардией не-сколько моложе пациентов с типичным ОКС без подъе-ма сегмента ST и часто являются злостными курильщи-ками. Симптомы обычно тяжелые и могут сопровождать-ся обмороками. Приступы стенокардии Принцметал-ла возникают в период с 12.00 ночи до 8.00 утра. Спазм может быть спонтанным или провоцируется ацетилхо-лином, холодовой пробой или гипервентиляцией.Для профилактики стенокардии Принцметалла приме-няют антагонисты кальция, которые предупреждают ко-ронарный спазм. Их назначают в максимальных пере-носимых дозах в виде монотерапии или в комбинациис нитратами.Синдром Х диагностируют у пациентов со стенокар-дией напряжения, у которых определяется депрессиясегмента ST при выполнении пробы с нагрузкой, а приангиографии отсутствует обструкция коронарных арте-рий. Частота или интенсивность приступов стенокардиимогут нарастать, или они возникают в покое. Могут на-блюдаться типичные признаки нестабильной стенокар-дии. Прогноз обычно хороший. Причина синдрома Х не установлена, однако он чаще всего сочетается с на-рушением эндотелий-зависимой артериальной вазо-дилатации, снижением секреции оксида азота и повы-шением чувствительности к симпатической стимуляции.Имеются данные о том, что у пациентов часто повыше-на реакция на боль. Учитывая благоприятный прогноз,необходимо в первую очередь успокоить пациентов иназначить нитраты, бета-адреноблокаторы или антаго-нисты кальция для купирования боли.Кардиомиопатия такоцубо (транзиторное шарооб-разное расширение верхушки левого желудочка) можетпроявляться клинической картиной ИМ с подъемом сег-мента ST или ОКС без подъема сегмента ST и характе-ризуется отсутствием ангиографических изменений в ко-ронарных артериях в сочетании с верхушечной и ино-гда медиовентрикулярной или базальной акинезиеймиокарда. Заболевание чаще встречается у женщин и,как правило, развивается после большого эмоцио-нального напряжения. Дисфункция левого желудочкаобычно обратима в течение нескольких дней или недель.В редких случаях ОКС без подъема сегмента ST с нор-мальными или практически неизмененными коро-нарными артериями развивается вследствие эмбо-лии в коронарную артерию на фоне фибрилляции илитрепетания предсердий. Фибрилляция предсердийчасто остается недиагностированной, поэтому частотаэтого механизма развития ОКС может быть заниженной.
Анемия
Анемия сопровождается ухудшением прогноза(сердечно-сосудистая смерть, ИМ или рецидивирую-щая ишемия) у пациентов с любыми вариантами ОКС[69]. Во время госпитализации персистирующая или на-растающая анемия ассоциируется с увеличением смерт-ности или частоты сердечной недостаточности посравнению с таковыми у пациентов без анемии или спреходящей анемией [282]. Анемия чаще встречаетсяу пациентов пожилого возраста, больных сахарным диа-бетом и почечной недостаточностью, а также с други-ми состояниями (геморрагический диатез или злока-чественная опухоль), которые могут вносить вклад вухудшение прогноза. Исходный уровень гемоглобинаоказался независимым предиктором кровотечений:чем ниже содержание гемоглобина, тем выше риск ге-моррагических осложнений, связанных и не связанныхс вмешательствами [283].Тактика ведения пациентов с анемией и ОКС безподъема сегмента ST эмпирическая. Необходимо уста-новить причину анемии, особенно скрытое крово-течение. Особое внимание следует уделять антитром-ботической терапии. Применение стентов, выделяющихлекарства, следует ограничивать, учитывая необходи-мость в длительной двойной антитромбоцитарной те-рапии. Необходимо тщательно взвесить показания к ангиографии и выбор сосудистого доступа (лучевая ар-терия), чтобы избежать дополнительной потери крови[284,285]. Трансфузии эритроцитарной массы прово-дят только по строгим показаниям, так как они сопро-вождаются увеличением смертности у больных с ОКС без подъема сегмента ST. Наблюдательные исследова-ния свидетельствуют о том, что трансфузий следует из-бегать, если гематокрит превышает 25%, а анемия хорошо переносится [286].
Рекомендации по лечению пациентов с анемией
Необструктивная коронарная болезнь сердца
У значительной части пациентов (около 15%) с ОКСбез подъема сегмента ST отсутствуют изменения коро-нарных артерий или имеется необструктивный коронар-ный атеросклероз. ОКС без подъема сегмента ST харак-теризуется неоднородным патогенезом, а возможныемеханизмы его развития включают в себя спазм коро-нарной артерии (стенокардия Принцметалла), ост-рый тромбоз на фоне интрамуральной бляшки с после-дующей реканализацией коронарной артерии, эмбо-лии в коронарные артерии и синдром Х. У пациентовс ОКС без подъема сегмента ST наличие неизмененныхили практически неизмененных коронарных артерийпри ангиографии позволяет усомниться в диагнозе. Од-нако изменения сегмента ST и выделение биомаркерову пациентов с типичной болью в груди и проходимы-ми коронарными артериями без выраженного стено-за могут быть следствием истинного некроза, а не от-ражать ложноположительные результаты. ОКС без из-менений коронарных артерий чаще встречается у жен-щин. Выраженные атеросклеротические изменениямогут наблюдаться даже при отсутствии ангиографиче-ского стеноза, так как диффузный атеросклероз приво-дит к ремоделированию стенки артерии. При этом утол-щение стенки сосуда происходит кнаружи, а просвет егоне суживается. Прогноз у таких пациентов более бла-гоприятный, чем при наличии выраженного коронар-ного атеросклероза, поэтому они нуждаются в оптималь-ной антитромботической терапии и вторичной профи-лактике антитромбоцитарными препаратами и стати-нами [281].Вариантная стенокардия Принцметалла часто оста-ется недиагностированной и характеризуется ишеми-ческой болью в груди, которая не связана с физическойнагрузкой или эмоциональным напряжением и сопро-вождается преходящим подъемом сегмента ST. Причи-ной стенокардии считают спазм эпикардиальной коро-нарной артерии, который может развиться в области тя-желого локального стеноза, однако в типичном случаеопределяется при минимальном атеросклеротическомпоражении. Пациенты с вариантной стенокардией не-сколько моложе пациентов с типичным ОКС без подъе-ма сегмента ST и часто являются злостными курильщи-ками. Симптомы обычно тяжелые и могут сопровождать-ся обмороками. Приступы стенокардии Принцметал-ла возникают в период с 12.00 ночи до 8.00 утра. Спазм может быть спонтанным или провоцируется ацетилхо-лином, холодовой пробой или гипервентиляцией.Для профилактики стенокардии Принцметалла приме-няют антагонисты кальция, которые предупреждают ко-ронарный спазм. Их назначают в максимальных пере-носимых дозах в виде монотерапии или в комбинациис нитратами.Синдром Х диагностируют у пациентов со стенокар-дией напряжения, у которых определяется депрессиясегмента ST при выполнении пробы с нагрузкой, а приангиографии отсутствует обструкция коронарных арте-рий. Частота или интенсивность приступов стенокардиимогут нарастать, или они возникают в покое. Могут на-блюдаться типичные признаки нестабильной стенокар-дии. Прогноз обычно хороший. Причина синдрома Х не установлена, однако он чаще всего сочетается с на-рушением эндотелий-зависимой артериальной вазо-дилатации, снижением секреции оксида азота и повы-шением чувствительности к симпатической стимуляции.Имеются данные о том, что у пациентов часто повыше-на реакция на боль. Учитывая благоприятный прогноз,необходимо в первую очередь успокоить пациентов иназначить нитраты, бета-адреноблокаторы или антаго-нисты кальция для купирования боли.Кардиомиопатия такоцубо (транзиторное шарооб-разное расширение верхушки левого желудочка) можетпроявляться клинической картиной ИМ с подъемом сег-мента ST или ОКС без подъема сегмента ST и характе-ризуется отсутствием ангиографических изменений в ко-ронарных артериях в сочетании с верхушечной и ино-гда медиовентрикулярной или базальной акинезиеймиокарда. Заболевание чаще встречается у женщин и,как правило, развивается после большого эмоцио-нального напряжения. Дисфункция левого желудочкаобычно обратима в течение нескольких дней или недель.В редких случаях ОКС без подъема сегмента ST с нор-мальными или практически неизмененными коро-нарными артериями развивается вследствие эмбо-лии в коронарную артерию на фоне фибрилляции илитрепетания предсердий. Фибрилляция предсердийчасто остается недиагностированной, поэтому частотаэтого механизма развития ОКС может быть заниженной.
Анемия
Анемия сопровождается ухудшением прогноза(сердечно-сосудистая смерть, ИМ или рецидивирую-щая ишемия) у пациентов с любыми вариантами ОКС[69]. Во время госпитализации персистирующая или на-растающая анемия ассоциируется с увеличением смерт-ности или частоты сердечной недостаточности посравнению с таковыми у пациентов без анемии или спреходящей анемией [282]. Анемия чаще встречаетсяу пациентов пожилого возраста, больных сахарным диа-бетом и почечной недостаточностью, а также с други-ми состояниями (геморрагический диатез или злока-чественная опухоль), которые могут вносить вклад вухудшение прогноза. Исходный уровень гемоглобинаоказался независимым предиктором кровотечений:чем ниже содержание гемоглобина, тем выше риск ге-моррагических осложнений, связанных и не связанныхс вмешательствами [283].Тактика ведения пациентов с анемией и ОКС безподъема сегмента ST эмпирическая. Необходимо уста-новить причину анемии, особенно скрытое крово-течение. Особое внимание следует уделять антитром-ботической терапии. Применение стентов, выделяющихлекарства, следует ограничивать, учитывая необходи-мость в длительной двойной антитромбоцитарной те-рапии. Необходимо тщательно взвесить показания к ангиографии и выбор сосудистого доступа (лучевая ар-терия), чтобы избежать дополнительной потери крови[284,285]. Трансфузии эритроцитарной массы прово-дят только по строгим показаниям, так как они сопро-вождаются увеличением смертности у больных с ОКС без подъема сегмента ST. Наблюдательные исследова-ния свидетельствуют о том, что трансфузий следует из-бегать, если гематокрит превышает 25%, а анемия хорошо переносится [286].
Рекомендации по лечению пациентов с анемией
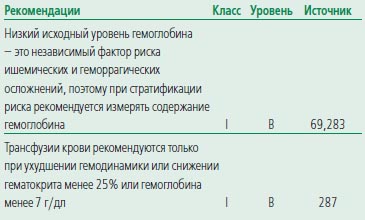 Кровотечения и трансфузии
Кровотечение — это самое частое неишемическоеосложнение при лечении ОКС без подъема сегмента ST,а также при ИМ с подъемом сегмента ST, ЧКВ и КШ. Важ-ность кровотечений была подробно рассмотрена впредыдущих рекомендациях [3] и подтверждена впоследующих исследованиях. В связи с этим в настоя-щем документе рассматриваются только новые данные.В связи с отсутствием общепринятого определениякровотечения оценить истинную частоту геморрагиче-ских осложнений в различных исследованиях и реги-страх трудно. «Универсальное определение» кровотече-ний, предложенное Bleeding Academic Research Consortium,позволит более объективно оценивать эти ослож-нений в будущих исследованиях [288]. Интересно, чточастота кровотечений в регистрах снизилась за послед-ние 7 лет, несмотря на более частое назначение двой-ной или тройной антитромбоцитарной терапии в со-четании с антикоагулянтами и более часто применениеинвазивных методов диагностики и лечения [289]. Этоможет указывать на то, что врачи осознают риск кро-вотечений при лечении ОКС и соответствующим обра-зом адаптируют стратегию ведения пациентов.Несмотря на вариабельность критериев оценкикровотечений, во многих исследованиях была подтвер-ждена дозозависимая ассоциация между кровотечения-ми и риском смерти и других ишемических осложне-ний. Большие кровотечения сопровождались 4-крат-ным увеличением риска смерти, 5-кратным увеличе-нием риска рецидивирующего ИМ и 3-кратнымувеличением риска инсульта в течение 30 дн [290]. Эти данные были подтверждены при анализе регистраGRACE и в клинических исследованиях, таких какOASIS-5 [291] и ACUITY [292]. Небольшие кровотече-ния также оказывают влияние на исходы, хотя и в мень-шей степени.Риск кровотечений тщательно изучен в первые 30дн после развития ОКС, в то время как риск поздних кро-вотечений на фоне длительной мощной антитромбо-цитарной терапии (более чем через 30 дн до конца на-блюдения или в течение 1 года) анализировался в мень-шей степени. В исследовании CURE [111] частота лю-бых больших кровотечений в течение первых 30 дн со-ставила 1,54% в группе плацебо и 2,01% в группе кло-пидогрела, а спустя 30 дн и до конца 1 года — 1,18%и 1,75%, соответственно. В исследовании TRITON нафоне инвазивного лечения частота больших кровотече-ний через 30-450 дн составила 1,23% в группе клопи-догрела и 1,71% в группе прасугрела [293]. В иссле-довании PLATO соответствующие показатели не оцени-вали. Общая частота больших кровотечений не отлича-лась, однако со временем было отмечено постепенноенарастание частоты больших кровотечений, не связан-ных с КШ; через 1 год отношение рисков составило1,19 (95% ДИ 1,02–1,38; p<0,03) [132]. При стабиль-ной ИБС было отмечено сходное постепенное увеличе-ние риска кровотечений в группах клопидогрела и пла-цебо; через 1 год отношение рисков составило1,88 (95% ДИ 1,45–2,45; p=0,001) [294]. Таким об-разом, риск кровотечений самый высокий в течение пер-вых 30 дн, однако длительная антитромбоцитарная те-рапия приводит к постепенному увеличению риска ге-моррагических осложнений.Независимыми предикторами больших кровотече-ний, установленными в клинических исследованиях ирегистрах, являются исходные показатели, особенно воз-раст, женский пол, кровотечения в анамнезе, исходныйуровень гемоглобина, диабет и почечная недостаточ-ность. Ухудшение функции почек, особенно клиренскреатинина менее 60 мл/мин, значительно увеличи-вает риск кровотечений. Важное значение имеет так-же метод лечения. Риск кровотечений повышаетсяпри увеличении числа назначенных антитромбоцитар-ных препаратов, включая антикоагулянты, аспирин, бло-каторы P2Y12 рецепторов и особенно блокаторыGP IIb/IIIa рецепторов, а также при применении фемо-рального, а не лучевого доступа [284,285]. Крометого, риск кровотечений увеличивается на фоне при-менения лекарственных препаратов в слишком высо-ких дозах, которое часто отмечается у пациентов с са-мым высоким риском геморрагических осложнений,в частности у женщин, пожилых людей и пациентов спочечной недостаточностью [168]. Двойная антитром-боцитарная терапия в сочетании с антагонистами ви-тамина К, которая часто показана пациентам с ОКС, так-же может способствовать увеличению риска кровотече-ний [295]. Индексы риска кровотечений см. в разделе4.4.Механизмы ухудшения прогноза при кровотеченияхостаются неясными. Основное значение, вероятно,имеет необходимость отмены антитромбоцитарных иантитромботических препаратов, которая приводит кувеличению риска ишемических исходов, особеннотромбоза стента после ЧКВ. Кроме того, факторы рис-ка кровотечений и ишемических осложнений в значи-тельной степени перекрещиваются. Нельзя исключить,что у пациентов с более высоким риском повышена ве-роятность осложнений обоих типов, поэтому они по-лучают наиболее агрессивное медикаментозное и ин-вазивное лечение. В регистре GRACE увеличение рис-ка кровотечений при снижении функции почек было па-раллельным увеличению риска смерти. Эти данные былиподтверждены при анализе post-hoc исследованияOASIS-5, в котором риск кровотечений зеркально отра-жал увеличение индекса риска GRACE [296]. Следова-тельно, развитие кровотечений может быть простымтриггером ухудшения прогноза у уязвимых пациентов.Другими факторами риска смерти при кровотеченияхмогут быть гемодинамические последствия кровопо-тери, потенциальные неблагоприятные эффекты гемо-трансфузии и протромботическое или провоспалитель-ное состояние, индуцированное кровотечением[297,298].Лечение геморрагических осложненийПредупреждение кровотечений — это важная состав-ная часть стратегии профилактики ишемических ослож-нений. Соответственно, при стратификации риска у па-циентов с ОКС без подъема сегмента ST следует оценитьриск как тромботических, так и геморрагическихосложнений. Профилактика кровотечений предпола-гает выбор более безопасных препаратов и адекватнойдозы (с учетом возраста, пола и клиренса креатинина),снижение длительности антитромботической тера-пии, применение комбинации антитромботических иантитромбоцитарных препаратов в соответствии сустановленными показаниями, использование лучево-го, а не феморального доступа для инвазивного вме-шательства [299]. По данным мета-анализа исследо-ваний ACUITY и HORIZONS, применение бивалируди-на вместо стандартных антикоагулянтов в сочетании сблокаторами GP IIb/IIIa рецепторов снижало риск кро-вотечений [300].Желудочно-кишечные кровотечения составляютоколо 50% в структуре спонтанных кровотечений в на-чальную фазу ОКС. В связи с этим следует назначать ин-гибиторы протонной помпы, особенно пациентам с же-лудочно-кишечными кровотечениями или пептиче-ской язвой в анамнезе. Возможное взаимодействие клопидогрела с омепразолом и в меньшей степени с дру-гими ингибиторами протонной помпы, по-видимому,не имеет клинического значения (см. раздел 5.2.2.).Небольшие кровотечения не требуют перерыва влечении, если они не продолжаются. При большом кро-вотечении, например желудочно-кишечном, ретропе-ритонеальном, внутричерепном, или другой тяжелойкровопотере необходимо прекратить терапию и ней-трализовать активность антитромбоцитарных и анти-тромботических препаратов, если кровотечение неудается остановить с помощью обычных мер. Преры-вать лечение антитромботическими препаратами не обя-зательно, если удается полностью остановить кровотече-ние. В клинической практике следует взвешивать риск,связанный с перерывом в лечении антитромботически-ми препаратами, и риск тромботических осложне-ний, особенно после имплантации стента.Действие НФГ можно нейтрализовать с помощью эк-вимолярных концентраций протамина сульфата. Про-тамин сульфат оказывает менее выраженное действиена эноксапарин и не влияет на эффекты фондапаринук-са или бивалирудина. Бивалирудин имеет очень корот-кий период полувыведения, поэтому нейтрализация егоактивности может не потребоваться. В случае фонда-паринукса рекомендуется введение рекомбинантногофактора VIIа, однако оно сопровождалось повышеннымриском тромботических осложнений [301]. Антидотынеобратимых антитромбоцитарных препаратов, та-ких как аспирин, клопидогрел или прасугрел, не-известны. Соответственно, их действие можно нейтра-лизовать только путем трансфузии свежей тромбоци-тарной массы. То же касается тикагрелора вскоре (<3дн) после отмены препарата.Блокаторы GP IIb/II рецепторов имеют различныефармакологические свойства, которые следует учиты-вать при выборе метода нейтрализации их действия.Низкомолекулярные препараты (тирофибан и эптифи-батид) обратимо связываются с рецепторами и быстровыводятся почками, поэтому функция тромбоцитов нор-мализуется через 4-8 ч после прекращения инфузии.После отмены абциксимаба функция тромбоцитоввосстанавливается в течение примерно 48 ч.Возобновлять лечение антитромбоцитарными пре-паратами и/или антикоагулянтами следует только в томслучае, если удается контролировать кровотечение втечение по крайней мере 24 ч.Эффекты гемотрансфузииГемотрансфузии дают неблагоприятные эффекты (по-вышение риска смерти и ИМ, а также пневмонии) вомногих клинических ситуациях, включая ОКС, ЧКВ, КШ,и во время интенсивной терапии [286,298]. Нежела-тельное действие гемотрансфузий объясняют различ-ными механизмами. Наибольшее значение имеет хра-нение крови. Негативный эффект гемотрансфузий нариск неблагоприятных исходов в значительной степе-ни зависит от минимального гематокрита и уровня ге-моглобина, при которых начинают трансфузию. Пере-ливание крови оправданно при гематокрите менее 25%,но не выше этого значения [286,298]. Трансфузию сле-дует проводить при уровне гемоглобина 7 г/дл, доби-ваясь его увеличения до 9-10 г/дл. В этом случае ре-зультаты лучше, чем при более «либеральных» показа-ниях к гемотрансфузии [287,302]. У пациентов состабильной гемодинамикой гемотрансфузия целесооб-разна только при исходном уровне гемоглобина <7 г/дл,в то время как при нестабильной гемодинамике какие-либо ограничения отсутствуют.Препараты железа и эритропоэтинПрепараты железа вводят, если анемия связана с де-фицитом железа или происходит массивная кровопо-теря. Лечение дефицита железа предполагает длитель-ное пероральное применение препаратов железа.Если пациент плохо переносит препараты для приемавнутрь, возможно внутривенное введение. Сочетанноеприменение эритропоэтина при ОКС невозможно,учитывая повышенный риск тромбоза глубоких вен, ин-сульта и острых коронарных исходов [303].
Тромбоцитопения
При лечении ОКС без подъема сегмента ST можетразвиться тромбоцитопения — снижение числа тром-боцитов менее 100 000 в мкл или по крайней мере на50% по сравнению с исходным. Тромбоцитопению счи-тают умеренной, если число тромбоцитов составляет20 000-50 000 в мкл, и тяжелой, если оно снижаетсяменее 20 000 в мкл.При ОКС выделяют два основных типа тромбоцито-пении, вызванной лекарствами (гепарин и блокаторыGP IIb/IIIa рецепторов), которые отличаются по прогно-зу. Полную информацию об обоих типах тромбоцито-пении можно найти в предыдущих рекомендациях [3].Гепарин-индуцированную тромбоцитопению следу-ет предполагать при снижении числа тромбоцитов бо-лее чем на 50% или до 100 000 в мкл. Она развивает-ся у 15% пациентов, получающих НФГ, встречается режепри применении НМГ и не наблюдается при лечениифондапаринуксом. Если подозревается гепарин-ин-дуцированная тромбоцитопения, следует немедленноотменить НФГ или НМГ. Могут быть назначены альтер-нативные антитромботические препараты даже приотсутствии тромботических осложнений. Можно исполь-зовать гепариноиды, такие как данапароид натрий, хотяin vitro наблюдали перекрестные реакции с НФГ или НМГ,однако они не осложнялись тромбозом. Альтернатива— применение прямых ингибиторов тромбина, таких какаргатробан, гирудин или его производные, которые не вызывают тромбоцитопению. Они обеспечивают стой-кий антитромботический эффект, который контролируютс помощью аЧТВ, хотя зависимость эффекта от дозы не-линейная и сглаживается при увеличении доз. Фонда-паринукс также можно применять в этой ситуации, таккак он оказывает мощное антитромботическое действиеи не взаимодействует с тромбоцитами, однако данноепоказание не зарегистрировано.Частота тромбоцитопении, вызванной блокаторамиGP IIb/IIIa рецепторов, в клинических исследованияхсоставляла от 0,5 до 5,6% в зависимости от типа пре-парата. Тяжелая тромбоцитопения может быть бессимп-томной и сопровождаться только небольшими крово-течениями в области сосудистого доступа. Большие кро-вотечения развиваются редко, но могут угрожать жиз-ни. У всех пациентов, получающих блокаторыGP IIb/IIIa рецепторов, рекомендуется измерить числотромбоцитов через 8 ч после начала инфузии или в слу-чае кровотечения. Если число тромбоцитов снижаетсяменее 10 000 в мкл, рекомендуется отменить блокато-ры GP IIb/IIIa рецепторов, а также НФГ или эноксапа-рин. При кровотечении рекомендуется трансфузиятромбоцитарной массы. Предлагалось также введениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с трансфу-зией тромбоцитарной массы.
Рекомендации по лечению геморрагических осложнений
Кровотечения и трансфузии
Кровотечение — это самое частое неишемическоеосложнение при лечении ОКС без подъема сегмента ST,а также при ИМ с подъемом сегмента ST, ЧКВ и КШ. Важ-ность кровотечений была подробно рассмотрена впредыдущих рекомендациях [3] и подтверждена впоследующих исследованиях. В связи с этим в настоя-щем документе рассматриваются только новые данные.В связи с отсутствием общепринятого определениякровотечения оценить истинную частоту геморрагиче-ских осложнений в различных исследованиях и реги-страх трудно. «Универсальное определение» кровотече-ний, предложенное Bleeding Academic Research Consortium,позволит более объективно оценивать эти ослож-нений в будущих исследованиях [288]. Интересно, чточастота кровотечений в регистрах снизилась за послед-ние 7 лет, несмотря на более частое назначение двой-ной или тройной антитромбоцитарной терапии в со-четании с антикоагулянтами и более часто применениеинвазивных методов диагностики и лечения [289]. Этоможет указывать на то, что врачи осознают риск кро-вотечений при лечении ОКС и соответствующим обра-зом адаптируют стратегию ведения пациентов.Несмотря на вариабельность критериев оценкикровотечений, во многих исследованиях была подтвер-ждена дозозависимая ассоциация между кровотечения-ми и риском смерти и других ишемических осложне-ний. Большие кровотечения сопровождались 4-крат-ным увеличением риска смерти, 5-кратным увеличе-нием риска рецидивирующего ИМ и 3-кратнымувеличением риска инсульта в течение 30 дн [290]. Эти данные были подтверждены при анализе регистраGRACE и в клинических исследованиях, таких какOASIS-5 [291] и ACUITY [292]. Небольшие кровотече-ния также оказывают влияние на исходы, хотя и в мень-шей степени.Риск кровотечений тщательно изучен в первые 30дн после развития ОКС, в то время как риск поздних кро-вотечений на фоне длительной мощной антитромбо-цитарной терапии (более чем через 30 дн до конца на-блюдения или в течение 1 года) анализировался в мень-шей степени. В исследовании CURE [111] частота лю-бых больших кровотечений в течение первых 30 дн со-ставила 1,54% в группе плацебо и 2,01% в группе кло-пидогрела, а спустя 30 дн и до конца 1 года — 1,18%и 1,75%, соответственно. В исследовании TRITON нафоне инвазивного лечения частота больших кровотече-ний через 30-450 дн составила 1,23% в группе клопи-догрела и 1,71% в группе прасугрела [293]. В иссле-довании PLATO соответствующие показатели не оцени-вали. Общая частота больших кровотечений не отлича-лась, однако со временем было отмечено постепенноенарастание частоты больших кровотечений, не связан-ных с КШ; через 1 год отношение рисков составило1,19 (95% ДИ 1,02–1,38; p<0,03) [132]. При стабиль-ной ИБС было отмечено сходное постепенное увеличе-ние риска кровотечений в группах клопидогрела и пла-цебо; через 1 год отношение рисков составило1,88 (95% ДИ 1,45–2,45; p=0,001) [294]. Таким об-разом, риск кровотечений самый высокий в течение пер-вых 30 дн, однако длительная антитромбоцитарная те-рапия приводит к постепенному увеличению риска ге-моррагических осложнений.Независимыми предикторами больших кровотече-ний, установленными в клинических исследованиях ирегистрах, являются исходные показатели, особенно воз-раст, женский пол, кровотечения в анамнезе, исходныйуровень гемоглобина, диабет и почечная недостаточ-ность. Ухудшение функции почек, особенно клиренскреатинина менее 60 мл/мин, значительно увеличи-вает риск кровотечений. Важное значение имеет так-же метод лечения. Риск кровотечений повышаетсяпри увеличении числа назначенных антитромбоцитар-ных препаратов, включая антикоагулянты, аспирин, бло-каторы P2Y12 рецепторов и особенно блокаторыGP IIb/IIIa рецепторов, а также при применении фемо-рального, а не лучевого доступа [284,285]. Крометого, риск кровотечений увеличивается на фоне при-менения лекарственных препаратов в слишком высо-ких дозах, которое часто отмечается у пациентов с са-мым высоким риском геморрагических осложнений,в частности у женщин, пожилых людей и пациентов спочечной недостаточностью [168]. Двойная антитром-боцитарная терапия в сочетании с антагонистами ви-тамина К, которая часто показана пациентам с ОКС, так-же может способствовать увеличению риска кровотече-ний [295]. Индексы риска кровотечений см. в разделе4.4.Механизмы ухудшения прогноза при кровотеченияхостаются неясными. Основное значение, вероятно,имеет необходимость отмены антитромбоцитарных иантитромботических препаратов, которая приводит кувеличению риска ишемических исходов, особеннотромбоза стента после ЧКВ. Кроме того, факторы рис-ка кровотечений и ишемических осложнений в значи-тельной степени перекрещиваются. Нельзя исключить,что у пациентов с более высоким риском повышена ве-роятность осложнений обоих типов, поэтому они по-лучают наиболее агрессивное медикаментозное и ин-вазивное лечение. В регистре GRACE увеличение рис-ка кровотечений при снижении функции почек было па-раллельным увеличению риска смерти. Эти данные былиподтверждены при анализе post-hoc исследованияOASIS-5, в котором риск кровотечений зеркально отра-жал увеличение индекса риска GRACE [296]. Следова-тельно, развитие кровотечений может быть простымтриггером ухудшения прогноза у уязвимых пациентов.Другими факторами риска смерти при кровотеченияхмогут быть гемодинамические последствия кровопо-тери, потенциальные неблагоприятные эффекты гемо-трансфузии и протромботическое или провоспалитель-ное состояние, индуцированное кровотечением[297,298].Лечение геморрагических осложненийПредупреждение кровотечений — это важная состав-ная часть стратегии профилактики ишемических ослож-нений. Соответственно, при стратификации риска у па-циентов с ОКС без подъема сегмента ST следует оценитьриск как тромботических, так и геморрагическихосложнений. Профилактика кровотечений предпола-гает выбор более безопасных препаратов и адекватнойдозы (с учетом возраста, пола и клиренса креатинина),снижение длительности антитромботической тера-пии, применение комбинации антитромботических иантитромбоцитарных препаратов в соответствии сустановленными показаниями, использование лучево-го, а не феморального доступа для инвазивного вме-шательства [299]. По данным мета-анализа исследо-ваний ACUITY и HORIZONS, применение бивалируди-на вместо стандартных антикоагулянтов в сочетании сблокаторами GP IIb/IIIa рецепторов снижало риск кро-вотечений [300].Желудочно-кишечные кровотечения составляютоколо 50% в структуре спонтанных кровотечений в на-чальную фазу ОКС. В связи с этим следует назначать ин-гибиторы протонной помпы, особенно пациентам с же-лудочно-кишечными кровотечениями или пептиче-ской язвой в анамнезе. Возможное взаимодействие клопидогрела с омепразолом и в меньшей степени с дру-гими ингибиторами протонной помпы, по-видимому,не имеет клинического значения (см. раздел 5.2.2.).Небольшие кровотечения не требуют перерыва влечении, если они не продолжаются. При большом кро-вотечении, например желудочно-кишечном, ретропе-ритонеальном, внутричерепном, или другой тяжелойкровопотере необходимо прекратить терапию и ней-трализовать активность антитромбоцитарных и анти-тромботических препаратов, если кровотечение неудается остановить с помощью обычных мер. Преры-вать лечение антитромботическими препаратами не обя-зательно, если удается полностью остановить кровотече-ние. В клинической практике следует взвешивать риск,связанный с перерывом в лечении антитромботически-ми препаратами, и риск тромботических осложне-ний, особенно после имплантации стента.Действие НФГ можно нейтрализовать с помощью эк-вимолярных концентраций протамина сульфата. Про-тамин сульфат оказывает менее выраженное действиена эноксапарин и не влияет на эффекты фондапаринук-са или бивалирудина. Бивалирудин имеет очень корот-кий период полувыведения, поэтому нейтрализация егоактивности может не потребоваться. В случае фонда-паринукса рекомендуется введение рекомбинантногофактора VIIа, однако оно сопровождалось повышеннымриском тромботических осложнений [301]. Антидотынеобратимых антитромбоцитарных препаратов, та-ких как аспирин, клопидогрел или прасугрел, не-известны. Соответственно, их действие можно нейтра-лизовать только путем трансфузии свежей тромбоци-тарной массы. То же касается тикагрелора вскоре (<3дн) после отмены препарата.Блокаторы GP IIb/II рецепторов имеют различныефармакологические свойства, которые следует учиты-вать при выборе метода нейтрализации их действия.Низкомолекулярные препараты (тирофибан и эптифи-батид) обратимо связываются с рецепторами и быстровыводятся почками, поэтому функция тромбоцитов нор-мализуется через 4-8 ч после прекращения инфузии.После отмены абциксимаба функция тромбоцитоввосстанавливается в течение примерно 48 ч.Возобновлять лечение антитромбоцитарными пре-паратами и/или антикоагулянтами следует только в томслучае, если удается контролировать кровотечение втечение по крайней мере 24 ч.Эффекты гемотрансфузииГемотрансфузии дают неблагоприятные эффекты (по-вышение риска смерти и ИМ, а также пневмонии) вомногих клинических ситуациях, включая ОКС, ЧКВ, КШ,и во время интенсивной терапии [286,298]. Нежела-тельное действие гемотрансфузий объясняют различ-ными механизмами. Наибольшее значение имеет хра-нение крови. Негативный эффект гемотрансфузий нариск неблагоприятных исходов в значительной степе-ни зависит от минимального гематокрита и уровня ге-моглобина, при которых начинают трансфузию. Пере-ливание крови оправданно при гематокрите менее 25%,но не выше этого значения [286,298]. Трансфузию сле-дует проводить при уровне гемоглобина 7 г/дл, доби-ваясь его увеличения до 9-10 г/дл. В этом случае ре-зультаты лучше, чем при более «либеральных» показа-ниях к гемотрансфузии [287,302]. У пациентов состабильной гемодинамикой гемотрансфузия целесооб-разна только при исходном уровне гемоглобина <7 г/дл,в то время как при нестабильной гемодинамике какие-либо ограничения отсутствуют.Препараты железа и эритропоэтинПрепараты железа вводят, если анемия связана с де-фицитом железа или происходит массивная кровопо-теря. Лечение дефицита железа предполагает длитель-ное пероральное применение препаратов железа.Если пациент плохо переносит препараты для приемавнутрь, возможно внутривенное введение. Сочетанноеприменение эритропоэтина при ОКС невозможно,учитывая повышенный риск тромбоза глубоких вен, ин-сульта и острых коронарных исходов [303].
Тромбоцитопения
При лечении ОКС без подъема сегмента ST можетразвиться тромбоцитопения — снижение числа тром-боцитов менее 100 000 в мкл или по крайней мере на50% по сравнению с исходным. Тромбоцитопению счи-тают умеренной, если число тромбоцитов составляет20 000-50 000 в мкл, и тяжелой, если оно снижаетсяменее 20 000 в мкл.При ОКС выделяют два основных типа тромбоцито-пении, вызванной лекарствами (гепарин и блокаторыGP IIb/IIIa рецепторов), которые отличаются по прогно-зу. Полную информацию об обоих типах тромбоцито-пении можно найти в предыдущих рекомендациях [3].Гепарин-индуцированную тромбоцитопению следу-ет предполагать при снижении числа тромбоцитов бо-лее чем на 50% или до 100 000 в мкл. Она развивает-ся у 15% пациентов, получающих НФГ, встречается режепри применении НМГ и не наблюдается при лечениифондапаринуксом. Если подозревается гепарин-ин-дуцированная тромбоцитопения, следует немедленноотменить НФГ или НМГ. Могут быть назначены альтер-нативные антитромботические препараты даже приотсутствии тромботических осложнений. Можно исполь-зовать гепариноиды, такие как данапароид натрий, хотяin vitro наблюдали перекрестные реакции с НФГ или НМГ,однако они не осложнялись тромбозом. Альтернатива— применение прямых ингибиторов тромбина, таких какаргатробан, гирудин или его производные, которые не вызывают тромбоцитопению. Они обеспечивают стой-кий антитромботический эффект, который контролируютс помощью аЧТВ, хотя зависимость эффекта от дозы не-линейная и сглаживается при увеличении доз. Фонда-паринукс также можно применять в этой ситуации, таккак он оказывает мощное антитромботическое действиеи не взаимодействует с тромбоцитами, однако данноепоказание не зарегистрировано.Частота тромбоцитопении, вызванной блокаторамиGP IIb/IIIa рецепторов, в клинических исследованияхсоставляла от 0,5 до 5,6% в зависимости от типа пре-парата. Тяжелая тромбоцитопения может быть бессимп-томной и сопровождаться только небольшими крово-течениями в области сосудистого доступа. Большие кро-вотечения развиваются редко, но могут угрожать жиз-ни. У всех пациентов, получающих блокаторыGP IIb/IIIa рецепторов, рекомендуется измерить числотромбоцитов через 8 ч после начала инфузии или в слу-чае кровотечения. Если число тромбоцитов снижаетсяменее 10 000 в мкл, рекомендуется отменить блокато-ры GP IIb/IIIa рецепторов, а также НФГ или эноксапа-рин. При кровотечении рекомендуется трансфузиятромбоцитарной массы. Предлагалось также введениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с трансфу-зией тромбоцитарной массы.
Рекомендации по лечению геморрагических осложнений
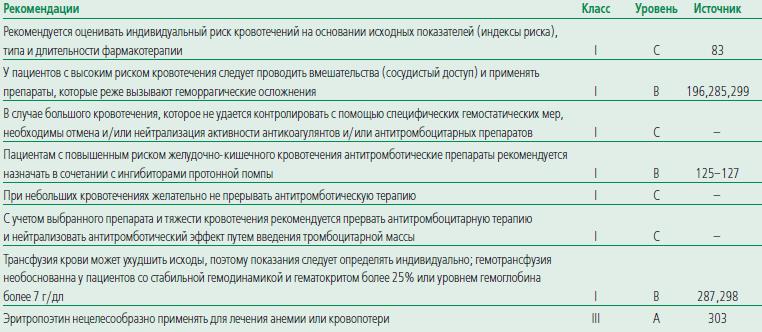 Рекомендации по ведению пациентов с тромбоцитопенией
Рекомендации по ведению пациентов с тромбоцитопенией
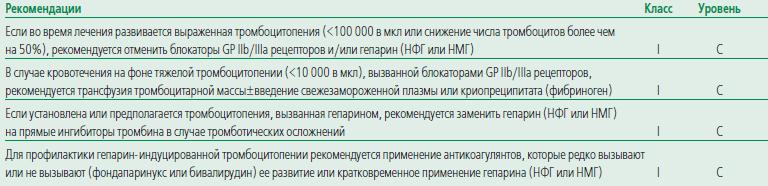 Вторичная профилактика
Вторичная профилактика имеет очень важное значе-ние, учитывая высокую частоту развития ишемическихосложнений после завершения острой фазы. Среди16 321 пациента с ОКС 20% больных госпитализиро-вались повторно, а 18% мужчин и 23% женщин в воз-расте старше 40 лет умерли в течение первого года на-блюдения [304]. Вторичная профилактика значитель-но улучшает отдаленный прогноз. Длительная профи-лактика после ОКС без подъема сегмента ST былаподробно описана в предыдущих рекомендациях, ко-торые сохраняют свое значение [3]. Кроме того, мето-ды вторичной профилактики обсуждаются в рекомен-дациях Европейского общества кардиологов по профи-лактике сердечно-сосудистых заболеваний в клиниче-ской практике [252]. Эти рекомендации распространяют-ся на всех пациентов группы риска и пациентов с сер-дечно-сосудистыми заболеваниями. Наличие послед-них указывает на высокий риск. В рекомендацияхАмериканской ассоциации сердца/Американской кол-легии кардиологов (AHA/ACC) по вторичной профилактике специально обсуждается тактика ведения па-циентов с ОКС (т.е. вторичная профилактика) [305]. Со-ответственно, в данном разделе рассматриваются толь-ко новые данные. Более подробную информацию см.в перечисленных документах. Цели вторичной профи-лактики и модификации сердечно-сосудистых факто-ров риска определены в таблице в приложении(www.escardio.org/guidelines).Необходимо использовать все меры вторичнойпрофилактики, обладающие доказанной эффектив-ностью: модификацию образа жизни, контроль факто-ров риска и медикаментозную терапию аспирином, бло-каторами P2Y12 рецепторов, бета-адреноблокаторами,статинами, ингибиторами АПФ или блокаторами ре-цепторов ангиотензина II и эплереноном. Недавнобыло показано, что у больных с ОКС без подъема сег-мента ST, у которых отсутствуют биомаркеры (нестабиль-ная стенокардия), ниже вероятность проведения адек-ватной вторичной профилактики по сравнению с тако-вой у пациентов с ИМ без подъема сегмента ST [59]. Сле-дует подчеркнуть, что вторичная профилактика эффек-тивна у всех пациентов с ОКС.Включение пациента в программу реабилитации/вторичной профилактики может привести к увеличе-нию приверженности и настоятельно рекомендуетсябольным среднего и высокого риска. Эффективность мервторичной профилактики была установлена у пациен-тов, принимавших участие в исследовании OASIS-5. Вэтом исследовании пациентам с ОКС без подъемасегмента рекомендовали соблюдать здоровую диету,регулярно выполнять физические нагрузки и прекра-тить курить в течение 30 дн после появления симпто-мов. У пациентов, соблюдавших диету и занимав-шихся физическими упражнениями, относительныйриск ИМ, инсульта и смерти снизился на 54% (ОШ 0,46;95% ДИ 0,38–0,57; p<0,0001), а у пациентов, бросив-ших курить, относительный риск ИМ снизился на 43%(ОШ 0,57; 95% ДИ 0,36–0,89; p=0,0145) [306]. В двухдругих исследованиях было подтверждено, что вторич-ная профилактика после ОКС позволяет снизить рисксмерти в той же степени, что и лечение в острую фазу[307,308].Ингибиторы АПФ и блокаторы рецепторов ангио-тензина II обладают доказанной эффективностью во вто-ричной профилактике [309,310] и в первую очередьпоказаны пациентам со сниженной функцией левогожелудочка. При плохой переносимости ингибиторовАПФ могут быть использованы блокаторы рецепторовангиотензина II. В крупном исследовании телмисартанпо эффективности по крайней мере не уступал рами-прилу и реже вызывал побочные эффекты [311]. Ком-бинированная терапия ингибиторами АПФ и блокато-рами рецепторов ангиотензина II обычно не рекомен-дуется. Рекомендации по применению ингибиторов АПФи блокаторов рецепторов ангиотензина II распростра-няются на пациентов, недавно перенесших ОКС безподъема сегмента ST.Антагонисты альдостерона, в частности эплеренон,снижали сердечно-сосудистую смертность после ИМ упациентов со сниженной функцией левого желудочка(фракция выброса ≤35%) даже при наличии легко вы-раженных симптомов [277]. Эти результаты можно экс-траполировать на пациентов со сниженной функциейлевого желудочка, перенесших ОКС без подъема сег-мента ST.Статины рекомендуются всем пациентам с ОКС безподъема сегмента ST (при отсутствии противопоказаний)независимо от уровней холестерина. Лечение рекомен-дуется начинать в течение 1-4 дн после госпитализации.Целевой уровень холестерина липопротеинов низкойплотности (ЛНП) составляет <2,6 ммоль/л (100 мг/дл).Эта рекомендация основывается на результатах крупных исследований аторвастатина и правастатина. При мета-анализе исследований ранней терапии статинами не былподтвержден благоприятный эффект в течение первых4 мес [312]. Однако при более длительном наблюдении(2 года) было отмечено снижение смертности и часто-ты сердечно-сосудистых исходов.Дополнительное снижение риска неблагоприятныхсобытий было выявлено при снижении уровня холесте-рина ЛНП менее 1,81 ммоль/л (70 мг/дл) [313]. Длядостижения максимального эффекта необходимы вы-сокие дозы (например, 80 мг аторвастатина).Эффект, по-видимому, не зависит от противовоспа-лительного действия статинов (снижение уровня вчСРБ)или дополняет его. Не установлено, характерен ли эф-фект аторвастатина и правастатина для всего класса ста-тинов.
Рекомендации по вторичной профилактике (отдельно см. антитромботические средства)
Вторичная профилактика
Вторичная профилактика имеет очень важное значе-ние, учитывая высокую частоту развития ишемическихосложнений после завершения острой фазы. Среди16 321 пациента с ОКС 20% больных госпитализиро-вались повторно, а 18% мужчин и 23% женщин в воз-расте старше 40 лет умерли в течение первого года на-блюдения [304]. Вторичная профилактика значитель-но улучшает отдаленный прогноз. Длительная профи-лактика после ОКС без подъема сегмента ST былаподробно описана в предыдущих рекомендациях, ко-торые сохраняют свое значение [3]. Кроме того, мето-ды вторичной профилактики обсуждаются в рекомен-дациях Европейского общества кардиологов по профи-лактике сердечно-сосудистых заболеваний в клиниче-ской практике [252]. Эти рекомендации распространяют-ся на всех пациентов группы риска и пациентов с сер-дечно-сосудистыми заболеваниями. Наличие послед-них указывает на высокий риск. В рекомендацияхАмериканской ассоциации сердца/Американской кол-легии кардиологов (AHA/ACC) по вторичной профилактике специально обсуждается тактика ведения па-циентов с ОКС (т.е. вторичная профилактика) [305]. Со-ответственно, в данном разделе рассматриваются толь-ко новые данные. Более подробную информацию см.в перечисленных документах. Цели вторичной профи-лактики и модификации сердечно-сосудистых факто-ров риска определены в таблице в приложении(www.escardio.org/guidelines).Необходимо использовать все меры вторичнойпрофилактики, обладающие доказанной эффектив-ностью: модификацию образа жизни, контроль факто-ров риска и медикаментозную терапию аспирином, бло-каторами P2Y12 рецепторов, бета-адреноблокаторами,статинами, ингибиторами АПФ или блокаторами ре-цепторов ангиотензина II и эплереноном. Недавнобыло показано, что у больных с ОКС без подъема сег-мента ST, у которых отсутствуют биомаркеры (нестабиль-ная стенокардия), ниже вероятность проведения адек-ватной вторичной профилактики по сравнению с тако-вой у пациентов с ИМ без подъема сегмента ST [59]. Сле-дует подчеркнуть, что вторичная профилактика эффек-тивна у всех пациентов с ОКС.Включение пациента в программу реабилитации/вторичной профилактики может привести к увеличе-нию приверженности и настоятельно рекомендуетсябольным среднего и высокого риска. Эффективность мервторичной профилактики была установлена у пациен-тов, принимавших участие в исследовании OASIS-5. Вэтом исследовании пациентам с ОКС без подъемасегмента рекомендовали соблюдать здоровую диету,регулярно выполнять физические нагрузки и прекра-тить курить в течение 30 дн после появления симпто-мов. У пациентов, соблюдавших диету и занимав-шихся физическими упражнениями, относительныйриск ИМ, инсульта и смерти снизился на 54% (ОШ 0,46;95% ДИ 0,38–0,57; p<0,0001), а у пациентов, бросив-ших курить, относительный риск ИМ снизился на 43%(ОШ 0,57; 95% ДИ 0,36–0,89; p=0,0145) [306]. В двухдругих исследованиях было подтверждено, что вторич-ная профилактика после ОКС позволяет снизить рисксмерти в той же степени, что и лечение в острую фазу[307,308].Ингибиторы АПФ и блокаторы рецепторов ангио-тензина II обладают доказанной эффективностью во вто-ричной профилактике [309,310] и в первую очередьпоказаны пациентам со сниженной функцией левогожелудочка. При плохой переносимости ингибиторовАПФ могут быть использованы блокаторы рецепторовангиотензина II. В крупном исследовании телмисартанпо эффективности по крайней мере не уступал рами-прилу и реже вызывал побочные эффекты [311]. Ком-бинированная терапия ингибиторами АПФ и блокато-рами рецепторов ангиотензина II обычно не рекомен-дуется. Рекомендации по применению ингибиторов АПФи блокаторов рецепторов ангиотензина II распростра-няются на пациентов, недавно перенесших ОКС безподъема сегмента ST.Антагонисты альдостерона, в частности эплеренон,снижали сердечно-сосудистую смертность после ИМ упациентов со сниженной функцией левого желудочка(фракция выброса ≤35%) даже при наличии легко вы-раженных симптомов [277]. Эти результаты можно экс-траполировать на пациентов со сниженной функциейлевого желудочка, перенесших ОКС без подъема сег-мента ST.Статины рекомендуются всем пациентам с ОКС безподъема сегмента ST (при отсутствии противопоказаний)независимо от уровней холестерина. Лечение рекомен-дуется начинать в течение 1-4 дн после госпитализации.Целевой уровень холестерина липопротеинов низкойплотности (ЛНП) составляет <2,6 ммоль/л (100 мг/дл).Эта рекомендация основывается на результатах крупных исследований аторвастатина и правастатина. При мета-анализе исследований ранней терапии статинами не былподтвержден благоприятный эффект в течение первых4 мес [312]. Однако при более длительном наблюдении(2 года) было отмечено снижение смертности и часто-ты сердечно-сосудистых исходов.Дополнительное снижение риска неблагоприятныхсобытий было выявлено при снижении уровня холесте-рина ЛНП менее 1,81 ммоль/л (70 мг/дл) [313]. Длядостижения максимального эффекта необходимы вы-сокие дозы (например, 80 мг аторвастатина).Эффект, по-видимому, не зависит от противовоспа-лительного действия статинов (снижение уровня вчСРБ)или дополняет его. Не установлено, характерен ли эф-фект аторвастатина и правастатина для всего класса ста-тинов.
Рекомендации по вторичной профилактике (отдельно см. антитромботические средства)
 Методы оценки качества лечения
Вариабельность применения рекомендуемых стра-тегий лечения определяет разницу неблагоприятных ис-ходов. В нескольких крупных регистрах было показа-но, что лечение пациентов с ОКС без подъема сегмен-та ST нередко не соответствует современным рекомен-дациям. Часто отмечается недостаточно активное при-менение рекомендуемых методов лечения. Выполне-ние рекомендаций приводило к улучшению исходов упациентов с ОКС, в том числе к снижению смертности[318]. Таким образом, повышение степени выполнениярекомендаций является приоритетной задачей. Коэф-фициенты риск/польза рекомендуемых методов лече-ния (NNT и NNH) изображены на рис. 4.Чтобы повысить качество лечения и свести к миниму-му его отклонения от рекомендаций, необходимо посто-янно контролировать показатели адекватности тактикиведения пациентов. Внедрение методов лечения, обладающих доказанной эффективностью (рис. 4), может при-вести к более выраженному улучшению сердечно-сосу-дистого здоровья населения по сравнению с таковым вклинических исследованиях, особенно при одновремен-ном применении нескольких эффективных методов.Подобные программы были успешно внедрены в несколь-ких странах, включая Швецию (регистр RIKS-HIA), Вели-кобританию (регистр MINAP), Германию, Италию и Из-раиль. Программы оценки качества лечения были так-же разработаны Европейским обществом кардиологови используются в рамках Euro Heart Survey Programme.Наиболее информативные показатели перечисле-ны в табл. 11.
Таблица 11. Критерии качества медицинской помощипациентам с ИМ без подъема сегмента ST
Методы оценки качества лечения
Вариабельность применения рекомендуемых стра-тегий лечения определяет разницу неблагоприятных ис-ходов. В нескольких крупных регистрах было показа-но, что лечение пациентов с ОКС без подъема сегмен-та ST нередко не соответствует современным рекомен-дациям. Часто отмечается недостаточно активное при-менение рекомендуемых методов лечения. Выполне-ние рекомендаций приводило к улучшению исходов упациентов с ОКС, в том числе к снижению смертности[318]. Таким образом, повышение степени выполнениярекомендаций является приоритетной задачей. Коэф-фициенты риск/польза рекомендуемых методов лече-ния (NNT и NNH) изображены на рис. 4.Чтобы повысить качество лечения и свести к миниму-му его отклонения от рекомендаций, необходимо посто-янно контролировать показатели адекватности тактикиведения пациентов. Внедрение методов лечения, обладающих доказанной эффективностью (рис. 4), может при-вести к более выраженному улучшению сердечно-сосу-дистого здоровья населения по сравнению с таковым вклинических исследованиях, особенно при одновремен-ном применении нескольких эффективных методов.Подобные программы были успешно внедрены в несколь-ких странах, включая Швецию (регистр RIKS-HIA), Вели-кобританию (регистр MINAP), Германию, Италию и Из-раиль. Программы оценки качества лечения были так-же разработаны Европейским обществом кардиологови используются в рамках Euro Heart Survey Programme.Наиболее информативные показатели перечисле-ны в табл. 11.
Таблица 11. Критерии качества медицинской помощипациентам с ИМ без подъема сегмента ST
 Рекомендации по оценке качества медицинскойпомощи
Рекомендации по оценке качества медицинскойпомощи
 Рис. 4. Польза и риск различных методов лечения
Рис. 4. Польза и риск различных методов лечения
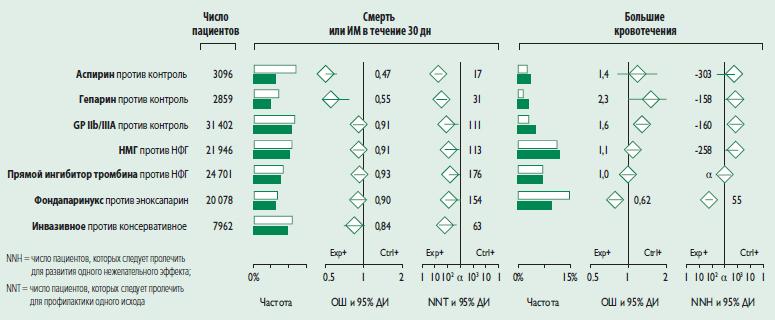 Стратегия ведения пациентов
В этом разделе обобщены этапы диагностики илечения, которые более подробно рассматриваются впредыдущих разделах. Эта информация поможет стан-дартизовать ведение пациентов и улучшить качество ока-зываемой им помощи. Однако у конкретных пациен-тов возможны отклонения от предлагаемой стратегиилечения, так как ОКС без подъема сегмента ST являет-ся неоднородным заболеванием с точки зрения рискасмерти, ИМ или повторного ИМ. В каждом случае врачдолжен принять индивидуальное решение с учетоманамнеза (сопутствующие заболевания, возраст и т.д.),клинического состояния, результатов первых исследо-ваний и доступных медикаментозных и немедика-ментозных методов лечения.
Первый этап: начальное обследованиеБоль или дискомфорт в груди и другие симптомы,заставляющие заподозрить ОКС. Они вынуждают пациента обратиться за медицинской помощью или госпитализироваться. Пациент с предпо-лагаемым диагнозом ОКС без подъема сегмента ST дол-жен быть немедленно осмотрен квалифицированнымврачом. Наиболее адекватная медицинская помощь мо-жет быть оказана в специализированных отделениях ин-тенсивной терапии [47].На первом этапе необходимо быстро установить ра-бочий диагноз и выбрать стратегию лечения на осно-вании следующих критериев: • характер боли в груди и результаты физического об-следования; • вероятность ИБС (возраст, факторы риска, ИМ, КШили ЧКВ в анамнезе);• ЭКГ (отклонения сегмента ST или другие измене-ния).На основании этих данных в течение первых 10 минможно установить один из следующих рабочих диаг-нозов:• ИМ с подъемом сегмента ST;• ОКС без подъема сегмента ST;• ОКС маловероятен.Лечение пациентов с ИМ с подъемом сегмента STрассматривается в соответствующих рекомендациях [2]. Относить пациентов к третьей категории (маловеро-ятный диагноз ОКС) следует осторожно при наличиидругой явной причины (например, травма грудной клет-ки). Методы лечения обобщены в табл. 12.При поступлении пациента в стационар необходи-мо взять кровь, результаты анализа которой должныбыть известны в течение 60 мин. Их используют на вто-ром этапе оказания помощи. Первые анализы кровивключают в себя тропонин Т или I, креатинин, гемогло-бин, глюкозу крови и число клеток крови в дополнениек стандартным биохимическим показателям.Если установлен диагноз ОКС без подъема сегмен-та ST, переходят ко второму этапу.
Таблица 12. Начальные лечебные меры
Стратегия ведения пациентов
В этом разделе обобщены этапы диагностики илечения, которые более подробно рассматриваются впредыдущих разделах. Эта информация поможет стан-дартизовать ведение пациентов и улучшить качество ока-зываемой им помощи. Однако у конкретных пациен-тов возможны отклонения от предлагаемой стратегиилечения, так как ОКС без подъема сегмента ST являет-ся неоднородным заболеванием с точки зрения рискасмерти, ИМ или повторного ИМ. В каждом случае врачдолжен принять индивидуальное решение с учетоманамнеза (сопутствующие заболевания, возраст и т.д.),клинического состояния, результатов первых исследо-ваний и доступных медикаментозных и немедика-ментозных методов лечения.
Первый этап: начальное обследованиеБоль или дискомфорт в груди и другие симптомы,заставляющие заподозрить ОКС. Они вынуждают пациента обратиться за медицинской помощью или госпитализироваться. Пациент с предпо-лагаемым диагнозом ОКС без подъема сегмента ST дол-жен быть немедленно осмотрен квалифицированнымврачом. Наиболее адекватная медицинская помощь мо-жет быть оказана в специализированных отделениях ин-тенсивной терапии [47].На первом этапе необходимо быстро установить ра-бочий диагноз и выбрать стратегию лечения на осно-вании следующих критериев: • характер боли в груди и результаты физического об-следования; • вероятность ИБС (возраст, факторы риска, ИМ, КШили ЧКВ в анамнезе);• ЭКГ (отклонения сегмента ST или другие измене-ния).На основании этих данных в течение первых 10 минможно установить один из следующих рабочих диаг-нозов:• ИМ с подъемом сегмента ST;• ОКС без подъема сегмента ST;• ОКС маловероятен.Лечение пациентов с ИМ с подъемом сегмента STрассматривается в соответствующих рекомендациях [2]. Относить пациентов к третьей категории (маловеро-ятный диагноз ОКС) следует осторожно при наличиидругой явной причины (например, травма грудной клет-ки). Методы лечения обобщены в табл. 12.При поступлении пациента в стационар необходи-мо взять кровь, результаты анализа которой должныбыть известны в течение 60 мин. Их используют на вто-ром этапе оказания помощи. Первые анализы кровивключают в себя тропонин Т или I, креатинин, гемогло-бин, глюкозу крови и число клеток крови в дополнениек стандартным биохимическим показателям.Если установлен диагноз ОКС без подъема сегмен-та ST, переходят ко второму этапу.
Таблица 12. Начальные лечебные меры
 Второй этап: подтверждение диагноза и оценкарискаПациентам с диагнозом ОКС без подъема сегментаST назначают антитромботические препараты внутри-венно и внутрь (табл. 13). Тактику дальнейшего веде-ния определяют с учетом дополнительной информации:• ответ на антиангинальную терапию;• биохимические показатели, особенно уровнитропонинов (при поступлении и через 6-9 ч) и другиебиомаркеры с учетом рабочих диагнозов (например,D-димер, МНП, NT-проМНП); если возможно приме-нение высокочувствительного метода анализа тропо-нинов, может быть внедрен протокол быстрого исклю-чения ОКС (3 ч) (рис. 5);• повторное или постоянное (если возможно) мо-ниторирование сегмента ST; • оценка риска ишемических исходов (индексGRACE);• эхокардиография;• дополнительные методы: рентгенография груднойклетки, КТ, МРТ или сцинтиграфия для дифференци-альной диагностики (например, расслоение стенкиаорты, тромбоэмболия легочной артерии и др.);• оценка риска кровотечений (индекс CRUSADE).На втором этапе подтверждают или исключаютдругие диагнозы, такие как тромбоэмболия легочнойартерии или аневризма аорты (см. табл. 4 и раздел 3.3.).Лечение выбирают индивидуально с учетом рисканеблагоприятных исходов, который оценивали при по-ступлении, а также в динамике с учетом клиническихсимптомов и результатов биохимических исследованийи визуализирующих методов.Оценка риска является важным компонентом про-цесса принятия решения. Риск следует постоянно оце-нивать в динамике. Необходимо определять рискишемических исходов и геморрагических осложнений.Факторы риска часто перекрещиваются, поэтому у па-циентов с высоким риском ишемических исходов рисккровотечений часто также высокий. Важное значениеимеет выбор адекватной терапии (двойная или трой-ная антитромбоцитарная терапия или антикоагулянты),а также доз лекарственных препаратов и доступа для ан-гиографии. Особое внимание следует уделять дисфунк-ции почек, которая особенно часто встречается у пожи-лых людей и пациентов с диабетом. Методы медика-ментозной терапии суммированы в табл. 13.
Таблица 13. Методы лечения, которые рекомендуютсяв тех случаях, когда диагноз ОКСпредставляется вероятным
Второй этап: подтверждение диагноза и оценкарискаПациентам с диагнозом ОКС без подъема сегментаST назначают антитромботические препараты внутри-венно и внутрь (табл. 13). Тактику дальнейшего веде-ния определяют с учетом дополнительной информации:• ответ на антиангинальную терапию;• биохимические показатели, особенно уровнитропонинов (при поступлении и через 6-9 ч) и другиебиомаркеры с учетом рабочих диагнозов (например,D-димер, МНП, NT-проМНП); если возможно приме-нение высокочувствительного метода анализа тропо-нинов, может быть внедрен протокол быстрого исклю-чения ОКС (3 ч) (рис. 5);• повторное или постоянное (если возможно) мо-ниторирование сегмента ST; • оценка риска ишемических исходов (индексGRACE);• эхокардиография;• дополнительные методы: рентгенография груднойклетки, КТ, МРТ или сцинтиграфия для дифференци-альной диагностики (например, расслоение стенкиаорты, тромбоэмболия легочной артерии и др.);• оценка риска кровотечений (индекс CRUSADE).На втором этапе подтверждают или исключаютдругие диагнозы, такие как тромбоэмболия легочнойартерии или аневризма аорты (см. табл. 4 и раздел 3.3.).Лечение выбирают индивидуально с учетом рисканеблагоприятных исходов, который оценивали при по-ступлении, а также в динамике с учетом клиническихсимптомов и результатов биохимических исследованийи визуализирующих методов.Оценка риска является важным компонентом про-цесса принятия решения. Риск следует постоянно оце-нивать в динамике. Необходимо определять рискишемических исходов и геморрагических осложнений.Факторы риска часто перекрещиваются, поэтому у па-циентов с высоким риском ишемических исходов рисккровотечений часто также высокий. Важное значениеимеет выбор адекватной терапии (двойная или трой-ная антитромбоцитарная терапия или антикоагулянты),а также доз лекарственных препаратов и доступа для ан-гиографии. Особое внимание следует уделять дисфунк-ции почек, которая особенно часто встречается у пожи-лых людей и пациентов с диабетом. Методы медика-ментозной терапии суммированы в табл. 13.
Таблица 13. Методы лечения, которые рекомендуютсяв тех случаях, когда диагноз ОКСпредставляется вероятным
 Рис. 5. Алгоритм быстрого исключения ОКС с помощью высокочувствительного метода определения тропонина
Рис. 5. Алгоритм быстрого исключения ОКС с помощью высокочувствительного метода определения тропонина
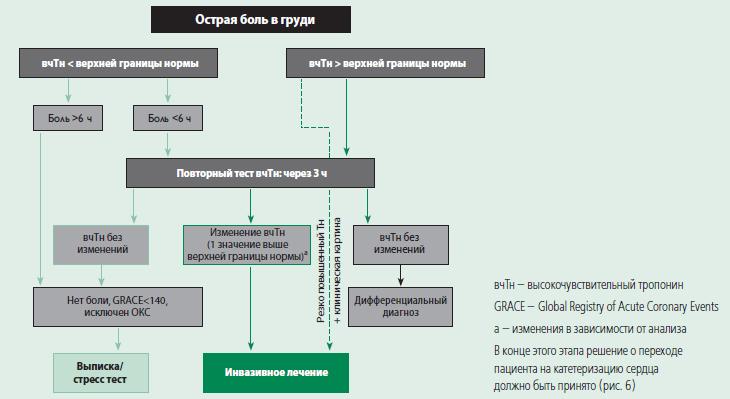 Третий этап: инвазивная стратегия• Катетеризация сердца с последующей реваскуля-ризацией предупреждали развитие рецидивирующейишемии и/или улучшали ближайший или отдаленныйпрогноз. Выделены несколько факторов риска (повы-шение уровня тропонина, депрессия сегмента ST, по-чечная недостаточность и др.), которые позволяютпредсказать отдаленную эффективность инвазивнойстратегии. В зависимости от степени повышения рис-ка ангиография может быть проведена в следующиесроки (рис. 6):• Инвазивное лечение (<72 ч)— неотложное (<120 мин);— раннее (<24 ч).• Первичная консервативная стратегия.Оптимальные сроки вмешательства зависят от про-филя риска конкретного пациента и могут быть выбра-ны на основании нескольких показателей.Неотложная инвазивная стратегия (в течение первых 120 минпосле первого контакта с врачом)Эта стратегия обоснованна у пациентов с оченьвысоким риском:• Рефрактерная стенокардия (включая формирую-щийся ИМ без отклонений сегмента ST).• Рецидивирующая стенокардия, несмотря на анти-ангинальную терапию, в сочетании с депрессией сег-мента ST (2 мм) или глубокими отрицательными зуб-цами Т.• Клинические симптомы сердечной недостаточно-сти или нестабильная гемодинамика (шок). • Угрожающие жизни аритмии (желудочковая тахи-кардия или фибрилляция желудочков).Перед катетеризацией таким пациентам можноввести блокатор GP IIb/IIIa рецепторов (эптифибатидили тирофибан). Список антитромботических препа-ратов, которые применяют перед ЧКВ, приведен втабл. 14.
Рис. 6. Алгоритм принятия решения при ОКС
Третий этап: инвазивная стратегия• Катетеризация сердца с последующей реваскуля-ризацией предупреждали развитие рецидивирующейишемии и/или улучшали ближайший или отдаленныйпрогноз. Выделены несколько факторов риска (повы-шение уровня тропонина, депрессия сегмента ST, по-чечная недостаточность и др.), которые позволяютпредсказать отдаленную эффективность инвазивнойстратегии. В зависимости от степени повышения рис-ка ангиография может быть проведена в следующиесроки (рис. 6):• Инвазивное лечение (<72 ч)— неотложное (<120 мин);— раннее (<24 ч).• Первичная консервативная стратегия.Оптимальные сроки вмешательства зависят от про-филя риска конкретного пациента и могут быть выбра-ны на основании нескольких показателей.Неотложная инвазивная стратегия (в течение первых 120 минпосле первого контакта с врачом)Эта стратегия обоснованна у пациентов с оченьвысоким риском:• Рефрактерная стенокардия (включая формирую-щийся ИМ без отклонений сегмента ST).• Рецидивирующая стенокардия, несмотря на анти-ангинальную терапию, в сочетании с депрессией сег-мента ST (2 мм) или глубокими отрицательными зуб-цами Т.• Клинические симптомы сердечной недостаточно-сти или нестабильная гемодинамика (шок). • Угрожающие жизни аритмии (желудочковая тахи-кардия или фибрилляция желудочков).Перед катетеризацией таким пациентам можноввести блокатор GP IIb/IIIa рецепторов (эптифибатидили тирофибан). Список антитромботических препа-ратов, которые применяют перед ЧКВ, приведен втабл. 14.
Рис. 6. Алгоритм принятия решения при ОКС
 Таблица 14. Антитромботические препаратыперед ЧКВ
Таблица 14. Антитромботические препаратыперед ЧКВ
 Ранняя инвазивная стратегия (в течение первых 24 ч послепервого контакта с врачом)Большинство пациентов первоначально отвечают наантиангинальную терапию, однако у них отмечается повышенный риск и необходима ангиография с реваску-ляризацией. Пациентам с высоким риском (индексGRACE>140 и/или наличие по крайней мере одногокритерия высокого риска; табл. 9) инвазивное обсле-дование следует провести в течение 24 ч.Инвазивная стратегия (в течение 72 ч после первого контакта сврачом)У пациентов с более низким риском, у которых нерецидивируют симптомы, ангиография может быть про-ведена в течение 72 ч. Таким образом, им следует про-вести плановое инвазивное обследование при первойвозможности с учетом локальных условий.Консервативная стратегия (ангиография не проводится иливыполняется в плановом порядке)При отсутствии перечисленных ниже критериевриск является низким, поэтому раннее инвазивноеобследование не требуется:• отсутствие рецидивирующей боли в груди;• отсутствие сердечной недостаточности;• отсутствие изменений на первой или второй(через 6-9 ч) ЭКГ;• нормальный уровень тропонина (при поступлениии через 6-9 ч);• отсутствие стресс-индуцированной ишемии.Пациентам с низким риском (см. раздел 4.4.) пока-зано консервативное ведение. Последующее лечениевыбирают с учетом тактики ведения пациентов со ста-бильной ИБС [319]. Перед выпиской из стационара не-обходимо провести стресс-пробу с целью планирова-ния дальнейшего ведения и оценки необходимости вплановой ангиографии.
Таблица 15. Рекомендуемые методы леченияперед выпиской
Ранняя инвазивная стратегия (в течение первых 24 ч послепервого контакта с врачом)Большинство пациентов первоначально отвечают наантиангинальную терапию, однако у них отмечается повышенный риск и необходима ангиография с реваску-ляризацией. Пациентам с высоким риском (индексGRACE>140 и/или наличие по крайней мере одногокритерия высокого риска; табл. 9) инвазивное обсле-дование следует провести в течение 24 ч.Инвазивная стратегия (в течение 72 ч после первого контакта сврачом)У пациентов с более низким риском, у которых нерецидивируют симптомы, ангиография может быть про-ведена в течение 72 ч. Таким образом, им следует про-вести плановое инвазивное обследование при первойвозможности с учетом локальных условий.Консервативная стратегия (ангиография не проводится иливыполняется в плановом порядке)При отсутствии перечисленных ниже критериевриск является низким, поэтому раннее инвазивноеобследование не требуется:• отсутствие рецидивирующей боли в груди;• отсутствие сердечной недостаточности;• отсутствие изменений на первой или второй(через 6-9 ч) ЭКГ;• нормальный уровень тропонина (при поступлениии через 6-9 ч);• отсутствие стресс-индуцированной ишемии.Пациентам с низким риском (см. раздел 4.4.) пока-зано консервативное ведение. Последующее лечениевыбирают с учетом тактики ведения пациентов со ста-бильной ИБС [319]. Перед выпиской из стационара не-обходимо провести стресс-пробу с целью планирова-ния дальнейшего ведения и оценки необходимости вплановой ангиографии.
Таблица 15. Рекомендуемые методы леченияперед выпиской
 Четвертый этап: методы реваскуляризацииЕсли при ангиографии выявлены атероматозныеизменения, однако отсутствует критический стеноз ко-ронарных артерий, показана медикаментозная терапия.Необходимо пересмотреть диагноз ОКС без подъема сег-мента ST с учетом других возможных причин появлениясимптомов. Однако отсутствие критического стеноза неисключает диагноз ОКС, если клинические симптомы ука-зывают на ишемическую боль в груди и определяютсябиомаркеры. В этом случае пациенты должны получатьлечение в соответствии с рекомендациями по ведениюпациентов с ОКС без подъема сегмента ST.Рекомендации по выбору метода реваскуляризацииу пациентов с ОКС без подъема сегмента ST соответ-ствуют рекомендациям по выбору метода плановоговмешательства. У пациента со стенозом одной коронар-ной артерии методом выбора является ЧКВ. У пациен-тов с поражением нескольких сосудов выбор между ЧКВи КШ должен быть индивидуальным в соответствии спротоколом лечебного учреждения. В некоторых слу-чаях оправданно ЧКВ на ведущей артерии и последую-щее плановое шунтирование других пораженных со-судов с учетом результатов оценки ишемии и/илифункционального резерва кровотока.Во время ЧКВ не следует менять антикоагулянты. Па-циентам, получавшим фондапаринукс, перед ЧКВ сле-дует добавить НФГ. Применение блокатора GP IIb/IIIaрецепторов оправданно при повышенном уровне тро-понинов или наличии ангиографических признаковтромба. Если планируется КШ, следует отменить бло-каторы P2Y12 рецепторов и отложить операцию, еслиэто позволяют клиническое состояние и ангиографиче-ские данные.Если ангиография указывает на невозможность ре-васкуляризации в связи с распространенностью и/илилокализацией поражений, необходимо усилить меди-каментозную терапию и назначить меры вторичной про-филактики.
Пятый этап: выписка из стационара и наблюдениепосле выпискиХотя большинство нежелательных событий у паци-ентов с ОКС без подъема сегмента ST наблюдают на ран-нем этапе, риск ИМ или смерти остается повышеннымв течение нескольких мес. После ранней реваскуляри-зации риск развития угрожающих жизни аритмийнизкий (2,5%); 80% из них развиваются в течение пер-вых 12 ч после появления симптомов [320]. Соответ-ственно, продолжение мониторирования после24-48 ч обычно не требуется. Пациенты с ОКС безподъема сегмента ST должны находиться в стациона-ре в течение по крайней мере 24 ч после успешного стен-тирования ведущего стеноза. Всем пациентам показа-ны интенсивная модификация риска и улучшение об-раза жизни (см. раздел 5.6.). Включение пациента в про-грамму реабилитации после выписки повышает при-верженность и может способствовать модификациифакторов риска. Необходимые меры профилактикипосле выписки из стационара указаны в табл. 15.
Литература
1. Murray CJ, Lopez AD. Alternative projections of mortality and disability by cause 1990–2020: Global Burden ofDisease Study. Lancet 1997;349:1498–1504. 2. Van deWerf F, Bax J, Betriu A, Blomstrom-Lundqvist C, Crea F, Falk V, Filippatos G, Fox K, Huber K, Kastrati A,Rosengren A, Steg PG, Tubaro M, Verheugt F, Weidinger F, Weis M. Management of acute myocardial infarctionin patients presenting with persistent ST-segment elevation: the Task Force on the Management of ST-SegmentElevation Acute Myocardial Infarction of the European Society of Cardiology. Eur Heart J 2008;29:2909–2945.3. Bassand JP, Hamm CW, Ardissino D, Boersma E, Budaj A, Fernandez-Aviles F, Fox KA, Hasdai D, Ohman EM,Wallentin L, Wijns W. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronarysyndromes. Eur Heart J 2007;28:1598–1660.4. Yeh RW, Sidney S, Chandra M, Sorel M, Selby JV, Go AS. Population trends in the incidence and outcomes of acutemyocardial infarction. N Engl J Med 2010;362:2155–2165.5. Fox KA, Eagle KA, Gore JM, Steg PG, Anderson FA. The Global Registry of Acute Coronary Events, 1999 to 2009—GRACE. Heart 2010;96:1095–1101.6. Savonitto S, Ardissino D, Granger CB, Morando G, Prando MD, Mafrici A, Cavallini C, Melandri G, Thompson TD,Vahanian A, Ohman EM, Califf RM, Van de Werf F, Topol EJ. Prognostic value of the admission electrocardiogramin acute coronary syndromes. JAMA 1999;281:707–713.7. Mandelzweig L, Battler A, Boyko V, Bueno H, Danchin N, Filippatos G, Gitt A, Hasdai D, Hasin Y, Marrugat J,Van de Werf F, Wallentin L, Behar S. The second Euro Heart Survey on acute coronary syndromes: characteristics,treatment, and outcome of patients with ACS in Europe and the Mediterranean Basin in 2004. Eur Heart J2006;27:2285–2293.8. Terkelsen CJ, Lassen JF, Norgaard BL, Gerdes JC, Jensen T, Gotzsche LB, Nielsen TT, Andersen HR. Mortality ratesin patients with ST-elevation vs. non-ST-elevation acute myocardial infarction: observations from an unselectedcohort. Eur Heart J 2005;26:18–26.9. Hamm CW, Mo¨llmann H, Bassand JP, Van deWerf F. Acute coronary syndrome. In: Camm AJ, Lu¨scher TF, SerruysPW, eds. The ESC Textbook of Cardiovascular Medicine. 2nd ed. Oxford: Oxford University Press; 2009.10. Stone GW, Maehara A, Lansky AJ, de Bruyne B, Cristea E, Mintz GS, Mehran R, McPherson J, Farhat N, MarsoSP, Parise H, Templin B, White R, Zhang Z, Serruys PW. A prospective natural-history study of coronary atherosclerosis.N Engl J Med 2011;364:226–235.11. Campeau L. Grading of angina pectoris. Circulation 1976;54:522–523.12. van Domburg RT, van Miltenburg-van Zijl AJ, Veerhoek RJ, Simoons ML. Unstable angina: good long-term outcomeafter a complicated early course. J Am Coll Cardiol 1998;31:1534–1539.13. Canto JG, Fincher C, Kiefe CI, Allison JJ, Li Q, Funkhouser E, Centor RM, Selker HP,Weissman NW. Atypical presentationsamong Medicare beneficiaries with unstable angina pectoris. Am J Cardiol 2002;90:248–253.14. Culic V, Eterovic D, Miric D, Silic N. Symptom presentation of acute myocardial infarction: influence of sex, age,and risk factors. Am Heart J 2002;144:1012–1017.15. Brieger D, Eagle KA, Goodman SG, Steg PG, Budaj A, White K, Montalescot G. Acute coronary syndromeswithout chest pain, an underdiagnosed and undertreated high-risk group: insights from the Global Registry ofAcute Coronary Events. Chest 2004;126:461–469.16. Lev EI, Battler A, Behar S, Porter A, Haim M, Boyko V, Hasdai D. Frequency, characteristics, and outcome of patientshospitalized with acute coronary syndromes with undetermined electrocardiographic patterns. Am J Cardiol2003;91:224–227.17. Diercks DB, Peacock WF, Hiestand BC, Chen AY, Pollack CV Jr., Kirk JD, Smith SC Jr., Gibler WB, Ohman EM,Blomkalns AL, Newby LK, Hochman JS, Peterson ED, Roe MT. Frequency and consequences of recording an electrocardiogram.10 min after arrival in an emergency room in non-ST-segment elevation acute coronary syndromes(from the CRUSADE Initiative). Am J Cardiol 2006;97:437–442.18. Thygesen K, Alpert JS, White HD, Jaffe AS, Apple FS, Galvani M, Katus HA, Newby LK, Ravkilde J, Chaitman B,Clemmensen PM, Dellborg M, Hod H, Porela P, Underwood R, Bax JJ, Beller GA, Bonow R, Van der Wall EE, BassandJP, Wijns W, Ferguson TB, Steg PG, Uretsky BF, Williams DO, Armstrong PW, Antman EM, Fox KA, HammCW, Ohman EM, Simoons ML, Poole-Wilson PA, Gurfinkel EP, Lopez-Sendon JL, Pais P, Mendis S, Zhu JR, WallentinLC, Fernandez-Aviles F, Fox KM, Parkhomenko AN, Priori SG, Tendera M, Voipio-Pulkki LM, Vahanian A,Camm AJ, De Caterina R, Dean V, Dickstein K, Filippatos G, Funck-Brentano C, Hellemans I, Kristensen SD, Mc-Gregor K, Sechtem U, Silber S, Widimsky P, Zamorano JL, Morais J, Brener S, Harrington R, Morrow D, Lim M,Martinez-Rios MA, Steinhubl S, Levine GN, Gibler WB, Goff D, Tubaro M, Dudek D, Al-Attar N. Universal definitionof myocardial infarction. Circulation 2007;116:2634–2653.19. Okamatsu K, Takano M, Sakai S, Ishibashi F, Uemura R, Takano T, Mizuno K. Elevated troponin T levels and lesioncharacteristics in non-ST-elevation acute coronary syndromes. Circulation 2004;109:465–470.20. Keller T, Zeller T, Peetz D, Tzikas S, Roth A, Czyz E, Bickel C, Baldus S, Warnholtz A, Frohlich M, Sinning CR,Eleftheriadis MS, Wild PS, Schnabel RB, Lubos E, Jachmann N, Genth-Zotz S, Post F, Nicaud V, Tiret L, LacknerKJ, Munzel TF, Blankenberg S. Sensitive troponin I assay in early diagnosis of acute myocardial infarction. N EnglJ Med 2009;361:868–877.21. Reichlin T, Hochholzer W, Bassetti S, Steuer S, Stelzig C, Hartwiger S, Biedert S, Schaub N, Buerge C, Potocki M,Noveanu M, Breidthardt T, Twerenbold R, Winkler K, Bingisser R, Mueller C. Early diagnosis of myocardial infarctionwith sensitive cardiac troponin assays. N Engl J Med 2009;361:858–867.22. Giannitsis E, Becker M, Kurz K, Hess G, Zdunek D, Katus HA. High-sensitivity cardiac troponin T for early predictionof evolving non-ST-segment elevation myocardial infarction in patients with suspected acute coronarysyndrome and negative troponin results on admission. Clin Chem 2010;56:642–650.23. Weber M, Bazzino O, Estrada JJN, Miguel R, Salzberg S, Fuselli JJ, Liebetrau C, Woelken M, Moellmann H, NefH, Hamm C. Improved diagnostic and prognostic performance of a new high-sensitive troponin T assay in patientswith acute coronary syndrome. Am Heart J 2011;162:81–88.24. Omland T, de Lemos JA, Sabatine MS, Christophi CA, Rice MM, Jablonski KA, Tjora S, Domanski MJ, Gersh BJ,Rouleau JL, Pfeffer MA, Braunwald E. A sensitive cardiac troponin T assay in stable coronary artery disease. NEngl J Med 2009;361:2538–2547.25. de Lemos JA, Drazner MH, Omland T, Ayers CR, Khera A, Rohatgi A, Hashim I, Berry JD, Das SR, Morrow DA,McGuire DK. Association of troponin T detected with a highly sensitive assay and cardiac structure and mortalityrisk in the general population. JAMA 2010;304:2503–2512.26. Otsuka T, Kawada T, Ibuki C, Seino Y. Association between high-sensitivity cardiac troponin T levels and thepredicted cardiovascular risk in middle-aged men without overt cardiovascular disease. Am Heart J2010;159:972–978.27. Thygesen K, Mair J, Katus H, Plebani M, Venge P, Collinson P, Lindahl B, Giannitsis E, Hasin Y, Galvani M, TubaroM, Alpert JS, Biasucci LM, Koenig W, Mueller C, Huber K, Hamm C, Jaffe AS. Recommendations for the use ofcardiac troponin measurement in acute cardiac care. Eur Heart J 2010;31:2197–2204.28. Apple FS, Murakami MM, Pearce LA, Herzog CA. Predictive value of cardiac troponin I and T for subsequentdeath in end-stage renal disease. Circulation 2002;106:2941–2945.29. Aviles RJ, Askari AT, Lindahl B, Wallentin L, Jia G, Ohman EM, Mahaffey KW, Newby LK, Califf RM, Simoons ML,Topol EJ, Berger P, Lauer MS. Troponin T levels in patients with acute coronary syndromes, with or without renaldysfunction. N Engl J Med 2002;346:2047–2052.30. Hamm CW, Goldmann BU, Heeschen C, Kreymann G, Berger J, Meinertz T. Emergency room triage of patientswith acute chest pain by means of rapid testing for cardiac troponin T or troponin I. N Engl J Med1997;337:1648–1653.31. Wu AH, Apple FS, Gibler WB, Jesse RL, Warshaw MM, Valdes R Jr. National Academy of Clinical BiochemistryStandards of Laboratory Practice: recommendations for the use of cardiac markers in coronary artery diseases.Clin Chem 1999;45:1104–1121.32. Than M, Cullen L, Reid CM, Lim SH, Aldous S, Ardagh MW, Peacock WF, Parsonage WA, Ho HF, Ko HF, KasliwalRR, Bansal M, Soerianata S, Hu D, Ding R, Hua Q, Seok-Min K, Sritara P, Sae-Lee R, Chiu TF, Tsai KC, Chu FY, ChenWK, Chang WH, Flaws DF, George PM, Richards AM. A 2-h diagnostic protocol to assess patients with chestpain symptoms in the Asia-Pacific region (ASPECT): a prospective observational validation study. Lancet2011;377:1077–1084.33. Cheitlin MD, Armstrong WF, Aurigemma GP, Beller GA, Bierman FZ, Davis JL, Douglas PS, Faxon DP, Gillam LD,Kimball TR, Kussmaul WG, Pearlman AS, Philbrick JT, Rakowski H, Thys DM, Antman EM, Smith SC Jr., AlpertJS, Gregoratos G, Anderson JL, Hiratzka LF, Hunt SA, Fuster V, Jacobs AK, Gibbons RJ, Russell RO. ACC/AHA/ASE2003 guideline update for the clinical application of echocardiography: summary article: a report of the AmericanCollege of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASE Committeeto Update the 1997 Guidelines for the Clinical Application of Echocardiography). Circulation2003;108:1146–1162.34. Nucifora G, Badano LP, Sarraf-Zadegan N, Karavidas A, Trocino G, Scaffidi G, Pettinati G, Astarita C, VysniauskasV, Gregori D, Ilerigelen B, Marinigh R, Fioretti PM. Comparison of early dobutamine stress echocardiography andexercise electrocardiographic testing for management of patients presenting to the emergency departmentwith chest pain. Am J Cardiol 2007;100:1068–1073.35. Kwong RY, Schussheim AE, Rekhraj S, Aletras AH, Geller N, Davis J, Christian TF, Balaban RS, Arai AE. Detectingacute coronary syndrome in the emergency department with cardiac magnetic resonance imaging. Circulation2003;107:531–537.36. Udelson JE, Beshansky JR, Ballin DS, Feldman JA, Griffith JL, Handler J, Heller GV, Hendel RC, Pope JH, RuthazerR, Spiegler EJ, Woolard RH, Selker HP. Myocardial perfusion imaging for evaluation and triage of patientswith suspected acute cardiac ischemia: a randomized controlled trial. JAMA 2002;288:2693–2700.37. Hoffmann U, Bamberg F, Chae CU, Nichols JH, Rogers IS, Seneviratne SK, Truong QA, Cury RC, Abbara S, ShapiroMD, Moloo J, Butler J, Ferencik M, Lee H, Jang IK, Parry BA, Brown DF, Udelson JE, Achenbach S, Brady TJ,Nagurney JT. Coronary computed tomography angiography for early triage of patients with acute chest pain:the ROMICAT (Rule Out Myocardial Infarction using Computer Assisted Tomography) trial. J Am Coll Cardiol2009;53:1642–1650.38. Rubinshtein R, Halon DA, Gaspar T, Jaffe R, Karkabi B, Flugelman MY, Kogan A, Shapira R, Peled N, Lewis BS.Usefulness of 64-slice cardiac computed tomographic angiography for diagnosing acute coronary syndromesand predicting clinical outcome in emergency department patients with chest pain of uncertain origin. Circulation2007;115:1762–1768.39. Meijboom WB, Mollet NR, Van Mieghem CA, Weustink AC, Pugliese F, van Pelt N, Cademartiri F, Vourvouri E,de Jaegere P, Krestin GP, de Feyter PJ 64-Slice CT coronary angiography in patients with non-ST elevation acutecoronary syndrome. Heart 2007;93:1386–1392.40. Hollander JE, Chang AM, Shofer FS, Collin MJ, Walsh KM, McCusker CM, Baxt WG, Litt HI. One-year outcomesfollowing coronary computerized tomographic angiography for evaluation of emergency department patientswith potential acute coronary syndrome. Acad Emerg Med 2009;16:693–698.41. Chang SA, Choi SI, Choi EK, Kim HK, Jung JW, Chun EJ, Kim KS, Cho YS, Chung WY, Youn TJ, Chae IH, Choi DJ,Chang HJ. Usefulness of 64-slice multidetector computed tomography as an initial diagnostic approach in patientswith acute chest pain. Am Heart J 2008;156:375–383.42. Effects of tissue plasminogen activator and a comparison of early invasive and conservative strategies in unstableangina and non-Q-wave myocardial infarction. Results of the TIMI IIIB Trial. Thrombolysis in Myocardial Ischemia.Circulation 1994;89:1545–1556.43. Invasive compared with non-invasive treatment in unstable coronary-artery disease: FRISC II prospective randomisedmulticentre study. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators.Lancet 1999;354:708–715.44. Tonino PA, De Bruyne B, Pijls NH, Siebert U, Ikeno F, van’ t Veer M, Klauss V, Manoharan G, Engstrom T, OldroydKG, Ver Lee PN, MacCarthy PA, Fearon WF. Fractional flow reserve versus angiography for guiding percutaneouscoronary intervention. N Engl J Med 2009;360:213–224.45. Jolly SS, Yusuf S, Cairns J, Niemela K, Xavier D, Widimsky P, Budaj A, Niemela M, Valentin V, Lewis BS, AvezumA, Steg PG, Rao SV, Gao P, Afzal R, Joyner CD, Chrolavicius S, Mehta SR. Radial versus femoral access for coronaryangiography and intervention in patients with acute coronary syndromes (RIVAL): a randomised, parallelgroup, multicentre trial. Lancet 2011;377:1409–1420.46. Hasdai D, Lev EI, Behar S, Boyko V, Danchin N, Vahanian A, Battler A. Acute coronary syndromes in patients withpre-existing moderate to severe valvular disease of the heart: lessons from the Euro-Heart Survey of acute coronarysyndromes. Eur Heart J 2003;24:623–629.47. Hasin Y, Danchin N, Filippatos GS, Heras M, Janssens U, Leor J, Nahir M, Parkhomenko A, Thygesen K, TubaroM, Wallentin LC, Zakke I. Recommendations for the structure, organization, and operation of intensive cardiaccare units. Eur Heart J 2005;26:1676–1682.48. Granger CB, Goldberg RJ, Dabbous O, Pieper KS, Eagle KA, Cannon CP, Van De Werf F, Avezum A, GoodmanSG, Flather MD, Fox KA. Predictors of hospital mortality in the global registry of acute coronary events. Arch InternMed 2003;163:2345–2353.49. Antman EM, Cohen M, Bernink PJ, McCabe CH, Horacek T, Papuchis G, Mautner B, Corbalan R, Radley D,Braunwald E. The TIMI risk score for unstable angina/non-ST elevation MI: a method for prognostication andtherapeutic decision making. JAMA 2000;284:835–842.50. Fox KA, Dabbous OH, Goldberg RJ, Pieper KS, Eagle KA, Van de Werf F, Avezum A, Goodman SG, Flather MD,Anderson FA Jr., Granger CB. Prediction of risk of death and myocardial infarction in the six months after presentationwith acute coronary syndrome: prospective multinational observational study (GRACE). BMJ2006;333:1091. 51. Carrillo X, Curos A, Muga R, Serra J, Sanvisens A, Bayes-Genis A. Acute coronary syndrome and cocaine use:8-year prevalence and inhospital outcomes. Eur Heart J 2011;32:1244–1250.52. Holmvang L, Clemmensen P, Lindahl B, Lagerqvist B, Venge P, Wagner G, Wallentin L, Grande P. Quantitativeanalysis of the admission electrocardiogram identifies patients with unstable coronary artery disease who benefitthe most from early invasive treatment. J Am Coll Cardiol 2003;41:905–915.53. Kaul P, Fu Y, Chang WC, Harrington RA, Wagner GS, Goodman SG, Granger CB, Moliterno DJ, Van de Werf F,Califf RM, Topol EJ, Armstrong PW. Prognostic value of ST segment depression in acute coronary syndromes:insights from PARAGON-A applied to GUSTO-IIb. PARAGON-A and GUSTO IIb Investigators. Platelet IIb/IIIa Antagonismfor the Reduction of Acute Global Organization Network. J Am Coll Cardiol 2001;38:64–71.54. Nyman I, Wallentin L, Areskog M, Areskog NH, Swahn E. Risk stratification by early exercise testing after anepisode of unstable coronary artery disease. The RISC Study Group. Int J Cardiol 1993;39:131–142.55. Amsterdam EA, Kirk JD, Diercks DB, Lewis WR, Turnipseed SD. Immediate exercise testing to evaluate low-riskpatients presenting to the emergency department with chest pain. J Am Coll Cardiol 2002;40:251–256.56. Scirica BM, Morrow DA, Budaj A, Dalby AJ, Mohanavelu S, Qin J, Aroesty J, Hedgepeth CM, Stone PH, BraunwaldE. Ischemia detected on continuous electrocardiography after acute coronary syndrome: observationsfrom the MERLIN-TIMI 36 (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST-Elevation AcuteCoronary Syndrome-Thrombolysis In Myocardial Infarction 36) trial. J Am Coll Cardiol 2009;53:1411–1421.57. Akkerhuis KM, Klootwijk PA, Lindeboom W, Umans VA, Meij S, Kint PP, Simoons ML. Recurrent ischaemia duringcontinuous multilead ST-segment monitoring identifies patients with acute coronary syndromes at highrisk of adverse cardiac events; meta-analysis of three studies involving 995 patients. Eur Heart J2001;22:1997–2006.58. Antman EM, Tanasijevic MJ, Thompson B, Schactman M, McCabe CH, Cannon CP, Fischer GA, Fung AY, ThompsonC, Wybenga D, Braunwald E. Cardiac-specific troponin I levels to predict the risk of mortality in patients withacute coronary syndromes. N Engl J Med 1996;335:1342–1349.59. Kontos MC, de Lemos JA, Ou FS, Wiviott SD, Foody JM, Newby LK, Chen A, Roe MT. Troponin-positive, MBnegativepatients with non-ST-elevation myocardial infarction: an undertreated but high-risk patient group:results from the National Cardiovascular Data Registry Acute Coronary Treatment and Intervention OutcomesNetwork—Get With The Guidelines (NCDR ACTION-GWTG) Registry. Am Heart J 2010;160:819–825.60. James SK, Lindahl B, Siegbahn A, Stridsberg M, Venge P, Armstrong P, Barnathan ES, Califf R, Topol EJ, SimoonsML, Wallentin L. N-terminal pro-brain natriuretic peptide and other risk markers for the separate prediction ofmortality and subsequent myocardial infarction in patients with unstable coronary artery disease: a Global Utilizationof Strategies To Open occluded arteries (GUSTO)-IV substudy. Circulation 2003;108:275–281.61. Steg PG, FitzGerald G, Fox KA. Risk stratification in non-ST-segment elevation acute coronary syndromes: troponinalone is not enough. Am J Med 2009;122: 107–108.62. Thygesen K, Mair J, Mueller C, Huber K, Weber M, Plebani M, Hasin Y, Biasucci LM, Giannitsis E, Lindahl B,Koenig W, Tubaro M, Collinson P, Katus H, Galvani M, Venge P, Alpert JS, Hamm C, Jaffe AS. Recommendationsfor the use of natriuretic peptides in acute cardiac care: a position statement from the Study Group on Biomarkersin Cardiology of the ESC Working Group on Acute Cardiac Care. Eur Heart J 2011;10.1093/eurheartj/ehq509.63. Heeschen C, Hamm CW, Bruemmer J, Simoons ML. Predictive value of Creactive protein and troponin T in patientswith unstable angina: a comparative analysis. CAPTURE Investigators. Chimeric c7E3 AntiPlatelet Therapyin Unstable angina REfractory to standard treatment trial. J Am Coll Cardiol 2000;35:1535–1542.64. Morrow DA, Rifai N, Antman EM, Weiner DL, McCabe CH, Cannon CP, Braunwald E. C-reactive protein is a potentpredictor of mortality independently of and in combination with troponin T in acute coronary syndromes:a TIMI 11A substudy. Thrombolysis in Myocardial Infarction. J Am Coll Cardiol 1998;31:1460–1465.65. Lindahl B, Toss H, Siegbahn A, Venge P, Wallentin L. Markers of myocardial damage and inflammation in relationto long-term mortality in unstable coronary artery disease. FRISC Study Group. Fragmin during Instabilityin Coronary Artery Disease. N Engl J Med 2000;343:1139–1147.66. Currie CJ, Poole CD, Conway P. Evaluation of the association between the first observation and the longitudinalchange in C-reactive protein, and all-cause mortality. Heart 2008;94:457–462.67. Aronson D, Hammerman H, Suleiman M, Markiewicz W. Usefulness of changes in fasting glucose during hospitalizationto predict long-term mortality in patients with acute myocardial infarction. Am J Cardiol2009;104:1013–1017.68. Suleiman M, Hammerman H, Boulos M, Kapeliovich MR, Suleiman A, Agmon Y, Markiewicz W, Aronson D. Fastingglucose is an important independent risk factor for 30-day mortality in patients with acute myocardial infarction:a prospective study. Circulation 2005;111:754–760.69. Sabatine MS, Morrow DA, Giugliano RP, Burton PB, Murphy SA, McCabe CH, Gibson CM, Braunwald E. Associationof hemoglobin levels with clinical outcomes in acute coronary syndromes. Circulation2005;111:2042–2049.70. Mahaffey KW, Yang Q, Pieper KS, Antman EM, White HD, Goodman SG, Cohen M, Kleiman NS, Langer A,Aylward PE, Col JJ, Reist C, Ferguson JJ, Califf RM. Prediction of one-year survival in high-risk patients withacute coronary syndromes: results from the SYNERGY trial. J Gen Intern Med 2008;23:310–316.71. Al Suwaidi J, Reddan DN, Williams K, Pieper KS, Harrington RA, Califf RM, Granger CB, Ohman EM, Holmes DRJr. Prognostic implications of abnormalities in renal function in patients with acute coronary syndromes. Circulation2002;106:974–980.72. Baldus S, Heeschen C, Meinertz T, Zeiher AM, Eiserich JP, Munzel T, Simoons ML, Hamm CW. Myeloperoxidaseserum levels predict risk in patients with acute coronary syndromes. Circulation 2003;108:1440–1445.73. Brennan ML, Penn MS, Van Lente F, Nambi V, Shishehbor MH, Aviles RJ, Goormastic M, Pepoy ML, McErleanES, Topol EJ, Nissen SE, Hazen SL. Prognostic value of myeloperoxidase in patients with chest pain. N Engl JMed 2003;349:1595–1604.74. Wollert KC, Kempf T, Peter T, Olofsson S, James S, Johnston N, Lindahl B, Horn-Wichmann R, Brabant G, SimoonsML, Armstrong PW, Califf RM, Drexler H, Wallentin L. Prognostic value of growth-differentiation factor-15 inpatients with non-ST-elevation acute coronary syndrome. Circulation 2007;115:962–971.75. Morrow DA, Sabatine MS, Brennan ML, de Lemos JA, Murphy SA, Ruff CT, Rifai N, Cannon CP, Hazen SL. Concurrentevaluation of novel cardiac biomarkers in acute coronary syndrome: myeloperoxidase and soluble CD40ligand and the risk of recurrent ischaemic events in TACTICS-TIMI 18. Eur Heart J 2008;29:1096–1102.76. Viswanathan K, Kilcullen N, Morrell C, Thistlethwaite SJ, Sivananthan MU, Hassan TB, Barth JH, Hall AS. Hearttypefatty acid-binding protein predicts long-term mortality and re-infarction in consecutive patients with suspectedacute coronary syndrome who are troponin-negative. J Am Coll Cardiol 2010;55:2590–2598.77. Van Belle E, Dallongeville J, Vicaut E, Degrandsart A, Baulac C, Montalescot G. Ischemia-modified albumin levelspredict long-term outcome in patients with acute myocardial infarction. The French Nationwide OPERAstudy. Am Heart J 2010;159:570–576.78. Reichlin T, Hochholzer W, Stelzig C, Laule K, Freidank H, Morgenthaler NG, Bergmann A, Potocki M, NoveanuM, Breidthardt T, Christ A, Boldanova T, Merki R, Schaub N, Bingisser R, Christ M, Mueller C. Incremental valueof copeptin for rapid rule out of acute myocardial infarction. J Am Coll Cardiol 2009;54:60–68.79. de Araujo Goncalves P, Ferreira J, Aguiar C, Seabra-Gomes R. TIMI, PURSUIT, and GRACE risk scores: sustainedprognostic value and interaction with revascularization in NSTE-ACS. Eur Heart J 2005;26:865–872.80. Aragam KG, Tamhane UU, Kline-Rogers E, Li J, Fox KA, Goodman SG, Eagle KA, Gurm HS. Does simplicitycompromise accuracy in ACS risk prediction? A retrospective analysis of the TIMI and GRACE risk scores. PLoSOne 2009;4:e7947.81. Eggers KM, Kempf T, Venge P, Wallentin L, Wollert KC, Lindahl B. Improving long-term risk prediction in patientswith acute chest pain: the Global Registry of Acute Coronary Events (GRACE) risk score is enhanced by selectednonnecrosis biomarkers. Am Heart J 2010;160:88–94.82. Khot UN, Jia G, Moliterno DJ, Lincoff AM, Khot MB, Harrington RA, Topol EJ. Prognostic importance of physicalexamination for heart failure in non-ST-elevation acute coronary syndromes: the enduring value of Killip classification.JAMA 2003;290:2174–2181.83. Subherwal S, Bach RG, Chen AY, Gage BF, Rao SV, Newby LK, Wang TY, Gibler WB, Ohman EM, Roe MT, PollackCV Jr., Peterson ED, Alexander KP. Baseline risk of major bleeding in non-ST-segment-elevation myocardialinfarction: the CRUSADE (Can Rapid risk stratification of Unstable angina patients Suppress ADverseoutcomes with Early implementation of the ACC/AHA Guidelines) Bleeding Score. Circulation2009;119:1873–1882.84. Mehran R, Pocock SJ, Nikolsky E, Clayton T, Dangas GD, Kirtane AJ, Parise H, Fahy M, Manoukian SV, Feit F,Ohman ME, Witzenbichler B, Guagliumi G, Lansky AJ, Stone GW. A risk score to predict bleeding in patients withacute coronary syndromes. J Am Coll Cardiol 2010;55:2556–2566.85. Yusuf S, Peto R, Lewis J, Collins R, Sleight P. Beta blockade during and after myocardial infarction: an overviewof the randomized trials. Prog Cardiovasc Dis 1985;27:335–371.86. Randomised trial of intravenous atenolol among 16 027 cases of suspected acute myocardial infarction: ISIS-1. First International Study of Infarct Survival Collaborative Group. Lancet 1986;2:57–66.87. Telford AM, Wilson C. Trial of heparin versus atenolol in prevention of myocardial infarction in intermediatecoronary syndrome. Lancet 1981;1:1225–1228.88. Lubsen J, Tijssen JG. Efficacy of nifedipine and metoprolol in the early treatment of unstable angina in the coronarycare unit: findings from the Holland Interuniversity Nifedipine/metoprolol Trial (HINT). Am J Cardiol1987;60:18A–25A.89. Yusuf S, Wittes J, Friedman L. Overview of results of randomized clinical trials in heart disease. I. Treatments followingmyocardial infarction. JAMA 1988;260:2088–2093.90. Metoprolol in acute myocardial infarction (MIAMI). A randomised placebocontrolled international trial. TheMIAMI Trial Research Group. Eur Heart J 1985;6:199–226.91. Miller CD, Roe MT, Mulgund J, Hoekstra JW, Santos R, Pollack CV Jr., Ohman EM, Gibler WB, Peterson ED. Impactof acute beta-blocker therapy for patients with non-ST-segment elevation myocardial infarction. Am JMed 2007;120:685–692.92. Brandler E, Paladino L, Sinert R. Does the early administration of beta-blockers improve the in-hospital mortalityrate of patients admitted with acute coronary syndrome? Acad Emerg Med 2010;17:1–10.93. Chen ZM, Pan HC, Chen YP, Peto R, Collins R, Jiang LX, Xie JX, Liu LS. Early intravenous then oral metoprolol in45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet2005;366:1622–1632.94. Borzak S, Cannon CP, Kraft PL, Douthat L, Becker RC, Palmeri ST, Henry T, Hochman JS, Fuchs J, Antman EM,McCabe C, Braunwald E. Effects of prior aspirin and anti-ischemic therapy on outcome of patients with unstableangina. TIMI 7 Investigators. Thrombin Inhibition in Myocardial Ischemia. Am J Cardiol 1998;81:678–681.95. Ambrosio G, Del Pinto M, Tritto I, Agnelli G, Bentivoglio M, Zuchi C, Anderson FA, Gore JM, Lopez-Sendon J,Wyman A, Kennelly BM, Fox KA. Chronic nitrate therapy is associated with different presentation and evolutionof acute coronary syndromes: insights from 52,693 patients in the Global Registry of Acute Coronary Events.Eur Heart J 2010;31:430–438.96. Cotter G, Faibel H, Barash P, Shemesh E, Moshkovitz Y, Metzkor E, Simovitz A, Miller R, Schlezinger Z, Golik A.High-dose nitrates in the immediate management of unstable angina: optimal dosage, route of administration,and therapeutic goals. Am J Emerg Med 1998;16:219–224.97. Theroux P, Taeymans Y, Morissette D, Bosch X, Pelletier GB, Waters DD. A randomized study comparing propranololand diltiazem in the treatment of unstable angina. J Am Coll Cardiol 1985;5:717–722.98. Parodi O, Simonetti I, Michelassi C, Carpeggiani C, Biagini A, L’Abbate A, Maseri A. Comparison of verapamiland propranolol therapy for angina pectoris at rest: a randomized, multiple-crossover, controlled trial in thecoronary care unit. Am J Cardiol 1986;57:899–906.99. Hansen JF. Treatment with verapamil after an acute myocardial infarction. Review of the Danish studies on verapamilin myocardial infarction (DAVIT I and II). Drugs 1991;42 Suppl 2:43–53.100. Moss AJ, Oakes D, Rubison M, McDermott M, Carleen E, Eberly S, Brown M. Effects of diltiazem on long-termoutcome after acute myocardial infarction in patients with and without a history of systemic hypertension.The Multicenter Diltiazem Postinfarction Trial Research Group. Am J Cardiol 1991;68:429–433.101. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina(IONA) randomised trial. Lancet 2002;359:1269–1275.102. Borer JS. Therapeutic effects of I(f) blockade: evidence and perspective. Pharmacol Res 2006;53:440–445.103. Morrow DA, Scirica BM, Karwatowska-Prokopczuk E, Murphy SA, Budaj A, Varshavsky S, Wolff AA, Skene A,McCabe CH, Braunwald E. Effects of ranolazine on recurrent cardiovascular events in patients with non-ST-elevationacute coronary syndromes: the MERLIN-TIMI 36 randomized trial. JAMA 2007;297:1775–1783.104. Theroux P, Ouimet H, McCans J, Latour JG, Joly P, Levy G, Pelletier E, Juneau M, Stasiak J, de Guise P, PelletierG, Rinzler D, Waters D. Aspirin, heparin, or both to treat acute unstable angina. N Engl J Med1988;319:1105–1111.105. Theroux P, Waters D, Qiu S, McCans J, de Guise P, Juneau M. Aspirin versus heparin to prevent myocardial infarctionduring the acute phase of unstable angina. Circulation 1993;88:2045–2048.106. Cairns JA, Gent M, Singer J, Finnie KJ, Froggatt GM, Holder DA, Jablonsky G, Kostok WJ, Melendez LJ, MyersMG, Sackett DL, Staley BJ, Tanser PH. Aspirin, sulfinpyrazone, or both in unstable angina. Results of a Canadianmulticenter trial. N Engl J Med 1985;313:1369–1375.107. Baigent C, Blackwell L, Collins R, Emberson J, Godwin J, Peto R, Buring J, Hennekens C, Kearney P, Meade T,Patrono C, Roncaglioni MC, Zanchetti A. Aspirin in the primary and secondary prevention of vascular disease:collaborative meta-analysis 108. Mehta SR, Tanguay JF, Eikelboom JW, Jolly SS, Joyner CD, Granger CB, Faxon DP, Rupprecht HJ, Budaj A,Avezum A, Widimsky P, Steg PG, Bassand JP, Montalescot G, Macaya C, Di Pasquale G, Niemela K, Ajani AE,White HD, Chrolavicius S, Gao P, Fox KA, Yusuf S. Double-dose versus standard-dose clopidogrel and highdoseversus low-dose aspirin in individuals undergoing percutaneous coronary intervention for acute coronarysyndromes (CURRENT-OASIS 7): a randomised factorial trial. Lancet 2010;376:1233–1243.109. Gislason GH, Jacobsen S, Rasmussen JN, Rasmussen S, Buch P, Friberg J, Schramm TK, Abildstrom SZ, KoberL, Madsen M, Torp-Pedersen C. Risk of death or reinfarction associated with the use of selective cyclooxygenase-2 inhibitors and nonselective nonsteroidal antiinflammatory drugs after acute myocardial infarction. Circulation2006;113:2906–2913.110. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Effects of clopidogrel in addition to aspirin inpatients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345:494–502.111. Yusuf S, Mehta SR, Zhao F, Gersh BJ, Commerford PJ, Blumenthal M, Budaj A, Wittlinger T, Fox KA. Early andlate effects of clopidogrel in patients with acute coronary syndromes. Circulation 2003;107:966–972.112. Ho PM, Peterson ED, Wang L, Magid DJ, Fihn SD, Larsen GC, Jesse RA, Rumsfeld JS. Incidence of death andacute myocardial infarction associated with stopping clopidogrel after acute coronary syndrome. JAMA2008;299:532–539.113. Fox KA, Mehta SR, Peters R, Zhao F, Lakkis N, Gersh BJ, Yusuf S. Benefits and risks of the combination of clopidogreland aspirin in patients undergoing surgical revascularization for non-ST-elevation acute coronary syndrome:the Clopidogrel in Unstable angina to prevent Recurrent ischemic Events (CURE) Trial. Circulation2004;110:1202–1208.114. Montalescot G, Sideris G, Meuleman C, Bal-dit-Sollier C, Lellouche N, Steg PG, Slama M, Milleron O, ColletJ-P, Henry P, Beygui F, Drouet L. A randomized comparison of high clopidogrel loading doses in patients withnon-ST-segment elevation acute coronary syndromes: the ALBION (Assessment of the Best Loading Dose ofClopidogrel to Blunt Platelet Activation, Inflammation and Ongoing Necrosis) Trial. J Am Coll Cardiol2006;48:931–938.115. Snoep JD, Hovens MM, Eikenboom JC, van der Bom JG, Jukema JW, Huisman MV. Clopidogrel nonresponsivenessin patients undergoing percutaneous coronary intervention with stenting: a systematic review andmeta-analysis. Am Heart J 2007;154:221–231.116. Aleil B, Jacquemin L, De Poli F, Zaehringer M, Collet J-P, Montalescot G, Cazenave J-P, Dickele M-C, MonassierJ-P, Gachet C. Clopidogrel 150 mg/day to overcome low responsiveness in patients undergoing elective percutaneouscoronary intervention: results from the VASP-02 (Vasodilator-Stimulated Phosphoprotein-02)Randomized Study. JACC Cardiovasc Interv 2008;1:631–638.117. The CURRENT-OASIS 7 Investigators. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes.N Engl J Med 2010;363:930–942.118. Taubert D, von Beckerath N, Grimberg G, Lazar A, Jung N, Goeser T, Kastrati A, Schomig A, Schomig E. Impactof P-glycoprotein on clopidogrel absorption. Clin Pharmacol Ther 2006;80:486–501.119. Mega JL, Close SL, Wiviott SD, Shen L, Walker JR, Simon T, Antman EM, Braunwald E, Sabatine MS. Geneticvariants in ABCB1 and CYP2C19 and cardiovascular outcomes after treatment with clopidogrel and prasugrelin the TRITON-TIMI 38 trial: a pharmacogenetic analysis. Lancet 2010;376:1312–1319.120. Mega JL, Simon T, Collet JP, Anderson JL, Antman EM, Bliden K, Cannon CP, Danchin N, Giusti B, Gurbel P,Horne BD, Hulot JS, Kastrati A, Montalescot G, Neumann FJ, Shen L, Sibbing D, Steg PG, Trenk D, Wiviott SD,Sabatine MS. Reduced-function CYP2C19 genotype and risk of adverse clinical outcomes among patientstreated with clopidogrel predominantly for PCI: a meta-analysis. JAMA 2010;304:1821–1830.121. Breet N, van Werkum J, Bouman H, Kelder J, Ruven H, Bal E, Deneer V, Harmsze A, van der Heyden J, RensingB, Suttorp M, Hackeng C, ten Berg J. Comparison of platelet function tests in predicting clinical outcomein patients undergoing coronary stent implantation. JAMA 2010;303:754–762.122. Geisler T, Langer H, Wydymus M, Gohring K, Zurn C, Bigalke B, Stellos K, May AE, Gawaz M. Low responseto clopidogrel is associated with cardiovascular outcome after coronary stent implantation. Eur Heart J2006;27:2420–2425.123. Trenk D, Hochholzer W, Fromm MF, Chialda LE, Pahl A, Valina CM, Stratz C, Schmiebusch P, Bestehorn HP,Buttner HJ, Neumann FJ. Cytochrome P450 2C19 681G.A polymorphism and high on-clopidogrel platelet reactivityassociated with adverse 1-year clinical outcome of elective percutaneous coronary intervention withdrug-eluting or bare-metal stents. J Am Coll Cardiol 2008;51:1925–1934.124. Price MJ, Berger PB, Teirstein PS, Tanguay JF, Angiolillo DJ, Spriggs D, Puri S, Robbins M, Garratt KN, BertrandOF, Stillablower ME, Aragon JR, Kandzari DE, Stinis CT, Lee MS, Manoukian SV, Cannon CP, Schork NJ, TopolEJ. Standard- vs high-dose clopidogrel based on platelet function testing after percutaneous coronary intervention:the GRAVITAS randomized trial. JAMA 2011;305:1097–1105.125. O’Donoghue ML, Braunwald E, Antman EM, Murphy SA, Bates ER, Rozenman Y, Michelson AD, HautvastRW, Ver Lee PN, Close SL, Shen L, Mega JL, Sabatine MS, Wiviott SD. Pharmacodynamic effect and clinical efficacyof clopidogrel and prasugrel with or without a proton-pump inhibitor: an analysis of two randomisedtrials. Lancet 2009;374:989–997.126. Abraham NS, Hlatky MA, Antman EM, Bhatt DL, Bjorkman DJ, Clark CB, Furberg CD, Johnson DA, Kahi CJ,Laine L, Mahaffey KW, Quigley EM, Scheiman J, Sperling LS, Tomaselli GF. ACCF/ACG/AHA 2010 Expert ConsensusDocument on the concomitant use of proton pump inhibitors and thienopyridines: a focused updateof the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelettherapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Expert ConsensusDocuments. Circulation 2010;122:2619–2633.127. Bhatt DL, Cryer BL, Contant CF, Cohen M, Lanas A, Schnitzer TJ, Shook TL, Lapuerta P, Goldsmith MA, LaineL, Scirica BM, Murphy SA, Cannon CP. Clopidogrel with or without omeprazole in coronary artery disease. NEngl J Med 2010;363:1909–1917.128. Wiviott SD, Trenk D, Frelinger AL, O’Donoghue M, Neumann F-J, Michelson AD, Angiolillo DJ, Hod H, MontalescotG, Miller DL, Jakubowski JA, Cairns R, Murphy SA, McCabe CH, Antman EM, Braunwald E, PRINCIPLE-TIMI 44 Investigators. Prasugrel compared with high loading- and maintenance-dose clopidogrel inpatients with planned percutaneous coronary intervention: the Prasugrel in Comparison to Clopidogrel for Inhibitionof Platelet Activation and Aggregation Thrombolysis in Myocardial Infarction 44 Trial. Circulation2007;116:2923–2932.129. Small DS, Farid NA, Payne CD, Weerakkody GJ, Li YG, Brandt JT, Salazar DE, Winters KJ. Effects of the protonpump inhibitor lansoprazole on the pharmacokinetics and pharmacodynamics of prasugrel and clopidogrel.J Clin Pharmacol 2008;48:475–484.130. Wiviott S, Braunwald E, McCabe C, Montalescot G, Ruzyllo W, Gottlieb S, Neumann F-J, Ardissino D, De ServiS, Murphy S, Riesmeyer J, Weerakkody G, Gibson C, Antman E. Prasugrel versus clopidogrel in patients withacute coronary syndromes. N Engl J Med 2007;357:2001–2015.131. Gurbel PA, Bliden KP, Butler K, Tantry US, Gesheff T, Wei C, Teng R, Antonino MJ, Patil SB, Karunakaran A,Kereiakes DJ, Paris C, Purdy D, Wilson V, Ledley GS, Storey RF. Randomized double-blind assessment of theONSET and OFFSet of the antiplatelet effects of ticagrelor versus clopidogrel in patients with stable coronaryartery disease: the ONSET/OFFSET Study. Circulation 2009;120:2577–2585.132. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C, Horrow J, Husted S, James S, Katus H,Mahaffey KW, Scirica BM, Skene A, Steg PG, Storey RF, Harrington RA, for the PLATO Investigators. Ticagrelorversus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361:1045–1057.133. Cannon C, Harrington R, James S, Ardissino D, Becker R, Emanuelsson H, Husted S, Katus H, Keltaih M, KhurmiN, Kontny F, Lewis B, Steg P, Storey R, Wojdyla D, Wallentin L, the PLATelet inhibition and patient Outcomes(PLATO) investigators. Ticagrelor compared with clopidogrel in acute coronary syndromes patients with aplanned invasive strategy (PLATO): a randomised double-blind study. Lancet 2010;375:283–293.134. Held C, Asenblad N, Bassand JP, Becker RC, Cannon CP, Claeys MJ, Harrington RA, Horrow J, Husted S, JamesSK, Mahaffey KW, Nicolau JC, Scirica BM, Storey RF, Vintila M, Ycas J, Wallentin L. Ticagrelor versus clopidogrelin patients with acute coronary syndromes undergoing coronary artery bypass surgery results from thePLATO (Platelet Inhibition and Patient Outcomes) Trial. J Am Coll Cardiol 2011;57:672–684.135. Husted S, Emanuelsson H, Heptinstall S, Sandset PM, Wickens M, Peters G. Pharmacodynamics, pharmacokinetics,and safety of the oral reversible P2Y12 antagonist AZD6140 with aspirin in patients with atherosclerosis:a double-blind comparison to clopidogrel with aspirin. Eur Heart J 2006;27:1038–1047.136. Cannon CP, Husted S, Harrington RA, Scirica BM, Emanuelsson H, Peters G, Storey RF. Safety, tolerability, andinitial efficacy of AZD6140, the First reversible oral adenosine diphosphate receptor antagonist, comparedwith clopidogrel, in patients with non-ST-segment elevation acute coronary syndrome: primary results of theDISPERSE-2 Trial. J Am Coll Cardiol 2007;50:1844–1851.137. Storey RF, Bliden K, Patil SB, Karunakaran A, Ecob R, Butler K, Teng R, Wei C, Tantry US, Gurbel P. Incidence ofdyspnea and assessment of cardiac and pulmonary function in patients with stable coronary artery disease receivingticagrelor, clopidogrel or placebo in the ONSET/OFFSET Study. J Am Coll Cardiol 2010;56:185–193.138. Berger JS, Frye CB, Harshaw Q, Edwards FH, Steinhubl SR, Becker RC. Impact of clopidogrel in patients withacute coronary syndromes requiring coronary artery bypass surgery: a multicenter analysis. J Am Coll Cardiol2008;52:1693–1701.139. Kapetanakis EI, Medlam DA, Boyce SW, Haile E, Hill PC, Dullum MK, Bafi AS, Petro KR, Corso PJ. Clopidogreladministration prior to coronary artery bypass grafting surgery: the cardiologist’s panacea or the surgeon’sheadache? Eur Heart J 2005;26:576–583.140. Mehta RH, Roe MT, Mulgund J, Ohman EM, Cannon CP, Gibler WB, Pollack CV Jr., Smith SC Jr., Ferguson TB,Peterson ED. Acute clopidogrel use and outcomes in patients with non-ST-segment elevation acute coronarysyndromes undergoing coronary artery bypass surgery. J Am Coll Cardiol 2006;48:281–286.141. Ebrahimi R, Dyke C, Mehran R, Manoukian SV, Feit F, Cox DA, Gersh BJ, Ohman EM, White HD, Moses JW,WareJH, Lincoff AM, Stone GW. Outcomes following pre-operative clopidogrel administration in patients with acutecoronary syndromes undergoing coronary artery bypass surgery: the ACUITY (Acute Catheterization and UrgentIntervention Triage strategY) Trial. J Am Coll Cardiol 2009;53:1965–1972.142. Kim JH, Newby LK, Clare RM, Shaw LK, Lodge AJ, Smith PK, Jolicoeur EM, Rao SV, Becker RC, Mark DB,Granger CB. Clopidogrel use and bleeding after coronary artery bypass graft surgery. Am Heart J2008;156:886–892.143. Fitchett D, Eikelboom J, Fremes S, Mazer D, Singh S, Bittira B, Brister S, Graham JJ, Gupta M, Karkouti K, LeeA, Love M, McArthur R, Peterson M, Verma S, Yau TM. Dual antiplatelet therapy in patients requiring urgentcoronary artery bypass grafting surgery: a position statement of the Canadian Cardiovascular Society. Can J Cardiol2009;25:683–689.144. Collet JP, Montalescot G, Blanchet B, Tanguy ML, Golmard JL, Choussat R, Beygui F, Payot L, Vignolles N, MetzgerJP, Thomas D. Impact of prior use or recent withdrawal of oral antiplatelet agents on acute coronary syndromes.Circulation 2004;110:2361–2367.145. Grines CL, Bonow RO, Casey DE Jr., Gardner TJ, Lockhart PB, Moliterno DJ, O’Gara P, Whitlow P. Prevention ofpremature discontinuation of dual antiplatelet therapy in patients with coronary artery stents: a science advisoryfrom the American Heart Association, American College of Cardiology, Society for Cardiovascular Angiographyand Interventions, American College of Surgeons, and American Dental Association, withrepresentation from the American College of Physicians. Circulation 2007;115:813–818.146. Mehta SR, Yusuf S, Peters RJ, Bertrand ME, Lewis BS, Natarajan MK, Malmberg K, Rupprecht H, Zhao F,Chrolavicius S, Copland I, Fox KA. Effects of pretreatment with clopidogrel and aspirin followed by long-termtherapy in patients undergoing percutaneous coronary intervention: the PCI-CURE study. Lancet2001;358:527–533.147. Steinhubl SR, Berger PB, Mann JT 3rd, Fry ET, DeLago A, Wilmer C, Topol EJ. Early and sustained dual oral antiplatelettherapy following percutaneous coronary intervention: a randomized controlled trial. JAMA2002;288:2411–2420.148. Wijns W, Kolh P, Danchin N, Di Mario C, Falk V, Folliguet T, Garg S, Huber K, James S, Knuuti J, Lopez-SendonJ, Marco J, Menicanti L, Ostojic M, Piepoli MF, Pirlet C, Pomar JL, Reifart N, Ribichini FL, Schalij MJ, SergeantP, Serruys PW, Silber S, Sousa Uva M, Taggart D. Guidelines on myocardial revascularization: the Task Force onMyocardial Revascularization of the European Society of Cardiology (ESC) and the European Association forCardio-Thoracic Surgery (EACTS). Eur Heart J 2010;31:2501–2555.149. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Moliterno DJ, Heeschen C, Hamm CW, Robbins MA,Kleiman NS, Theroux P, White HD, Topol EJ. Platelet glycoprotein IIb/IIIa inhibition in acute coronary syndromes.Gradient of benefit related to the revascularisation strategy. Eur Heart J 2002; 23:1441–1448.150. Stone GW, Bertrand ME, Moses JW, Ohman EM, Lincoff AM, Ware JH, Pocock SJ, McLaurin BT, Cox DA, JafarMZ, Chandna H, Hartmann F, Leisch F, Strasser RH, Desaga M, Stuckey TD, Zelman RB, Lieber IH, Cohen DJ,Mehran R, White HD. Routine upstream initiation vs deferred selective use of glycoprotein IIb/IIIa inhibitorsin acute coronary syndromes: the ACUITY Timing trial. JAMA 2007;297:591–602.151. Giugliano RP, White JA, Bode C, Armstrong PW, Montalescot G, Lewis BS, van’t Hof A, Berdan LG, Lee KL,Strony JT, Hildemann S, Veltri E, Van de Werf F, Braunwald E, Harrington RA, Califf RM, Newby LK, the EARLYACS Investigators. Early versus delayed, provisional eptifibatide in acute coronary syndromes. N Engl J Med2009;360:2176–2190.152. Kastrati A, Mehilli J, Neumann F-J, Dotzer F, ten Berg J, Bollwein H, Graf I, Ibrahim M, Pache J, Seyfarth M,Schuhlen H, Dirschinger J, Berger PB, Schomig A, for the Intracoronary Stenting, Antithrombotic Regimen:Rapid Early Action for Coronary Treatment 2 Trial I. Abciximab in patients with acute coronary syndromes undergoingpercutaneous coronary intervention after clopidogrel pretreatment: the ISAR-REACT 2 RandomizedTrial. JAMA 2006;295:1531–1538. 153. Dasgupta H, Blankenship JC, Wood GC, Frey CM, Demko SL, Menapace FJ. Thrombocytopenia complicatingtreatment with intravenous glycoprotein IIb/IIIa receptor inhibitors: a pooled analysis. Am Heart J2000;140:206–211.154. Jubelirer SJ, Koenig BA, Bates MC. Acute profound thrombocytopenia following C7E3 Fab (Abciximab) therapy:case reports, review of the literature and implications for therapy. Am J Hematol 1999;61:205–208.155. Lajus S, Clofent-Sanchez G, Jais C, Coste P, Nurden P, Nurden AT. Thrombocytopenia after abciximab use resultsfrom different mechanisms. Thromb Haemost 2010;103 651–661.156. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute coronary syndromes. ThePURSUIT Trial Investigators. Platelet glycoprotein IIb/IIIa in unstable angina: receptor suppression using integrilintherapy. N Engl J Med 1998;339:436–443.157. Merlini PA, Rossi M, Menozzi A, Buratti S, Brennan DM, Moliterno DJ, Topol EJ, Ardissino D. Thrombocytopeniacaused by abciximab or tirofiban and its association with clinical outcome in patients undergoing coronarystenting. Circulation 2004;109:2203–2206.158. Topol EJ, Moliterno DJ, Herrmann HC, Powers ER, Grines CL, Cohen DJ, Cohen EA, Bertrand M, Neumann FJ,Stone GW, DiBattiste PM, Yakubov SJ, DeLucca PT, Demopoulos L, the TARGET Investigators. Comparisonof two platelet glycoprotein IIb/IIIa inhibitors, tirofiban and abciximab, for the prevention of ischemic eventswith percutaneous coronary revascularization. N Engl J Med 2001;344:1888–1894.159. Moliterno DJ, Yakubov SJ, DiBattiste PM, Herrmann HC, Stone GW, Macaya C, Neumann F-J, Ardissino D,Bassand J-P, Borzi L. Outcomes at 6 months for the direct comparison of tirofiban and abciximab during percutaneouscoronary revascularisation with stent placement: the TARGET follow-up study. Lancet2002;360:355–360.160. De Luca G, Ucci G, Cassetti E, Marino P. Benefits from small molecule administration as compared with abciximabamong patients with ST-segment elevation myocardial infarction treated with primary angioplasty: ameta-analysis. J Am Coll Cardiol 2009;53:1668–1673.161. Valgimigli M, Biondi-Zoccai G, Tebaldi M, van’t Hof AWJ, Campo G, Hamm C, ten Berg J, Bolognese L, Saia F,Danzi GB, Briguori C, Okmen E, King SB, Moliterno DJ, Topol EJ. Tirofiban as adjunctive therapy for acutecoronary syndromes and percutaneous coronary intervention: a meta-analysis of randomized trials. Eur HeartJ 2010;31:35–49.162. O’Donoghue M, Antman EM, Braunwald E, Murphy SA, Steg PG, Finkelstein A, Penny WF, Fridrich V, McCabeCH, Sabatine MS, Wiviott SD. The efficacy and safety of prasugrel with and without a glycoprotein IIb/IIIa inhibitorin patients with acute coronary syndromes undergoing percutaneous intervention: a TRITON-TIMI 38(Trial to Assess Improvement in Therapeutic Outcomes by Optimizing Platelet Inhibition With Prasugrel-ThrombolysisIn Myocardial Infarction 38) analysis. J Am Coll Cardiol 2009;54:678–685.163. Buller C, Pate G, Armstrong P, O’Neill B, Webb J, Gallo R, Welsh R. Catheter thrombosis during primary percutaneouscoronary intervention for acute ST elevation myocardial infarction despite subcutaneous low-molecular-weight heparin, acetylsalicylic acid, clopidogrel and abciximab pretreatment. Can J Cardiol2006;22:511–515.164. Jolly SS, Faxon DP, Fox KA, Afzal R, Boden WE, Widimsky P, Steg PG, Valentin V, Budaj A, Granger CB, JoynerCD, Chrolavicius S, Yusuf S, Mehta SR. Efficacy and safety of fondaparinux versus enoxaparin in patients withacute coronary syndromes treated with glycoprotein IIb/IIIa inhibitors or thienopyridines: results from theOASIS 5 (Fifth Organization to Assess Strategies in Ischemic Syndromes) trial. J Am Coll Cardiol2009;54:468–476.165. White HD, Ohman EM, Lincoff AM, Bertrand ME, Colombo A, McLaurin BT, Cox DA, Pocock SJ, Ware JA,Manoukian SV, Lansky AJ, Mehran R, Moses JW, Stone GW. Safety and efficacy of bivalirudin with and withoutglycoprotein IIb/IIIa inhibitors in patients with acute coronary syndromes undergoing percutaneous coronaryintervention: 1-year results from the ACUITY (Acute Catheterization and Urgent Intervention TriagestrategY) trial. J Am Coll Cardiol 2008;52:807–814.166. Lincoff AM, Steinhubl SR, Manoukian SV, Chew D, Pollack CV Jr, Feit F,Ware JH, Bertrand ME, Ohman EM,DesmetW, Cox DA, Mehran R, Stone GW. Influence of timing of clopidogrel treatment on the efficacy andsafety of bivalirudin in patients with non-ST-segment elevation acute coronary syndromes undergoing percutaneouscoronary intervention: an analysis of the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. JACC Cardiovasc Interv 2008;1:639–648.167. Brieger D, Van de Werf F, Avezum A, Montalescot G, Kennelly B, Granger CB, Goodman SG, Dabbous O, AgnelliG. Interactions between heparins, glycoprotein IIb/IIIa antagonists, and coronary intervention. The GlobalRegistry of Acute Coronary Events (GRACE). Am Heart J 2007;153:960–969.168. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED, for the CRUSADE Investigators. Excess dosing of antiplatelet and antithrombin agents in thetreatment of non-ST-segment elevation acute coronary syndromes. JAMA 2005;294:3108–3116.169. Li Y, Spencer F, Becker R. Comparative efficacy of fibrinogen and platelet supplementation on the in vitro reversibilityof competitive glycoprotein IIb/IIIa receptor-directed platelet inhibition. Am Heart J2002;143:725–732.170. Neumann FJ, Kastrati A, Pogatsa-Murray G, Mehilli J, Bollwein H, Bestehorn HP, Schmitt C, Seyfarth M,Dirschinger J, Schomig A. Evaluation of prolonged antithrombotic pretreatment (‘cooling-off’ strategy) beforeintervention in patients with unstable coronary syndromes: a randomized controlled trial. JAMA2003;290:1593–1599.171. Harrington RA, Becker RC, Cannon CP, Gutterman D, Lincoff AM, Popma JJ, Steg G, Guyatt GH, Goodman SG.Antithrombotic therapy for non-ST-segment elevation acute coronary syndromes: American College of ChestPhysicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008;133:670S–707S.172. Eikelboom JW, Anand SS, Malmberg K, Weitz JI, Ginsberg JS, Yusuf S. Unfractionated heparin and low-molecular-weight heparin in acute coronary syndrome without ST elevation: a meta-analysis. Lancet2000;355:1936–1942.173. Simoons ML, Bobbink IW, Boland J, Gardien M, Klootwijk P, Lensing AW, Ruzyllo W, Umans VA, Vahanian A,Van De Werf F, Zeymer U; PENTUA Investigators. A dose-finding study of fondaparinux in patients with non-ST-segment elevation acute coronary syndromes: the Pentasaccharide in Unstable Angina (PENTUA) Study.J Am Coll Cardiol 2004;43:2183–2190.174. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Effects of fondaparinux on mortality and reinfarction in patients with acute ST-segment elevationmyocardial infarction: the OASIS-6 randomized trial. JAMA 2006;295:1519–1530.175. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Comparison of fondaparinux and enoxaparin in acute coronary syndromes. N Engl J Med2006;354:1464–1476.176. Mehta SR, Steg PG, Granger CB, Bassand JP, Faxon DP,Weitz JI, Afzal R, Rush B, Peters RJ, Natarajan MK,Velianou JL, Goodhart DM, Labinaz M, Tanguay JF, Fox KA, Yusuf S. Randomized, blinded trial comparingfondaparinux with unfractionated heparin in patients undergoing contemporary percutaneous coronary intervention:Arixtra Study in Percutaneous Coronary Intervention: a Randomized Evaluation (ASPIRE) pilot trial.Circulation 2005;111:1390–1397.177. Anderson JA, Hirsh J, Yusuf S, Johnston M, Afzal R, Mehta SR, Fox KA, Budaj A, Eikelboom JW. Comparisonof the anticoagulant intensities of fondaparinux and enoxaparin in the Organization to Assess Strategies inAcute Ischemic Syndromes (OASIS)-5 trial. J Thromb Haemost 2010;8:243–249.178. Steg PG, Jolly SS, Mehta SR, Afzal R, Xavier D, Rupprecht HJ, Lopez-Sendon JL, Budaj A, Diaz R, Avezum A,Widimsky P, Rao SV, Chrolavicius S, Meeks B, Joyner C, Pogue J, Yusuf S. Low-dose vs standard-dose unfractionatedheparin for percutaneous coronary intervention in acute coronary syndromes treated with fondaparinux:the FUTURA/OASIS-8 randomized trial. JAMA 2010;304:1339–1349.179. Antman EM, McCabe CH, Gurfinkel EP, Turpie AG, Bernink PJ, Salein D, Bayes De Luna A, Fox K, Lablanche JM,Radley D, Premmereur J, Braunwald E. Enoxaparin prevents death and cardiac ischemic events in unstableangina/non-Q-wave myocardial infarction. Results of the thrombolysis in myocardial infarction (TIMI) 11Btrial. Circulation 1999;100:1593–1601.180. Cohen M, Demers C, Gurfinkel EP, Turpie AG, Fromell GJ, Goodman S, Langer A, Califf RM, Fox KA, PremmereurJ, Bigonzi F. A comparison of low-molecular-weight heparin with unfractionated heparin for unstablecoronary artery disease. Efficacy and Safety of Subcutaneous Enoxaparin in Non-Q-Wave Coronary EventsStudy Group. N Engl J Med 1997;337:447–452.181. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators. Long-term lowmolecular-mass heparin in unstable coronary-artery disease: FRISC II prospective randomised multicentrestudy. Lancet 1999;354:701–707.182. Fragmin during Instability in Coronary Artery Disease (FRISC) study group. Low-molecular-weight heparinduring instability in coronary artery disease Lancet 1996;347:561–568.183. Hirsh J, Raschke R. Heparin and low-molecular-weight heparin: the Seventh ACCP Conference on Antithromboticand Thrombolytic Therapy. Chest 2004;126:188S–203S.184. TIMI 11A Investigators. Dose-ranging trial of enoxaparin for unstable angina: results of TIMI 11A. The Thrombolysisin Myocardial Infarction (TIMI) 11A Trial Investigators. J Am Coll Cardiol 1997;29:1474–1482.185. Montalescot G, Collet JP, Tanguy ML, Ankri A, Payot L, Dumaine R, Choussat R, Beygui F, Gallois V, Thomas D.Anti-Xa activity relates to survival and efficacy in unselected acute coronary syndrome patients treated withenoxaparin. Circulation 2004;110:392–398.186. Choussat R, Montalescot G, Collet JP, Vicaut E, Ankri A, Gallois V, Drobinski G, Sotirov I, Thomas D. A unique,low dose of intravenous enoxaparin in elective percutaneous coronary intervention. J Am Coll Cardiol2002;40:1943–1950.187. Collet JP, Montalescot G, Lison L, Choussat R, Ankri A, Drobinski G, Sotirov I, Thomas D. Percutaneous coronaryintervention after subcutaneous enoxaparin pretreatment in patients with unstable angina pectoris. Circulation2001;103:658–663.188. Murphy S, Gibson C, Morrow D, Van de Werf F, Menown I, Goodman S, Mahaffey K, Cohen M, McCabe C,Antman EM, Braunwald E. Efficacy and safety of the low-molecular weight heparin enoxaparin comparedwith unfractionated heparin across the acute coronary syndrome spectrum: a meta-analysis.Eur Heart J2007;28:2077–2086.189. Blazing MA, de Lemos JA, White HD, Fox KA, Verheugt FW, Ardissino D, DiBattiste PM, Palmisano J, BilheimerDW, Snapinn SM, Ramsey KE, Gardner LH, Hasselblad V, Pfeffer MA, Lewis EF, Braunwald E, Califf RM. Safetyand efficacy of enoxaparin vs unfractionated heparin in patients with non-ST-segment elevation acute coronarysyndromes who receive tirofiban and aspirin: a randomized controlled trial. JAMA 2004;292:55–64.190. Cohen M, Theroux P, Borzak S, Frey MJ, White HD, Van Mieghem W, Senatore F, Lis J, Mukherjee R, Harris K,Bigonzi F. Randomized double-blind safety study of enoxaparin versus unfractionated heparin in patients withnon-ST-segment elevation acute coronary syndromes treated with tirofiban and aspirin: the ACUTE II study.The Antithrombotic Combination Using Tirofiban and Enoxaparin. Am Heart J 2002;144:470–477.191. Goodman SG, Fitchett D, Armstrong PW, Tan M, Langer A. Randomized evaluation of the safety and efficacyof enoxaparin versus unfractionated heparin in high-risk patients with non-ST-segment elevation acute coronarysyndromes receiving the glycoprotein IIb/IIIa inhibitor eptifibatide. Circulation 2003;107:238–244.192. Ferguson JJ, Califf RM, Antman EM, Cohen M, Grines CL, Goodman S, Kereiakes DJ, Langer A, Mahaffey KW,Nessel CC, Armstrong PW, Avezum A, Aylward P, Becker RC, Biasucci L, Borzak S, Col J, Frey MJ, Fry E, GulbaDC, Guneri S, Gurfinkel E, Harrington R, Hochman JS, Kleiman NS, Leon MB, Lopez-Sendon JL, Pepine CJ,Ruzyllo W, Steinhubl SR, Teirstein PS, Toro-Figueroa L, White H. Enoxaparin vs unfractionated heparin in highriskpatients with non-ST-segment elevation acute coronary syndromes managed with an intended early invasivestrategy: primary results of the SYNERGY randomized trial. JAMA 2004;292:45–54.193. Petersen JL, Mahaffey KW, Hasselblad V, Antman EM, Cohen M, Goodman SG, Langer A, Blazing MA, Le-Moigne-Amrani A, de Lemos JA, Nessel CC, Harrington RA, Ferguson JJ, Braunwald E, Califf RM. Efficacy andbleeding complications among patients randomized to enoxaparin or unfractionated heparin for antithrombintherapy in non-ST-Segment elevation acute coronary syndromes: a systematic overview. JAMA2004;292:89–96.194. Sanchez-Pena P, Hulot JS, Urien S, Ankri A, Collet JP, Choussat R, Lechat P, Montalescot G. Anti-factor Xa kineticsafter intravenous enoxaparin in patients undergoing percutaneous coronary intervention: a populationmodel analysis. Br J Clin Pharmacol 2005;60:364–373.195. Montalescot G, White HD, Gallo R, Cohen M, Steg PG, Aylward PE, Bode C, Chiariello M, King SB 3rd, HarringtonRA, Desmet WJ, Macaya C, Steinhubl SR. Enoxaparin versus unfractionated heparin in elective percutaneouscoronary intervention. N Engl J Med 2006;355:1006–1017.196. Stone GW, McLaurin BT, Cox DA, Bertrand ME, Lincoff AM, Moses JW, White HD, Pocock SJ, Ware JH, Feit F,Colombo A, Aylward PE, Cequier AR, Darius H, Desmet W, Ebrahimi R, Hamon M, Rasmussen LH, RupprechtHJ, Hoekstra J, Mehran R, Ohman EM; ACUITY Investigators. Bivalirudin for patients with acute coronary syndromes.N Engl J Med 2006;355:2203–2216.197. Stone GW, White HD, Ohman EM, Bertrand ME, Lincoff AM, McLaurin BT, Cox DA, Pocock SJ, Ware JH, FeitF, Colombo A, Manoukian SV, Lansky AJ, Mehran R, Moses JW. Acute Catheterization and Urgent InterventionTriage strategy (ACUITY) trial investigators. Bivalirudin in patients with acute coronary syndromes undergoingpercutaneous coronary intervention: a subgroup analysis from the Acute Catheterization and UrgentIntervention Triage strategy (ACUITY) trial. Lancet 2007;369:907–919.198. Stone G, Ware J, Bertrand M, Lincoff A, Moses J, Ohman E, White H, Feit F, Colombo A, McLaurin B, Cox D,Manoukian S, Fahy M, Clayton T, Mehran R, Pocock S. For the ACUITY Investigators. Antithrombotic strategiesin patients with acute coronary syndromes undergoing early invasive management: one-year results fromthe ACUITY trial. JAMA 2007;298:2497–2506. 199. White HD, Chew DP, Hoekstra JW, Miller CD, Pollack CV Jr., Feit F, Lincoff AM, Bertrand M, Pocock S, Ware J,Ohman EM, Mehran R, Stone GW. Safety and efficacy of switching from either unfractionated heparin orenoxaparin to bivalirudin in patients with non-ST-segment elevation acute coronary syndromes managedwith an invasive strategy: results from the ACUITY (Acute Catheterization and Urgent Intervention Triage strategY)trial. J Am Coll Cardiol 2008;51:1734–1741.200. Alexander JH, Becker RC, Bhatt DL, Cools F, Crea F, Dellborg M, Fox KA, Goodman SG, Harrington RA, HuberK, Husted S, Lewis BS, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, WallentinL. Apixaban, an oral, direct, selective factor Xa inhibitor, in combination with antiplatelet therapy after acutecoronary syndrome: results of the Apixaban for Prevention of Acute Ischemic and Safety Events (APPRAISE)trial. Circulation 2009;119:2877–2885.201. Mega JL, Braunwald E, Mohanavelu S, Burton P, Poulter R, Misselwitz F, Hricak V, Barnathan ES, Bordes P,Witkowski A, Markov V, Oppenheimer L, Gibson CM. Rivaroxaban versus placebo in patients with acute coronarysyndromes (ATLAS ACS-TIMI 46): a randomised, double-blind, phase II trial. Lancet 2009;374:29–38.202. Alexander J, Becker R, Bhatt D, Cools F, Crea F, Dellborg M, Fox K, Goodman S, Harrington R, Huber K, HustedS, Lewis B, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, Wallentin L. For the APPRAISESteering Committee and Investigators. Apixaban, an oral, direct, selective factor Xa inhibitor, in combinationwith antiplatelet therapy after acute coronary syndrome: results of the Apixaban for Prevention ofAcute Ischemic and Safety Events (APPRAISE) trial. Circulation 2009;119:2877–2885.203. Sabatine MS, Antman EM, Widimsky P, Ebrahim IO, Kiss RG, Saaiman A, Polasek R, Contant CF, McCabe CH,Braunwald E. Otamixaban for the treatment of patients with non-ST-elevation acute coronary syndromes(SEPIA-ACS1 TIMI 42): a randomised, double-blind, active-controlled, phase 2 trial. Lancet2009;374:787–795.204. Lip GY, Huber K, Andreotti F, Arnesen H, Airaksinen JK, Cuisset T, Kirchhof P, Marin F. Antithrombotic managementof atrial fibrillation patients presenting with acute coronary syndrome and/or undergoing coronarystenting: executive summary—a Consensus Document of the European Society of Cardiology Working Groupon Thrombosis, endorsed by the European Heart Rhythm Association (EHRA) and the European Associationof Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2010;31:1311–1318.205. Yan AT, Yan RT, Tan M, Eagle KA, Granger CB, Dabbous OH, Fitchett D, Grima E, Langer A, Goodman SG. Inhospitalrevascularization and one-year outcome of acute coronary syndrome patients stratified by the GRACErisk score. Am J Cardiol 2005;96:913–916.206. Mehta SR, Cannon CP, Fox KA, Wallentin L, Boden WE, Spacek R, Widimsky P, McCullough PA, Hunt D, BraunwaldE, Yusuf S. Routine vs selective invasive strategies in patients with acute coronary syndromes: a collaborativemeta-analysis of randomized trials. JAMA 2005;293:2908–2917.207. Bavry AA, Kumbhani DJ, Rassi AN, Bhatt DL, Askari AT. Benefit of early invasive therapy in acute coronary syndromes:a meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006;48:1319–1325.208. O’Donoghue M, Boden WE, Braunwald E, Cannon CP, Clayton TC, de Winter RJ, Fox KA, Lagerqvist B, McCulloughPA, Murphy SA, Spacek R, Swahn E,Wallentin L, Windhausen F, Sabatine MS. Early invasive vs conservativetreatment strategies in women and men with unstable angina and non-ST-segment elevation myocardialinfarction: a meta-analysis. JAMA 2008; 300:71–80.209. Fox KA, Clayton TC, Damman P, Pocock SJ, de Winter RJ, Tijssen JG, Lagerqvist B,Wallentin L. Long-term outcomeof a routine versus selective invasive strategy in patients with non-ST-segment elevation acute coronarysyndrome a meta-analysis of individual patient data. J Am Coll Cardiol 2010;55:2435–2445.210. Montalescot G, Cayla G, Collet JP, Elhadad S, Beygui F, Le Breton H, Choussat R, Leclercq F, Silvain J, Duclos F,Aout M, Dubois-Rande JL, Barthelemy O, Ducrocq G, Bellemain-Appaix A, Payot L, Steg PG, Henry P, SpauldingC, Vicaut E. Immediate vs delayed intervention for acute coronary syndromes: a randomized clinical trial.JAMA 2009;302:947–954.211. van’t Hof AW, de Vries ST, Dambrink JH, Miedema K, Suryapranata H, Hoorntje JC, Gosselink AT, Zijlstra F, deBoer MJ. A comparison of two invasive strategies in patients with non-ST elevation acute coronary syndromes:results of the Early or Late Intervention in unStable Angina (ELISA) pilot study. 2b/3a upstream therapy andacute coronary syndromes. Eur Heart J 2003;24:1401–1405.212. Mehta SR, Granger CB, Boden WE, Steg PG, Bassand JP, Faxon DP, Afzal R, Chrolavicius S, Jolly SS, WidimskyP, Avezum A, Rupprecht HJ, Zhu J, Col J, Natarajan MK, Horsman C, Fox KA, Yusuf S. Early versus delayed invasiveintervention in acute coronary syndromes. N Engl J Med 2009;360:2165–2175.213. Katritsis DG, Siontis GC, Kastrati A, van’t Hof AW, Neumann FJ, Siontis KC, Ioannidis JP. Optimal timing ofcoronary angiography and potential intervention in non-ST-elevation acute coronary syndromes. Eur Heart J2010;32:32–40.214. Riezebos RK, Ronner E, Ter Bals E, Slagboom T, Smits PC, ten Berg JM, Kiemeneij F, Amoroso G, Patterson MS,Suttorp MJ, Tijssen JG, Laarman GJ. Immediate versus deferred coronary angioplasty in non-ST-segment elevationacute coronary syndromes. Heart 2009;95:807–812.215. Sorajja P, Gersh BJ, Cox DA, McLaughlin MG, Zimetbaum P, Costantini C, Stuckey T, Tcheng JE, Mehran R,Lansky AJ, Grines CL, Stone GW. Impact of delay to angioplasty in patients with acute coronary syndromes undergoinginvasive management: analysis from the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. J Am Coll Cardiol 2010;55:1416–1424.216. Brener SJ, Milford-Beland S, Roe MT, Bhatt DL, Weintraub WS, Brindis RG. Culprit-only or multivessel revascularizationin patients with acute coronary syndromes: an American College of Cardiology National CardiovascularDatabase Registry report. Am Heart J 2008;155:140–146.217. Ben-Gal Y, Moses JW, Mehran R, Lansky AJ,Weisz G, Nikolsky E, Argenziano M, Williams MR, Colombo A, AylwardPE, Stone GW. Surgical versus percutaneous revascularization for multivessel disease in patients withacute coronary syndromes: analysis from the ACUITY (Acute Catheterization and Urgent Intervention TriageStrategy) trial. JACC Cardiovasc Interv 2010;3:1059–1067.218. Serruys PW, Morice MC, Kappetein AP, Colombo A, Holmes DR, Mack MJ, Stahle E, Feldman TE, van denBrand M, Bass EJ, Van Dyck N, Leadley K, Dawkins KD, Mohr FW. Percutaneous coronary intervention versuscoronary-artery bypass grafting for severe coronary artery disease. N Engl J Med 2009;360:961–972.219. Sianos G, Morel MA, Kappetein AP, Morice MC, Colombo A, Dawkins K, van den Brand M, Van Dyck N, RussellME, Mohr FW, Serruys PW. The SYNTAX Score: an angiographic tool grading the complexity of coronaryartery disease. EuroIntervention 2005;1:219–227.220. de Winter RJ, Windhausen F, Cornel JH, Dunselman PH, Janus CL, Bendermacher PE, Michels HR, Sanders GT,Tijssen JG, Verheugt FW. Early invasive versus selectively invasive management for acute coronary syndromes.N Engl J Med 2005;353:1095–1104.221. Monteiro P. Impact of early coronary artery bypass graft in an unselected acute coronary syndrome patient population.Circulation 2006;114:I467–I472.222. Parikh SV, de Lemos JA, Jessen ME, Brilakis ES, Ohman EM, Chen AY, Wang TY, Peterson ED, Roe MT, HolperEM. Timing of in-hospital coronary artery bypass graft surgery for non-ST-segment elevation myocardial infarctionpatients results from the National Cardiovascular Data Registry ACTION Registry-GWTG (Acute CoronaryTreatment and Intervention Outcomes Network Registry-Get With The Guidelines). JACC CardiovascInterv 2010;3:419–427.223. Chu MW, Wilson SR, Novick RJ, Stitt LW, Quantz MA. Does clopidogrel increase blood loss following coronaryartery bypass surgery? Ann Thorac Surg 2004;78:1536–1541.224. Solodky A, Behar S, Boyko V, Battler A, Hasdai D. The outcome of coronary artery bypass grafting surgeryamong patients hospitalized with acute coronary syndrome: the Euro Heart Survey of acute coronary syndromeexperience. Cardiology 2005;103:44–47.225. Kaiser C, Galatius S, Erne P, Eberli F, Alber H, Rickli H, Pedrazzini G, Hornig B, Bertel O, Bonetti P, De Servi S,Brunner-La Rocca HP, Ricard I, Pfisterer M. Drug-eluting versus bare-metal stents in large coronary arteries. NEngl J Med 2010;363:2310–2319.226. Greenhalgh J, Hockenhull J, Rao N, Dundar Y, Dickson RC, Bagust A. Drug-eluting stents versus bare metalstents for angina or acute coronary syndromes. Cochrane Database Syst Rev 2010;5:CD004587.227. Vlaar PJ, Diercks GF, Svilaas T, Vogelzang M, de Smet BJ, van den Heuvel AF, Anthonio RL, Jessurun GA, TanES, Suurmeijer AJ, Zijlstra F. The feasibility and safety of routine thrombus aspiration in patients with non-STelevationmyocardial infarction. Catheter Cardiovasc Interv 2008;72:937–942.228. Rosengren A, Wallentin L, Simoons M, Gitt AK, Behar S, Battler A, Hasdai D. Age, clinical presentation, andoutcome of acute coronary syndromes in the Euroheart acute coronary syndrome survey. Eur Heart J2006;27:789–795.229. Bauer T, Koeth O, Junger C, Heer T, Wienbergen H, Gitt A, Zahn R, Senges J, Zeymer U. Effect of an invasivestrategy on in-hospital outcome in elderly patients with non-ST-elevation myocardial infarction. Eur Heart J2007;28:2873–2878.230. Alexander KP, Newby LK, Cannon CP, Armstrong PW, Gibler WB, Rich MW, Van de Werf F, White HD, WeaverWD, Naylor MD, Gore JM, Krumholz HM, Ohman EM. Acute coronary care in the elderly, part I: non-ST-segment-elevation acute coronary syndromes: a scientific statement for healthcare professionals from the AmericanHeart Association Council on Clinical Cardiology: in collaboration with the Society of Geriatric Cardiology.Circulation 2007;115:2549–2569.231. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED. Excess dosing of antiplatelet and antithrombin agents in the treatment of non-ST-segment elevationacute coronary syndromes. JAMA 2005;294:3108–3116.232. Lopes RD, Alexander KP, Marcucci G, White HD, Spinler S, Col J, Aylward PE, Califf RM, Mahaffey KW. Outcomesin elderly patients with acute coronary syndromes randomized to enoxaparin vs. unfractionated heparin:results from the SYNERGY trial. Eur Heart J 2008;29:1827–1833.233. Wallentin L, Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E. Outcome at 1 year after an invasive comparedwith a non-invasive strategy in unstable coronary-artery disease: the FRISC II invasive randomised trial. FRISCII Investigators. Fast Revascularisation during Instability in Coronary artery disease. Lancet 2000;356:9–16.234. Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E, Wallentin L. 5-Year outcomes in the FRISC-II randomisedtrial of an invasive versus a non-invasive strategy in non-ST-elevation acute coronary syndrome: a follow-upstudy. Lancet 2006;368:998–1004.235. Bach RG, Cannon CP, Weintraub WS, DiBattiste PM, Demopoulos LA, Anderson HV, DeLucca PT, Mahoney EM,Murphy SA, Braunwald E. The effect of routine, early invasive management on outcome for elderly patientswith non-ST-segment elevation acute coronary syndromes. Ann Intern Med 2004;141:186–195.236. Rosengren A, Wallentin L, Gitt AK, Behar S, Battler A, Hasdai D. Sex, age, and clinical presentation of acutecoronary syndromes. Eur Heart J 2004;25:663–670.237. Alfredsson J, Stenestrand U, Wallentin L, Swahn E. Gender differences in management and outcome in non-ST-elevation acute coronary syndrome. Heart 2007;93:1357–1362.238. Hvelplund A, Galatius S, Madsen M, Rasmussen JN, Rasmussen S, Madsen JK, Sand NP, Tilsted HH, ThayssenP, Sindby E, Hojbjerg S, Abildstrom SZ. Women with acute coronary syndrome are less invasively examined andsubsequently less treated than men. Eur Heart J 2010;31:684–690.239. Diercks DB, Owen KP, Kontos MC, Blomkalns A, Chen AY, Miller C, Wiviott S, Peterson ED. Gender differencesin time to presentation for myocardial infarction before and after a national women’s cardiovascular awarenesscampaign: a temporal analysis from the Can Rapid Risk Stratification of Unstable Angina Patients SuppressADverse Outcomes with Early Implementation (CRUSADE) and the National Cardiovascular Data RegistryAcute Coronary Treatment and Intervention Outcomes Network-Get with the Guidelines (NCDR ACTION Registry-GWTG). Am Heart J 2010;160:80–87 e83.240. Heer T, Gitt AK, Juenger C, Schiele R, Wienbergen H, Towae F, Gottwitz M, Zahn R, Zeymer U, Senges J. Genderdifferences in acute non-ST-segment elevation myocardial infarction. Am J Cardiol 2006;98:160–166.241. Bavry AA, Kumbhani DJ, Quiroz R, Ramchandani SR, Kenchaiah S, Antman EM. Invasive therapy along withglycoprotein IIb/IIIa inhibitors and intracoronary stents improves survival in non-ST-segment elevation acutecoronary syndromes: a meta-analysis and review of the literature. Am J Cardiol 2004;93:830–835.242. Fox KA, Poole-Wilson PA, Henderson RA, Clayton TC, Chamberlain DA, Shaw TR, Wheatley DJ, Pocock SJ. Interventionalversus conservative treatment for patients with unstable angina or non-ST-elevation myocardialinfarction: the British Heart Foundation RITA 3 randomised trial. Randomized Intervention Trial of unstableAngina. Lancet 2002;360:743–751.243. Hoenig MR, Doust JA, Aroney CN, Scott IA. Early invasive versus conservative strategies for unstable angina& non-ST-elevation myocardial infarction in the stent era. Cochrane Database Syst Rev 2006;3:CD004815.244. Glaser R, Herrmann HC, Murphy SA, Demopoulos LA, DiBattiste PM, Cannon CP, Braunwald E. Benefit of anearly invasive management strategy in women with acute coronary syndromes. JAMA2002;288:3124–3129.245. Boersma E, Harrington RA, Moliterno DJ, White H, Simoons ML. Platelet glycoprotein IIb/IIIa inhibitors inacute coronary syndromes. Lancet 2002;360:342–343.246. Berger JS, Elliott L, Gallup D, Roe M, Granger CB, Armstrong PW, Simes RJ, White HD, Van de Werf F, TopolEJ, Hochman JS, Newby LK, Harrington RA, Califf RM, Becker RC, Douglas PS. Sex differences in mortalityfollowing acute coronary syndromes. JAMA 2009;302:874–882.247. Bartnik M, Malmberg K, Norhammar A, Tenerz A, Ohrvik J, Ryden L. Newly detected abnormal glucose tolerance:an important predictor of long-term outcome after myocardial infarction. Eur Heart J2004;25:1990–1997.248. Dotevall A, Hasdai D, Wallentin L, Battler A, Rosengren A. Diabetes mellitus: clinical presentation and outcomein men and women with acute coronary syndromes. Data from the Euro Heart Survey ACS. Diabet Med2005;22:1542–1550. 249. Donahoe SM, Stewart GC, McCabe CH, Mohanavelu S, Murphy SA, Cannon CP, Antman EM. Diabetes andmortality following acute coronary syndromes. JAMA 2007;298:765–775.250. Hasin T, Hochadel M, Gitt AK, Behar S, Bueno H, Hasin Y. Comparison of treatment and outcome of acute coronarysyndrome in patients with versus patients without diabetes mellitus. Am J Cardiol 2009;103:772–778.251. De Caterina R, Madonna R, Sourij H, Wascher T. Glycaemic control in acute coronary syndromes: prognosticvalue and therapeutic options. Eur Heart J 2010;31:1557–1564.252. Graham I, Atar D, Borch-Johnsen K, Boysen G, Burell G, Cifkova R, Dallongeville J, De Backer G, Ebrahim S,Gjelsvik B, Herrmann-Lingen C, Hoes A, Humphries S, Knapton M, Perk J, Priori SG, Pyorala K, Reiner Z, RuilopeL, Sans-Menendez S, Scholte op Reimer W, Weissberg P, Wood D, Yarnell J, Zamorano JL, Walma E,Fitzgerald T, Cooney MT, Dudina A. European guidelines on cardiovascular disease prevention in clinical practice:executive summary: Fourth Joint Task Force of the European Society of Cardiology and Other Societies onCardiovascular Disease Prevention in Clinical Practice (Constituted by representatives of nine societies and byinvited experts). Eur Heart J 2007;28:2375–2414.253. Finfer S, Chittock DR, Su SY, Blair D, Foster D, Dhingra V, Bellomo R, Cook D, Dodek P, Henderson WR, HebertPC, Heritier S, Heyland DK, McArthur C, McDonald E, Mitchell I, Myburgh JA, Norton R, Potter J, RobinsonBG, Ronco JJ. Intensive versus conventional glucose control in critically ill patients. N Engl J Med2009;360:1283–1297.254. Diaz R, Goyal A, Mehta SR, Afzal R, Xavier D, Pais P, Chrolavicius S, Zhu J, Kazmi K, Liu L, Budaj A, Zubaid M,Avezum A, Ruda M, Yusuf S. Glucose–insulin–potassium therapy in patients with ST-segment elevation myocardialinfarction. JAMA 2007;298:2399–2405.255. Cannon CP, Weintraub WS, Demopoulos LA, Vicari R, Frey MJ, Lakkis N, Neumann FJ, Robertson DH, DeLuccaPT, DiBattiste PM, Gibson CM, Braunwald E. Comparison of early invasive and conservative strategies in patientswith unstable coronary syndromes treated with the glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med2001;344:1879–1887.256. Hlatky MA, Boothroyd DB, Bravata DM, Boersma E, Booth J, Brooks MM, Carrie D, Clayton TC, Danchin N,Flather M, Hamm CW, Hueb WA, Kahler J, Kelsey SF, King SB, Kosinski AS, Lopes N, McDonald KM, RodriguezA, Serruys P, Sigwart U, Stables RH, Owens DK, Pocock SJ. Coronary artery bypass surgery compared withpercutaneous coronary interventions for multivessel disease: a collaborative analysis of individual patient datafrom ten randomised trials. Lancet 2009;373:1190–1197.257. Chaitman BR, Hardison RM, Adler D, Gebhart S, Grogan M, Ocampo S, Sopko G, Ramires JA, Schneider D,Frye RL. The Bypass Angioplasty Revascularization Investigation 2 Diabetes randomized trial of different treatmentstrategies in type 2 diabetes mellitus with stable ischemic heart disease: impact of treatment strategy oncardiac mortality and myocardial infarction. Circulation 2009;120:2529–2540.258. Frye RL, August P, Brooks MM, Hardison RM, Kelsey SF, MacGregor JM, Orchard TJ, Chaitman BR, Genuth SM,Goldberg SH, Hlatky MA, Jones TL, Molitch ME, Nesto RW, Sako EY, Sobel BE. A randomized trial of therapiesfor type 2 diabetes and coronary artery disease. N Engl J Med 2009;360:2503–2515.259. Banning AP, Westaby S, Morice MC, Kappetein AP, Mohr FW, Berti S, Glauber M, Kellett MA, Kramer RS,Leadley K, Dawkins KD, Serruys PW. Diabetic and nondiabetic patients with left main and/or 3-vessel coronaryartery disease: comparison of outcomes with cardiac surgery and paclitaxel-eluting stents. J Am Coll Cardiol2010;55:1067–1075.260. Hannan EL, Wu C, Walford G, Culliford AT, Gold JP, Smith CR, Higgins RS, Carlson RE, Jones RH. Drug-elutingstents vs. coronary-artery bypass grafting in multivessel coronary disease. N Engl J Med 2008;358:331–341.261. Stettler C, Allemann S, Wandel S, Kastrati A, Morice MC, Schomig A, Pfisterer ME, Stone GW, Leon MB, de LezoJS, Goy JJ, Park SJ, Sabate M, Suttorp MJ, Kelbaek H, Spaulding C, Menichelli M, Vermeersch P, Dirksen MT,Cervinka P, De Carlo M, Erglis A, Chechi T, Ortolani P, Schalij MJ, Diem P, Meier B, Windecker S, Juni P. Drugeluting and bare metal stents in people with and without diabetes: collaborative network meta-analysis. BMJ2008;337:a1331.262. Wiviott SD, Braunwald E, Angiolillo DJ, Meisel S, Dalby AJ, Verheugt FW, Goodman SG, Corbalan R, PurdyDA, Murphy SA, McCabe CH, Antman EM. Greater clinical benefit of more intensive oral antiplatelet therapywith prasugrel in patients with diabetes mellitus in the trial to assess improvement in therapeutic outcomes byoptimizing platelet inhibition with prasugrel-Thrombolysis in Myocardial Infarction 38. Circulation2008;118:1626–1636.263. James S, Angiolillo DJ, Cornel JH, Erlinge D, Husted S, Kontny F, Maya J, Nicolau JC, Spinar J, Storey RF, StevensSR, Wallentin L. Ticagrelor vs. clopidogrel in patients with acute coronary syndromes and diabetes: a substudyfrom the PLATelet inhibition and patient Outcomes (PLATO) trial. Eur Heart J 2010;31:3006–3016.264. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Heeschen C, Hamm CW, Moliterno DJ, Califf RM, WhiteHD, Kleiman NS, Theroux P, Topol EJ. Platelet glycoprotein IIb/IIIa inhibitors reduce mortality in diabetic patientswith non-ST-segment-elevation acute coronary syndromes. Circulation 2001;104:2767–2771.265. Salpeter SR, Greyber E, Pasternak GA, Salpeter EE. Risk of fatal and nonfatal lactic acidosis with metformin usein type 2 diabetes mellitus. Cochrane Database Syst Rev 2010;4:CD002967.266. Hasdai D, Behar S, Wallentin L, Danchin N, Gitt AK, Boersma E, Fioretti PM, Simoons ML, Battler A. A prospectivesurvey of the characteristics, treatments and outcomes of patients with acute coronary syndromes in Europeand the Mediterranean basin; the Euro Heart Survey of Acute Coronary Syndromes (Euro Heart SurveyACS). Eur Heart J 2002;23:1190–1201.267. Goldenberg I, Subirana I, Boyko V, Vila J, Elosua R, Permanyer-Miralda G, Ferreira-Gonzalez I, Benderly M,Guetta V, Behar S, Marrugat J. Relation between renal function and outcomes in patients with non-ST-segmentelevation acute coronary syndrome: real-world data from the European Public Health Outcome Researchand Indicators Collection Project. Arch Intern Med 2010;170:888–895.268. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Relationbetween renal function, presentation, use of therapies and in-hospital complications in acute coronary syndrome:data from the SWEDEHEART register. J Intern Med 2010;268:40–49.269. Collet JP, Montalescot G, Agnelli G, Van de Werf F, Gurfinkel EP, Lopez-Sendon J, Laufenberg CV, Klutman M,Gowda N, Gulba D. Non-ST-segment elevation acute coronary syndrome in patients with renal dysfunction:benefit of low-molecular-weight heparin alone or with glycoprotein IIb/IIIa inhibitors on outcomes. The GlobalRegistry of Acute Coronary Events. Eur Heart J 2005;26:2285–2293.270. Fox KA, Bassand JP, Mehta SR, Wallentin L, Theroux P, Piegas LS, Valentin V, Moccetti T, Chrolavicius S, AfzalR, Yusuf S. Influence of renal function on the efficacy and safety of fondaparinux relative to enoxaparin in nonST-segment elevation acute coronary syndromes. Ann Intern Med 2007;147:304–310.271. James S, Budaj A, Aylward P, Buck KK, Cannon CP, Cornel JH, Harrington RA, Horrow J, Katus H, Keltai M, LewisBS, Parikh K, Storey RF, Szummer K, Wojdyla D, Wallentin L. Ticagrelor versus clopidogrel in acute coronary syndromesin relation to renal function: results from the Platelet Inhibition and Patient Outcomes (PLATO) trial.Circulation 2010;122:1056–1067.272. Pannu N, Wiebe N, Tonelli M. Prophylaxis strategies for contrast-induced nephropathy. JAMA2006;295:2765–2779.273. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Influenceof renal function on the effects of early revascularization in non-ST-elevation myocardial infarction: data fromthe Swedish Web-System for Enhancement and Development of Evidence-Based Care in Heart Disease EvaluatedAccording to Recommended Therapies (SWEDEHEART). Circulation 2009;120:851–858.274. Steg PG, Dabbous OH, Feldman LJ, Cohen-Solal A, Aumont MC, Lopez-Sendon J, Budaj A, Goldberg RJ, KleinW, Anderson FA Jr. Determinants and prognostic impact of heart failure complicating acute coronary syndromes:observations from the Global Registry of Acute Coronary Events (GRACE). Circulation2004;109:494–499.275. Dickstein K, Vardas PE, Auricchio A, Daubert JC, Linde C, McMurray J, Ponikowski P, Priori SG, Sutton R, vanVeldhuisen DJ, Vahanian A, Bax J, Ceconi C, Dean V, Filippatos G, Funck-Brentano C, Hobbs R, Kearney P, Mc-Donagh T, Popescu BA, Reiner Z, Sechtem U, Sirnes PA, Tendera M, Vardas P, Widimsky P, Anker SD, Blanc JJ,Gasparini M, Hoes AW, Israel CW, Kalarus Z, Merkely B, Swedberg K, Camm AJ. 2010 Focused Update of ESCGuidelines on device therapy in heart failure: an update of the 2008 ESC Guidelines for the diagnosis andtreatment of acute and chronic heart failure and the 2007 ESC guidelines for cardiac and resynchronizationtherapy. Developed with the special contribution of the Heart Failure Association and the European HeartRhythm Association. Eur Heart J 2010;31:2677–2687.276. Pitt B, Remme W, Zannad F, Neaton J, Martinez F, Roniker B, Bittman R, Hurley S, Kleiman J, Gatlin M.Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction.N Engl J Med 2003;348:1309–1321.277. Zannad F, McMurray JJ, Krum H, van Veldhuisen DJ, Swedberg K, Shi H, Vincent J, Pocock SJ, Pitt B. Eplerenonein patients with systolic heart failure and mild symptoms. N Engl J Med 2011;364:11–21.278. Moss AJ, Zareba W, Hall WJ, Klein H, Wilber DJ, Cannom DS, Daubert JP, Higgins SL, Brown MW, Andrews ML.Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction.N Engl J Med 2002;346:877–883.279. Diercks DB, Roe MT, Mulgund J, Pollack CV Jr., Kirk JD, Gibler WB, Ohman EM, Smith SC Jr., Boden WE, PetersonED. The obesity paradox in non-ST-segment elevation acute coronary syndromes: results from the CanRapid risk stratification of Unstable angina patients Suppress ADverse outcomes with Early implementation ofthe American College of Cardiology/American Heart Association Guidelines Quality Improvement Initiative.Am Heart J 2006;152:140–148.280. Steinberg BA, Cannon CP, Hernandez AF, Pan W, Peterson ED, Fonarow GC. Medical therapies and invasivetreatments for coronary artery disease by body mass: the ‘obesity paradox’ in the Get With The Guidelines database.Am J Cardiol 2007;100:1331–1335.281. Ong P, Athanasiadis A, Borgulya G, Voehringer M, Sechtem U. 3-Year follow-up of patients with coronary arteryspasm as cause of acute coronary syndrome: the CASPAR (coronary artery spasm in patients with acutecoronary syndrome) study follow-up. J Am Coll Cardiol 2011;57:147–152.282. Hasin T, Sorkin A, Markiewicz W, Hammerman H, Aronson D. Prevalence and prognostic significance of transient,persistent, and new-onset anemia after acute myocardial infarction. Am J Cardiol 2009;104:486–491.283. Bassand JP, Afzal R, Eikelboom J, Wallentin L, Peters R, Budaj A, Fox KA, Joyner CD, Chrolavicius S, GrangerCB, Mehta S, Yusuf S. Relationship between baseline haemoglobin and major bleeding complications in acutecoronary syndromes. Eur Heart J 2010;31:50–58.284. Chase AJ, Fretz EB, Warburton WP, Klinke WP, Carere RG, Pi D, Berry B, Hilton JD. Association of the arterialaccess site at angioplasty with transfusion and mortality: the M.O.R.T.A.L study (Mortality benefit Of ReducedTransfusion after percutaneous coronary intervention via the Arm or Leg). Heart 2008;94:1019–1025.285. Agostoni P, Biondi-Zoccai GG, de Benedictis ML, Rigattieri S, Turri M, Anselmi M, Vassanelli C, Zardini P, LouvardY, Hamon M. Radial versus femoral approach for percutaneous coronary diagnostic and interventional procedures;systematic overview and meta-analysis of randomized trials. J Am Coll Cardiol 2004;44:349–356.286. Alexander KP, Chen AY, Wang TY, Rao SV, Newby LK, LaPointe NM, Ohman EM, Roe MT, Boden WE, HarringtonRA, Peterson ED. Transfusion practice and outcomes in non-ST-segment elevation acute coronary syndromes.Am Heart J 2008;155:1047–1053.287. Hill SR, Carless PA, Henry DA, Carson JL, Hebert PC, McClelland DB, Henderson KM. Transfusion thresholdsand other strategies for guiding allogeneic red blood cell transfusion. Cochrane Database Syst Rev2002;2:CD002042.288. Mehran R, Rao SV, Bhatt DL, Gibson CM, Caixeta A, Eikelboom J, Kaul S, Wiviott SD, Menon V, Nikolsky E, SerebruanyV, Valgimigli M, Vranckx P, Taggart D, Sabik JF, Cutlip DE, Krucoff MW, Ohman EM, Steg PG, White H.Standardized bleeding definitions for cardiovascular clinical trials: a consensus report from the Bleeding AcademicResearch Consortium (BARC). Circulation 2011;123:2736–2747.289. Fox KA, Carruthers K, Steg PG, Avezum A, Granger CB, Montalescot G, Goodman SG, Gore JM, Quill AL,Eagle KA. Has the frequency of bleeding changed over time for patients presenting with an acute coronary syndrome?The global registry of acute coronary events. Eur Heart J 2010;31:667–675.290. Eikelboom JW, Mehta SR, Anand SS, Xie C, Fox KA, Yusuf S. Adverse impact of bleeding on prognosis in patientswith acute coronary syndromes. Circulation 2006;114:774–782.291. Budaj A, Eikelboom JW, Mehta SR, Afzal R, Chrolavicius S, Bassand JP, Fox KA, Wallentin L, Peters RJ, GrangerCB, Joyner CD, Yusuf S. Improving clinical outcomes by reducing bleeding in patients with non-ST-elevationacute coronary syndromes. Eur Heart J 2009;30:655–661.292. Mehran R, Pocock SJ, Stone GW, Clayton TC, Dangas GD, Feit F, Manoukian SV, Nikolsky E, Lansky AJ, KirtaneA, White HD, Colombo A, Ware JH, Moses JW, Ohman EM. Associations of major bleeding and myocardialinfarction with the incidence and timing of mortality in patients presenting with non-ST-elevation acute coronarysyndromes: a risk model from the ACUITY trial. Eur Heart J 2009;30:1457–1466.293. Antman EM, Wiviott SD, Murphy SA, Voitk J, Hasin Y, Widimsky P, Chandna H, Macias W, McCabe CH, BraunwaldE. Early and late benefits of prasugrel in patients with acute coronary syndromes undergoing percutaneouscoronary intervention: a TRITON-TIMI 38 (TRial to Assess Improvement in Therapeutic Outcomes byOptimizing Platelet InhibitioN with Prasugrel-Thrombolysis In Myocardial Infarction) analysis. J Am Coll Cardiol2008;51:2028–2033.294. Berger PB, Bhatt DL, Fuster V, Steg PG, Fox KA, Shao M, Brennan DM, Hacke W, Montalescot G, Steinhubl SR,Topol EJ. Bleeding complications with dual antiplatelet therapy among patients with stable vascular disease orrisk factors for vascular disease: results from the Clopidogrel for High Atherothrombotic Risk and IschemicStabilization, Management, and Avoidance (CHARISMA) trial. Circulation 2010;121:2575–2583.295. Sorensen R, Hansen ML, Abildstrom SZ, Hvelplund A, Andersson C, Jorgensen C, Madsen JK, Hansen PR,Kober L, Torp-Pedersen C, Gislason GH. Risk of bleeding in patients with acute myocardial infarction treatedwith different combinations of aspirin, clopidogrel, and vitamin K antagonists in Denmark: a retrospectiveanalysis of nationwide registry data. Lancet 2009;374:1967–1974. 296. Joyner CD, Peters RJ, Afzal R, Chrolavicius S, Mehta SR, Fox KA, Granger CB, Franzosi MG, Flather M, BudajA, Bassand JP, Yusuf S. Fondaparinux compared to enoxaparin in patients with acute coronary syndromeswithout ST-segment elevation: outcomes and treatment effect across different levels of risk. Am Heart J2009;157:502–508.297. Spencer FA, Moscucci M, Granger CB, Gore JM, Goldberg RJ, Steg PG, Goodman SG, Budaj A, FitzGerald G,Fox KA. Does comorbidity account for the excess mortality in patients with major bleeding in acute myocardialinfarction? Circulation 2007;116:2793–2801.298. Rao SV, Jollis JG, Harrington RA, Granger CB, Newby LK, Armstrong PW, Moliterno DJ, Lindblad L, Pieper K,Topol EJ, Stamler JS, Califf RM. Relationship of blood transfusion and clinical outcomes in patients with acutecoronary syndromes. JAMA 2004;292:1555–1562.299. Alexander KP, Peterson ED. Minimizing the risks of anticoagulants and platelet inhibitors. Circulation2010;121:1960–1970.300. Marso SP, Amin AP, House JA, Kennedy KF, Spertus JA, Rao SV, Cohen DJ, Messenger JC, Rumsfeld JS. Associationbetween use of bleeding avoidance strategies and risk of periprocedural bleeding among patients undergoingpercutaneous coronary intervention. JAMA 2010;303:2156–2164.301. Yank V, Tuohy CV, Logan AC, Bravata DM, Staudenmayer K, Eisenhut R, Sundaram V, McMahon D, Olkin I,McDonald KM, Owens DK, Stafford RS. Systematic review: benefits and harms of in-hospital use of recombinantfactor VIIa for off-label indications. Ann Intern Med 2011;154:529–540.302. Hebert PC, Wells G, Blajchman MA, Marshall J, Martin C, Pagliarello G, Tweeddale M, Schweitzer I, Yetisir E.A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. Transfusion Requirementsin Critical Care Investigators, Canadian Critical Care Trials Group. N Engl J Med1999;340:409–417.303. Singh AK, Szczech L, Tang KL, Barnhart H, Sapp S, Wolfson M, Reddan D. Correction of anemia with epoetinalfa in chronic kidney disease. N Engl J Med 2006;355:2085–2098.304. Menzin J, Wygant G, Hauch O, Jackel J, Friedman M. One-year costs of ischemic heart disease among patientswith acute coronary syndromes: findings from a multi-employer claims database. Curr Med Res Opin2008;24:461–468.305. Smith SC Jr., Allen J, Blair SN, Bonow RO, Brass LM, Fonarow GC, Grundy SM, Hiratzka L, Jones D, KrumholzHM, Mosca L, Pasternak RC, Pearson T, Pfeffer MA, Taubert KA. AHA/ACC guidelines for secondary preventionfor patients with coronary and other atherosclerotic vascular disease: 2006 update: endorsed by the NationalHeart, Lung, and Blood Institute. Circulation 2006;113:2363–2372.306. Chow CK, Jolly S, Rao-Melacini P, Fox KA, Anand SS, Yusuf S. Association of diet, exercise, and smoking modificationwith risk of early cardiovascular events after acute coronary syndromes. Circulation2010;121:750–758.307. Chew DP, Huynh LT, Liew D, Astley C, Soman A, Brieger D. Potential survival gains in the treatment of myocardialinfarction. Heart 2009;95:1844–1850.308. Ford ES, Ajani UA, Croft JB, Critchley JA, Labarthe DR, Kottke TE, Giles WH, Capewell S. Explaining the decreasein U.S. deaths from coronary disease, 1980–2000. N Engl J Med 2007;356:2388–2398.309. Dagenais GR, Pogue J, Fox K, Simoons ML, Yusuf S. Angiotensinconverting-enzyme inhibitors in stable vasculardisease without left ventricular systolic dysfunction or heart failure: a combined analysis of three trials.Lancet 2006;368:581–588.310. Danchin N, Cucherat M, Thuillez C, Durand E, Kadri Z, Steg PG. Angiotensinconverting enzyme inhibitors inpatients with coronary artery disease and absence of heart failure or left ventricular systolic dysfunction: anoverview of long-term randomized controlled trials. Arch Intern Med 2006;166:787–796.311. Yusuf S, Teo KK, Pogue J, Dyal L, Copland I, Schumacher H, Dagenais G, Sleight P, Anderson C. Telmisartan,ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008;358:1547–1559.312. Hulten E, Jackson JL, Douglas K, George S, Villines TC. The effect of early, intensive statin therapy on acute coronarysyndrome: a meta-analysis of randomized controlled trials. Arch Intern Med 2006;166:1814–1821.313. Cannon CP, Braunwald E, McCabe CH, Rader DJ, Rouleau JL, Belder R, Joyal SV, Hill KA, Pfeffer MA, Skene AM.Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med2004;350:1495–1504.314. Lopez-Sendon J, Swedberg K, McMurray J, Tamargo J, Maggioni AP, Dargie H, Tendera M, Waagstein F, KjekshusJ, Lechat P, Torp-Pedersen C. Expert consensus document on beta-adrenergic receptor blockers. Eur HeartJ 2004;25:1341–1362.315. Pfeffer MA, Braunwald E, Moye LA, Basta L, Brown EJ Jr., Cuddy TE, Davis BR, Geltman EM, Goldman S, FlakerGC, Klein M, Lamas GA, Packer M, Rouleau J, Rouleau JL, Rutherford J, Wertheimer JH, Hawkins CM. Effectof captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction.Results of the survival and ventricular enlargement trial. The SAVE Investigators. N Engl J Med1992;327:669–677.316. Torp-Pedersen C, Kober L. Effect of ACE inhibitor trandolapril on life expectancy of patients with reduced leftventricularfunction after acute myocardial infarction. TRACE Study Group. Trandolapril Cardiac Evaluation.Lancet 1999;354:9–12.317. Pfeffer MA, McMurray JJ, Velazquez EJ, Rouleau JL, Kober L, Maggioni AP, Solomon SD, Swedberg K, Van deWerf F, White H, Leimberger JD, Henis M, Edwards S, Zelenkofske S, Sellers MA, Califf RM. Valsartan, captopril,or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N EnglJ Med 2003;349:1893–1906.318. Fox KA, Steg PG, Eagle KA, Goodman SG, Anderson FA Jr., Granger CB, Flather MD, Budaj A, Quill A, GoreJM. Decline in rates of death and heart failure in acute coronary syndromes, 1999–2006. JAMA2007;297:1892–1900.319. Fox K, Garcia MA, Ardissino D, Buszman P, Camici PG, Crea F, Daly C, De Backer G, Hjemdahl P, Lopez-SendonJ, Marco J, Morais J, Pepper J, Sechtem U, Simoons M, Thygesen K, Priori SG, Blanc JJ, Budaj A, Camm J,Dean V, Deckers J, Dickstein K, Lekakis J, McGregor K, Metra M, Osterspey A, Tamargo J, Zamorano JL. Guidelineson the management of stable angina pectoris: executive summary: the Task Force on the Managementof Stable Angina Pectoris of the European Society of Cardiology. Eur Heart J 2006;27:1341–1381.320. Rahimi K, Watzlawek S, Thiele H, Secknus MA, Hayerizadeh BF, Niebauer J, Schuler G. Incidence, time course,and predictors of early malignant ventricular arrhythmias after non-ST-segment elevation myocardial infarctionin patients with early invasive treatment. Eur Heart J 2006;27:1706–1711.
Цели вторичной профилактики после ОКС/ИМ без подъема сегмента ST
Четвертый этап: методы реваскуляризацииЕсли при ангиографии выявлены атероматозныеизменения, однако отсутствует критический стеноз ко-ронарных артерий, показана медикаментозная терапия.Необходимо пересмотреть диагноз ОКС без подъема сег-мента ST с учетом других возможных причин появлениясимптомов. Однако отсутствие критического стеноза неисключает диагноз ОКС, если клинические симптомы ука-зывают на ишемическую боль в груди и определяютсябиомаркеры. В этом случае пациенты должны получатьлечение в соответствии с рекомендациями по ведениюпациентов с ОКС без подъема сегмента ST.Рекомендации по выбору метода реваскуляризацииу пациентов с ОКС без подъема сегмента ST соответ-ствуют рекомендациям по выбору метода плановоговмешательства. У пациента со стенозом одной коронар-ной артерии методом выбора является ЧКВ. У пациен-тов с поражением нескольких сосудов выбор между ЧКВи КШ должен быть индивидуальным в соответствии спротоколом лечебного учреждения. В некоторых слу-чаях оправданно ЧКВ на ведущей артерии и последую-щее плановое шунтирование других пораженных со-судов с учетом результатов оценки ишемии и/илифункционального резерва кровотока.Во время ЧКВ не следует менять антикоагулянты. Па-циентам, получавшим фондапаринукс, перед ЧКВ сле-дует добавить НФГ. Применение блокатора GP IIb/IIIaрецепторов оправданно при повышенном уровне тро-понинов или наличии ангиографических признаковтромба. Если планируется КШ, следует отменить бло-каторы P2Y12 рецепторов и отложить операцию, еслиэто позволяют клиническое состояние и ангиографиче-ские данные.Если ангиография указывает на невозможность ре-васкуляризации в связи с распространенностью и/илилокализацией поражений, необходимо усилить меди-каментозную терапию и назначить меры вторичной про-филактики.
Пятый этап: выписка из стационара и наблюдениепосле выпискиХотя большинство нежелательных событий у паци-ентов с ОКС без подъема сегмента ST наблюдают на ран-нем этапе, риск ИМ или смерти остается повышеннымв течение нескольких мес. После ранней реваскуляри-зации риск развития угрожающих жизни аритмийнизкий (2,5%); 80% из них развиваются в течение пер-вых 12 ч после появления симптомов [320]. Соответ-ственно, продолжение мониторирования после24-48 ч обычно не требуется. Пациенты с ОКС безподъема сегмента ST должны находиться в стациона-ре в течение по крайней мере 24 ч после успешного стен-тирования ведущего стеноза. Всем пациентам показа-ны интенсивная модификация риска и улучшение об-раза жизни (см. раздел 5.6.). Включение пациента в про-грамму реабилитации после выписки повышает при-верженность и может способствовать модификациифакторов риска. Необходимые меры профилактикипосле выписки из стационара указаны в табл. 15.
Литература
1. Murray CJ, Lopez AD. Alternative projections of mortality and disability by cause 1990–2020: Global Burden ofDisease Study. Lancet 1997;349:1498–1504. 2. Van deWerf F, Bax J, Betriu A, Blomstrom-Lundqvist C, Crea F, Falk V, Filippatos G, Fox K, Huber K, Kastrati A,Rosengren A, Steg PG, Tubaro M, Verheugt F, Weidinger F, Weis M. Management of acute myocardial infarctionin patients presenting with persistent ST-segment elevation: the Task Force on the Management of ST-SegmentElevation Acute Myocardial Infarction of the European Society of Cardiology. Eur Heart J 2008;29:2909–2945.3. Bassand JP, Hamm CW, Ardissino D, Boersma E, Budaj A, Fernandez-Aviles F, Fox KA, Hasdai D, Ohman EM,Wallentin L, Wijns W. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronarysyndromes. Eur Heart J 2007;28:1598–1660.4. Yeh RW, Sidney S, Chandra M, Sorel M, Selby JV, Go AS. Population trends in the incidence and outcomes of acutemyocardial infarction. N Engl J Med 2010;362:2155–2165.5. Fox KA, Eagle KA, Gore JM, Steg PG, Anderson FA. The Global Registry of Acute Coronary Events, 1999 to 2009—GRACE. Heart 2010;96:1095–1101.6. Savonitto S, Ardissino D, Granger CB, Morando G, Prando MD, Mafrici A, Cavallini C, Melandri G, Thompson TD,Vahanian A, Ohman EM, Califf RM, Van de Werf F, Topol EJ. Prognostic value of the admission electrocardiogramin acute coronary syndromes. JAMA 1999;281:707–713.7. Mandelzweig L, Battler A, Boyko V, Bueno H, Danchin N, Filippatos G, Gitt A, Hasdai D, Hasin Y, Marrugat J,Van de Werf F, Wallentin L, Behar S. The second Euro Heart Survey on acute coronary syndromes: characteristics,treatment, and outcome of patients with ACS in Europe and the Mediterranean Basin in 2004. Eur Heart J2006;27:2285–2293.8. Terkelsen CJ, Lassen JF, Norgaard BL, Gerdes JC, Jensen T, Gotzsche LB, Nielsen TT, Andersen HR. Mortality ratesin patients with ST-elevation vs. non-ST-elevation acute myocardial infarction: observations from an unselectedcohort. Eur Heart J 2005;26:18–26.9. Hamm CW, Mo¨llmann H, Bassand JP, Van deWerf F. Acute coronary syndrome. In: Camm AJ, Lu¨scher TF, SerruysPW, eds. The ESC Textbook of Cardiovascular Medicine. 2nd ed. Oxford: Oxford University Press; 2009.10. Stone GW, Maehara A, Lansky AJ, de Bruyne B, Cristea E, Mintz GS, Mehran R, McPherson J, Farhat N, MarsoSP, Parise H, Templin B, White R, Zhang Z, Serruys PW. A prospective natural-history study of coronary atherosclerosis.N Engl J Med 2011;364:226–235.11. Campeau L. Grading of angina pectoris. Circulation 1976;54:522–523.12. van Domburg RT, van Miltenburg-van Zijl AJ, Veerhoek RJ, Simoons ML. Unstable angina: good long-term outcomeafter a complicated early course. J Am Coll Cardiol 1998;31:1534–1539.13. Canto JG, Fincher C, Kiefe CI, Allison JJ, Li Q, Funkhouser E, Centor RM, Selker HP,Weissman NW. Atypical presentationsamong Medicare beneficiaries with unstable angina pectoris. Am J Cardiol 2002;90:248–253.14. Culic V, Eterovic D, Miric D, Silic N. Symptom presentation of acute myocardial infarction: influence of sex, age,and risk factors. Am Heart J 2002;144:1012–1017.15. Brieger D, Eagle KA, Goodman SG, Steg PG, Budaj A, White K, Montalescot G. Acute coronary syndromeswithout chest pain, an underdiagnosed and undertreated high-risk group: insights from the Global Registry ofAcute Coronary Events. Chest 2004;126:461–469.16. Lev EI, Battler A, Behar S, Porter A, Haim M, Boyko V, Hasdai D. Frequency, characteristics, and outcome of patientshospitalized with acute coronary syndromes with undetermined electrocardiographic patterns. Am J Cardiol2003;91:224–227.17. Diercks DB, Peacock WF, Hiestand BC, Chen AY, Pollack CV Jr., Kirk JD, Smith SC Jr., Gibler WB, Ohman EM,Blomkalns AL, Newby LK, Hochman JS, Peterson ED, Roe MT. Frequency and consequences of recording an electrocardiogram.10 min after arrival in an emergency room in non-ST-segment elevation acute coronary syndromes(from the CRUSADE Initiative). Am J Cardiol 2006;97:437–442.18. Thygesen K, Alpert JS, White HD, Jaffe AS, Apple FS, Galvani M, Katus HA, Newby LK, Ravkilde J, Chaitman B,Clemmensen PM, Dellborg M, Hod H, Porela P, Underwood R, Bax JJ, Beller GA, Bonow R, Van der Wall EE, BassandJP, Wijns W, Ferguson TB, Steg PG, Uretsky BF, Williams DO, Armstrong PW, Antman EM, Fox KA, HammCW, Ohman EM, Simoons ML, Poole-Wilson PA, Gurfinkel EP, Lopez-Sendon JL, Pais P, Mendis S, Zhu JR, WallentinLC, Fernandez-Aviles F, Fox KM, Parkhomenko AN, Priori SG, Tendera M, Voipio-Pulkki LM, Vahanian A,Camm AJ, De Caterina R, Dean V, Dickstein K, Filippatos G, Funck-Brentano C, Hellemans I, Kristensen SD, Mc-Gregor K, Sechtem U, Silber S, Widimsky P, Zamorano JL, Morais J, Brener S, Harrington R, Morrow D, Lim M,Martinez-Rios MA, Steinhubl S, Levine GN, Gibler WB, Goff D, Tubaro M, Dudek D, Al-Attar N. Universal definitionof myocardial infarction. Circulation 2007;116:2634–2653.19. Okamatsu K, Takano M, Sakai S, Ishibashi F, Uemura R, Takano T, Mizuno K. Elevated troponin T levels and lesioncharacteristics in non-ST-elevation acute coronary syndromes. Circulation 2004;109:465–470.20. Keller T, Zeller T, Peetz D, Tzikas S, Roth A, Czyz E, Bickel C, Baldus S, Warnholtz A, Frohlich M, Sinning CR,Eleftheriadis MS, Wild PS, Schnabel RB, Lubos E, Jachmann N, Genth-Zotz S, Post F, Nicaud V, Tiret L, LacknerKJ, Munzel TF, Blankenberg S. Sensitive troponin I assay in early diagnosis of acute myocardial infarction. N EnglJ Med 2009;361:868–877.21. Reichlin T, Hochholzer W, Bassetti S, Steuer S, Stelzig C, Hartwiger S, Biedert S, Schaub N, Buerge C, Potocki M,Noveanu M, Breidthardt T, Twerenbold R, Winkler K, Bingisser R, Mueller C. Early diagnosis of myocardial infarctionwith sensitive cardiac troponin assays. N Engl J Med 2009;361:858–867.22. Giannitsis E, Becker M, Kurz K, Hess G, Zdunek D, Katus HA. High-sensitivity cardiac troponin T for early predictionof evolving non-ST-segment elevation myocardial infarction in patients with suspected acute coronarysyndrome and negative troponin results on admission. Clin Chem 2010;56:642–650.23. Weber M, Bazzino O, Estrada JJN, Miguel R, Salzberg S, Fuselli JJ, Liebetrau C, Woelken M, Moellmann H, NefH, Hamm C. Improved diagnostic and prognostic performance of a new high-sensitive troponin T assay in patientswith acute coronary syndrome. Am Heart J 2011;162:81–88.24. Omland T, de Lemos JA, Sabatine MS, Christophi CA, Rice MM, Jablonski KA, Tjora S, Domanski MJ, Gersh BJ,Rouleau JL, Pfeffer MA, Braunwald E. A sensitive cardiac troponin T assay in stable coronary artery disease. NEngl J Med 2009;361:2538–2547.25. de Lemos JA, Drazner MH, Omland T, Ayers CR, Khera A, Rohatgi A, Hashim I, Berry JD, Das SR, Morrow DA,McGuire DK. Association of troponin T detected with a highly sensitive assay and cardiac structure and mortalityrisk in the general population. JAMA 2010;304:2503–2512.26. Otsuka T, Kawada T, Ibuki C, Seino Y. Association between high-sensitivity cardiac troponin T levels and thepredicted cardiovascular risk in middle-aged men without overt cardiovascular disease. Am Heart J2010;159:972–978.27. Thygesen K, Mair J, Katus H, Plebani M, Venge P, Collinson P, Lindahl B, Giannitsis E, Hasin Y, Galvani M, TubaroM, Alpert JS, Biasucci LM, Koenig W, Mueller C, Huber K, Hamm C, Jaffe AS. Recommendations for the use ofcardiac troponin measurement in acute cardiac care. Eur Heart J 2010;31:2197–2204.28. Apple FS, Murakami MM, Pearce LA, Herzog CA. Predictive value of cardiac troponin I and T for subsequentdeath in end-stage renal disease. Circulation 2002;106:2941–2945.29. Aviles RJ, Askari AT, Lindahl B, Wallentin L, Jia G, Ohman EM, Mahaffey KW, Newby LK, Califf RM, Simoons ML,Topol EJ, Berger P, Lauer MS. Troponin T levels in patients with acute coronary syndromes, with or without renaldysfunction. N Engl J Med 2002;346:2047–2052.30. Hamm CW, Goldmann BU, Heeschen C, Kreymann G, Berger J, Meinertz T. Emergency room triage of patientswith acute chest pain by means of rapid testing for cardiac troponin T or troponin I. N Engl J Med1997;337:1648–1653.31. Wu AH, Apple FS, Gibler WB, Jesse RL, Warshaw MM, Valdes R Jr. National Academy of Clinical BiochemistryStandards of Laboratory Practice: recommendations for the use of cardiac markers in coronary artery diseases.Clin Chem 1999;45:1104–1121.32. Than M, Cullen L, Reid CM, Lim SH, Aldous S, Ardagh MW, Peacock WF, Parsonage WA, Ho HF, Ko HF, KasliwalRR, Bansal M, Soerianata S, Hu D, Ding R, Hua Q, Seok-Min K, Sritara P, Sae-Lee R, Chiu TF, Tsai KC, Chu FY, ChenWK, Chang WH, Flaws DF, George PM, Richards AM. A 2-h diagnostic protocol to assess patients with chestpain symptoms in the Asia-Pacific region (ASPECT): a prospective observational validation study. Lancet2011;377:1077–1084.33. Cheitlin MD, Armstrong WF, Aurigemma GP, Beller GA, Bierman FZ, Davis JL, Douglas PS, Faxon DP, Gillam LD,Kimball TR, Kussmaul WG, Pearlman AS, Philbrick JT, Rakowski H, Thys DM, Antman EM, Smith SC Jr., AlpertJS, Gregoratos G, Anderson JL, Hiratzka LF, Hunt SA, Fuster V, Jacobs AK, Gibbons RJ, Russell RO. ACC/AHA/ASE2003 guideline update for the clinical application of echocardiography: summary article: a report of the AmericanCollege of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASE Committeeto Update the 1997 Guidelines for the Clinical Application of Echocardiography). Circulation2003;108:1146–1162.34. Nucifora G, Badano LP, Sarraf-Zadegan N, Karavidas A, Trocino G, Scaffidi G, Pettinati G, Astarita C, VysniauskasV, Gregori D, Ilerigelen B, Marinigh R, Fioretti PM. Comparison of early dobutamine stress echocardiography andexercise electrocardiographic testing for management of patients presenting to the emergency departmentwith chest pain. Am J Cardiol 2007;100:1068–1073.35. Kwong RY, Schussheim AE, Rekhraj S, Aletras AH, Geller N, Davis J, Christian TF, Balaban RS, Arai AE. Detectingacute coronary syndrome in the emergency department with cardiac magnetic resonance imaging. Circulation2003;107:531–537.36. Udelson JE, Beshansky JR, Ballin DS, Feldman JA, Griffith JL, Handler J, Heller GV, Hendel RC, Pope JH, RuthazerR, Spiegler EJ, Woolard RH, Selker HP. Myocardial perfusion imaging for evaluation and triage of patientswith suspected acute cardiac ischemia: a randomized controlled trial. JAMA 2002;288:2693–2700.37. Hoffmann U, Bamberg F, Chae CU, Nichols JH, Rogers IS, Seneviratne SK, Truong QA, Cury RC, Abbara S, ShapiroMD, Moloo J, Butler J, Ferencik M, Lee H, Jang IK, Parry BA, Brown DF, Udelson JE, Achenbach S, Brady TJ,Nagurney JT. Coronary computed tomography angiography for early triage of patients with acute chest pain:the ROMICAT (Rule Out Myocardial Infarction using Computer Assisted Tomography) trial. J Am Coll Cardiol2009;53:1642–1650.38. Rubinshtein R, Halon DA, Gaspar T, Jaffe R, Karkabi B, Flugelman MY, Kogan A, Shapira R, Peled N, Lewis BS.Usefulness of 64-slice cardiac computed tomographic angiography for diagnosing acute coronary syndromesand predicting clinical outcome in emergency department patients with chest pain of uncertain origin. Circulation2007;115:1762–1768.39. Meijboom WB, Mollet NR, Van Mieghem CA, Weustink AC, Pugliese F, van Pelt N, Cademartiri F, Vourvouri E,de Jaegere P, Krestin GP, de Feyter PJ 64-Slice CT coronary angiography in patients with non-ST elevation acutecoronary syndrome. Heart 2007;93:1386–1392.40. Hollander JE, Chang AM, Shofer FS, Collin MJ, Walsh KM, McCusker CM, Baxt WG, Litt HI. One-year outcomesfollowing coronary computerized tomographic angiography for evaluation of emergency department patientswith potential acute coronary syndrome. Acad Emerg Med 2009;16:693–698.41. Chang SA, Choi SI, Choi EK, Kim HK, Jung JW, Chun EJ, Kim KS, Cho YS, Chung WY, Youn TJ, Chae IH, Choi DJ,Chang HJ. Usefulness of 64-slice multidetector computed tomography as an initial diagnostic approach in patientswith acute chest pain. Am Heart J 2008;156:375–383.42. Effects of tissue plasminogen activator and a comparison of early invasive and conservative strategies in unstableangina and non-Q-wave myocardial infarction. Results of the TIMI IIIB Trial. Thrombolysis in Myocardial Ischemia.Circulation 1994;89:1545–1556.43. Invasive compared with non-invasive treatment in unstable coronary-artery disease: FRISC II prospective randomisedmulticentre study. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators.Lancet 1999;354:708–715.44. Tonino PA, De Bruyne B, Pijls NH, Siebert U, Ikeno F, van’ t Veer M, Klauss V, Manoharan G, Engstrom T, OldroydKG, Ver Lee PN, MacCarthy PA, Fearon WF. Fractional flow reserve versus angiography for guiding percutaneouscoronary intervention. N Engl J Med 2009;360:213–224.45. Jolly SS, Yusuf S, Cairns J, Niemela K, Xavier D, Widimsky P, Budaj A, Niemela M, Valentin V, Lewis BS, AvezumA, Steg PG, Rao SV, Gao P, Afzal R, Joyner CD, Chrolavicius S, Mehta SR. Radial versus femoral access for coronaryangiography and intervention in patients with acute coronary syndromes (RIVAL): a randomised, parallelgroup, multicentre trial. Lancet 2011;377:1409–1420.46. Hasdai D, Lev EI, Behar S, Boyko V, Danchin N, Vahanian A, Battler A. Acute coronary syndromes in patients withpre-existing moderate to severe valvular disease of the heart: lessons from the Euro-Heart Survey of acute coronarysyndromes. Eur Heart J 2003;24:623–629.47. Hasin Y, Danchin N, Filippatos GS, Heras M, Janssens U, Leor J, Nahir M, Parkhomenko A, Thygesen K, TubaroM, Wallentin LC, Zakke I. Recommendations for the structure, organization, and operation of intensive cardiaccare units. Eur Heart J 2005;26:1676–1682.48. Granger CB, Goldberg RJ, Dabbous O, Pieper KS, Eagle KA, Cannon CP, Van De Werf F, Avezum A, GoodmanSG, Flather MD, Fox KA. Predictors of hospital mortality in the global registry of acute coronary events. Arch InternMed 2003;163:2345–2353.49. Antman EM, Cohen M, Bernink PJ, McCabe CH, Horacek T, Papuchis G, Mautner B, Corbalan R, Radley D,Braunwald E. The TIMI risk score for unstable angina/non-ST elevation MI: a method for prognostication andtherapeutic decision making. JAMA 2000;284:835–842.50. Fox KA, Dabbous OH, Goldberg RJ, Pieper KS, Eagle KA, Van de Werf F, Avezum A, Goodman SG, Flather MD,Anderson FA Jr., Granger CB. Prediction of risk of death and myocardial infarction in the six months after presentationwith acute coronary syndrome: prospective multinational observational study (GRACE). BMJ2006;333:1091. 51. Carrillo X, Curos A, Muga R, Serra J, Sanvisens A, Bayes-Genis A. Acute coronary syndrome and cocaine use:8-year prevalence and inhospital outcomes. Eur Heart J 2011;32:1244–1250.52. Holmvang L, Clemmensen P, Lindahl B, Lagerqvist B, Venge P, Wagner G, Wallentin L, Grande P. Quantitativeanalysis of the admission electrocardiogram identifies patients with unstable coronary artery disease who benefitthe most from early invasive treatment. J Am Coll Cardiol 2003;41:905–915.53. Kaul P, Fu Y, Chang WC, Harrington RA, Wagner GS, Goodman SG, Granger CB, Moliterno DJ, Van de Werf F,Califf RM, Topol EJ, Armstrong PW. Prognostic value of ST segment depression in acute coronary syndromes:insights from PARAGON-A applied to GUSTO-IIb. PARAGON-A and GUSTO IIb Investigators. Platelet IIb/IIIa Antagonismfor the Reduction of Acute Global Organization Network. J Am Coll Cardiol 2001;38:64–71.54. Nyman I, Wallentin L, Areskog M, Areskog NH, Swahn E. Risk stratification by early exercise testing after anepisode of unstable coronary artery disease. The RISC Study Group. Int J Cardiol 1993;39:131–142.55. Amsterdam EA, Kirk JD, Diercks DB, Lewis WR, Turnipseed SD. Immediate exercise testing to evaluate low-riskpatients presenting to the emergency department with chest pain. J Am Coll Cardiol 2002;40:251–256.56. Scirica BM, Morrow DA, Budaj A, Dalby AJ, Mohanavelu S, Qin J, Aroesty J, Hedgepeth CM, Stone PH, BraunwaldE. Ischemia detected on continuous electrocardiography after acute coronary syndrome: observationsfrom the MERLIN-TIMI 36 (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST-Elevation AcuteCoronary Syndrome-Thrombolysis In Myocardial Infarction 36) trial. J Am Coll Cardiol 2009;53:1411–1421.57. Akkerhuis KM, Klootwijk PA, Lindeboom W, Umans VA, Meij S, Kint PP, Simoons ML. Recurrent ischaemia duringcontinuous multilead ST-segment monitoring identifies patients with acute coronary syndromes at highrisk of adverse cardiac events; meta-analysis of three studies involving 995 patients. Eur Heart J2001;22:1997–2006.58. Antman EM, Tanasijevic MJ, Thompson B, Schactman M, McCabe CH, Cannon CP, Fischer GA, Fung AY, ThompsonC, Wybenga D, Braunwald E. Cardiac-specific troponin I levels to predict the risk of mortality in patients withacute coronary syndromes. N Engl J Med 1996;335:1342–1349.59. Kontos MC, de Lemos JA, Ou FS, Wiviott SD, Foody JM, Newby LK, Chen A, Roe MT. Troponin-positive, MBnegativepatients with non-ST-elevation myocardial infarction: an undertreated but high-risk patient group:results from the National Cardiovascular Data Registry Acute Coronary Treatment and Intervention OutcomesNetwork—Get With The Guidelines (NCDR ACTION-GWTG) Registry. Am Heart J 2010;160:819–825.60. James SK, Lindahl B, Siegbahn A, Stridsberg M, Venge P, Armstrong P, Barnathan ES, Califf R, Topol EJ, SimoonsML, Wallentin L. N-terminal pro-brain natriuretic peptide and other risk markers for the separate prediction ofmortality and subsequent myocardial infarction in patients with unstable coronary artery disease: a Global Utilizationof Strategies To Open occluded arteries (GUSTO)-IV substudy. Circulation 2003;108:275–281.61. Steg PG, FitzGerald G, Fox KA. Risk stratification in non-ST-segment elevation acute coronary syndromes: troponinalone is not enough. Am J Med 2009;122: 107–108.62. Thygesen K, Mair J, Mueller C, Huber K, Weber M, Plebani M, Hasin Y, Biasucci LM, Giannitsis E, Lindahl B,Koenig W, Tubaro M, Collinson P, Katus H, Galvani M, Venge P, Alpert JS, Hamm C, Jaffe AS. Recommendationsfor the use of natriuretic peptides in acute cardiac care: a position statement from the Study Group on Biomarkersin Cardiology of the ESC Working Group on Acute Cardiac Care. Eur Heart J 2011;10.1093/eurheartj/ehq509.63. Heeschen C, Hamm CW, Bruemmer J, Simoons ML. Predictive value of Creactive protein and troponin T in patientswith unstable angina: a comparative analysis. CAPTURE Investigators. Chimeric c7E3 AntiPlatelet Therapyin Unstable angina REfractory to standard treatment trial. J Am Coll Cardiol 2000;35:1535–1542.64. Morrow DA, Rifai N, Antman EM, Weiner DL, McCabe CH, Cannon CP, Braunwald E. C-reactive protein is a potentpredictor of mortality independently of and in combination with troponin T in acute coronary syndromes:a TIMI 11A substudy. Thrombolysis in Myocardial Infarction. J Am Coll Cardiol 1998;31:1460–1465.65. Lindahl B, Toss H, Siegbahn A, Venge P, Wallentin L. Markers of myocardial damage and inflammation in relationto long-term mortality in unstable coronary artery disease. FRISC Study Group. Fragmin during Instabilityin Coronary Artery Disease. N Engl J Med 2000;343:1139–1147.66. Currie CJ, Poole CD, Conway P. Evaluation of the association between the first observation and the longitudinalchange in C-reactive protein, and all-cause mortality. Heart 2008;94:457–462.67. Aronson D, Hammerman H, Suleiman M, Markiewicz W. Usefulness of changes in fasting glucose during hospitalizationto predict long-term mortality in patients with acute myocardial infarction. Am J Cardiol2009;104:1013–1017.68. Suleiman M, Hammerman H, Boulos M, Kapeliovich MR, Suleiman A, Agmon Y, Markiewicz W, Aronson D. Fastingglucose is an important independent risk factor for 30-day mortality in patients with acute myocardial infarction:a prospective study. Circulation 2005;111:754–760.69. Sabatine MS, Morrow DA, Giugliano RP, Burton PB, Murphy SA, McCabe CH, Gibson CM, Braunwald E. Associationof hemoglobin levels with clinical outcomes in acute coronary syndromes. Circulation2005;111:2042–2049.70. Mahaffey KW, Yang Q, Pieper KS, Antman EM, White HD, Goodman SG, Cohen M, Kleiman NS, Langer A,Aylward PE, Col JJ, Reist C, Ferguson JJ, Califf RM. Prediction of one-year survival in high-risk patients withacute coronary syndromes: results from the SYNERGY trial. J Gen Intern Med 2008;23:310–316.71. Al Suwaidi J, Reddan DN, Williams K, Pieper KS, Harrington RA, Califf RM, Granger CB, Ohman EM, Holmes DRJr. Prognostic implications of abnormalities in renal function in patients with acute coronary syndromes. Circulation2002;106:974–980.72. Baldus S, Heeschen C, Meinertz T, Zeiher AM, Eiserich JP, Munzel T, Simoons ML, Hamm CW. Myeloperoxidaseserum levels predict risk in patients with acute coronary syndromes. Circulation 2003;108:1440–1445.73. Brennan ML, Penn MS, Van Lente F, Nambi V, Shishehbor MH, Aviles RJ, Goormastic M, Pepoy ML, McErleanES, Topol EJ, Nissen SE, Hazen SL. Prognostic value of myeloperoxidase in patients with chest pain. N Engl JMed 2003;349:1595–1604.74. Wollert KC, Kempf T, Peter T, Olofsson S, James S, Johnston N, Lindahl B, Horn-Wichmann R, Brabant G, SimoonsML, Armstrong PW, Califf RM, Drexler H, Wallentin L. Prognostic value of growth-differentiation factor-15 inpatients with non-ST-elevation acute coronary syndrome. Circulation 2007;115:962–971.75. Morrow DA, Sabatine MS, Brennan ML, de Lemos JA, Murphy SA, Ruff CT, Rifai N, Cannon CP, Hazen SL. Concurrentevaluation of novel cardiac biomarkers in acute coronary syndrome: myeloperoxidase and soluble CD40ligand and the risk of recurrent ischaemic events in TACTICS-TIMI 18. Eur Heart J 2008;29:1096–1102.76. Viswanathan K, Kilcullen N, Morrell C, Thistlethwaite SJ, Sivananthan MU, Hassan TB, Barth JH, Hall AS. Hearttypefatty acid-binding protein predicts long-term mortality and re-infarction in consecutive patients with suspectedacute coronary syndrome who are troponin-negative. J Am Coll Cardiol 2010;55:2590–2598.77. Van Belle E, Dallongeville J, Vicaut E, Degrandsart A, Baulac C, Montalescot G. Ischemia-modified albumin levelspredict long-term outcome in patients with acute myocardial infarction. The French Nationwide OPERAstudy. Am Heart J 2010;159:570–576.78. Reichlin T, Hochholzer W, Stelzig C, Laule K, Freidank H, Morgenthaler NG, Bergmann A, Potocki M, NoveanuM, Breidthardt T, Christ A, Boldanova T, Merki R, Schaub N, Bingisser R, Christ M, Mueller C. Incremental valueof copeptin for rapid rule out of acute myocardial infarction. J Am Coll Cardiol 2009;54:60–68.79. de Araujo Goncalves P, Ferreira J, Aguiar C, Seabra-Gomes R. TIMI, PURSUIT, and GRACE risk scores: sustainedprognostic value and interaction with revascularization in NSTE-ACS. Eur Heart J 2005;26:865–872.80. Aragam KG, Tamhane UU, Kline-Rogers E, Li J, Fox KA, Goodman SG, Eagle KA, Gurm HS. Does simplicitycompromise accuracy in ACS risk prediction? A retrospective analysis of the TIMI and GRACE risk scores. PLoSOne 2009;4:e7947.81. Eggers KM, Kempf T, Venge P, Wallentin L, Wollert KC, Lindahl B. Improving long-term risk prediction in patientswith acute chest pain: the Global Registry of Acute Coronary Events (GRACE) risk score is enhanced by selectednonnecrosis biomarkers. Am Heart J 2010;160:88–94.82. Khot UN, Jia G, Moliterno DJ, Lincoff AM, Khot MB, Harrington RA, Topol EJ. Prognostic importance of physicalexamination for heart failure in non-ST-elevation acute coronary syndromes: the enduring value of Killip classification.JAMA 2003;290:2174–2181.83. Subherwal S, Bach RG, Chen AY, Gage BF, Rao SV, Newby LK, Wang TY, Gibler WB, Ohman EM, Roe MT, PollackCV Jr., Peterson ED, Alexander KP. Baseline risk of major bleeding in non-ST-segment-elevation myocardialinfarction: the CRUSADE (Can Rapid risk stratification of Unstable angina patients Suppress ADverseoutcomes with Early implementation of the ACC/AHA Guidelines) Bleeding Score. Circulation2009;119:1873–1882.84. Mehran R, Pocock SJ, Nikolsky E, Clayton T, Dangas GD, Kirtane AJ, Parise H, Fahy M, Manoukian SV, Feit F,Ohman ME, Witzenbichler B, Guagliumi G, Lansky AJ, Stone GW. A risk score to predict bleeding in patients withacute coronary syndromes. J Am Coll Cardiol 2010;55:2556–2566.85. Yusuf S, Peto R, Lewis J, Collins R, Sleight P. Beta blockade during and after myocardial infarction: an overviewof the randomized trials. Prog Cardiovasc Dis 1985;27:335–371.86. Randomised trial of intravenous atenolol among 16 027 cases of suspected acute myocardial infarction: ISIS-1. First International Study of Infarct Survival Collaborative Group. Lancet 1986;2:57–66.87. Telford AM, Wilson C. Trial of heparin versus atenolol in prevention of myocardial infarction in intermediatecoronary syndrome. Lancet 1981;1:1225–1228.88. Lubsen J, Tijssen JG. Efficacy of nifedipine and metoprolol in the early treatment of unstable angina in the coronarycare unit: findings from the Holland Interuniversity Nifedipine/metoprolol Trial (HINT). Am J Cardiol1987;60:18A–25A.89. Yusuf S, Wittes J, Friedman L. Overview of results of randomized clinical trials in heart disease. I. Treatments followingmyocardial infarction. JAMA 1988;260:2088–2093.90. Metoprolol in acute myocardial infarction (MIAMI). A randomised placebocontrolled international trial. TheMIAMI Trial Research Group. Eur Heart J 1985;6:199–226.91. Miller CD, Roe MT, Mulgund J, Hoekstra JW, Santos R, Pollack CV Jr., Ohman EM, Gibler WB, Peterson ED. Impactof acute beta-blocker therapy for patients with non-ST-segment elevation myocardial infarction. Am JMed 2007;120:685–692.92. Brandler E, Paladino L, Sinert R. Does the early administration of beta-blockers improve the in-hospital mortalityrate of patients admitted with acute coronary syndrome? Acad Emerg Med 2010;17:1–10.93. Chen ZM, Pan HC, Chen YP, Peto R, Collins R, Jiang LX, Xie JX, Liu LS. Early intravenous then oral metoprolol in45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet2005;366:1622–1632.94. Borzak S, Cannon CP, Kraft PL, Douthat L, Becker RC, Palmeri ST, Henry T, Hochman JS, Fuchs J, Antman EM,McCabe C, Braunwald E. Effects of prior aspirin and anti-ischemic therapy on outcome of patients with unstableangina. TIMI 7 Investigators. Thrombin Inhibition in Myocardial Ischemia. Am J Cardiol 1998;81:678–681.95. Ambrosio G, Del Pinto M, Tritto I, Agnelli G, Bentivoglio M, Zuchi C, Anderson FA, Gore JM, Lopez-Sendon J,Wyman A, Kennelly BM, Fox KA. Chronic nitrate therapy is associated with different presentation and evolutionof acute coronary syndromes: insights from 52,693 patients in the Global Registry of Acute Coronary Events.Eur Heart J 2010;31:430–438.96. Cotter G, Faibel H, Barash P, Shemesh E, Moshkovitz Y, Metzkor E, Simovitz A, Miller R, Schlezinger Z, Golik A.High-dose nitrates in the immediate management of unstable angina: optimal dosage, route of administration,and therapeutic goals. Am J Emerg Med 1998;16:219–224.97. Theroux P, Taeymans Y, Morissette D, Bosch X, Pelletier GB, Waters DD. A randomized study comparing propranololand diltiazem in the treatment of unstable angina. J Am Coll Cardiol 1985;5:717–722.98. Parodi O, Simonetti I, Michelassi C, Carpeggiani C, Biagini A, L’Abbate A, Maseri A. Comparison of verapamiland propranolol therapy for angina pectoris at rest: a randomized, multiple-crossover, controlled trial in thecoronary care unit. Am J Cardiol 1986;57:899–906.99. Hansen JF. Treatment with verapamil after an acute myocardial infarction. Review of the Danish studies on verapamilin myocardial infarction (DAVIT I and II). Drugs 1991;42 Suppl 2:43–53.100. Moss AJ, Oakes D, Rubison M, McDermott M, Carleen E, Eberly S, Brown M. Effects of diltiazem on long-termoutcome after acute myocardial infarction in patients with and without a history of systemic hypertension.The Multicenter Diltiazem Postinfarction Trial Research Group. Am J Cardiol 1991;68:429–433.101. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina(IONA) randomised trial. Lancet 2002;359:1269–1275.102. Borer JS. Therapeutic effects of I(f) blockade: evidence and perspective. Pharmacol Res 2006;53:440–445.103. Morrow DA, Scirica BM, Karwatowska-Prokopczuk E, Murphy SA, Budaj A, Varshavsky S, Wolff AA, Skene A,McCabe CH, Braunwald E. Effects of ranolazine on recurrent cardiovascular events in patients with non-ST-elevationacute coronary syndromes: the MERLIN-TIMI 36 randomized trial. JAMA 2007;297:1775–1783.104. Theroux P, Ouimet H, McCans J, Latour JG, Joly P, Levy G, Pelletier E, Juneau M, Stasiak J, de Guise P, PelletierG, Rinzler D, Waters D. Aspirin, heparin, or both to treat acute unstable angina. N Engl J Med1988;319:1105–1111.105. Theroux P, Waters D, Qiu S, McCans J, de Guise P, Juneau M. Aspirin versus heparin to prevent myocardial infarctionduring the acute phase of unstable angina. Circulation 1993;88:2045–2048.106. Cairns JA, Gent M, Singer J, Finnie KJ, Froggatt GM, Holder DA, Jablonsky G, Kostok WJ, Melendez LJ, MyersMG, Sackett DL, Staley BJ, Tanser PH. Aspirin, sulfinpyrazone, or both in unstable angina. Results of a Canadianmulticenter trial. N Engl J Med 1985;313:1369–1375.107. Baigent C, Blackwell L, Collins R, Emberson J, Godwin J, Peto R, Buring J, Hennekens C, Kearney P, Meade T,Patrono C, Roncaglioni MC, Zanchetti A. Aspirin in the primary and secondary prevention of vascular disease:collaborative meta-analysis 108. Mehta SR, Tanguay JF, Eikelboom JW, Jolly SS, Joyner CD, Granger CB, Faxon DP, Rupprecht HJ, Budaj A,Avezum A, Widimsky P, Steg PG, Bassand JP, Montalescot G, Macaya C, Di Pasquale G, Niemela K, Ajani AE,White HD, Chrolavicius S, Gao P, Fox KA, Yusuf S. Double-dose versus standard-dose clopidogrel and highdoseversus low-dose aspirin in individuals undergoing percutaneous coronary intervention for acute coronarysyndromes (CURRENT-OASIS 7): a randomised factorial trial. Lancet 2010;376:1233–1243.109. Gislason GH, Jacobsen S, Rasmussen JN, Rasmussen S, Buch P, Friberg J, Schramm TK, Abildstrom SZ, KoberL, Madsen M, Torp-Pedersen C. Risk of death or reinfarction associated with the use of selective cyclooxygenase-2 inhibitors and nonselective nonsteroidal antiinflammatory drugs after acute myocardial infarction. Circulation2006;113:2906–2913.110. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Effects of clopidogrel in addition to aspirin inpatients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345:494–502.111. Yusuf S, Mehta SR, Zhao F, Gersh BJ, Commerford PJ, Blumenthal M, Budaj A, Wittlinger T, Fox KA. Early andlate effects of clopidogrel in patients with acute coronary syndromes. Circulation 2003;107:966–972.112. Ho PM, Peterson ED, Wang L, Magid DJ, Fihn SD, Larsen GC, Jesse RA, Rumsfeld JS. Incidence of death andacute myocardial infarction associated with stopping clopidogrel after acute coronary syndrome. JAMA2008;299:532–539.113. Fox KA, Mehta SR, Peters R, Zhao F, Lakkis N, Gersh BJ, Yusuf S. Benefits and risks of the combination of clopidogreland aspirin in patients undergoing surgical revascularization for non-ST-elevation acute coronary syndrome:the Clopidogrel in Unstable angina to prevent Recurrent ischemic Events (CURE) Trial. Circulation2004;110:1202–1208.114. Montalescot G, Sideris G, Meuleman C, Bal-dit-Sollier C, Lellouche N, Steg PG, Slama M, Milleron O, ColletJ-P, Henry P, Beygui F, Drouet L. A randomized comparison of high clopidogrel loading doses in patients withnon-ST-segment elevation acute coronary syndromes: the ALBION (Assessment of the Best Loading Dose ofClopidogrel to Blunt Platelet Activation, Inflammation and Ongoing Necrosis) Trial. J Am Coll Cardiol2006;48:931–938.115. Snoep JD, Hovens MM, Eikenboom JC, van der Bom JG, Jukema JW, Huisman MV. Clopidogrel nonresponsivenessin patients undergoing percutaneous coronary intervention with stenting: a systematic review andmeta-analysis. Am Heart J 2007;154:221–231.116. Aleil B, Jacquemin L, De Poli F, Zaehringer M, Collet J-P, Montalescot G, Cazenave J-P, Dickele M-C, MonassierJ-P, Gachet C. Clopidogrel 150 mg/day to overcome low responsiveness in patients undergoing elective percutaneouscoronary intervention: results from the VASP-02 (Vasodilator-Stimulated Phosphoprotein-02)Randomized Study. JACC Cardiovasc Interv 2008;1:631–638.117. The CURRENT-OASIS 7 Investigators. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes.N Engl J Med 2010;363:930–942.118. Taubert D, von Beckerath N, Grimberg G, Lazar A, Jung N, Goeser T, Kastrati A, Schomig A, Schomig E. Impactof P-glycoprotein on clopidogrel absorption. Clin Pharmacol Ther 2006;80:486–501.119. Mega JL, Close SL, Wiviott SD, Shen L, Walker JR, Simon T, Antman EM, Braunwald E, Sabatine MS. Geneticvariants in ABCB1 and CYP2C19 and cardiovascular outcomes after treatment with clopidogrel and prasugrelin the TRITON-TIMI 38 trial: a pharmacogenetic analysis. Lancet 2010;376:1312–1319.120. Mega JL, Simon T, Collet JP, Anderson JL, Antman EM, Bliden K, Cannon CP, Danchin N, Giusti B, Gurbel P,Horne BD, Hulot JS, Kastrati A, Montalescot G, Neumann FJ, Shen L, Sibbing D, Steg PG, Trenk D, Wiviott SD,Sabatine MS. Reduced-function CYP2C19 genotype and risk of adverse clinical outcomes among patientstreated with clopidogrel predominantly for PCI: a meta-analysis. JAMA 2010;304:1821–1830.121. Breet N, van Werkum J, Bouman H, Kelder J, Ruven H, Bal E, Deneer V, Harmsze A, van der Heyden J, RensingB, Suttorp M, Hackeng C, ten Berg J. Comparison of platelet function tests in predicting clinical outcomein patients undergoing coronary stent implantation. JAMA 2010;303:754–762.122. Geisler T, Langer H, Wydymus M, Gohring K, Zurn C, Bigalke B, Stellos K, May AE, Gawaz M. Low responseto clopidogrel is associated with cardiovascular outcome after coronary stent implantation. Eur Heart J2006;27:2420–2425.123. Trenk D, Hochholzer W, Fromm MF, Chialda LE, Pahl A, Valina CM, Stratz C, Schmiebusch P, Bestehorn HP,Buttner HJ, Neumann FJ. Cytochrome P450 2C19 681G.A polymorphism and high on-clopidogrel platelet reactivityassociated with adverse 1-year clinical outcome of elective percutaneous coronary intervention withdrug-eluting or bare-metal stents. J Am Coll Cardiol 2008;51:1925–1934.124. Price MJ, Berger PB, Teirstein PS, Tanguay JF, Angiolillo DJ, Spriggs D, Puri S, Robbins M, Garratt KN, BertrandOF, Stillablower ME, Aragon JR, Kandzari DE, Stinis CT, Lee MS, Manoukian SV, Cannon CP, Schork NJ, TopolEJ. Standard- vs high-dose clopidogrel based on platelet function testing after percutaneous coronary intervention:the GRAVITAS randomized trial. JAMA 2011;305:1097–1105.125. O’Donoghue ML, Braunwald E, Antman EM, Murphy SA, Bates ER, Rozenman Y, Michelson AD, HautvastRW, Ver Lee PN, Close SL, Shen L, Mega JL, Sabatine MS, Wiviott SD. Pharmacodynamic effect and clinical efficacyof clopidogrel and prasugrel with or without a proton-pump inhibitor: an analysis of two randomisedtrials. Lancet 2009;374:989–997.126. Abraham NS, Hlatky MA, Antman EM, Bhatt DL, Bjorkman DJ, Clark CB, Furberg CD, Johnson DA, Kahi CJ,Laine L, Mahaffey KW, Quigley EM, Scheiman J, Sperling LS, Tomaselli GF. ACCF/ACG/AHA 2010 Expert ConsensusDocument on the concomitant use of proton pump inhibitors and thienopyridines: a focused updateof the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelettherapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Expert ConsensusDocuments. Circulation 2010;122:2619–2633.127. Bhatt DL, Cryer BL, Contant CF, Cohen M, Lanas A, Schnitzer TJ, Shook TL, Lapuerta P, Goldsmith MA, LaineL, Scirica BM, Murphy SA, Cannon CP. Clopidogrel with or without omeprazole in coronary artery disease. NEngl J Med 2010;363:1909–1917.128. Wiviott SD, Trenk D, Frelinger AL, O’Donoghue M, Neumann F-J, Michelson AD, Angiolillo DJ, Hod H, MontalescotG, Miller DL, Jakubowski JA, Cairns R, Murphy SA, McCabe CH, Antman EM, Braunwald E, PRINCIPLE-TIMI 44 Investigators. Prasugrel compared with high loading- and maintenance-dose clopidogrel inpatients with planned percutaneous coronary intervention: the Prasugrel in Comparison to Clopidogrel for Inhibitionof Platelet Activation and Aggregation Thrombolysis in Myocardial Infarction 44 Trial. Circulation2007;116:2923–2932.129. Small DS, Farid NA, Payne CD, Weerakkody GJ, Li YG, Brandt JT, Salazar DE, Winters KJ. Effects of the protonpump inhibitor lansoprazole on the pharmacokinetics and pharmacodynamics of prasugrel and clopidogrel.J Clin Pharmacol 2008;48:475–484.130. Wiviott S, Braunwald E, McCabe C, Montalescot G, Ruzyllo W, Gottlieb S, Neumann F-J, Ardissino D, De ServiS, Murphy S, Riesmeyer J, Weerakkody G, Gibson C, Antman E. Prasugrel versus clopidogrel in patients withacute coronary syndromes. N Engl J Med 2007;357:2001–2015.131. Gurbel PA, Bliden KP, Butler K, Tantry US, Gesheff T, Wei C, Teng R, Antonino MJ, Patil SB, Karunakaran A,Kereiakes DJ, Paris C, Purdy D, Wilson V, Ledley GS, Storey RF. Randomized double-blind assessment of theONSET and OFFSet of the antiplatelet effects of ticagrelor versus clopidogrel in patients with stable coronaryartery disease: the ONSET/OFFSET Study. Circulation 2009;120:2577–2585.132. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C, Horrow J, Husted S, James S, Katus H,Mahaffey KW, Scirica BM, Skene A, Steg PG, Storey RF, Harrington RA, for the PLATO Investigators. Ticagrelorversus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361:1045–1057.133. Cannon C, Harrington R, James S, Ardissino D, Becker R, Emanuelsson H, Husted S, Katus H, Keltaih M, KhurmiN, Kontny F, Lewis B, Steg P, Storey R, Wojdyla D, Wallentin L, the PLATelet inhibition and patient Outcomes(PLATO) investigators. Ticagrelor compared with clopidogrel in acute coronary syndromes patients with aplanned invasive strategy (PLATO): a randomised double-blind study. Lancet 2010;375:283–293.134. Held C, Asenblad N, Bassand JP, Becker RC, Cannon CP, Claeys MJ, Harrington RA, Horrow J, Husted S, JamesSK, Mahaffey KW, Nicolau JC, Scirica BM, Storey RF, Vintila M, Ycas J, Wallentin L. Ticagrelor versus clopidogrelin patients with acute coronary syndromes undergoing coronary artery bypass surgery results from thePLATO (Platelet Inhibition and Patient Outcomes) Trial. J Am Coll Cardiol 2011;57:672–684.135. Husted S, Emanuelsson H, Heptinstall S, Sandset PM, Wickens M, Peters G. Pharmacodynamics, pharmacokinetics,and safety of the oral reversible P2Y12 antagonist AZD6140 with aspirin in patients with atherosclerosis:a double-blind comparison to clopidogrel with aspirin. Eur Heart J 2006;27:1038–1047.136. Cannon CP, Husted S, Harrington RA, Scirica BM, Emanuelsson H, Peters G, Storey RF. Safety, tolerability, andinitial efficacy of AZD6140, the First reversible oral adenosine diphosphate receptor antagonist, comparedwith clopidogrel, in patients with non-ST-segment elevation acute coronary syndrome: primary results of theDISPERSE-2 Trial. J Am Coll Cardiol 2007;50:1844–1851.137. Storey RF, Bliden K, Patil SB, Karunakaran A, Ecob R, Butler K, Teng R, Wei C, Tantry US, Gurbel P. Incidence ofdyspnea and assessment of cardiac and pulmonary function in patients with stable coronary artery disease receivingticagrelor, clopidogrel or placebo in the ONSET/OFFSET Study. J Am Coll Cardiol 2010;56:185–193.138. Berger JS, Frye CB, Harshaw Q, Edwards FH, Steinhubl SR, Becker RC. Impact of clopidogrel in patients withacute coronary syndromes requiring coronary artery bypass surgery: a multicenter analysis. J Am Coll Cardiol2008;52:1693–1701.139. Kapetanakis EI, Medlam DA, Boyce SW, Haile E, Hill PC, Dullum MK, Bafi AS, Petro KR, Corso PJ. Clopidogreladministration prior to coronary artery bypass grafting surgery: the cardiologist’s panacea or the surgeon’sheadache? Eur Heart J 2005;26:576–583.140. Mehta RH, Roe MT, Mulgund J, Ohman EM, Cannon CP, Gibler WB, Pollack CV Jr., Smith SC Jr., Ferguson TB,Peterson ED. Acute clopidogrel use and outcomes in patients with non-ST-segment elevation acute coronarysyndromes undergoing coronary artery bypass surgery. J Am Coll Cardiol 2006;48:281–286.141. Ebrahimi R, Dyke C, Mehran R, Manoukian SV, Feit F, Cox DA, Gersh BJ, Ohman EM, White HD, Moses JW,WareJH, Lincoff AM, Stone GW. Outcomes following pre-operative clopidogrel administration in patients with acutecoronary syndromes undergoing coronary artery bypass surgery: the ACUITY (Acute Catheterization and UrgentIntervention Triage strategY) Trial. J Am Coll Cardiol 2009;53:1965–1972.142. Kim JH, Newby LK, Clare RM, Shaw LK, Lodge AJ, Smith PK, Jolicoeur EM, Rao SV, Becker RC, Mark DB,Granger CB. Clopidogrel use and bleeding after coronary artery bypass graft surgery. Am Heart J2008;156:886–892.143. Fitchett D, Eikelboom J, Fremes S, Mazer D, Singh S, Bittira B, Brister S, Graham JJ, Gupta M, Karkouti K, LeeA, Love M, McArthur R, Peterson M, Verma S, Yau TM. Dual antiplatelet therapy in patients requiring urgentcoronary artery bypass grafting surgery: a position statement of the Canadian Cardiovascular Society. Can J Cardiol2009;25:683–689.144. Collet JP, Montalescot G, Blanchet B, Tanguy ML, Golmard JL, Choussat R, Beygui F, Payot L, Vignolles N, MetzgerJP, Thomas D. Impact of prior use or recent withdrawal of oral antiplatelet agents on acute coronary syndromes.Circulation 2004;110:2361–2367.145. Grines CL, Bonow RO, Casey DE Jr., Gardner TJ, Lockhart PB, Moliterno DJ, O’Gara P, Whitlow P. Prevention ofpremature discontinuation of dual antiplatelet therapy in patients with coronary artery stents: a science advisoryfrom the American Heart Association, American College of Cardiology, Society for Cardiovascular Angiographyand Interventions, American College of Surgeons, and American Dental Association, withrepresentation from the American College of Physicians. Circulation 2007;115:813–818.146. Mehta SR, Yusuf S, Peters RJ, Bertrand ME, Lewis BS, Natarajan MK, Malmberg K, Rupprecht H, Zhao F,Chrolavicius S, Copland I, Fox KA. Effects of pretreatment with clopidogrel and aspirin followed by long-termtherapy in patients undergoing percutaneous coronary intervention: the PCI-CURE study. Lancet2001;358:527–533.147. Steinhubl SR, Berger PB, Mann JT 3rd, Fry ET, DeLago A, Wilmer C, Topol EJ. Early and sustained dual oral antiplatelettherapy following percutaneous coronary intervention: a randomized controlled trial. JAMA2002;288:2411–2420.148. Wijns W, Kolh P, Danchin N, Di Mario C, Falk V, Folliguet T, Garg S, Huber K, James S, Knuuti J, Lopez-SendonJ, Marco J, Menicanti L, Ostojic M, Piepoli MF, Pirlet C, Pomar JL, Reifart N, Ribichini FL, Schalij MJ, SergeantP, Serruys PW, Silber S, Sousa Uva M, Taggart D. Guidelines on myocardial revascularization: the Task Force onMyocardial Revascularization of the European Society of Cardiology (ESC) and the European Association forCardio-Thoracic Surgery (EACTS). Eur Heart J 2010;31:2501–2555.149. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Moliterno DJ, Heeschen C, Hamm CW, Robbins MA,Kleiman NS, Theroux P, White HD, Topol EJ. Platelet glycoprotein IIb/IIIa inhibition in acute coronary syndromes.Gradient of benefit related to the revascularisation strategy. Eur Heart J 2002; 23:1441–1448.150. Stone GW, Bertrand ME, Moses JW, Ohman EM, Lincoff AM, Ware JH, Pocock SJ, McLaurin BT, Cox DA, JafarMZ, Chandna H, Hartmann F, Leisch F, Strasser RH, Desaga M, Stuckey TD, Zelman RB, Lieber IH, Cohen DJ,Mehran R, White HD. Routine upstream initiation vs deferred selective use of glycoprotein IIb/IIIa inhibitorsin acute coronary syndromes: the ACUITY Timing trial. JAMA 2007;297:591–602.151. Giugliano RP, White JA, Bode C, Armstrong PW, Montalescot G, Lewis BS, van’t Hof A, Berdan LG, Lee KL,Strony JT, Hildemann S, Veltri E, Van de Werf F, Braunwald E, Harrington RA, Califf RM, Newby LK, the EARLYACS Investigators. Early versus delayed, provisional eptifibatide in acute coronary syndromes. N Engl J Med2009;360:2176–2190.152. Kastrati A, Mehilli J, Neumann F-J, Dotzer F, ten Berg J, Bollwein H, Graf I, Ibrahim M, Pache J, Seyfarth M,Schuhlen H, Dirschinger J, Berger PB, Schomig A, for the Intracoronary Stenting, Antithrombotic Regimen:Rapid Early Action for Coronary Treatment 2 Trial I. Abciximab in patients with acute coronary syndromes undergoingpercutaneous coronary intervention after clopidogrel pretreatment: the ISAR-REACT 2 RandomizedTrial. JAMA 2006;295:1531–1538. 153. Dasgupta H, Blankenship JC, Wood GC, Frey CM, Demko SL, Menapace FJ. Thrombocytopenia complicatingtreatment with intravenous glycoprotein IIb/IIIa receptor inhibitors: a pooled analysis. Am Heart J2000;140:206–211.154. Jubelirer SJ, Koenig BA, Bates MC. Acute profound thrombocytopenia following C7E3 Fab (Abciximab) therapy:case reports, review of the literature and implications for therapy. Am J Hematol 1999;61:205–208.155. Lajus S, Clofent-Sanchez G, Jais C, Coste P, Nurden P, Nurden AT. Thrombocytopenia after abciximab use resultsfrom different mechanisms. Thromb Haemost 2010;103 651–661.156. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute coronary syndromes. ThePURSUIT Trial Investigators. Platelet glycoprotein IIb/IIIa in unstable angina: receptor suppression using integrilintherapy. N Engl J Med 1998;339:436–443.157. Merlini PA, Rossi M, Menozzi A, Buratti S, Brennan DM, Moliterno DJ, Topol EJ, Ardissino D. Thrombocytopeniacaused by abciximab or tirofiban and its association with clinical outcome in patients undergoing coronarystenting. Circulation 2004;109:2203–2206.158. Topol EJ, Moliterno DJ, Herrmann HC, Powers ER, Grines CL, Cohen DJ, Cohen EA, Bertrand M, Neumann FJ,Stone GW, DiBattiste PM, Yakubov SJ, DeLucca PT, Demopoulos L, the TARGET Investigators. Comparisonof two platelet glycoprotein IIb/IIIa inhibitors, tirofiban and abciximab, for the prevention of ischemic eventswith percutaneous coronary revascularization. N Engl J Med 2001;344:1888–1894.159. Moliterno DJ, Yakubov SJ, DiBattiste PM, Herrmann HC, Stone GW, Macaya C, Neumann F-J, Ardissino D,Bassand J-P, Borzi L. Outcomes at 6 months for the direct comparison of tirofiban and abciximab during percutaneouscoronary revascularisation with stent placement: the TARGET follow-up study. Lancet2002;360:355–360.160. De Luca G, Ucci G, Cassetti E, Marino P. Benefits from small molecule administration as compared with abciximabamong patients with ST-segment elevation myocardial infarction treated with primary angioplasty: ameta-analysis. J Am Coll Cardiol 2009;53:1668–1673.161. Valgimigli M, Biondi-Zoccai G, Tebaldi M, van’t Hof AWJ, Campo G, Hamm C, ten Berg J, Bolognese L, Saia F,Danzi GB, Briguori C, Okmen E, King SB, Moliterno DJ, Topol EJ. Tirofiban as adjunctive therapy for acutecoronary syndromes and percutaneous coronary intervention: a meta-analysis of randomized trials. Eur HeartJ 2010;31:35–49.162. O’Donoghue M, Antman EM, Braunwald E, Murphy SA, Steg PG, Finkelstein A, Penny WF, Fridrich V, McCabeCH, Sabatine MS, Wiviott SD. The efficacy and safety of prasugrel with and without a glycoprotein IIb/IIIa inhibitorin patients with acute coronary syndromes undergoing percutaneous intervention: a TRITON-TIMI 38(Trial to Assess Improvement in Therapeutic Outcomes by Optimizing Platelet Inhibition With Prasugrel-ThrombolysisIn Myocardial Infarction 38) analysis. J Am Coll Cardiol 2009;54:678–685.163. Buller C, Pate G, Armstrong P, O’Neill B, Webb J, Gallo R, Welsh R. Catheter thrombosis during primary percutaneouscoronary intervention for acute ST elevation myocardial infarction despite subcutaneous low-molecular-weight heparin, acetylsalicylic acid, clopidogrel and abciximab pretreatment. Can J Cardiol2006;22:511–515.164. Jolly SS, Faxon DP, Fox KA, Afzal R, Boden WE, Widimsky P, Steg PG, Valentin V, Budaj A, Granger CB, JoynerCD, Chrolavicius S, Yusuf S, Mehta SR. Efficacy and safety of fondaparinux versus enoxaparin in patients withacute coronary syndromes treated with glycoprotein IIb/IIIa inhibitors or thienopyridines: results from theOASIS 5 (Fifth Organization to Assess Strategies in Ischemic Syndromes) trial. J Am Coll Cardiol2009;54:468–476.165. White HD, Ohman EM, Lincoff AM, Bertrand ME, Colombo A, McLaurin BT, Cox DA, Pocock SJ, Ware JA,Manoukian SV, Lansky AJ, Mehran R, Moses JW, Stone GW. Safety and efficacy of bivalirudin with and withoutglycoprotein IIb/IIIa inhibitors in patients with acute coronary syndromes undergoing percutaneous coronaryintervention: 1-year results from the ACUITY (Acute Catheterization and Urgent Intervention TriagestrategY) trial. J Am Coll Cardiol 2008;52:807–814.166. Lincoff AM, Steinhubl SR, Manoukian SV, Chew D, Pollack CV Jr, Feit F,Ware JH, Bertrand ME, Ohman EM,DesmetW, Cox DA, Mehran R, Stone GW. Influence of timing of clopidogrel treatment on the efficacy andsafety of bivalirudin in patients with non-ST-segment elevation acute coronary syndromes undergoing percutaneouscoronary intervention: an analysis of the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. JACC Cardiovasc Interv 2008;1:639–648.167. Brieger D, Van de Werf F, Avezum A, Montalescot G, Kennelly B, Granger CB, Goodman SG, Dabbous O, AgnelliG. Interactions between heparins, glycoprotein IIb/IIIa antagonists, and coronary intervention. The GlobalRegistry of Acute Coronary Events (GRACE). Am Heart J 2007;153:960–969.168. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED, for the CRUSADE Investigators. Excess dosing of antiplatelet and antithrombin agents in thetreatment of non-ST-segment elevation acute coronary syndromes. JAMA 2005;294:3108–3116.169. Li Y, Spencer F, Becker R. Comparative efficacy of fibrinogen and platelet supplementation on the in vitro reversibilityof competitive glycoprotein IIb/IIIa receptor-directed platelet inhibition. Am Heart J2002;143:725–732.170. Neumann FJ, Kastrati A, Pogatsa-Murray G, Mehilli J, Bollwein H, Bestehorn HP, Schmitt C, Seyfarth M,Dirschinger J, Schomig A. Evaluation of prolonged antithrombotic pretreatment (‘cooling-off’ strategy) beforeintervention in patients with unstable coronary syndromes: a randomized controlled trial. JAMA2003;290:1593–1599.171. Harrington RA, Becker RC, Cannon CP, Gutterman D, Lincoff AM, Popma JJ, Steg G, Guyatt GH, Goodman SG.Antithrombotic therapy for non-ST-segment elevation acute coronary syndromes: American College of ChestPhysicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008;133:670S–707S.172. Eikelboom JW, Anand SS, Malmberg K, Weitz JI, Ginsberg JS, Yusuf S. Unfractionated heparin and low-molecular-weight heparin in acute coronary syndrome without ST elevation: a meta-analysis. Lancet2000;355:1936–1942.173. Simoons ML, Bobbink IW, Boland J, Gardien M, Klootwijk P, Lensing AW, Ruzyllo W, Umans VA, Vahanian A,Van De Werf F, Zeymer U; PENTUA Investigators. A dose-finding study of fondaparinux in patients with non-ST-segment elevation acute coronary syndromes: the Pentasaccharide in Unstable Angina (PENTUA) Study.J Am Coll Cardiol 2004;43:2183–2190.174. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Effects of fondaparinux on mortality and reinfarction in patients with acute ST-segment elevationmyocardial infarction: the OASIS-6 randomized trial. JAMA 2006;295:1519–1530.175. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Comparison of fondaparinux and enoxaparin in acute coronary syndromes. N Engl J Med2006;354:1464–1476.176. Mehta SR, Steg PG, Granger CB, Bassand JP, Faxon DP,Weitz JI, Afzal R, Rush B, Peters RJ, Natarajan MK,Velianou JL, Goodhart DM, Labinaz M, Tanguay JF, Fox KA, Yusuf S. Randomized, blinded trial comparingfondaparinux with unfractionated heparin in patients undergoing contemporary percutaneous coronary intervention:Arixtra Study in Percutaneous Coronary Intervention: a Randomized Evaluation (ASPIRE) pilot trial.Circulation 2005;111:1390–1397.177. Anderson JA, Hirsh J, Yusuf S, Johnston M, Afzal R, Mehta SR, Fox KA, Budaj A, Eikelboom JW. Comparisonof the anticoagulant intensities of fondaparinux and enoxaparin in the Organization to Assess Strategies inAcute Ischemic Syndromes (OASIS)-5 trial. J Thromb Haemost 2010;8:243–249.178. Steg PG, Jolly SS, Mehta SR, Afzal R, Xavier D, Rupprecht HJ, Lopez-Sendon JL, Budaj A, Diaz R, Avezum A,Widimsky P, Rao SV, Chrolavicius S, Meeks B, Joyner C, Pogue J, Yusuf S. Low-dose vs standard-dose unfractionatedheparin for percutaneous coronary intervention in acute coronary syndromes treated with fondaparinux:the FUTURA/OASIS-8 randomized trial. JAMA 2010;304:1339–1349.179. Antman EM, McCabe CH, Gurfinkel EP, Turpie AG, Bernink PJ, Salein D, Bayes De Luna A, Fox K, Lablanche JM,Radley D, Premmereur J, Braunwald E. Enoxaparin prevents death and cardiac ischemic events in unstableangina/non-Q-wave myocardial infarction. Results of the thrombolysis in myocardial infarction (TIMI) 11Btrial. Circulation 1999;100:1593–1601.180. Cohen M, Demers C, Gurfinkel EP, Turpie AG, Fromell GJ, Goodman S, Langer A, Califf RM, Fox KA, PremmereurJ, Bigonzi F. A comparison of low-molecular-weight heparin with unfractionated heparin for unstablecoronary artery disease. Efficacy and Safety of Subcutaneous Enoxaparin in Non-Q-Wave Coronary EventsStudy Group. N Engl J Med 1997;337:447–452.181. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators. Long-term lowmolecular-mass heparin in unstable coronary-artery disease: FRISC II prospective randomised multicentrestudy. Lancet 1999;354:701–707.182. Fragmin during Instability in Coronary Artery Disease (FRISC) study group. Low-molecular-weight heparinduring instability in coronary artery disease Lancet 1996;347:561–568.183. Hirsh J, Raschke R. Heparin and low-molecular-weight heparin: the Seventh ACCP Conference on Antithromboticand Thrombolytic Therapy. Chest 2004;126:188S–203S.184. TIMI 11A Investigators. Dose-ranging trial of enoxaparin for unstable angina: results of TIMI 11A. The Thrombolysisin Myocardial Infarction (TIMI) 11A Trial Investigators. J Am Coll Cardiol 1997;29:1474–1482.185. Montalescot G, Collet JP, Tanguy ML, Ankri A, Payot L, Dumaine R, Choussat R, Beygui F, Gallois V, Thomas D.Anti-Xa activity relates to survival and efficacy in unselected acute coronary syndrome patients treated withenoxaparin. Circulation 2004;110:392–398.186. Choussat R, Montalescot G, Collet JP, Vicaut E, Ankri A, Gallois V, Drobinski G, Sotirov I, Thomas D. A unique,low dose of intravenous enoxaparin in elective percutaneous coronary intervention. J Am Coll Cardiol2002;40:1943–1950.187. Collet JP, Montalescot G, Lison L, Choussat R, Ankri A, Drobinski G, Sotirov I, Thomas D. Percutaneous coronaryintervention after subcutaneous enoxaparin pretreatment in patients with unstable angina pectoris. Circulation2001;103:658–663.188. Murphy S, Gibson C, Morrow D, Van de Werf F, Menown I, Goodman S, Mahaffey K, Cohen M, McCabe C,Antman EM, Braunwald E. Efficacy and safety of the low-molecular weight heparin enoxaparin comparedwith unfractionated heparin across the acute coronary syndrome spectrum: a meta-analysis.Eur Heart J2007;28:2077–2086.189. Blazing MA, de Lemos JA, White HD, Fox KA, Verheugt FW, Ardissino D, DiBattiste PM, Palmisano J, BilheimerDW, Snapinn SM, Ramsey KE, Gardner LH, Hasselblad V, Pfeffer MA, Lewis EF, Braunwald E, Califf RM. Safetyand efficacy of enoxaparin vs unfractionated heparin in patients with non-ST-segment elevation acute coronarysyndromes who receive tirofiban and aspirin: a randomized controlled trial. JAMA 2004;292:55–64.190. Cohen M, Theroux P, Borzak S, Frey MJ, White HD, Van Mieghem W, Senatore F, Lis J, Mukherjee R, Harris K,Bigonzi F. Randomized double-blind safety study of enoxaparin versus unfractionated heparin in patients withnon-ST-segment elevation acute coronary syndromes treated with tirofiban and aspirin: the ACUTE II study.The Antithrombotic Combination Using Tirofiban and Enoxaparin. Am Heart J 2002;144:470–477.191. Goodman SG, Fitchett D, Armstrong PW, Tan M, Langer A. Randomized evaluation of the safety and efficacyof enoxaparin versus unfractionated heparin in high-risk patients with non-ST-segment elevation acute coronarysyndromes receiving the glycoprotein IIb/IIIa inhibitor eptifibatide. Circulation 2003;107:238–244.192. Ferguson JJ, Califf RM, Antman EM, Cohen M, Grines CL, Goodman S, Kereiakes DJ, Langer A, Mahaffey KW,Nessel CC, Armstrong PW, Avezum A, Aylward P, Becker RC, Biasucci L, Borzak S, Col J, Frey MJ, Fry E, GulbaDC, Guneri S, Gurfinkel E, Harrington R, Hochman JS, Kleiman NS, Leon MB, Lopez-Sendon JL, Pepine CJ,Ruzyllo W, Steinhubl SR, Teirstein PS, Toro-Figueroa L, White H. Enoxaparin vs unfractionated heparin in highriskpatients with non-ST-segment elevation acute coronary syndromes managed with an intended early invasivestrategy: primary results of the SYNERGY randomized trial. JAMA 2004;292:45–54.193. Petersen JL, Mahaffey KW, Hasselblad V, Antman EM, Cohen M, Goodman SG, Langer A, Blazing MA, Le-Moigne-Amrani A, de Lemos JA, Nessel CC, Harrington RA, Ferguson JJ, Braunwald E, Califf RM. Efficacy andbleeding complications among patients randomized to enoxaparin or unfractionated heparin for antithrombintherapy in non-ST-Segment elevation acute coronary syndromes: a systematic overview. JAMA2004;292:89–96.194. Sanchez-Pena P, Hulot JS, Urien S, Ankri A, Collet JP, Choussat R, Lechat P, Montalescot G. Anti-factor Xa kineticsafter intravenous enoxaparin in patients undergoing percutaneous coronary intervention: a populationmodel analysis. Br J Clin Pharmacol 2005;60:364–373.195. Montalescot G, White HD, Gallo R, Cohen M, Steg PG, Aylward PE, Bode C, Chiariello M, King SB 3rd, HarringtonRA, Desmet WJ, Macaya C, Steinhubl SR. Enoxaparin versus unfractionated heparin in elective percutaneouscoronary intervention. N Engl J Med 2006;355:1006–1017.196. Stone GW, McLaurin BT, Cox DA, Bertrand ME, Lincoff AM, Moses JW, White HD, Pocock SJ, Ware JH, Feit F,Colombo A, Aylward PE, Cequier AR, Darius H, Desmet W, Ebrahimi R, Hamon M, Rasmussen LH, RupprechtHJ, Hoekstra J, Mehran R, Ohman EM; ACUITY Investigators. Bivalirudin for patients with acute coronary syndromes.N Engl J Med 2006;355:2203–2216.197. Stone GW, White HD, Ohman EM, Bertrand ME, Lincoff AM, McLaurin BT, Cox DA, Pocock SJ, Ware JH, FeitF, Colombo A, Manoukian SV, Lansky AJ, Mehran R, Moses JW. Acute Catheterization and Urgent InterventionTriage strategy (ACUITY) trial investigators. Bivalirudin in patients with acute coronary syndromes undergoingpercutaneous coronary intervention: a subgroup analysis from the Acute Catheterization and UrgentIntervention Triage strategy (ACUITY) trial. Lancet 2007;369:907–919.198. Stone G, Ware J, Bertrand M, Lincoff A, Moses J, Ohman E, White H, Feit F, Colombo A, McLaurin B, Cox D,Manoukian S, Fahy M, Clayton T, Mehran R, Pocock S. For the ACUITY Investigators. Antithrombotic strategiesin patients with acute coronary syndromes undergoing early invasive management: one-year results fromthe ACUITY trial. JAMA 2007;298:2497–2506. 199. White HD, Chew DP, Hoekstra JW, Miller CD, Pollack CV Jr., Feit F, Lincoff AM, Bertrand M, Pocock S, Ware J,Ohman EM, Mehran R, Stone GW. Safety and efficacy of switching from either unfractionated heparin orenoxaparin to bivalirudin in patients with non-ST-segment elevation acute coronary syndromes managedwith an invasive strategy: results from the ACUITY (Acute Catheterization and Urgent Intervention Triage strategY)trial. J Am Coll Cardiol 2008;51:1734–1741.200. Alexander JH, Becker RC, Bhatt DL, Cools F, Crea F, Dellborg M, Fox KA, Goodman SG, Harrington RA, HuberK, Husted S, Lewis BS, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, WallentinL. Apixaban, an oral, direct, selective factor Xa inhibitor, in combination with antiplatelet therapy after acutecoronary syndrome: results of the Apixaban for Prevention of Acute Ischemic and Safety Events (APPRAISE)trial. Circulation 2009;119:2877–2885.201. Mega JL, Braunwald E, Mohanavelu S, Burton P, Poulter R, Misselwitz F, Hricak V, Barnathan ES, Bordes P,Witkowski A, Markov V, Oppenheimer L, Gibson CM. Rivaroxaban versus placebo in patients with acute coronarysyndromes (ATLAS ACS-TIMI 46): a randomised, double-blind, phase II trial. Lancet 2009;374:29–38.202. Alexander J, Becker R, Bhatt D, Cools F, Crea F, Dellborg M, Fox K, Goodman S, Harrington R, Huber K, HustedS, Lewis B, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, Wallentin L. For the APPRAISESteering Committee and Investigators. Apixaban, an oral, direct, selective factor Xa inhibitor, in combinationwith antiplatelet therapy after acute coronary syndrome: results of the Apixaban for Prevention ofAcute Ischemic and Safety Events (APPRAISE) trial. Circulation 2009;119:2877–2885.203. Sabatine MS, Antman EM, Widimsky P, Ebrahim IO, Kiss RG, Saaiman A, Polasek R, Contant CF, McCabe CH,Braunwald E. Otamixaban for the treatment of patients with non-ST-elevation acute coronary syndromes(SEPIA-ACS1 TIMI 42): a randomised, double-blind, active-controlled, phase 2 trial. Lancet2009;374:787–795.204. Lip GY, Huber K, Andreotti F, Arnesen H, Airaksinen JK, Cuisset T, Kirchhof P, Marin F. Antithrombotic managementof atrial fibrillation patients presenting with acute coronary syndrome and/or undergoing coronarystenting: executive summary—a Consensus Document of the European Society of Cardiology Working Groupon Thrombosis, endorsed by the European Heart Rhythm Association (EHRA) and the European Associationof Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2010;31:1311–1318.205. Yan AT, Yan RT, Tan M, Eagle KA, Granger CB, Dabbous OH, Fitchett D, Grima E, Langer A, Goodman SG. Inhospitalrevascularization and one-year outcome of acute coronary syndrome patients stratified by the GRACErisk score. Am J Cardiol 2005;96:913–916.206. Mehta SR, Cannon CP, Fox KA, Wallentin L, Boden WE, Spacek R, Widimsky P, McCullough PA, Hunt D, BraunwaldE, Yusuf S. Routine vs selective invasive strategies in patients with acute coronary syndromes: a collaborativemeta-analysis of randomized trials. JAMA 2005;293:2908–2917.207. Bavry AA, Kumbhani DJ, Rassi AN, Bhatt DL, Askari AT. Benefit of early invasive therapy in acute coronary syndromes:a meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006;48:1319–1325.208. O’Donoghue M, Boden WE, Braunwald E, Cannon CP, Clayton TC, de Winter RJ, Fox KA, Lagerqvist B, McCulloughPA, Murphy SA, Spacek R, Swahn E,Wallentin L, Windhausen F, Sabatine MS. Early invasive vs conservativetreatment strategies in women and men with unstable angina and non-ST-segment elevation myocardialinfarction: a meta-analysis. JAMA 2008; 300:71–80.209. Fox KA, Clayton TC, Damman P, Pocock SJ, de Winter RJ, Tijssen JG, Lagerqvist B,Wallentin L. Long-term outcomeof a routine versus selective invasive strategy in patients with non-ST-segment elevation acute coronarysyndrome a meta-analysis of individual patient data. J Am Coll Cardiol 2010;55:2435–2445.210. Montalescot G, Cayla G, Collet JP, Elhadad S, Beygui F, Le Breton H, Choussat R, Leclercq F, Silvain J, Duclos F,Aout M, Dubois-Rande JL, Barthelemy O, Ducrocq G, Bellemain-Appaix A, Payot L, Steg PG, Henry P, SpauldingC, Vicaut E. Immediate vs delayed intervention for acute coronary syndromes: a randomized clinical trial.JAMA 2009;302:947–954.211. van’t Hof AW, de Vries ST, Dambrink JH, Miedema K, Suryapranata H, Hoorntje JC, Gosselink AT, Zijlstra F, deBoer MJ. A comparison of two invasive strategies in patients with non-ST elevation acute coronary syndromes:results of the Early or Late Intervention in unStable Angina (ELISA) pilot study. 2b/3a upstream therapy andacute coronary syndromes. Eur Heart J 2003;24:1401–1405.212. Mehta SR, Granger CB, Boden WE, Steg PG, Bassand JP, Faxon DP, Afzal R, Chrolavicius S, Jolly SS, WidimskyP, Avezum A, Rupprecht HJ, Zhu J, Col J, Natarajan MK, Horsman C, Fox KA, Yusuf S. Early versus delayed invasiveintervention in acute coronary syndromes. N Engl J Med 2009;360:2165–2175.213. Katritsis DG, Siontis GC, Kastrati A, van’t Hof AW, Neumann FJ, Siontis KC, Ioannidis JP. Optimal timing ofcoronary angiography and potential intervention in non-ST-elevation acute coronary syndromes. Eur Heart J2010;32:32–40.214. Riezebos RK, Ronner E, Ter Bals E, Slagboom T, Smits PC, ten Berg JM, Kiemeneij F, Amoroso G, Patterson MS,Suttorp MJ, Tijssen JG, Laarman GJ. Immediate versus deferred coronary angioplasty in non-ST-segment elevationacute coronary syndromes. Heart 2009;95:807–812.215. Sorajja P, Gersh BJ, Cox DA, McLaughlin MG, Zimetbaum P, Costantini C, Stuckey T, Tcheng JE, Mehran R,Lansky AJ, Grines CL, Stone GW. Impact of delay to angioplasty in patients with acute coronary syndromes undergoinginvasive management: analysis from the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. J Am Coll Cardiol 2010;55:1416–1424.216. Brener SJ, Milford-Beland S, Roe MT, Bhatt DL, Weintraub WS, Brindis RG. Culprit-only or multivessel revascularizationin patients with acute coronary syndromes: an American College of Cardiology National CardiovascularDatabase Registry report. Am Heart J 2008;155:140–146.217. Ben-Gal Y, Moses JW, Mehran R, Lansky AJ,Weisz G, Nikolsky E, Argenziano M, Williams MR, Colombo A, AylwardPE, Stone GW. Surgical versus percutaneous revascularization for multivessel disease in patients withacute coronary syndromes: analysis from the ACUITY (Acute Catheterization and Urgent Intervention TriageStrategy) trial. JACC Cardiovasc Interv 2010;3:1059–1067.218. Serruys PW, Morice MC, Kappetein AP, Colombo A, Holmes DR, Mack MJ, Stahle E, Feldman TE, van denBrand M, Bass EJ, Van Dyck N, Leadley K, Dawkins KD, Mohr FW. Percutaneous coronary intervention versuscoronary-artery bypass grafting for severe coronary artery disease. N Engl J Med 2009;360:961–972.219. Sianos G, Morel MA, Kappetein AP, Morice MC, Colombo A, Dawkins K, van den Brand M, Van Dyck N, RussellME, Mohr FW, Serruys PW. The SYNTAX Score: an angiographic tool grading the complexity of coronaryartery disease. EuroIntervention 2005;1:219–227.220. de Winter RJ, Windhausen F, Cornel JH, Dunselman PH, Janus CL, Bendermacher PE, Michels HR, Sanders GT,Tijssen JG, Verheugt FW. Early invasive versus selectively invasive management for acute coronary syndromes.N Engl J Med 2005;353:1095–1104.221. Monteiro P. Impact of early coronary artery bypass graft in an unselected acute coronary syndrome patient population.Circulation 2006;114:I467–I472.222. Parikh SV, de Lemos JA, Jessen ME, Brilakis ES, Ohman EM, Chen AY, Wang TY, Peterson ED, Roe MT, HolperEM. Timing of in-hospital coronary artery bypass graft surgery for non-ST-segment elevation myocardial infarctionpatients results from the National Cardiovascular Data Registry ACTION Registry-GWTG (Acute CoronaryTreatment and Intervention Outcomes Network Registry-Get With The Guidelines). JACC CardiovascInterv 2010;3:419–427.223. Chu MW, Wilson SR, Novick RJ, Stitt LW, Quantz MA. Does clopidogrel increase blood loss following coronaryartery bypass surgery? Ann Thorac Surg 2004;78:1536–1541.224. Solodky A, Behar S, Boyko V, Battler A, Hasdai D. The outcome of coronary artery bypass grafting surgeryamong patients hospitalized with acute coronary syndrome: the Euro Heart Survey of acute coronary syndromeexperience. Cardiology 2005;103:44–47.225. Kaiser C, Galatius S, Erne P, Eberli F, Alber H, Rickli H, Pedrazzini G, Hornig B, Bertel O, Bonetti P, De Servi S,Brunner-La Rocca HP, Ricard I, Pfisterer M. Drug-eluting versus bare-metal stents in large coronary arteries. NEngl J Med 2010;363:2310–2319.226. Greenhalgh J, Hockenhull J, Rao N, Dundar Y, Dickson RC, Bagust A. Drug-eluting stents versus bare metalstents for angina or acute coronary syndromes. Cochrane Database Syst Rev 2010;5:CD004587.227. Vlaar PJ, Diercks GF, Svilaas T, Vogelzang M, de Smet BJ, van den Heuvel AF, Anthonio RL, Jessurun GA, TanES, Suurmeijer AJ, Zijlstra F. The feasibility and safety of routine thrombus aspiration in patients with non-STelevationmyocardial infarction. Catheter Cardiovasc Interv 2008;72:937–942.228. Rosengren A, Wallentin L, Simoons M, Gitt AK, Behar S, Battler A, Hasdai D. Age, clinical presentation, andoutcome of acute coronary syndromes in the Euroheart acute coronary syndrome survey. Eur Heart J2006;27:789–795.229. Bauer T, Koeth O, Junger C, Heer T, Wienbergen H, Gitt A, Zahn R, Senges J, Zeymer U. Effect of an invasivestrategy on in-hospital outcome in elderly patients with non-ST-elevation myocardial infarction. Eur Heart J2007;28:2873–2878.230. Alexander KP, Newby LK, Cannon CP, Armstrong PW, Gibler WB, Rich MW, Van de Werf F, White HD, WeaverWD, Naylor MD, Gore JM, Krumholz HM, Ohman EM. Acute coronary care in the elderly, part I: non-ST-segment-elevation acute coronary syndromes: a scientific statement for healthcare professionals from the AmericanHeart Association Council on Clinical Cardiology: in collaboration with the Society of Geriatric Cardiology.Circulation 2007;115:2549–2569.231. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED. Excess dosing of antiplatelet and antithrombin agents in the treatment of non-ST-segment elevationacute coronary syndromes. JAMA 2005;294:3108–3116.232. Lopes RD, Alexander KP, Marcucci G, White HD, Spinler S, Col J, Aylward PE, Califf RM, Mahaffey KW. Outcomesin elderly patients with acute coronary syndromes randomized to enoxaparin vs. unfractionated heparin:results from the SYNERGY trial. Eur Heart J 2008;29:1827–1833.233. Wallentin L, Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E. Outcome at 1 year after an invasive comparedwith a non-invasive strategy in unstable coronary-artery disease: the FRISC II invasive randomised trial. FRISCII Investigators. Fast Revascularisation during Instability in Coronary artery disease. Lancet 2000;356:9–16.234. Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E, Wallentin L. 5-Year outcomes in the FRISC-II randomisedtrial of an invasive versus a non-invasive strategy in non-ST-elevation acute coronary syndrome: a follow-upstudy. Lancet 2006;368:998–1004.235. Bach RG, Cannon CP, Weintraub WS, DiBattiste PM, Demopoulos LA, Anderson HV, DeLucca PT, Mahoney EM,Murphy SA, Braunwald E. The effect of routine, early invasive management on outcome for elderly patientswith non-ST-segment elevation acute coronary syndromes. Ann Intern Med 2004;141:186–195.236. Rosengren A, Wallentin L, Gitt AK, Behar S, Battler A, Hasdai D. Sex, age, and clinical presentation of acutecoronary syndromes. Eur Heart J 2004;25:663–670.237. Alfredsson J, Stenestrand U, Wallentin L, Swahn E. Gender differences in management and outcome in non-ST-elevation acute coronary syndrome. Heart 2007;93:1357–1362.238. Hvelplund A, Galatius S, Madsen M, Rasmussen JN, Rasmussen S, Madsen JK, Sand NP, Tilsted HH, ThayssenP, Sindby E, Hojbjerg S, Abildstrom SZ. Women with acute coronary syndrome are less invasively examined andsubsequently less treated than men. Eur Heart J 2010;31:684–690.239. Diercks DB, Owen KP, Kontos MC, Blomkalns A, Chen AY, Miller C, Wiviott S, Peterson ED. Gender differencesin time to presentation for myocardial infarction before and after a national women’s cardiovascular awarenesscampaign: a temporal analysis from the Can Rapid Risk Stratification of Unstable Angina Patients SuppressADverse Outcomes with Early Implementation (CRUSADE) and the National Cardiovascular Data RegistryAcute Coronary Treatment and Intervention Outcomes Network-Get with the Guidelines (NCDR ACTION Registry-GWTG). Am Heart J 2010;160:80–87 e83.240. Heer T, Gitt AK, Juenger C, Schiele R, Wienbergen H, Towae F, Gottwitz M, Zahn R, Zeymer U, Senges J. Genderdifferences in acute non-ST-segment elevation myocardial infarction. Am J Cardiol 2006;98:160–166.241. Bavry AA, Kumbhani DJ, Quiroz R, Ramchandani SR, Kenchaiah S, Antman EM. Invasive therapy along withglycoprotein IIb/IIIa inhibitors and intracoronary stents improves survival in non-ST-segment elevation acutecoronary syndromes: a meta-analysis and review of the literature. Am J Cardiol 2004;93:830–835.242. Fox KA, Poole-Wilson PA, Henderson RA, Clayton TC, Chamberlain DA, Shaw TR, Wheatley DJ, Pocock SJ. Interventionalversus conservative treatment for patients with unstable angina or non-ST-elevation myocardialinfarction: the British Heart Foundation RITA 3 randomised trial. Randomized Intervention Trial of unstableAngina. Lancet 2002;360:743–751.243. Hoenig MR, Doust JA, Aroney CN, Scott IA. Early invasive versus conservative strategies for unstable angina& non-ST-elevation myocardial infarction in the stent era. Cochrane Database Syst Rev 2006;3:CD004815.244. Glaser R, Herrmann HC, Murphy SA, Demopoulos LA, DiBattiste PM, Cannon CP, Braunwald E. Benefit of anearly invasive management strategy in women with acute coronary syndromes. JAMA2002;288:3124–3129.245. Boersma E, Harrington RA, Moliterno DJ, White H, Simoons ML. Platelet glycoprotein IIb/IIIa inhibitors inacute coronary syndromes. Lancet 2002;360:342–343.246. Berger JS, Elliott L, Gallup D, Roe M, Granger CB, Armstrong PW, Simes RJ, White HD, Van de Werf F, TopolEJ, Hochman JS, Newby LK, Harrington RA, Califf RM, Becker RC, Douglas PS. Sex differences in mortalityfollowing acute coronary syndromes. JAMA 2009;302:874–882.247. Bartnik M, Malmberg K, Norhammar A, Tenerz A, Ohrvik J, Ryden L. Newly detected abnormal glucose tolerance:an important predictor of long-term outcome after myocardial infarction. Eur Heart J2004;25:1990–1997.248. Dotevall A, Hasdai D, Wallentin L, Battler A, Rosengren A. Diabetes mellitus: clinical presentation and outcomein men and women with acute coronary syndromes. Data from the Euro Heart Survey ACS. Diabet Med2005;22:1542–1550. 249. Donahoe SM, Stewart GC, McCabe CH, Mohanavelu S, Murphy SA, Cannon CP, Antman EM. Diabetes andmortality following acute coronary syndromes. JAMA 2007;298:765–775.250. Hasin T, Hochadel M, Gitt AK, Behar S, Bueno H, Hasin Y. Comparison of treatment and outcome of acute coronarysyndrome in patients with versus patients without diabetes mellitus. Am J Cardiol 2009;103:772–778.251. De Caterina R, Madonna R, Sourij H, Wascher T. Glycaemic control in acute coronary syndromes: prognosticvalue and therapeutic options. Eur Heart J 2010;31:1557–1564.252. Graham I, Atar D, Borch-Johnsen K, Boysen G, Burell G, Cifkova R, Dallongeville J, De Backer G, Ebrahim S,Gjelsvik B, Herrmann-Lingen C, Hoes A, Humphries S, Knapton M, Perk J, Priori SG, Pyorala K, Reiner Z, RuilopeL, Sans-Menendez S, Scholte op Reimer W, Weissberg P, Wood D, Yarnell J, Zamorano JL, Walma E,Fitzgerald T, Cooney MT, Dudina A. European guidelines on cardiovascular disease prevention in clinical practice:executive summary: Fourth Joint Task Force of the European Society of Cardiology and Other Societies onCardiovascular Disease Prevention in Clinical Practice (Constituted by representatives of nine societies and byinvited experts). Eur Heart J 2007;28:2375–2414.253. Finfer S, Chittock DR, Su SY, Blair D, Foster D, Dhingra V, Bellomo R, Cook D, Dodek P, Henderson WR, HebertPC, Heritier S, Heyland DK, McArthur C, McDonald E, Mitchell I, Myburgh JA, Norton R, Potter J, RobinsonBG, Ronco JJ. Intensive versus conventional glucose control in critically ill patients. N Engl J Med2009;360:1283–1297.254. Diaz R, Goyal A, Mehta SR, Afzal R, Xavier D, Pais P, Chrolavicius S, Zhu J, Kazmi K, Liu L, Budaj A, Zubaid M,Avezum A, Ruda M, Yusuf S. Glucose–insulin–potassium therapy in patients with ST-segment elevation myocardialinfarction. JAMA 2007;298:2399–2405.255. Cannon CP, Weintraub WS, Demopoulos LA, Vicari R, Frey MJ, Lakkis N, Neumann FJ, Robertson DH, DeLuccaPT, DiBattiste PM, Gibson CM, Braunwald E. Comparison of early invasive and conservative strategies in patientswith unstable coronary syndromes treated with the glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med2001;344:1879–1887.256. Hlatky MA, Boothroyd DB, Bravata DM, Boersma E, Booth J, Brooks MM, Carrie D, Clayton TC, Danchin N,Flather M, Hamm CW, Hueb WA, Kahler J, Kelsey SF, King SB, Kosinski AS, Lopes N, McDonald KM, RodriguezA, Serruys P, Sigwart U, Stables RH, Owens DK, Pocock SJ. Coronary artery bypass surgery compared withpercutaneous coronary interventions for multivessel disease: a collaborative analysis of individual patient datafrom ten randomised trials. Lancet 2009;373:1190–1197.257. Chaitman BR, Hardison RM, Adler D, Gebhart S, Grogan M, Ocampo S, Sopko G, Ramires JA, Schneider D,Frye RL. The Bypass Angioplasty Revascularization Investigation 2 Diabetes randomized trial of different treatmentstrategies in type 2 diabetes mellitus with stable ischemic heart disease: impact of treatment strategy oncardiac mortality and myocardial infarction. Circulation 2009;120:2529–2540.258. Frye RL, August P, Brooks MM, Hardison RM, Kelsey SF, MacGregor JM, Orchard TJ, Chaitman BR, Genuth SM,Goldberg SH, Hlatky MA, Jones TL, Molitch ME, Nesto RW, Sako EY, Sobel BE. A randomized trial of therapiesfor type 2 diabetes and coronary artery disease. N Engl J Med 2009;360:2503–2515.259. Banning AP, Westaby S, Morice MC, Kappetein AP, Mohr FW, Berti S, Glauber M, Kellett MA, Kramer RS,Leadley K, Dawkins KD, Serruys PW. Diabetic and nondiabetic patients with left main and/or 3-vessel coronaryartery disease: comparison of outcomes with cardiac surgery and paclitaxel-eluting stents. J Am Coll Cardiol2010;55:1067–1075.260. Hannan EL, Wu C, Walford G, Culliford AT, Gold JP, Smith CR, Higgins RS, Carlson RE, Jones RH. Drug-elutingstents vs. coronary-artery bypass grafting in multivessel coronary disease. N Engl J Med 2008;358:331–341.261. Stettler C, Allemann S, Wandel S, Kastrati A, Morice MC, Schomig A, Pfisterer ME, Stone GW, Leon MB, de LezoJS, Goy JJ, Park SJ, Sabate M, Suttorp MJ, Kelbaek H, Spaulding C, Menichelli M, Vermeersch P, Dirksen MT,Cervinka P, De Carlo M, Erglis A, Chechi T, Ortolani P, Schalij MJ, Diem P, Meier B, Windecker S, Juni P. Drugeluting and bare metal stents in people with and without diabetes: collaborative network meta-analysis. BMJ2008;337:a1331.262. Wiviott SD, Braunwald E, Angiolillo DJ, Meisel S, Dalby AJ, Verheugt FW, Goodman SG, Corbalan R, PurdyDA, Murphy SA, McCabe CH, Antman EM. Greater clinical benefit of more intensive oral antiplatelet therapywith prasugrel in patients with diabetes mellitus in the trial to assess improvement in therapeutic outcomes byoptimizing platelet inhibition with prasugrel-Thrombolysis in Myocardial Infarction 38. Circulation2008;118:1626–1636.263. James S, Angiolillo DJ, Cornel JH, Erlinge D, Husted S, Kontny F, Maya J, Nicolau JC, Spinar J, Storey RF, StevensSR, Wallentin L. Ticagrelor vs. clopidogrel in patients with acute coronary syndromes and diabetes: a substudyfrom the PLATelet inhibition and patient Outcomes (PLATO) trial. Eur Heart J 2010;31:3006–3016.264. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Heeschen C, Hamm CW, Moliterno DJ, Califf RM, WhiteHD, Kleiman NS, Theroux P, Topol EJ. Platelet glycoprotein IIb/IIIa inhibitors reduce mortality in diabetic patientswith non-ST-segment-elevation acute coronary syndromes. Circulation 2001;104:2767–2771.265. Salpeter SR, Greyber E, Pasternak GA, Salpeter EE. Risk of fatal and nonfatal lactic acidosis with metformin usein type 2 diabetes mellitus. Cochrane Database Syst Rev 2010;4:CD002967.266. Hasdai D, Behar S, Wallentin L, Danchin N, Gitt AK, Boersma E, Fioretti PM, Simoons ML, Battler A. A prospectivesurvey of the characteristics, treatments and outcomes of patients with acute coronary syndromes in Europeand the Mediterranean basin; the Euro Heart Survey of Acute Coronary Syndromes (Euro Heart SurveyACS). Eur Heart J 2002;23:1190–1201.267. Goldenberg I, Subirana I, Boyko V, Vila J, Elosua R, Permanyer-Miralda G, Ferreira-Gonzalez I, Benderly M,Guetta V, Behar S, Marrugat J. Relation between renal function and outcomes in patients with non-ST-segmentelevation acute coronary syndrome: real-world data from the European Public Health Outcome Researchand Indicators Collection Project. Arch Intern Med 2010;170:888–895.268. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Relationbetween renal function, presentation, use of therapies and in-hospital complications in acute coronary syndrome:data from the SWEDEHEART register. J Intern Med 2010;268:40–49.269. Collet JP, Montalescot G, Agnelli G, Van de Werf F, Gurfinkel EP, Lopez-Sendon J, Laufenberg CV, Klutman M,Gowda N, Gulba D. Non-ST-segment elevation acute coronary syndrome in patients with renal dysfunction:benefit of low-molecular-weight heparin alone or with glycoprotein IIb/IIIa inhibitors on outcomes. The GlobalRegistry of Acute Coronary Events. Eur Heart J 2005;26:2285–2293.270. Fox KA, Bassand JP, Mehta SR, Wallentin L, Theroux P, Piegas LS, Valentin V, Moccetti T, Chrolavicius S, AfzalR, Yusuf S. Influence of renal function on the efficacy and safety of fondaparinux relative to enoxaparin in nonST-segment elevation acute coronary syndromes. Ann Intern Med 2007;147:304–310.271. James S, Budaj A, Aylward P, Buck KK, Cannon CP, Cornel JH, Harrington RA, Horrow J, Katus H, Keltai M, LewisBS, Parikh K, Storey RF, Szummer K, Wojdyla D, Wallentin L. Ticagrelor versus clopidogrel in acute coronary syndromesin relation to renal function: results from the Platelet Inhibition and Patient Outcomes (PLATO) trial.Circulation 2010;122:1056–1067.272. Pannu N, Wiebe N, Tonelli M. Prophylaxis strategies for contrast-induced nephropathy. JAMA2006;295:2765–2779.273. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Influenceof renal function on the effects of early revascularization in non-ST-elevation myocardial infarction: data fromthe Swedish Web-System for Enhancement and Development of Evidence-Based Care in Heart Disease EvaluatedAccording to Recommended Therapies (SWEDEHEART). Circulation 2009;120:851–858.274. Steg PG, Dabbous OH, Feldman LJ, Cohen-Solal A, Aumont MC, Lopez-Sendon J, Budaj A, Goldberg RJ, KleinW, Anderson FA Jr. Determinants and prognostic impact of heart failure complicating acute coronary syndromes:observations from the Global Registry of Acute Coronary Events (GRACE). Circulation2004;109:494–499.275. Dickstein K, Vardas PE, Auricchio A, Daubert JC, Linde C, McMurray J, Ponikowski P, Priori SG, Sutton R, vanVeldhuisen DJ, Vahanian A, Bax J, Ceconi C, Dean V, Filippatos G, Funck-Brentano C, Hobbs R, Kearney P, Mc-Donagh T, Popescu BA, Reiner Z, Sechtem U, Sirnes PA, Tendera M, Vardas P, Widimsky P, Anker SD, Blanc JJ,Gasparini M, Hoes AW, Israel CW, Kalarus Z, Merkely B, Swedberg K, Camm AJ. 2010 Focused Update of ESCGuidelines on device therapy in heart failure: an update of the 2008 ESC Guidelines for the diagnosis andtreatment of acute and chronic heart failure and the 2007 ESC guidelines for cardiac and resynchronizationtherapy. Developed with the special contribution of the Heart Failure Association and the European HeartRhythm Association. Eur Heart J 2010;31:2677–2687.276. Pitt B, Remme W, Zannad F, Neaton J, Martinez F, Roniker B, Bittman R, Hurley S, Kleiman J, Gatlin M.Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction.N Engl J Med 2003;348:1309–1321.277. Zannad F, McMurray JJ, Krum H, van Veldhuisen DJ, Swedberg K, Shi H, Vincent J, Pocock SJ, Pitt B. Eplerenonein patients with systolic heart failure and mild symptoms. N Engl J Med 2011;364:11–21.278. Moss AJ, Zareba W, Hall WJ, Klein H, Wilber DJ, Cannom DS, Daubert JP, Higgins SL, Brown MW, Andrews ML.Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction.N Engl J Med 2002;346:877–883.279. Diercks DB, Roe MT, Mulgund J, Pollack CV Jr., Kirk JD, Gibler WB, Ohman EM, Smith SC Jr., Boden WE, PetersonED. The obesity paradox in non-ST-segment elevation acute coronary syndromes: results from the CanRapid risk stratification of Unstable angina patients Suppress ADverse outcomes with Early implementation ofthe American College of Cardiology/American Heart Association Guidelines Quality Improvement Initiative.Am Heart J 2006;152:140–148.280. Steinberg BA, Cannon CP, Hernandez AF, Pan W, Peterson ED, Fonarow GC. Medical therapies and invasivetreatments for coronary artery disease by body mass: the ‘obesity paradox’ in the Get With The Guidelines database.Am J Cardiol 2007;100:1331–1335.281. Ong P, Athanasiadis A, Borgulya G, Voehringer M, Sechtem U. 3-Year follow-up of patients with coronary arteryspasm as cause of acute coronary syndrome: the CASPAR (coronary artery spasm in patients with acutecoronary syndrome) study follow-up. J Am Coll Cardiol 2011;57:147–152.282. Hasin T, Sorkin A, Markiewicz W, Hammerman H, Aronson D. Prevalence and prognostic significance of transient,persistent, and new-onset anemia after acute myocardial infarction. Am J Cardiol 2009;104:486–491.283. Bassand JP, Afzal R, Eikelboom J, Wallentin L, Peters R, Budaj A, Fox KA, Joyner CD, Chrolavicius S, GrangerCB, Mehta S, Yusuf S. Relationship between baseline haemoglobin and major bleeding complications in acutecoronary syndromes. Eur Heart J 2010;31:50–58.284. Chase AJ, Fretz EB, Warburton WP, Klinke WP, Carere RG, Pi D, Berry B, Hilton JD. Association of the arterialaccess site at angioplasty with transfusion and mortality: the M.O.R.T.A.L study (Mortality benefit Of ReducedTransfusion after percutaneous coronary intervention via the Arm or Leg). Heart 2008;94:1019–1025.285. Agostoni P, Biondi-Zoccai GG, de Benedictis ML, Rigattieri S, Turri M, Anselmi M, Vassanelli C, Zardini P, LouvardY, Hamon M. Radial versus femoral approach for percutaneous coronary diagnostic and interventional procedures;systematic overview and meta-analysis of randomized trials. J Am Coll Cardiol 2004;44:349–356.286. Alexander KP, Chen AY, Wang TY, Rao SV, Newby LK, LaPointe NM, Ohman EM, Roe MT, Boden WE, HarringtonRA, Peterson ED. Transfusion practice and outcomes in non-ST-segment elevation acute coronary syndromes.Am Heart J 2008;155:1047–1053.287. Hill SR, Carless PA, Henry DA, Carson JL, Hebert PC, McClelland DB, Henderson KM. Transfusion thresholdsand other strategies for guiding allogeneic red blood cell transfusion. Cochrane Database Syst Rev2002;2:CD002042.288. Mehran R, Rao SV, Bhatt DL, Gibson CM, Caixeta A, Eikelboom J, Kaul S, Wiviott SD, Menon V, Nikolsky E, SerebruanyV, Valgimigli M, Vranckx P, Taggart D, Sabik JF, Cutlip DE, Krucoff MW, Ohman EM, Steg PG, White H.Standardized bleeding definitions for cardiovascular clinical trials: a consensus report from the Bleeding AcademicResearch Consortium (BARC). Circulation 2011;123:2736–2747.289. Fox KA, Carruthers K, Steg PG, Avezum A, Granger CB, Montalescot G, Goodman SG, Gore JM, Quill AL,Eagle KA. Has the frequency of bleeding changed over time for patients presenting with an acute coronary syndrome?The global registry of acute coronary events. Eur Heart J 2010;31:667–675.290. Eikelboom JW, Mehta SR, Anand SS, Xie C, Fox KA, Yusuf S. Adverse impact of bleeding on prognosis in patientswith acute coronary syndromes. Circulation 2006;114:774–782.291. Budaj A, Eikelboom JW, Mehta SR, Afzal R, Chrolavicius S, Bassand JP, Fox KA, Wallentin L, Peters RJ, GrangerCB, Joyner CD, Yusuf S. Improving clinical outcomes by reducing bleeding in patients with non-ST-elevationacute coronary syndromes. Eur Heart J 2009;30:655–661.292. Mehran R, Pocock SJ, Stone GW, Clayton TC, Dangas GD, Feit F, Manoukian SV, Nikolsky E, Lansky AJ, KirtaneA, White HD, Colombo A, Ware JH, Moses JW, Ohman EM. Associations of major bleeding and myocardialinfarction with the incidence and timing of mortality in patients presenting with non-ST-elevation acute coronarysyndromes: a risk model from the ACUITY trial. Eur Heart J 2009;30:1457–1466.293. Antman EM, Wiviott SD, Murphy SA, Voitk J, Hasin Y, Widimsky P, Chandna H, Macias W, McCabe CH, BraunwaldE. Early and late benefits of prasugrel in patients with acute coronary syndromes undergoing percutaneouscoronary intervention: a TRITON-TIMI 38 (TRial to Assess Improvement in Therapeutic Outcomes byOptimizing Platelet InhibitioN with Prasugrel-Thrombolysis In Myocardial Infarction) analysis. J Am Coll Cardiol2008;51:2028–2033.294. Berger PB, Bhatt DL, Fuster V, Steg PG, Fox KA, Shao M, Brennan DM, Hacke W, Montalescot G, Steinhubl SR,Topol EJ. Bleeding complications with dual antiplatelet therapy among patients with stable vascular disease orrisk factors for vascular disease: results from the Clopidogrel for High Atherothrombotic Risk and IschemicStabilization, Management, and Avoidance (CHARISMA) trial. Circulation 2010;121:2575–2583.295. Sorensen R, Hansen ML, Abildstrom SZ, Hvelplund A, Andersson C, Jorgensen C, Madsen JK, Hansen PR,Kober L, Torp-Pedersen C, Gislason GH. Risk of bleeding in patients with acute myocardial infarction treatedwith different combinations of aspirin, clopidogrel, and vitamin K antagonists in Denmark: a retrospectiveanalysis of nationwide registry data. Lancet 2009;374:1967–1974. 296. Joyner CD, Peters RJ, Afzal R, Chrolavicius S, Mehta SR, Fox KA, Granger CB, Franzosi MG, Flather M, BudajA, Bassand JP, Yusuf S. Fondaparinux compared to enoxaparin in patients with acute coronary syndromeswithout ST-segment elevation: outcomes and treatment effect across different levels of risk. Am Heart J2009;157:502–508.297. Spencer FA, Moscucci M, Granger CB, Gore JM, Goldberg RJ, Steg PG, Goodman SG, Budaj A, FitzGerald G,Fox KA. Does comorbidity account for the excess mortality in patients with major bleeding in acute myocardialinfarction? Circulation 2007;116:2793–2801.298. Rao SV, Jollis JG, Harrington RA, Granger CB, Newby LK, Armstrong PW, Moliterno DJ, Lindblad L, Pieper K,Topol EJ, Stamler JS, Califf RM. Relationship of blood transfusion and clinical outcomes in patients with acutecoronary syndromes. JAMA 2004;292:1555–1562.299. Alexander KP, Peterson ED. Minimizing the risks of anticoagulants and platelet inhibitors. Circulation2010;121:1960–1970.300. Marso SP, Amin AP, House JA, Kennedy KF, Spertus JA, Rao SV, Cohen DJ, Messenger JC, Rumsfeld JS. Associationbetween use of bleeding avoidance strategies and risk of periprocedural bleeding among patients undergoingpercutaneous coronary intervention. JAMA 2010;303:2156–2164.301. Yank V, Tuohy CV, Logan AC, Bravata DM, Staudenmayer K, Eisenhut R, Sundaram V, McMahon D, Olkin I,McDonald KM, Owens DK, Stafford RS. Systematic review: benefits and harms of in-hospital use of recombinantfactor VIIa for off-label indications. Ann Intern Med 2011;154:529–540.302. Hebert PC, Wells G, Blajchman MA, Marshall J, Martin C, Pagliarello G, Tweeddale M, Schweitzer I, Yetisir E.A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. Transfusion Requirementsin Critical Care Investigators, Canadian Critical Care Trials Group. N Engl J Med1999;340:409–417.303. Singh AK, Szczech L, Tang KL, Barnhart H, Sapp S, Wolfson M, Reddan D. Correction of anemia with epoetinalfa in chronic kidney disease. N Engl J Med 2006;355:2085–2098.304. Menzin J, Wygant G, Hauch O, Jackel J, Friedman M. One-year costs of ischemic heart disease among patientswith acute coronary syndromes: findings from a multi-employer claims database. Curr Med Res Opin2008;24:461–468.305. Smith SC Jr., Allen J, Blair SN, Bonow RO, Brass LM, Fonarow GC, Grundy SM, Hiratzka L, Jones D, KrumholzHM, Mosca L, Pasternak RC, Pearson T, Pfeffer MA, Taubert KA. AHA/ACC guidelines for secondary preventionfor patients with coronary and other atherosclerotic vascular disease: 2006 update: endorsed by the NationalHeart, Lung, and Blood Institute. Circulation 2006;113:2363–2372.306. Chow CK, Jolly S, Rao-Melacini P, Fox KA, Anand SS, Yusuf S. Association of diet, exercise, and smoking modificationwith risk of early cardiovascular events after acute coronary syndromes. Circulation2010;121:750–758.307. Chew DP, Huynh LT, Liew D, Astley C, Soman A, Brieger D. Potential survival gains in the treatment of myocardialinfarction. Heart 2009;95:1844–1850.308. Ford ES, Ajani UA, Croft JB, Critchley JA, Labarthe DR, Kottke TE, Giles WH, Capewell S. Explaining the decreasein U.S. deaths from coronary disease, 1980–2000. N Engl J Med 2007;356:2388–2398.309. Dagenais GR, Pogue J, Fox K, Simoons ML, Yusuf S. Angiotensinconverting-enzyme inhibitors in stable vasculardisease without left ventricular systolic dysfunction or heart failure: a combined analysis of three trials.Lancet 2006;368:581–588.310. Danchin N, Cucherat M, Thuillez C, Durand E, Kadri Z, Steg PG. Angiotensinconverting enzyme inhibitors inpatients with coronary artery disease and absence of heart failure or left ventricular systolic dysfunction: anoverview of long-term randomized controlled trials. Arch Intern Med 2006;166:787–796.311. Yusuf S, Teo KK, Pogue J, Dyal L, Copland I, Schumacher H, Dagenais G, Sleight P, Anderson C. Telmisartan,ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008;358:1547–1559.312. Hulten E, Jackson JL, Douglas K, George S, Villines TC. The effect of early, intensive statin therapy on acute coronarysyndrome: a meta-analysis of randomized controlled trials. Arch Intern Med 2006;166:1814–1821.313. Cannon CP, Braunwald E, McCabe CH, Rader DJ, Rouleau JL, Belder R, Joyal SV, Hill KA, Pfeffer MA, Skene AM.Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med2004;350:1495–1504.314. Lopez-Sendon J, Swedberg K, McMurray J, Tamargo J, Maggioni AP, Dargie H, Tendera M, Waagstein F, KjekshusJ, Lechat P, Torp-Pedersen C. Expert consensus document on beta-adrenergic receptor blockers. Eur HeartJ 2004;25:1341–1362.315. Pfeffer MA, Braunwald E, Moye LA, Basta L, Brown EJ Jr., Cuddy TE, Davis BR, Geltman EM, Goldman S, FlakerGC, Klein M, Lamas GA, Packer M, Rouleau J, Rouleau JL, Rutherford J, Wertheimer JH, Hawkins CM. Effectof captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction.Results of the survival and ventricular enlargement trial. The SAVE Investigators. N Engl J Med1992;327:669–677.316. Torp-Pedersen C, Kober L. Effect of ACE inhibitor trandolapril on life expectancy of patients with reduced leftventricularfunction after acute myocardial infarction. TRACE Study Group. Trandolapril Cardiac Evaluation.Lancet 1999;354:9–12.317. Pfeffer MA, McMurray JJ, Velazquez EJ, Rouleau JL, Kober L, Maggioni AP, Solomon SD, Swedberg K, Van deWerf F, White H, Leimberger JD, Henis M, Edwards S, Zelenkofske S, Sellers MA, Califf RM. Valsartan, captopril,or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N EnglJ Med 2003;349:1893–1906.318. Fox KA, Steg PG, Eagle KA, Goodman SG, Anderson FA Jr., Granger CB, Flather MD, Budaj A, Quill A, GoreJM. Decline in rates of death and heart failure in acute coronary syndromes, 1999–2006. JAMA2007;297:1892–1900.319. Fox K, Garcia MA, Ardissino D, Buszman P, Camici PG, Crea F, Daly C, De Backer G, Hjemdahl P, Lopez-SendonJ, Marco J, Morais J, Pepper J, Sechtem U, Simoons M, Thygesen K, Priori SG, Blanc JJ, Budaj A, Camm J,Dean V, Deckers J, Dickstein K, Lekakis J, McGregor K, Metra M, Osterspey A, Tamargo J, Zamorano JL. Guidelineson the management of stable angina pectoris: executive summary: the Task Force on the Managementof Stable Angina Pectoris of the European Society of Cardiology. Eur Heart J 2006;27:1341–1381.320. Rahimi K, Watzlawek S, Thiele H, Secknus MA, Hayerizadeh BF, Niebauer J, Schuler G. Incidence, time course,and predictors of early malignant ventricular arrhythmias after non-ST-segment elevation myocardial infarctionin patients with early invasive treatment. Eur Heart J 2006;27:1706–1711.
Цели вторичной профилактики после ОКС/ИМ без подъема сегмента ST
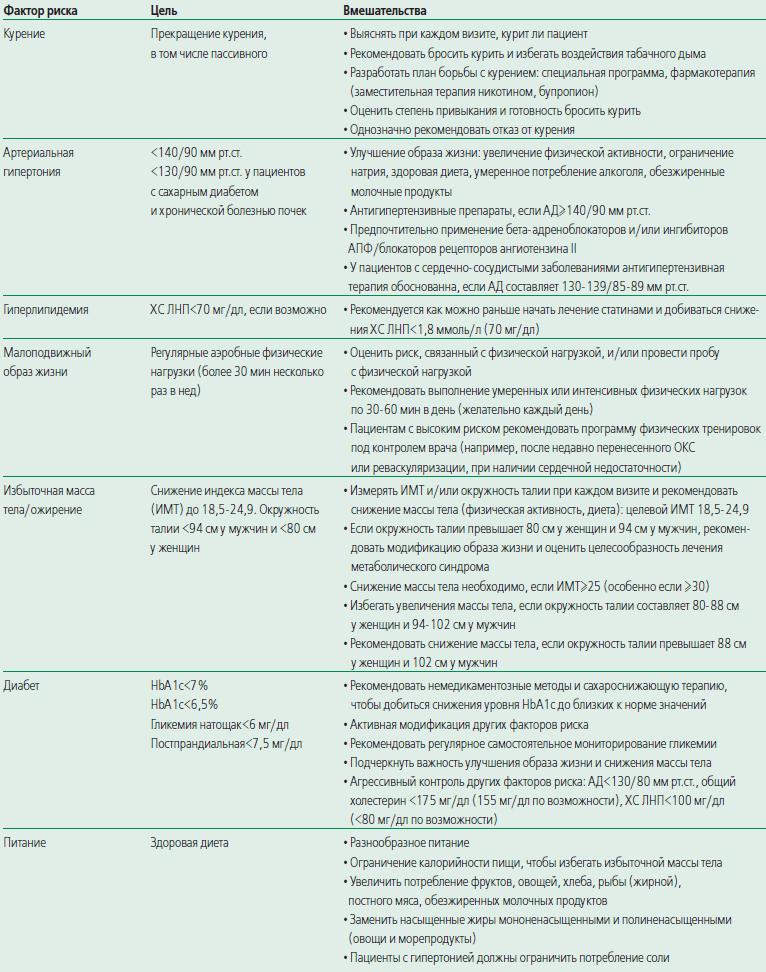
 Таблица 2. Уровни доказательности
Таблица 2. Уровни доказательности
 Сердечно-сосудистые заболевания являются веду-щей причиной смертности в индустриально развитыхстранах. Ожидается, что к 2020 г. они займут первое ме-сто в структуре смертности в развивающихся странах [1].Среди сердечно-сосудистых заболеваний чаще всеговстречается ишемическая болезнь сердца (ИБС), кото-рая характеризуется высокой частотой осложнений, втом числе смерти. Клинические проявления ИБС вклю-чают в себя «немую» ишемию, стабильную стенокардию,нестабильную стенокардию, инфаркт миокарда (ИМ),сердечную недостаточность и внезапную смерть. Больв груди относится к числу основных причин неотлож-ных госпитализаций в Европе. Диагностика ОКС у па-циентов с болью в груди может быть достаточно труд-ной задачей, особенно при отсутствии характерныхсимптомов или электрокардиографических изменений.Несмотря на современное лечение, смертность, часто-та ИМ и повторных госпитализаций у пациентов сОКС остаются высокими.Установлено, что различные клинические вариантыОКС имеют общие механизмы развития. Результаты ауто-псийных и клинических исследований свидетель-ствуют о том, что в основе большинства случаев ОКС ле-жат разрыв или эрозия атеросклеротической бляшки,которые сопровождаются тромбообразованием и дис-тальной эмболизацией и приводят к ухудшению пер-фузии миокарда.ОКС — это угрожающее жизни атеротромботическоесостояние, поэтому разработаны критерии стратифи-кации риска, которые помогают врачам своевременновыбрать тактику индивидуализированного лечения, включающего в себя применение различных лекарст-венных средств, а также реваскуляризацию коронар-ных артерий. Ведущим симптомом является боль в гру-ди, однако ОКС классифицируют на основании изме-нений на ЭКГ. Выделают два варианта этого синдрома:1. Пациенты с острой болью в груди и персисти-рующим (>20 мин) подъемом сегмента ST — ОКС сподъемом сегмента SТ, который обычно отражает пол-ную окклюзию коронарной артерии. У большинства па-циентов формируется ИМ с подъемом сегмента ST. Пер-вичная цель лечения — быстрая, полная и стойкая ре-перфузия путем ангиопластики или тромболизиса.2. Пациенты с острой болью в груди без стойко-го подъема сегмента ST. У таких пациентов наблюдаютстойкую или преходящую депрессию сегмента ST, ин-версию зубца Т, сглаживание зубца Т, псевдонормали-зацию зубца Т, однако изменения на ЭКГ могут и отсут-ствовать. Тактика ведения пациентов предполагает ку-пирование ишемии и симптомов, мониторирование ЭКГи повторное определение маркеров некроза миокар-да. В зависимости от результатов измерения уровня тро-понинов выделяют ИМ без подъема сегмента ST и не-стабильную стенокардию (рис. 1). У части пациентовпроводимое исследование позволяет исключить ИБСкак причину боли в сердце.Ведение пациентов с ОКС с подъемом сегмента STрассматривается в соответствующих рекомендациях Ев-ропейского общества кардиологов [2]. В настоящем до-кументе обсуждается лечение пациентов с предпола-гаемым ОКС без подъема сегмента ST. Он заменяет до-кумент, впервые опубликованный в 2000 г. и изменен-ный в 2002 и 2007 гг. [3]. В рекомендации включенырезультаты всех исследований, опубликованных в ре-цензируемых журналах до мая 2011 г.Уровень доказательства А в настоящем документе —это результаты рандомизированных двойных слепых ис-следований адекватного размера, предполагавшихсовременную базовую терапию и анализ конечныхточек, не подверженных системной ошибке, таких каксмерть и ИМ. Результаты рандомизированных, но недвойных слепых исследований и/или исследований,предполагавших анализ менее «твердых» конечных то-чек (например, рефрактерной ишемии или необходи-мости в реваскуляризации), считали менее доказатель-ными. При наличии только небольших исследованийиспользовали результаты мета-анализа. Однако дажесамые крупные контролируемые исследования неохватывают все аспекты реальной жизни. В связи с этимнекоторые рекомендации основываются на результа-тах анализа подгрупп в более крупных исследованияхпри отсутствии соответствующих независимых иссле-дований, обладающих достаточной статистическойсилой.
Эпидемиология и естественное течение
Результаты регистров показали, что ОКС без подъе-ма сегмента ST встречается чаще, чем ОКС с подъемомсегмента ST [4]. Ежегодная заболеваемость составляет примерно 3 на 1000 населения, хотя она отличается вразных странах [5]. Госпитальная смертность у пациен-тов с ИМ с подъемом сегмента ST выше, чем у больныхОКС без подъема сегмента ST (7% и 3-5%, соответствен-но), однако через 6 мес смертность сопоставима придвух состояниях (12% и 13%, соответственно) [4,6,7].В отдаленном периоде смертность у пациентов с ОКСбез подъема сегмента ST превышала таковую у паци-ентов с ОКС с подъемом сегмента ST: например, через4 года она была в 2 раза выше [8]. Различия естествен-ного течения вариантов ОКС могут отражать особенно-сти пациентов: в частности, больные с ОКС без подъе-ма сегмента ST обычно старше, у них чаще встречают-ся сопутствующие заболевания, особенно сахарный диа-бет и почечная недостаточность.Результаты эпидемиологических исследований сви-детельствуют о том, что пациенты с ОКС без подъемасегмента ST нуждаются в интенсивном лечении нетолько в остром, но и в отдаленном периоде. Дополни-тельные данные об эпидемиологии и естественном тече-нии ОКС без подъема сегмента ST содержатся в преды-дущих рекомендациях [3] и учебнике Европейского об-щества кардиологов по сердечно-сосудистой медици-не [9].
Рис. 1. Спектр ОКС
Сердечно-сосудистые заболевания являются веду-щей причиной смертности в индустриально развитыхстранах. Ожидается, что к 2020 г. они займут первое ме-сто в структуре смертности в развивающихся странах [1].Среди сердечно-сосудистых заболеваний чаще всеговстречается ишемическая болезнь сердца (ИБС), кото-рая характеризуется высокой частотой осложнений, втом числе смерти. Клинические проявления ИБС вклю-чают в себя «немую» ишемию, стабильную стенокардию,нестабильную стенокардию, инфаркт миокарда (ИМ),сердечную недостаточность и внезапную смерть. Больв груди относится к числу основных причин неотлож-ных госпитализаций в Европе. Диагностика ОКС у па-циентов с болью в груди может быть достаточно труд-ной задачей, особенно при отсутствии характерныхсимптомов или электрокардиографических изменений.Несмотря на современное лечение, смертность, часто-та ИМ и повторных госпитализаций у пациентов сОКС остаются высокими.Установлено, что различные клинические вариантыОКС имеют общие механизмы развития. Результаты ауто-псийных и клинических исследований свидетель-ствуют о том, что в основе большинства случаев ОКС ле-жат разрыв или эрозия атеросклеротической бляшки,которые сопровождаются тромбообразованием и дис-тальной эмболизацией и приводят к ухудшению пер-фузии миокарда.ОКС — это угрожающее жизни атеротромботическоесостояние, поэтому разработаны критерии стратифи-кации риска, которые помогают врачам своевременновыбрать тактику индивидуализированного лечения, включающего в себя применение различных лекарст-венных средств, а также реваскуляризацию коронар-ных артерий. Ведущим симптомом является боль в гру-ди, однако ОКС классифицируют на основании изме-нений на ЭКГ. Выделают два варианта этого синдрома:1. Пациенты с острой болью в груди и персисти-рующим (>20 мин) подъемом сегмента ST — ОКС сподъемом сегмента SТ, который обычно отражает пол-ную окклюзию коронарной артерии. У большинства па-циентов формируется ИМ с подъемом сегмента ST. Пер-вичная цель лечения — быстрая, полная и стойкая ре-перфузия путем ангиопластики или тромболизиса.2. Пациенты с острой болью в груди без стойко-го подъема сегмента ST. У таких пациентов наблюдаютстойкую или преходящую депрессию сегмента ST, ин-версию зубца Т, сглаживание зубца Т, псевдонормали-зацию зубца Т, однако изменения на ЭКГ могут и отсут-ствовать. Тактика ведения пациентов предполагает ку-пирование ишемии и симптомов, мониторирование ЭКГи повторное определение маркеров некроза миокар-да. В зависимости от результатов измерения уровня тро-понинов выделяют ИМ без подъема сегмента ST и не-стабильную стенокардию (рис. 1). У части пациентовпроводимое исследование позволяет исключить ИБСкак причину боли в сердце.Ведение пациентов с ОКС с подъемом сегмента STрассматривается в соответствующих рекомендациях Ев-ропейского общества кардиологов [2]. В настоящем до-кументе обсуждается лечение пациентов с предпола-гаемым ОКС без подъема сегмента ST. Он заменяет до-кумент, впервые опубликованный в 2000 г. и изменен-ный в 2002 и 2007 гг. [3]. В рекомендации включенырезультаты всех исследований, опубликованных в ре-цензируемых журналах до мая 2011 г.Уровень доказательства А в настоящем документе —это результаты рандомизированных двойных слепых ис-следований адекватного размера, предполагавшихсовременную базовую терапию и анализ конечныхточек, не подверженных системной ошибке, таких каксмерть и ИМ. Результаты рандомизированных, но недвойных слепых исследований и/или исследований,предполагавших анализ менее «твердых» конечных то-чек (например, рефрактерной ишемии или необходи-мости в реваскуляризации), считали менее доказатель-ными. При наличии только небольших исследованийиспользовали результаты мета-анализа. Однако дажесамые крупные контролируемые исследования неохватывают все аспекты реальной жизни. В связи с этимнекоторые рекомендации основываются на результа-тах анализа подгрупп в более крупных исследованияхпри отсутствии соответствующих независимых иссле-дований, обладающих достаточной статистическойсилой.
Эпидемиология и естественное течение
Результаты регистров показали, что ОКС без подъе-ма сегмента ST встречается чаще, чем ОКС с подъемомсегмента ST [4]. Ежегодная заболеваемость составляет примерно 3 на 1000 населения, хотя она отличается вразных странах [5]. Госпитальная смертность у пациен-тов с ИМ с подъемом сегмента ST выше, чем у больныхОКС без подъема сегмента ST (7% и 3-5%, соответствен-но), однако через 6 мес смертность сопоставима придвух состояниях (12% и 13%, соответственно) [4,6,7].В отдаленном периоде смертность у пациентов с ОКСбез подъема сегмента ST превышала таковую у паци-ентов с ОКС с подъемом сегмента ST: например, через4 года она была в 2 раза выше [8]. Различия естествен-ного течения вариантов ОКС могут отражать особенно-сти пациентов: в частности, больные с ОКС без подъе-ма сегмента ST обычно старше, у них чаще встречают-ся сопутствующие заболевания, особенно сахарный диа-бет и почечная недостаточность.Результаты эпидемиологических исследований сви-детельствуют о том, что пациенты с ОКС без подъемасегмента ST нуждаются в интенсивном лечении нетолько в остром, но и в отдаленном периоде. Дополни-тельные данные об эпидемиологии и естественном тече-нии ОКС без подъема сегмента ST содержатся в преды-дущих рекомендациях [3] и учебнике Европейского об-щества кардиологов по сердечно-сосудистой медици-не [9].
Рис. 1. Спектр ОКС
 Патофизиология
ОКС — это угрожающее жизни проявление атеросклероза. Оно обычно развивается в результате острого тром-боза на фоне разрыва или эрозии атеросклеротическойбляшки в коронарной артерии±вазоконстрикции, ко-торые приводят к внезапному ухудшению коронарно-го кровотока. Ключевое значение в патогенезе разры-ва бляшки имеет воспаление. В редких случаях ОКС име-ет неатеросклеротическое происхождение и можетбыть обусловлен артериитом, травмой, расслоениемстенки артерии, тромбоэмболией, врожденными по-роками, употреблением кокаина или осложняет кате-теризацию сердца. Для адекватного лечения необхо-димо понимать ключевые концепции патогенеза ОКС,в том числе уязвимость бляшки, коронарный тромбоз,уязвимость пациента, эндотелиальную дисфункцию,ускоренный атеротромбоз, вторичные механизмы ОКСбез подъема сегмента ST и повреждение миокарда.Предсказать развитие ОКС позволяет наличие неболь-ших бляшек с тонкой оболочкой, крупных бляшек илизначительного сужения просвета сосуда [10]. Этот во-прос более подробно рассматривается в предыдущихрекомендациях [3] и учебнике Европейского обществакардиологов по сердечно-сосудистой медицине [9].
Диагноз
Ведущим симптомом ОКС обычно является боль вгруди. Наличие ОКС без подъема сегмента ST подтвер-ждается с помощью ЭКГ (отсутствие стойкого подъемасегмента ST). ИМ без подъема сегмента ST и нестабиль-ную стенокардию дифференцируют на основанииуровней биомаркеров (тропонинов). Эхокардиографиюи сцинтиграфию миокарда используют для исключениядругих заболеваний. Методы диагностики и стратифи-кации риска тесно связаны друг с другом.
Клиническая картина
Клинические проявления ОКС без подъема сегмента ST включают в себя различные симптомы. Тради-ционно выделяют несколько клинических вариантовОКС:
• длительная (≥20 мин) ангинозная боль в покое;
• впервые возникшая стенокардия II-III функциональ-ного класса по классификации Канадского сердечно-сосудистого общества [11];
• недавнее прогрессирование ранее стабильнойстенокардии, по крайней мере до III функционально-го класса (стенокардия crescendo);
• постинфарктная стенокардия.Длительный приступ боли в области сердца наблю-дается у 80% пациентов, а впервые возникшая стено-кардия или прогрессирующая стенокардия — у 20% [12].Типичный клинический симптом ОКС без подъемасегмента ST — боль или тяжесть за грудиной (груднаяжаба), иррадиирующая в левую руку, шею или челюсть,которая может быть интермиттирующей (обычно про-должается несколько мин) или стойкой. Боль может со-провождаться потливостью, тошнотой, болью в живо-те, одышкой и обмороком. Нередко отмечаются атипич-ные проявления ОКС, такие как боль в эпигастральнойобласти, диспепсия, кинжальная боль в груди, плевраль-ная боль или нарастающая одышка. Атипичные симп-томы чаще отмечаются у пациентов пожилого возрас-та (≥75 лет), больных сахарным диабетом, хроническойпочечной недостаточностью или деменцией [13,14]. Отсутствие боли в груди является причиной несвоевремен-ной диагностики и неадекватного лечения [15]. Труд-ности диагностики обычно возникают в тех случаях, ко-гда ЭКГ нормальная или практически нормальная,или, наоборот, если на исходной ЭКГ имеются измене-ния, связанные с нарушением внутрижелудочковой про-водимости или гипертрофией левого желудочка [16].Заподозрить диагноз ИБС помогают некоторые осо-бенности клинической картины. Появление симптомовпри физической нагрузке или их уменьшение в покоеили после приема нитратов подтверждает диагнозишемия миокарда. Важное значение имеет выявлениефакторов, провоцирующих развитие ОКС без подъе-ма сегмента ST, таких как анемия, инфекция, воспале-ние, лихорадка и метаболические или эндокринные за-болевания (особенно щитовидной железы).При наличии клинических симптомов некоторыефакторы риска повышают вероятность ИБС и, соответ-ственно, ОКС без подъема сегмента ST. К ним относят-ся пожилой возраст, мужской пол, отягощенный семей-ный анамнез, а также наличие атеросклероза некоро-нарных артерий, в частности периферических и сонных.Важное диагностическое значение имеет наличие дру-гих факторов риска, особенно сахарного диабета и по-чечной недостаточности, и проявлений ИБС в анамне-зе [перенесенный ИМ, чрескожное коронарное вмеша-тельство (ЧКВ) или коронарное шунтирование (КШ) ванамнезе).
Методы диагностики
Физическое обследование
При физическом обследовании изменения часто отсутствуют. Основанием для диагностики и лечениямогут быть симптомы сердечной недостаточности илинарушения гемодинамики. Важная цель физическогообследования — исключение несердечных причинболи в сердце и неишемических заболеваний сердца(например, тромбоэмболии легочной артерии, расслое-ния стенки аорты, перикардита, порока клапана серд-ца) или экстракардиальных причин, таких как остроезаболевание легких (пневмоторакс, пневмония илиплевральный выпот). Разница АД на верхних и нижнихконечностях, аритмичный пульс, шумы в сердце, шумтрения перикарда, боль при пальпации и пальпируе-мое образование в брюшной полости позволяют запо-дозрить другие диагнозы. Некоторые физические дан-ные, такие как бледность, потливость или тремор,указывают на анемию и тиреотоксикоз, которые могутспровоцировать развитие ОКС без подъема сегментаST.
Электрокардиография
ЭКГ в 12 отведениях — это первый метод диагности-ки, который используют при подозрении на ОКС безподъема сегмента ST. ЭКГ следует зарегистрировать втечение первых 10 мин после поступления в при-емное отделение или приезда машины скорой помо-щи. ЭКГ должен немедленно проанализировать опыт-ный врач [17]. Для ОКС без подъема сегмента ST харак-терны депрессия или преходящий подъем сегмента STи/или изменения зубца Т [6,18]. Наличие стойкогоподъема сегмента ST (≥20 мин) указывает на наличиеИМ с подъемом сегмента ST, тактика лечения которо-го отличается [2]. Если исходная ЭКГ нормальная илирезультаты ее неоднозначные, то необходимо регистри-ровать ЭКГ в динамике [18]. Важное значение имеетсравнение полученных данных с предыдущими ЭКГ, осо-бенно при наличии заболеваний сердца, таких как ги-пертрофия левого желудочка или перенесенный ИМ.ЭКГ следует зарегистрировать повторно по крайней меречерез 3 ч, 6-9 ч и 24 ч после обращения к врачу и не-медленно при рецидиве боли в груди или симптомов.Рекомендуется также зарегистрировать ЭКГ перед вы-пиской.Необходимо учитывать, что нормальная ЭКГ неисключает диагноз ОКС без подъема сегмента ST. В част-ности, при ишемии в бассейне огибающей артерии илиизолированной ишемии правого желудочка измененияна ЭКГ в 12 отведениях часто отсутствуют, однако онимогут быть выявлены в отведениях V7–V9 и отведенияхV3R и V4R, соответственно [18]. При эпизодах ишемиимиокарда иногда наблюдается преходящая блокада но-жек пучка Гиса.Стандартная ЭКГ в покое неадекватно отражает ди-намический характер коронарного тромбоза и ишемиимиокарда. Почти 2/3 эпизодов ишемии в нестабиль-ную фазу клинически бессимптомные и не регистри-руются с помощью стандартной ЭКГ. Соответственно,важное диагностическое значение имеет мониториро-вание ЭКГ в 12 отведениях.
Биомаркеры
Сердечные тропонины играют центральную роль вдиагностике и стратификации риска и позволяют так-же дифференцировать ИМ без подъема сегмента ST инестабильную стенокардию. По специфичности и чув-ствительности тропонины превосходят традиционныесердечные ферменты, такие как креатинкиназа (КК),МВ-фракция КК, и миоглобин. Повышение уровня сер-дечных тропонинов отражает повреждение кардиомио-цитов, которое при ОКС без подъема сегмента ST мо-жет быть связано с дистальной эмболизацией тромбо-цитарными тромбами, образующимися в области раз-рыва или эрозии бляшки. Соответственно, тропонинможно рассматривать как суррогатный маркер актив-ного тромбообразования [19]. При наличии ишемиимиокарда (боль в груди, изменения на ЭКГ и появле-ние асинергии стенки сердца) увеличение уровня тро-понина указывает на ИМ [18].У пациентов с ИМ уровень тропонина начинает уве-личиваться в течение примерно 4 ч после появлениясимптомов. Содержание тропонина может оставатьсяповышенным в течение 2 нед вследствие протеолизасократительного аппарата. При ОКС без подъема сег-мента ST уровень тропонина обычно нормализуется че-рез 48-72 ч. Тропонины T и I не имеют фундаменталь-ных отличий. Неоднозначные результаты исследованиймогут быть связаны с особенностями критериев включе-ния, вариабельностью сроков взятия крови и примене-ния различных методов исследования.В клинической практике необходимо использоватьметоды, позволяющие надежно исключить (предска-зательное значение отрицательного результата) и пра-вильно диагностировать ОКС (предсказательное значе-ние положительного результата). Диагноз ИМ устанав-ливают, если уровень сердечного тропонина превышает 99-й перцентиль нормального диапазона. Коэффи-циент вариации метода должен составлять ≤10% [18].Адекватность такого подхода была установлена в не-скольких исследованиях [20,21]. Первые методы ана-лиза тропонинов Т и I были недостаточно точными. Не-давно были разработаны высоко- или ультрачувстви-тельные методы (пороговый уровень в 10-100 разниже), обладающие необходимой точностью. Соответ-ственно, сегодня ИМ удается диагностировать чаще ираньше [20,21]. Преимущество новых методов анали-за, особенно в раннюю фазу, было установлено в про-спективных исследованиях [20,21]. Предсказатель-ное значение отрицательного результата при однократ-ном измерении при поступлении составляет ≥95% и покрайней мере такое же высокое как при анализе уров-ней тропонинов в динамике с помощью старых мето-дов. Уровень тропонина может быть нормальнымтолько на очень ранней стадии ИМ. Если провести по-вторное исследование в течение 3 ч после появлениясимптомов, то чувствительность диагностики ИМ при-ближается к 100% [22,23].Благодаря увеличению чувствительности анализанизкие уровни тропонина сегодня могут быть выявле-ны у многих пациентов со стабильной стенокардией[24,25] и здоровых людей [26]. Механизмы увеличе-ния уровня тропонина у таких пациентов не установле-ны, однако наличие тропонина в крови указывает на не-благоприятный прогноз [24]. Чтобы обеспечить специ-фичность диагностики ИМ, необходимо дифференци-ровать хроническое и острое повышение уровня тро-понина. Для этого имеет значение степень измененияпоказателя. Клинически значимое повышение уровнятропонина по сравнению с исходным показателемпродолжает дискутироваться. Пограничные измененияуровня тропонина должны превышать естественную ва-риабельность этого показателя, которую необходимоопределить для каждого метода [27].Другие угрожающие жизни состояния, сопровождаю-щиеся болью в груди, такие как расслаивающая анев-ризма аорты или тромбоэмболия легочной артерии, так-же могут привести к увеличению уровней тропонинов,поэтому их необходимо учитывать при проведении диф-ференциального диагноза. Увеличение концентрациисердечных тропонинов наблюдается также при повреж-дении миокарда некоронарного происхождения(табл. 3). Эти данные отражают чувствительность мар-кера в диагностике поражения кардиомиоцитов, поэто-му их не следует считать ложноположительными. Лож-ноположительные результаты анализа уровней тропо-нинов регистрировали при поражении скелетных мышцили хронической почечной недостаточности. Уровеньтропонинов часто повышается при концентрации сы-вороточного креатинина ≥2,5 мг/дл (221 мкмоль/л)при отсутствии доказанного ОКС; такое повышениетакже ассоциируется с неблагоприятным прогнозом[28,29].
Таблица 3. Возможные некоронарные причиныповышения уровня тропонина (полужирнымшрифтом выделены заболевания, которыеимеют важное значение с дифференци-ально-диагностической точки зрения)
Патофизиология
ОКС — это угрожающее жизни проявление атеросклероза. Оно обычно развивается в результате острого тром-боза на фоне разрыва или эрозии атеросклеротическойбляшки в коронарной артерии±вазоконстрикции, ко-торые приводят к внезапному ухудшению коронарно-го кровотока. Ключевое значение в патогенезе разры-ва бляшки имеет воспаление. В редких случаях ОКС име-ет неатеросклеротическое происхождение и можетбыть обусловлен артериитом, травмой, расслоениемстенки артерии, тромбоэмболией, врожденными по-роками, употреблением кокаина или осложняет кате-теризацию сердца. Для адекватного лечения необхо-димо понимать ключевые концепции патогенеза ОКС,в том числе уязвимость бляшки, коронарный тромбоз,уязвимость пациента, эндотелиальную дисфункцию,ускоренный атеротромбоз, вторичные механизмы ОКСбез подъема сегмента ST и повреждение миокарда.Предсказать развитие ОКС позволяет наличие неболь-ших бляшек с тонкой оболочкой, крупных бляшек илизначительного сужения просвета сосуда [10]. Этот во-прос более подробно рассматривается в предыдущихрекомендациях [3] и учебнике Европейского обществакардиологов по сердечно-сосудистой медицине [9].
Диагноз
Ведущим симптомом ОКС обычно является боль вгруди. Наличие ОКС без подъема сегмента ST подтвер-ждается с помощью ЭКГ (отсутствие стойкого подъемасегмента ST). ИМ без подъема сегмента ST и нестабиль-ную стенокардию дифференцируют на основанииуровней биомаркеров (тропонинов). Эхокардиографиюи сцинтиграфию миокарда используют для исключениядругих заболеваний. Методы диагностики и стратифи-кации риска тесно связаны друг с другом.
Клиническая картина
Клинические проявления ОКС без подъема сегмента ST включают в себя различные симптомы. Тради-ционно выделяют несколько клинических вариантовОКС:
• длительная (≥20 мин) ангинозная боль в покое;
• впервые возникшая стенокардия II-III функциональ-ного класса по классификации Канадского сердечно-сосудистого общества [11];
• недавнее прогрессирование ранее стабильнойстенокардии, по крайней мере до III функционально-го класса (стенокардия crescendo);
• постинфарктная стенокардия.Длительный приступ боли в области сердца наблю-дается у 80% пациентов, а впервые возникшая стено-кардия или прогрессирующая стенокардия — у 20% [12].Типичный клинический симптом ОКС без подъемасегмента ST — боль или тяжесть за грудиной (груднаяжаба), иррадиирующая в левую руку, шею или челюсть,которая может быть интермиттирующей (обычно про-должается несколько мин) или стойкой. Боль может со-провождаться потливостью, тошнотой, болью в живо-те, одышкой и обмороком. Нередко отмечаются атипич-ные проявления ОКС, такие как боль в эпигастральнойобласти, диспепсия, кинжальная боль в груди, плевраль-ная боль или нарастающая одышка. Атипичные симп-томы чаще отмечаются у пациентов пожилого возрас-та (≥75 лет), больных сахарным диабетом, хроническойпочечной недостаточностью или деменцией [13,14]. Отсутствие боли в груди является причиной несвоевремен-ной диагностики и неадекватного лечения [15]. Труд-ности диагностики обычно возникают в тех случаях, ко-гда ЭКГ нормальная или практически нормальная,или, наоборот, если на исходной ЭКГ имеются измене-ния, связанные с нарушением внутрижелудочковой про-водимости или гипертрофией левого желудочка [16].Заподозрить диагноз ИБС помогают некоторые осо-бенности клинической картины. Появление симптомовпри физической нагрузке или их уменьшение в покоеили после приема нитратов подтверждает диагнозишемия миокарда. Важное значение имеет выявлениефакторов, провоцирующих развитие ОКС без подъе-ма сегмента ST, таких как анемия, инфекция, воспале-ние, лихорадка и метаболические или эндокринные за-болевания (особенно щитовидной железы).При наличии клинических симптомов некоторыефакторы риска повышают вероятность ИБС и, соответ-ственно, ОКС без подъема сегмента ST. К ним относят-ся пожилой возраст, мужской пол, отягощенный семей-ный анамнез, а также наличие атеросклероза некоро-нарных артерий, в частности периферических и сонных.Важное диагностическое значение имеет наличие дру-гих факторов риска, особенно сахарного диабета и по-чечной недостаточности, и проявлений ИБС в анамне-зе [перенесенный ИМ, чрескожное коронарное вмеша-тельство (ЧКВ) или коронарное шунтирование (КШ) ванамнезе).
Методы диагностики
Физическое обследование
При физическом обследовании изменения часто отсутствуют. Основанием для диагностики и лечениямогут быть симптомы сердечной недостаточности илинарушения гемодинамики. Важная цель физическогообследования — исключение несердечных причинболи в сердце и неишемических заболеваний сердца(например, тромбоэмболии легочной артерии, расслое-ния стенки аорты, перикардита, порока клапана серд-ца) или экстракардиальных причин, таких как остроезаболевание легких (пневмоторакс, пневмония илиплевральный выпот). Разница АД на верхних и нижнихконечностях, аритмичный пульс, шумы в сердце, шумтрения перикарда, боль при пальпации и пальпируе-мое образование в брюшной полости позволяют запо-дозрить другие диагнозы. Некоторые физические дан-ные, такие как бледность, потливость или тремор,указывают на анемию и тиреотоксикоз, которые могутспровоцировать развитие ОКС без подъема сегментаST.
Электрокардиография
ЭКГ в 12 отведениях — это первый метод диагности-ки, который используют при подозрении на ОКС безподъема сегмента ST. ЭКГ следует зарегистрировать втечение первых 10 мин после поступления в при-емное отделение или приезда машины скорой помо-щи. ЭКГ должен немедленно проанализировать опыт-ный врач [17]. Для ОКС без подъема сегмента ST харак-терны депрессия или преходящий подъем сегмента STи/или изменения зубца Т [6,18]. Наличие стойкогоподъема сегмента ST (≥20 мин) указывает на наличиеИМ с подъемом сегмента ST, тактика лечения которо-го отличается [2]. Если исходная ЭКГ нормальная илирезультаты ее неоднозначные, то необходимо регистри-ровать ЭКГ в динамике [18]. Важное значение имеетсравнение полученных данных с предыдущими ЭКГ, осо-бенно при наличии заболеваний сердца, таких как ги-пертрофия левого желудочка или перенесенный ИМ.ЭКГ следует зарегистрировать повторно по крайней меречерез 3 ч, 6-9 ч и 24 ч после обращения к врачу и не-медленно при рецидиве боли в груди или симптомов.Рекомендуется также зарегистрировать ЭКГ перед вы-пиской.Необходимо учитывать, что нормальная ЭКГ неисключает диагноз ОКС без подъема сегмента ST. В част-ности, при ишемии в бассейне огибающей артерии илиизолированной ишемии правого желудочка измененияна ЭКГ в 12 отведениях часто отсутствуют, однако онимогут быть выявлены в отведениях V7–V9 и отведенияхV3R и V4R, соответственно [18]. При эпизодах ишемиимиокарда иногда наблюдается преходящая блокада но-жек пучка Гиса.Стандартная ЭКГ в покое неадекватно отражает ди-намический характер коронарного тромбоза и ишемиимиокарда. Почти 2/3 эпизодов ишемии в нестабиль-ную фазу клинически бессимптомные и не регистри-руются с помощью стандартной ЭКГ. Соответственно,важное диагностическое значение имеет мониториро-вание ЭКГ в 12 отведениях.
Биомаркеры
Сердечные тропонины играют центральную роль вдиагностике и стратификации риска и позволяют так-же дифференцировать ИМ без подъема сегмента ST инестабильную стенокардию. По специфичности и чув-ствительности тропонины превосходят традиционныесердечные ферменты, такие как креатинкиназа (КК),МВ-фракция КК, и миоглобин. Повышение уровня сер-дечных тропонинов отражает повреждение кардиомио-цитов, которое при ОКС без подъема сегмента ST мо-жет быть связано с дистальной эмболизацией тромбо-цитарными тромбами, образующимися в области раз-рыва или эрозии бляшки. Соответственно, тропонинможно рассматривать как суррогатный маркер актив-ного тромбообразования [19]. При наличии ишемиимиокарда (боль в груди, изменения на ЭКГ и появле-ние асинергии стенки сердца) увеличение уровня тро-понина указывает на ИМ [18].У пациентов с ИМ уровень тропонина начинает уве-личиваться в течение примерно 4 ч после появлениясимптомов. Содержание тропонина может оставатьсяповышенным в течение 2 нед вследствие протеолизасократительного аппарата. При ОКС без подъема сег-мента ST уровень тропонина обычно нормализуется че-рез 48-72 ч. Тропонины T и I не имеют фундаменталь-ных отличий. Неоднозначные результаты исследованиймогут быть связаны с особенностями критериев включе-ния, вариабельностью сроков взятия крови и примене-ния различных методов исследования.В клинической практике необходимо использоватьметоды, позволяющие надежно исключить (предска-зательное значение отрицательного результата) и пра-вильно диагностировать ОКС (предсказательное значе-ние положительного результата). Диагноз ИМ устанав-ливают, если уровень сердечного тропонина превышает 99-й перцентиль нормального диапазона. Коэффи-циент вариации метода должен составлять ≤10% [18].Адекватность такого подхода была установлена в не-скольких исследованиях [20,21]. Первые методы ана-лиза тропонинов Т и I были недостаточно точными. Не-давно были разработаны высоко- или ультрачувстви-тельные методы (пороговый уровень в 10-100 разниже), обладающие необходимой точностью. Соответ-ственно, сегодня ИМ удается диагностировать чаще ираньше [20,21]. Преимущество новых методов анали-за, особенно в раннюю фазу, было установлено в про-спективных исследованиях [20,21]. Предсказатель-ное значение отрицательного результата при однократ-ном измерении при поступлении составляет ≥95% и покрайней мере такое же высокое как при анализе уров-ней тропонинов в динамике с помощью старых мето-дов. Уровень тропонина может быть нормальнымтолько на очень ранней стадии ИМ. Если провести по-вторное исследование в течение 3 ч после появлениясимптомов, то чувствительность диагностики ИМ при-ближается к 100% [22,23].Благодаря увеличению чувствительности анализанизкие уровни тропонина сегодня могут быть выявле-ны у многих пациентов со стабильной стенокардией[24,25] и здоровых людей [26]. Механизмы увеличе-ния уровня тропонина у таких пациентов не установле-ны, однако наличие тропонина в крови указывает на не-благоприятный прогноз [24]. Чтобы обеспечить специ-фичность диагностики ИМ, необходимо дифференци-ровать хроническое и острое повышение уровня тро-понина. Для этого имеет значение степень измененияпоказателя. Клинически значимое повышение уровнятропонина по сравнению с исходным показателемпродолжает дискутироваться. Пограничные измененияуровня тропонина должны превышать естественную ва-риабельность этого показателя, которую необходимоопределить для каждого метода [27].Другие угрожающие жизни состояния, сопровождаю-щиеся болью в груди, такие как расслаивающая анев-ризма аорты или тромбоэмболия легочной артерии, так-же могут привести к увеличению уровней тропонинов,поэтому их необходимо учитывать при проведении диф-ференциального диагноза. Увеличение концентрациисердечных тропонинов наблюдается также при повреж-дении миокарда некоронарного происхождения(табл. 3). Эти данные отражают чувствительность мар-кера в диагностике поражения кардиомиоцитов, поэто-му их не следует считать ложноположительными. Лож-ноположительные результаты анализа уровней тропо-нинов регистрировали при поражении скелетных мышцили хронической почечной недостаточности. Уровеньтропонинов часто повышается при концентрации сы-вороточного креатинина ≥2,5 мг/дл (221 мкмоль/л)при отсутствии доказанного ОКС; такое повышениетакже ассоциируется с неблагоприятным прогнозом[28,29].
Таблица 3. Возможные некоронарные причиныповышения уровня тропонина (полужирнымшрифтом выделены заболевания, которыеимеют важное значение с дифференци-ально-диагностической точки зрения)
 Определение уровней биомаркеров у постели больногоДиагноз ОКС без подъема сегмента ST следует уста-новить как можно быстрее, чтобы назначить адекват-ное лечение. Экспресс-методы позволяют измеритьуровни биомаркеров в минимальные сроки [30]. Их сле-дует внедрять в тех случаях, когда в центральной лабо-ратории не удается выполнить это исследование втечение 60 мин [31]. Для интерпретации результатов те-ста не требуются специальные навыки или длительноеобучение. Соответственно, исследование могут вы-полнить различные медицинские работники. Однакорезультаты этих качественных тестов анализируются ви-зуально, что отражается на полученных данных. Суще-ствуют также оптические устройства, позволяющиепровести количественный анализ. Тесты обычно надеж-ны, если они положительные. Однако если диагноз не-стабильная ИБС остается вероятным, то исследованиеследует повторить в динамике, а также определить уров-ни тропонинов в сертифицированной лаборатории. Не-давно была показана возможность выделения пациентов низкого риска с помощью экспресс-алгоритма (2 ч),предполагающего применение экспресс-метода из-мерения уровня тропонинов, индекса риска и ЭКГ[32].
Визуализирующие методы
Неинвазивные методыСреди неинвазивных методов в острую фазу чащевсего проводят эхокардиографию в связи с доступностьюметода. Систолическая функция левого желудочка — этоважный прогностический показатель у пациентов сИБС, который можно легко и точно измерить с помо-щью эхокардиографии. Опытный специалист может вы-явить преходящую гипокинезию или акинезию сегмен-тов левого желудочка во время ишемии. Кроме того, ме-тод позволяет дифференцировать расслоение стенкиаорты, тромбоэмболию легочной артерии, аортальныйстеноз, гипертрофическую кардиомиопатию или пери-кардиальный выпот [33]. В связи с этим эхокардиогра-фию в отделениях интенсивной терапии следует про-водить всем пациентам.Если ЭКГ в 12 отведениях не информативна, ауровни сердечных биомаркеров у пациентов с предпо-лагаемым ОКС нормальные, может быть выполненасцинтиграфия миокарда с нагрузкой при условии от-сутствия боли в сердце. В различных исследованиях при-меняли также стресс-эхокардиографию, которая харак-теризовалась высоким предсказательным значениемотрицательного результата [34].Магнитно-резонансная томография (МРТ) сердцапозволяет одновременно оценить функцию и перфу-зию миокарда и выявить рубцовые изменения, одна-ко этот метод исследования пока малодоступен. В раз-личных исследованиях была показана информативностьМРТ в диагностике ОКС [35]. Кроме того, этот метод ис-пользуют для оценки жизнеспособности миокарда и ди-агностики миокардита.Показана также информативность перфузионнойсцинтиграфии миокарда, однако этот метод также не-достаточно широко доступен в круглосуточном режи-ме. Сцинтиграфия миокарда в покое была полезной наначальном этапе обследования пациентов с болью в гру-ди, у которых отсутствуют изменения на ЭКГ, или при-знаки сохраняющейся ишемии, или ИМ [36]. Проба снагрузкой имеет преимущество, так как она позволяетвыявить индуцируемую ишемию.Мультиспиральную компьютерную томографию(КТ) не применяют для диагностики ишемии, однакоэтот метод дает возможность прямо визуализироватькоронарные артерии. Теоретически с помощью муль-тиспиральной КТ можно исключить наличие ИБС. В раз-личных исследованиях было показано высокое пред-сказательное значение отрицательного результата ис-следования [37-41]. Для исключения ОКС или другихпричин боли в груди может быть полезной КТ-ангио-графия.
Инвазивные методы (коронарная ангиография)С помощью коронарной ангиографии получаютуникальную информацию о наличии и тяжести коро-нарного атеросклероза, поэтому данный метод по-преж-нему считают золотым стандартом. Ангиографию реко-мендуется проводить до и после интракоронарного вве-дения вазодилататоров (нитратов), чтобы уменьшитьвазоконстрикцию и устранить динамический компонентстеноза, который часто отмечается при ОКС. У пациен-тов с нарушением гемодинамики (отек легких, гипото-ния или тяжелые угрожающие жизни аритмии) целе-сообразно проводить исследования после введения ин-трааортального баллонного насоса.Ангиографию следует выполнять в неотложном по-рядке с диагностическими целями у пациентов высо-кого риска, а также в тех случаях, когда диагноз не ясен. Выявление острой тромботиче-ской окклюзии (например, огибающей артерии) име-ет особое значение у пациентов с сохраняющимисясимптомами или повышением уровня тропонинапри отсутствии диагностически значимых измене-ний на ЭКГ.В исследованиях TIMI-3B [42] и FRISC-2 [43] былопоказано, что у 30-38% пациентов с ОКС имеется по-ражение одной коронарной артерии, а у 44-49% — не-скольких (стеноз ≥50%). Частота стеноза левой глав-ной коронарной артерии составляет от 4-8%. У паци-ентов с поражением нескольких сосудов, а также ство-ла левой коронарной артерии имеется самый высокийриск развития серьезных неблагоприятных исходов. Ко-ронарная ангиография в сочетании с данными ЭКГ иасинергией стенки левого желудочка часто позволяетустановить, поражение какого сосуда стало причинойОКС. При ангиографии в типичном случае выявляют экс-центричный стеноз, неровные контуры, изъязвление идефекты наполнения, которые указывают на наличиеинтракоронарного тромба. Если трудно оценить тяжестьпоражения, то проводят внутрисосудистую эхографиюили измеряют фракционный резерв кровотока через >5дней после события [44]. Эти методы помогают выбратьстратегию лечения.Выбор сосудистого доступа зависит от опыта врача;этот выбор имеет важное значение, так как геморраги-ческие осложнения оказывают неблагоприятное влия-ние на клинические исходы. Лучевой доступ ассоции-ровался со снижением риска кровотечения по сравне-нию с таковым при феморальном доступе, поэтому пер-вый является предпочтительным при высоком риске ге-моррагических осложнений при условии, что врачимеет необходимый опыт. При лучевом доступе сни-жается риск образования крупной гематомы ценой более высокого облучения пациента и медицинских ра-ботников [45]. Феморальный доступ может быть пред-почтительным при нарушении гемодинамики, так какон облегчает проведение интрааортальной баллоннойконтрпульсации.
Дифференциальный диагноз
Некоторые заболевания сердца и других органов мо-гут имитировать ОКС без подъема сегмента ST (табл. 4).Гипертрофическая кардиомиопатия и пороки сердца(например, аортальный стеноз или аортальная недо-статочность) могут сопровождаться типичными симп-томами ОКС без подъема сегмента ST, повышеннымиуровнями биомаркеров или изменениями на ЭКГ [46].Иногда пароксизмальная фибрилляция предсердий(ФП) также имитирует ОКС. Некоторые такие пациен-ты страдают ИБС, что может быть причиной диагности-ческих трудностей. Миокардит, перикардит или мио-перикардит различной этиологии могут сопровож-даться болью в груди, сходной с типичной стенокарди-ей, и повышением уровней сердечных биомаркеров,изменениями ЭКГ и асинергией стенки левого желудоч-ка. Гриппоподобные симптомы, лихорадка и симпто-мы со стороны верхних дыхательных путей часто пред-шествуют развитию этих состояний или сопровож-дают их. Однако инфекции, особенно верхних отделовдыхательных путей, часто отмечают у пациентов с ОКСбез подъема сегмента ST. Установить диагноз миокар-дит или миоперикардит нередко удается только во вре-мя госпитализации.Необходимо также исключать угрожающие жизнизаболевания других органов. Например, тромбоэмбо-лия легочной артерии может сопровождаться одышкой,болью в груди и изменениями на ЭКГ, а также повышен-ными уровнями сердечных биомаркеров. Для диагно-стики тромбоэмболии легочной артерии определяютуровень Д-димера и проводят эхокардиографию иКТ. Альтернативный метод — МР-ангиография легочныхартерий, если этот метод доступен. Расслоение стенкиаорты — это еще одно заболевание, которое необходи-мо исключать при проведении дифференциального ди-агноза. ОКС без подъема сегмента ST может бытьосложнением расслоения стенки аорты, если оно рас-пространяется на коронарные артерии. Инсульт такжеможет сопровождаться изменениями на ЭКГ, асинер-гией стенки левого желудочка и повышением уровнейсердечных биомаркеров. Наоборот, атипичные симп-томы, такие как головная боль и головокружение, в ред-ких случаях могут быть единственным проявлением ише-мии миокарда.
4. Оценка прогнозаОКС без подъема сегмента ST — это нестабильное за-болевание, характеризующееся рецидивами ишемиии развитием других осложнений, которые могут при-вести к смерти или инфаркту миокарда в ближайшемили отдаленном периодах. Цели лечения, включающе-го в себя применение антиишемических и антитром-ботических лекарственных средств и различные стра-тегии реваскуляризации коронарных артерий, — пред-упредить или снизить риск таких осложнений и улуч-шить прогноз. Сроки и интенсивность вмешательствавыбирают с учетом индивидуального риска. Многие ме-тоды лечения повышают риск геморрагических ослож-нений, который необходимо тщательно взвешивать.Спектр риска, ассоциирующегося с ОКС без подъема сег-мента ST, широкий и особенно высокий в первыечасы, поэтому его необходимо тщательно оценивать не-медленно после первого контакта с врачом. Оценка рис-ка — это непрерывный процесс, который продолжает-ся до выписки пациента из стационара и может в лю-бые сроки оказать влияние на стратегию лечения. Гос-питализация пациентов в специальные отделения мо-жет улучшить результаты лечения больных с ОКС [47].У пациентов с ОКС без подъема сегмента ST риск оста-ется повышенным даже после выписки, поэтому они тре-буют особого внимания.
Таблица 4. Заболевания сердца и других органов, которые могут имитировать ОКС
Определение уровней биомаркеров у постели больногоДиагноз ОКС без подъема сегмента ST следует уста-новить как можно быстрее, чтобы назначить адекват-ное лечение. Экспресс-методы позволяют измеритьуровни биомаркеров в минимальные сроки [30]. Их сле-дует внедрять в тех случаях, когда в центральной лабо-ратории не удается выполнить это исследование втечение 60 мин [31]. Для интерпретации результатов те-ста не требуются специальные навыки или длительноеобучение. Соответственно, исследование могут вы-полнить различные медицинские работники. Однакорезультаты этих качественных тестов анализируются ви-зуально, что отражается на полученных данных. Суще-ствуют также оптические устройства, позволяющиепровести количественный анализ. Тесты обычно надеж-ны, если они положительные. Однако если диагноз не-стабильная ИБС остается вероятным, то исследованиеследует повторить в динамике, а также определить уров-ни тропонинов в сертифицированной лаборатории. Не-давно была показана возможность выделения пациентов низкого риска с помощью экспресс-алгоритма (2 ч),предполагающего применение экспресс-метода из-мерения уровня тропонинов, индекса риска и ЭКГ[32].
Визуализирующие методы
Неинвазивные методыСреди неинвазивных методов в острую фазу чащевсего проводят эхокардиографию в связи с доступностьюметода. Систолическая функция левого желудочка — этоважный прогностический показатель у пациентов сИБС, который можно легко и точно измерить с помо-щью эхокардиографии. Опытный специалист может вы-явить преходящую гипокинезию или акинезию сегмен-тов левого желудочка во время ишемии. Кроме того, ме-тод позволяет дифференцировать расслоение стенкиаорты, тромбоэмболию легочной артерии, аортальныйстеноз, гипертрофическую кардиомиопатию или пери-кардиальный выпот [33]. В связи с этим эхокардиогра-фию в отделениях интенсивной терапии следует про-водить всем пациентам.Если ЭКГ в 12 отведениях не информативна, ауровни сердечных биомаркеров у пациентов с предпо-лагаемым ОКС нормальные, может быть выполненасцинтиграфия миокарда с нагрузкой при условии от-сутствия боли в сердце. В различных исследованиях при-меняли также стресс-эхокардиографию, которая харак-теризовалась высоким предсказательным значениемотрицательного результата [34].Магнитно-резонансная томография (МРТ) сердцапозволяет одновременно оценить функцию и перфу-зию миокарда и выявить рубцовые изменения, одна-ко этот метод исследования пока малодоступен. В раз-личных исследованиях была показана информативностьМРТ в диагностике ОКС [35]. Кроме того, этот метод ис-пользуют для оценки жизнеспособности миокарда и ди-агностики миокардита.Показана также информативность перфузионнойсцинтиграфии миокарда, однако этот метод также не-достаточно широко доступен в круглосуточном режи-ме. Сцинтиграфия миокарда в покое была полезной наначальном этапе обследования пациентов с болью в гру-ди, у которых отсутствуют изменения на ЭКГ, или при-знаки сохраняющейся ишемии, или ИМ [36]. Проба снагрузкой имеет преимущество, так как она позволяетвыявить индуцируемую ишемию.Мультиспиральную компьютерную томографию(КТ) не применяют для диагностики ишемии, однакоэтот метод дает возможность прямо визуализироватькоронарные артерии. Теоретически с помощью муль-тиспиральной КТ можно исключить наличие ИБС. В раз-личных исследованиях было показано высокое пред-сказательное значение отрицательного результата ис-следования [37-41]. Для исключения ОКС или другихпричин боли в груди может быть полезной КТ-ангио-графия.
Инвазивные методы (коронарная ангиография)С помощью коронарной ангиографии получаютуникальную информацию о наличии и тяжести коро-нарного атеросклероза, поэтому данный метод по-преж-нему считают золотым стандартом. Ангиографию реко-мендуется проводить до и после интракоронарного вве-дения вазодилататоров (нитратов), чтобы уменьшитьвазоконстрикцию и устранить динамический компонентстеноза, который часто отмечается при ОКС. У пациен-тов с нарушением гемодинамики (отек легких, гипото-ния или тяжелые угрожающие жизни аритмии) целе-сообразно проводить исследования после введения ин-трааортального баллонного насоса.Ангиографию следует выполнять в неотложном по-рядке с диагностическими целями у пациентов высо-кого риска, а также в тех случаях, когда диагноз не ясен. Выявление острой тромботиче-ской окклюзии (например, огибающей артерии) име-ет особое значение у пациентов с сохраняющимисясимптомами или повышением уровня тропонинапри отсутствии диагностически значимых измене-ний на ЭКГ.В исследованиях TIMI-3B [42] и FRISC-2 [43] былопоказано, что у 30-38% пациентов с ОКС имеется по-ражение одной коронарной артерии, а у 44-49% — не-скольких (стеноз ≥50%). Частота стеноза левой глав-ной коронарной артерии составляет от 4-8%. У паци-ентов с поражением нескольких сосудов, а также ство-ла левой коронарной артерии имеется самый высокийриск развития серьезных неблагоприятных исходов. Ко-ронарная ангиография в сочетании с данными ЭКГ иасинергией стенки левого желудочка часто позволяетустановить, поражение какого сосуда стало причинойОКС. При ангиографии в типичном случае выявляют экс-центричный стеноз, неровные контуры, изъязвление идефекты наполнения, которые указывают на наличиеинтракоронарного тромба. Если трудно оценить тяжестьпоражения, то проводят внутрисосудистую эхографиюили измеряют фракционный резерв кровотока через >5дней после события [44]. Эти методы помогают выбратьстратегию лечения.Выбор сосудистого доступа зависит от опыта врача;этот выбор имеет важное значение, так как геморраги-ческие осложнения оказывают неблагоприятное влия-ние на клинические исходы. Лучевой доступ ассоции-ровался со снижением риска кровотечения по сравне-нию с таковым при феморальном доступе, поэтому пер-вый является предпочтительным при высоком риске ге-моррагических осложнений при условии, что врачимеет необходимый опыт. При лучевом доступе сни-жается риск образования крупной гематомы ценой более высокого облучения пациента и медицинских ра-ботников [45]. Феморальный доступ может быть пред-почтительным при нарушении гемодинамики, так какон облегчает проведение интрааортальной баллоннойконтрпульсации.
Дифференциальный диагноз
Некоторые заболевания сердца и других органов мо-гут имитировать ОКС без подъема сегмента ST (табл. 4).Гипертрофическая кардиомиопатия и пороки сердца(например, аортальный стеноз или аортальная недо-статочность) могут сопровождаться типичными симп-томами ОКС без подъема сегмента ST, повышеннымиуровнями биомаркеров или изменениями на ЭКГ [46].Иногда пароксизмальная фибрилляция предсердий(ФП) также имитирует ОКС. Некоторые такие пациен-ты страдают ИБС, что может быть причиной диагности-ческих трудностей. Миокардит, перикардит или мио-перикардит различной этиологии могут сопровож-даться болью в груди, сходной с типичной стенокарди-ей, и повышением уровней сердечных биомаркеров,изменениями ЭКГ и асинергией стенки левого желудоч-ка. Гриппоподобные симптомы, лихорадка и симпто-мы со стороны верхних дыхательных путей часто пред-шествуют развитию этих состояний или сопровож-дают их. Однако инфекции, особенно верхних отделовдыхательных путей, часто отмечают у пациентов с ОКСбез подъема сегмента ST. Установить диагноз миокар-дит или миоперикардит нередко удается только во вре-мя госпитализации.Необходимо также исключать угрожающие жизнизаболевания других органов. Например, тромбоэмбо-лия легочной артерии может сопровождаться одышкой,болью в груди и изменениями на ЭКГ, а также повышен-ными уровнями сердечных биомаркеров. Для диагно-стики тромбоэмболии легочной артерии определяютуровень Д-димера и проводят эхокардиографию иКТ. Альтернативный метод — МР-ангиография легочныхартерий, если этот метод доступен. Расслоение стенкиаорты — это еще одно заболевание, которое необходи-мо исключать при проведении дифференциального ди-агноза. ОКС без подъема сегмента ST может бытьосложнением расслоения стенки аорты, если оно рас-пространяется на коронарные артерии. Инсульт такжеможет сопровождаться изменениями на ЭКГ, асинер-гией стенки левого желудочка и повышением уровнейсердечных биомаркеров. Наоборот, атипичные симп-томы, такие как головная боль и головокружение, в ред-ких случаях могут быть единственным проявлением ише-мии миокарда.
4. Оценка прогнозаОКС без подъема сегмента ST — это нестабильное за-болевание, характеризующееся рецидивами ишемиии развитием других осложнений, которые могут при-вести к смерти или инфаркту миокарда в ближайшемили отдаленном периодах. Цели лечения, включающе-го в себя применение антиишемических и антитром-ботических лекарственных средств и различные стра-тегии реваскуляризации коронарных артерий, — пред-упредить или снизить риск таких осложнений и улуч-шить прогноз. Сроки и интенсивность вмешательствавыбирают с учетом индивидуального риска. Многие ме-тоды лечения повышают риск геморрагических ослож-нений, который необходимо тщательно взвешивать.Спектр риска, ассоциирующегося с ОКС без подъема сег-мента ST, широкий и особенно высокий в первыечасы, поэтому его необходимо тщательно оценивать не-медленно после первого контакта с врачом. Оценка рис-ка — это непрерывный процесс, который продолжает-ся до выписки пациента из стационара и может в лю-бые сроки оказать влияние на стратегию лечения. Гос-питализация пациентов в специальные отделения мо-жет улучшить результаты лечения больных с ОКС [47].У пациентов с ОКС без подъема сегмента ST риск оста-ется повышенным даже после выписки, поэтому они тре-буют особого внимания.
Таблица 4. Заболевания сердца и других органов, которые могут имитировать ОКС
 Клиническая оценка риска
Помимо некоторых универсальных факторов рис-ка, таких как пожилой возраст, сахарный диабет, почеч-ная недостаточность и другие состояния, важное значе-ние для оценки прогноза имеют первые клиническиепроявления. Например, симптомы в покое прогности-чески более неблагоприятны, чем симптомы, возникаю-щие при физической нагрузке. У пациентов с интермит-тирующими симптомами увеличение числа эпизодовишемии перед ОКС также оказывает влияние на про-гноз. Неблагоприятными прогностическими фактора-ми являются тахикардия, артериальная гипотония илисердечная недостаточность при поступлении; в таких слу-чаях необходимо быстро установить диагноз и назна-чить лечение [48-50]. У пациентов более молодого воз-раста с клиническими проявлениями ОКС необходимоисключать применение кокаина, которое сопровожда-ется более распространенным поражением миокардаи повышенным риском осложнений [51].
Электрокардиографические изменения
ЭКГ при поступлении позволяет предсказать риск вострую фазу. Если изменения на ЭКГ отсутствуют, то про-гноз более благоприятный, чем при наличии отрицатель-ных зубцов Т. У пациентов с депрессией сегмента ST про-гноз еще хуже и зависит от выраженности и распростра-ненности изменений на ЭКГ [52,53]. Число отведений,в которых определяются депрессия сегмента ST и степеньего депрессии, отражают распространенность и тяжестьишемии и коррелируют с прогнозом [52]. Депрессия сег-мента ST≥0,05 мВ в двух или более соседних отведенияхв сочетании с соответствующими клиническими проявле-ниями позволяет заподозрить ОКС без подъема сегмен-та ST и имеет прогностическое значение. Небольшую де-прессию сегмента ST (0,05 мВ) бывает трудно выявитьв клинической практике. Более важное клиническоезначение имеет депрессия сегмента ST≥0,1 мВ. В такихслучаях частота смерти и ИМ в течение ближайшего годасоставляет 11%. При депрессии сегмента ST≥0,2 мВ рисксмерти увеличивается примерно в 6 раз [53]. Депрессиясегмента ST в сочетании с преходящим его подъемом ука-зывает на еще более высокий риск.У пациентов с депрессией сегмента ST риск сердеч-но-сосудистых исходов выше, чем у пациентов с изо-лированной инверсией (≥0,1 мВ) зубца Т в отведенияхс преобладающим зубцом R, а у последних риск выше,чем у пациентов с нормальной ЭКГ при поступлении.Некоторые авторы высказывали сомнения по поводупрогностического значения изолированной инверсиизубцов Т, однако глубокие симметричные отрицатель-ные зубцы Т в передних грудных отведениях часто от-ражают выраженный стеноз проксимальной части ле-вой передней нисходящей коронарной артерии иствола левой коронарной артерии.Другие изменения, такие как подъем сегмента ST(≥0,1 мВ) в aVR, ассоциировались с высокой веро-ятностью стеноза левой основной коронарной артерииили трех коронарных артерий и неблагоприятнымпрогнозом [53].Пробы с нагрузкойПри сохранении типичной стенокардии покоя про-водить пробу с нагрузкой не следует. Однако проба с фи-зической нагрузкой позволяет сделать прогноз, поэто-му ее целесообразно выполнить перед выпиской приотсутствии диагностически значимых изменений на ЭКГ,а также боли, признаков сердечной недостаточности иповышенных уровней биомаркеров в динамике. Ран-няя проба с физической нагрузкой характеризуется вы-соким предсказательным значением отрицательного ре-зультата. Показатели, отражающие сократительнуюфункцию миокарда, имеют такое же прогностическоезначение, как показатели ишемии миокарда, а комби-нация таких показателей позволяет наиболее надежнооценить прогноз [54,55].Непрерывное мониторирование сегмента STВ нескольких исследованиях при непрерывном мо-ниторировании сегмента ST было показано, что у 15-30% пациентов с ОКС без подъема сегмента ST наблю-даются преходящие изменения сегмента ST, в основномего депрессия. У таких пациентов повышен риск раз-вития сердечно-сосудистых исходов, в том числе смер-ти [56]. Мониторирование сегмента ST дополняет про-гностическую информацию, полученную на основанииЭКГ в покое, уровней тропонинов и других клиническихпоказателей [56,57].
Биомаркеры
Биомаркеры отражают различные патофизиологи-ческие аспекты ОКС без подъема сегмента ST, такие какповреждение кардиомиоцитов, воспаление, активациятромбоцитов и нейрогуморальных систем. Для оценкириска развития ИМ и смерти в ближайшие 30 дн пред-почтительно использовать уровни тропонина Т или I[30,58]. Уровни тропонинов позволяли предсказать иотдаленный прогноз (1 год и более). У пациентов с ОКСбез подъема сегмента ST, у которых определяется по-вышенный уровень тропонина, но не изменена актив-ность МВ-фракции КК (доля их составляет около 28%от общего числа пациентов ОКС без подъема сегмен-та ST), отмечаются более высокий риск и пониженнаягоспитальная смертность по сравнению с пациентами,у которых повышены уровни обоих биомаркеров [59].Риск, связанный с повышенными уровнями тропони-на, не зависит от других факторов риска, таких как из-менения на ЭКГ в покое или при непрерывном мони-торировании и маркеры воспаления, и оказывает аддитивное действие на общий риск [60]. Выявление па-циентов с повышенными уровнями тропонина имеетзначение для выбора тактики ведения ОКС без подъе-ма сегмента ST. Однако при принятии решения не сле-дует учитывать только уровень тропонина, так как в опре-деленных группах пациентов высокого риска, у которыхуровень тропонина оставался нормальным, госпи-тальная летальность достигала 12,7% [61].Один отрицательный результат теста при первом ис-следовании может быть недостаточным для исключе-ния ОКС без подъема сегмента ST, так как у многих па-циентов уровень тропонина увеличивается в ближай-шие часы. В связи с этим рекомендуется повторный ана-лиз через 6-9 ч [27,30]. Разработанный недавно ульт-рачувствительный метод анализа тропонина позволяетнадежнее выделить пациентов группы риска и быстрооценить прогноз (дополнительную информацию см. вразделе 3.2.3. и на рис. 5).Хотя сердечные тропонины являются ключевымибиомаркерами при начальной стратификации риска,в клинических исследованиях изучалось прогностиче-ское значение многочисленных других биомаркеров.Среди них лучше всего изучены и используются вобычной практике высокочувствительный С-реактив-ный белок (вчСРБ) и мозговой натрийуретическийпептид (МНП). Натрийуретические пептиды, такиекак МНП и его N-терминальный фрагмент предшествен-ника МНП (NT-проМНП), — это высокочувствительныеи достаточно специфичные маркеры дисфункции ле-вого желудочка. Ретроспективные исследования пока-зали, что повышенные уровни МНП или NT-проМНПу пациентов с ОКС без подъема сегмента ST сопровож-даются увеличением смертности в 3-5 раз, а увеличе-ние риска не зависит от уровней тропонина или вчСРБ[62]. Риск смерти оставался повышенным даже послевнесения поправки на возраст, класс по Killip и фрак-цию выброса левого желудочка [60]. Уровни мозговыхнатрийуретических пептидов через несколько днейпосле появления симптомов позволяют предсказать про-гноз точнее, чем уровни при поступлении. Натрийуре-тические пептиды — это информативные маркеры в не-отложных ситуациях у пациентов с болью в груди илиодышкой, в частности они позволяли дифференциро-вать сердечные и несердечные причины одышки. Од-нако при оценке отдаленного прогноза они имеютограниченное значение при начальной стратификациириска и, соответственно, выбора тактики ведения па-циентов с ОКС без подъема сегмента ST [62].Среди многочисленных маркеров воспаления, ко-торые изучались на протяжении последнего десятиле-тия, СРБ, измеренный с помощью высокочувствитель-ного метода, лучше всего изучен и ассоциировался с не-желательными исходами. Установлено, что даже у па-циентов с тропонин-отрицательным ОКС без подъемасегмента ST повышенные уровни вчСРБ (≥10 мг/л) поз-воляют предсказать смертность в отдаленном периоде(от 6 мес до 4 лет) [60,63,64]. Исследование FRISC под-твердило, что повышенные уровни вчСРБ ассоциируют-ся с повышенной смертностью в раннем периоде и в от-даленные сроки (более 4 лет) [65]. Сходные результа-ты были получены в крупных когортах пациентов, ко-торых направляли на плановое ЧКВ. Самый высокийриск имели пациенты с персистирующим повышени-ем уровня вчСРБ [66]. Однако вчСРБ не имеет никако-го значения в диагностике ОКС.Гипергликемия при поступлении — это мощныйпредиктор смерти и сердечной недостаточности дажеу пациентов без диабета [67,68]. Недавно было пока-зано, что уровни гликемии натощак в начале госпита-лизации позволяют предсказать смертность лучше,чем уровни глюкозы при поступлении [68]. Крометого, изменения уровней гликемии натощак во времяпребывания в стационаре тесно ассоциируются с исхо-дами, а стойко нарушенная гликемия натощак указы-вает на неблагоприятный прогноз [67].Некоторые показатели общего анализа крови такжеявляются неблагоприятными прогностическими фак-торами. Риск неблагоприятных исходов повышается упациентов с анемией [69,70]. Увеличение числа лей-коцитов или снижение числа тромбоцитов в крови припоступлении также ассоциируется с неблагоприятнымпрогнозом [70].Нарушение функции почек — это независимыйпредиктор смертности в отдаленном периоде у паци-ентов с ОКС [60,71]. Сывороточная концентрациякреатинина — это менее надежный индикатор функциипочек, чем клиренс креатинина или расчетная скоростьклубочковой фильтрации (СКФ), так как она зависит отразличных факторов, включая возраст, массу тела,расу и прием различных лекарственных препаратов.Предложены несколько методов расчета СКФ на осно-вании сывороточного уровня креатинина, в частностиформулы Кокрофта-Голта и MDRD. Смертность в отда-ленном периоде экспоненциально увеличивается приснижении СКФ/клиренса креатинина.Новые биомаркерыВ клинических исследованиях изучались также дру-гие биомаркеры с целью более точной оценки риска,а также более раннего исключения диагноза ОКС.Наиболее перспективными считают биомаркеры, отра-жающие процессы сосудистого воспаления и оксида-тивного стресса. К ним, в частности, относят миелопе-роксидазу, фактор роста 15 и ассоциированную с ли-попротеином фосфолипазу А2 [72-75]. Для ранней ди-агностики ОКС могут быть использованы белок, связы-вающийся с жирными кислотами [76], или альбумин,модифицирующийся при ишемии [77], а также маркеры системного стресса (копептин) [78]. Однако их дополнительное значение, особенно по сравнению с вы-сокочувствительными методами измерения уровнятропонина, не изучалось, что не позволяет дать какие-либо практические рекомендации.
Индексы риска
Количественная оценка риска имеет важное значение для выбора метода лечения ОКС. Разработаны не-сколько индексов риска ишемических осложнений икровотечений, которые рассчитывают в различныесроки. В клинической практике предпочтительно при-менение простых показателей.Риск исходовДля оценки риска ишемических исходов в ближай-шие и средние сроки чаще всего используют индексыGRACE [50] или TIMI [49], которые несколько отличают-ся друг от друга (выборки пациентов, исходы, сроки,а также предикторы, которые оценивают на основанииисходных показателей, анамнеза, клинических проявле-ний, гемодинамических изменений, ЭКГ, лабораторныхпоказателей и лечения). По данным прямого сравне-ния [79,80], индекс GRACE позволяет точнее всегостратифицировать риск как при поступлении, так и пе-ред выпиской (табл. 5). Однако он предполагает слож-ные расчеты, требующие применения компьютера илиспециальных программ (расчеты могут быть выполне-ны online; http://www.outcomes.org/grace). Добавле-ние уровней биомаркеров (например, NT-проМНП) поз-воляет дополнительно повысить информативность ин-декса GRACE и улучшить оценку риска в отдаленном пе-риоде [81].Рассчитать индекс TIMI проще (учитываются только6 показателей), однако по точности он уступает индек-су GRACE [80]. Это связано с тем, что при расчете сум-марного индекса не учитываются ключевые факторыриска, такие как класс по Killip, частота сердечных со-кращений и систолическое АД [82].Риск кровотеченийКровотечение ухудшает прогноз у пациентов с ОКСбез подъема сегмента ST, поэтому необходимо пред-принимать все меры для профилактики геморрагиче-ских осложнений. Выделяют несколько факторов, ко-торые позволяют предсказать риск больших кровотече-ний во время госпитализации. На основании регистрови когортных исследований (ОКС и ЧКВ) разработаныиндексы риска кровотечения. Например, индексCRUSADE (www.crusadebleedingscore.org/) был пред-ложен на основании соответствующего регистра, в ко-торый были включены 71 277 пациентов. В последую-щем этот индекс был валидирован в когорте из 17 857пациентов из той же когорты (табл. 6) [83]. При увеличении индекса частота больших кровотечений посте-пенно увеличивалась (рис. 2). Этот индекс позволял до-статочно точно оценить риск кровотечений на основа-нии различных факторов, которые оценивали при по-ступлении и на фоне лечения. При расчете индекса неучитывается возраст, однако он используется при рас-чете клиренса креатинина [83].Другой индекс риска кровотечений был разработанна основании обследования 17 421 пациента, включен-ного в исследования ACUITY и HORIZONS [84]. Были вы-делены 6 независимых исходных предикторов (женскийпол, пожилой возраст, повышенный сывороточныйуровень креатинина, число лейкоцитов, анемия, ИМ сподъемом или без подъема сегмента ST) и 1 фактор,отражающий лечение (лечение гепарином или блока-тором гликопротеиновых IIb/IIIa рецепторов против при-менения только бивалирудина). Индекс позволяет вы-делить пациентов с повышенным риском кровотечений,не связанных с КШ, и смерти в течение 1 года, однакоон не был валидирован в независимом когортном ис-следовании.Оба индекса были предложены на основании обсле-дования пациентов, у которых применяли в основномили исключительно феморальный доступ для катетери-зации сердца. Их предсказательное значение может бытьниже при применении лучевого доступа. Любой индексне может заменить мнение врача, основывающееся наклинических данных, однако индексы представляют со-бой объективный инструмент, который используютдля оценки риска кровотечений у конкретного пациен-та или в определенной выборке.
Таблица 5. Смертность в стационаре и в течение 6 мес[50] в группах низкого, среднего и высокогориска, выделенных на основании индекса GRACE
Клиническая оценка риска
Помимо некоторых универсальных факторов рис-ка, таких как пожилой возраст, сахарный диабет, почеч-ная недостаточность и другие состояния, важное значе-ние для оценки прогноза имеют первые клиническиепроявления. Например, симптомы в покое прогности-чески более неблагоприятны, чем симптомы, возникаю-щие при физической нагрузке. У пациентов с интермит-тирующими симптомами увеличение числа эпизодовишемии перед ОКС также оказывает влияние на про-гноз. Неблагоприятными прогностическими фактора-ми являются тахикардия, артериальная гипотония илисердечная недостаточность при поступлении; в таких слу-чаях необходимо быстро установить диагноз и назна-чить лечение [48-50]. У пациентов более молодого воз-раста с клиническими проявлениями ОКС необходимоисключать применение кокаина, которое сопровожда-ется более распространенным поражением миокардаи повышенным риском осложнений [51].
Электрокардиографические изменения
ЭКГ при поступлении позволяет предсказать риск вострую фазу. Если изменения на ЭКГ отсутствуют, то про-гноз более благоприятный, чем при наличии отрицатель-ных зубцов Т. У пациентов с депрессией сегмента ST про-гноз еще хуже и зависит от выраженности и распростра-ненности изменений на ЭКГ [52,53]. Число отведений,в которых определяются депрессия сегмента ST и степеньего депрессии, отражают распространенность и тяжестьишемии и коррелируют с прогнозом [52]. Депрессия сег-мента ST≥0,05 мВ в двух или более соседних отведенияхв сочетании с соответствующими клиническими проявле-ниями позволяет заподозрить ОКС без подъема сегмен-та ST и имеет прогностическое значение. Небольшую де-прессию сегмента ST (0,05 мВ) бывает трудно выявитьв клинической практике. Более важное клиническоезначение имеет депрессия сегмента ST≥0,1 мВ. В такихслучаях частота смерти и ИМ в течение ближайшего годасоставляет 11%. При депрессии сегмента ST≥0,2 мВ рисксмерти увеличивается примерно в 6 раз [53]. Депрессиясегмента ST в сочетании с преходящим его подъемом ука-зывает на еще более высокий риск.У пациентов с депрессией сегмента ST риск сердеч-но-сосудистых исходов выше, чем у пациентов с изо-лированной инверсией (≥0,1 мВ) зубца Т в отведенияхс преобладающим зубцом R, а у последних риск выше,чем у пациентов с нормальной ЭКГ при поступлении.Некоторые авторы высказывали сомнения по поводупрогностического значения изолированной инверсиизубцов Т, однако глубокие симметричные отрицатель-ные зубцы Т в передних грудных отведениях часто от-ражают выраженный стеноз проксимальной части ле-вой передней нисходящей коронарной артерии иствола левой коронарной артерии.Другие изменения, такие как подъем сегмента ST(≥0,1 мВ) в aVR, ассоциировались с высокой веро-ятностью стеноза левой основной коронарной артерииили трех коронарных артерий и неблагоприятнымпрогнозом [53].Пробы с нагрузкойПри сохранении типичной стенокардии покоя про-водить пробу с нагрузкой не следует. Однако проба с фи-зической нагрузкой позволяет сделать прогноз, поэто-му ее целесообразно выполнить перед выпиской приотсутствии диагностически значимых изменений на ЭКГ,а также боли, признаков сердечной недостаточности иповышенных уровней биомаркеров в динамике. Ран-няя проба с физической нагрузкой характеризуется вы-соким предсказательным значением отрицательного ре-зультата. Показатели, отражающие сократительнуюфункцию миокарда, имеют такое же прогностическоезначение, как показатели ишемии миокарда, а комби-нация таких показателей позволяет наиболее надежнооценить прогноз [54,55].Непрерывное мониторирование сегмента STВ нескольких исследованиях при непрерывном мо-ниторировании сегмента ST было показано, что у 15-30% пациентов с ОКС без подъема сегмента ST наблю-даются преходящие изменения сегмента ST, в основномего депрессия. У таких пациентов повышен риск раз-вития сердечно-сосудистых исходов, в том числе смер-ти [56]. Мониторирование сегмента ST дополняет про-гностическую информацию, полученную на основанииЭКГ в покое, уровней тропонинов и других клиническихпоказателей [56,57].
Биомаркеры
Биомаркеры отражают различные патофизиологи-ческие аспекты ОКС без подъема сегмента ST, такие какповреждение кардиомиоцитов, воспаление, активациятромбоцитов и нейрогуморальных систем. Для оценкириска развития ИМ и смерти в ближайшие 30 дн пред-почтительно использовать уровни тропонина Т или I[30,58]. Уровни тропонинов позволяли предсказать иотдаленный прогноз (1 год и более). У пациентов с ОКСбез подъема сегмента ST, у которых определяется по-вышенный уровень тропонина, но не изменена актив-ность МВ-фракции КК (доля их составляет около 28%от общего числа пациентов ОКС без подъема сегмен-та ST), отмечаются более высокий риск и пониженнаягоспитальная смертность по сравнению с пациентами,у которых повышены уровни обоих биомаркеров [59].Риск, связанный с повышенными уровнями тропони-на, не зависит от других факторов риска, таких как из-менения на ЭКГ в покое или при непрерывном мони-торировании и маркеры воспаления, и оказывает аддитивное действие на общий риск [60]. Выявление па-циентов с повышенными уровнями тропонина имеетзначение для выбора тактики ведения ОКС без подъе-ма сегмента ST. Однако при принятии решения не сле-дует учитывать только уровень тропонина, так как в опре-деленных группах пациентов высокого риска, у которыхуровень тропонина оставался нормальным, госпи-тальная летальность достигала 12,7% [61].Один отрицательный результат теста при первом ис-следовании может быть недостаточным для исключе-ния ОКС без подъема сегмента ST, так как у многих па-циентов уровень тропонина увеличивается в ближай-шие часы. В связи с этим рекомендуется повторный ана-лиз через 6-9 ч [27,30]. Разработанный недавно ульт-рачувствительный метод анализа тропонина позволяетнадежнее выделить пациентов группы риска и быстрооценить прогноз (дополнительную информацию см. вразделе 3.2.3. и на рис. 5).Хотя сердечные тропонины являются ключевымибиомаркерами при начальной стратификации риска,в клинических исследованиях изучалось прогностиче-ское значение многочисленных других биомаркеров.Среди них лучше всего изучены и используются вобычной практике высокочувствительный С-реактив-ный белок (вчСРБ) и мозговой натрийуретическийпептид (МНП). Натрийуретические пептиды, такиекак МНП и его N-терминальный фрагмент предшествен-ника МНП (NT-проМНП), — это высокочувствительныеи достаточно специфичные маркеры дисфункции ле-вого желудочка. Ретроспективные исследования пока-зали, что повышенные уровни МНП или NT-проМНПу пациентов с ОКС без подъема сегмента ST сопровож-даются увеличением смертности в 3-5 раз, а увеличе-ние риска не зависит от уровней тропонина или вчСРБ[62]. Риск смерти оставался повышенным даже послевнесения поправки на возраст, класс по Killip и фрак-цию выброса левого желудочка [60]. Уровни мозговыхнатрийуретических пептидов через несколько днейпосле появления симптомов позволяют предсказать про-гноз точнее, чем уровни при поступлении. Натрийуре-тические пептиды — это информативные маркеры в не-отложных ситуациях у пациентов с болью в груди илиодышкой, в частности они позволяли дифференциро-вать сердечные и несердечные причины одышки. Од-нако при оценке отдаленного прогноза они имеютограниченное значение при начальной стратификациириска и, соответственно, выбора тактики ведения па-циентов с ОКС без подъема сегмента ST [62].Среди многочисленных маркеров воспаления, ко-торые изучались на протяжении последнего десятиле-тия, СРБ, измеренный с помощью высокочувствитель-ного метода, лучше всего изучен и ассоциировался с не-желательными исходами. Установлено, что даже у па-циентов с тропонин-отрицательным ОКС без подъемасегмента ST повышенные уровни вчСРБ (≥10 мг/л) поз-воляют предсказать смертность в отдаленном периоде(от 6 мес до 4 лет) [60,63,64]. Исследование FRISC под-твердило, что повышенные уровни вчСРБ ассоциируют-ся с повышенной смертностью в раннем периоде и в от-даленные сроки (более 4 лет) [65]. Сходные результа-ты были получены в крупных когортах пациентов, ко-торых направляли на плановое ЧКВ. Самый высокийриск имели пациенты с персистирующим повышени-ем уровня вчСРБ [66]. Однако вчСРБ не имеет никако-го значения в диагностике ОКС.Гипергликемия при поступлении — это мощныйпредиктор смерти и сердечной недостаточности дажеу пациентов без диабета [67,68]. Недавно было пока-зано, что уровни гликемии натощак в начале госпита-лизации позволяют предсказать смертность лучше,чем уровни глюкозы при поступлении [68]. Крометого, изменения уровней гликемии натощак во времяпребывания в стационаре тесно ассоциируются с исхо-дами, а стойко нарушенная гликемия натощак указы-вает на неблагоприятный прогноз [67].Некоторые показатели общего анализа крови такжеявляются неблагоприятными прогностическими фак-торами. Риск неблагоприятных исходов повышается упациентов с анемией [69,70]. Увеличение числа лей-коцитов или снижение числа тромбоцитов в крови припоступлении также ассоциируется с неблагоприятнымпрогнозом [70].Нарушение функции почек — это независимыйпредиктор смертности в отдаленном периоде у паци-ентов с ОКС [60,71]. Сывороточная концентрациякреатинина — это менее надежный индикатор функциипочек, чем клиренс креатинина или расчетная скоростьклубочковой фильтрации (СКФ), так как она зависит отразличных факторов, включая возраст, массу тела,расу и прием различных лекарственных препаратов.Предложены несколько методов расчета СКФ на осно-вании сывороточного уровня креатинина, в частностиформулы Кокрофта-Голта и MDRD. Смертность в отда-ленном периоде экспоненциально увеличивается приснижении СКФ/клиренса креатинина.Новые биомаркерыВ клинических исследованиях изучались также дру-гие биомаркеры с целью более точной оценки риска,а также более раннего исключения диагноза ОКС.Наиболее перспективными считают биомаркеры, отра-жающие процессы сосудистого воспаления и оксида-тивного стресса. К ним, в частности, относят миелопе-роксидазу, фактор роста 15 и ассоциированную с ли-попротеином фосфолипазу А2 [72-75]. Для ранней ди-агностики ОКС могут быть использованы белок, связы-вающийся с жирными кислотами [76], или альбумин,модифицирующийся при ишемии [77], а также маркеры системного стресса (копептин) [78]. Однако их дополнительное значение, особенно по сравнению с вы-сокочувствительными методами измерения уровнятропонина, не изучалось, что не позволяет дать какие-либо практические рекомендации.
Индексы риска
Количественная оценка риска имеет важное значение для выбора метода лечения ОКС. Разработаны не-сколько индексов риска ишемических осложнений икровотечений, которые рассчитывают в различныесроки. В клинической практике предпочтительно при-менение простых показателей.Риск исходовДля оценки риска ишемических исходов в ближай-шие и средние сроки чаще всего используют индексыGRACE [50] или TIMI [49], которые несколько отличают-ся друг от друга (выборки пациентов, исходы, сроки,а также предикторы, которые оценивают на основанииисходных показателей, анамнеза, клинических проявле-ний, гемодинамических изменений, ЭКГ, лабораторныхпоказателей и лечения). По данным прямого сравне-ния [79,80], индекс GRACE позволяет точнее всегостратифицировать риск как при поступлении, так и пе-ред выпиской (табл. 5). Однако он предполагает слож-ные расчеты, требующие применения компьютера илиспециальных программ (расчеты могут быть выполне-ны online; http://www.outcomes.org/grace). Добавле-ние уровней биомаркеров (например, NT-проМНП) поз-воляет дополнительно повысить информативность ин-декса GRACE и улучшить оценку риска в отдаленном пе-риоде [81].Рассчитать индекс TIMI проще (учитываются только6 показателей), однако по точности он уступает индек-су GRACE [80]. Это связано с тем, что при расчете сум-марного индекса не учитываются ключевые факторыриска, такие как класс по Killip, частота сердечных со-кращений и систолическое АД [82].Риск кровотеченийКровотечение ухудшает прогноз у пациентов с ОКСбез подъема сегмента ST, поэтому необходимо пред-принимать все меры для профилактики геморрагиче-ских осложнений. Выделяют несколько факторов, ко-торые позволяют предсказать риск больших кровотече-ний во время госпитализации. На основании регистрови когортных исследований (ОКС и ЧКВ) разработаныиндексы риска кровотечения. Например, индексCRUSADE (www.crusadebleedingscore.org/) был пред-ложен на основании соответствующего регистра, в ко-торый были включены 71 277 пациентов. В последую-щем этот индекс был валидирован в когорте из 17 857пациентов из той же когорты (табл. 6) [83]. При увеличении индекса частота больших кровотечений посте-пенно увеличивалась (рис. 2). Этот индекс позволял до-статочно точно оценить риск кровотечений на основа-нии различных факторов, которые оценивали при по-ступлении и на фоне лечения. При расчете индекса неучитывается возраст, однако он используется при рас-чете клиренса креатинина [83].Другой индекс риска кровотечений был разработанна основании обследования 17 421 пациента, включен-ного в исследования ACUITY и HORIZONS [84]. Были вы-делены 6 независимых исходных предикторов (женскийпол, пожилой возраст, повышенный сывороточныйуровень креатинина, число лейкоцитов, анемия, ИМ сподъемом или без подъема сегмента ST) и 1 фактор,отражающий лечение (лечение гепарином или блока-тором гликопротеиновых IIb/IIIa рецепторов против при-менения только бивалирудина). Индекс позволяет вы-делить пациентов с повышенным риском кровотечений,не связанных с КШ, и смерти в течение 1 года, однакоон не был валидирован в независимом когортном ис-следовании.Оба индекса были предложены на основании обсле-дования пациентов, у которых применяли в основномили исключительно феморальный доступ для катетери-зации сердца. Их предсказательное значение может бытьниже при применении лучевого доступа. Любой индексне может заменить мнение врача, основывающееся наклинических данных, однако индексы представляют со-бой объективный инструмент, который используютдля оценки риска кровотечений у конкретного пациен-та или в определенной выборке.
Таблица 5. Смертность в стационаре и в течение 6 мес[50] в группах низкого, среднего и высокогориска, выделенных на основании индекса GRACE
 Таблица 6. Индекс риска кровотечений CRUSADE [83]
Таблица 6. Индекс риска кровотечений CRUSADE [83]
 Рис. 2. Риск больших кровотечений в зависимостиот индекса CRUSADE(www.crusadebleedingscore.org/)
Рис. 2. Риск больших кровотечений в зависимостиот индекса CRUSADE(www.crusadebleedingscore.org/)
 Рекомендации по диагностике и оценке риска
Рекомендации по диагностике и оценке риска
 Риск в отдаленном периоде
Помимо факторов, позволяющих предсказать бли-жайший прогноз, выделяют также предикторы риска вотдаленном периоде. Они имеют важное значениедля пересмотра риска и могут привести к интенсифи-кации начальной тактики лечения. К таким факторамотносят осложненное течение ОКС, систолическуюфункцию левого желудочка, тяжесть ИБС, наличиереваскуляризации и признаки резидуальной ишемиипо данным неинвазивных методов.
Лечение
Антиишемические препараты
Антиишемические препараты снижают потребностьмиокарда в кислороде (за счет уменьшения частоты сер-дечных сокращений, АД, преднагрузки или сократимо-сти миокарда) или увеличивают доставку кислорода кмиокарду (за счет дилатации коронарных артерий).Бета-адреноблокаторыБета-адреноблокаторы подавляют эффекты цирку-лирующих катехоламинов на миокард и уменьшают по-требность его в кислороде за счет снижения частоты сер-дечных сокращений, АД и сократимости. Благоприятныеэффекты бета-адреноблокаторов были установлены упациентов с ИМ с подъемом сегмента ST и стабильнойстенокардией [85,86]. В двух двойных слепых рандо-мизированных исследованиях бета-адреноблокаторысравнивали с плацебо у пациентов с нестабильнойстенокардией [87,88]. При мета-анализе было показа-но, что лечение бета-адреноблокатором вызывает сни-жение относительного риска прогрессирования и раз-вития ИМ с подъемом сегмента ST на 13% [89]. Хотя вэтих относительно небольших исследованиях не былоподтверждено снижение смертности у пациентов сОКС без подъема сегмента ST, тем не менее, можно экс-траполировать результаты более крупных рандомизи-рованных исследований бета-адреноблокаторов убольных ИМ [90]. В регистре CRUSADE, в которыйвключали пациентов с ИМ без подъема сегментаST/нестабильной стенокардией из 509 американскихбольниц с 2001 по 2004 гг., у больных, получавших бета-адреноблокаторы в острый период, выявили снижениескорректированного риска госпитальной летальности на34% (3,9% и 6,9%, соответственно; p<0,001) [91].При систематизированном обзоре литературы небыло убедительно подтверждено снижение госпи-тальной летальности при раннем применении бета-ад-реноблокаторов у пациентов с острым или предпола-гаемым ИМ. Был сделан вывод, что имеющиеся дан-ные не позволяют рекомендовать назначение бета-ад-реноблокаторов в первые 8 ч после развития ОКС[92]. В пользу данной рекомендации свидетельствуютрезультаты исследования COMMIT, в которое в основ-ном включали пациентов с ИМ с подъемом сегмента ST.У пациентов группы метопролола частота кардиогенно-го шока была значительно выше, чем в контрольнойгруппе (5,0% и 3,9%; p<0,0001) [93]. После исклю-чения результатов COMMIT из мета-анализа было вы-явлено изменение относительного риска (ОР) госпиталь-ной летальности [ОР 0,86; 95% доверительный интер-вал (ДИ) 0,77–0,96] в пользу бета-адреноблокатора[92].НитратыПрименение нитратов при нестабильной стенокар-дии преимущественно основывается на патофизиоло-гических данных и клиническом опыте. Терапевтическиеэффекты нитратов и сходных препаратов, таких как син-донимины, связано с действием на периферические икоронарные сосуды. В основном эффективность нит-ратов, вероятно, отражает дилатацию вен, котораяприводит к снижению преднагрузки миокарда и конеч-ного диастолического объема левого желудочка, в ре-зультате чего уменьшается потребление миокардом кис-лорода. Кроме того, нитраты расширяют нормаль-ные, а также атеросклеротически измененные коронар-ные артерии и увеличивают коронарный коллатераль-ный кровоток.Исследования нитратов у пациентов с нестабильнойстенокардией были небольшими и неконтролируе-мыми. Эффективность этих препаратов в профилакти-ке неблагоприятных сердечно-сосудистых исходов в ран-домизированных плацебо-контролируемых исследо-ваниях не изучалась. Хотя при анализе результатов ис-следования TIMI-7 не был подтвержден протективныйэффект хронической терапии нитратами в отношениинестабильной стенокардии или ИМ [94], в регистреGRACE применение нитратов ассоциировалось с изме-нением структуры ОКС в пользу развития ОКС безподъема сегмента ST, а не ИМ с подъемом сегмента ST,и с уменьшением уровней маркеров некроза миокар-да [95].У пациентов с ОКС без подъема сегмента ST, кото-рым необходима госпитализация, внутривенное вве-дение нитратов купирует симптомы и вызывает регрессдепрессии сегмента ST более эффективно, чем их суб-лингвальное применение [96]. Дозу следует постепен-но увеличивать, пока не будут купированы симптомы(стенокардия и/или одышка), при условии отсутствияпобочных эффектов (особенно головной боли илигипотонии). При постоянном приеме нитратов разви-вается привыкание, которое зависит как от дозы, так иот длительности лечения.Нитраты не следует назначать пациентам, принимаю-щим ингибиторы фосфодиэстеразы-5 (силденафил,варденафил или тадалафил), учитывая риск выражен-ной вазодилатации и критического снижения АД.
Рекомендации по применению антиишемических препаратов
Риск в отдаленном периоде
Помимо факторов, позволяющих предсказать бли-жайший прогноз, выделяют также предикторы риска вотдаленном периоде. Они имеют важное значениедля пересмотра риска и могут привести к интенсифи-кации начальной тактики лечения. К таким факторамотносят осложненное течение ОКС, систолическуюфункцию левого желудочка, тяжесть ИБС, наличиереваскуляризации и признаки резидуальной ишемиипо данным неинвазивных методов.
Лечение
Антиишемические препараты
Антиишемические препараты снижают потребностьмиокарда в кислороде (за счет уменьшения частоты сер-дечных сокращений, АД, преднагрузки или сократимо-сти миокарда) или увеличивают доставку кислорода кмиокарду (за счет дилатации коронарных артерий).Бета-адреноблокаторыБета-адреноблокаторы подавляют эффекты цирку-лирующих катехоламинов на миокард и уменьшают по-требность его в кислороде за счет снижения частоты сер-дечных сокращений, АД и сократимости. Благоприятныеэффекты бета-адреноблокаторов были установлены упациентов с ИМ с подъемом сегмента ST и стабильнойстенокардией [85,86]. В двух двойных слепых рандо-мизированных исследованиях бета-адреноблокаторысравнивали с плацебо у пациентов с нестабильнойстенокардией [87,88]. При мета-анализе было показа-но, что лечение бета-адреноблокатором вызывает сни-жение относительного риска прогрессирования и раз-вития ИМ с подъемом сегмента ST на 13% [89]. Хотя вэтих относительно небольших исследованиях не былоподтверждено снижение смертности у пациентов сОКС без подъема сегмента ST, тем не менее, можно экс-траполировать результаты более крупных рандомизи-рованных исследований бета-адреноблокаторов убольных ИМ [90]. В регистре CRUSADE, в которыйвключали пациентов с ИМ без подъема сегментаST/нестабильной стенокардией из 509 американскихбольниц с 2001 по 2004 гг., у больных, получавших бета-адреноблокаторы в острый период, выявили снижениескорректированного риска госпитальной летальности на34% (3,9% и 6,9%, соответственно; p<0,001) [91].При систематизированном обзоре литературы небыло убедительно подтверждено снижение госпи-тальной летальности при раннем применении бета-ад-реноблокаторов у пациентов с острым или предпола-гаемым ИМ. Был сделан вывод, что имеющиеся дан-ные не позволяют рекомендовать назначение бета-ад-реноблокаторов в первые 8 ч после развития ОКС[92]. В пользу данной рекомендации свидетельствуютрезультаты исследования COMMIT, в которое в основ-ном включали пациентов с ИМ с подъемом сегмента ST.У пациентов группы метопролола частота кардиогенно-го шока была значительно выше, чем в контрольнойгруппе (5,0% и 3,9%; p<0,0001) [93]. После исклю-чения результатов COMMIT из мета-анализа было вы-явлено изменение относительного риска (ОР) госпиталь-ной летальности [ОР 0,86; 95% доверительный интер-вал (ДИ) 0,77–0,96] в пользу бета-адреноблокатора[92].НитратыПрименение нитратов при нестабильной стенокар-дии преимущественно основывается на патофизиоло-гических данных и клиническом опыте. Терапевтическиеэффекты нитратов и сходных препаратов, таких как син-донимины, связано с действием на периферические икоронарные сосуды. В основном эффективность нит-ратов, вероятно, отражает дилатацию вен, котораяприводит к снижению преднагрузки миокарда и конеч-ного диастолического объема левого желудочка, в ре-зультате чего уменьшается потребление миокардом кис-лорода. Кроме того, нитраты расширяют нормаль-ные, а также атеросклеротически измененные коронар-ные артерии и увеличивают коронарный коллатераль-ный кровоток.Исследования нитратов у пациентов с нестабильнойстенокардией были небольшими и неконтролируе-мыми. Эффективность этих препаратов в профилакти-ке неблагоприятных сердечно-сосудистых исходов в ран-домизированных плацебо-контролируемых исследо-ваниях не изучалась. Хотя при анализе результатов ис-следования TIMI-7 не был подтвержден протективныйэффект хронической терапии нитратами в отношениинестабильной стенокардии или ИМ [94], в регистреGRACE применение нитратов ассоциировалось с изме-нением структуры ОКС в пользу развития ОКС безподъема сегмента ST, а не ИМ с подъемом сегмента ST,и с уменьшением уровней маркеров некроза миокар-да [95].У пациентов с ОКС без подъема сегмента ST, кото-рым необходима госпитализация, внутривенное вве-дение нитратов купирует симптомы и вызывает регрессдепрессии сегмента ST более эффективно, чем их суб-лингвальное применение [96]. Дозу следует постепен-но увеличивать, пока не будут купированы симптомы(стенокардия и/или одышка), при условии отсутствияпобочных эффектов (особенно головной боли илигипотонии). При постоянном приеме нитратов разви-вается привыкание, которое зависит как от дозы, так иот длительности лечения.Нитраты не следует назначать пациентам, принимаю-щим ингибиторы фосфодиэстеразы-5 (силденафил,варденафил или тадалафил), учитывая риск выражен-ной вазодилатации и критического снижения АД.
Рекомендации по применению антиишемических препаратов
 Антагонисты кальция
Антагонисты кальция — это вазодилататоры. Неко-торые из них оказывают также прямое действие на ат-риовентрикулярное проведение и частоту сердечныхсокращений. Выделяют три класса антагонистов каль-ция, которые отличаются друг от друга по химическо-му строению и фармакологическому действию: дигид-ропиридины (такие как нифедипин), бензотиазепины(дилтиазем) и фенилэтиламины (верапамил). Препа-раты этих классов отличаются по степени вазодилати-рующего действия, снижения сократимости миокардаи замедления атриовентрикулярной проводимости. Не-дигидропиридиновые антагонисты кальция могут вы-звать атриовентрикулярную блокаду. Нифедипин иамлодипин оказывают более выраженное расширяю-щее действие на периферические артерии, в то времякак дилтиазем дает менее выраженный вазодилатирую-щий эффект. Препараты всех классов оказывают сопо-ставимое расширяющее действие на коронарные ар-терии. Соответственно, антагонисты кальция — этопрепараты выбора при вазоспастической стенокар-дии. Дилтиазем и верапамил обладают сопоставимойсимптоматической эффективностью и эквивалентныбета-адреноблокаторам [97,98].Влияние антагонистов кальция на прогноз больныхОКС без подъема сегмента ST изучалось только в неболь-ших рандомизированных исследованиях. Среди дигид-ропиридинов в основном применяли нифедипин. Вовсех исследованиях лечение нифедипином было не-эффективным при ИМ или во вторичной профилакти-ке после ИМ, а исследование HINT было прекращенодосрочно в связи с более высокой частотой повторно-го ИМ в группе нифедипина по сравнению с группойметопролола [88]. Напротив, в исследованияхDAVIT-I и DAVIT-II применение верапамила привело кснижению риска внезапной смерти, повторного инфарк-та и смерти от любых причин; эффект препарата былнаиболее выраженным у пациентов с сохранной функ-цией левого желудочка [99]. Сходная тенденция былаотмечена в исследованиях дилтиазема [100]. В отли-чие от бета-адреноблокаторов антагонисты кальция, по-видимому, не обладают общими эффектами, характер-ными для всего класса.Другие антиангинальные препаратыНикорандил, открывающий калиевые каналы, сни-жал частоту комбинированной первичной конечной точ-ки у пациентов со стабильной стенокардией, однако онне изучался у пациентов с ОКС [101]. Ивабрадин, се-лективно ингибирующий If каналы синусового узла, мо-жет применяться у отдельных пациентов при наличиипротивопоказаний к лечению бета-адреноблокатора-ми [102]. Ранолазин оказывает антиангинальное дей-ствие за счет ингибирования позднего натриевоготока. Он не влиял на риск основных сердечно-сосуди-стых исходов в исследовании MERLIN-TIMI 36, носнижал частоту рецидивирующей ишемии [103].
Антитромбоцитарные препараты
Активация и последующая агрегация тромбоцитовиграют основную роль в развитии артериального тром-боза и, соответственно, рассматриваются как ключевыемишени при лечении ОКС. Антитромбоцитарную тера-пию следует начинать как можно раньше, чтобы сни-зить риск как острых ишемических осложнений, так иповторных атеротромботических событий. Для ингиби-рования тромбоцитов используют препараты 3 классов,которые отличаются по механизму действия.Аспирин (ацетилсалициловая кислота) ингибируетциклооксигеназу (ЦОГ-1), блокирует образованиетромбоксана А2 и вызывает необратимую блокадуфункции тромбоцитов. Однако для эффективного лечения и профилактики коронарного тромбоза необхо-димо ингибировать дополнительные пути агрегациитромбоцитов. Взаимодействие АДФ с P2Y12 рецепто-рами тромбоцитов играет важную роль в активации иагрегации тромбоцитов и усиливает начальный ответклеток на повреждение сосудов. Блокаторы P2Y12рецепторов широко применяют для лечения ОКС. Тие-нопиридины клопидогрел и прасугрел — это пролекарст-ва, которые превращаются в активные молекулы, не-обратимо связывающиеся с P2Y12 рецепторами. Новымпрепаратом является тикагрелор — производное пири-мидина, которое после биотрансформации необрати-мо связывается с P2Y12 рецепторами, блокирует сигналь-ную систему АДФ и активацию тромбоцитов. Блокато-ры GP IIb/IIIa рецепторов, предназначенные для внут-ривенного введения (абциксимаб, эптифибатид и ти-рофибан), оказывают действие на последний общийэтап агрегации тромбоцитов.
Аспирин
В исследованиях, проводившихся 30 лет назад, былопоказано, что аспирин снижает частоту повторногоИМ и смерти у пациентов с нестабильной стенокарди-ей [отношение шансов (ОШ) 0,47; 95% ДИ 0,37–0,61;р<0,001] [104–106]. Лечение рекомендуется начинатьс нагрузочной дозы обычного аспирина (150-300мг), который следует разжевать [107]. Альтернативныйпуть — внутривенное введение аспирина, однако этаформа препарата не изучалась в рандомизированныхконтролируемых исследованиях и не везде доступна.Суточная поддерживающая доза 75-100 мг по эффек-тивности сопоставима с более высокими дозами, нореже вызывает желудочно-кишечные расстройства[108]; последние служат причиной отмены препаратау 1% больных. Аллергические реакции на аспирин (ана-филактический шок, кожная сыпь и астматическиереакции) встречаются редко (<0,5%). У части пациен-тов возможно десенсибилизация.Аспирин надежно ингибирует ЦОГ-1, поэтому мо-ниторирование его эффектов при хорошей привержен-ности не требуется. Нестероидные противовоспалитель-ные препараты (НПВП), такие как ибупрофен, обрати-мо блокируют ЦОГ-1 и препятствуют ее необратимо-му ингибированию под действием аспирина, а такжемогут оказывать протромботическое действие вследствиеингибирования ЦОГ-2. Соответственно, НПВП повышаютриск ишемических осложнений, поэтому их примене-ния следует избегать [109].
Блокаторы
P2Y12 рецепторов5.2.2.1. КлопидогрелИнформация о блокаторах P2Y12 рецепторов при-ведена в табл. 7. Тиклопидин был первым тиенопири-дином, который изучался у пациентов с ОКС, однакопозднее он был заменен клопидогрелом в связи с по-бочными эффектами. Сегодня тиклопидин можноприменять у пациентов с аллергией на клопидогрел, хотявозможна перекрестная реактивность. В исследованииCURE лечение клопидогрелом в нагрузочной дозе 300мг, а затем по 75 мг/сут в течение 9-12 мес в сочета-нии с аспирином привело к снижению частоты сердеч-но-сосудистой смерти, нефатального ИМ или инсуль-та по сравнению с монотерапией аспирином (9,3% и11,4%; ОР 0,80; 95% ДИ 0,72–0,90; p<0,001) у па-циентов с ОКС без подъема сегмента ST, у которых былиповышены уровни сердечных биомаркеров или опре-делялась депрессия сегмента ST, а также у пациентов ввозрасте старше 60 лет без ИБС в анамнезе [110]. Сни-жение риска развития ИМ было достоверным. От-мечена тенденция к снижению сердечно-сосудистойсмертности и частоты инсульта. Благоприятный эффектбыл сопоставимым во всех подгруппах пациентов, от-личавшихся по уровню сердечно-сосудистого риска, атакже у пожилых людей, пациентов с отклонениями сег-мента ST от изолинии, больных с повышенными инормальными уровнями биомаркеров, перенесших ине перенесших ЧКВ, пациентов с диабетом. Эффект со-хранялся в течение первых 30 дн, а также в последую-щие 11 мес [111]. После отмены клопидогрела возмож-но увеличение риска неблагоприятных исходов, осо-бенно у пациентов, получавших консервативное лече-ние [112]. Однако польза продолжения терапии более12 мес не установлена.В группе клопидогрела выявили увеличение часто-ты больших кровотечений (3,7% и 2,7%; ОР 1,38; 95%ДИ 1,13–1,67; p=0,001), однако достоверное увеличе-ние частоты угрожающих жизни и фатальных кровотече-ний отсутствовало [110]. Во всей когорте, включаяпациентов, направленных на реваскуляризацию (ЧКВили КШ), польза клопидогрела перевешивала риск кро-вотечений. Лечение клопидогрелом у 1000 пациентовпозволяло избежать 21 случая сердечно-сосудистойсмерти, ИМ или инсульта ценой 7 дополнительных слу-чаев кровотечения, требующего трансфузии крови, и4 дополнительных случаев угрожающих жизни крово-течений [113].В нагрузочной дозе 600 мг клопидогрел оказываетболее быстрое и мощное действие, чем в дозе 300 мг[114,115]. В поддерживающей дозе 150 мг/сут клопи-догрел также давал несколько более выраженный и по-стоянный эффект, чем в дозе 75 мг/сут [116]. В иссле-довании CURRENT-OASIS [117] сравнивали эффек-тивность клопидогрела в нагрузочной дозе 600 мг, за-тем 150 мг/сут (в течение 7 дней) и 75 мг/сут и стан-дартных доз у пациентов с ИМ с подъемом сегмента STили ОКС без подъема сегмента ST. В исследованиевключали пациентов с признаками ишемии миокардаи повышенными уровнями сердечных биомаркеров. Коронарную ангиографию с целью выполнения ЧКВ про-водили как можно раньше, но не позднее, чем через72 ч после рандомизации. В целом клопидогрел в бо-лее высокой дозе не имел преимуществ перед обычнойсхемой. Частота сердечно-сосудистой смерти, ИМ илиинсульта через 30 дн была сопоставимой в двух груп-пах [4,2% и 4,4%, соответственно; ОШ 0,94; 0,83–1,06;p=0,30], однако было отмечено увеличение частотыбольших кровотечений, которые оценивали по крите-риям CURRENT (2,5% и 2,0%; ОШ 1,24; 1,05–1,46;p=0,01) или TIMI (1,7% и 1,3%; ОШ 1,26; 1,03–1,54;p=0,03), а также необходимости в гемотрансфузиях(2,2% и 1,7%; ОШ 1,28; 1,07–1,54; p=0,01). В вы-борке больных (17623 пациента; у 63,1% из нихимелся ОКС без подъема сегмента ST), которым выпол-нено ЧКВ, отмечено снижение риска комбинированнойпервичной конечной точки, включавшей в себя сердеч-но-сосудистую смерть, ИМ и инсульт (3,9% и 4,5%; ОШ0,86; 95% ДИ 0,74–0,99; p=0,039) за счет уменьше-ния частоты ИМ на фоне применения клопидогрела вболее высокой дозе (2,0% и 2,6%; ОШ 0,69; 95% ДИ0,56–0,87; p=0,001). Частота тромбоза стента [покритериям Academic Research Consortium (ARC)] значи-тельно снизилась независимо от типа стента, в том чис-ле частота определенного или вероятного тромбоза (ОШ0,69; 95% ДИ 0,56–0,87; p=0,001) и частота опреде-ленного тромбоза (ОШ 0,54; 95% ДИ 0,39–0,74;p=0,0001). Большие кровотечения, которые диагно-стировали в соответствии с критериями CURRENT, приприменении клопидогрела в двойной дозе встречалисьчаще, чем при лечении стандартной дозой (1,6% и1,1%; ОШ 1,41; 95% ДИ 1,09–1,83; p=0,009). Одна-ко частота больших кровотечений в соответствии скритериями TIMI достоверно не отличалась междугруппами (1,0% и 0,7%; ОШ 1,36; 95% ДИ 0,97–1,90;p=0,074). Значительного увеличения риска фатальныхили внутричерепных кровотечений или кровотече-ний, связанных с КШ, в основной группе не выявили.Результаты лечения существенно не отличались у паци-ентов с ИМ с подъемом сегмента ST и ОКС без подъе-ма сегмента ST. Снижение риска первичной комбини-рованной конечной точки было сопоставимым в этихдвух выборках пациентов (ИМ с подъемом сегмента ST:4,2% и 5,0%; ОШ 0,83; 95% ДИ 0,66–1,05; p=0,117;ОКС без подъема сегмента ST: 3,6% и 4,2%; ОШ0,87; 95% ДИ 0,72–1,06; p=0,167) [108].Фармакодинамический ответ на клопидогрел оченьвариабельный, что связано с несколькими факторами,включая генетический полиморфизм. Клопидогрелпревращается в активный метаболит в печени в два эта-па, которые опосредуются изоферментами цитохромаР450, включая CYP3A4 и CYP2C19. Кроме того, всасы-вание клопидогрела (и прасугрела) регулируется Р-гли-копротеином (кодируется ABCB1), который представ-ляет собой АТФ-зависимый эффлюксный насос итранспортирует различные молекулы через внекле-точные и внутриклеточные оболочки. В частности он экс-прессируется эпителиальными клетками кишечника, аповышенная экспрессия или функция Р-гликопротеи-на может отразиться на биодоступности лекарственныхвеществ, являющихся его субстратами. В результате эф-фективность образования активного метаболита кло-пидогрела значительно отличается у разных людей и за-висит (в числе других факторов, таких как возраст, на-личие диабета и функция почек) от генетических поли-морфизмов, определяющих функцию Р-гликопротеи-на и CYP2C19 [118]. Нуклеотидные полиморфизмыABCB1 и CYP2C19, сопровождающиеся частичной илиполной утратой функции ферментов, ассоциировалисьс уменьшением степени ингибирования агрегациитромбоцитов и увеличением риска сердечно-сосуди-стых исходов, хотя результаты исследований, посвящен-ных этому вопросу, были противоречивыми [119,120].Хотя генетические тесты не являются рутинными в кли-нической практике, предпринимались попытки иден-тификации пациентов, плохо отвечающих на клопидо-грел, на основании анализа функции тромбоцитов exvivo [121]. Сохранение высокой реактивности тромбо-цитов после начала лечения клопидогрелом ассоции-ровалось с повышенным риском тромбоза стента и дру-гих ишемических исходов [122,123]. Однако клиниче-ское значение тестирования функции тромбоцитовокончательно не установлено. В единственном рандо-мизированном исследовании, в котором дозу клопи-догрела адаптировали с учетом остаточной реактивно-сти тромбоцитов, не было отмечено клинических пре-имуществ увеличения дозы препарата, несмотря на уме-ренное усиление блокады функции тромбоцитов [124].В настоящее время проводятся несколько исследова-ний с целью изучения целесообразности модификацииантитромбоцитарной терапии на основании результа-тов анализа функции тромбоцитов, однако в настоящеевремя рекомендовать измерение агрегации тромбоци-тов при лечении клопидогрелом у больных ОК Снельзя.Ингибиторы протонной помпы, которые подав-ляют CYP2C19, особенно омепразол, снижают антитром-боцитарную активность клопидогрела ex vivo, однакоубедительных клинических данных, подтверждающихвозможность увеличения риска ишемических исходовпри сочетанном применении клопидогрела и ингиби-торов протонной помпы, нет [125,126]. В одном ран-домизированном исследовании (было прекращенодосрочно в связи с отсутствием спонсора) сравнивалирезультаты применения клопидогрела в сочетании с оме-празолом и одного клопидогрела в течение 12 мес у па-циентов, нуждавшихся в двойной антитромбоцитарнойтерапии, включая больных, перенесших ЧКВ, пациен
Таблица 7. Результаты исследований блокаторов P2Y12 рецепторов
Антагонисты кальция
Антагонисты кальция — это вазодилататоры. Неко-торые из них оказывают также прямое действие на ат-риовентрикулярное проведение и частоту сердечныхсокращений. Выделяют три класса антагонистов каль-ция, которые отличаются друг от друга по химическо-му строению и фармакологическому действию: дигид-ропиридины (такие как нифедипин), бензотиазепины(дилтиазем) и фенилэтиламины (верапамил). Препа-раты этих классов отличаются по степени вазодилати-рующего действия, снижения сократимости миокардаи замедления атриовентрикулярной проводимости. Не-дигидропиридиновые антагонисты кальция могут вы-звать атриовентрикулярную блокаду. Нифедипин иамлодипин оказывают более выраженное расширяю-щее действие на периферические артерии, в то времякак дилтиазем дает менее выраженный вазодилатирую-щий эффект. Препараты всех классов оказывают сопо-ставимое расширяющее действие на коронарные ар-терии. Соответственно, антагонисты кальция — этопрепараты выбора при вазоспастической стенокар-дии. Дилтиазем и верапамил обладают сопоставимойсимптоматической эффективностью и эквивалентныбета-адреноблокаторам [97,98].Влияние антагонистов кальция на прогноз больныхОКС без подъема сегмента ST изучалось только в неболь-ших рандомизированных исследованиях. Среди дигид-ропиридинов в основном применяли нифедипин. Вовсех исследованиях лечение нифедипином было не-эффективным при ИМ или во вторичной профилакти-ке после ИМ, а исследование HINT было прекращенодосрочно в связи с более высокой частотой повторно-го ИМ в группе нифедипина по сравнению с группойметопролола [88]. Напротив, в исследованияхDAVIT-I и DAVIT-II применение верапамила привело кснижению риска внезапной смерти, повторного инфарк-та и смерти от любых причин; эффект препарата былнаиболее выраженным у пациентов с сохранной функ-цией левого желудочка [99]. Сходная тенденция былаотмечена в исследованиях дилтиазема [100]. В отли-чие от бета-адреноблокаторов антагонисты кальция, по-видимому, не обладают общими эффектами, характер-ными для всего класса.Другие антиангинальные препаратыНикорандил, открывающий калиевые каналы, сни-жал частоту комбинированной первичной конечной точ-ки у пациентов со стабильной стенокардией, однако онне изучался у пациентов с ОКС [101]. Ивабрадин, се-лективно ингибирующий If каналы синусового узла, мо-жет применяться у отдельных пациентов при наличиипротивопоказаний к лечению бета-адреноблокатора-ми [102]. Ранолазин оказывает антиангинальное дей-ствие за счет ингибирования позднего натриевоготока. Он не влиял на риск основных сердечно-сосуди-стых исходов в исследовании MERLIN-TIMI 36, носнижал частоту рецидивирующей ишемии [103].
Антитромбоцитарные препараты
Активация и последующая агрегация тромбоцитовиграют основную роль в развитии артериального тром-боза и, соответственно, рассматриваются как ключевыемишени при лечении ОКС. Антитромбоцитарную тера-пию следует начинать как можно раньше, чтобы сни-зить риск как острых ишемических осложнений, так иповторных атеротромботических событий. Для ингиби-рования тромбоцитов используют препараты 3 классов,которые отличаются по механизму действия.Аспирин (ацетилсалициловая кислота) ингибируетциклооксигеназу (ЦОГ-1), блокирует образованиетромбоксана А2 и вызывает необратимую блокадуфункции тромбоцитов. Однако для эффективного лечения и профилактики коронарного тромбоза необхо-димо ингибировать дополнительные пути агрегациитромбоцитов. Взаимодействие АДФ с P2Y12 рецепто-рами тромбоцитов играет важную роль в активации иагрегации тромбоцитов и усиливает начальный ответклеток на повреждение сосудов. Блокаторы P2Y12рецепторов широко применяют для лечения ОКС. Тие-нопиридины клопидогрел и прасугрел — это пролекарст-ва, которые превращаются в активные молекулы, не-обратимо связывающиеся с P2Y12 рецепторами. Новымпрепаратом является тикагрелор — производное пири-мидина, которое после биотрансформации необрати-мо связывается с P2Y12 рецепторами, блокирует сигналь-ную систему АДФ и активацию тромбоцитов. Блокато-ры GP IIb/IIIa рецепторов, предназначенные для внут-ривенного введения (абциксимаб, эптифибатид и ти-рофибан), оказывают действие на последний общийэтап агрегации тромбоцитов.
Аспирин
В исследованиях, проводившихся 30 лет назад, былопоказано, что аспирин снижает частоту повторногоИМ и смерти у пациентов с нестабильной стенокарди-ей [отношение шансов (ОШ) 0,47; 95% ДИ 0,37–0,61;р<0,001] [104–106]. Лечение рекомендуется начинатьс нагрузочной дозы обычного аспирина (150-300мг), который следует разжевать [107]. Альтернативныйпуть — внутривенное введение аспирина, однако этаформа препарата не изучалась в рандомизированныхконтролируемых исследованиях и не везде доступна.Суточная поддерживающая доза 75-100 мг по эффек-тивности сопоставима с более высокими дозами, нореже вызывает желудочно-кишечные расстройства[108]; последние служат причиной отмены препаратау 1% больных. Аллергические реакции на аспирин (ана-филактический шок, кожная сыпь и астматическиереакции) встречаются редко (<0,5%). У части пациен-тов возможно десенсибилизация.Аспирин надежно ингибирует ЦОГ-1, поэтому мо-ниторирование его эффектов при хорошей привержен-ности не требуется. Нестероидные противовоспалитель-ные препараты (НПВП), такие как ибупрофен, обрати-мо блокируют ЦОГ-1 и препятствуют ее необратимо-му ингибированию под действием аспирина, а такжемогут оказывать протромботическое действие вследствиеингибирования ЦОГ-2. Соответственно, НПВП повышаютриск ишемических осложнений, поэтому их примене-ния следует избегать [109].
Блокаторы
P2Y12 рецепторов5.2.2.1. КлопидогрелИнформация о блокаторах P2Y12 рецепторов при-ведена в табл. 7. Тиклопидин был первым тиенопири-дином, который изучался у пациентов с ОКС, однакопозднее он был заменен клопидогрелом в связи с по-бочными эффектами. Сегодня тиклопидин можноприменять у пациентов с аллергией на клопидогрел, хотявозможна перекрестная реактивность. В исследованииCURE лечение клопидогрелом в нагрузочной дозе 300мг, а затем по 75 мг/сут в течение 9-12 мес в сочета-нии с аспирином привело к снижению частоты сердеч-но-сосудистой смерти, нефатального ИМ или инсуль-та по сравнению с монотерапией аспирином (9,3% и11,4%; ОР 0,80; 95% ДИ 0,72–0,90; p<0,001) у па-циентов с ОКС без подъема сегмента ST, у которых былиповышены уровни сердечных биомаркеров или опре-делялась депрессия сегмента ST, а также у пациентов ввозрасте старше 60 лет без ИБС в анамнезе [110]. Сни-жение риска развития ИМ было достоверным. От-мечена тенденция к снижению сердечно-сосудистойсмертности и частоты инсульта. Благоприятный эффектбыл сопоставимым во всех подгруппах пациентов, от-личавшихся по уровню сердечно-сосудистого риска, атакже у пожилых людей, пациентов с отклонениями сег-мента ST от изолинии, больных с повышенными инормальными уровнями биомаркеров, перенесших ине перенесших ЧКВ, пациентов с диабетом. Эффект со-хранялся в течение первых 30 дн, а также в последую-щие 11 мес [111]. После отмены клопидогрела возмож-но увеличение риска неблагоприятных исходов, осо-бенно у пациентов, получавших консервативное лече-ние [112]. Однако польза продолжения терапии более12 мес не установлена.В группе клопидогрела выявили увеличение часто-ты больших кровотечений (3,7% и 2,7%; ОР 1,38; 95%ДИ 1,13–1,67; p=0,001), однако достоверное увеличе-ние частоты угрожающих жизни и фатальных кровотече-ний отсутствовало [110]. Во всей когорте, включаяпациентов, направленных на реваскуляризацию (ЧКВили КШ), польза клопидогрела перевешивала риск кро-вотечений. Лечение клопидогрелом у 1000 пациентовпозволяло избежать 21 случая сердечно-сосудистойсмерти, ИМ или инсульта ценой 7 дополнительных слу-чаев кровотечения, требующего трансфузии крови, и4 дополнительных случаев угрожающих жизни крово-течений [113].В нагрузочной дозе 600 мг клопидогрел оказываетболее быстрое и мощное действие, чем в дозе 300 мг[114,115]. В поддерживающей дозе 150 мг/сут клопи-догрел также давал несколько более выраженный и по-стоянный эффект, чем в дозе 75 мг/сут [116]. В иссле-довании CURRENT-OASIS [117] сравнивали эффек-тивность клопидогрела в нагрузочной дозе 600 мг, за-тем 150 мг/сут (в течение 7 дней) и 75 мг/сут и стан-дартных доз у пациентов с ИМ с подъемом сегмента STили ОКС без подъема сегмента ST. В исследованиевключали пациентов с признаками ишемии миокардаи повышенными уровнями сердечных биомаркеров. Коронарную ангиографию с целью выполнения ЧКВ про-водили как можно раньше, но не позднее, чем через72 ч после рандомизации. В целом клопидогрел в бо-лее высокой дозе не имел преимуществ перед обычнойсхемой. Частота сердечно-сосудистой смерти, ИМ илиинсульта через 30 дн была сопоставимой в двух груп-пах [4,2% и 4,4%, соответственно; ОШ 0,94; 0,83–1,06;p=0,30], однако было отмечено увеличение частотыбольших кровотечений, которые оценивали по крите-риям CURRENT (2,5% и 2,0%; ОШ 1,24; 1,05–1,46;p=0,01) или TIMI (1,7% и 1,3%; ОШ 1,26; 1,03–1,54;p=0,03), а также необходимости в гемотрансфузиях(2,2% и 1,7%; ОШ 1,28; 1,07–1,54; p=0,01). В вы-борке больных (17623 пациента; у 63,1% из нихимелся ОКС без подъема сегмента ST), которым выпол-нено ЧКВ, отмечено снижение риска комбинированнойпервичной конечной точки, включавшей в себя сердеч-но-сосудистую смерть, ИМ и инсульт (3,9% и 4,5%; ОШ0,86; 95% ДИ 0,74–0,99; p=0,039) за счет уменьше-ния частоты ИМ на фоне применения клопидогрела вболее высокой дозе (2,0% и 2,6%; ОШ 0,69; 95% ДИ0,56–0,87; p=0,001). Частота тромбоза стента [покритериям Academic Research Consortium (ARC)] значи-тельно снизилась независимо от типа стента, в том чис-ле частота определенного или вероятного тромбоза (ОШ0,69; 95% ДИ 0,56–0,87; p=0,001) и частота опреде-ленного тромбоза (ОШ 0,54; 95% ДИ 0,39–0,74;p=0,0001). Большие кровотечения, которые диагно-стировали в соответствии с критериями CURRENT, приприменении клопидогрела в двойной дозе встречалисьчаще, чем при лечении стандартной дозой (1,6% и1,1%; ОШ 1,41; 95% ДИ 1,09–1,83; p=0,009). Одна-ко частота больших кровотечений в соответствии скритериями TIMI достоверно не отличалась междугруппами (1,0% и 0,7%; ОШ 1,36; 95% ДИ 0,97–1,90;p=0,074). Значительного увеличения риска фатальныхили внутричерепных кровотечений или кровотече-ний, связанных с КШ, в основной группе не выявили.Результаты лечения существенно не отличались у паци-ентов с ИМ с подъемом сегмента ST и ОКС без подъе-ма сегмента ST. Снижение риска первичной комбини-рованной конечной точки было сопоставимым в этихдвух выборках пациентов (ИМ с подъемом сегмента ST:4,2% и 5,0%; ОШ 0,83; 95% ДИ 0,66–1,05; p=0,117;ОКС без подъема сегмента ST: 3,6% и 4,2%; ОШ0,87; 95% ДИ 0,72–1,06; p=0,167) [108].Фармакодинамический ответ на клопидогрел оченьвариабельный, что связано с несколькими факторами,включая генетический полиморфизм. Клопидогрелпревращается в активный метаболит в печени в два эта-па, которые опосредуются изоферментами цитохромаР450, включая CYP3A4 и CYP2C19. Кроме того, всасы-вание клопидогрела (и прасугрела) регулируется Р-гли-копротеином (кодируется ABCB1), который представ-ляет собой АТФ-зависимый эффлюксный насос итранспортирует различные молекулы через внекле-точные и внутриклеточные оболочки. В частности он экс-прессируется эпителиальными клетками кишечника, аповышенная экспрессия или функция Р-гликопротеи-на может отразиться на биодоступности лекарственныхвеществ, являющихся его субстратами. В результате эф-фективность образования активного метаболита кло-пидогрела значительно отличается у разных людей и за-висит (в числе других факторов, таких как возраст, на-личие диабета и функция почек) от генетических поли-морфизмов, определяющих функцию Р-гликопротеи-на и CYP2C19 [118]. Нуклеотидные полиморфизмыABCB1 и CYP2C19, сопровождающиеся частичной илиполной утратой функции ферментов, ассоциировалисьс уменьшением степени ингибирования агрегациитромбоцитов и увеличением риска сердечно-сосуди-стых исходов, хотя результаты исследований, посвящен-ных этому вопросу, были противоречивыми [119,120].Хотя генетические тесты не являются рутинными в кли-нической практике, предпринимались попытки иден-тификации пациентов, плохо отвечающих на клопидо-грел, на основании анализа функции тромбоцитов exvivo [121]. Сохранение высокой реактивности тромбо-цитов после начала лечения клопидогрелом ассоции-ровалось с повышенным риском тромбоза стента и дру-гих ишемических исходов [122,123]. Однако клиниче-ское значение тестирования функции тромбоцитовокончательно не установлено. В единственном рандо-мизированном исследовании, в котором дозу клопи-догрела адаптировали с учетом остаточной реактивно-сти тромбоцитов, не было отмечено клинических пре-имуществ увеличения дозы препарата, несмотря на уме-ренное усиление блокады функции тромбоцитов [124].В настоящее время проводятся несколько исследова-ний с целью изучения целесообразности модификацииантитромбоцитарной терапии на основании результа-тов анализа функции тромбоцитов, однако в настоящеевремя рекомендовать измерение агрегации тромбоци-тов при лечении клопидогрелом у больных ОК Снельзя.Ингибиторы протонной помпы, которые подав-ляют CYP2C19, особенно омепразол, снижают антитром-боцитарную активность клопидогрела ex vivo, однакоубедительных клинических данных, подтверждающихвозможность увеличения риска ишемических исходовпри сочетанном применении клопидогрела и ингиби-торов протонной помпы, нет [125,126]. В одном ран-домизированном исследовании (было прекращенодосрочно в связи с отсутствием спонсора) сравнивалирезультаты применения клопидогрела в сочетании с оме-празолом и одного клопидогрела в течение 12 мес у па-циентов, нуждавшихся в двойной антитромбоцитарнойтерапии, включая больных, перенесших ЧКВ, пациен
Таблица 7. Результаты исследований блокаторов P2Y12 рецепторов
 тов с ОКС и др. Увеличения частоты ишемических ис-ходов отмечено не было, однако в группе омепразоланаблюдалось снижение риска кровотечений из верх-них отделов желудочно-кишечного тракта [127]. Часто-та ишемических событий была низкой, что не позволяетсделать вывод о влиянии омепразола на эффективностьклопидогрела у пациентов более высокого риска.Мощные ингибиторы (например, кетоконазол) или ин-дукторы (например, рифампицин) CYP3A4 могутзначительно снизить или усилить, соответственно, ин-гибирующий эффект клопидогрела, однако эти препа-раты редко применяют у пациентов с ОКС без подъе-ма сегмента ST.Нежелательные эффекты клопидогрела. Помимокровотечений при лечении клопидогрелом могут наблю-даться желудочно-кишечные расстройства (диарея,дискомфорт в животе) и сыпь. Тромботическая тром-боцитопеническая пурпура и дискразии крови встре-чаются редко. При аллергии на клопидогрел возмож-на десенсибилизация.5.2.2.2. ПрасугрелПрасугрел в два этапа превращается в активный ме-таболит, который по химическому строению сходен с ак-тивным метаболитом клопидогрела [119]. Первыйэтап биотрансформации происходит под действиемэстераз плазмы, а второй осуществляется в печени приучастии изоферментов CYP. Соответственно, прасу-грел оказывает более быстрое и постоянное ингибирую-щее действие на тромбоциты по сравнению с клопидо-грелом [128]. Ответ на прасугрел существенно не зави-сит от действия ингибиторов CYP, включая ингибиторыпротонной помпы, и полиморфизма гена CYP2C19, атакже функции ABCB1 [129].В исследовании TRITON-TIMI 38 сравнивали прасу-грел в нагрузочной дозе 60 мг, а затем 10 мг/сут и кло-пидогрел в нагрузочной дозе 300 мг, а затем 75 мг/сутпосле ЧКВ у пациентов, не получавших ранее клопидо-грел; показаниями к ЧКВ были острый ИМ с подъемомсегмента ST (первичное вмешательство) или недавноперенесенный ИМ с подъемом сегмента ST, а также ОКСбез подъема сегмента у пациентов среднего или высо-кого риска [130]. Пациентов с ОКС без подъема сегмен-та ST, которым проводилось консервативное лечение,в исследование не включали. Критериями включениябыли симптомы ишемии в течение 72 ч, индекс рискаTIMI≥3 и отклонение сегмента ST≥1 или повышенныеуровни сердечного биомаркера. В когорте пациентовс ОКС без подъема сегмента ST (n=10074) лечение ис-следуемым препаратом начинали в течение 1 ч послеангиографии, подтвердившей возможность ЧКВ. Ча-стота комбинированной первичной конечной точки (сер-дечно-сосудистая смерть, нефатальный ИМ или инсульт)составила 11,2% в группе клопидогрела и 9,3% в груп-пе прасугрела (ОШ 0,82; 95% ДИ 0,73–0,93; p=0,002);снижение ее частоты во второй группе в основном от-ражало достоверное снижение риска развития ИМ(с 9,2% до 7,1%; на 23,9%; 95% ДИ 12,7–33,7;p<0,001) [130]. Частота нефатального инсульта или сер-дечно-сосудистой смерти достоверно не отличаласьмежду группами. Во всей когорте частота определен-ного или вероятного тромбоза стента (ко критериямARC) в группе прасугрела значительно снизилась посравнению с группой клопидогрела (1,1% и 2,4%,соответственно; ОШ 0,48; 95% ДИ 0,36–0,64;p<0,001). Соответствующие показатели у пациентов сОКС без подъема сегмента SТ не известны.Во всей когорте в группе прасугрела отмечалосьзначительное увеличение частоты больших (по крите-риям TIMI) кровотечений, не связанных с КШ (2,4% и1,8%; ОШ 1,32; 95% ДИ 1,03–1,68; p=0,03), в основ-ном за счет спонтанных кровотечений (1,6% и 1,1%;ОШ 1,51; 95% ДИ 1,09–2,08; p=0,01), а не кровотече-ний, связанных с пункцией артерии (0,7% и 0,6%; ОШ1,18; 95% ДИ 0,77–1,82; p=0,45). В группе прасугре-ла значительно увеличился риск угрожающих жизникровотечений (1,4% и 0,9%; ОШ 1,52; 95% ДИ1,08–2,13; p=0,01), а также фатальных кровотечений(0,4% и 0,1%; ОШ 4,19; 95% ДИ 1,58–11,11;p=0,002). У пациентов с цереброваскулярными нару-шениями в анамнезе риск кровотечений при лечениипрасугрелом перевешивал его пользу [130]. Кроме того,не было отмечено «чистой» клинической пользы лече-ния у пациентов в возрасте ≥75 лет и больных с низкоймассой тела (≤60 кг). Более выраженный клиническийэффект без увеличения риска кровотечений наблюдал-ся у пациентов с диабетом. У пациентов с нарушениемфункции почек (клиренс креатинина≤60 мл/мин) и нор-мальной функцией почек (клиренс креатинина>60мл/мин) эффективность препарата не отличалась.Нежелательные эффекты прасугрела. Частота дру-гих нежелательных явлений в исследовании TRITONбыла сопоставимой в группах прасугрела и клопидо-грела. Тромбоцитопения встречалась в двух группах содинаковой частотой (0,3%), в то время как нейтропе-ния реже развивалась в группе прасугрела (<0,1% и0,2%; p=0,02).5.2.2.3. ТикагрелорТикагрелор принадлежит к новому химическомуклассу (циклопентилтриазолопиримидины) и являет-ся пероральным обратимым ингибитором P2Y12рецепторов с периодом полувыведения из плазмыоколо 12 ч. Степень блокады P2Y12 рецепторов зави-сит от уровня тикагрелора в плазме и в меньшей сте-пени его метаболита. Как и прасугрел, он оказывает бо-лее быстрое и постоянное действие, чем клопидо-грел. Кроме того, его действие прекращается быстрее, поэтому функция тромбоцитов также восстанавлива-ется в более короткие сроки (табл. 8) [131]. Тикагре-лор увеличивает уровни препаратов, которые метабо-лизируются под действием CYP3A, таких как симваста-тин, в то время как умеренные ингибиторы CYP3A, та-кие как дилтиазем, увеличивают уровни и снижают ско-рость прекращения действия тикагрелора.
Таблица 8. Блокаторы P2Y12 рецепторов
тов с ОКС и др. Увеличения частоты ишемических ис-ходов отмечено не было, однако в группе омепразоланаблюдалось снижение риска кровотечений из верх-них отделов желудочно-кишечного тракта [127]. Часто-та ишемических событий была низкой, что не позволяетсделать вывод о влиянии омепразола на эффективностьклопидогрела у пациентов более высокого риска.Мощные ингибиторы (например, кетоконазол) или ин-дукторы (например, рифампицин) CYP3A4 могутзначительно снизить или усилить, соответственно, ин-гибирующий эффект клопидогрела, однако эти препа-раты редко применяют у пациентов с ОКС без подъе-ма сегмента ST.Нежелательные эффекты клопидогрела. Помимокровотечений при лечении клопидогрелом могут наблю-даться желудочно-кишечные расстройства (диарея,дискомфорт в животе) и сыпь. Тромботическая тром-боцитопеническая пурпура и дискразии крови встре-чаются редко. При аллергии на клопидогрел возмож-на десенсибилизация.5.2.2.2. ПрасугрелПрасугрел в два этапа превращается в активный ме-таболит, который по химическому строению сходен с ак-тивным метаболитом клопидогрела [119]. Первыйэтап биотрансформации происходит под действиемэстераз плазмы, а второй осуществляется в печени приучастии изоферментов CYP. Соответственно, прасу-грел оказывает более быстрое и постоянное ингибирую-щее действие на тромбоциты по сравнению с клопидо-грелом [128]. Ответ на прасугрел существенно не зави-сит от действия ингибиторов CYP, включая ингибиторыпротонной помпы, и полиморфизма гена CYP2C19, атакже функции ABCB1 [129].В исследовании TRITON-TIMI 38 сравнивали прасу-грел в нагрузочной дозе 60 мг, а затем 10 мг/сут и кло-пидогрел в нагрузочной дозе 300 мг, а затем 75 мг/сутпосле ЧКВ у пациентов, не получавших ранее клопидо-грел; показаниями к ЧКВ были острый ИМ с подъемомсегмента ST (первичное вмешательство) или недавноперенесенный ИМ с подъемом сегмента ST, а также ОКСбез подъема сегмента у пациентов среднего или высо-кого риска [130]. Пациентов с ОКС без подъема сегмен-та ST, которым проводилось консервативное лечение,в исследование не включали. Критериями включениябыли симптомы ишемии в течение 72 ч, индекс рискаTIMI≥3 и отклонение сегмента ST≥1 или повышенныеуровни сердечного биомаркера. В когорте пациентовс ОКС без подъема сегмента ST (n=10074) лечение ис-следуемым препаратом начинали в течение 1 ч послеангиографии, подтвердившей возможность ЧКВ. Ча-стота комбинированной первичной конечной точки (сер-дечно-сосудистая смерть, нефатальный ИМ или инсульт)составила 11,2% в группе клопидогрела и 9,3% в груп-пе прасугрела (ОШ 0,82; 95% ДИ 0,73–0,93; p=0,002);снижение ее частоты во второй группе в основном от-ражало достоверное снижение риска развития ИМ(с 9,2% до 7,1%; на 23,9%; 95% ДИ 12,7–33,7;p<0,001) [130]. Частота нефатального инсульта или сер-дечно-сосудистой смерти достоверно не отличаласьмежду группами. Во всей когорте частота определен-ного или вероятного тромбоза стента (ко критериямARC) в группе прасугрела значительно снизилась посравнению с группой клопидогрела (1,1% и 2,4%,соответственно; ОШ 0,48; 95% ДИ 0,36–0,64;p<0,001). Соответствующие показатели у пациентов сОКС без подъема сегмента SТ не известны.Во всей когорте в группе прасугрела отмечалосьзначительное увеличение частоты больших (по крите-риям TIMI) кровотечений, не связанных с КШ (2,4% и1,8%; ОШ 1,32; 95% ДИ 1,03–1,68; p=0,03), в основ-ном за счет спонтанных кровотечений (1,6% и 1,1%;ОШ 1,51; 95% ДИ 1,09–2,08; p=0,01), а не кровотече-ний, связанных с пункцией артерии (0,7% и 0,6%; ОШ1,18; 95% ДИ 0,77–1,82; p=0,45). В группе прасугре-ла значительно увеличился риск угрожающих жизникровотечений (1,4% и 0,9%; ОШ 1,52; 95% ДИ1,08–2,13; p=0,01), а также фатальных кровотечений(0,4% и 0,1%; ОШ 4,19; 95% ДИ 1,58–11,11;p=0,002). У пациентов с цереброваскулярными нару-шениями в анамнезе риск кровотечений при лечениипрасугрелом перевешивал его пользу [130]. Кроме того,не было отмечено «чистой» клинической пользы лече-ния у пациентов в возрасте ≥75 лет и больных с низкоймассой тела (≤60 кг). Более выраженный клиническийэффект без увеличения риска кровотечений наблюдал-ся у пациентов с диабетом. У пациентов с нарушениемфункции почек (клиренс креатинина≤60 мл/мин) и нор-мальной функцией почек (клиренс креатинина>60мл/мин) эффективность препарата не отличалась.Нежелательные эффекты прасугрела. Частота дру-гих нежелательных явлений в исследовании TRITONбыла сопоставимой в группах прасугрела и клопидо-грела. Тромбоцитопения встречалась в двух группах содинаковой частотой (0,3%), в то время как нейтропе-ния реже развивалась в группе прасугрела (<0,1% и0,2%; p=0,02).5.2.2.3. ТикагрелорТикагрелор принадлежит к новому химическомуклассу (циклопентилтриазолопиримидины) и являет-ся пероральным обратимым ингибитором P2Y12рецепторов с периодом полувыведения из плазмыоколо 12 ч. Степень блокады P2Y12 рецепторов зави-сит от уровня тикагрелора в плазме и в меньшей сте-пени его метаболита. Как и прасугрел, он оказывает бо-лее быстрое и постоянное действие, чем клопидо-грел. Кроме того, его действие прекращается быстрее, поэтому функция тромбоцитов также восстанавлива-ется в более короткие сроки (табл. 8) [131]. Тикагре-лор увеличивает уровни препаратов, которые метабо-лизируются под действием CYP3A, таких как симваста-тин, в то время как умеренные ингибиторы CYP3A, та-кие как дилтиазем, увеличивают уровни и снижают ско-рость прекращения действия тикагрелора.
Таблица 8. Блокаторы P2Y12 рецепторов
 В исследовании PLATO рандомизировали пациен-тов с ОКС без подъема сегмента ST среднего или высо-кого риска (которым планировалось консервативное илиинвазивное лечение) или ИМ с подъемом сегмента ST(которым планировалось первичное ЧКВ). Пациентамназначали клопидогрел в нагрузочной дозе 300 мг, азатем по 75 мг/сут или тикагрелор в нагрузочной дозе180 мг, а затем 90 мг два раза в день [132]. При выпол-нении ЧКВ пациентам разрешалось ввести дополнитель-но нагрузочную дозу клопидогрела 300 мг (суммарнаянагрузочная доза 600 мг) или плацебо и рекомендо-валось ввести дополнительно 90 мг тикагрелора (илисоответствующего плацебо), если ЧКВ выполняли бо-лее чем через 24 ч после приема первой нагрузочнойдозы. Лечение продолжали в течение 12 мес (мини-мальная длительность составляла 6 мес, а медиана —9 мес) [132]. В целом в исследование были включены11 067 пациентов с ИМ без подъема сегмента ST илинестабильной стенокардией. Пациентов с ОКС в иссле-дование включали в течение 24 ч после появления симп-томов при наличии по крайней мере двух из следую-щих критериев: повышение биомаркеров некрозамиокарда; ишемические изменения сегмента ST; повы-шенный риск (возраст ≥60 лет, ИМ или КШ в анамне-зе, стеноз по крайней мере двух коронарных артерий≥50%, цереброваскулярная болезнь, сахарный диабет,заболевание периферических сосудов или хроническаядисфункция почек). Во всей когорте частота комбини-рованной первичной конечной точки снизилась с11,7% в группе клопидогрела до 9,8% в группе тика-грелора (ОШ 0,84; 95% ДИ 0,77–0,92; p<0,001).Смертность от сосудистых причин снизилась с 5,1% до4,0% (ОШ 0,79; 95% ДИ 0,69–0,91; p=0,001), а ча-стота ИМ — с 6,9% до 5,8% (ОШ 0,84; 95% ДИ0,75–0,95; p=0,005). Смертность от инсульта досто-верно не отличалась (1,3% и 1,5%; p=0,22). Частотаопределенного тромбоза стента снизилась с 1,9% до1,3% (p<0,01), а общая смертность — с 5,9% до4,5% (p<0,001).Частота больших кровотечений, которые диагности-ровали в соответствии с критериями PLATO, достовер-но не отличалась между группами клопидогрела и ти-кагрелора (11,2% и 11,6%, соответственно; p=0,43).Частота больших кровотечений, не связанных с КШ, уве-личилась с 3,8% в группе клопидогрела до 4,5% в груп-пе тикагрелора (ОШ 1,19; 95% ДИ 1,02–1,38; p=0,03).Частота больших кровотечений, связанных с КШ, быласопоставимой в группах тикагрелора и клопидогрела(7,4% и 7,9%, соответственно; p=0,32). Небольшиекровотечения в группе тикагрелора развивались чаще,чем в группе клопидогрела. Смертность от кровотече-ний в целом не отличалась между группами (0,3%), не-смотря на более высокую частоту фатальных внутриче-репных кровотечений в группе тикагрелора. У пациен-тов с положительным исходным тропонином частотапервичной конечной точки значительно снизилась вгруппе тикагрелора (10,3% и 12,3%; ОШ 0,85; 95%ДИ 0,77–0,94), в отличие от пациентов с нормальнымуровнем тропонина (7,0% и 7,0%). Значительноеснижение риска первичной конечной точки выявили так-же у пациентов с окончательным диагнозом ИМ безподъема сегмента ST (11,4% и 13,9%; ОШ 0,83;95% ДИ 0,73–0,94), в отличие от пациентов с оконча-тельным диагнозом нестабильной стенокардии (8,6%и 9,1%, соответственно; ОШ 0,96; 95% ДИ 0,75–1,22).Хотя снижение частоты тромбоза стента при лечении ти-кагрелором было отмечено в ранние сроки [133],благоприятный эффект на риск ИМ и смерти продол-жал нарастать в течение 12 мес [132].Тикагрелор снижал раннюю и позднюю смертностьпосле КШ. У 1 261 пациента, перенесшего КШ и полу-чавшего исследуемый препарат в течение <7 дн до опе-рации, частота комбинированной первичной конечнойточки составила 10,6% в группе тикагрелора и 13,1%в группе клопидогрела (ОШ 0,84; 95% ДИ 0,60–1,16;p=0,29). Общая смертность при лечении тикагрелоромснизилась с 9,7% до 4,7% (ОШ 0,49; ДИ 0,32–0,77;p<0,01), сердечно-сосудистая смертность — с 7,9% до4,1% (ОШ 0,52; 95% ДИ 0,32–0,85; p<0,01), смерт-ность от других причин — с 2,0% до 0,7% (p=0,07). Ча-стота больших кровотечений, связанных с КШ, досто-верно не отличалась между двумя группами. В соответствии с протоколом, лечение тикагрелором возобнов-ляли, когда его применение считалось безопасным с точ-ки зрения кровотечений (см. ниже) [134].Нежелательные эффекты тикагрелора. Помимо уве-личения частоты небольших и не связанных с КШбольших кровотечений нежелательные эффекты тика-грелора включали в себя одышку, увеличение частотыжелудочковых пауз и бессимптомной гиперурикемии[132,135,136]. Одышка, вызванная тикагрелором,чаще всего (до 15%) развивается в течение первой не-дели после начала лечения и может быть преходящейили сохраняется до прекращения лечения, однако онаобычно не требует прекращения лечения [132,137].Одышка, по-видимому, не связана с ухудшением функ-ции сердца или легких [137]. Желудочковые паузы приприменении тикагрелора в основном представляют со-бой бессимптомные эпизоды ночной синоатриаль-ной блокады. Рекомендуется соблюдать осторожностьу пациентов с выраженной синоатриальной блокадойили атриовентрикулярной блокадой II-III степени, еслипациенту не установлен постоянный водитель ритма. Ме-ханизмы развития одышки и желудочковых пауз не уста-новлены [137]. В исследовании PLATO в группе тика-грелора было выявлено несколько более выраженноеувеличение сывороточного уровня креатинина, од-нако разница между группами отсутствовала через 1 меспосле прекращения лечения [132]. Частота желудочно-кишечных расстройств и сыпи была сходной в двух груп-пах [136].5.2.2.4. Отмена блокаторов P2Y12 рецепторовперед операциейУ пациентов с ОКС без подъема сегмента ST двой-ную антитромбоцитарную терапию следует начинатьрано, так как польза перевешивает риск во всех случаях.Высказывалось предположение, что тиенопиридины сле-дует на время отменить перед ангиографией, учитываявозможную необходимость в КШ. В нескольких иссле-дованиях было отмечено увеличение риска большихкровотечений у пациентов, получавших клопидогрелперед КШ. В исследовании CURE медиана времени доКШ составила 26 дн; в среднем операцию проводиличерез 12 дн после госпитализации [113]. Решение оботмене препарата принимали лечащие врачи. Эф-фективность клопидогрела в профилактике ишемиче-ских исходов по сравнению с плацебо была отмеченаперед операцией (ОР 0,82; 95% ДИ 0,58–1,16) и от-сутствовала после нее (ОР 0,97; 95% ДИ 0,75–1,26).Частота больших кровотечений была выше в группе кло-пидогрела (ОР 1,27; 95% ДИ 0,96–1,69), однакоона снижалась в случае отмены клопидогрела за 5 дндо КШ. В последующих наблюдательных исследованияхбыло выявлено значительное увеличение частоты ге-мотрансфузий и повторных операций, но не смертно-сти в тех случаях, когда клопидогрел применяли в тече-ние 5 дн до КШ [138-140]. В исследовании ACUITY1 539 пациентов перенесли КШ, а 50,9% из них полу-чали клопидогрел до операции. У последних пациен-тов отмечалось увеличение длительности госпитализа-ции (12,0 и 8,9 дня, соответственно; p=0,0001), но сни-жение частоты ишемических осложнений (смерть,ИМ или внеплановая реваскуляризация) через 30 дн(12,7% и 17,3%; p<0,01), которое не сопровождалосьувеличением частоты больших кровотечений, не свя-занных с КШ (3,4% и 3,2%; p=0,87), или больших кро-вотечений после КШ (50,3% и 50,9%; p=0,83) посравнению с пациентами, не получавшими клопидогрелперед КШ. Прием клопидогрела перед операциейбыл независимым предиктором снижения частотыишемических исходов, но не влиял на риск кровотече-ний [141]. Причиной увеличения частоты кровотечениймогут быть не только сроки применения клопидогре-ла перед КШ, но и другие факторы. У 4 974 пациентов,которым проводилось плановое и внеплановое КШ, не-зависимыми предикторами кровотечений (повторноевмешательство по поводу кровотечения, трансфузияэритроцитарной массы или снижение гематокрита бо-лее чем на 15%) были исходный гематокрит(p<0,0001), искусственное кровообращение(p<0,0001), опыт сосудистого хирурга, выполнявше-го КШ (p=0,02), женский пол (p<0,0001), понижен-ный клиренс креатинина (p=0,0002), стенокардия(p=0,0003), введение блокаторов GP IIb/IIIa рецепто-ров перед КШ (p=0,0004) и число суженных сосудов(p=0,002) [142]. Лечение клопидогрелом в течение 5дн до операции не ассоциировалось с более высокимриском кровотечения после внесения поправки надругие факторы риска (ОР 1,23; 95% ДИ 0,52–2,10;p=0,45).Отменять клопидогрел у пациентов высокого рис-ка, например, с сохраняющейся ишемией миокарда всочетании со стенозом ствола левой коронарной арте-рии и тяжелым проксимальным стенозом несколькихартерий, не рекомендуется. Таким пациентам следуетпроводить КШ на фоне лечения клопидогрелом, одна-ко необходимо уделять особое внимание мерам, на-правленным на профилактику кровотечения [143].Если риск кровотечения очень высокий, например, приповторном КШ или сложном КШ в сочетании с опера-цией на клапане, оправдан перерыв в лечении клопи-догрелом на 3-5 дн перед операцией даже у пациен-тов с активной ишемией миокарда (см. ниже).В исследовании PLATO лечение клопидогрелом и ти-кагрелором рекомендовали на время прекратить за 5и 1-3 дн, соответственно, до КШ. У пациентов, получав-ших исследуемые препараты в течение 7 дн до КШ, ча-стота больших кровотечений, связанных с операцией,и гемотрансфузий, достоверно не отличалась между группами клопидогрела и тикагрелора [134]. Хотя ча-стота нефатального ИМ и инсульта в двух группахбыла сопоставимой в этой когорте, смертность была в2 раза ниже в группе тикагрелора (4,7% и 9,7%; ОШ0,49; 95% ДИ 0,32–0,77; p<0,01); в основном разни-ца была достигнута в ранние сроки после КШ. 36% па-циентов каждой группы возобновили лечение тикагре-лором или клопидогрелом в течение 7 дн после опе-рации, 26-27% — более чем через 7 дней и 37-38%— больше не принимали препарат [134]. Оптимальныесроки возобновления антитромботической терапиипосле КШ не установлены.5.2.2.5. Прекращение двойной антитромбоцитарнойтерапииОтмена антитромбоцитарных препаратов можетпривести к увеличению частоты рецидивирующихосложнений [112,144]. Прекращение двойной анти-тромбоцитарной терапии вскоре после имплантациистента повышает риск подострого его тромбоза, которыйхарактеризуется неблагоприятным прогнозом; смертностьчерез 1 мес достигает 15-45%. Временное прекраще-ние двойной антитромбоцитарной терапии перед хи-рургическим вмешательством более чем через 1 меспосле ОКС обоснованно у пациентов без стента, выде-ляющего лекарства. Если необходим перерыв в двой-ной антитромбоцитарной терапии, например, в случаенеотложного хирургического вмешательства (например,нейрохирургического) или развития большого крово-течения, которое не удается контролировать местнымисредствами, эффективных альтернативных методовлечения не существует. Обсуждалась возможность при-менения низкомолекулярных гепаринов (НМГ), одна-ко их эффективность не доказана [145].
Рекомендации по применению пероральных антитромбоцитарных препаратов
В исследовании PLATO рандомизировали пациен-тов с ОКС без подъема сегмента ST среднего или высо-кого риска (которым планировалось консервативное илиинвазивное лечение) или ИМ с подъемом сегмента ST(которым планировалось первичное ЧКВ). Пациентамназначали клопидогрел в нагрузочной дозе 300 мг, азатем по 75 мг/сут или тикагрелор в нагрузочной дозе180 мг, а затем 90 мг два раза в день [132]. При выпол-нении ЧКВ пациентам разрешалось ввести дополнитель-но нагрузочную дозу клопидогрела 300 мг (суммарнаянагрузочная доза 600 мг) или плацебо и рекомендо-валось ввести дополнительно 90 мг тикагрелора (илисоответствующего плацебо), если ЧКВ выполняли бо-лее чем через 24 ч после приема первой нагрузочнойдозы. Лечение продолжали в течение 12 мес (мини-мальная длительность составляла 6 мес, а медиана —9 мес) [132]. В целом в исследование были включены11 067 пациентов с ИМ без подъема сегмента ST илинестабильной стенокардией. Пациентов с ОКС в иссле-дование включали в течение 24 ч после появления симп-томов при наличии по крайней мере двух из следую-щих критериев: повышение биомаркеров некрозамиокарда; ишемические изменения сегмента ST; повы-шенный риск (возраст ≥60 лет, ИМ или КШ в анамне-зе, стеноз по крайней мере двух коронарных артерий≥50%, цереброваскулярная болезнь, сахарный диабет,заболевание периферических сосудов или хроническаядисфункция почек). Во всей когорте частота комбини-рованной первичной конечной точки снизилась с11,7% в группе клопидогрела до 9,8% в группе тика-грелора (ОШ 0,84; 95% ДИ 0,77–0,92; p<0,001).Смертность от сосудистых причин снизилась с 5,1% до4,0% (ОШ 0,79; 95% ДИ 0,69–0,91; p=0,001), а ча-стота ИМ — с 6,9% до 5,8% (ОШ 0,84; 95% ДИ0,75–0,95; p=0,005). Смертность от инсульта досто-верно не отличалась (1,3% и 1,5%; p=0,22). Частотаопределенного тромбоза стента снизилась с 1,9% до1,3% (p<0,01), а общая смертность — с 5,9% до4,5% (p<0,001).Частота больших кровотечений, которые диагности-ровали в соответствии с критериями PLATO, достовер-но не отличалась между группами клопидогрела и ти-кагрелора (11,2% и 11,6%, соответственно; p=0,43).Частота больших кровотечений, не связанных с КШ, уве-личилась с 3,8% в группе клопидогрела до 4,5% в груп-пе тикагрелора (ОШ 1,19; 95% ДИ 1,02–1,38; p=0,03).Частота больших кровотечений, связанных с КШ, быласопоставимой в группах тикагрелора и клопидогрела(7,4% и 7,9%, соответственно; p=0,32). Небольшиекровотечения в группе тикагрелора развивались чаще,чем в группе клопидогрела. Смертность от кровотече-ний в целом не отличалась между группами (0,3%), не-смотря на более высокую частоту фатальных внутриче-репных кровотечений в группе тикагрелора. У пациен-тов с положительным исходным тропонином частотапервичной конечной точки значительно снизилась вгруппе тикагрелора (10,3% и 12,3%; ОШ 0,85; 95%ДИ 0,77–0,94), в отличие от пациентов с нормальнымуровнем тропонина (7,0% и 7,0%). Значительноеснижение риска первичной конечной точки выявили так-же у пациентов с окончательным диагнозом ИМ безподъема сегмента ST (11,4% и 13,9%; ОШ 0,83;95% ДИ 0,73–0,94), в отличие от пациентов с оконча-тельным диагнозом нестабильной стенокардии (8,6%и 9,1%, соответственно; ОШ 0,96; 95% ДИ 0,75–1,22).Хотя снижение частоты тромбоза стента при лечении ти-кагрелором было отмечено в ранние сроки [133],благоприятный эффект на риск ИМ и смерти продол-жал нарастать в течение 12 мес [132].Тикагрелор снижал раннюю и позднюю смертностьпосле КШ. У 1 261 пациента, перенесшего КШ и полу-чавшего исследуемый препарат в течение <7 дн до опе-рации, частота комбинированной первичной конечнойточки составила 10,6% в группе тикагрелора и 13,1%в группе клопидогрела (ОШ 0,84; 95% ДИ 0,60–1,16;p=0,29). Общая смертность при лечении тикагрелоромснизилась с 9,7% до 4,7% (ОШ 0,49; ДИ 0,32–0,77;p<0,01), сердечно-сосудистая смертность — с 7,9% до4,1% (ОШ 0,52; 95% ДИ 0,32–0,85; p<0,01), смерт-ность от других причин — с 2,0% до 0,7% (p=0,07). Ча-стота больших кровотечений, связанных с КШ, досто-верно не отличалась между двумя группами. В соответствии с протоколом, лечение тикагрелором возобнов-ляли, когда его применение считалось безопасным с точ-ки зрения кровотечений (см. ниже) [134].Нежелательные эффекты тикагрелора. Помимо уве-личения частоты небольших и не связанных с КШбольших кровотечений нежелательные эффекты тика-грелора включали в себя одышку, увеличение частотыжелудочковых пауз и бессимптомной гиперурикемии[132,135,136]. Одышка, вызванная тикагрелором,чаще всего (до 15%) развивается в течение первой не-дели после начала лечения и может быть преходящейили сохраняется до прекращения лечения, однако онаобычно не требует прекращения лечения [132,137].Одышка, по-видимому, не связана с ухудшением функ-ции сердца или легких [137]. Желудочковые паузы приприменении тикагрелора в основном представляют со-бой бессимптомные эпизоды ночной синоатриаль-ной блокады. Рекомендуется соблюдать осторожностьу пациентов с выраженной синоатриальной блокадойили атриовентрикулярной блокадой II-III степени, еслипациенту не установлен постоянный водитель ритма. Ме-ханизмы развития одышки и желудочковых пауз не уста-новлены [137]. В исследовании PLATO в группе тика-грелора было выявлено несколько более выраженноеувеличение сывороточного уровня креатинина, од-нако разница между группами отсутствовала через 1 меспосле прекращения лечения [132]. Частота желудочно-кишечных расстройств и сыпи была сходной в двух груп-пах [136].5.2.2.4. Отмена блокаторов P2Y12 рецепторовперед операциейУ пациентов с ОКС без подъема сегмента ST двой-ную антитромбоцитарную терапию следует начинатьрано, так как польза перевешивает риск во всех случаях.Высказывалось предположение, что тиенопиридины сле-дует на время отменить перед ангиографией, учитываявозможную необходимость в КШ. В нескольких иссле-дованиях было отмечено увеличение риска большихкровотечений у пациентов, получавших клопидогрелперед КШ. В исследовании CURE медиана времени доКШ составила 26 дн; в среднем операцию проводиличерез 12 дн после госпитализации [113]. Решение оботмене препарата принимали лечащие врачи. Эф-фективность клопидогрела в профилактике ишемиче-ских исходов по сравнению с плацебо была отмеченаперед операцией (ОР 0,82; 95% ДИ 0,58–1,16) и от-сутствовала после нее (ОР 0,97; 95% ДИ 0,75–1,26).Частота больших кровотечений была выше в группе кло-пидогрела (ОР 1,27; 95% ДИ 0,96–1,69), однакоона снижалась в случае отмены клопидогрела за 5 дндо КШ. В последующих наблюдательных исследованияхбыло выявлено значительное увеличение частоты ге-мотрансфузий и повторных операций, но не смертно-сти в тех случаях, когда клопидогрел применяли в тече-ние 5 дн до КШ [138-140]. В исследовании ACUITY1 539 пациентов перенесли КШ, а 50,9% из них полу-чали клопидогрел до операции. У последних пациен-тов отмечалось увеличение длительности госпитализа-ции (12,0 и 8,9 дня, соответственно; p=0,0001), но сни-жение частоты ишемических осложнений (смерть,ИМ или внеплановая реваскуляризация) через 30 дн(12,7% и 17,3%; p<0,01), которое не сопровождалосьувеличением частоты больших кровотечений, не свя-занных с КШ (3,4% и 3,2%; p=0,87), или больших кро-вотечений после КШ (50,3% и 50,9%; p=0,83) посравнению с пациентами, не получавшими клопидогрелперед КШ. Прием клопидогрела перед операциейбыл независимым предиктором снижения частотыишемических исходов, но не влиял на риск кровотече-ний [141]. Причиной увеличения частоты кровотечениймогут быть не только сроки применения клопидогре-ла перед КШ, но и другие факторы. У 4 974 пациентов,которым проводилось плановое и внеплановое КШ, не-зависимыми предикторами кровотечений (повторноевмешательство по поводу кровотечения, трансфузияэритроцитарной массы или снижение гематокрита бо-лее чем на 15%) были исходный гематокрит(p<0,0001), искусственное кровообращение(p<0,0001), опыт сосудистого хирурга, выполнявше-го КШ (p=0,02), женский пол (p<0,0001), понижен-ный клиренс креатинина (p=0,0002), стенокардия(p=0,0003), введение блокаторов GP IIb/IIIa рецепто-ров перед КШ (p=0,0004) и число суженных сосудов(p=0,002) [142]. Лечение клопидогрелом в течение 5дн до операции не ассоциировалось с более высокимриском кровотечения после внесения поправки надругие факторы риска (ОР 1,23; 95% ДИ 0,52–2,10;p=0,45).Отменять клопидогрел у пациентов высокого рис-ка, например, с сохраняющейся ишемией миокарда всочетании со стенозом ствола левой коронарной арте-рии и тяжелым проксимальным стенозом несколькихартерий, не рекомендуется. Таким пациентам следуетпроводить КШ на фоне лечения клопидогрелом, одна-ко необходимо уделять особое внимание мерам, на-правленным на профилактику кровотечения [143].Если риск кровотечения очень высокий, например, приповторном КШ или сложном КШ в сочетании с опера-цией на клапане, оправдан перерыв в лечении клопи-догрелом на 3-5 дн перед операцией даже у пациен-тов с активной ишемией миокарда (см. ниже).В исследовании PLATO лечение клопидогрелом и ти-кагрелором рекомендовали на время прекратить за 5и 1-3 дн, соответственно, до КШ. У пациентов, получав-ших исследуемые препараты в течение 7 дн до КШ, ча-стота больших кровотечений, связанных с операцией,и гемотрансфузий, достоверно не отличалась между группами клопидогрела и тикагрелора [134]. Хотя ча-стота нефатального ИМ и инсульта в двух группахбыла сопоставимой в этой когорте, смертность была в2 раза ниже в группе тикагрелора (4,7% и 9,7%; ОШ0,49; 95% ДИ 0,32–0,77; p<0,01); в основном разни-ца была достигнута в ранние сроки после КШ. 36% па-циентов каждой группы возобновили лечение тикагре-лором или клопидогрелом в течение 7 дн после опе-рации, 26-27% — более чем через 7 дней и 37-38%— больше не принимали препарат [134]. Оптимальныесроки возобновления антитромботической терапиипосле КШ не установлены.5.2.2.5. Прекращение двойной антитромбоцитарнойтерапииОтмена антитромбоцитарных препаратов можетпривести к увеличению частоты рецидивирующихосложнений [112,144]. Прекращение двойной анти-тромбоцитарной терапии вскоре после имплантациистента повышает риск подострого его тромбоза, которыйхарактеризуется неблагоприятным прогнозом; смертностьчерез 1 мес достигает 15-45%. Временное прекраще-ние двойной антитромбоцитарной терапии перед хи-рургическим вмешательством более чем через 1 меспосле ОКС обоснованно у пациентов без стента, выде-ляющего лекарства. Если необходим перерыв в двой-ной антитромбоцитарной терапии, например, в случаенеотложного хирургического вмешательства (например,нейрохирургического) или развития большого крово-течения, которое не удается контролировать местнымисредствами, эффективных альтернативных методовлечения не существует. Обсуждалась возможность при-менения низкомолекулярных гепаринов (НМГ), одна-ко их эффективность не доказана [145].
Рекомендации по применению пероральных антитромбоцитарных препаратов
 В инструкциях по применению всех трех ингибито-ров P2Y12 рецепторов указано, что их следует отменитьза 7 дн до операции. Однако тактика ведения пациен-тов, которых направляют на хирургическое вмеша-тельство на фоне двойной антитромбоцитарной тера-пии, зависит от степени неотложности операции, атакже индивидуального риска тромбообразования и кро-вотечения. Большинство хирургических вмешательствмогут выполнены на фоне двойной антитромбоцитар-ной терапии или по крайней мере монотерапии ацетил-салициловой кислотой; при этом риск кровотечений счи-тают приемлемым. Для оценки риска и выбора оптималь-ной стратегии необходим мультидисциплинарный под-ход (кардиолог, анестезиолог, гематолог и хирург).У пациентов с ОКС без подъема сегмента ST необхо-димо взвешивать риск кровотечений во время опера-ции и повторных ишемических осложнений, связанныхс прекращением антитромбоцитарной терапии. Приэтом следует учитывать характер операции, риск ише-мических исходов и тяжесть ИБС, срок, прошедшийпосле ОКС или ЧКВ (если оно было выполнено), нали-чие стента, выделяющего лекарства, и риск тромбозастента. При хирургических операциях, сопровождаю-щихся низким или средним риском кровотечения, це-лесообразно продолжать двойную антитромбоцитар-ную терапию. Если приемлемо умеренное подавлениеP2Y12 во время вмешательств, например при выполне-нии КШ в ранние сроки после ОКС, то препаратыможно отменить незадолго до операции. В таких слу-чаях целесообразно прекратить прием клопидогрелаза 5 дн до хирургического вмешательства или позднее,если валидированный метод оценки функции тромбо-цитов подтверждает низкий ответ на клопидогрел.Прасугрел отменяют за 7 дн до операции, а тикагрелор— за 5 дн. Если прекращение антитромбоцитарной те-рапии перед операцией сопровождается высокимриском (например, в первые недели после импланта-ции стента), некоторые авторы рекомендовали на-значить обратимый антитромбоцитарный препарат с ко-ротким периодом полувыведения, например, ингиби-торы GP IIb/IIIa рецепторов тирофибан или эптифиба-тид, однако эффективность такого подхода пока не до-казана. Двойную антитромбоцитарную терапию следу-ет возобновить, когда она представляется безопасной.
Блокаторы гликопротеиновых IIb/IIIa рецепторов
Три блокатора GP IIb/IIIa рецепторов предназначе-ны для внутривенного введения и принадлежат к раз-личным классам: абциксимаб — фрагмент моноклональ-ных антител, эптифибатид — циклический пептид, ти-рофибан — пептидомиметик. При мета-анализе 29 570пациентов, которым планировалось ЧКВ после первич-ного консервативного ведения, было выявлено сниже-ние относительного риска смерти или нефатального ИМпри лечении блокаторами GP IIb/IIIa рецепторов на 9%(10,7% и 11,5%; p=0,02) [149]. У пациентов, получав-ших только консервативное лечение, риск смерти илиИМ при применении блокаторов GP IIb/IIIa рецепторовне отличался от такового в группе плацебо. Лечение эти-ми препаратами было эффективным только во времяЧКВ (10,5% и 13,6%; ОШ 0,74; 95% ДИ 0,57–0,96;p=0,02). Применение блокаторов GP IIb/IIIa рецепто-ров сопровождалось увеличением частоты больших кро-вотечений, но не внутричерепных кровотечений. Пер-вые исследования этих препаратов проводились в тотпериод, когда отсутствовали клопидогрел или новыеблокаторы P2Y12 рецепторов.«Upstream» терапия или выборочное применениеблокаторов GP IIb/IIIa рецепторов при ЧКВВ исследовании ACUITY Timing сравнивали резуль-таты выборочного (только во время ЧКВ) и рутинногоприменения блокаторов GP IIb/IIIa рецепторов до вме-шательства (upstream) у 9 207 пациентов [150]. Впервой группе блокаторы GP IIb/IIIa рецепторов при-меняли у 55,7% пациентов в течение 13,1 ч, а во вто-рой группе — у 98,3% пациентов в течение 18,4 ч. В це-лом 64% пациентов получали тиенопиридины передангиографией или ЧКВ. Частота больших кровотечений,не связанных с КШ, в течение 30 дн была ниже на фоневыборочного применения блокаторов GP IIb/IIIa рецеп-торов (4,9% и 6,1%; ОР 0,80; 95% ДИ 0,67–0,95;p=0,009), в то время как частота ишемических исхо-дов достоверно не отличалась между двумя группами(7,9% и 7,1%; ОР 1,12; 95% ДИ 0,97–1,29; p=0,13).Суммарная частота ишемических исходов и большихкровотечений (чистый клинический эффект) через 30дн была сходной (11,7% и 11,7%; ОР 1,00; 95% ДИ0,89–1,11; p=0,93; значение р для сопоставимости<0,001).В исследовании EARLY-ACS были рандомизирова-ны 9 492 пациентов, которым планировалось инвазив-ное лечение. Пациентам вводили эптифибатид или пла-цебо в ранние сроки; кроме того, допускалось введе-ние эптифибатида после ангиографии перед ЧКВ[151]. Первичным критерием эффективности была сум-марная частота смерти, ИМ, неотложной реваскуляри-зации по поводу рецидивирующей ишемии или ост-рой или угрожающей тромботической окклюзии сосу-да через 96 ч. Среди 5 559 пациентов группы плаце-бо 38% получили эптифибатид после ангиографии.При раннем и отложенном введении эптифибатида ча-стота первичной конечной точки достоверно не отлича-лась (9,3% и 10,0%; ОШ 0,92; 95% ДИ 0,80–1,06;p=0,23). Частота вторичной конечной точки (смертьот любой причины или развитие ИМ в течение 30 дн)также была сопоставимой (11,2% и 12,3%; ОШ 0,89;95% ДИ 0,89–1,01; p=0,08). Частота той же конечной точки на фоне консервативного ведения (доЧКВ или КШ или в течение 30 дн у всех пациентов, ко-торые получали только медикаментозное лечение) так-же была сопоставимой (4,3% в группе эптифибатидаи 4,2% в группе плацебо). Это свидетельствует о том,что введение эптифибатида не приносит пользы паци-ентам, которым проводится консервативное лечение.Частота больших кровотечений на фоне раннего вве-дения эптифибатида была выше, чем при отложенномвведении препарата (частота больших кровотеченийпо критериям TIMI через 120 ч составила 2,6% и 1,8%,соответственно; ОР 1,42; 95% ДИ 1,97–1,89;p=0,015). Таким образом, это исследование не под-твердило преимуществ раннего (upstream) примене-ния эптифибатида перед современной стандартной так-тикой ведения, когда у части пациентов, которымпроводили ЧКВ, эптифибатид вводили в более позд-ние сроки.Во всех исследованиях отмечалось увеличение ча-стоты кровотечений на фоне раннего применения бло-каторов GP IIb/IIIa рецепторов. В связи с этим их не сле-дует вводить до ангиографии. При оценке целесообраз-ности введения блокаторов GP IIb/IIIa рецепторов передЧКВ следует учитывать результаты ангиографии (нали-чие тромба и распространенность атеросклероза), по-вышение уровня тропонина, предыдущую терапиюингибиторами P2Y12 рецепторов, возраст и другиефакторы, оказывающие влияние на риск серьезных кро-вотечений [2,152]. «Upstream» терапия блокаторамиGP IIb/IIIa рецепторов может быть обоснованной при со-хранении ишемии у пациентов группы высокого рискаили невозможности двойной антитромбоцитарной те-рапии. Пациентам, которым вводили эптифибатид илитирофибан перед ангиографией, следует продолжатьлечение тем же препаратом во время и после ЧКВ.ТромбоцитопенияПри применении всех трех зарегистрированныхблокаторов GP IIb/IIIa рецепторов может развиться тром-боцитопения (см. раздел 5.5.10.). Частота остройтромбоцитопении в клинических исследованиях парен-теральных блокаторов GP IIb/IIIa рецепторов составля-ла от 0,5 до 5,6% и была сопоставимой с таковой привведении одного нефракционированного гепарина(НФГ) [153,154]. Через 5-11 дн возможно развитиепоздней тромбоцитопении. Оба типа тромбоцитопениимогут быть следствием образования антител [155]. Прилечении абциксимабом частота тяжелой тромбоцито-пении была более чем в 2 раза выше, чем в группе пла-цебо. Риск ее ниже при введении эптифибатида (0,2%в исследовании PURSUIT) [156] и тирофибана. В иссле-довании TARGET развитие тромбоцитопении наблюда-ли у 2,4% пациентов группы абциксимаба и 0,5% —группы тирофибана (p<0,001) [157].Сравнительная эффективность блокаторовGP IIb/IIIa рецепторовАбциксимаб сравнивали с тирофибаном в исследо-вании TARGET, в котором у 2/3 пациентов имелсяОКС без подъема сегмента ST [158]. Абциксимаб пре-восходил тирофибан в стандартных дозах по эффектив-ности в профилактике смерти, ИМ и неотложной ревас-куляризации в течение 30 дн, однако через 6 мес раз-ница была недостоверной [159]. Дополнительные ис-следования, в которых тирофибан применяли в болеевысоких дозах в различных ситуациях, результатымета-анализа показали, что тирофибан в высокойдозе (25 мг/кг в виде болюса, а затем инфузия) по эф-фективности сопоставим с абциксимабом [160,161].Сравнительные исследования эптифибатида не прово-дились.Комбинация блокаторов GP IIb/IIIa рецепторовс аспирином и ингибиторами P2Y12Данные о пользе присоединения блокатораGP IIb/IIIa рецепторов к комбинированной терапии аспи-рином и блокатором P2Y12 рецепторов при ОКС безподъема сегмента ST ограниченны. В исследованииISAR-REACT-2 были рандомизированы 2 022 пациен-та высокого риска с ОКС без подъема сегмента ST, ко-торым после приема аспирина и клопидогрела в дозе600 мг вводили абциксимаб или плацебо во время ЧКВ.Доля пациентов с сахарным диабетом в двух группахбыла сопоставимой (в среднем 26,5%); у 52% боль-ных был повышен уровень тропонина, а у 24,1%имелся ИМ в анамнезе. Суммарная частота смерти, ИМили неотложной реваскуляризации целевого сосуда втечение 30 дн в группе абциксимаба была значитель-но ниже, чем в группе плацебо (8,9% и 11,9%; ОР 0,75;95% ДИ 0,58–0,97; p=0,03). Снижение риска про-изошло в основном за счет уменьшения риска смертии нефатального ИМ. Эффект препарата был болеевыраженным в некоторых подгруппах пациентов, в част-ности с повышенным уровнем тропонина (13,1% и18,3%; отношение рисков 0,71; 95% ДИ 0,54–0,95;p=0,02). Длительность терапии клопидогрелом передвведением блокатора GP IIb/IIIa рецепторов не оказы-вала влияния на исходы. У пациентов с нормальнымуровнем тропонина и сахарным диабетом лечениеабциксимабом оказалось неэффективным. Однакочисло пациентов с диабетом в этом исследованиибыло недостаточным для статистического анализа эф-фективности терапии.В исследованиях TRITON и PLATO частота примене-ния блокаторов GP IIb/IIIa рецепторов составила 55%и 27%, соответственно. У пациентов, получавших этипрепараты в исследовании TRITON, была выше часто-та больших и небольших кровотечений (по крите-риям TIMI), не связанных с КШ, однако применение блокаторов GP IIb/IIIa рецепторов не влияло на относитель-ный риск кровотечений, который сравнивали в группахпрасугрела и клопидогрела (значение Р для взаимодей-ствия 0,19) [162]. Лечение прасугрелом привело к сни-жению риска смерти, ИМ или инсульта по сравнениюс клопидогрелом как на фоне применения блокаторовGP IIb/IIIa рецепторов (6,5% и 8,5%; отношение рис-ков 0,76; 95% ДИ 0,64–0,90), так и без лечения эти-ми препаратами (4,8% и 6,1%; отношение рисков 0,78;95% ДИ 0,63–0,97). В исследовании PLATO тикагре-лор также снизил риск смерти, ИМ или инсульта посравнению с клопидогрелом у пациентов, получавших(10,0% и 11,1%; отношение рисков 0,90; 95% ДИ0,76–1,07) и не получавших (9,7% и 11,9%; отноше-ние рисков 0,82; 95% ДИ 0,74–0,92) блокатор GPIIb/IIIa рецепторов [132]. В целом применение блока-тора GP IIb/IIIa рецепторов в сочетании с аспирином иблокатором P2Y12 рецепторов оправданно при ЧКВ упациентов с ОКС без подъема сегмента, если риск раз-вития ИМ высокий, а риск кровотечений низкий.Блокаторы GP IIb/IIIa рецепторови антикоагулянтыВ большинстве исследований, показавших эффек-тивность блокаторов GP IIb/IIIa рецепторов, применя-лись антикоагулянты. В нескольких исследованиях у па-циентов с ОКС без подъема сегмента ST, а также в на-блюдательных исследованиях у пациентов, перенесшихЧКВ, было установлено, что НМГ, прежде всего энокса-парин, можно безопасно применять в сочетании сблокаторами GP IIb/IIIa рецепторов, хотя подкожное вве-дение эноксапарина не обеспечивает адекватную про-филактику катетерного тромбоза при первичном ЧКВ[163]. В исследовании OASIS-5 блокаторы GP IIb/IIIa ре-цепторов применяли в сочетании с аспирином и кло-пидогрелом, а также фондапаринуксом (n=1308) илиэноксапарином (n=1273) [164]. В целом частота кро-вотечений при лечении фондапаринуксом была ниже,чем при применении эноксапарина (см. раздел 5.3.).Бивалирудин и НФГ/НМГ характеризовались одинако-выми безопасностью и эффективностью в комбинациис аспирином, клопидогрелом и блокатором GP IIb/IIIaрецепторов в исследовании ACUITY [165]. Комбиниро-ванная терапия бивалирудином и блокаторомGP IIb/IIIa рецепторов привела к сходному снижениючастоты ишемических осложнений по сравнению содним бивалирудином, но сопровождалась более вы-сокой частотой больших кровотечений [166]. Эти дан-ные не позволяют рекомендовать широкое применениеданной комбинации.Выбор дозы блокаторов GP IIb/IIIa рецепторовЭффективность и безопасность блокаторовGP IIb/IIIa рецепторов в обычной клинической практи-ке изучалась в нескольких регистрах. Была отмечена вы-сокая частота больших кровотечений, которые были ча-стично связаны с назначением больших доз [167,168].Причинами передозировки были пожилой возраст, жен-ский пол, почечная недостаточность, низкая массатела, сахарный диабет и застойная сердечная недоста-точность. У пациентов, получавших слишком высокиедозы блокаторов GP IIb/IIIa рецепторов, скорректиро-ванная частота больших кровотечений была на 30%выше таковой при применении адекватных доз. Такимобразом, частота геморрагических осложнений в кли-нических исследований может быть заниженной посравнению с таковой в клинической практике, когда бло-каторы GP IIb/IIIa рецепторов применяют у пациентов,у которых чаще встречаются сопутствующие заболева-ния.Блокаторы GP IIb/IIIa рецепторови коронарное шунтированиеПри выполнении КШ у пациентов, получающихблокаторы GP IIb/IIIa рецепторов, необходимо обеспе-чить адекватный гемостаз и отменить блокаторGP IIb/IIIa рецепторов перед операцией или, если не-возможно, во время вмешательства. Эптифибатид и ти-рофибан обладают коротким периодом полувыведе-ния (около 2 ч), поэтому функция тромбоцитов при об-ратимом связывании рецепторов может восстановить-ся в конце КШ. Абциксимаб имеет короткий период по-лувыведения (10 мин), однако он медленно высвобож-дается из комплекса с рецептором с периодом полувы-ведения около 4 ч, поэтому восстановление нормаль-ной или близкой к норме агрегации тромбоцитовпроисходит в течение 48 ч после завершения инфузии(хотя абциксимаб, связанный с рецепторами, можетопределяться в течение более длительного времени).В случае значительного кровотечения возможна транс-фузия тромбоцитарной массы (см. раздел 5.5.9.). Длякупирования больших кровотечений при введениитирофибана и эптифибатида возможно применениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с тромбоци-тарной массой [169].
Антикоагулянты
Антикоагулянты применяют у пациентов с ОКС безподъема сегмента ST для ингибирования образованияи/или активности тромбина и для профилактики тром-бообразования. Установлена эффективность антикоа-гулянтов в сочетании с блокаторами функции тромбо-цитов, а комбинированная терапия была более эффек-тивной, чем монотерапия обоими средствами [171,172].У пациентов с ОКС без подъема сегмента ST изучалисьили изучаются несколько антикоагулянтов, действующихна различных уровнях каскада свертывания крови:
Рекомендации по применению блокаторов GP IIb/IIIa рецепторов
В инструкциях по применению всех трех ингибито-ров P2Y12 рецепторов указано, что их следует отменитьза 7 дн до операции. Однако тактика ведения пациен-тов, которых направляют на хирургическое вмеша-тельство на фоне двойной антитромбоцитарной тера-пии, зависит от степени неотложности операции, атакже индивидуального риска тромбообразования и кро-вотечения. Большинство хирургических вмешательствмогут выполнены на фоне двойной антитромбоцитар-ной терапии или по крайней мере монотерапии ацетил-салициловой кислотой; при этом риск кровотечений счи-тают приемлемым. Для оценки риска и выбора оптималь-ной стратегии необходим мультидисциплинарный под-ход (кардиолог, анестезиолог, гематолог и хирург).У пациентов с ОКС без подъема сегмента ST необхо-димо взвешивать риск кровотечений во время опера-ции и повторных ишемических осложнений, связанныхс прекращением антитромбоцитарной терапии. Приэтом следует учитывать характер операции, риск ише-мических исходов и тяжесть ИБС, срок, прошедшийпосле ОКС или ЧКВ (если оно было выполнено), нали-чие стента, выделяющего лекарства, и риск тромбозастента. При хирургических операциях, сопровождаю-щихся низким или средним риском кровотечения, це-лесообразно продолжать двойную антитромбоцитар-ную терапию. Если приемлемо умеренное подавлениеP2Y12 во время вмешательств, например при выполне-нии КШ в ранние сроки после ОКС, то препаратыможно отменить незадолго до операции. В таких слу-чаях целесообразно прекратить прием клопидогрелаза 5 дн до хирургического вмешательства или позднее,если валидированный метод оценки функции тромбо-цитов подтверждает низкий ответ на клопидогрел.Прасугрел отменяют за 7 дн до операции, а тикагрелор— за 5 дн. Если прекращение антитромбоцитарной те-рапии перед операцией сопровождается высокимриском (например, в первые недели после импланта-ции стента), некоторые авторы рекомендовали на-значить обратимый антитромбоцитарный препарат с ко-ротким периодом полувыведения, например, ингиби-торы GP IIb/IIIa рецепторов тирофибан или эптифиба-тид, однако эффективность такого подхода пока не до-казана. Двойную антитромбоцитарную терапию следу-ет возобновить, когда она представляется безопасной.
Блокаторы гликопротеиновых IIb/IIIa рецепторов
Три блокатора GP IIb/IIIa рецепторов предназначе-ны для внутривенного введения и принадлежат к раз-личным классам: абциксимаб — фрагмент моноклональ-ных антител, эптифибатид — циклический пептид, ти-рофибан — пептидомиметик. При мета-анализе 29 570пациентов, которым планировалось ЧКВ после первич-ного консервативного ведения, было выявлено сниже-ние относительного риска смерти или нефатального ИМпри лечении блокаторами GP IIb/IIIa рецепторов на 9%(10,7% и 11,5%; p=0,02) [149]. У пациентов, получав-ших только консервативное лечение, риск смерти илиИМ при применении блокаторов GP IIb/IIIa рецепторовне отличался от такового в группе плацебо. Лечение эти-ми препаратами было эффективным только во времяЧКВ (10,5% и 13,6%; ОШ 0,74; 95% ДИ 0,57–0,96;p=0,02). Применение блокаторов GP IIb/IIIa рецепто-ров сопровождалось увеличением частоты больших кро-вотечений, но не внутричерепных кровотечений. Пер-вые исследования этих препаратов проводились в тотпериод, когда отсутствовали клопидогрел или новыеблокаторы P2Y12 рецепторов.«Upstream» терапия или выборочное применениеблокаторов GP IIb/IIIa рецепторов при ЧКВВ исследовании ACUITY Timing сравнивали резуль-таты выборочного (только во время ЧКВ) и рутинногоприменения блокаторов GP IIb/IIIa рецепторов до вме-шательства (upstream) у 9 207 пациентов [150]. Впервой группе блокаторы GP IIb/IIIa рецепторов при-меняли у 55,7% пациентов в течение 13,1 ч, а во вто-рой группе — у 98,3% пациентов в течение 18,4 ч. В це-лом 64% пациентов получали тиенопиридины передангиографией или ЧКВ. Частота больших кровотечений,не связанных с КШ, в течение 30 дн была ниже на фоневыборочного применения блокаторов GP IIb/IIIa рецеп-торов (4,9% и 6,1%; ОР 0,80; 95% ДИ 0,67–0,95;p=0,009), в то время как частота ишемических исхо-дов достоверно не отличалась между двумя группами(7,9% и 7,1%; ОР 1,12; 95% ДИ 0,97–1,29; p=0,13).Суммарная частота ишемических исходов и большихкровотечений (чистый клинический эффект) через 30дн была сходной (11,7% и 11,7%; ОР 1,00; 95% ДИ0,89–1,11; p=0,93; значение р для сопоставимости<0,001).В исследовании EARLY-ACS были рандомизирова-ны 9 492 пациентов, которым планировалось инвазив-ное лечение. Пациентам вводили эптифибатид или пла-цебо в ранние сроки; кроме того, допускалось введе-ние эптифибатида после ангиографии перед ЧКВ[151]. Первичным критерием эффективности была сум-марная частота смерти, ИМ, неотложной реваскуляри-зации по поводу рецидивирующей ишемии или ост-рой или угрожающей тромботической окклюзии сосу-да через 96 ч. Среди 5 559 пациентов группы плаце-бо 38% получили эптифибатид после ангиографии.При раннем и отложенном введении эптифибатида ча-стота первичной конечной точки достоверно не отлича-лась (9,3% и 10,0%; ОШ 0,92; 95% ДИ 0,80–1,06;p=0,23). Частота вторичной конечной точки (смертьот любой причины или развитие ИМ в течение 30 дн)также была сопоставимой (11,2% и 12,3%; ОШ 0,89;95% ДИ 0,89–1,01; p=0,08). Частота той же конечной точки на фоне консервативного ведения (доЧКВ или КШ или в течение 30 дн у всех пациентов, ко-торые получали только медикаментозное лечение) так-же была сопоставимой (4,3% в группе эптифибатидаи 4,2% в группе плацебо). Это свидетельствует о том,что введение эптифибатида не приносит пользы паци-ентам, которым проводится консервативное лечение.Частота больших кровотечений на фоне раннего вве-дения эптифибатида была выше, чем при отложенномвведении препарата (частота больших кровотеченийпо критериям TIMI через 120 ч составила 2,6% и 1,8%,соответственно; ОР 1,42; 95% ДИ 1,97–1,89;p=0,015). Таким образом, это исследование не под-твердило преимуществ раннего (upstream) примене-ния эптифибатида перед современной стандартной так-тикой ведения, когда у части пациентов, которымпроводили ЧКВ, эптифибатид вводили в более позд-ние сроки.Во всех исследованиях отмечалось увеличение ча-стоты кровотечений на фоне раннего применения бло-каторов GP IIb/IIIa рецепторов. В связи с этим их не сле-дует вводить до ангиографии. При оценке целесообраз-ности введения блокаторов GP IIb/IIIa рецепторов передЧКВ следует учитывать результаты ангиографии (нали-чие тромба и распространенность атеросклероза), по-вышение уровня тропонина, предыдущую терапиюингибиторами P2Y12 рецепторов, возраст и другиефакторы, оказывающие влияние на риск серьезных кро-вотечений [2,152]. «Upstream» терапия блокаторамиGP IIb/IIIa рецепторов может быть обоснованной при со-хранении ишемии у пациентов группы высокого рискаили невозможности двойной антитромбоцитарной те-рапии. Пациентам, которым вводили эптифибатид илитирофибан перед ангиографией, следует продолжатьлечение тем же препаратом во время и после ЧКВ.ТромбоцитопенияПри применении всех трех зарегистрированныхблокаторов GP IIb/IIIa рецепторов может развиться тром-боцитопения (см. раздел 5.5.10.). Частота остройтромбоцитопении в клинических исследованиях парен-теральных блокаторов GP IIb/IIIa рецепторов составля-ла от 0,5 до 5,6% и была сопоставимой с таковой привведении одного нефракционированного гепарина(НФГ) [153,154]. Через 5-11 дн возможно развитиепоздней тромбоцитопении. Оба типа тромбоцитопениимогут быть следствием образования антител [155]. Прилечении абциксимабом частота тяжелой тромбоцито-пении была более чем в 2 раза выше, чем в группе пла-цебо. Риск ее ниже при введении эптифибатида (0,2%в исследовании PURSUIT) [156] и тирофибана. В иссле-довании TARGET развитие тромбоцитопении наблюда-ли у 2,4% пациентов группы абциксимаба и 0,5% —группы тирофибана (p<0,001) [157].Сравнительная эффективность блокаторовGP IIb/IIIa рецепторовАбциксимаб сравнивали с тирофибаном в исследо-вании TARGET, в котором у 2/3 пациентов имелсяОКС без подъема сегмента ST [158]. Абциксимаб пре-восходил тирофибан в стандартных дозах по эффектив-ности в профилактике смерти, ИМ и неотложной ревас-куляризации в течение 30 дн, однако через 6 мес раз-ница была недостоверной [159]. Дополнительные ис-следования, в которых тирофибан применяли в болеевысоких дозах в различных ситуациях, результатымета-анализа показали, что тирофибан в высокойдозе (25 мг/кг в виде болюса, а затем инфузия) по эф-фективности сопоставим с абциксимабом [160,161].Сравнительные исследования эптифибатида не прово-дились.Комбинация блокаторов GP IIb/IIIa рецепторовс аспирином и ингибиторами P2Y12Данные о пользе присоединения блокатораGP IIb/IIIa рецепторов к комбинированной терапии аспи-рином и блокатором P2Y12 рецепторов при ОКС безподъема сегмента ST ограниченны. В исследованииISAR-REACT-2 были рандомизированы 2 022 пациен-та высокого риска с ОКС без подъема сегмента ST, ко-торым после приема аспирина и клопидогрела в дозе600 мг вводили абциксимаб или плацебо во время ЧКВ.Доля пациентов с сахарным диабетом в двух группахбыла сопоставимой (в среднем 26,5%); у 52% боль-ных был повышен уровень тропонина, а у 24,1%имелся ИМ в анамнезе. Суммарная частота смерти, ИМили неотложной реваскуляризации целевого сосуда втечение 30 дн в группе абциксимаба была значитель-но ниже, чем в группе плацебо (8,9% и 11,9%; ОР 0,75;95% ДИ 0,58–0,97; p=0,03). Снижение риска про-изошло в основном за счет уменьшения риска смертии нефатального ИМ. Эффект препарата был болеевыраженным в некоторых подгруппах пациентов, в част-ности с повышенным уровнем тропонина (13,1% и18,3%; отношение рисков 0,71; 95% ДИ 0,54–0,95;p=0,02). Длительность терапии клопидогрелом передвведением блокатора GP IIb/IIIa рецепторов не оказы-вала влияния на исходы. У пациентов с нормальнымуровнем тропонина и сахарным диабетом лечениеабциксимабом оказалось неэффективным. Однакочисло пациентов с диабетом в этом исследованиибыло недостаточным для статистического анализа эф-фективности терапии.В исследованиях TRITON и PLATO частота примене-ния блокаторов GP IIb/IIIa рецепторов составила 55%и 27%, соответственно. У пациентов, получавших этипрепараты в исследовании TRITON, была выше часто-та больших и небольших кровотечений (по крите-риям TIMI), не связанных с КШ, однако применение блокаторов GP IIb/IIIa рецепторов не влияло на относитель-ный риск кровотечений, который сравнивали в группахпрасугрела и клопидогрела (значение Р для взаимодей-ствия 0,19) [162]. Лечение прасугрелом привело к сни-жению риска смерти, ИМ или инсульта по сравнениюс клопидогрелом как на фоне применения блокаторовGP IIb/IIIa рецепторов (6,5% и 8,5%; отношение рис-ков 0,76; 95% ДИ 0,64–0,90), так и без лечения эти-ми препаратами (4,8% и 6,1%; отношение рисков 0,78;95% ДИ 0,63–0,97). В исследовании PLATO тикагре-лор также снизил риск смерти, ИМ или инсульта посравнению с клопидогрелом у пациентов, получавших(10,0% и 11,1%; отношение рисков 0,90; 95% ДИ0,76–1,07) и не получавших (9,7% и 11,9%; отноше-ние рисков 0,82; 95% ДИ 0,74–0,92) блокатор GPIIb/IIIa рецепторов [132]. В целом применение блока-тора GP IIb/IIIa рецепторов в сочетании с аспирином иблокатором P2Y12 рецепторов оправданно при ЧКВ упациентов с ОКС без подъема сегмента, если риск раз-вития ИМ высокий, а риск кровотечений низкий.Блокаторы GP IIb/IIIa рецепторови антикоагулянтыВ большинстве исследований, показавших эффек-тивность блокаторов GP IIb/IIIa рецепторов, применя-лись антикоагулянты. В нескольких исследованиях у па-циентов с ОКС без подъема сегмента ST, а также в на-блюдательных исследованиях у пациентов, перенесшихЧКВ, было установлено, что НМГ, прежде всего энокса-парин, можно безопасно применять в сочетании сблокаторами GP IIb/IIIa рецепторов, хотя подкожное вве-дение эноксапарина не обеспечивает адекватную про-филактику катетерного тромбоза при первичном ЧКВ[163]. В исследовании OASIS-5 блокаторы GP IIb/IIIa ре-цепторов применяли в сочетании с аспирином и кло-пидогрелом, а также фондапаринуксом (n=1308) илиэноксапарином (n=1273) [164]. В целом частота кро-вотечений при лечении фондапаринуксом была ниже,чем при применении эноксапарина (см. раздел 5.3.).Бивалирудин и НФГ/НМГ характеризовались одинако-выми безопасностью и эффективностью в комбинациис аспирином, клопидогрелом и блокатором GP IIb/IIIaрецепторов в исследовании ACUITY [165]. Комбиниро-ванная терапия бивалирудином и блокаторомGP IIb/IIIa рецепторов привела к сходному снижениючастоты ишемических осложнений по сравнению содним бивалирудином, но сопровождалась более вы-сокой частотой больших кровотечений [166]. Эти дан-ные не позволяют рекомендовать широкое применениеданной комбинации.Выбор дозы блокаторов GP IIb/IIIa рецепторовЭффективность и безопасность блокаторовGP IIb/IIIa рецепторов в обычной клинической практи-ке изучалась в нескольких регистрах. Была отмечена вы-сокая частота больших кровотечений, которые были ча-стично связаны с назначением больших доз [167,168].Причинами передозировки были пожилой возраст, жен-ский пол, почечная недостаточность, низкая массатела, сахарный диабет и застойная сердечная недоста-точность. У пациентов, получавших слишком высокиедозы блокаторов GP IIb/IIIa рецепторов, скорректиро-ванная частота больших кровотечений была на 30%выше таковой при применении адекватных доз. Такимобразом, частота геморрагических осложнений в кли-нических исследований может быть заниженной посравнению с таковой в клинической практике, когда бло-каторы GP IIb/IIIa рецепторов применяют у пациентов,у которых чаще встречаются сопутствующие заболева-ния.Блокаторы GP IIb/IIIa рецепторови коронарное шунтированиеПри выполнении КШ у пациентов, получающихблокаторы GP IIb/IIIa рецепторов, необходимо обеспе-чить адекватный гемостаз и отменить блокаторGP IIb/IIIa рецепторов перед операцией или, если не-возможно, во время вмешательства. Эптифибатид и ти-рофибан обладают коротким периодом полувыведе-ния (около 2 ч), поэтому функция тромбоцитов при об-ратимом связывании рецепторов может восстановить-ся в конце КШ. Абциксимаб имеет короткий период по-лувыведения (10 мин), однако он медленно высвобож-дается из комплекса с рецептором с периодом полувы-ведения около 4 ч, поэтому восстановление нормаль-ной или близкой к норме агрегации тромбоцитовпроисходит в течение 48 ч после завершения инфузии(хотя абциксимаб, связанный с рецепторами, можетопределяться в течение более длительного времени).В случае значительного кровотечения возможна транс-фузия тромбоцитарной массы (см. раздел 5.5.9.). Длякупирования больших кровотечений при введениитирофибана и эптифибатида возможно применениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с тромбоци-тарной массой [169].
Антикоагулянты
Антикоагулянты применяют у пациентов с ОКС безподъема сегмента ST для ингибирования образованияи/или активности тромбина и для профилактики тром-бообразования. Установлена эффективность антикоа-гулянтов в сочетании с блокаторами функции тромбо-цитов, а комбинированная терапия была более эффек-тивной, чем монотерапия обоими средствами [171,172].У пациентов с ОКС без подъема сегмента ST изучалисьили изучаются несколько антикоагулянтов, действующихна различных уровнях каскада свертывания крови:
Рекомендации по применению блокаторов GP IIb/IIIa рецепторов
 Непрямые ингибиторы свертывания (для реализа-ции эффекта необходим антитромбин):Непрямые ингибиторы тромбина: НФГ НМГ. Непрямые ингибиторы Xa фактора: НМГ Фондапаринукс. Прямые ингибиторы свертывания. Прямые ингибиторы Ха фактора: апиксабан, ривароксабан, отамиксабан. Прямые ингибиторы тромбина: бивалирудин, дабигатран. Механизмы действия антикоагулянтов см. на рис. 3.Более подробную информацию можно найти в опуликованных обзорах [171].
Непрямые ингибиторы каскада коагуляции
Фондапаринукс. Единственным селективным ингибитором активиро-ванного фактора Х (фактора Ха) является фондапари-нукс — синтетический пентасахарид, который по строе-нию сходен с участком гепарина, связывающим анти-тромбин. Он ингибирует фактор Ха вследствие обрати-мого, высокоаффинного и неконвалентного связыванияс антитромбином. Фондапаринукс катализирует опосре-дованное антитромбином ингибирование фактора Хаи предупреждает образование тромбина. Препаратувеличивает способность к ингибированию фактора Хав 300 раз. Ингибирование 1 единицы фактора Ха по-давляет образование 50 единиц тромбина.Биодоступность фондапаринукса при подкожномвведении составляет 100%, а период полувыведения— 17 ч, поэтому его можно назначать один раз в день.Препарат выводится почками и противопоказан паци-ентам с клиренсом креатинина менее 20 мл/мин.Фондапаринукс не чувствителен к инактивирующемудействию белков, выделяющихся тромбоцитами инейтрализующих гепарин. При применении фондапа-ринукса не были описаны подтвержденные случаитромбоцитопении, индуцированной гепарином, дажепри широком его применении для профилактики и лече-ния венозных тромбоэмболических осложнений. Всвязи с этим мониторирование числа тромбоцитов нетребуется. При лечении фондапаринуксом нет не-обходимости в подборе дозы и контроле анти-Ха ак-тивности. Фондапаринукс не оказывает существенно-го влияния на стандартные показатели антикоагуляции,такие как активированное частичное тромбопластино-вое время (аЧТВ), активированное время свертывания(АВС), уровень протромбина и тромбиновое время.При ОКС фондапаринукс рекомендуется применятьв фиксированной дозе 2,5 мг/сут. Эта доза была вы-брана на основании результатов исследования PENTUA(дозо-определяющем исследовании фондапаринукса)и изучалась в двух крупных исследованиях III фазы(OASIS-5 и OASIS-6) [173–175]. В исследованииPENTUA доза 2,5 мг по эффективности и безопасностибыла по крайней мере сопоставима с более высокимидозами. Фондапаринукс применяли также в дозах2,5 и 5 мг внутривенно при плановых и неотложных ЧКВ.По эффективности и безопасности две дозы достовер-но не отличались друг от друга и от контроля (НФГ)[176]; однако в исследование были включены только350 пациентов, поэтому оно не обладало необходимойстатистической силой. Частота острой окклюзии сосу-да и тромбоза, выявленного при ангиографии, в двухгруппах фондапаринукса была несколько выше, чем вгруппе НФГ (фондапаринукс 2,5 мг — 2,5% и 5,1%,соответственно, фондапаринукс 5,0 мг — 0% и 4,3%,НФГ — 0,9% и 0,9%) [176].В исследовании OASIS-5 были рандомизированы20 078 пациентов с ОКС без подъема сегмента ST, ко-торым вводили фондапаринукс в дозе 2,5 мг один разв день подкожно или эноксапарин в дозе 1 мг/кг два раза в день подкожно в течение максимум 8 дн (в сред-нем 5,2 и 5,4 дн, соответственно) [175]. Частота пер-вичной конечной точки (смерть, ИМ или рефрактернаяишемия) через 9 дн составила 5,7% в группе энокса-парина и 5,8% в группе фондапаринукса (отноше-ние рисков 1,01; 95% ДИ 0,90–1,13), что подтвержда-ло сопоставимость эффектов двух препаратов. В то жевремя частота больших кровотечений была в 2 раза нижев группе фондапаринукса: 2,2% и 4,1%, соответ-ственно (отношение рисков 0,52; 95% ДИ 0,44–0,61;p<0,001). Большие кровотечения были независимымпредиктором смертности в отдаленном периоде, кото-рая значительно снизилась в группе фондапаринуксачерез 30 дн (2,9% и 3,5%; отношение рисков 0,83; 95%ДИ 0,71–0,97; p=0,02) и 6 мес (5,8% и 6,5%; отно-шение рисков 0,89; 95% ДИ 0,80–1,00; p=0,05). Че-рез 6 мес суммарная частота смерти, ИМ или инсуль-та в группе фондапаринукса была значительно ниже,чем в группе эноксапарина (11,3% и 12,5%; отноше-ние рисков 0,89; 95% ДИ 0,82–0,97; p=0,007). В вы-борке пациентов, которым проводили ЧКВ, частота боль-ших кровотечений (в том числе в области сосудистогодоступа) через 9 дн была значительно ниже в группефондапаринукса (2,4% и 5,1%; отношение рисков 0,46;95% ДИ 0,35–0,61; p<0,001). Интересно, что срок вме-шательства после введения последней дозы фондапа-ринукса не влиял на частоту больших кровотечений(1,6% и 1,3% — <6 ч и >6 ч, соответственно). Тромбозкатетера в группе фондапаринукса встречался чаще(0,9%), чем в группе эноксапарина (0,4%), однако егоудавалось ликвидировать путем введения эмпириче-ски подобранной болюсной дозы НФГ во время ЧКВ.Учитывая сопоставимую частоту ишемических исходовв группах фондапаринукса и гепарина через 9 дн, почистому клиническому эффекту (суммарной частотесмерти, ИМ, инсульта и больших кровотечений) фон-дапаринукс имел преимущества перед эноксапарином(8,2% и 10,4%; отношение рисков 0,78; 95% ДИ0,67–0,93; p=0,004).Предложено механистическое объяснение разницымежду фондапаринуксом и эноксапарином [177].Фондапаринукс в дозе 2,5 мг/сут по антикоагулянтнойактивности (анти-Ха активности) примерно в два разауступает эноксапарину в стандартной дозе. Степень ин-гибирования образования тромбина при примене-нии фондапаринукса также в два раза ниже. Это сви-детельствует о том, что низкий уровень антикоагуляциидостаточен для профилактики повторных ишемическихисходов в острую фазу ОКС без подъема сегмента ST упациентов, получающих полноценную антитромбо-цитарную терапию, в том числе аспирином и клопидо-грелом, а также блокатором GP IIb/IIIa рецепторов, учи-тывая отсутствие разницы частоты первичной конечнойточки через 9 дн между группами фондапаринукса иэноксапарина в исследовании OASIS-5 [175]. Низкийуровень антикоагуляции объясняет значительное сни-жение риска кровотечений. Однако подобная антикоа-гуляция недостаточна для профилактики тромбоза катетера во время ЧКВ. Это указывает на необходимостьвведения дополнительного болюса НФГ во время ЧКВу пациентов, получавших фондапаринукс.Оптимальная доза НФГ, которую следует вводить ввиде болюса во время ЧКВ пациентам, получающимфондапаринукс, изучалась в исследовании FUTURA/OASIS-8 [178]. В этом исследовании 2 026 пациентам,получавшим фондапаринукс и направленным на ЧКВв течение 72 ч после начала терапии, вводили НФГ ввиде болюса в низкой дозе (50 МЕ/кг) независимо отдозы блокатора GP IIb/IIIa рецепторов (если он приме-нялся) или в стандартной дозе 85 МЕ/кг (снижали до60 ЕД/кг в случае введения блокатора GP IIb/IIIa рецеп-торов), которую подбирали под контролем АВС. ЧКВбыло выполнено вскоре после введения последней дозыфондапаринукса (4 ч). Частота комбинированной пер-вичной конечной точки (большое кровотечение, неболь-шое кровотечение или большие кровотечения в обла-сти сосудистого доступа) через 48 ч после ЧКВ досто-верно не отличалась между двумя группами (4,7% и5,8%, соответственно; ОШ 0,80; 95% ДИ 0,54–1,19;p=0,27). Частота больших кровотечений была сходнойв двух группах (1,4% и 1,2%, соответственно) и сопо-ставимой с таковой у пациентов, направленных на ЧКВв группе фондапаринукса в исследовании OASIS-5(1,5% через 48 ч; те же критерии оценки кровотечений).Частота небольших кровотечений была ниже при вве-дении гепарина в низкой дозе (0,7% и 1,7%; ОШ 0,40;95% ДИ 0,16–0,97; p=0,04). По чистому клиническо-му эффекту (большое кровотечение через 48 ч или ре-васкуляризация целевого сосуда через 30 дн) преиму-щество имел гепарин в стандартной дозе (5,8% и3,9% — низкая и стандартная дозы, соответственно; ОШ1,51; 95% ДИ 1,00–2,28; p=0,05). Частота вторичнойконечной точки, включавшей в себя смерть, ИМ или ре-васкуляризацию целевого сосуда, также была ниже привведении гепарина в стандартной дозе (4,5% и 2,9%— низкая и стандартная дозы, соответственно; ОШ1,58; 95% ДИ 0,98–2,53; p=0,06). Тромбоз катетеравстречался редко (0,5% — низкая доза, 0,1% — стан-дартная доза; p=0,15). Полученные данные свидетель-ствуют о том, что пациентам, получавшим фондапари-нукс, во время ЧКВ обычный гепарин следует вводитьв стандартной дозе с учетом более выраженного чисто-го клинического эффекта и пониженного риска тром-боза катетера.
Рис. 3. Мишени действия антитромботических препаратов. АТ — антитромбин, GP — гликопротеин
Непрямые ингибиторы свертывания (для реализа-ции эффекта необходим антитромбин):Непрямые ингибиторы тромбина: НФГ НМГ. Непрямые ингибиторы Xa фактора: НМГ Фондапаринукс. Прямые ингибиторы свертывания. Прямые ингибиторы Ха фактора: апиксабан, ривароксабан, отамиксабан. Прямые ингибиторы тромбина: бивалирудин, дабигатран. Механизмы действия антикоагулянтов см. на рис. 3.Более подробную информацию можно найти в опуликованных обзорах [171].
Непрямые ингибиторы каскада коагуляции
Фондапаринукс. Единственным селективным ингибитором активиро-ванного фактора Х (фактора Ха) является фондапари-нукс — синтетический пентасахарид, который по строе-нию сходен с участком гепарина, связывающим анти-тромбин. Он ингибирует фактор Ха вследствие обрати-мого, высокоаффинного и неконвалентного связыванияс антитромбином. Фондапаринукс катализирует опосре-дованное антитромбином ингибирование фактора Хаи предупреждает образование тромбина. Препаратувеличивает способность к ингибированию фактора Хав 300 раз. Ингибирование 1 единицы фактора Ха по-давляет образование 50 единиц тромбина.Биодоступность фондапаринукса при подкожномвведении составляет 100%, а период полувыведения— 17 ч, поэтому его можно назначать один раз в день.Препарат выводится почками и противопоказан паци-ентам с клиренсом креатинина менее 20 мл/мин.Фондапаринукс не чувствителен к инактивирующемудействию белков, выделяющихся тромбоцитами инейтрализующих гепарин. При применении фондапа-ринукса не были описаны подтвержденные случаитромбоцитопении, индуцированной гепарином, дажепри широком его применении для профилактики и лече-ния венозных тромбоэмболических осложнений. Всвязи с этим мониторирование числа тромбоцитов нетребуется. При лечении фондапаринуксом нет не-обходимости в подборе дозы и контроле анти-Ха ак-тивности. Фондапаринукс не оказывает существенно-го влияния на стандартные показатели антикоагуляции,такие как активированное частичное тромбопластино-вое время (аЧТВ), активированное время свертывания(АВС), уровень протромбина и тромбиновое время.При ОКС фондапаринукс рекомендуется применятьв фиксированной дозе 2,5 мг/сут. Эта доза была вы-брана на основании результатов исследования PENTUA(дозо-определяющем исследовании фондапаринукса)и изучалась в двух крупных исследованиях III фазы(OASIS-5 и OASIS-6) [173–175]. В исследованииPENTUA доза 2,5 мг по эффективности и безопасностибыла по крайней мере сопоставима с более высокимидозами. Фондапаринукс применяли также в дозах2,5 и 5 мг внутривенно при плановых и неотложных ЧКВ.По эффективности и безопасности две дозы достовер-но не отличались друг от друга и от контроля (НФГ)[176]; однако в исследование были включены только350 пациентов, поэтому оно не обладало необходимойстатистической силой. Частота острой окклюзии сосу-да и тромбоза, выявленного при ангиографии, в двухгруппах фондапаринукса была несколько выше, чем вгруппе НФГ (фондапаринукс 2,5 мг — 2,5% и 5,1%,соответственно, фондапаринукс 5,0 мг — 0% и 4,3%,НФГ — 0,9% и 0,9%) [176].В исследовании OASIS-5 были рандомизированы20 078 пациентов с ОКС без подъема сегмента ST, ко-торым вводили фондапаринукс в дозе 2,5 мг один разв день подкожно или эноксапарин в дозе 1 мг/кг два раза в день подкожно в течение максимум 8 дн (в сред-нем 5,2 и 5,4 дн, соответственно) [175]. Частота пер-вичной конечной точки (смерть, ИМ или рефрактернаяишемия) через 9 дн составила 5,7% в группе энокса-парина и 5,8% в группе фондапаринукса (отноше-ние рисков 1,01; 95% ДИ 0,90–1,13), что подтвержда-ло сопоставимость эффектов двух препаратов. В то жевремя частота больших кровотечений была в 2 раза нижев группе фондапаринукса: 2,2% и 4,1%, соответ-ственно (отношение рисков 0,52; 95% ДИ 0,44–0,61;p<0,001). Большие кровотечения были независимымпредиктором смертности в отдаленном периоде, кото-рая значительно снизилась в группе фондапаринуксачерез 30 дн (2,9% и 3,5%; отношение рисков 0,83; 95%ДИ 0,71–0,97; p=0,02) и 6 мес (5,8% и 6,5%; отно-шение рисков 0,89; 95% ДИ 0,80–1,00; p=0,05). Че-рез 6 мес суммарная частота смерти, ИМ или инсуль-та в группе фондапаринукса была значительно ниже,чем в группе эноксапарина (11,3% и 12,5%; отноше-ние рисков 0,89; 95% ДИ 0,82–0,97; p=0,007). В вы-борке пациентов, которым проводили ЧКВ, частота боль-ших кровотечений (в том числе в области сосудистогодоступа) через 9 дн была значительно ниже в группефондапаринукса (2,4% и 5,1%; отношение рисков 0,46;95% ДИ 0,35–0,61; p<0,001). Интересно, что срок вме-шательства после введения последней дозы фондапа-ринукса не влиял на частоту больших кровотечений(1,6% и 1,3% — <6 ч и >6 ч, соответственно). Тромбозкатетера в группе фондапаринукса встречался чаще(0,9%), чем в группе эноксапарина (0,4%), однако егоудавалось ликвидировать путем введения эмпириче-ски подобранной болюсной дозы НФГ во время ЧКВ.Учитывая сопоставимую частоту ишемических исходовв группах фондапаринукса и гепарина через 9 дн, почистому клиническому эффекту (суммарной частотесмерти, ИМ, инсульта и больших кровотечений) фон-дапаринукс имел преимущества перед эноксапарином(8,2% и 10,4%; отношение рисков 0,78; 95% ДИ0,67–0,93; p=0,004).Предложено механистическое объяснение разницымежду фондапаринуксом и эноксапарином [177].Фондапаринукс в дозе 2,5 мг/сут по антикоагулянтнойактивности (анти-Ха активности) примерно в два разауступает эноксапарину в стандартной дозе. Степень ин-гибирования образования тромбина при примене-нии фондапаринукса также в два раза ниже. Это сви-детельствует о том, что низкий уровень антикоагуляциидостаточен для профилактики повторных ишемическихисходов в острую фазу ОКС без подъема сегмента ST упациентов, получающих полноценную антитромбо-цитарную терапию, в том числе аспирином и клопидо-грелом, а также блокатором GP IIb/IIIa рецепторов, учи-тывая отсутствие разницы частоты первичной конечнойточки через 9 дн между группами фондапаринукса иэноксапарина в исследовании OASIS-5 [175]. Низкийуровень антикоагуляции объясняет значительное сни-жение риска кровотечений. Однако подобная антикоа-гуляция недостаточна для профилактики тромбоза катетера во время ЧКВ. Это указывает на необходимостьвведения дополнительного болюса НФГ во время ЧКВу пациентов, получавших фондапаринукс.Оптимальная доза НФГ, которую следует вводить ввиде болюса во время ЧКВ пациентам, получающимфондапаринукс, изучалась в исследовании FUTURA/OASIS-8 [178]. В этом исследовании 2 026 пациентам,получавшим фондапаринукс и направленным на ЧКВв течение 72 ч после начала терапии, вводили НФГ ввиде болюса в низкой дозе (50 МЕ/кг) независимо отдозы блокатора GP IIb/IIIa рецепторов (если он приме-нялся) или в стандартной дозе 85 МЕ/кг (снижали до60 ЕД/кг в случае введения блокатора GP IIb/IIIa рецеп-торов), которую подбирали под контролем АВС. ЧКВбыло выполнено вскоре после введения последней дозыфондапаринукса (4 ч). Частота комбинированной пер-вичной конечной точки (большое кровотечение, неболь-шое кровотечение или большие кровотечения в обла-сти сосудистого доступа) через 48 ч после ЧКВ досто-верно не отличалась между двумя группами (4,7% и5,8%, соответственно; ОШ 0,80; 95% ДИ 0,54–1,19;p=0,27). Частота больших кровотечений была сходнойв двух группах (1,4% и 1,2%, соответственно) и сопо-ставимой с таковой у пациентов, направленных на ЧКВв группе фондапаринукса в исследовании OASIS-5(1,5% через 48 ч; те же критерии оценки кровотечений).Частота небольших кровотечений была ниже при вве-дении гепарина в низкой дозе (0,7% и 1,7%; ОШ 0,40;95% ДИ 0,16–0,97; p=0,04). По чистому клиническо-му эффекту (большое кровотечение через 48 ч или ре-васкуляризация целевого сосуда через 30 дн) преиму-щество имел гепарин в стандартной дозе (5,8% и3,9% — низкая и стандартная дозы, соответственно; ОШ1,51; 95% ДИ 1,00–2,28; p=0,05). Частота вторичнойконечной точки, включавшей в себя смерть, ИМ или ре-васкуляризацию целевого сосуда, также была ниже привведении гепарина в стандартной дозе (4,5% и 2,9%— низкая и стандартная дозы, соответственно; ОШ1,58; 95% ДИ 0,98–2,53; p=0,06). Тромбоз катетеравстречался редко (0,5% — низкая доза, 0,1% — стан-дартная доза; p=0,15). Полученные данные свидетель-ствуют о том, что пациентам, получавшим фондапари-нукс, во время ЧКВ обычный гепарин следует вводитьв стандартной дозе с учетом более выраженного чисто-го клинического эффекта и пониженного риска тром-боза катетера.
Рис. 3. Мишени действия антитромботических препаратов. АТ — антитромбин, GP — гликопротеин
 Низкомолекулярные гепарины
НМГ — это производные гепарина с молекулярноймассой от 2000 до 10000 Да. Они характеризуются сба-лансированной анти-Ха и анти-IIa активностью, кото-рая зависит от молекулярной массы препарата. При уве-личении последней повышается анти-IIa активность.НМГ отличаются по фармакокинетическим и анти-коагулянтным свойствам и, соответственно, не яв-ляются взаимозаменяемыми. НМГ имеют несколько пре-имуществ перед НФГ, включая более полное всасыва-ние после подкожного введения, меньшее связываниес белками, менее выраженную активацию тромбоци-тов и более предсказуемую зависимость эффекта от дозы[171]. При лечении НМГ риск развития тромбоцитопе-нии, индуцированной гепарином, ниже, чем при лече-нии НФГ; НМГ, по крайней мере частично, выводятсяпочками. Риск накопления увеличивается при сниже-нии функции почек, которое сопровождается повыше-нием риска кровотечения. Большинство НМГ противо-показаны пациентам с почечной недостаточностью(клиренс креатинина ниже 30 мл/мин). Однако дозуэноксапарина у пациентов с клиренсом креатинина ме-нее 30 мл/мин можно снизить (1 мг/кг один раз в день,а не два раза в день).НМГ при ОКС без подъема сегмента ST назначают вподобранной по массе тела и обычно вводят подкож-но два раза в день, хотя у пациентов высокого рискалечение можно начинать с внутривенного введения бо-люса [179-182]. При применении НМГ в стандартныхдозах мониторирование анти-Ха активности не требу-ется за исключением особых ситуаций, например у па-циентов с почечной недостаточностью или ожирением.Оптимальный уровень анти-Ха активности, который дол-жен быть достигнут у пациентов с ОКС без подъема сег-мента ST, не установлен. У пациентов с венозной тром-боэмболией (ВТЭ) терапевтический диапазон состав-ляет 0,6-1,0 МЕ/мл. Четкая связь между анти-Ха актив-ностью и клиническими исходами не установлена.Однако риск кровотечений увеличивается, когда анти-Ха активность превышает 1,0 МЕ/мл [183]. В дозоопре-деляющем исследовании у пациентов с ОКС без подъе-ма сегмента ST эноксапарин изучали в дозах 1,25 и 1,0мг/кг два раза в день. Максимальная анти-Ха активностьв двух группах составляла 1,5 и 1,0 МЕ/мл, соответ-ственно. При применении эноксапарина в дозе 1,25мг/кг частота больших кровотечений в течение 14 днравнялась 6,5% (в основном в области сосудистого до-ступа). В группе эноксапарина 1,0 мг/кг частота боль-ших кровотечений снизилась до 1,9%. У пациентов сбольшими кровотечениями анти-Ха активность нахо-дилась в диапазоне 1,8-2,0 МЕ/мл [184]. В крупной ко-горте пациентов с нестабильной стенокардией/ИМбез подъема сегмента ST низкая анти-Ха активность(<0,5 МЕ/мл) при лечении эноксапарином ассоции-ровалась с трехкратным увеличением смертности у па-циентов с анти-Ха активностью в целевом диапазоне0,5-1,2 МЕ/мл. Низкие уровни анти-Ха (<0,05 МЕ/мл)были независимым предиктором смертности в течение30 дн. Это свидетельствует о том, что при лечении энок-сапарином уровень анти-Ха активности по возможно-сти должен составлять по крайней мере 0,5 МЕ/мл [185]. В неконтролируемых исследованиях и неболь-ших контролируемых исследованиях у пациентов, ко-торым проводились ЧКВ, анти-Ха активность >0,5МЕ/мл ассоциировалась с низкой частотой ишемиче-ских и геморрагических осложнений [186,187].Опубликованы результаты нескольких мета-анали-зов исследований, в которых сравнивали эффективностьНМГ и НФГ у пациентов с ОКС без подъема сегмента ST.В первый мета-анализ были включены 12 клиническихисследований различных препаратов в целом у 17 157пациентов с ОКС без подъема сегмента ST, получавшихаспирин. Гепарины достоверно превосходили плаце-бо по эффективности в профилактике смерти или ИМ(ОШ 0,53; 95% ДИ 0,38–0,73; p=0,0001). НМГ неимели преимуществ перед НФГ по эффективностиили безопасности [172]. При мета-анализе всех иссле-дований, в которых изучались эноксапарин и НФГ, в це-лом у 21 946 пациентов достоверной разницы смерт-ности через 30 дн не выявлено (3,0% и 3,0%, соответ-ственно; ОШ 1,00; 95% ДИ 0,85–1,17; p=незначимый).При лечении эноксапарином выявлено дополнитель-ное снижение риска смерти или ИМ в течение 30 дн посравнению с гепарином (10,1% и 11,0%; ОШ 0,91;95% ДИ 0,83–0,99). При анализе post-hoc в подгруп-пе пациентов, не получавших НФГ перед рандомиза-цией, выявлено значительное снижение смертности иличастоты ИМ в течение 30 дн при лечении эноксапари-ном по сравнению с НФГ (8,0% и 9,4%, соответ-ственно; ОШ 0,81; 95% ДИ 0,70–0,94). Достовернойразницы частоты гемотрансфузий (7,2% и 7,5%;ОШ 1,01; 95% ДИ 0,89–1,14) или больших кровотече-ний (4,7% и 4,5%; ОШ 1,04; 95% ДИ 0,83–1,30) че-рез 7 дн после рандомизации отмечено не было как вовсей выборке, так и в выборке пациентов, не получав-ших антикоагулянты перед рандомизацией. При допол-нительном мета-анализе, в который были включены всеисследования эноксапарина у пациентов с ОКС (как безподъема сегмента ST, так и с подъемом сегмента ST),были получены сходные результаты [188].И, наконец, в небольших исследованиях сравнива-ли эффективность и безопасность НМГ и НФГ в комби-нации с блокаторами GP IIb/IIIa рецепторов. По безопас-ности две схемы лечения не отличались. Ни в одном ис-следовании не было выявлено разницы риска «твердых»конечных точек, за исключением исследованияINTERACT, в котором имелась достоверная разница меж-ду группами эноксапарина/эптифибатида и НФГ/эп-тифибатида в пользу первой схемы [189-191]. Одна-ко все эти исследования не обладали необходимойстатистической силой, чтобы сделать окончательныевыводы.Большинство исследований проводились в то вре-мя, когда инвазивная стратегия еще не была внедренав широкую практику, а в некоторых исследованиях при-менение инвазивных методов вообще не рекомендо-валось. В результате инвазивное лечение проводилосьтолько у небольшой части пациентов, поэтому любыевыводы, сделанные на основании этих исследований,сегодня будут устаревшими.Единственным исследованием, в котором эноксапа-рин сравнивали с НФГ на фоне высокой частоты ЧКВ,реваскуляризации, стентирования и активной антитром-боцитарной терапии аспирином, клопидогрелом иблокаторами GP IIb/IIIa, было SYNERGY [192]. В это ис-следование были включены 10 027 пациентов высо-кого риска, которым проводили инвазивное обследо-вание и реваскуляризацию. 76% пациентов получалиантикоагулянты перед рандомизацией. Достовернойразницы частоты смерти и ИМ через 30 дн между груп-пами эноксапарина и НФГ не выявили (14,0% и14,5%, соответственно; ОШ 0,96; 95% ДИ 0,86–1,06;p=незначимый) [193]. Частота кровотечений былавыше в группе эноксапарина, в частности было отмече-но достоверное увеличение частоты больших кровотече-ний в соответствии с критериями TIMI (9,1% и 7,6%;p=0,008), но недостоверное увеличение частоты тяже-лых кровотечений в соответствии с критериямиGUSTO (2,7% и 2,2%; p=0,08) и гемотрансфузий(17,0% и 16,0%; p=0,16). Повышенная частота кро-вотечений, вероятно, отражала частое применениеантикоагулянтов перед рандомизацией и, возможно,частую смену антикоагулянта после рандомизации.Тем не менее, НМГ, особенно эноксапарин, часто при-меняют при ЧКВ, хотя мониторировать антикоагуляциюнелегко. Фармакокинетические/фармакодинамиче-ские свойства эноксапарина отличаются при подкожноми внутривенном применении. При плановом ЧКВ энок-сапарин вводят в дозе 1 мг/кг внутривенно. Внутривен-ные дозы, которые изучались в клинических исследова-ниях, были ниже (обычно 0,5 мг/кг) и обеспечивали туже максимальную анти-Ха активность в течение 3 мин[194]. Эноксапарин при внутривенном введении даетбыстрый и предсказуемый антикоагулянтный эффект втечение 2 ч. Более низкие дозы изучались также в иссле-довании STEEPLE [195]. У пациентов без ОКС частота кро-вотечений в группе эноксапарина в дозах 0,5 и 0,75 мг/кгбыла ниже, чем в группе НФГ. Однако исследование необладало статистической силой, необходимой для вы-явления различий между группами эноксапарина.У пациентов с ОКС без подъема сегмента ST, полу-чавших эноксапарин, не рекомендуется дополнитель-ное введение эноксапарина во время ЧКВ, если послед-няя подкожная инъекция препарата была выполненаменее чем за 8 ч до вмешательства. Если эноксапаринвводили более чем за 8 ч до ЧКВ, то рекомендуется до-полнительное введение 0,3 мг/кг внутривенно в видеболюса. Переход с одного антикоагулянта на другой вовремя ЧКВ не рекомендуется.
Нефракционированный гепарин
НФГ — это неоднородная смесь полисахаридов с мо-лекулярной массой от 2 000 до 30 000 Да (в основном15 000-18 000 Да). Одна треть молекул, входящих всостав НФГ, содержит пентасахарид, который связыва-ется с антитромбином и увеличивает скорость ингиби-рования фактора Ха. Для подавления фактора IIa необхо-димо взаимодействие гепарина с тромбином и анти-тромбином с образованием связи между ними. НФГплохо всасывается после подкожного введения, поэто-му его предпочтительно вводить внутривенно. Препа-рат обладает узким терапевтическим окном, в связи счем необходимо частое мониторирование аЧТВ. Целе-вой его уровень составляет 50-75 с (в 1,5-2,5 раза вышеверхней границы нормы). При более высоких значенияхаЧТВ увеличивается риск геморрагических осложнений,а дополнительный антитромботический эффект отсут-ствует. При аЧТВ менее 50 с антитромботическое дей-ствие ограниченно. НФГ рекомендуется назначать в дозе,подобранной по массе тела. Лечение начинают с вве-дения болюса 60-70 ед/кг (максимум 5 000 ед) с после-дующей инфузией по 12-15 ед/кг/ч (максимум1 000 ед/ч). Такая схема чаще всего обеспечивает до-стижение целевых значений аЧТВ [171]. Антикоагулянт-ный эффект НФГ быстро прекращается (в течение не-скольких часов после прекращения введения). В пер-вые 24 ч после прекращения терапии существует рискреактивации процесса свертывания и, соответственно,преходящего повышения риска рецидивирующих ише-мических осложнений, несмотря на одновременную те-рапию аспирином.При мета-анализе 6 исследований было показано,что кратковременное введение НФГ приводит к сниже-нию риска смерти или ИМ на 33% по сравнению с пла-цебо или отсутствием антикоагуляции (ОШ 0,67; 95%ДИ 0,45–0,99; p=0,04) [172]. Благоприятный эф-фект препарата был связан со снижением риска разви-тия ИМ. В клинических исследованиях, в которыхсравнивали комбинированную терапию НФГ+аспирини монотерапию аспирином у пациентов с ОКС безподъема сегмента ST, было отмечено небольшое пре-имущество комбинированной терапии, но ценой уве-личения риска кровотечений. Рецидивы ишемическихосложнений после отмены НФГ объясняют, почему этотэффект не сохранялся в более поздние сроки, если па-циентам не проводили реваскуляризацию до прекра-щения введения НФГ.При ЧКВ стандартный гепарин вводят внутривеннов виде болюса под контролем АВС (250-350 с или200-250 с, если вводился блокатор GP IIb/IIIa рецеп-торов) или в дозе, подобранной пo массе тела (обыч-но 70-100 ед/кг или 50-60 ед/кг в комбинации с бло-каторами GP IIb/IIIa рецепторов) [171]. Учитываязначительную вариабельность биодоступности НФГ, егорекомендуется применять под контролем АВС, особен-но при длительных вмешательствах, когда может потре-боваться введение дополнительной дозы. Продолже-ние гепаринизации после завершения вмешательства(до или после удаления проводника) не рекомендуется.Если пациент поступает в ангиографическую лабо-раторию на фоне продолжающейся инфузии гепари-на, то введение дополнительного болюса НФГ не-обходимо адаптировать с учетом АВС и применения бло-каторов GP IIb/IIIa рецепторов.
Прямые ингибиторы тромбина (бивалирудин)
Хотя разрабатывались несколько прямых ингибито-ров тромбина, только бивалирудин был разрешен к кли-ническому применению при ЧКВ и ОКС. Бивалирудиннепосредственно связывается с тромбином (факторомIIa) и ингибирует индуцированное им превращениефибриногена в фибрин. Бивалирудин инактивируеттромбин, связанный с фибрином, а также находя-щийся в жидкой фазе. Он не связывается с белками плаз-мы, поэтому антикоагулянтное действие препаратаболее предсказуемое. Бивалирудин полностью выво-дится почками. Показатели свертывания (аЧТВ, АВС) тес-но коррелируют с концентрациями в плазме, поэтомуэти два теста можно использовать для мониторирова-ния антикоагулянтной активности бивалирудина.Бивалирудин первоначально изучали при ЧКВ. В ис-следовании REPLACE-2 бивалирудин±блокаторыGP IIb/IIIa рецепторов не уступали НФГ±блокаторыGP IIb/IIIa рецепторов по эффективности в профилак-тике ишемических осложнений при ЧКВ, но значитель-но реже вызывали большие кровотечения (2,4% и4,1%; p<0,001). Достоверной разницы частоты твер-дых конечных точек через 1 мес, 6 мес и 1 год не вы-явили. Бивалирудин в настоящее время разрешен к при-менению при неотложных и плановых ЧКВ в дозе0,75 мг/кг в виде болюса с последующей инфузией по1,75 мг/кг/ч. У пациентов с ОКС без подъема сегмен-та ST бивалирудин рекомендуется вводить в дозе0,1 мг/кг внутривенно в виде болюса, а затем по0,25 мг/кг/ч до ЧКВ.ACUITY было единственным исследованием, в ко-тором бивалирудин специально изучали у пациентовс ОКС без подъема сегмента ST [196]. В это рандоми-зированное открытое исследование были включены13 819 пациентов с ОКС без подъема сегмента ST вы-сокого риска, которым планировалось инвазивноелечение. Пациентов рандомизировали в три группы:стандартная комбинированная терапия НФГ или НМГв сочетании с блокатором GP IIb/IIIa рецепторов (конт-рольная группа) (n=4 603); бивалирудин в комбина-ции с блокатором GP IIb/IIIa рецепторов (n=4 604);только бивалирудин (n=4 612). Лечение бивалируди-ном начинали перед ангиографией с внутривенного введения болюса 0,1 мг/кг с последующей инфузиейпо 0,25 мг/кгч. Перед ЧКВ вводили дополнительно бо-люс 0,5 мг/кг внутривенно, а затем проводили инфу-зию по 1,75 мг/кг/ч. После ЧКВ введение препаратапрекращали. У пациентов, получавших НФН/НМГ в со-четании с блокатором GP IIb/IIIa рецепторов или бива-лирудин в комбинации с блокатором GP IIb/IIIa рецеп-торов, частота комбинированной конечной точки (ише-мические осложнения) через 30 дн (7,3% и 7,7%, со-ответственно; ОР 1,07; 95% ДИ 0,92–1,23; p=0,39) ибольших кровотечений (5,7% и 5,3%; ОР 0,93; 95%ДИ 0,78–1,10; p=0,38) достоверно не отличалась. Би-валирудин не уступал стандартной терапии по эффек-тивности в профилактике ишемических исходов (7,8%и 7,3%; ОР 1,08; 95% ДИ 0,93–1,24; p=0,32), но до-стоверно реже вызывал большие кровотечения (3,0%и 5,7%; ОР 0,53; 95% ДИ 0,43–0,65; p<0,001). Со-ответственно, через 30 дн он имел достоверные пре-имущества перед НФГ/НМГ в сочетании с блокаторомGP IIb/IIIa рецепторов по «чистому» клиническому эф-фекту (10,1% и 11,7%; ОР 0,86; 95% ДИ 0,77–0,94;p=0,02) [196]. Эффективность монотерапии бивали-рудином была сопоставимой в большинстве подгрупп,выделенных в соответствии с протоколом, за исключе-нием пациентов, получавших клопидогрел перед ЧКВ,у которых была отмечена более высокая частота ише-мических исходов в группе бивалирудина (9,1% и7,1%; ОР 1,29; 95% ДИ 1,03–1,63).В целом лечение бивалирудином±блокаторомGP IIb/IIIa рецепторов по эффективности было сопоста-вимым с терапией НФГ/НМГ в сочетании с системати-ческим применением блокаторов GP IIb/IIIa рецепто-ров, но сопровождалось значительным снижениемриска больших кровотечений [197]. Однако в исследо-вании ACUITY не было выявлено достоверной разни-цы исходов в ближайшем и отдаленном периоде присравнении двух стратегий антикоагулянтной терапии[198]. И наконец, полученные данные показали, что пе-реход с НФГ или НМГ на бивалирудин во время ЧКВ неприводит к увеличению риска кровотечений, а факти-чески способствует их предупреждению [199].
Новые антикоагулянты
В настоящее время изучаются эффективность и без-опасность новых антикоагулянтов у пациентов с ОКС. Боль-шинство из них предназначены, скорее, для вторичнойпрофилактики, а не для лечения в острую фазу заболе-вания. Ингибиторы фактора Ха изучались в исследова-ниях II фазы [200,201]. Прямые пероральные ингиби-торы фактора Ха апиксабан (APPRAISE) [202] и риварок-сабан (ATLAS ACS-TIMI) [201] в различных дозах приме-няли в течение 6 мес у пациентов, недавно перенесшихОКС, на фоне лечения аспирином или двойной антитром-боцитарной терапии ацетилсалициловой кислотой и кло-пидогрелом. В обоих исследованиях были выявлены до-зозависимое увеличение частоты кровотечений и тенден-ция к снижению риска ишемических осложнений, осо-бенно у пациентов, получавших один аспирин. На осно-вании полученных данных были начаты исследованияIII фазы (APPRAISE-2 и ATLAS-2). ИсследованиеAPPRAISE-2 было прекращено досрочно в связи с повы-шенным риском кровотечений в группе апиксабана.Прямой ингибитор тромбина дабигатран изучалсяв дозоопределяющем исследовании II фазы (RE-DEEM),результаты которого пока не опубликованы. Отамикса-бан, являющийся прямым ингибитором фактора Ха,предназначенным для внутривенного введения, такжеизучался в исследовании II фазы [203]; исследованиеIII фазы продолжается.
Комбинированная терапия антикоагулянтамии антитромбоцитарными препаратами
Антикоагуляцию и двойную антитромбоцитарнуютерапию аспирином и блокатором P2Y12 рецептороврекомендуется начинать сразу после развития ОКСбез подъема сегмента ST. Антикоагуляцию продолжаюттолько в острую фазу, а двойную антитромбоцитарнуютерапию рекомендуется проводить в течение 12 мес какпосле стентирования, так и без стентирования. У значи-тельной части пациентов (6-8%) с ОКС без подъема сег-мента ST имеются показания к длительной терапии пе-роральными антагонистами витамина К, в том числефибрилляция предсердий со средним или высоким рис-ком тромбоэмболических осложнений, протез клапа-на сердца или ВТЭ. Двойная антитромботическая тера-пия (аспирин или клопидогрел+антагонист витаминаК) или тройная терапия (аспирин, клопидогрел и ан-тагонист витамина К) сопровождается 3-4-кратным уве-личением частоты больших кровотечений. Ведениетаких пациентов представляет трудную задачу. Так, вострую фазу и в последующем необходимо поддержи-вать адекватный уровень антикоагуляции. Перерыв влечении антагонистами витамина К может привести кповышению риска тромбоэмболических осложнений.На фоне полной антикоагуляции антагонистами вита-мина К может быть затруднительным или невозмож-ным выполнение ангиографии, ЧКВ или КШ, а длитель-ная тройная терапия сопровождается высоким рискомкровотечений. В связи с этим необходимо соблюдатьмеры предосторожности, которые рассматриваются внедавно опубликованных рекомендациях по плановымвмешательствам на коронарных артериях и ведению па-циентов в острую фазу (ИМ с подъемом и без подъе-ма сегмента ST) [204]. Стенты, выделяющие лекарства,следует имплантировать только в тех клиническихи/или анатомических ситуациях (распространеннаябляшка, небольшие сосуды, диабет и т.д.), когда ониимеют значительные преимущества перед голометаллическими стентами. Если пациенту, получающемудвойную или тройную терапию, требуется повторная ан-гиография, предпочтительно применение лучевогодоступа с целью снижения риска кровотечений. Реко-мендовалось также проводить ЧКВ на фоне терапии ан-тагонистами витамина К.В острую фазу может быть оправданным прекраще-ние приема антагонистов витамина К и назначение ан-титромбоцитарных препаратов и антикоагулянтов приснижении МНО менее 2,0. Если необходима дли-тельная терапия антагонистами витамина К в сочетаниис клопидогрелом и/или аспирином в низкой дозе, сле-дует тщательно контролировать МНО (целевой диапа-зон 2,0-2,5). Длительность тройной терапии следуетограничивать с учетом клинической ситуации, им-плантации стента, выделяющего или не выделяющеголекарства, и риска ишемических и геморрагическихосложнений, который оценивают на основании индек-сов и/или исходных показателей (табл. 6). Около по-ловины спонтанных кровотечений являются желудоч-но-кишечными, поэтому следует назначать ингибито-ры протонной помпы с целью гастропротекции.
Рекомендации по применению антикоагулянтов
Низкомолекулярные гепарины
НМГ — это производные гепарина с молекулярноймассой от 2000 до 10000 Да. Они характеризуются сба-лансированной анти-Ха и анти-IIa активностью, кото-рая зависит от молекулярной массы препарата. При уве-личении последней повышается анти-IIa активность.НМГ отличаются по фармакокинетическим и анти-коагулянтным свойствам и, соответственно, не яв-ляются взаимозаменяемыми. НМГ имеют несколько пре-имуществ перед НФГ, включая более полное всасыва-ние после подкожного введения, меньшее связываниес белками, менее выраженную активацию тромбоци-тов и более предсказуемую зависимость эффекта от дозы[171]. При лечении НМГ риск развития тромбоцитопе-нии, индуцированной гепарином, ниже, чем при лече-нии НФГ; НМГ, по крайней мере частично, выводятсяпочками. Риск накопления увеличивается при сниже-нии функции почек, которое сопровождается повыше-нием риска кровотечения. Большинство НМГ противо-показаны пациентам с почечной недостаточностью(клиренс креатинина ниже 30 мл/мин). Однако дозуэноксапарина у пациентов с клиренсом креатинина ме-нее 30 мл/мин можно снизить (1 мг/кг один раз в день,а не два раза в день).НМГ при ОКС без подъема сегмента ST назначают вподобранной по массе тела и обычно вводят подкож-но два раза в день, хотя у пациентов высокого рискалечение можно начинать с внутривенного введения бо-люса [179-182]. При применении НМГ в стандартныхдозах мониторирование анти-Ха активности не требу-ется за исключением особых ситуаций, например у па-циентов с почечной недостаточностью или ожирением.Оптимальный уровень анти-Ха активности, который дол-жен быть достигнут у пациентов с ОКС без подъема сег-мента ST, не установлен. У пациентов с венозной тром-боэмболией (ВТЭ) терапевтический диапазон состав-ляет 0,6-1,0 МЕ/мл. Четкая связь между анти-Ха актив-ностью и клиническими исходами не установлена.Однако риск кровотечений увеличивается, когда анти-Ха активность превышает 1,0 МЕ/мл [183]. В дозоопре-деляющем исследовании у пациентов с ОКС без подъе-ма сегмента ST эноксапарин изучали в дозах 1,25 и 1,0мг/кг два раза в день. Максимальная анти-Ха активностьв двух группах составляла 1,5 и 1,0 МЕ/мл, соответ-ственно. При применении эноксапарина в дозе 1,25мг/кг частота больших кровотечений в течение 14 днравнялась 6,5% (в основном в области сосудистого до-ступа). В группе эноксапарина 1,0 мг/кг частота боль-ших кровотечений снизилась до 1,9%. У пациентов сбольшими кровотечениями анти-Ха активность нахо-дилась в диапазоне 1,8-2,0 МЕ/мл [184]. В крупной ко-горте пациентов с нестабильной стенокардией/ИМбез подъема сегмента ST низкая анти-Ха активность(<0,5 МЕ/мл) при лечении эноксапарином ассоции-ровалась с трехкратным увеличением смертности у па-циентов с анти-Ха активностью в целевом диапазоне0,5-1,2 МЕ/мл. Низкие уровни анти-Ха (<0,05 МЕ/мл)были независимым предиктором смертности в течение30 дн. Это свидетельствует о том, что при лечении энок-сапарином уровень анти-Ха активности по возможно-сти должен составлять по крайней мере 0,5 МЕ/мл [185]. В неконтролируемых исследованиях и неболь-ших контролируемых исследованиях у пациентов, ко-торым проводились ЧКВ, анти-Ха активность >0,5МЕ/мл ассоциировалась с низкой частотой ишемиче-ских и геморрагических осложнений [186,187].Опубликованы результаты нескольких мета-анали-зов исследований, в которых сравнивали эффективностьНМГ и НФГ у пациентов с ОКС без подъема сегмента ST.В первый мета-анализ были включены 12 клиническихисследований различных препаратов в целом у 17 157пациентов с ОКС без подъема сегмента ST, получавшихаспирин. Гепарины достоверно превосходили плаце-бо по эффективности в профилактике смерти или ИМ(ОШ 0,53; 95% ДИ 0,38–0,73; p=0,0001). НМГ неимели преимуществ перед НФГ по эффективностиили безопасности [172]. При мета-анализе всех иссле-дований, в которых изучались эноксапарин и НФГ, в це-лом у 21 946 пациентов достоверной разницы смерт-ности через 30 дн не выявлено (3,0% и 3,0%, соответ-ственно; ОШ 1,00; 95% ДИ 0,85–1,17; p=незначимый).При лечении эноксапарином выявлено дополнитель-ное снижение риска смерти или ИМ в течение 30 дн посравнению с гепарином (10,1% и 11,0%; ОШ 0,91;95% ДИ 0,83–0,99). При анализе post-hoc в подгруп-пе пациентов, не получавших НФГ перед рандомиза-цией, выявлено значительное снижение смертности иличастоты ИМ в течение 30 дн при лечении эноксапари-ном по сравнению с НФГ (8,0% и 9,4%, соответ-ственно; ОШ 0,81; 95% ДИ 0,70–0,94). Достовернойразницы частоты гемотрансфузий (7,2% и 7,5%;ОШ 1,01; 95% ДИ 0,89–1,14) или больших кровотече-ний (4,7% и 4,5%; ОШ 1,04; 95% ДИ 0,83–1,30) че-рез 7 дн после рандомизации отмечено не было как вовсей выборке, так и в выборке пациентов, не получав-ших антикоагулянты перед рандомизацией. При допол-нительном мета-анализе, в который были включены всеисследования эноксапарина у пациентов с ОКС (как безподъема сегмента ST, так и с подъемом сегмента ST),были получены сходные результаты [188].И, наконец, в небольших исследованиях сравнива-ли эффективность и безопасность НМГ и НФГ в комби-нации с блокаторами GP IIb/IIIa рецепторов. По безопас-ности две схемы лечения не отличались. Ни в одном ис-следовании не было выявлено разницы риска «твердых»конечных точек, за исключением исследованияINTERACT, в котором имелась достоверная разница меж-ду группами эноксапарина/эптифибатида и НФГ/эп-тифибатида в пользу первой схемы [189-191]. Одна-ко все эти исследования не обладали необходимойстатистической силой, чтобы сделать окончательныевыводы.Большинство исследований проводились в то вре-мя, когда инвазивная стратегия еще не была внедренав широкую практику, а в некоторых исследованиях при-менение инвазивных методов вообще не рекомендо-валось. В результате инвазивное лечение проводилосьтолько у небольшой части пациентов, поэтому любыевыводы, сделанные на основании этих исследований,сегодня будут устаревшими.Единственным исследованием, в котором эноксапа-рин сравнивали с НФГ на фоне высокой частоты ЧКВ,реваскуляризации, стентирования и активной антитром-боцитарной терапии аспирином, клопидогрелом иблокаторами GP IIb/IIIa, было SYNERGY [192]. В это ис-следование были включены 10 027 пациентов высо-кого риска, которым проводили инвазивное обследо-вание и реваскуляризацию. 76% пациентов получалиантикоагулянты перед рандомизацией. Достовернойразницы частоты смерти и ИМ через 30 дн между груп-пами эноксапарина и НФГ не выявили (14,0% и14,5%, соответственно; ОШ 0,96; 95% ДИ 0,86–1,06;p=незначимый) [193]. Частота кровотечений былавыше в группе эноксапарина, в частности было отмече-но достоверное увеличение частоты больших кровотече-ний в соответствии с критериями TIMI (9,1% и 7,6%;p=0,008), но недостоверное увеличение частоты тяже-лых кровотечений в соответствии с критериямиGUSTO (2,7% и 2,2%; p=0,08) и гемотрансфузий(17,0% и 16,0%; p=0,16). Повышенная частота кро-вотечений, вероятно, отражала частое применениеантикоагулянтов перед рандомизацией и, возможно,частую смену антикоагулянта после рандомизации.Тем не менее, НМГ, особенно эноксапарин, часто при-меняют при ЧКВ, хотя мониторировать антикоагуляциюнелегко. Фармакокинетические/фармакодинамиче-ские свойства эноксапарина отличаются при подкожноми внутривенном применении. При плановом ЧКВ энок-сапарин вводят в дозе 1 мг/кг внутривенно. Внутривен-ные дозы, которые изучались в клинических исследова-ниях, были ниже (обычно 0,5 мг/кг) и обеспечивали туже максимальную анти-Ха активность в течение 3 мин[194]. Эноксапарин при внутривенном введении даетбыстрый и предсказуемый антикоагулянтный эффект втечение 2 ч. Более низкие дозы изучались также в иссле-довании STEEPLE [195]. У пациентов без ОКС частота кро-вотечений в группе эноксапарина в дозах 0,5 и 0,75 мг/кгбыла ниже, чем в группе НФГ. Однако исследование необладало статистической силой, необходимой для вы-явления различий между группами эноксапарина.У пациентов с ОКС без подъема сегмента ST, полу-чавших эноксапарин, не рекомендуется дополнитель-ное введение эноксапарина во время ЧКВ, если послед-няя подкожная инъекция препарата была выполненаменее чем за 8 ч до вмешательства. Если эноксапаринвводили более чем за 8 ч до ЧКВ, то рекомендуется до-полнительное введение 0,3 мг/кг внутривенно в видеболюса. Переход с одного антикоагулянта на другой вовремя ЧКВ не рекомендуется.
Нефракционированный гепарин
НФГ — это неоднородная смесь полисахаридов с мо-лекулярной массой от 2 000 до 30 000 Да (в основном15 000-18 000 Да). Одна треть молекул, входящих всостав НФГ, содержит пентасахарид, который связыва-ется с антитромбином и увеличивает скорость ингиби-рования фактора Ха. Для подавления фактора IIa необхо-димо взаимодействие гепарина с тромбином и анти-тромбином с образованием связи между ними. НФГплохо всасывается после подкожного введения, поэто-му его предпочтительно вводить внутривенно. Препа-рат обладает узким терапевтическим окном, в связи счем необходимо частое мониторирование аЧТВ. Целе-вой его уровень составляет 50-75 с (в 1,5-2,5 раза вышеверхней границы нормы). При более высоких значенияхаЧТВ увеличивается риск геморрагических осложнений,а дополнительный антитромботический эффект отсут-ствует. При аЧТВ менее 50 с антитромботическое дей-ствие ограниченно. НФГ рекомендуется назначать в дозе,подобранной по массе тела. Лечение начинают с вве-дения болюса 60-70 ед/кг (максимум 5 000 ед) с после-дующей инфузией по 12-15 ед/кг/ч (максимум1 000 ед/ч). Такая схема чаще всего обеспечивает до-стижение целевых значений аЧТВ [171]. Антикоагулянт-ный эффект НФГ быстро прекращается (в течение не-скольких часов после прекращения введения). В пер-вые 24 ч после прекращения терапии существует рискреактивации процесса свертывания и, соответственно,преходящего повышения риска рецидивирующих ише-мических осложнений, несмотря на одновременную те-рапию аспирином.При мета-анализе 6 исследований было показано,что кратковременное введение НФГ приводит к сниже-нию риска смерти или ИМ на 33% по сравнению с пла-цебо или отсутствием антикоагуляции (ОШ 0,67; 95%ДИ 0,45–0,99; p=0,04) [172]. Благоприятный эф-фект препарата был связан со снижением риска разви-тия ИМ. В клинических исследованиях, в которыхсравнивали комбинированную терапию НФГ+аспирини монотерапию аспирином у пациентов с ОКС безподъема сегмента ST, было отмечено небольшое пре-имущество комбинированной терапии, но ценой уве-личения риска кровотечений. Рецидивы ишемическихосложнений после отмены НФГ объясняют, почему этотэффект не сохранялся в более поздние сроки, если па-циентам не проводили реваскуляризацию до прекра-щения введения НФГ.При ЧКВ стандартный гепарин вводят внутривеннов виде болюса под контролем АВС (250-350 с или200-250 с, если вводился блокатор GP IIb/IIIa рецеп-торов) или в дозе, подобранной пo массе тела (обыч-но 70-100 ед/кг или 50-60 ед/кг в комбинации с бло-каторами GP IIb/IIIa рецепторов) [171]. Учитываязначительную вариабельность биодоступности НФГ, егорекомендуется применять под контролем АВС, особен-но при длительных вмешательствах, когда может потре-боваться введение дополнительной дозы. Продолже-ние гепаринизации после завершения вмешательства(до или после удаления проводника) не рекомендуется.Если пациент поступает в ангиографическую лабо-раторию на фоне продолжающейся инфузии гепари-на, то введение дополнительного болюса НФГ не-обходимо адаптировать с учетом АВС и применения бло-каторов GP IIb/IIIa рецепторов.
Прямые ингибиторы тромбина (бивалирудин)
Хотя разрабатывались несколько прямых ингибито-ров тромбина, только бивалирудин был разрешен к кли-ническому применению при ЧКВ и ОКС. Бивалирудиннепосредственно связывается с тромбином (факторомIIa) и ингибирует индуцированное им превращениефибриногена в фибрин. Бивалирудин инактивируеттромбин, связанный с фибрином, а также находя-щийся в жидкой фазе. Он не связывается с белками плаз-мы, поэтому антикоагулянтное действие препаратаболее предсказуемое. Бивалирудин полностью выво-дится почками. Показатели свертывания (аЧТВ, АВС) тес-но коррелируют с концентрациями в плазме, поэтомуэти два теста можно использовать для мониторирова-ния антикоагулянтной активности бивалирудина.Бивалирудин первоначально изучали при ЧКВ. В ис-следовании REPLACE-2 бивалирудин±блокаторыGP IIb/IIIa рецепторов не уступали НФГ±блокаторыGP IIb/IIIa рецепторов по эффективности в профилак-тике ишемических осложнений при ЧКВ, но значитель-но реже вызывали большие кровотечения (2,4% и4,1%; p<0,001). Достоверной разницы частоты твер-дых конечных точек через 1 мес, 6 мес и 1 год не вы-явили. Бивалирудин в настоящее время разрешен к при-менению при неотложных и плановых ЧКВ в дозе0,75 мг/кг в виде болюса с последующей инфузией по1,75 мг/кг/ч. У пациентов с ОКС без подъема сегмен-та ST бивалирудин рекомендуется вводить в дозе0,1 мг/кг внутривенно в виде болюса, а затем по0,25 мг/кг/ч до ЧКВ.ACUITY было единственным исследованием, в ко-тором бивалирудин специально изучали у пациентовс ОКС без подъема сегмента ST [196]. В это рандоми-зированное открытое исследование были включены13 819 пациентов с ОКС без подъема сегмента ST вы-сокого риска, которым планировалось инвазивноелечение. Пациентов рандомизировали в три группы:стандартная комбинированная терапия НФГ или НМГв сочетании с блокатором GP IIb/IIIa рецепторов (конт-рольная группа) (n=4 603); бивалирудин в комбина-ции с блокатором GP IIb/IIIa рецепторов (n=4 604);только бивалирудин (n=4 612). Лечение бивалируди-ном начинали перед ангиографией с внутривенного введения болюса 0,1 мг/кг с последующей инфузиейпо 0,25 мг/кгч. Перед ЧКВ вводили дополнительно бо-люс 0,5 мг/кг внутривенно, а затем проводили инфу-зию по 1,75 мг/кг/ч. После ЧКВ введение препаратапрекращали. У пациентов, получавших НФН/НМГ в со-четании с блокатором GP IIb/IIIa рецепторов или бива-лирудин в комбинации с блокатором GP IIb/IIIa рецеп-торов, частота комбинированной конечной точки (ише-мические осложнения) через 30 дн (7,3% и 7,7%, со-ответственно; ОР 1,07; 95% ДИ 0,92–1,23; p=0,39) ибольших кровотечений (5,7% и 5,3%; ОР 0,93; 95%ДИ 0,78–1,10; p=0,38) достоверно не отличалась. Би-валирудин не уступал стандартной терапии по эффек-тивности в профилактике ишемических исходов (7,8%и 7,3%; ОР 1,08; 95% ДИ 0,93–1,24; p=0,32), но до-стоверно реже вызывал большие кровотечения (3,0%и 5,7%; ОР 0,53; 95% ДИ 0,43–0,65; p<0,001). Со-ответственно, через 30 дн он имел достоверные пре-имущества перед НФГ/НМГ в сочетании с блокаторомGP IIb/IIIa рецепторов по «чистому» клиническому эф-фекту (10,1% и 11,7%; ОР 0,86; 95% ДИ 0,77–0,94;p=0,02) [196]. Эффективность монотерапии бивали-рудином была сопоставимой в большинстве подгрупп,выделенных в соответствии с протоколом, за исключе-нием пациентов, получавших клопидогрел перед ЧКВ,у которых была отмечена более высокая частота ише-мических исходов в группе бивалирудина (9,1% и7,1%; ОР 1,29; 95% ДИ 1,03–1,63).В целом лечение бивалирудином±блокаторомGP IIb/IIIa рецепторов по эффективности было сопоста-вимым с терапией НФГ/НМГ в сочетании с системати-ческим применением блокаторов GP IIb/IIIa рецепто-ров, но сопровождалось значительным снижениемриска больших кровотечений [197]. Однако в исследо-вании ACUITY не было выявлено достоверной разни-цы исходов в ближайшем и отдаленном периоде присравнении двух стратегий антикоагулянтной терапии[198]. И наконец, полученные данные показали, что пе-реход с НФГ или НМГ на бивалирудин во время ЧКВ неприводит к увеличению риска кровотечений, а факти-чески способствует их предупреждению [199].
Новые антикоагулянты
В настоящее время изучаются эффективность и без-опасность новых антикоагулянтов у пациентов с ОКС. Боль-шинство из них предназначены, скорее, для вторичнойпрофилактики, а не для лечения в острую фазу заболе-вания. Ингибиторы фактора Ха изучались в исследова-ниях II фазы [200,201]. Прямые пероральные ингиби-торы фактора Ха апиксабан (APPRAISE) [202] и риварок-сабан (ATLAS ACS-TIMI) [201] в различных дозах приме-няли в течение 6 мес у пациентов, недавно перенесшихОКС, на фоне лечения аспирином или двойной антитром-боцитарной терапии ацетилсалициловой кислотой и кло-пидогрелом. В обоих исследованиях были выявлены до-зозависимое увеличение частоты кровотечений и тенден-ция к снижению риска ишемических осложнений, осо-бенно у пациентов, получавших один аспирин. На осно-вании полученных данных были начаты исследованияIII фазы (APPRAISE-2 и ATLAS-2). ИсследованиеAPPRAISE-2 было прекращено досрочно в связи с повы-шенным риском кровотечений в группе апиксабана.Прямой ингибитор тромбина дабигатран изучалсяв дозоопределяющем исследовании II фазы (RE-DEEM),результаты которого пока не опубликованы. Отамикса-бан, являющийся прямым ингибитором фактора Ха,предназначенным для внутривенного введения, такжеизучался в исследовании II фазы [203]; исследованиеIII фазы продолжается.
Комбинированная терапия антикоагулянтамии антитромбоцитарными препаратами
Антикоагуляцию и двойную антитромбоцитарнуютерапию аспирином и блокатором P2Y12 рецептороврекомендуется начинать сразу после развития ОКСбез подъема сегмента ST. Антикоагуляцию продолжаюттолько в острую фазу, а двойную антитромбоцитарнуютерапию рекомендуется проводить в течение 12 мес какпосле стентирования, так и без стентирования. У значи-тельной части пациентов (6-8%) с ОКС без подъема сег-мента ST имеются показания к длительной терапии пе-роральными антагонистами витамина К, в том числефибрилляция предсердий со средним или высоким рис-ком тромбоэмболических осложнений, протез клапа-на сердца или ВТЭ. Двойная антитромботическая тера-пия (аспирин или клопидогрел+антагонист витаминаК) или тройная терапия (аспирин, клопидогрел и ан-тагонист витамина К) сопровождается 3-4-кратным уве-личением частоты больших кровотечений. Ведениетаких пациентов представляет трудную задачу. Так, вострую фазу и в последующем необходимо поддержи-вать адекватный уровень антикоагуляции. Перерыв влечении антагонистами витамина К может привести кповышению риска тромбоэмболических осложнений.На фоне полной антикоагуляции антагонистами вита-мина К может быть затруднительным или невозмож-ным выполнение ангиографии, ЧКВ или КШ, а длитель-ная тройная терапия сопровождается высоким рискомкровотечений. В связи с этим необходимо соблюдатьмеры предосторожности, которые рассматриваются внедавно опубликованных рекомендациях по плановымвмешательствам на коронарных артериях и ведению па-циентов в острую фазу (ИМ с подъемом и без подъе-ма сегмента ST) [204]. Стенты, выделяющие лекарства,следует имплантировать только в тех клиническихи/или анатомических ситуациях (распространеннаябляшка, небольшие сосуды, диабет и т.д.), когда ониимеют значительные преимущества перед голометаллическими стентами. Если пациенту, получающемудвойную или тройную терапию, требуется повторная ан-гиография, предпочтительно применение лучевогодоступа с целью снижения риска кровотечений. Реко-мендовалось также проводить ЧКВ на фоне терапии ан-тагонистами витамина К.В острую фазу может быть оправданным прекраще-ние приема антагонистов витамина К и назначение ан-титромбоцитарных препаратов и антикоагулянтов приснижении МНО менее 2,0. Если необходима дли-тельная терапия антагонистами витамина К в сочетаниис клопидогрелом и/или аспирином в низкой дозе, сле-дует тщательно контролировать МНО (целевой диапа-зон 2,0-2,5). Длительность тройной терапии следуетограничивать с учетом клинической ситуации, им-плантации стента, выделяющего или не выделяющеголекарства, и риска ишемических и геморрагическихосложнений, который оценивают на основании индек-сов и/или исходных показателей (табл. 6). Около по-ловины спонтанных кровотечений являются желудоч-но-кишечными, поэтому следует назначать ингибито-ры протонной помпы с целью гастропротекции.
Рекомендации по применению антикоагулянтов
 Реваскуляризация коронарных артерийРеваскуляризация у пациентов с ОКС без подъемасегмента ST приводит к купированию симптомов, со-кращению длительности госпитализации и улучшениюпрогноза. Показания и сроки реваскуляризации мио-карда и выбор метода лечения (ЧКВ или КШ) зависятот многих факторов, включая состояние пациента, на-личие факторов риска и сопутствующих заболеванийи распространенность и тяжесть поражения коронар-ных артерий (по данным ангиографии).Стратификацию риска следует проводить как мож-но раньше, чтобы быстро выделить пациентов высоко-го риска и сократить срок до инвазивного лечения. Од-нако с точки зрения риска и прогноза пациенты с ОКСбез подъема сегмента ST представляют собой неодно-родную группу больных. Среди них могут быть паци-енты группы низкого риска, у которых возможны кон-сервативное лечение и выборочное инвазивное вме-шательство, и больные с высоким риском смерти и сер-дечно-сосудистых исходов, которых следует быстро на-правлять на ангиографию и реваскуляризацию. В свя-зи с этим стратификация риска имеет ключевое значе-ние для выбора оптимальной стратегии ведения. Рискоценивают на основании общепринятых факторовриска и/или с помощью специальных индексов, такихкак GRACE (см. раздел 4.4.) [205].
Инвазивное или консервативное ведение
В многочисленных рандомизированных контроли-руемых исследованиях и мета-анализах сравнивали эф-фективность инвазивного и консервативного или вы-борочного консервативного подходов к лечению ОКСв ближайшие и отдаленные сроки. Оценить пользу ре-васкуляризации в таких исследования трудно. Онаможет быть заниженной, учитывая разницу доли паци-ентов, которые переходят из одной группы в другую(консервативное лечение — инвазивное вмешательство;доля таких пациентов варьируется от 28% до 58%). Вцелом, польза реваскуляризации более выражена в техслучаях, когда разница частоты ее между двумя груп-пами высокая. Кроме того, возможно наличие си-стемной ошибки, связанной с отбором пациентов, таккак в некоторые исследования включали всех пациен тов подряд, в то время как из других исследований ис-ключали пациентов с тяжелыми нарушениями гемоди-намики.При мета-анализе 7 рандомизированных контро-лируемых исследований, в которых сравнивали рутин-ную ангиографию с последующей реваскуляризациейи выборочное инвазивное лечение, было выявлено не-достоверное снижение смертности и достоверноеснижение риска ИМ на фоне инвазивной стратегиилечения [206]. Однако было отмечено значительноеувеличение риска смерти, а также смерти и ИМ во вре-мя первичной госпитализации для инвазивного лече-ния. Тем не менее, 4 из 7 исследований, включенныхв мета-анализ, не соответствовали современной прак-тике, учитывая редкость имплантации стентов и при-менения блокаторов GP IIb/IIIa рецепторов. В другоммета-анализе 7 исследований, в которых вспомогатель-ная терапия была более современной, выявленозначительное снижение риска смерти от любых при-чин и нефатального ИМ в течение 2 лет после ранне-го инвазивного лечения, которое не сопровождалосьповышением риска смерти и нефатального ИМ втечение 1 мес [207]. В последнем мета-анализе 8 ран-домизированных исследований отмечено значитель-ное снижение риска смерти, ИМ или повторной гос-питализации через 1 год у пациентов с ОКС, которымпроводилось инвазивное лечение [208]. Однако бла-гоприятный эффект был достигнут в основном за счетулучшения исходов у пациентов с положительнымибиомаркерами (высокий риск). При этом результатылечения были сопоставимыми у женщин и мужчин сположительными биомаркерами. Важно отметить,что у женщин с отрицательными биомаркерами былавыявлена тенденция к увеличению частоты неблагопри-ятных исходов на фоне ранней инвазивной стратегии.Эти данные свидетельствуют о том, что ее следует из-бегать у женщин группы низкого риска, у которых неопределяется тропонин. По данным мета-анализа ин-дивидуальных результатов лечения пациентов в иссле-дованиях FRISC-2, ICTUS и RITA-3, в которых сравни-вали рутинную и выборочную инвазивную стратегиюлечения, было выявлено снижение смертности и ча-стоты нефатального ИМ в течение 5 лет; разницамежду группами была наиболее выраженной у паци-ентов с высоким риском [209]. Независимыми предик-торами смерти и нефатального ИМ были возраст, са-харный диабет, перенесенный ИМ, депрессия сегмен-та ST, артериальная гипертония, индекс массы тела (≥25или ≥35 кг/м2) и стратегия лечения [209]. В группахнизкого и среднего риска абсолютное снижение часто-ты смерти от сердечно-сосудистых причин и нефаталь-ного ИМ составило 2,0-3,8%, а в группе высокого рис-ка — 11,1%. Полученные данные обосновывают ши-рокое применение инвазивной стратегии, однако ониподчеркивают также роль стратификации риска при вы-боре метода лечения.Подгруппы пациентов высокого риска, у которых об-основанно раннее инвазивное лечение (пациенты с диа-бетом или почечной недостаточностью, пожилые люди)обсуждаются в соответствующих разделах.
Сроки ангиографии и вмешательства
Оптимальные сроки ангиографии и реваскуляриза-ции миокарда у пациентов с ОКС без подъема сегмен-та ST изучались в многочисленных исследованиях.Однако из рандомизированных контролируемых иссле-дований обычно исключали пациентов с очень высо-ким риском, например с рефрактерной стенокардией,тяжелой сердечной недостаточностью, угрожающи-ми жизни желудочковыми аритмиями или гемодина-мическими нарушениями, чтобы не отказывать им влечении, которое потенциально может сохранитьжизнь. У таких пациентов может иметься формирую-щийся ИМ, поэтому им следует проводить немедлен-ное (<2 ч) инвазивное обследование независимо от дан-ных ЭКГ и уровней биомаркеров.Ранее высказывались опасения по поводу того, чторанняя ангиография с последующей реваскуляризаци-ей могут сопровождаться увеличением риска осложне-ний в острую фазу [206]. В 5 проспективных рандоми-зированных исследованиях сравнивали очень ран-нюю (0,5-14 ч) и отсроченную (21-86 ч) стратегии ин-вазивного лечения; среди этих исследований было одноисследование адекватного размера — TIMACS (см. ре-комендации Европейского общества кардиологов по ре-васкуляризации [148]). По данным мета-анализа 3 ис-следований, в том числе ABOARD [210], ELISA [211] иISAR-COOL [170], и исследования TIMACS [212], ран-няя катетеризация с последующим коронарным вмеша-тельством в первый день госпитализации были безопас-ными и привели к снижению риска рецидивирующейишемии миокарда (–41%) и сокращению длительно-сти госпитализации (–28%) [213]. При анализе твер-дых конечных точек только в небольшом исследованииOPTIMA было выявлено увеличение частоты ИМ, свя-занного с вмешательством, у больных, которым ревас-куляризацию проводили немедленно (30 мин), а не вболее поздние сроки (25 ч) [214]. Напротив, исследо-вание ABOARD не подтвердило разницу частоты ИМ,который диагностировали на основании уровня тропо-нина, при немедленном ЧКВ (1,2 ч) или выполнениивмешательства на следующий рабочий день (в среднем21 ч) [210].Учитывая неоднородность профиля риска, оптималь-ные сроки инвазивного лечения могут отличаться в раз-личных когортах. Накапливаются данные о том, что ин-вазивная стратегия дает благоприятный эффект в тече-ние первых 24 ч у пациентов высокого риска. В исследовании TIMACS при раннем инвазивном лечении у па-циентов с высоким риском (индекс GRACE≥140) быловыявлено достоверное снижение частоты смерти, ИМили инсульта через 6 мес по сравнению с отсроченнымвмешательством (≥36 ч). У пациентов с низким илисредним риском (индекс GRACE≤140) достоверной раз-ницы исходов выявлено не было [212]. Важно отметить,что ранняя инвазивная стратегия в этом исследованиине сопровождалась какими-либо проблемами с точкизрения безопасности. В исследовании ACUITY выпол-нение ЧКВ более чем через 24 ч было независимым пре-диктором смертности в течение 30 дн и 1 года [215].Увеличение риска ишемических исходов было наибо-лее очевидным у пациентов со средним и высоким рис-ком (в соответствии с индексом TIMI).При выборе инвазивной стратегии важное значениеимеет оптимальная вспомогательная фармакотера-пия, однако она не должна задерживать ангиографиюи вмешательство [151]. Намеренная задержка инвазив-ного лечения с целью стабилизации пациентов передвмешательством, в том числе с помощью блокаторовGP IIb/IIIa рецепторов (стратегия «охлаждения»), не при-носит пользы [151,170].
Таблица 9. Критерии оценки высокого риска(показания к инвазивному лечению)
Реваскуляризация коронарных артерийРеваскуляризация у пациентов с ОКС без подъемасегмента ST приводит к купированию симптомов, со-кращению длительности госпитализации и улучшениюпрогноза. Показания и сроки реваскуляризации мио-карда и выбор метода лечения (ЧКВ или КШ) зависятот многих факторов, включая состояние пациента, на-личие факторов риска и сопутствующих заболеванийи распространенность и тяжесть поражения коронар-ных артерий (по данным ангиографии).Стратификацию риска следует проводить как мож-но раньше, чтобы быстро выделить пациентов высоко-го риска и сократить срок до инвазивного лечения. Од-нако с точки зрения риска и прогноза пациенты с ОКСбез подъема сегмента ST представляют собой неодно-родную группу больных. Среди них могут быть паци-енты группы низкого риска, у которых возможны кон-сервативное лечение и выборочное инвазивное вме-шательство, и больные с высоким риском смерти и сер-дечно-сосудистых исходов, которых следует быстро на-правлять на ангиографию и реваскуляризацию. В свя-зи с этим стратификация риска имеет ключевое значе-ние для выбора оптимальной стратегии ведения. Рискоценивают на основании общепринятых факторовриска и/или с помощью специальных индексов, такихкак GRACE (см. раздел 4.4.) [205].
Инвазивное или консервативное ведение
В многочисленных рандомизированных контроли-руемых исследованиях и мета-анализах сравнивали эф-фективность инвазивного и консервативного или вы-борочного консервативного подходов к лечению ОКСв ближайшие и отдаленные сроки. Оценить пользу ре-васкуляризации в таких исследования трудно. Онаможет быть заниженной, учитывая разницу доли паци-ентов, которые переходят из одной группы в другую(консервативное лечение — инвазивное вмешательство;доля таких пациентов варьируется от 28% до 58%). Вцелом, польза реваскуляризации более выражена в техслучаях, когда разница частоты ее между двумя груп-пами высокая. Кроме того, возможно наличие си-стемной ошибки, связанной с отбором пациентов, таккак в некоторые исследования включали всех пациен тов подряд, в то время как из других исследований ис-ключали пациентов с тяжелыми нарушениями гемоди-намики.При мета-анализе 7 рандомизированных контро-лируемых исследований, в которых сравнивали рутин-ную ангиографию с последующей реваскуляризациейи выборочное инвазивное лечение, было выявлено не-достоверное снижение смертности и достоверноеснижение риска ИМ на фоне инвазивной стратегиилечения [206]. Однако было отмечено значительноеувеличение риска смерти, а также смерти и ИМ во вре-мя первичной госпитализации для инвазивного лече-ния. Тем не менее, 4 из 7 исследований, включенныхв мета-анализ, не соответствовали современной прак-тике, учитывая редкость имплантации стентов и при-менения блокаторов GP IIb/IIIa рецепторов. В другоммета-анализе 7 исследований, в которых вспомогатель-ная терапия была более современной, выявленозначительное снижение риска смерти от любых при-чин и нефатального ИМ в течение 2 лет после ранне-го инвазивного лечения, которое не сопровождалосьповышением риска смерти и нефатального ИМ втечение 1 мес [207]. В последнем мета-анализе 8 ран-домизированных исследований отмечено значитель-ное снижение риска смерти, ИМ или повторной гос-питализации через 1 год у пациентов с ОКС, которымпроводилось инвазивное лечение [208]. Однако бла-гоприятный эффект был достигнут в основном за счетулучшения исходов у пациентов с положительнымибиомаркерами (высокий риск). При этом результатылечения были сопоставимыми у женщин и мужчин сположительными биомаркерами. Важно отметить,что у женщин с отрицательными биомаркерами былавыявлена тенденция к увеличению частоты неблагопри-ятных исходов на фоне ранней инвазивной стратегии.Эти данные свидетельствуют о том, что ее следует из-бегать у женщин группы низкого риска, у которых неопределяется тропонин. По данным мета-анализа ин-дивидуальных результатов лечения пациентов в иссле-дованиях FRISC-2, ICTUS и RITA-3, в которых сравни-вали рутинную и выборочную инвазивную стратегиюлечения, было выявлено снижение смертности и ча-стоты нефатального ИМ в течение 5 лет; разницамежду группами была наиболее выраженной у паци-ентов с высоким риском [209]. Независимыми предик-торами смерти и нефатального ИМ были возраст, са-харный диабет, перенесенный ИМ, депрессия сегмен-та ST, артериальная гипертония, индекс массы тела (≥25или ≥35 кг/м2) и стратегия лечения [209]. В группахнизкого и среднего риска абсолютное снижение часто-ты смерти от сердечно-сосудистых причин и нефаталь-ного ИМ составило 2,0-3,8%, а в группе высокого рис-ка — 11,1%. Полученные данные обосновывают ши-рокое применение инвазивной стратегии, однако ониподчеркивают также роль стратификации риска при вы-боре метода лечения.Подгруппы пациентов высокого риска, у которых об-основанно раннее инвазивное лечение (пациенты с диа-бетом или почечной недостаточностью, пожилые люди)обсуждаются в соответствующих разделах.
Сроки ангиографии и вмешательства
Оптимальные сроки ангиографии и реваскуляриза-ции миокарда у пациентов с ОКС без подъема сегмен-та ST изучались в многочисленных исследованиях.Однако из рандомизированных контролируемых иссле-дований обычно исключали пациентов с очень высо-ким риском, например с рефрактерной стенокардией,тяжелой сердечной недостаточностью, угрожающи-ми жизни желудочковыми аритмиями или гемодина-мическими нарушениями, чтобы не отказывать им влечении, которое потенциально может сохранитьжизнь. У таких пациентов может иметься формирую-щийся ИМ, поэтому им следует проводить немедлен-ное (<2 ч) инвазивное обследование независимо от дан-ных ЭКГ и уровней биомаркеров.Ранее высказывались опасения по поводу того, чторанняя ангиография с последующей реваскуляризаци-ей могут сопровождаться увеличением риска осложне-ний в острую фазу [206]. В 5 проспективных рандоми-зированных исследованиях сравнивали очень ран-нюю (0,5-14 ч) и отсроченную (21-86 ч) стратегии ин-вазивного лечения; среди этих исследований было одноисследование адекватного размера — TIMACS (см. ре-комендации Европейского общества кардиологов по ре-васкуляризации [148]). По данным мета-анализа 3 ис-следований, в том числе ABOARD [210], ELISA [211] иISAR-COOL [170], и исследования TIMACS [212], ран-няя катетеризация с последующим коронарным вмеша-тельством в первый день госпитализации были безопас-ными и привели к снижению риска рецидивирующейишемии миокарда (–41%) и сокращению длительно-сти госпитализации (–28%) [213]. При анализе твер-дых конечных точек только в небольшом исследованииOPTIMA было выявлено увеличение частоты ИМ, свя-занного с вмешательством, у больных, которым ревас-куляризацию проводили немедленно (30 мин), а не вболее поздние сроки (25 ч) [214]. Напротив, исследо-вание ABOARD не подтвердило разницу частоты ИМ,который диагностировали на основании уровня тропо-нина, при немедленном ЧКВ (1,2 ч) или выполнениивмешательства на следующий рабочий день (в среднем21 ч) [210].Учитывая неоднородность профиля риска, оптималь-ные сроки инвазивного лечения могут отличаться в раз-личных когортах. Накапливаются данные о том, что ин-вазивная стратегия дает благоприятный эффект в тече-ние первых 24 ч у пациентов высокого риска. В исследовании TIMACS при раннем инвазивном лечении у па-циентов с высоким риском (индекс GRACE≥140) быловыявлено достоверное снижение частоты смерти, ИМили инсульта через 6 мес по сравнению с отсроченнымвмешательством (≥36 ч). У пациентов с низким илисредним риском (индекс GRACE≤140) достоверной раз-ницы исходов выявлено не было [212]. Важно отметить,что ранняя инвазивная стратегия в этом исследованиине сопровождалась какими-либо проблемами с точкизрения безопасности. В исследовании ACUITY выпол-нение ЧКВ более чем через 24 ч было независимым пре-диктором смертности в течение 30 дн и 1 года [215].Увеличение риска ишемических исходов было наибо-лее очевидным у пациентов со средним и высоким рис-ком (в соответствии с индексом TIMI).При выборе инвазивной стратегии важное значениеимеет оптимальная вспомогательная фармакотера-пия, однако она не должна задерживать ангиографиюи вмешательство [151]. Намеренная задержка инвазив-ного лечения с целью стабилизации пациентов передвмешательством, в том числе с помощью блокаторовGP IIb/IIIa рецепторов (стратегия «охлаждения»), не при-носит пользы [151,170].
Таблица 9. Критерии оценки высокого риска(показания к инвазивному лечению)
 В целом, сроки ангиографии и реваскуляризации вы-бирают с учетом профиля риска пациентов. Пациентамс очень высоким риском (см. выше) показана не-отложная коронарная ангиография (<2 ч). У пациен-тов с высоким риском (индекс GRACE>140 и наличиепо крайней мере одного фактора высокого риска) об-основанна ранняя инвазивная стратегия в течениепервых 24 ч. Эта стратегия предполагает перевод па-циентов в лечебные учреждения, в которых может бытьвыполнена катетеризация. У пациентов с более низкимриском, у которых индекс GRACE составляет ≤140, од-нако, имеется по крайней мере один критерий высо-кого риска (табл. 9), инвазивное обследование можетбыть отложено, однако его следует провести во времягоспитализации, предпочтительно в течение 72 ч послепоступления. В таких случаях немедленный перевод па-циента не требуется, однако его следует организоватьв течение 72 ч (например, у пациентов с диабетом). Па-циентам с низким риском, у которых отсутствуют симп-томы ишемии, необходимо провести неинвазивнуюстресс-пробу перед выпиской. Если определяется об-ратимая ишемия миокарда, показана коронарная ан-гиография.
Чрескожное коронарное вмешательство
или коронарное шунтированиеВ рандомизированных контролируемых исследова-ниях ЧКВ и КШ у пациентов с ОКС без подъема сегмен-та ST специально не сравнивали. Во всех исследованиях,в которых сравнивали раннее или позднее лечение, атакже инвазивное или консервативное ведение, реше-ние о выборе вмешательства (КШ или ЧКВ) принима-ли исследователи.У стабильных пациентов, перенесших ОКС, метод ре-васкуляризации выбирают так же, как при стабильнойИБС [148]. Примерно у трети пациентов при ангиогра-фии выявляют стеноз одной коронарной артерии, чтопозволяет в большинстве случаев выполнить ЧКВ. У по-ловины пациентов наблюдается поражение несколькихкоронарных артерий [181,182]. В таких случаях выбратьтип вмешательства сложнее (ЧКВ на артерии, пораже-ние которой было причиной ОКС, ЧКВ на несколькихсосудах, КШ или комбинированная (гибридная) ревас-куляризация). Стратегию реваскуляризации выбираютс учетом клинического состояния, тяжести и распростра-ненности коронарного атеросклероза и особенностейатеросклеротической бляшки.У большинства пациентов с поражением несколькихартерий обычно начинают с ЧКВ на артерии, пораже-ние которой было причиной развития ОКС. Этот под-ход не сравнивали со стентированием нескольких со-судов в рандомизированных исследованиях. Однако прианализе крупной базы данных, включающей в себя105 866 пациентов с ОКС без подъема сегмента ST, у ко-торых имелось поражение нескольких коронарных ар-терий, были сопоставлены результаты ЧКВ на несколь-ких и одном сосуде [216]. Вмешательство на несколькихартериях реже было успешным, однако госпитальная ле-тальность и частота осложнений были сопоставимыми,хотя результаты длительного наблюдения отсутствуют.КШ сравнивали с ЧКВ у пациентов с поражениемнескольких коронарных артерий, которые быливключены в исследование ACUITY [217]. У пациентов,которым проводили ЧКВ, была ниже частота инсуль-та, ИМ, кровотечений и повреждения почек. Смерт-ность через 1 мес и 1 год была сходной в двух груп-пах, однако через 1 мес и 1 год после ЧКВ выявили значительное увеличение частоты внеплановой ревас-куляризации. Однако только 43% пациентов, перенес-ших КШ, были сопоставимы с пациентами группы ЧКВ.Кроме того, через 1 год выявили тенденцию к увеличе-нию риска основных сердечно-сосудистых событийпосле ЧКВ по сравнению с КШ (25,0% и 19,5%;р=0,05). Полученные данные согласуются с резуль-татами исследования SYNTAX, в котором 28,5% па-циентов перенесли ОКС [218]. Однако субанализэтих пациентов не проводился.В каждом лечебном учреждении необходимо иметьпротокол ведения пациентов, разработанный на осно-вании индекса SYNTAX. При этом следует выделить ана-томические и клинические критерии, позволяющиеопределить возможность выполнения ЧКВ после ангио-графии или целесообразность направления пациентана КШ [219]. После стентирования основного поражен-ного сосуда у пациентов с индексами SYNTAX, находя-щимися в двух верхних терцилях, следует оценить функ-циональное значение поражения других сосудов сучетом сопутствующих заболеваний и индивидуальныхособенностей пациента.
Коронарное шунтирование
Доля пациентов с ОКС без подъема сегмента ST, ко-торым проводится КШ во время первичной госпитали-зации, составляет около 10% [220]. Польза ЧКВ у та-ких пациентов отражает ранние сроки вмешательства,в то время как КШ дает наиболее выраженный эффект,если пациентов оперируют через несколько дней послестабилизации их состояния в зависимости от индиви-дуального риска. Результаты раннего и отсроченного КШв рандомизированном исследовании не сравнивали,поэтому после ЧКВ на основном пораженном сосуде упациентов с тяжелым коронарным атеросклерозомрекомендуется выждать 48-72 ч. По данным анализабольшого числа пациентов, госпитализированных с ОКС,раннее КШ, даже у пациентов с более высоким риском,сопровождалось очень низкой госпитальной смерт-ностью [221]. В регистрах CRUSADE и ACTION не быловыявлено достоверной разницы исходов у пациентов,которым КШ в проводили в течение ≤48 ч или >48 ч,хотя операцию чаще откладывали у пациентов с болеевысоким риском [222]. У пациентов, которым плани-руется КШ, сроки операции следует выбирать индиви-дуально с учетом симптомов, состояния гемодинами-ки, анатомии коронарных артерий, наличия ишемии ирезерва кровотока. Если сохраняется или рецидивиру-ет ишемия, имеются желудочковые аритмии или неста-бильность гемодинамики, КШ следует выполнить не-медленно. У пациентов со стенозом ствола левой коро-нарной артерии или стенозом трех коронарных арте-рий, включая проксимальную часть левой передней нис-ходящей артерии, операцию необходимо провестиво время первичной госпитализации. При принятии ре-шения следует учитывать риск геморрагических ослож-нений у пациентов, которым КШ проводят на фонеагрессивной антитромбоцитарной терапии[142,223,224]. Однако применение двух или трехантитромбоцитарных препаратов рассматривают толь-ко как относительное противопоказание к раннемуКШ, хотя в таких случаях во время операции следуетпринять меры, чтобы свести к минимуму риск крово-течения. Если неотложную операцию проводят до за-вершения отмывочного периода тиенопиридинов, тодля профилактики кровотечений рекомендуется выпол-нять КШ в режиме off-pump или свести к минимуму ис-кусственное кровообращение, а также использоватьтрансфузию тромбоцитарной массы.
5.4.5. Техника чрескожного коронарного вмешательстваРезультаты ЧКВ у пациентов с ОКС без стойкогоподъема сегмента ST значительно улучшились на фонестентирования коронарных артерий и применения со-временных антитромботических и антитромбоцитар-ных препаратов. Имплантация стента во время ЧКВ поз-воляет уменьшить угрозу внезапной окклюзии и ресте-ноза. Безопасность и эффективность стентов, выделяю-щих лекарства, в проспективных исследованиях в этойпопуляции пациентов специально не изучались, хотя вбольшинстве исследований, в которых изучались ре-зультаты ЧКВ, доля пациентов, недавно перенесших ОКСбез подъема сегмента ST, достигала 50%. Учитывая ак-тивацию тромбоцитов и воспалительные изменения упациентов с ОКС, результаты имплантации стентов, вы-деляющих лекарства, могут отличаться от таковых у ста-бильных пациентов. Однако в рандомизированном ис-следовании HORIZONS AMI, в котором сравнивалистенты, выделяющие лекарства, и голометаллическиестенты у пациентов с ИМ с подъемом сегмента ST, небыло выявлено каких-либо проблем с точки зрения без-опасности, в то время как после имплантации стентовс лекарственным покрытием было отмечено снижениечастоты рестеноза и внеплановых повторных реваску-ляризаций [225]. В связи с отсутствием рандомизиро-ванных исследований у больных с ОКС без подъема сег-мента ST выбирать тип стента следует на основании ин-дивидуальной оценки возможных пользы и риска[226]. Двойную антитромбоцитарную терапию следу-ет продолжать в течение 12 мес независимо от типа стен-та. При наличии обязательных показаний к длительнойантикоагуляции возможны имплантация голометалли-ческого стента, только баллонная ангиопластика или КШ,чтобы сократить длительность тройной терапии до 1 мес.При ИМ без подъема сегмента ST возможна аспира-ционная тромбоэктомия, однако ее пользу не изучалив проспективных рандомизированных исследованияху пациентов с ОКС без подъема сегмента ST [227]. Остается неясным, следует ли проводить вмешательства надругих умеренно суженных сегментах коронарных ар-терий при наличии уязвимых бляшек.
Рекомендации по инвазивному обследованию и реваскуляризации
В целом, сроки ангиографии и реваскуляризации вы-бирают с учетом профиля риска пациентов. Пациентамс очень высоким риском (см. выше) показана не-отложная коронарная ангиография (<2 ч). У пациен-тов с высоким риском (индекс GRACE>140 и наличиепо крайней мере одного фактора высокого риска) об-основанна ранняя инвазивная стратегия в течениепервых 24 ч. Эта стратегия предполагает перевод па-циентов в лечебные учреждения, в которых может бытьвыполнена катетеризация. У пациентов с более низкимриском, у которых индекс GRACE составляет ≤140, од-нако, имеется по крайней мере один критерий высо-кого риска (табл. 9), инвазивное обследование можетбыть отложено, однако его следует провести во времягоспитализации, предпочтительно в течение 72 ч послепоступления. В таких случаях немедленный перевод па-циента не требуется, однако его следует организоватьв течение 72 ч (например, у пациентов с диабетом). Па-циентам с низким риском, у которых отсутствуют симп-томы ишемии, необходимо провести неинвазивнуюстресс-пробу перед выпиской. Если определяется об-ратимая ишемия миокарда, показана коронарная ан-гиография.
Чрескожное коронарное вмешательство
или коронарное шунтированиеВ рандомизированных контролируемых исследова-ниях ЧКВ и КШ у пациентов с ОКС без подъема сегмен-та ST специально не сравнивали. Во всех исследованиях,в которых сравнивали раннее или позднее лечение, атакже инвазивное или консервативное ведение, реше-ние о выборе вмешательства (КШ или ЧКВ) принима-ли исследователи.У стабильных пациентов, перенесших ОКС, метод ре-васкуляризации выбирают так же, как при стабильнойИБС [148]. Примерно у трети пациентов при ангиогра-фии выявляют стеноз одной коронарной артерии, чтопозволяет в большинстве случаев выполнить ЧКВ. У по-ловины пациентов наблюдается поражение несколькихкоронарных артерий [181,182]. В таких случаях выбратьтип вмешательства сложнее (ЧКВ на артерии, пораже-ние которой было причиной ОКС, ЧКВ на несколькихсосудах, КШ или комбинированная (гибридная) ревас-куляризация). Стратегию реваскуляризации выбираютс учетом клинического состояния, тяжести и распростра-ненности коронарного атеросклероза и особенностейатеросклеротической бляшки.У большинства пациентов с поражением несколькихартерий обычно начинают с ЧКВ на артерии, пораже-ние которой было причиной развития ОКС. Этот под-ход не сравнивали со стентированием нескольких со-судов в рандомизированных исследованиях. Однако прианализе крупной базы данных, включающей в себя105 866 пациентов с ОКС без подъема сегмента ST, у ко-торых имелось поражение нескольких коронарных ар-терий, были сопоставлены результаты ЧКВ на несколь-ких и одном сосуде [216]. Вмешательство на несколькихартериях реже было успешным, однако госпитальная ле-тальность и частота осложнений были сопоставимыми,хотя результаты длительного наблюдения отсутствуют.КШ сравнивали с ЧКВ у пациентов с поражениемнескольких коронарных артерий, которые быливключены в исследование ACUITY [217]. У пациентов,которым проводили ЧКВ, была ниже частота инсуль-та, ИМ, кровотечений и повреждения почек. Смерт-ность через 1 мес и 1 год была сходной в двух груп-пах, однако через 1 мес и 1 год после ЧКВ выявили значительное увеличение частоты внеплановой ревас-куляризации. Однако только 43% пациентов, перенес-ших КШ, были сопоставимы с пациентами группы ЧКВ.Кроме того, через 1 год выявили тенденцию к увеличе-нию риска основных сердечно-сосудистых событийпосле ЧКВ по сравнению с КШ (25,0% и 19,5%;р=0,05). Полученные данные согласуются с резуль-татами исследования SYNTAX, в котором 28,5% па-циентов перенесли ОКС [218]. Однако субанализэтих пациентов не проводился.В каждом лечебном учреждении необходимо иметьпротокол ведения пациентов, разработанный на осно-вании индекса SYNTAX. При этом следует выделить ана-томические и клинические критерии, позволяющиеопределить возможность выполнения ЧКВ после ангио-графии или целесообразность направления пациентана КШ [219]. После стентирования основного поражен-ного сосуда у пациентов с индексами SYNTAX, находя-щимися в двух верхних терцилях, следует оценить функ-циональное значение поражения других сосудов сучетом сопутствующих заболеваний и индивидуальныхособенностей пациента.
Коронарное шунтирование
Доля пациентов с ОКС без подъема сегмента ST, ко-торым проводится КШ во время первичной госпитали-зации, составляет около 10% [220]. Польза ЧКВ у та-ких пациентов отражает ранние сроки вмешательства,в то время как КШ дает наиболее выраженный эффект,если пациентов оперируют через несколько дней послестабилизации их состояния в зависимости от индиви-дуального риска. Результаты раннего и отсроченного КШв рандомизированном исследовании не сравнивали,поэтому после ЧКВ на основном пораженном сосуде упациентов с тяжелым коронарным атеросклерозомрекомендуется выждать 48-72 ч. По данным анализабольшого числа пациентов, госпитализированных с ОКС,раннее КШ, даже у пациентов с более высоким риском,сопровождалось очень низкой госпитальной смерт-ностью [221]. В регистрах CRUSADE и ACTION не быловыявлено достоверной разницы исходов у пациентов,которым КШ в проводили в течение ≤48 ч или >48 ч,хотя операцию чаще откладывали у пациентов с болеевысоким риском [222]. У пациентов, которым плани-руется КШ, сроки операции следует выбирать индиви-дуально с учетом симптомов, состояния гемодинами-ки, анатомии коронарных артерий, наличия ишемии ирезерва кровотока. Если сохраняется или рецидивиру-ет ишемия, имеются желудочковые аритмии или неста-бильность гемодинамики, КШ следует выполнить не-медленно. У пациентов со стенозом ствола левой коро-нарной артерии или стенозом трех коронарных арте-рий, включая проксимальную часть левой передней нис-ходящей артерии, операцию необходимо провестиво время первичной госпитализации. При принятии ре-шения следует учитывать риск геморрагических ослож-нений у пациентов, которым КШ проводят на фонеагрессивной антитромбоцитарной терапии[142,223,224]. Однако применение двух или трехантитромбоцитарных препаратов рассматривают толь-ко как относительное противопоказание к раннемуКШ, хотя в таких случаях во время операции следуетпринять меры, чтобы свести к минимуму риск крово-течения. Если неотложную операцию проводят до за-вершения отмывочного периода тиенопиридинов, тодля профилактики кровотечений рекомендуется выпол-нять КШ в режиме off-pump или свести к минимуму ис-кусственное кровообращение, а также использоватьтрансфузию тромбоцитарной массы.
5.4.5. Техника чрескожного коронарного вмешательстваРезультаты ЧКВ у пациентов с ОКС без стойкогоподъема сегмента ST значительно улучшились на фонестентирования коронарных артерий и применения со-временных антитромботических и антитромбоцитар-ных препаратов. Имплантация стента во время ЧКВ поз-воляет уменьшить угрозу внезапной окклюзии и ресте-ноза. Безопасность и эффективность стентов, выделяю-щих лекарства, в проспективных исследованиях в этойпопуляции пациентов специально не изучались, хотя вбольшинстве исследований, в которых изучались ре-зультаты ЧКВ, доля пациентов, недавно перенесших ОКСбез подъема сегмента ST, достигала 50%. Учитывая ак-тивацию тромбоцитов и воспалительные изменения упациентов с ОКС, результаты имплантации стентов, вы-деляющих лекарства, могут отличаться от таковых у ста-бильных пациентов. Однако в рандомизированном ис-следовании HORIZONS AMI, в котором сравнивалистенты, выделяющие лекарства, и голометаллическиестенты у пациентов с ИМ с подъемом сегмента ST, небыло выявлено каких-либо проблем с точки зрения без-опасности, в то время как после имплантации стентовс лекарственным покрытием было отмечено снижениечастоты рестеноза и внеплановых повторных реваску-ляризаций [225]. В связи с отсутствием рандомизиро-ванных исследований у больных с ОКС без подъема сег-мента ST выбирать тип стента следует на основании ин-дивидуальной оценки возможных пользы и риска[226]. Двойную антитромбоцитарную терапию следу-ет продолжать в течение 12 мес независимо от типа стен-та. При наличии обязательных показаний к длительнойантикоагуляции возможны имплантация голометалли-ческого стента, только баллонная ангиопластика или КШ,чтобы сократить длительность тройной терапии до 1 мес.При ИМ без подъема сегмента ST возможна аспира-ционная тромбоэктомия, однако ее пользу не изучалив проспективных рандомизированных исследованияху пациентов с ОКС без подъема сегмента ST [227]. Остается неясным, следует ли проводить вмешательства надругих умеренно суженных сегментах коронарных ар-терий при наличии уязвимых бляшек.
Рекомендации по инвазивному обследованию и реваскуляризации
 Особые группы и состояния
Пожилые люди
Термином «пожилые» обозначают людей различно-го возраста. Традиционно к этой группе относят людейв возрасте старше 65 лет, хотя на фоне постарения на-селения более правильным было бы считать пожилы-ми людей в возрасте старше 75 или даже 80 лет. Поми-мо хронологического возраста следует учитывать состоя-ние пациента, когнитивные и функциональные расстрой-ства и наличие физической зависимости. В Европейскихрегистрах 27-34% пациентов с ОКС без подъема сег-мента ST были в возрасте старше 75 лет [228,229]. Темне менее, в последних клинических исследованиях доляпожилых людей (старше 75 лет) среди больных с ОКСбез подъема сегмента ST не превышала 20%. Даже еслипожилых людей включали в клинические исследова-ния, то у рандомизированных пациентов сопутствую-щие заболевания встречались реже, чем в обычной кли-нической практике [230]. В связи с этим возможностьэкстраполяции результатов клинических исследованийна всю выборку пожилых людей вызывает сомнения.Диагноз и стратификация риска у пожилых людейУ пожилых людей клинические проявления ОКС безподъема сегмента ST часто атипичные и нередко лег-ко выражены [15]. У пожилых людей с атипичнойклинической картиной ОКС без подъема сегмента ST ве-дущим симптомом является одышка, в то время как об-мороки, недомогание и дезориентация встречаютсяреже. На ЭКГ реже отмечают выраженные отклонениясегмента ST. У пожилых людей ОКС без подъема сегмен-та ST развивается чаще, чем ИМ с подъемом сегментаST. Одним из основных предикторов риска у пациентовс ОКС без подъема сегмента ST является возраст [50].У пациентов в возрасте старше 75 лет риск смерти покрайней мере в 2 раза выше, чем у пациентов в возрас-те до 75 лет. Частота осложнений ОКС, в том числе сер-дечной недостаточности, кровотечения, инсульта, по-чечной недостаточности и инфекций, значительно уве-личивается с возрастом.Терапевтические аспектыУ пожилых людей выше риск побочных эффектов ме-дикаментозной терапии. В частности это касается рис-ка кровотечений при лечении антитромбоцитарнымипрепаратами и антикоагулянтами, а также гипотонии,брадикардии и почечной недостаточности. Помимо бо-лее высокого риска кровотечений, характерного для по-жилых людей, у таких пациентов часто оказываютсячрезмерными дозы антитромботических препаратов,которые выводятся почками [231].У пожилых людей значительно увеличивается рискбольших кровотечений при лечении нефракциониро-ванным гепарином, эноксапарином, блокаторамиGP IIb/IIIa и P2Y12 рецепторов. В исследованииSYNERGY у пациентов в возрасте старше 75 лет не быловыявлено разницы частоты смерти или ИМ в течение30 дн, смертности в течение 30 дн и 1 года между груп-пами НФГ и эноксапарина. Однако частота больших кро-вотечений в соответствии с критериями TIMI и тяжелых кровотечений в соответствии с критериями GUSTOбыла значительно выше в группе эноксапарина. В свя-зи с этим следует осторожно применять эноксапарин упожилых людей и подбирать дозу с учетом функции по-чек. У пациентов в возрасте старше 75 лет целесообраз-но снизить дозу до 1 мг/кг один раз в день и монито-рировать анти-Ха активность [232]. В исследованииOASIS-5 риск кровотечений у пациентов в возрасте стар-ше 65 лет при лечении фондапаринуксом был значи-тельно ниже, чем при применении эноксапарина [175].У пожилых людей значительно ниже вероятность ин-вазивного лечения ОКС без подъема сегмента ST. Од-нако результаты отдельных исследований свидетель-ствуют о том, что польза инвазивной стратегии в основ-ном отмечается у пациентов в возрасте старше 65 лет[233,234]. По данным субанализа исследованияTACTICS-TIMI 18, у пациентов в возрасте старше 75 летс ОКС без подъема сегмента ST было отмечено наибо-лее значительное снижение относительного и абсолют-ного риска неблагоприятных исходов ценой увеличе-ния риска больших кровотечений и потребности втрансфузиях [235]. Это было недавно подтверждено примета-анализе [209].Тактику ведения пожилого пациента следует выби-рать индивидуально с учетом риска ишемическихосложнений и кровотечений, расчетной ожидаемой про-должительности жизни, сопутствующих заболеваний,качества жизни, желания пациента и расчетного рис-ка и пользы реваскуляризации.
Пол
Женщины с ОКС без подъема сегмента ST старшемужчин и чаще страдают сахарным диабетом, артери-альной гипертонией, сердечной недостаточностью и дру-гими сопутствующими заболеваниями [236-238]. У нихчаще отмечают атипичные проявления, включая одыш-ку и сердечную недостаточность [228,239]. Несмотряна разницу исходного риска, у женщин и мужчин с ОКСбез подъема сегмента ST прогноз сопоставимый, хотяв пожилом возрасте у женщин прогноз лучше, чем умужчин. Это может объясняться более высокой часто-той необструктивного коронарного атеросклероза, ко-торый обнаруживают при ангиографии у женщин[238]. С другой стороны, у женщин с ОКС без подъемасегмента ST риск кровотечений выше, чем у мужчин.Терапевтические аспектыХотя эффективность большинства лекарственныхсредств не зависела от пола, женщинам с ОКС безподъема сегмента по сравнению с мужчинами реже про-водят адекватное лечение, включая инвазивные диаг-ностические вмешательства и реваскуляризацию коро-нарных артерий [236,237,240]. Результаты изучениявлияния пола на эффективность инвазивной стратегиилечения ОКС без подъема сегмента ST оказались про-тиворечивыми. Хотя наблюдательные исследованиясвидетельствуют об улучшении отдаленного прогноза нафоне раннего инвазивного лечения у женщин, примета-анализе было показано, что инвазивные стратегиидают положительный эффект только у мужчин, в то вре-мя как у женщин какой-либо пользы в течение 1 года вы-явлено не было [241]. Более того, в ряде рандомизиро-ванных исследований [233,242] было выявлено увеличе-ние частоты смерти и нефатального ИМ у женщин с ОКСбез подъема сегмента ST, которым проводили раннее ин-вазивное лечение. В исследовании FRISC-2 в течение5 лет было выявлено достоверное взаимодействиемежду результатами лечения и полом. Инвазивнаястратегия привела к значительному снижению смертно-сти и частоты ИМ у мужчин, но не у женщин [234].При мета-анализе, выполненном экспертами CochraneCollaboration, было выявлено значительное снижениериска смерти или ИМ на фоне инвазивной стратегиилечения у женщин (ОР 0,73; 95% ДИ 0,59–0,91), хотяоно сопровождалось увеличением риска неблагопри-ятных исходов на раннем этапе [243]. Некоторые иссле-дования свидетельствуют о том, что ранняя инвазивнаястратегия оправданна только у женщин с высоким рис-ком, например с повышенным уровнем тропонина[244] или поражением нескольких коронарных артерий.Сходные данные были получены при изучении блока-торов GP IIb/IIIa у женщин [245]. В когорте из 35 128 па-циентов, которым проводили ангиографию в 11 иссле-дованиях, 30-дневная смертность с поправкой на тяжестьангиографических изменений достоверно не отличаласьот таковой у мужчин независимо от типа ОКС. Различия 30-дневной смертности, связанные с полом, у пациен-тов с ОКС значительно уменьшались после внесения по-правки на исходные показатели, ангиографическиеданные и стратегию лечения [246].Таким образом, имеющиеся данные свидетель-ствуют о том, что раннюю инвазивную стратегию сле-дует обсуждать у женщин на основании тех же принци-пов, что и у мужчин, т.е. тщательно взвешивая риск ише-мических исходов и кровотечений, включая клиниче-ское состояние и ЭКГ, уровни биомаркеров, сопутствую-щие заболевания и индексы риска.
Рекомендации по лечению пожилых людей
Особые группы и состояния
Пожилые люди
Термином «пожилые» обозначают людей различно-го возраста. Традиционно к этой группе относят людейв возрасте старше 65 лет, хотя на фоне постарения на-селения более правильным было бы считать пожилы-ми людей в возрасте старше 75 или даже 80 лет. Поми-мо хронологического возраста следует учитывать состоя-ние пациента, когнитивные и функциональные расстрой-ства и наличие физической зависимости. В Европейскихрегистрах 27-34% пациентов с ОКС без подъема сег-мента ST были в возрасте старше 75 лет [228,229]. Темне менее, в последних клинических исследованиях доляпожилых людей (старше 75 лет) среди больных с ОКСбез подъема сегмента ST не превышала 20%. Даже еслипожилых людей включали в клинические исследова-ния, то у рандомизированных пациентов сопутствую-щие заболевания встречались реже, чем в обычной кли-нической практике [230]. В связи с этим возможностьэкстраполяции результатов клинических исследованийна всю выборку пожилых людей вызывает сомнения.Диагноз и стратификация риска у пожилых людейУ пожилых людей клинические проявления ОКС безподъема сегмента ST часто атипичные и нередко лег-ко выражены [15]. У пожилых людей с атипичнойклинической картиной ОКС без подъема сегмента ST ве-дущим симптомом является одышка, в то время как об-мороки, недомогание и дезориентация встречаютсяреже. На ЭКГ реже отмечают выраженные отклонениясегмента ST. У пожилых людей ОКС без подъема сегмен-та ST развивается чаще, чем ИМ с подъемом сегментаST. Одним из основных предикторов риска у пациентовс ОКС без подъема сегмента ST является возраст [50].У пациентов в возрасте старше 75 лет риск смерти покрайней мере в 2 раза выше, чем у пациентов в возрас-те до 75 лет. Частота осложнений ОКС, в том числе сер-дечной недостаточности, кровотечения, инсульта, по-чечной недостаточности и инфекций, значительно уве-личивается с возрастом.Терапевтические аспектыУ пожилых людей выше риск побочных эффектов ме-дикаментозной терапии. В частности это касается рис-ка кровотечений при лечении антитромбоцитарнымипрепаратами и антикоагулянтами, а также гипотонии,брадикардии и почечной недостаточности. Помимо бо-лее высокого риска кровотечений, характерного для по-жилых людей, у таких пациентов часто оказываютсячрезмерными дозы антитромботических препаратов,которые выводятся почками [231].У пожилых людей значительно увеличивается рискбольших кровотечений при лечении нефракциониро-ванным гепарином, эноксапарином, блокаторамиGP IIb/IIIa и P2Y12 рецепторов. В исследованииSYNERGY у пациентов в возрасте старше 75 лет не быловыявлено разницы частоты смерти или ИМ в течение30 дн, смертности в течение 30 дн и 1 года между груп-пами НФГ и эноксапарина. Однако частота больших кро-вотечений в соответствии с критериями TIMI и тяжелых кровотечений в соответствии с критериями GUSTOбыла значительно выше в группе эноксапарина. В свя-зи с этим следует осторожно применять эноксапарин упожилых людей и подбирать дозу с учетом функции по-чек. У пациентов в возрасте старше 75 лет целесообраз-но снизить дозу до 1 мг/кг один раз в день и монито-рировать анти-Ха активность [232]. В исследованииOASIS-5 риск кровотечений у пациентов в возрасте стар-ше 65 лет при лечении фондапаринуксом был значи-тельно ниже, чем при применении эноксапарина [175].У пожилых людей значительно ниже вероятность ин-вазивного лечения ОКС без подъема сегмента ST. Од-нако результаты отдельных исследований свидетель-ствуют о том, что польза инвазивной стратегии в основ-ном отмечается у пациентов в возрасте старше 65 лет[233,234]. По данным субанализа исследованияTACTICS-TIMI 18, у пациентов в возрасте старше 75 летс ОКС без подъема сегмента ST было отмечено наибо-лее значительное снижение относительного и абсолют-ного риска неблагоприятных исходов ценой увеличе-ния риска больших кровотечений и потребности втрансфузиях [235]. Это было недавно подтверждено примета-анализе [209].Тактику ведения пожилого пациента следует выби-рать индивидуально с учетом риска ишемическихосложнений и кровотечений, расчетной ожидаемой про-должительности жизни, сопутствующих заболеваний,качества жизни, желания пациента и расчетного рис-ка и пользы реваскуляризации.
Пол
Женщины с ОКС без подъема сегмента ST старшемужчин и чаще страдают сахарным диабетом, артери-альной гипертонией, сердечной недостаточностью и дру-гими сопутствующими заболеваниями [236-238]. У нихчаще отмечают атипичные проявления, включая одыш-ку и сердечную недостаточность [228,239]. Несмотряна разницу исходного риска, у женщин и мужчин с ОКСбез подъема сегмента ST прогноз сопоставимый, хотяв пожилом возрасте у женщин прогноз лучше, чем умужчин. Это может объясняться более высокой часто-той необструктивного коронарного атеросклероза, ко-торый обнаруживают при ангиографии у женщин[238]. С другой стороны, у женщин с ОКС без подъемасегмента ST риск кровотечений выше, чем у мужчин.Терапевтические аспектыХотя эффективность большинства лекарственныхсредств не зависела от пола, женщинам с ОКС безподъема сегмента по сравнению с мужчинами реже про-водят адекватное лечение, включая инвазивные диаг-ностические вмешательства и реваскуляризацию коро-нарных артерий [236,237,240]. Результаты изучениявлияния пола на эффективность инвазивной стратегиилечения ОКС без подъема сегмента ST оказались про-тиворечивыми. Хотя наблюдательные исследованиясвидетельствуют об улучшении отдаленного прогноза нафоне раннего инвазивного лечения у женщин, примета-анализе было показано, что инвазивные стратегиидают положительный эффект только у мужчин, в то вре-мя как у женщин какой-либо пользы в течение 1 года вы-явлено не было [241]. Более того, в ряде рандомизиро-ванных исследований [233,242] было выявлено увеличе-ние частоты смерти и нефатального ИМ у женщин с ОКСбез подъема сегмента ST, которым проводили раннее ин-вазивное лечение. В исследовании FRISC-2 в течение5 лет было выявлено достоверное взаимодействиемежду результатами лечения и полом. Инвазивнаястратегия привела к значительному снижению смертно-сти и частоты ИМ у мужчин, но не у женщин [234].При мета-анализе, выполненном экспертами CochraneCollaboration, было выявлено значительное снижениериска смерти или ИМ на фоне инвазивной стратегиилечения у женщин (ОР 0,73; 95% ДИ 0,59–0,91), хотяоно сопровождалось увеличением риска неблагопри-ятных исходов на раннем этапе [243]. Некоторые иссле-дования свидетельствуют о том, что ранняя инвазивнаястратегия оправданна только у женщин с высоким рис-ком, например с повышенным уровнем тропонина[244] или поражением нескольких коронарных артерий.Сходные данные были получены при изучении блока-торов GP IIb/IIIa у женщин [245]. В когорте из 35 128 па-циентов, которым проводили ангиографию в 11 иссле-дованиях, 30-дневная смертность с поправкой на тяжестьангиографических изменений достоверно не отличаласьот таковой у мужчин независимо от типа ОКС. Различия 30-дневной смертности, связанные с полом, у пациен-тов с ОКС значительно уменьшались после внесения по-правки на исходные показатели, ангиографическиеданные и стратегию лечения [246].Таким образом, имеющиеся данные свидетель-ствуют о том, что раннюю инвазивную стратегию сле-дует обсуждать у женщин на основании тех же принци-пов, что и у мужчин, т.е. тщательно взвешивая риск ише-мических исходов и кровотечений, включая клиниче-ское состояние и ЭКГ, уровни биомаркеров, сопутствую-щие заболевания и индексы риска.
Рекомендации по лечению пожилых людей
 Рекомендации по лечению пациентов различного пола
Рекомендации по лечению пациентов различного пола
 5.5.3. Сахарный диабетПримерно 20-30% больных с ОКС без подъема сег-мента ST страдают сахарным диабетом. По крайней мере,у такого же процента пациентов имеются недиагности-рованный диабет или нарушение толерантности к глю-козе [247]. В исследовании Euro Heart Survey установ-ленный или вновь выявленный сахарный диабет имел-ся у 37% пациентов с ОКС без подъема сегмента ST [248].Пациенты с сахарным диабетом в целом старше, чащеявляются женщинами и чаще страдают сопутствующи-ми заболеваниями, такими как гипертония и почечнаянедостаточность. У них выше вероятность появления ати-пичных симптомов и развития осложнений, особенносердечной недостаточности и кровотечений [248].Сахарный диабет — это независимый предикторсмерти больных с ОКС без подъема сегмента ST. Рисксмерти у больных диабетом повышен в 2 раза [249,250].Кроме того, у пациентов с нарушением толерантностик глюкозе или нарушенной гликемией натощак прогнозхуже, чем у пациентов с нормальным метаболизмомглюкозы, однако лучше, чем у больных подтвержден-ным диабетом.Гипергликемия при поступлении или во время гос-питализации — это независимый неблагоприятныйпрогностический фактор при ОКС независимо от нали-чия сахарного диабета. Она может иметь даже большеенеблагоприятное прогностическое значение, чем уста-новленный диагноз диабета [251].Терапевтические аспектыРегистры показали, что у больных с ОКС без подъе-ма сегмента ST, сочетающимся с диабетом, выше рисксердечно-сосудистых исходов в ближайшем и отдален-ном периодах. При этом они получают субоптимальноелечение по сравнению с пациентами без диабета. В Ев-ропейских регистрах частота реваскуляризации (любо-го типа), применения тиенопиридинов и блокаторовGP IIb/IIIa рецепторов у больных диабетом была ниже,чем у пациентов без диабета, что сопровождалось чет-ким ухудшением госпитальной и отдаленной смертно-сти (5,9% и 3,2% через 1 мес и 15,2% и 7,6% через1 г). Кроме того, больным диабетом реперфузию илиреваскуляризацию проводят реже, чем у пациентам бездиабета [248,250].Пациенты с диабетом относятся к группе высокогориска, поэтому они нуждаются в более агрессивном ме-дикаментозном, а также инвазивном лечении. Крометого, им необходима адекватная вторичная профилак-тика, включающая медикаментозную терапию и моди-фикацию образа жизни [252].Результаты изучения эффективности жесткого конт-роля гликемии у пациентов с ИМ неоднозначные[251]. У пациентов с ИМ с подъемом сегмента STжесткий контроль гликемии путем внутривенного вве-дения инсулина в исследовании DIGAMI привел кснижению смертности в течение 1 года на 30%, одна-ко этот эффект не был подтвержден в исследованииDIGAMI-2. В последних исследованиях у стабильных па-циентов с диабетом, а также больных, находившихсяв отделениях интенсивной терапии, было выявлено улуч-шение исходов на фоне жесткого контроля гликемии,хотя он сопровождался увеличением частоты гипогли-кемических состояний [253]. Пока не будут полученыдополнительные данные, при сахароснижающей тера-пии следует добиваться отсутствия выраженной гипер-гликемии (>10-11 ммоль/л [180-200 мг/дл]), а так-же гипогликемии (<5 ммоль/л [90 мг/дл]). Эффектив-ность смеси глюкоза-инсулин-калий в профилактике ис-ходов не доказана; более того, она может даже даватьнежелательный эффект [254].Реваскуляризация у больных сахарным диабетом со-провождается особыми проблемами. У таких пациен-тов коронарный атеросклероз обычно диффузный и рас-пространенный и отмечается более высокая частота ре-стеноза, а также окклюзии после ЧКВ и КШ. После ЧКВповторную реваскуляризацию приходится проводитьчаще, чем после КШ. В этой группе пациентов с высо-ким риском установлена эффективность ранней инва-зивной стратегии, польза которой была более значитель-ной, чем у пациентов без диабета [255].У пациентов с сахарным диабетом и стенозом не-скольких сосудов КШ улучшало исходы по сравнениюс ЧКВ. По данным мета-анализа 7 812 пациентов, при-нимавших участие в 10 рандомизированных исследо-ваниях, смертность после КШ в течение 5,9 лет при на-личии сахарного диабета была значительно ниже, чемпосле ЧКВ [256]. В целом смертность в группах КШ иЧКВ не отличалась (15% и 16%; отношение рисков0,91; 95% ДИ 0,82–1,02; p=0,12), однако у 1 233 па-циентов было выявлено достоверное снижение смерт-ности после КШ [23% и 29%; отношение рисков 0,70; 95% 0,56–0,87; p=0,05; число больных, которых не-обходимо пролечить (NNT)=17]. В исследованииBARI-2D рандомизировали больных сахарным диабе-том и стабильной стенокардией, которым проводилиинтенсивную медикаментозную терапию или интенсив-ную медикаментозную терапию в сочетании с КШ илиЧКВ (по выбору врача). В течение 5 лет у пациентов, пе-ренесших КШ, по сравнению с группой больных, полу-чавших консервативную терапию, выявили снижениериска смерти и ИМ (21,1% и 29,2%; p<0,010), а так-же частоты сердечной смерти или ИМ (15,8% и 21,9%;p<0,03) и ИМ (10% и 17,6%; p<0,003). У пациентов,которым проводили ЧКВ, частота сердечно-сосудистыхисходов достоверно не отличалась от таковой на фонеконсервативной терапии [257,258]. В исследованииSYNTAX, в котором сравнивали результаты КШ и стен-тирования (применяли стенты, выделяющие лекарст-ва) у пациентов со стенозом ствола левой коронарнойартерии и нескольких коронарных артерий, разница ча-стоты нежелательных исходов в течение 1 года междугруппами КШ и ЧКВ удваивалась у пациентов с сахар-ным диабетом, в основном за счет повторной реваску-ляризации [259]. Однако достоверной разницы смерт-ности или частоты ИМ не выявили. И наконец, в NewYork Registry у пациентов с сахарным диабетом была вы-явлена тенденция к улучшению исходов после КШ посравнению с имплантацией стента, выделяющего ле-карства (ОШ смерти или ИМ в течение 18 мес 0,84; 95%ДИ 0,69–1,01) [260].Все эти исследования свидетельствуют о том, что КШимеет преимущества перед ЧКВ у больных сахарнымдиабетом. Однако следует отметить, что в большинствоперечисленных исследований включали только стабиль-ных пациентов с хронической ИБС, поэтому остается не-ясным, можно ли экстраполировать полученные дан-ные на пациентов с ОКС без подъема сегмента ST.По данным мета-анализа, имплантация стентов, вы-деляющих лекарства, по безопасности не уступалаимплантации голометаллических стентов, если двой-ную антитромбоцитарную терапию продолжали в тече-ние более 6 мес (подобная терапия в любом случае по-казана пациентам с ОКС) [261]. После установки стен-та, выделяющего лекарства, выявили значительноеснижение частоты повторной реваскуляризации целе-вого сосуда (ОШ 0,29 для стентов, выделяющих сиро-лимус и 0,38 — для стентов, выделяющих паклитаксел).Можно предположить, что у больных сахарным диабе-том будут получены сходные данные. Неконтролируе-мые исследования свидетельствуют о том, что артери-альные шунты имеют преимущества перед венозными.Влияние билатерального артериального шунтированияна риск отдаленных исходов и медиастинальных инфек-ций продолжает дискутироваться. У пациентов с ОКСспециальные исследования не проводились.Данных в пользу модификации схемы антитромбо-тической терапии у пациентов с сахарным диабетом нет.Однако в исследовании TRITON-TIMI 38 прасугрелпревосходил клопидогрел по эффективности в профи-лактике сердечно-сосудистой смерти, ИМ или инсуль-та и не вызывал увеличение риска кровотечений [262].В исследовании PLATO лечение тикагрелором посравнению с клопидогрелом привело к снижению ча-стоты ишемических исходов у пациентов с ОКС неза-висимо от наличия сахарного диабета и контроля гли-кемии и не сопровождалось увеличением частотыбольших кровотечений [263]. Применение тикагрело-ра привело к снижению общей смертности у пациен-тов с уровнем гемоглобина A1c выше медианы (>6%).Хотя при первом мета-анализе было установленоблагоприятное влияние блокаторов GP IIb/IIIa рецеп-торов (без сопутствующей терапии тиенопиридинами)на исходы у пациентов с сахарным диабетом [264], поль-за их широкого применения не была подтверждена висследовании EARLY-ACS [151]. Следовательно, нафоне современной терапии пероральными антитром-боцитарными препаратами дополнительно назначатьблокаторы GP IIb/IIIa рецепторов больным сахарнымдиабетом, по-видимому, не следует. У больных сахарным диабетом, которым проводят-ся ангиография и/или ЧКВ особое значение имеет про-филактика контрастной нефропатии.Откладывать ангиографию у пациентов, получающихметформин, не следует, так как риск развития лакта-цидоза минимальный [265]. После введения контраст-ных агентов следует тщательно контролировать функ-цию почек.
Рекомендации по лечению больных сахарным диабетом
5.5.3. Сахарный диабетПримерно 20-30% больных с ОКС без подъема сег-мента ST страдают сахарным диабетом. По крайней мере,у такого же процента пациентов имеются недиагности-рованный диабет или нарушение толерантности к глю-козе [247]. В исследовании Euro Heart Survey установ-ленный или вновь выявленный сахарный диабет имел-ся у 37% пациентов с ОКС без подъема сегмента ST [248].Пациенты с сахарным диабетом в целом старше, чащеявляются женщинами и чаще страдают сопутствующи-ми заболеваниями, такими как гипертония и почечнаянедостаточность. У них выше вероятность появления ати-пичных симптомов и развития осложнений, особенносердечной недостаточности и кровотечений [248].Сахарный диабет — это независимый предикторсмерти больных с ОКС без подъема сегмента ST. Рисксмерти у больных диабетом повышен в 2 раза [249,250].Кроме того, у пациентов с нарушением толерантностик глюкозе или нарушенной гликемией натощак прогнозхуже, чем у пациентов с нормальным метаболизмомглюкозы, однако лучше, чем у больных подтвержден-ным диабетом.Гипергликемия при поступлении или во время гос-питализации — это независимый неблагоприятныйпрогностический фактор при ОКС независимо от нали-чия сахарного диабета. Она может иметь даже большеенеблагоприятное прогностическое значение, чем уста-новленный диагноз диабета [251].Терапевтические аспектыРегистры показали, что у больных с ОКС без подъе-ма сегмента ST, сочетающимся с диабетом, выше рисксердечно-сосудистых исходов в ближайшем и отдален-ном периодах. При этом они получают субоптимальноелечение по сравнению с пациентами без диабета. В Ев-ропейских регистрах частота реваскуляризации (любо-го типа), применения тиенопиридинов и блокаторовGP IIb/IIIa рецепторов у больных диабетом была ниже,чем у пациентов без диабета, что сопровождалось чет-ким ухудшением госпитальной и отдаленной смертно-сти (5,9% и 3,2% через 1 мес и 15,2% и 7,6% через1 г). Кроме того, больным диабетом реперфузию илиреваскуляризацию проводят реже, чем у пациентам бездиабета [248,250].Пациенты с диабетом относятся к группе высокогориска, поэтому они нуждаются в более агрессивном ме-дикаментозном, а также инвазивном лечении. Крометого, им необходима адекватная вторичная профилак-тика, включающая медикаментозную терапию и моди-фикацию образа жизни [252].Результаты изучения эффективности жесткого конт-роля гликемии у пациентов с ИМ неоднозначные[251]. У пациентов с ИМ с подъемом сегмента STжесткий контроль гликемии путем внутривенного вве-дения инсулина в исследовании DIGAMI привел кснижению смертности в течение 1 года на 30%, одна-ко этот эффект не был подтвержден в исследованииDIGAMI-2. В последних исследованиях у стабильных па-циентов с диабетом, а также больных, находившихсяв отделениях интенсивной терапии, было выявлено улуч-шение исходов на фоне жесткого контроля гликемии,хотя он сопровождался увеличением частоты гипогли-кемических состояний [253]. Пока не будут полученыдополнительные данные, при сахароснижающей тера-пии следует добиваться отсутствия выраженной гипер-гликемии (>10-11 ммоль/л [180-200 мг/дл]), а так-же гипогликемии (<5 ммоль/л [90 мг/дл]). Эффектив-ность смеси глюкоза-инсулин-калий в профилактике ис-ходов не доказана; более того, она может даже даватьнежелательный эффект [254].Реваскуляризация у больных сахарным диабетом со-провождается особыми проблемами. У таких пациен-тов коронарный атеросклероз обычно диффузный и рас-пространенный и отмечается более высокая частота ре-стеноза, а также окклюзии после ЧКВ и КШ. После ЧКВповторную реваскуляризацию приходится проводитьчаще, чем после КШ. В этой группе пациентов с высо-ким риском установлена эффективность ранней инва-зивной стратегии, польза которой была более значитель-ной, чем у пациентов без диабета [255].У пациентов с сахарным диабетом и стенозом не-скольких сосудов КШ улучшало исходы по сравнениюс ЧКВ. По данным мета-анализа 7 812 пациентов, при-нимавших участие в 10 рандомизированных исследо-ваниях, смертность после КШ в течение 5,9 лет при на-личии сахарного диабета была значительно ниже, чемпосле ЧКВ [256]. В целом смертность в группах КШ иЧКВ не отличалась (15% и 16%; отношение рисков0,91; 95% ДИ 0,82–1,02; p=0,12), однако у 1 233 па-циентов было выявлено достоверное снижение смерт-ности после КШ [23% и 29%; отношение рисков 0,70; 95% 0,56–0,87; p=0,05; число больных, которых не-обходимо пролечить (NNT)=17]. В исследованииBARI-2D рандомизировали больных сахарным диабе-том и стабильной стенокардией, которым проводилиинтенсивную медикаментозную терапию или интенсив-ную медикаментозную терапию в сочетании с КШ илиЧКВ (по выбору врача). В течение 5 лет у пациентов, пе-ренесших КШ, по сравнению с группой больных, полу-чавших консервативную терапию, выявили снижениериска смерти и ИМ (21,1% и 29,2%; p<0,010), а так-же частоты сердечной смерти или ИМ (15,8% и 21,9%;p<0,03) и ИМ (10% и 17,6%; p<0,003). У пациентов,которым проводили ЧКВ, частота сердечно-сосудистыхисходов достоверно не отличалась от таковой на фонеконсервативной терапии [257,258]. В исследованииSYNTAX, в котором сравнивали результаты КШ и стен-тирования (применяли стенты, выделяющие лекарст-ва) у пациентов со стенозом ствола левой коронарнойартерии и нескольких коронарных артерий, разница ча-стоты нежелательных исходов в течение 1 года междугруппами КШ и ЧКВ удваивалась у пациентов с сахар-ным диабетом, в основном за счет повторной реваску-ляризации [259]. Однако достоверной разницы смерт-ности или частоты ИМ не выявили. И наконец, в NewYork Registry у пациентов с сахарным диабетом была вы-явлена тенденция к улучшению исходов после КШ посравнению с имплантацией стента, выделяющего ле-карства (ОШ смерти или ИМ в течение 18 мес 0,84; 95%ДИ 0,69–1,01) [260].Все эти исследования свидетельствуют о том, что КШимеет преимущества перед ЧКВ у больных сахарнымдиабетом. Однако следует отметить, что в большинствоперечисленных исследований включали только стабиль-ных пациентов с хронической ИБС, поэтому остается не-ясным, можно ли экстраполировать полученные дан-ные на пациентов с ОКС без подъема сегмента ST.По данным мета-анализа, имплантация стентов, вы-деляющих лекарства, по безопасности не уступалаимплантации голометаллических стентов, если двой-ную антитромбоцитарную терапию продолжали в тече-ние более 6 мес (подобная терапия в любом случае по-казана пациентам с ОКС) [261]. После установки стен-та, выделяющего лекарства, выявили значительноеснижение частоты повторной реваскуляризации целе-вого сосуда (ОШ 0,29 для стентов, выделяющих сиро-лимус и 0,38 — для стентов, выделяющих паклитаксел).Можно предположить, что у больных сахарным диабе-том будут получены сходные данные. Неконтролируе-мые исследования свидетельствуют о том, что артери-альные шунты имеют преимущества перед венозными.Влияние билатерального артериального шунтированияна риск отдаленных исходов и медиастинальных инфек-ций продолжает дискутироваться. У пациентов с ОКСспециальные исследования не проводились.Данных в пользу модификации схемы антитромбо-тической терапии у пациентов с сахарным диабетом нет.Однако в исследовании TRITON-TIMI 38 прасугрелпревосходил клопидогрел по эффективности в профи-лактике сердечно-сосудистой смерти, ИМ или инсуль-та и не вызывал увеличение риска кровотечений [262].В исследовании PLATO лечение тикагрелором посравнению с клопидогрелом привело к снижению ча-стоты ишемических исходов у пациентов с ОКС неза-висимо от наличия сахарного диабета и контроля гли-кемии и не сопровождалось увеличением частотыбольших кровотечений [263]. Применение тикагрело-ра привело к снижению общей смертности у пациен-тов с уровнем гемоглобина A1c выше медианы (>6%).Хотя при первом мета-анализе было установленоблагоприятное влияние блокаторов GP IIb/IIIa рецеп-торов (без сопутствующей терапии тиенопиридинами)на исходы у пациентов с сахарным диабетом [264], поль-за их широкого применения не была подтверждена висследовании EARLY-ACS [151]. Следовательно, нафоне современной терапии пероральными антитром-боцитарными препаратами дополнительно назначатьблокаторы GP IIb/IIIa рецепторов больным сахарнымдиабетом, по-видимому, не следует. У больных сахарным диабетом, которым проводят-ся ангиография и/или ЧКВ особое значение имеет про-филактика контрастной нефропатии.Откладывать ангиографию у пациентов, получающихметформин, не следует, так как риск развития лакта-цидоза минимальный [265]. После введения контраст-ных агентов следует тщательно контролировать функ-цию почек.
Рекомендации по лечению больных сахарным диабетом
 Таблица 10. Рекомендации по применениюантитромботических препаратов при ХБП
Таблица 10. Рекомендации по применениюантитромботических препаратов при ХБП
 Хроническая болезнь почек
Почечная дисфункция имеется у 30-40% пациен-тов с ОКС без подъема сегмента ST [266,267]. Оптималь-ным показателем функции почек является СКФ, кото-рую рассчитают с помощью уравнения MDRD с учетомэтнической принадлежности и пола. СКФ следует рас-считывать у всех пациентов с хронической болезнью по-чек (ХБП) или повышенным риском ее развития. В кли-нической практике можно рассчитывать также клиренскреатинина по формуле Кокрофта-Голта. КритерииХБП см. в предыдущих рекомендациях [3].У пациентов с ХБП часто развивается сердечная не-достаточность и отсутствует типичная боль в груди[268]. Пациенты с ОКС без подъема сегмента ST и ХБПнередко не получают адекватного лечения в соответствиис рекомендациями. ХБП ассоциируется с очень небла-гоприятным прогнозом [266,268] и является незави-симым предиктором смерти в ближайшем и отдален-ном периоде и больших кровотечений у больных с ОКСбез подъема сегмента ST [267].Терапевтические аспектыХотя доля пациентов с ОКС без подъема сегментаST и ХБП в клинических исследованиях была занижен-ной, это не может служить основанием для неадекват-ного лечения. Однако при применении антитромбо-тических препаратов необходимо соблюдать осто-рожность, учитывая риск геморрагических осложне-ний [168,269,270]. Данные регистров свидетель-ствуют о том, что у больных с ХБП часто отмечается пе-редозировка антитромботических препаратов, особен-но антикоагулянтов и блокаторов GP IIb/IIIa рецепто-ров, что повышает риск кровотечений. Многие препа-раты, которые исключительно или в значительнойстепени выводятся почками, следует назначать в по-ниженных дозах, а некоторые из них противопоказа-ны больным с ХБП, в том числе эноксапарин, фонда-паринукс, бивалирудин и низкомолекулярные блока-торы GP IIb/IIIa рецепторов (табл. 10). При тяжелой по-чечной недостаточности, когда противопоказаны фон-дапаринукс и эноксапарин, следует назначать НФГ. Од-нако в регистре GRACE применение НФГ не позволя-ло избежать геморрагических осложнений. При этомбыло отмечено постепенное нарастание риска крово-течений на фоне снижения функции почек, как и прилечении НМГ [269]. Преимущества НФГ перед други-ми антикоагулянтами у больных с ХБП связаны с лег-костью мониторирования антикоагулянтной актив-ности с помощью аЧТВ и возможностью быстрой ней-трализации активности препарата в случае крово-течения. Фондапаринукс по безопасности имел значи-тельные преимущества перед эноксапарином у боль-ных с ХБП. В исследовании OASIS-5 риск кровотече-ний при лечении фондапаринуксом был значительнониже, чем при применении эноксапарина. Тикагрелорв исследовании PLATO значительно снижал риск ише-мических осложнений и смерти по сравнению с кло-пидогрелом и не вызывал значительного увеличениячастоты больших кровотечений, хотя риск кровотече-ний, не связанных с вмешательствами, был недосто-верно выше в группе тикагрелора [271].
Систолическая дисфункция левого желудочкаи сердечная недостаточность
Сердечная недостаточность — это одно из самых ча-стых и тяжелых осложнений ОКС без подъема сегмен-та ST [274], хотя частота ее, по-видимому, снижается [50].Фракция выброса левого желудочка и сердечная недо-статочность — это независимые предикторы смерти идругих серьезных нежелательных исходов у пациентовс ОКС без подъема сегмента ST. Сердечная недостаточ-ность чаще встречается у пожилых людей и ассоцииру-ется с ухудшением прогноза, если нарушение функциисердца определяется при поступлении или во время гос-питализации [274]. У пациентов с сердечной недоста-точностью без боли в груди диагностировать ОКС бы-вает трудно, учитывая повышение уровня тропонинавследствие острой сердечной недостаточности. У такихпациентов иногда невозможно дифференцироватьострую сердечную недостаточность от ОКС без подъе-ма сегмента ST, осложнившегося сердечной недостаточ-ностью. Для дифференциальной диагностики двухсостояний может потребоваться ангиография.Терапевтические аспектыПациенты с ОКС без подъема сегмента ST, осложнив-шегося сердечной недостаточностью, реже получаютадекватное лечение в соответствии с рекомендациями,включая применение бета-адреноблокаторов и инги-биторов АПФ или блокаторов рецепторов ангиотензи-на II, коронарной ангиографии и реваскуляризации[50,274]. Все рекомендации, предложенные на осно-вании исследований у пациентов, перенесших ИМ, мож-но экстраполировать на пациентов с ОКС без подъемасегмента ST, осложнившимся сердечной недостаточ-ностью. Дополнительная информация содержится в со-ответствующих рекомендациях [275].
Низкая или высокая масса тела
Низкая масса тела ассоциируется с повышенным рис-ком смерти или ИМ и особенно кровотечений, которыечасто связаны с неадекватным выбором доз анти-тромботических препаратов [279]. У пациентов с низ-кой массой тела уровень креатинина может быть нормальным, несмотря на наличие почечной недостаточ-ности, особенно у пожилых людей. Нарушение функ-ции почек увеличивает риск токсических и вторичныхэффектов препаратов, которые выводятся почками. Всвязи с этим рекомендуется рассчитывать клиренскреатинина у пациентов с низкой массой тела и соот-ветствующим образом подбирать дозы препаратовдля внутривенного введения.Хотя ожирение сопровождается более высокимриском коронарных осложнений, у пациентов с ожи-рением и ОКС без подъема сегмента ST наблюдается па-радоксальное улучшение исходов во время пребыва-ния в стационаре и в течение 1 года, включая сниже-ние риска кровотечений [279,280]. У пациентов сожирением больше факторов риска, однако они моло-же. Таким пациентам чаще проводят адекватную тера-пию, что позволяет объяснить улучшение исходов[280].
Рекомендации по лечению пациентов с ХБП
Хроническая болезнь почек
Почечная дисфункция имеется у 30-40% пациен-тов с ОКС без подъема сегмента ST [266,267]. Оптималь-ным показателем функции почек является СКФ, кото-рую рассчитают с помощью уравнения MDRD с учетомэтнической принадлежности и пола. СКФ следует рас-считывать у всех пациентов с хронической болезнью по-чек (ХБП) или повышенным риском ее развития. В кли-нической практике можно рассчитывать также клиренскреатинина по формуле Кокрофта-Голта. КритерииХБП см. в предыдущих рекомендациях [3].У пациентов с ХБП часто развивается сердечная не-достаточность и отсутствует типичная боль в груди[268]. Пациенты с ОКС без подъема сегмента ST и ХБПнередко не получают адекватного лечения в соответствиис рекомендациями. ХБП ассоциируется с очень небла-гоприятным прогнозом [266,268] и является незави-симым предиктором смерти в ближайшем и отдален-ном периоде и больших кровотечений у больных с ОКСбез подъема сегмента ST [267].Терапевтические аспектыХотя доля пациентов с ОКС без подъема сегментаST и ХБП в клинических исследованиях была занижен-ной, это не может служить основанием для неадекват-ного лечения. Однако при применении антитромбо-тических препаратов необходимо соблюдать осто-рожность, учитывая риск геморрагических осложне-ний [168,269,270]. Данные регистров свидетель-ствуют о том, что у больных с ХБП часто отмечается пе-редозировка антитромботических препаратов, особен-но антикоагулянтов и блокаторов GP IIb/IIIa рецепто-ров, что повышает риск кровотечений. Многие препа-раты, которые исключительно или в значительнойстепени выводятся почками, следует назначать в по-ниженных дозах, а некоторые из них противопоказа-ны больным с ХБП, в том числе эноксапарин, фонда-паринукс, бивалирудин и низкомолекулярные блока-торы GP IIb/IIIa рецепторов (табл. 10). При тяжелой по-чечной недостаточности, когда противопоказаны фон-дапаринукс и эноксапарин, следует назначать НФГ. Од-нако в регистре GRACE применение НФГ не позволя-ло избежать геморрагических осложнений. При этомбыло отмечено постепенное нарастание риска крово-течений на фоне снижения функции почек, как и прилечении НМГ [269]. Преимущества НФГ перед други-ми антикоагулянтами у больных с ХБП связаны с лег-костью мониторирования антикоагулянтной актив-ности с помощью аЧТВ и возможностью быстрой ней-трализации активности препарата в случае крово-течения. Фондапаринукс по безопасности имел значи-тельные преимущества перед эноксапарином у боль-ных с ХБП. В исследовании OASIS-5 риск кровотече-ний при лечении фондапаринуксом был значительнониже, чем при применении эноксапарина. Тикагрелорв исследовании PLATO значительно снижал риск ише-мических осложнений и смерти по сравнению с кло-пидогрелом и не вызывал значительного увеличениячастоты больших кровотечений, хотя риск кровотече-ний, не связанных с вмешательствами, был недосто-верно выше в группе тикагрелора [271].
Систолическая дисфункция левого желудочкаи сердечная недостаточность
Сердечная недостаточность — это одно из самых ча-стых и тяжелых осложнений ОКС без подъема сегмен-та ST [274], хотя частота ее, по-видимому, снижается [50].Фракция выброса левого желудочка и сердечная недо-статочность — это независимые предикторы смерти идругих серьезных нежелательных исходов у пациентовс ОКС без подъема сегмента ST. Сердечная недостаточ-ность чаще встречается у пожилых людей и ассоцииру-ется с ухудшением прогноза, если нарушение функциисердца определяется при поступлении или во время гос-питализации [274]. У пациентов с сердечной недоста-точностью без боли в груди диагностировать ОКС бы-вает трудно, учитывая повышение уровня тропонинавследствие острой сердечной недостаточности. У такихпациентов иногда невозможно дифференцироватьострую сердечную недостаточность от ОКС без подъе-ма сегмента ST, осложнившегося сердечной недостаточ-ностью. Для дифференциальной диагностики двухсостояний может потребоваться ангиография.Терапевтические аспектыПациенты с ОКС без подъема сегмента ST, осложнив-шегося сердечной недостаточностью, реже получаютадекватное лечение в соответствии с рекомендациями,включая применение бета-адреноблокаторов и инги-биторов АПФ или блокаторов рецепторов ангиотензи-на II, коронарной ангиографии и реваскуляризации[50,274]. Все рекомендации, предложенные на осно-вании исследований у пациентов, перенесших ИМ, мож-но экстраполировать на пациентов с ОКС без подъемасегмента ST, осложнившимся сердечной недостаточ-ностью. Дополнительная информация содержится в со-ответствующих рекомендациях [275].
Низкая или высокая масса тела
Низкая масса тела ассоциируется с повышенным рис-ком смерти или ИМ и особенно кровотечений, которыечасто связаны с неадекватным выбором доз анти-тромботических препаратов [279]. У пациентов с низ-кой массой тела уровень креатинина может быть нормальным, несмотря на наличие почечной недостаточ-ности, особенно у пожилых людей. Нарушение функ-ции почек увеличивает риск токсических и вторичныхэффектов препаратов, которые выводятся почками. Всвязи с этим рекомендуется рассчитывать клиренскреатинина у пациентов с низкой массой тела и соот-ветствующим образом подбирать дозы препаратовдля внутривенного введения.Хотя ожирение сопровождается более высокимриском коронарных осложнений, у пациентов с ожи-рением и ОКС без подъема сегмента ST наблюдается па-радоксальное улучшение исходов во время пребыва-ния в стационаре и в течение 1 года, включая сниже-ние риска кровотечений [279,280]. У пациентов сожирением больше факторов риска, однако они моло-же. Таким пациентам чаще проводят адекватную тера-пию, что позволяет объяснить улучшение исходов[280].
Рекомендации по лечению пациентов с ХБП
 Рекомендации по лечению пациентов с сердечной недостаточностью
Рекомендации по лечению пациентов с сердечной недостаточностью
 Необструктивная коронарная болезнь сердца
У значительной части пациентов (около 15%) с ОКСбез подъема сегмента ST отсутствуют изменения коро-нарных артерий или имеется необструктивный коронар-ный атеросклероз. ОКС без подъема сегмента ST харак-теризуется неоднородным патогенезом, а возможныемеханизмы его развития включают в себя спазм коро-нарной артерии (стенокардия Принцметалла), ост-рый тромбоз на фоне интрамуральной бляшки с после-дующей реканализацией коронарной артерии, эмбо-лии в коронарные артерии и синдром Х. У пациентовс ОКС без подъема сегмента ST наличие неизмененныхили практически неизмененных коронарных артерийпри ангиографии позволяет усомниться в диагнозе. Од-нако изменения сегмента ST и выделение биомаркерову пациентов с типичной болью в груди и проходимы-ми коронарными артериями без выраженного стено-за могут быть следствием истинного некроза, а не от-ражать ложноположительные результаты. ОКС без из-менений коронарных артерий чаще встречается у жен-щин. Выраженные атеросклеротические изменениямогут наблюдаться даже при отсутствии ангиографиче-ского стеноза, так как диффузный атеросклероз приво-дит к ремоделированию стенки артерии. При этом утол-щение стенки сосуда происходит кнаружи, а просвет егоне суживается. Прогноз у таких пациентов более бла-гоприятный, чем при наличии выраженного коронар-ного атеросклероза, поэтому они нуждаются в оптималь-ной антитромботической терапии и вторичной профи-лактике антитромбоцитарными препаратами и стати-нами [281].Вариантная стенокардия Принцметалла часто оста-ется недиагностированной и характеризуется ишеми-ческой болью в груди, которая не связана с физическойнагрузкой или эмоциональным напряжением и сопро-вождается преходящим подъемом сегмента ST. Причи-ной стенокардии считают спазм эпикардиальной коро-нарной артерии, который может развиться в области тя-желого локального стеноза, однако в типичном случаеопределяется при минимальном атеросклеротическомпоражении. Пациенты с вариантной стенокардией не-сколько моложе пациентов с типичным ОКС без подъе-ма сегмента ST и часто являются злостными курильщи-ками. Симптомы обычно тяжелые и могут сопровождать-ся обмороками. Приступы стенокардии Принцметал-ла возникают в период с 12.00 ночи до 8.00 утра. Спазм может быть спонтанным или провоцируется ацетилхо-лином, холодовой пробой или гипервентиляцией.Для профилактики стенокардии Принцметалла приме-няют антагонисты кальция, которые предупреждают ко-ронарный спазм. Их назначают в максимальных пере-носимых дозах в виде монотерапии или в комбинациис нитратами.Синдром Х диагностируют у пациентов со стенокар-дией напряжения, у которых определяется депрессиясегмента ST при выполнении пробы с нагрузкой, а приангиографии отсутствует обструкция коронарных арте-рий. Частота или интенсивность приступов стенокардиимогут нарастать, или они возникают в покое. Могут на-блюдаться типичные признаки нестабильной стенокар-дии. Прогноз обычно хороший. Причина синдрома Х не установлена, однако он чаще всего сочетается с на-рушением эндотелий-зависимой артериальной вазо-дилатации, снижением секреции оксида азота и повы-шением чувствительности к симпатической стимуляции.Имеются данные о том, что у пациентов часто повыше-на реакция на боль. Учитывая благоприятный прогноз,необходимо в первую очередь успокоить пациентов иназначить нитраты, бета-адреноблокаторы или антаго-нисты кальция для купирования боли.Кардиомиопатия такоцубо (транзиторное шарооб-разное расширение верхушки левого желудочка) можетпроявляться клинической картиной ИМ с подъемом сег-мента ST или ОКС без подъема сегмента ST и характе-ризуется отсутствием ангиографических изменений в ко-ронарных артериях в сочетании с верхушечной и ино-гда медиовентрикулярной или базальной акинезиеймиокарда. Заболевание чаще встречается у женщин и,как правило, развивается после большого эмоцио-нального напряжения. Дисфункция левого желудочкаобычно обратима в течение нескольких дней или недель.В редких случаях ОКС без подъема сегмента ST с нор-мальными или практически неизмененными коро-нарными артериями развивается вследствие эмбо-лии в коронарную артерию на фоне фибрилляции илитрепетания предсердий. Фибрилляция предсердийчасто остается недиагностированной, поэтому частотаэтого механизма развития ОКС может быть заниженной.
Анемия
Анемия сопровождается ухудшением прогноза(сердечно-сосудистая смерть, ИМ или рецидивирую-щая ишемия) у пациентов с любыми вариантами ОКС[69]. Во время госпитализации персистирующая или на-растающая анемия ассоциируется с увеличением смерт-ности или частоты сердечной недостаточности посравнению с таковыми у пациентов без анемии или спреходящей анемией [282]. Анемия чаще встречаетсяу пациентов пожилого возраста, больных сахарным диа-бетом и почечной недостаточностью, а также с други-ми состояниями (геморрагический диатез или злока-чественная опухоль), которые могут вносить вклад вухудшение прогноза. Исходный уровень гемоглобинаоказался независимым предиктором кровотечений:чем ниже содержание гемоглобина, тем выше риск ге-моррагических осложнений, связанных и не связанныхс вмешательствами [283].Тактика ведения пациентов с анемией и ОКС безподъема сегмента ST эмпирическая. Необходимо уста-новить причину анемии, особенно скрытое крово-течение. Особое внимание следует уделять антитром-ботической терапии. Применение стентов, выделяющихлекарства, следует ограничивать, учитывая необходи-мость в длительной двойной антитромбоцитарной те-рапии. Необходимо тщательно взвесить показания к ангиографии и выбор сосудистого доступа (лучевая ар-терия), чтобы избежать дополнительной потери крови[284,285]. Трансфузии эритроцитарной массы прово-дят только по строгим показаниям, так как они сопро-вождаются увеличением смертности у больных с ОКС без подъема сегмента ST. Наблюдательные исследова-ния свидетельствуют о том, что трансфузий следует из-бегать, если гематокрит превышает 25%, а анемия хорошо переносится [286].
Рекомендации по лечению пациентов с анемией
Необструктивная коронарная болезнь сердца
У значительной части пациентов (около 15%) с ОКСбез подъема сегмента ST отсутствуют изменения коро-нарных артерий или имеется необструктивный коронар-ный атеросклероз. ОКС без подъема сегмента ST харак-теризуется неоднородным патогенезом, а возможныемеханизмы его развития включают в себя спазм коро-нарной артерии (стенокардия Принцметалла), ост-рый тромбоз на фоне интрамуральной бляшки с после-дующей реканализацией коронарной артерии, эмбо-лии в коронарные артерии и синдром Х. У пациентовс ОКС без подъема сегмента ST наличие неизмененныхили практически неизмененных коронарных артерийпри ангиографии позволяет усомниться в диагнозе. Од-нако изменения сегмента ST и выделение биомаркерову пациентов с типичной болью в груди и проходимы-ми коронарными артериями без выраженного стено-за могут быть следствием истинного некроза, а не от-ражать ложноположительные результаты. ОКС без из-менений коронарных артерий чаще встречается у жен-щин. Выраженные атеросклеротические изменениямогут наблюдаться даже при отсутствии ангиографиче-ского стеноза, так как диффузный атеросклероз приво-дит к ремоделированию стенки артерии. При этом утол-щение стенки сосуда происходит кнаружи, а просвет егоне суживается. Прогноз у таких пациентов более бла-гоприятный, чем при наличии выраженного коронар-ного атеросклероза, поэтому они нуждаются в оптималь-ной антитромботической терапии и вторичной профи-лактике антитромбоцитарными препаратами и стати-нами [281].Вариантная стенокардия Принцметалла часто оста-ется недиагностированной и характеризуется ишеми-ческой болью в груди, которая не связана с физическойнагрузкой или эмоциональным напряжением и сопро-вождается преходящим подъемом сегмента ST. Причи-ной стенокардии считают спазм эпикардиальной коро-нарной артерии, который может развиться в области тя-желого локального стеноза, однако в типичном случаеопределяется при минимальном атеросклеротическомпоражении. Пациенты с вариантной стенокардией не-сколько моложе пациентов с типичным ОКС без подъе-ма сегмента ST и часто являются злостными курильщи-ками. Симптомы обычно тяжелые и могут сопровождать-ся обмороками. Приступы стенокардии Принцметал-ла возникают в период с 12.00 ночи до 8.00 утра. Спазм может быть спонтанным или провоцируется ацетилхо-лином, холодовой пробой или гипервентиляцией.Для профилактики стенокардии Принцметалла приме-няют антагонисты кальция, которые предупреждают ко-ронарный спазм. Их назначают в максимальных пере-носимых дозах в виде монотерапии или в комбинациис нитратами.Синдром Х диагностируют у пациентов со стенокар-дией напряжения, у которых определяется депрессиясегмента ST при выполнении пробы с нагрузкой, а приангиографии отсутствует обструкция коронарных арте-рий. Частота или интенсивность приступов стенокардиимогут нарастать, или они возникают в покое. Могут на-блюдаться типичные признаки нестабильной стенокар-дии. Прогноз обычно хороший. Причина синдрома Х не установлена, однако он чаще всего сочетается с на-рушением эндотелий-зависимой артериальной вазо-дилатации, снижением секреции оксида азота и повы-шением чувствительности к симпатической стимуляции.Имеются данные о том, что у пациентов часто повыше-на реакция на боль. Учитывая благоприятный прогноз,необходимо в первую очередь успокоить пациентов иназначить нитраты, бета-адреноблокаторы или антаго-нисты кальция для купирования боли.Кардиомиопатия такоцубо (транзиторное шарооб-разное расширение верхушки левого желудочка) можетпроявляться клинической картиной ИМ с подъемом сег-мента ST или ОКС без подъема сегмента ST и характе-ризуется отсутствием ангиографических изменений в ко-ронарных артериях в сочетании с верхушечной и ино-гда медиовентрикулярной или базальной акинезиеймиокарда. Заболевание чаще встречается у женщин и,как правило, развивается после большого эмоцио-нального напряжения. Дисфункция левого желудочкаобычно обратима в течение нескольких дней или недель.В редких случаях ОКС без подъема сегмента ST с нор-мальными или практически неизмененными коро-нарными артериями развивается вследствие эмбо-лии в коронарную артерию на фоне фибрилляции илитрепетания предсердий. Фибрилляция предсердийчасто остается недиагностированной, поэтому частотаэтого механизма развития ОКС может быть заниженной.
Анемия
Анемия сопровождается ухудшением прогноза(сердечно-сосудистая смерть, ИМ или рецидивирую-щая ишемия) у пациентов с любыми вариантами ОКС[69]. Во время госпитализации персистирующая или на-растающая анемия ассоциируется с увеличением смерт-ности или частоты сердечной недостаточности посравнению с таковыми у пациентов без анемии или спреходящей анемией [282]. Анемия чаще встречаетсяу пациентов пожилого возраста, больных сахарным диа-бетом и почечной недостаточностью, а также с други-ми состояниями (геморрагический диатез или злока-чественная опухоль), которые могут вносить вклад вухудшение прогноза. Исходный уровень гемоглобинаоказался независимым предиктором кровотечений:чем ниже содержание гемоглобина, тем выше риск ге-моррагических осложнений, связанных и не связанныхс вмешательствами [283].Тактика ведения пациентов с анемией и ОКС безподъема сегмента ST эмпирическая. Необходимо уста-новить причину анемии, особенно скрытое крово-течение. Особое внимание следует уделять антитром-ботической терапии. Применение стентов, выделяющихлекарства, следует ограничивать, учитывая необходи-мость в длительной двойной антитромбоцитарной те-рапии. Необходимо тщательно взвесить показания к ангиографии и выбор сосудистого доступа (лучевая ар-терия), чтобы избежать дополнительной потери крови[284,285]. Трансфузии эритроцитарной массы прово-дят только по строгим показаниям, так как они сопро-вождаются увеличением смертности у больных с ОКС без подъема сегмента ST. Наблюдательные исследова-ния свидетельствуют о том, что трансфузий следует из-бегать, если гематокрит превышает 25%, а анемия хорошо переносится [286].
Рекомендации по лечению пациентов с анемией
 Кровотечения и трансфузии
Кровотечение — это самое частое неишемическоеосложнение при лечении ОКС без подъема сегмента ST,а также при ИМ с подъемом сегмента ST, ЧКВ и КШ. Важ-ность кровотечений была подробно рассмотрена впредыдущих рекомендациях [3] и подтверждена впоследующих исследованиях. В связи с этим в настоя-щем документе рассматриваются только новые данные.В связи с отсутствием общепринятого определениякровотечения оценить истинную частоту геморрагиче-ских осложнений в различных исследованиях и реги-страх трудно. «Универсальное определение» кровотече-ний, предложенное Bleeding Academic Research Consortium,позволит более объективно оценивать эти ослож-нений в будущих исследованиях [288]. Интересно, чточастота кровотечений в регистрах снизилась за послед-ние 7 лет, несмотря на более частое назначение двой-ной или тройной антитромбоцитарной терапии в со-четании с антикоагулянтами и более часто применениеинвазивных методов диагностики и лечения [289]. Этоможет указывать на то, что врачи осознают риск кро-вотечений при лечении ОКС и соответствующим обра-зом адаптируют стратегию ведения пациентов.Несмотря на вариабельность критериев оценкикровотечений, во многих исследованиях была подтвер-ждена дозозависимая ассоциация между кровотечения-ми и риском смерти и других ишемических осложне-ний. Большие кровотечения сопровождались 4-крат-ным увеличением риска смерти, 5-кратным увеличе-нием риска рецидивирующего ИМ и 3-кратнымувеличением риска инсульта в течение 30 дн [290]. Эти данные были подтверждены при анализе регистраGRACE и в клинических исследованиях, таких какOASIS-5 [291] и ACUITY [292]. Небольшие кровотече-ния также оказывают влияние на исходы, хотя и в мень-шей степени.Риск кровотечений тщательно изучен в первые 30дн после развития ОКС, в то время как риск поздних кро-вотечений на фоне длительной мощной антитромбо-цитарной терапии (более чем через 30 дн до конца на-блюдения или в течение 1 года) анализировался в мень-шей степени. В исследовании CURE [111] частота лю-бых больших кровотечений в течение первых 30 дн со-ставила 1,54% в группе плацебо и 2,01% в группе кло-пидогрела, а спустя 30 дн и до конца 1 года — 1,18%и 1,75%, соответственно. В исследовании TRITON нафоне инвазивного лечения частота больших кровотече-ний через 30-450 дн составила 1,23% в группе клопи-догрела и 1,71% в группе прасугрела [293]. В иссле-довании PLATO соответствующие показатели не оцени-вали. Общая частота больших кровотечений не отлича-лась, однако со временем было отмечено постепенноенарастание частоты больших кровотечений, не связан-ных с КШ; через 1 год отношение рисков составило1,19 (95% ДИ 1,02–1,38; p<0,03) [132]. При стабиль-ной ИБС было отмечено сходное постепенное увеличе-ние риска кровотечений в группах клопидогрела и пла-цебо; через 1 год отношение рисков составило1,88 (95% ДИ 1,45–2,45; p=0,001) [294]. Таким об-разом, риск кровотечений самый высокий в течение пер-вых 30 дн, однако длительная антитромбоцитарная те-рапия приводит к постепенному увеличению риска ге-моррагических осложнений.Независимыми предикторами больших кровотече-ний, установленными в клинических исследованиях ирегистрах, являются исходные показатели, особенно воз-раст, женский пол, кровотечения в анамнезе, исходныйуровень гемоглобина, диабет и почечная недостаточ-ность. Ухудшение функции почек, особенно клиренскреатинина менее 60 мл/мин, значительно увеличи-вает риск кровотечений. Важное значение имеет так-же метод лечения. Риск кровотечений повышаетсяпри увеличении числа назначенных антитромбоцитар-ных препаратов, включая антикоагулянты, аспирин, бло-каторы P2Y12 рецепторов и особенно блокаторыGP IIb/IIIa рецепторов, а также при применении фемо-рального, а не лучевого доступа [284,285]. Крометого, риск кровотечений увеличивается на фоне при-менения лекарственных препаратов в слишком высо-ких дозах, которое часто отмечается у пациентов с са-мым высоким риском геморрагических осложнений,в частности у женщин, пожилых людей и пациентов спочечной недостаточностью [168]. Двойная антитром-боцитарная терапия в сочетании с антагонистами ви-тамина К, которая часто показана пациентам с ОКС, так-же может способствовать увеличению риска кровотече-ний [295]. Индексы риска кровотечений см. в разделе4.4.Механизмы ухудшения прогноза при кровотеченияхостаются неясными. Основное значение, вероятно,имеет необходимость отмены антитромбоцитарных иантитромботических препаратов, которая приводит кувеличению риска ишемических исходов, особеннотромбоза стента после ЧКВ. Кроме того, факторы рис-ка кровотечений и ишемических осложнений в значи-тельной степени перекрещиваются. Нельзя исключить,что у пациентов с более высоким риском повышена ве-роятность осложнений обоих типов, поэтому они по-лучают наиболее агрессивное медикаментозное и ин-вазивное лечение. В регистре GRACE увеличение рис-ка кровотечений при снижении функции почек было па-раллельным увеличению риска смерти. Эти данные былиподтверждены при анализе post-hoc исследованияOASIS-5, в котором риск кровотечений зеркально отра-жал увеличение индекса риска GRACE [296]. Следова-тельно, развитие кровотечений может быть простымтриггером ухудшения прогноза у уязвимых пациентов.Другими факторами риска смерти при кровотеченияхмогут быть гемодинамические последствия кровопо-тери, потенциальные неблагоприятные эффекты гемо-трансфузии и протромботическое или провоспалитель-ное состояние, индуцированное кровотечением[297,298].Лечение геморрагических осложненийПредупреждение кровотечений — это важная состав-ная часть стратегии профилактики ишемических ослож-нений. Соответственно, при стратификации риска у па-циентов с ОКС без подъема сегмента ST следует оценитьриск как тромботических, так и геморрагическихосложнений. Профилактика кровотечений предпола-гает выбор более безопасных препаратов и адекватнойдозы (с учетом возраста, пола и клиренса креатинина),снижение длительности антитромботической тера-пии, применение комбинации антитромботических иантитромбоцитарных препаратов в соответствии сустановленными показаниями, использование лучево-го, а не феморального доступа для инвазивного вме-шательства [299]. По данным мета-анализа исследо-ваний ACUITY и HORIZONS, применение бивалируди-на вместо стандартных антикоагулянтов в сочетании сблокаторами GP IIb/IIIa рецепторов снижало риск кро-вотечений [300].Желудочно-кишечные кровотечения составляютоколо 50% в структуре спонтанных кровотечений в на-чальную фазу ОКС. В связи с этим следует назначать ин-гибиторы протонной помпы, особенно пациентам с же-лудочно-кишечными кровотечениями или пептиче-ской язвой в анамнезе. Возможное взаимодействие клопидогрела с омепразолом и в меньшей степени с дру-гими ингибиторами протонной помпы, по-видимому,не имеет клинического значения (см. раздел 5.2.2.).Небольшие кровотечения не требуют перерыва влечении, если они не продолжаются. При большом кро-вотечении, например желудочно-кишечном, ретропе-ритонеальном, внутричерепном, или другой тяжелойкровопотере необходимо прекратить терапию и ней-трализовать активность антитромбоцитарных и анти-тромботических препаратов, если кровотечение неудается остановить с помощью обычных мер. Преры-вать лечение антитромботическими препаратами не обя-зательно, если удается полностью остановить кровотече-ние. В клинической практике следует взвешивать риск,связанный с перерывом в лечении антитромботически-ми препаратами, и риск тромботических осложне-ний, особенно после имплантации стента.Действие НФГ можно нейтрализовать с помощью эк-вимолярных концентраций протамина сульфата. Про-тамин сульфат оказывает менее выраженное действиена эноксапарин и не влияет на эффекты фондапаринук-са или бивалирудина. Бивалирудин имеет очень корот-кий период полувыведения, поэтому нейтрализация егоактивности может не потребоваться. В случае фонда-паринукса рекомендуется введение рекомбинантногофактора VIIа, однако оно сопровождалось повышеннымриском тромботических осложнений [301]. Антидотынеобратимых антитромбоцитарных препаратов, та-ких как аспирин, клопидогрел или прасугрел, не-известны. Соответственно, их действие можно нейтра-лизовать только путем трансфузии свежей тромбоци-тарной массы. То же касается тикагрелора вскоре (<3дн) после отмены препарата.Блокаторы GP IIb/II рецепторов имеют различныефармакологические свойства, которые следует учиты-вать при выборе метода нейтрализации их действия.Низкомолекулярные препараты (тирофибан и эптифи-батид) обратимо связываются с рецепторами и быстровыводятся почками, поэтому функция тромбоцитов нор-мализуется через 4-8 ч после прекращения инфузии.После отмены абциксимаба функция тромбоцитоввосстанавливается в течение примерно 48 ч.Возобновлять лечение антитромбоцитарными пре-паратами и/или антикоагулянтами следует только в томслучае, если удается контролировать кровотечение втечение по крайней мере 24 ч.Эффекты гемотрансфузииГемотрансфузии дают неблагоприятные эффекты (по-вышение риска смерти и ИМ, а также пневмонии) вомногих клинических ситуациях, включая ОКС, ЧКВ, КШ,и во время интенсивной терапии [286,298]. Нежела-тельное действие гемотрансфузий объясняют различ-ными механизмами. Наибольшее значение имеет хра-нение крови. Негативный эффект гемотрансфузий нариск неблагоприятных исходов в значительной степе-ни зависит от минимального гематокрита и уровня ге-моглобина, при которых начинают трансфузию. Пере-ливание крови оправданно при гематокрите менее 25%,но не выше этого значения [286,298]. Трансфузию сле-дует проводить при уровне гемоглобина 7 г/дл, доби-ваясь его увеличения до 9-10 г/дл. В этом случае ре-зультаты лучше, чем при более «либеральных» показа-ниях к гемотрансфузии [287,302]. У пациентов состабильной гемодинамикой гемотрансфузия целесооб-разна только при исходном уровне гемоглобина <7 г/дл,в то время как при нестабильной гемодинамике какие-либо ограничения отсутствуют.Препараты железа и эритропоэтинПрепараты железа вводят, если анемия связана с де-фицитом железа или происходит массивная кровопо-теря. Лечение дефицита железа предполагает длитель-ное пероральное применение препаратов железа.Если пациент плохо переносит препараты для приемавнутрь, возможно внутривенное введение. Сочетанноеприменение эритропоэтина при ОКС невозможно,учитывая повышенный риск тромбоза глубоких вен, ин-сульта и острых коронарных исходов [303].
Тромбоцитопения
При лечении ОКС без подъема сегмента ST можетразвиться тромбоцитопения — снижение числа тром-боцитов менее 100 000 в мкл или по крайней мере на50% по сравнению с исходным. Тромбоцитопению счи-тают умеренной, если число тромбоцитов составляет20 000-50 000 в мкл, и тяжелой, если оно снижаетсяменее 20 000 в мкл.При ОКС выделяют два основных типа тромбоцито-пении, вызванной лекарствами (гепарин и блокаторыGP IIb/IIIa рецепторов), которые отличаются по прогно-зу. Полную информацию об обоих типах тромбоцито-пении можно найти в предыдущих рекомендациях [3].Гепарин-индуцированную тромбоцитопению следу-ет предполагать при снижении числа тромбоцитов бо-лее чем на 50% или до 100 000 в мкл. Она развивает-ся у 15% пациентов, получающих НФГ, встречается режепри применении НМГ и не наблюдается при лечениифондапаринуксом. Если подозревается гепарин-ин-дуцированная тромбоцитопения, следует немедленноотменить НФГ или НМГ. Могут быть назначены альтер-нативные антитромботические препараты даже приотсутствии тромботических осложнений. Можно исполь-зовать гепариноиды, такие как данапароид натрий, хотяin vitro наблюдали перекрестные реакции с НФГ или НМГ,однако они не осложнялись тромбозом. Альтернатива— применение прямых ингибиторов тромбина, таких какаргатробан, гирудин или его производные, которые не вызывают тромбоцитопению. Они обеспечивают стой-кий антитромботический эффект, который контролируютс помощью аЧТВ, хотя зависимость эффекта от дозы не-линейная и сглаживается при увеличении доз. Фонда-паринукс также можно применять в этой ситуации, таккак он оказывает мощное антитромботическое действиеи не взаимодействует с тромбоцитами, однако данноепоказание не зарегистрировано.Частота тромбоцитопении, вызванной блокаторамиGP IIb/IIIa рецепторов, в клинических исследованияхсоставляла от 0,5 до 5,6% в зависимости от типа пре-парата. Тяжелая тромбоцитопения может быть бессимп-томной и сопровождаться только небольшими крово-течениями в области сосудистого доступа. Большие кро-вотечения развиваются редко, но могут угрожать жиз-ни. У всех пациентов, получающих блокаторыGP IIb/IIIa рецепторов, рекомендуется измерить числотромбоцитов через 8 ч после начала инфузии или в слу-чае кровотечения. Если число тромбоцитов снижаетсяменее 10 000 в мкл, рекомендуется отменить блокато-ры GP IIb/IIIa рецепторов, а также НФГ или эноксапа-рин. При кровотечении рекомендуется трансфузиятромбоцитарной массы. Предлагалось также введениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с трансфу-зией тромбоцитарной массы.
Рекомендации по лечению геморрагических осложнений
Кровотечения и трансфузии
Кровотечение — это самое частое неишемическоеосложнение при лечении ОКС без подъема сегмента ST,а также при ИМ с подъемом сегмента ST, ЧКВ и КШ. Важ-ность кровотечений была подробно рассмотрена впредыдущих рекомендациях [3] и подтверждена впоследующих исследованиях. В связи с этим в настоя-щем документе рассматриваются только новые данные.В связи с отсутствием общепринятого определениякровотечения оценить истинную частоту геморрагиче-ских осложнений в различных исследованиях и реги-страх трудно. «Универсальное определение» кровотече-ний, предложенное Bleeding Academic Research Consortium,позволит более объективно оценивать эти ослож-нений в будущих исследованиях [288]. Интересно, чточастота кровотечений в регистрах снизилась за послед-ние 7 лет, несмотря на более частое назначение двой-ной или тройной антитромбоцитарной терапии в со-четании с антикоагулянтами и более часто применениеинвазивных методов диагностики и лечения [289]. Этоможет указывать на то, что врачи осознают риск кро-вотечений при лечении ОКС и соответствующим обра-зом адаптируют стратегию ведения пациентов.Несмотря на вариабельность критериев оценкикровотечений, во многих исследованиях была подтвер-ждена дозозависимая ассоциация между кровотечения-ми и риском смерти и других ишемических осложне-ний. Большие кровотечения сопровождались 4-крат-ным увеличением риска смерти, 5-кратным увеличе-нием риска рецидивирующего ИМ и 3-кратнымувеличением риска инсульта в течение 30 дн [290]. Эти данные были подтверждены при анализе регистраGRACE и в клинических исследованиях, таких какOASIS-5 [291] и ACUITY [292]. Небольшие кровотече-ния также оказывают влияние на исходы, хотя и в мень-шей степени.Риск кровотечений тщательно изучен в первые 30дн после развития ОКС, в то время как риск поздних кро-вотечений на фоне длительной мощной антитромбо-цитарной терапии (более чем через 30 дн до конца на-блюдения или в течение 1 года) анализировался в мень-шей степени. В исследовании CURE [111] частота лю-бых больших кровотечений в течение первых 30 дн со-ставила 1,54% в группе плацебо и 2,01% в группе кло-пидогрела, а спустя 30 дн и до конца 1 года — 1,18%и 1,75%, соответственно. В исследовании TRITON нафоне инвазивного лечения частота больших кровотече-ний через 30-450 дн составила 1,23% в группе клопи-догрела и 1,71% в группе прасугрела [293]. В иссле-довании PLATO соответствующие показатели не оцени-вали. Общая частота больших кровотечений не отлича-лась, однако со временем было отмечено постепенноенарастание частоты больших кровотечений, не связан-ных с КШ; через 1 год отношение рисков составило1,19 (95% ДИ 1,02–1,38; p<0,03) [132]. При стабиль-ной ИБС было отмечено сходное постепенное увеличе-ние риска кровотечений в группах клопидогрела и пла-цебо; через 1 год отношение рисков составило1,88 (95% ДИ 1,45–2,45; p=0,001) [294]. Таким об-разом, риск кровотечений самый высокий в течение пер-вых 30 дн, однако длительная антитромбоцитарная те-рапия приводит к постепенному увеличению риска ге-моррагических осложнений.Независимыми предикторами больших кровотече-ний, установленными в клинических исследованиях ирегистрах, являются исходные показатели, особенно воз-раст, женский пол, кровотечения в анамнезе, исходныйуровень гемоглобина, диабет и почечная недостаточ-ность. Ухудшение функции почек, особенно клиренскреатинина менее 60 мл/мин, значительно увеличи-вает риск кровотечений. Важное значение имеет так-же метод лечения. Риск кровотечений повышаетсяпри увеличении числа назначенных антитромбоцитар-ных препаратов, включая антикоагулянты, аспирин, бло-каторы P2Y12 рецепторов и особенно блокаторыGP IIb/IIIa рецепторов, а также при применении фемо-рального, а не лучевого доступа [284,285]. Крометого, риск кровотечений увеличивается на фоне при-менения лекарственных препаратов в слишком высо-ких дозах, которое часто отмечается у пациентов с са-мым высоким риском геморрагических осложнений,в частности у женщин, пожилых людей и пациентов спочечной недостаточностью [168]. Двойная антитром-боцитарная терапия в сочетании с антагонистами ви-тамина К, которая часто показана пациентам с ОКС, так-же может способствовать увеличению риска кровотече-ний [295]. Индексы риска кровотечений см. в разделе4.4.Механизмы ухудшения прогноза при кровотеченияхостаются неясными. Основное значение, вероятно,имеет необходимость отмены антитромбоцитарных иантитромботических препаратов, которая приводит кувеличению риска ишемических исходов, особеннотромбоза стента после ЧКВ. Кроме того, факторы рис-ка кровотечений и ишемических осложнений в значи-тельной степени перекрещиваются. Нельзя исключить,что у пациентов с более высоким риском повышена ве-роятность осложнений обоих типов, поэтому они по-лучают наиболее агрессивное медикаментозное и ин-вазивное лечение. В регистре GRACE увеличение рис-ка кровотечений при снижении функции почек было па-раллельным увеличению риска смерти. Эти данные былиподтверждены при анализе post-hoc исследованияOASIS-5, в котором риск кровотечений зеркально отра-жал увеличение индекса риска GRACE [296]. Следова-тельно, развитие кровотечений может быть простымтриггером ухудшения прогноза у уязвимых пациентов.Другими факторами риска смерти при кровотеченияхмогут быть гемодинамические последствия кровопо-тери, потенциальные неблагоприятные эффекты гемо-трансфузии и протромботическое или провоспалитель-ное состояние, индуцированное кровотечением[297,298].Лечение геморрагических осложненийПредупреждение кровотечений — это важная состав-ная часть стратегии профилактики ишемических ослож-нений. Соответственно, при стратификации риска у па-циентов с ОКС без подъема сегмента ST следует оценитьриск как тромботических, так и геморрагическихосложнений. Профилактика кровотечений предпола-гает выбор более безопасных препаратов и адекватнойдозы (с учетом возраста, пола и клиренса креатинина),снижение длительности антитромботической тера-пии, применение комбинации антитромботических иантитромбоцитарных препаратов в соответствии сустановленными показаниями, использование лучево-го, а не феморального доступа для инвазивного вме-шательства [299]. По данным мета-анализа исследо-ваний ACUITY и HORIZONS, применение бивалируди-на вместо стандартных антикоагулянтов в сочетании сблокаторами GP IIb/IIIa рецепторов снижало риск кро-вотечений [300].Желудочно-кишечные кровотечения составляютоколо 50% в структуре спонтанных кровотечений в на-чальную фазу ОКС. В связи с этим следует назначать ин-гибиторы протонной помпы, особенно пациентам с же-лудочно-кишечными кровотечениями или пептиче-ской язвой в анамнезе. Возможное взаимодействие клопидогрела с омепразолом и в меньшей степени с дру-гими ингибиторами протонной помпы, по-видимому,не имеет клинического значения (см. раздел 5.2.2.).Небольшие кровотечения не требуют перерыва влечении, если они не продолжаются. При большом кро-вотечении, например желудочно-кишечном, ретропе-ритонеальном, внутричерепном, или другой тяжелойкровопотере необходимо прекратить терапию и ней-трализовать активность антитромбоцитарных и анти-тромботических препаратов, если кровотечение неудается остановить с помощью обычных мер. Преры-вать лечение антитромботическими препаратами не обя-зательно, если удается полностью остановить кровотече-ние. В клинической практике следует взвешивать риск,связанный с перерывом в лечении антитромботически-ми препаратами, и риск тромботических осложне-ний, особенно после имплантации стента.Действие НФГ можно нейтрализовать с помощью эк-вимолярных концентраций протамина сульфата. Про-тамин сульфат оказывает менее выраженное действиена эноксапарин и не влияет на эффекты фондапаринук-са или бивалирудина. Бивалирудин имеет очень корот-кий период полувыведения, поэтому нейтрализация егоактивности может не потребоваться. В случае фонда-паринукса рекомендуется введение рекомбинантногофактора VIIа, однако оно сопровождалось повышеннымриском тромботических осложнений [301]. Антидотынеобратимых антитромбоцитарных препаратов, та-ких как аспирин, клопидогрел или прасугрел, не-известны. Соответственно, их действие можно нейтра-лизовать только путем трансфузии свежей тромбоци-тарной массы. То же касается тикагрелора вскоре (<3дн) после отмены препарата.Блокаторы GP IIb/II рецепторов имеют различныефармакологические свойства, которые следует учиты-вать при выборе метода нейтрализации их действия.Низкомолекулярные препараты (тирофибан и эптифи-батид) обратимо связываются с рецепторами и быстровыводятся почками, поэтому функция тромбоцитов нор-мализуется через 4-8 ч после прекращения инфузии.После отмены абциксимаба функция тромбоцитоввосстанавливается в течение примерно 48 ч.Возобновлять лечение антитромбоцитарными пре-паратами и/или антикоагулянтами следует только в томслучае, если удается контролировать кровотечение втечение по крайней мере 24 ч.Эффекты гемотрансфузииГемотрансфузии дают неблагоприятные эффекты (по-вышение риска смерти и ИМ, а также пневмонии) вомногих клинических ситуациях, включая ОКС, ЧКВ, КШ,и во время интенсивной терапии [286,298]. Нежела-тельное действие гемотрансфузий объясняют различ-ными механизмами. Наибольшее значение имеет хра-нение крови. Негативный эффект гемотрансфузий нариск неблагоприятных исходов в значительной степе-ни зависит от минимального гематокрита и уровня ге-моглобина, при которых начинают трансфузию. Пере-ливание крови оправданно при гематокрите менее 25%,но не выше этого значения [286,298]. Трансфузию сле-дует проводить при уровне гемоглобина 7 г/дл, доби-ваясь его увеличения до 9-10 г/дл. В этом случае ре-зультаты лучше, чем при более «либеральных» показа-ниях к гемотрансфузии [287,302]. У пациентов состабильной гемодинамикой гемотрансфузия целесооб-разна только при исходном уровне гемоглобина <7 г/дл,в то время как при нестабильной гемодинамике какие-либо ограничения отсутствуют.Препараты железа и эритропоэтинПрепараты железа вводят, если анемия связана с де-фицитом железа или происходит массивная кровопо-теря. Лечение дефицита железа предполагает длитель-ное пероральное применение препаратов железа.Если пациент плохо переносит препараты для приемавнутрь, возможно внутривенное введение. Сочетанноеприменение эритропоэтина при ОКС невозможно,учитывая повышенный риск тромбоза глубоких вен, ин-сульта и острых коронарных исходов [303].
Тромбоцитопения
При лечении ОКС без подъема сегмента ST можетразвиться тромбоцитопения — снижение числа тром-боцитов менее 100 000 в мкл или по крайней мере на50% по сравнению с исходным. Тромбоцитопению счи-тают умеренной, если число тромбоцитов составляет20 000-50 000 в мкл, и тяжелой, если оно снижаетсяменее 20 000 в мкл.При ОКС выделяют два основных типа тромбоцито-пении, вызванной лекарствами (гепарин и блокаторыGP IIb/IIIa рецепторов), которые отличаются по прогно-зу. Полную информацию об обоих типах тромбоцито-пении можно найти в предыдущих рекомендациях [3].Гепарин-индуцированную тромбоцитопению следу-ет предполагать при снижении числа тромбоцитов бо-лее чем на 50% или до 100 000 в мкл. Она развивает-ся у 15% пациентов, получающих НФГ, встречается режепри применении НМГ и не наблюдается при лечениифондапаринуксом. Если подозревается гепарин-ин-дуцированная тромбоцитопения, следует немедленноотменить НФГ или НМГ. Могут быть назначены альтер-нативные антитромботические препараты даже приотсутствии тромботических осложнений. Можно исполь-зовать гепариноиды, такие как данапароид натрий, хотяin vitro наблюдали перекрестные реакции с НФГ или НМГ,однако они не осложнялись тромбозом. Альтернатива— применение прямых ингибиторов тромбина, таких какаргатробан, гирудин или его производные, которые не вызывают тромбоцитопению. Они обеспечивают стой-кий антитромботический эффект, который контролируютс помощью аЧТВ, хотя зависимость эффекта от дозы не-линейная и сглаживается при увеличении доз. Фонда-паринукс также можно применять в этой ситуации, таккак он оказывает мощное антитромботическое действиеи не взаимодействует с тромбоцитами, однако данноепоказание не зарегистрировано.Частота тромбоцитопении, вызванной блокаторамиGP IIb/IIIa рецепторов, в клинических исследованияхсоставляла от 0,5 до 5,6% в зависимости от типа пре-парата. Тяжелая тромбоцитопения может быть бессимп-томной и сопровождаться только небольшими крово-течениями в области сосудистого доступа. Большие кро-вотечения развиваются редко, но могут угрожать жиз-ни. У всех пациентов, получающих блокаторыGP IIb/IIIa рецепторов, рекомендуется измерить числотромбоцитов через 8 ч после начала инфузии или в слу-чае кровотечения. Если число тромбоцитов снижаетсяменее 10 000 в мкл, рекомендуется отменить блокато-ры GP IIb/IIIa рецепторов, а также НФГ или эноксапа-рин. При кровотечении рекомендуется трансфузиятромбоцитарной массы. Предлагалось также введениефибриногена в виде свежезамороженной плазмы иликриопреципитата, в том числе в сочетании с трансфу-зией тромбоцитарной массы.
Рекомендации по лечению геморрагических осложнений
 Рекомендации по ведению пациентов с тромбоцитопенией
Рекомендации по ведению пациентов с тромбоцитопенией
 Вторичная профилактика
Вторичная профилактика имеет очень важное значе-ние, учитывая высокую частоту развития ишемическихосложнений после завершения острой фазы. Среди16 321 пациента с ОКС 20% больных госпитализиро-вались повторно, а 18% мужчин и 23% женщин в воз-расте старше 40 лет умерли в течение первого года на-блюдения [304]. Вторичная профилактика значитель-но улучшает отдаленный прогноз. Длительная профи-лактика после ОКС без подъема сегмента ST былаподробно описана в предыдущих рекомендациях, ко-торые сохраняют свое значение [3]. Кроме того, мето-ды вторичной профилактики обсуждаются в рекомен-дациях Европейского общества кардиологов по профи-лактике сердечно-сосудистых заболеваний в клиниче-ской практике [252]. Эти рекомендации распространяют-ся на всех пациентов группы риска и пациентов с сер-дечно-сосудистыми заболеваниями. Наличие послед-них указывает на высокий риск. В рекомендацияхАмериканской ассоциации сердца/Американской кол-легии кардиологов (AHA/ACC) по вторичной профилактике специально обсуждается тактика ведения па-циентов с ОКС (т.е. вторичная профилактика) [305]. Со-ответственно, в данном разделе рассматриваются толь-ко новые данные. Более подробную информацию см.в перечисленных документах. Цели вторичной профи-лактики и модификации сердечно-сосудистых факто-ров риска определены в таблице в приложении(www.escardio.org/guidelines).Необходимо использовать все меры вторичнойпрофилактики, обладающие доказанной эффектив-ностью: модификацию образа жизни, контроль факто-ров риска и медикаментозную терапию аспирином, бло-каторами P2Y12 рецепторов, бета-адреноблокаторами,статинами, ингибиторами АПФ или блокаторами ре-цепторов ангиотензина II и эплереноном. Недавнобыло показано, что у больных с ОКС без подъема сег-мента ST, у которых отсутствуют биомаркеры (нестабиль-ная стенокардия), ниже вероятность проведения адек-ватной вторичной профилактики по сравнению с тако-вой у пациентов с ИМ без подъема сегмента ST [59]. Сле-дует подчеркнуть, что вторичная профилактика эффек-тивна у всех пациентов с ОКС.Включение пациента в программу реабилитации/вторичной профилактики может привести к увеличе-нию приверженности и настоятельно рекомендуетсябольным среднего и высокого риска. Эффективность мервторичной профилактики была установлена у пациен-тов, принимавших участие в исследовании OASIS-5. Вэтом исследовании пациентам с ОКС без подъемасегмента рекомендовали соблюдать здоровую диету,регулярно выполнять физические нагрузки и прекра-тить курить в течение 30 дн после появления симпто-мов. У пациентов, соблюдавших диету и занимав-шихся физическими упражнениями, относительныйриск ИМ, инсульта и смерти снизился на 54% (ОШ 0,46;95% ДИ 0,38–0,57; p<0,0001), а у пациентов, бросив-ших курить, относительный риск ИМ снизился на 43%(ОШ 0,57; 95% ДИ 0,36–0,89; p=0,0145) [306]. В двухдругих исследованиях было подтверждено, что вторич-ная профилактика после ОКС позволяет снизить рисксмерти в той же степени, что и лечение в острую фазу[307,308].Ингибиторы АПФ и блокаторы рецепторов ангио-тензина II обладают доказанной эффективностью во вто-ричной профилактике [309,310] и в первую очередьпоказаны пациентам со сниженной функцией левогожелудочка. При плохой переносимости ингибиторовАПФ могут быть использованы блокаторы рецепторовангиотензина II. В крупном исследовании телмисартанпо эффективности по крайней мере не уступал рами-прилу и реже вызывал побочные эффекты [311]. Ком-бинированная терапия ингибиторами АПФ и блокато-рами рецепторов ангиотензина II обычно не рекомен-дуется. Рекомендации по применению ингибиторов АПФи блокаторов рецепторов ангиотензина II распростра-няются на пациентов, недавно перенесших ОКС безподъема сегмента ST.Антагонисты альдостерона, в частности эплеренон,снижали сердечно-сосудистую смертность после ИМ упациентов со сниженной функцией левого желудочка(фракция выброса ≤35%) даже при наличии легко вы-раженных симптомов [277]. Эти результаты можно экс-траполировать на пациентов со сниженной функциейлевого желудочка, перенесших ОКС без подъема сег-мента ST.Статины рекомендуются всем пациентам с ОКС безподъема сегмента ST (при отсутствии противопоказаний)независимо от уровней холестерина. Лечение рекомен-дуется начинать в течение 1-4 дн после госпитализации.Целевой уровень холестерина липопротеинов низкойплотности (ЛНП) составляет <2,6 ммоль/л (100 мг/дл).Эта рекомендация основывается на результатах крупных исследований аторвастатина и правастатина. При мета-анализе исследований ранней терапии статинами не былподтвержден благоприятный эффект в течение первых4 мес [312]. Однако при более длительном наблюдении(2 года) было отмечено снижение смертности и часто-ты сердечно-сосудистых исходов.Дополнительное снижение риска неблагоприятныхсобытий было выявлено при снижении уровня холесте-рина ЛНП менее 1,81 ммоль/л (70 мг/дл) [313]. Длядостижения максимального эффекта необходимы вы-сокие дозы (например, 80 мг аторвастатина).Эффект, по-видимому, не зависит от противовоспа-лительного действия статинов (снижение уровня вчСРБ)или дополняет его. Не установлено, характерен ли эф-фект аторвастатина и правастатина для всего класса ста-тинов.
Рекомендации по вторичной профилактике (отдельно см. антитромботические средства)
Вторичная профилактика
Вторичная профилактика имеет очень важное значе-ние, учитывая высокую частоту развития ишемическихосложнений после завершения острой фазы. Среди16 321 пациента с ОКС 20% больных госпитализиро-вались повторно, а 18% мужчин и 23% женщин в воз-расте старше 40 лет умерли в течение первого года на-блюдения [304]. Вторичная профилактика значитель-но улучшает отдаленный прогноз. Длительная профи-лактика после ОКС без подъема сегмента ST былаподробно описана в предыдущих рекомендациях, ко-торые сохраняют свое значение [3]. Кроме того, мето-ды вторичной профилактики обсуждаются в рекомен-дациях Европейского общества кардиологов по профи-лактике сердечно-сосудистых заболеваний в клиниче-ской практике [252]. Эти рекомендации распространяют-ся на всех пациентов группы риска и пациентов с сер-дечно-сосудистыми заболеваниями. Наличие послед-них указывает на высокий риск. В рекомендацияхАмериканской ассоциации сердца/Американской кол-легии кардиологов (AHA/ACC) по вторичной профилактике специально обсуждается тактика ведения па-циентов с ОКС (т.е. вторичная профилактика) [305]. Со-ответственно, в данном разделе рассматриваются толь-ко новые данные. Более подробную информацию см.в перечисленных документах. Цели вторичной профи-лактики и модификации сердечно-сосудистых факто-ров риска определены в таблице в приложении(www.escardio.org/guidelines).Необходимо использовать все меры вторичнойпрофилактики, обладающие доказанной эффектив-ностью: модификацию образа жизни, контроль факто-ров риска и медикаментозную терапию аспирином, бло-каторами P2Y12 рецепторов, бета-адреноблокаторами,статинами, ингибиторами АПФ или блокаторами ре-цепторов ангиотензина II и эплереноном. Недавнобыло показано, что у больных с ОКС без подъема сег-мента ST, у которых отсутствуют биомаркеры (нестабиль-ная стенокардия), ниже вероятность проведения адек-ватной вторичной профилактики по сравнению с тако-вой у пациентов с ИМ без подъема сегмента ST [59]. Сле-дует подчеркнуть, что вторичная профилактика эффек-тивна у всех пациентов с ОКС.Включение пациента в программу реабилитации/вторичной профилактики может привести к увеличе-нию приверженности и настоятельно рекомендуетсябольным среднего и высокого риска. Эффективность мервторичной профилактики была установлена у пациен-тов, принимавших участие в исследовании OASIS-5. Вэтом исследовании пациентам с ОКС без подъемасегмента рекомендовали соблюдать здоровую диету,регулярно выполнять физические нагрузки и прекра-тить курить в течение 30 дн после появления симпто-мов. У пациентов, соблюдавших диету и занимав-шихся физическими упражнениями, относительныйриск ИМ, инсульта и смерти снизился на 54% (ОШ 0,46;95% ДИ 0,38–0,57; p<0,0001), а у пациентов, бросив-ших курить, относительный риск ИМ снизился на 43%(ОШ 0,57; 95% ДИ 0,36–0,89; p=0,0145) [306]. В двухдругих исследованиях было подтверждено, что вторич-ная профилактика после ОКС позволяет снизить рисксмерти в той же степени, что и лечение в острую фазу[307,308].Ингибиторы АПФ и блокаторы рецепторов ангио-тензина II обладают доказанной эффективностью во вто-ричной профилактике [309,310] и в первую очередьпоказаны пациентам со сниженной функцией левогожелудочка. При плохой переносимости ингибиторовАПФ могут быть использованы блокаторы рецепторовангиотензина II. В крупном исследовании телмисартанпо эффективности по крайней мере не уступал рами-прилу и реже вызывал побочные эффекты [311]. Ком-бинированная терапия ингибиторами АПФ и блокато-рами рецепторов ангиотензина II обычно не рекомен-дуется. Рекомендации по применению ингибиторов АПФи блокаторов рецепторов ангиотензина II распростра-няются на пациентов, недавно перенесших ОКС безподъема сегмента ST.Антагонисты альдостерона, в частности эплеренон,снижали сердечно-сосудистую смертность после ИМ упациентов со сниженной функцией левого желудочка(фракция выброса ≤35%) даже при наличии легко вы-раженных симптомов [277]. Эти результаты можно экс-траполировать на пациентов со сниженной функциейлевого желудочка, перенесших ОКС без подъема сег-мента ST.Статины рекомендуются всем пациентам с ОКС безподъема сегмента ST (при отсутствии противопоказаний)независимо от уровней холестерина. Лечение рекомен-дуется начинать в течение 1-4 дн после госпитализации.Целевой уровень холестерина липопротеинов низкойплотности (ЛНП) составляет <2,6 ммоль/л (100 мг/дл).Эта рекомендация основывается на результатах крупных исследований аторвастатина и правастатина. При мета-анализе исследований ранней терапии статинами не былподтвержден благоприятный эффект в течение первых4 мес [312]. Однако при более длительном наблюдении(2 года) было отмечено снижение смертности и часто-ты сердечно-сосудистых исходов.Дополнительное снижение риска неблагоприятныхсобытий было выявлено при снижении уровня холесте-рина ЛНП менее 1,81 ммоль/л (70 мг/дл) [313]. Длядостижения максимального эффекта необходимы вы-сокие дозы (например, 80 мг аторвастатина).Эффект, по-видимому, не зависит от противовоспа-лительного действия статинов (снижение уровня вчСРБ)или дополняет его. Не установлено, характерен ли эф-фект аторвастатина и правастатина для всего класса ста-тинов.
Рекомендации по вторичной профилактике (отдельно см. антитромботические средства)
 Методы оценки качества лечения
Вариабельность применения рекомендуемых стра-тегий лечения определяет разницу неблагоприятных ис-ходов. В нескольких крупных регистрах было показа-но, что лечение пациентов с ОКС без подъема сегмен-та ST нередко не соответствует современным рекомен-дациям. Часто отмечается недостаточно активное при-менение рекомендуемых методов лечения. Выполне-ние рекомендаций приводило к улучшению исходов упациентов с ОКС, в том числе к снижению смертности[318]. Таким образом, повышение степени выполнениярекомендаций является приоритетной задачей. Коэф-фициенты риск/польза рекомендуемых методов лече-ния (NNT и NNH) изображены на рис. 4.Чтобы повысить качество лечения и свести к миниму-му его отклонения от рекомендаций, необходимо посто-янно контролировать показатели адекватности тактикиведения пациентов. Внедрение методов лечения, обладающих доказанной эффективностью (рис. 4), может при-вести к более выраженному улучшению сердечно-сосу-дистого здоровья населения по сравнению с таковым вклинических исследованиях, особенно при одновремен-ном применении нескольких эффективных методов.Подобные программы были успешно внедрены в несколь-ких странах, включая Швецию (регистр RIKS-HIA), Вели-кобританию (регистр MINAP), Германию, Италию и Из-раиль. Программы оценки качества лечения были так-же разработаны Европейским обществом кардиологови используются в рамках Euro Heart Survey Programme.Наиболее информативные показатели перечисле-ны в табл. 11.
Таблица 11. Критерии качества медицинской помощипациентам с ИМ без подъема сегмента ST
Методы оценки качества лечения
Вариабельность применения рекомендуемых стра-тегий лечения определяет разницу неблагоприятных ис-ходов. В нескольких крупных регистрах было показа-но, что лечение пациентов с ОКС без подъема сегмен-та ST нередко не соответствует современным рекомен-дациям. Часто отмечается недостаточно активное при-менение рекомендуемых методов лечения. Выполне-ние рекомендаций приводило к улучшению исходов упациентов с ОКС, в том числе к снижению смертности[318]. Таким образом, повышение степени выполнениярекомендаций является приоритетной задачей. Коэф-фициенты риск/польза рекомендуемых методов лече-ния (NNT и NNH) изображены на рис. 4.Чтобы повысить качество лечения и свести к миниму-му его отклонения от рекомендаций, необходимо посто-янно контролировать показатели адекватности тактикиведения пациентов. Внедрение методов лечения, обладающих доказанной эффективностью (рис. 4), может при-вести к более выраженному улучшению сердечно-сосу-дистого здоровья населения по сравнению с таковым вклинических исследованиях, особенно при одновремен-ном применении нескольких эффективных методов.Подобные программы были успешно внедрены в несколь-ких странах, включая Швецию (регистр RIKS-HIA), Вели-кобританию (регистр MINAP), Германию, Италию и Из-раиль. Программы оценки качества лечения были так-же разработаны Европейским обществом кардиологови используются в рамках Euro Heart Survey Programme.Наиболее информативные показатели перечисле-ны в табл. 11.
Таблица 11. Критерии качества медицинской помощипациентам с ИМ без подъема сегмента ST
 Рекомендации по оценке качества медицинскойпомощи
Рекомендации по оценке качества медицинскойпомощи
 Рис. 4. Польза и риск различных методов лечения
Рис. 4. Польза и риск различных методов лечения
 Стратегия ведения пациентов
В этом разделе обобщены этапы диагностики илечения, которые более подробно рассматриваются впредыдущих разделах. Эта информация поможет стан-дартизовать ведение пациентов и улучшить качество ока-зываемой им помощи. Однако у конкретных пациен-тов возможны отклонения от предлагаемой стратегиилечения, так как ОКС без подъема сегмента ST являет-ся неоднородным заболеванием с точки зрения рискасмерти, ИМ или повторного ИМ. В каждом случае врачдолжен принять индивидуальное решение с учетоманамнеза (сопутствующие заболевания, возраст и т.д.),клинического состояния, результатов первых исследо-ваний и доступных медикаментозных и немедика-ментозных методов лечения.
Первый этап: начальное обследованиеБоль или дискомфорт в груди и другие симптомы,заставляющие заподозрить ОКС. Они вынуждают пациента обратиться за медицинской помощью или госпитализироваться. Пациент с предпо-лагаемым диагнозом ОКС без подъема сегмента ST дол-жен быть немедленно осмотрен квалифицированнымврачом. Наиболее адекватная медицинская помощь мо-жет быть оказана в специализированных отделениях ин-тенсивной терапии [47].На первом этапе необходимо быстро установить ра-бочий диагноз и выбрать стратегию лечения на осно-вании следующих критериев: • характер боли в груди и результаты физического об-следования; • вероятность ИБС (возраст, факторы риска, ИМ, КШили ЧКВ в анамнезе);• ЭКГ (отклонения сегмента ST или другие измене-ния).На основании этих данных в течение первых 10 минможно установить один из следующих рабочих диаг-нозов:• ИМ с подъемом сегмента ST;• ОКС без подъема сегмента ST;• ОКС маловероятен.Лечение пациентов с ИМ с подъемом сегмента STрассматривается в соответствующих рекомендациях [2]. Относить пациентов к третьей категории (маловеро-ятный диагноз ОКС) следует осторожно при наличиидругой явной причины (например, травма грудной клет-ки). Методы лечения обобщены в табл. 12.При поступлении пациента в стационар необходи-мо взять кровь, результаты анализа которой должныбыть известны в течение 60 мин. Их используют на вто-ром этапе оказания помощи. Первые анализы кровивключают в себя тропонин Т или I, креатинин, гемогло-бин, глюкозу крови и число клеток крови в дополнениек стандартным биохимическим показателям.Если установлен диагноз ОКС без подъема сегмен-та ST, переходят ко второму этапу.
Таблица 12. Начальные лечебные меры
Стратегия ведения пациентов
В этом разделе обобщены этапы диагностики илечения, которые более подробно рассматриваются впредыдущих разделах. Эта информация поможет стан-дартизовать ведение пациентов и улучшить качество ока-зываемой им помощи. Однако у конкретных пациен-тов возможны отклонения от предлагаемой стратегиилечения, так как ОКС без подъема сегмента ST являет-ся неоднородным заболеванием с точки зрения рискасмерти, ИМ или повторного ИМ. В каждом случае врачдолжен принять индивидуальное решение с учетоманамнеза (сопутствующие заболевания, возраст и т.д.),клинического состояния, результатов первых исследо-ваний и доступных медикаментозных и немедика-ментозных методов лечения.
Первый этап: начальное обследованиеБоль или дискомфорт в груди и другие симптомы,заставляющие заподозрить ОКС. Они вынуждают пациента обратиться за медицинской помощью или госпитализироваться. Пациент с предпо-лагаемым диагнозом ОКС без подъема сегмента ST дол-жен быть немедленно осмотрен квалифицированнымврачом. Наиболее адекватная медицинская помощь мо-жет быть оказана в специализированных отделениях ин-тенсивной терапии [47].На первом этапе необходимо быстро установить ра-бочий диагноз и выбрать стратегию лечения на осно-вании следующих критериев: • характер боли в груди и результаты физического об-следования; • вероятность ИБС (возраст, факторы риска, ИМ, КШили ЧКВ в анамнезе);• ЭКГ (отклонения сегмента ST или другие измене-ния).На основании этих данных в течение первых 10 минможно установить один из следующих рабочих диаг-нозов:• ИМ с подъемом сегмента ST;• ОКС без подъема сегмента ST;• ОКС маловероятен.Лечение пациентов с ИМ с подъемом сегмента STрассматривается в соответствующих рекомендациях [2]. Относить пациентов к третьей категории (маловеро-ятный диагноз ОКС) следует осторожно при наличиидругой явной причины (например, травма грудной клет-ки). Методы лечения обобщены в табл. 12.При поступлении пациента в стационар необходи-мо взять кровь, результаты анализа которой должныбыть известны в течение 60 мин. Их используют на вто-ром этапе оказания помощи. Первые анализы кровивключают в себя тропонин Т или I, креатинин, гемогло-бин, глюкозу крови и число клеток крови в дополнениек стандартным биохимическим показателям.Если установлен диагноз ОКС без подъема сегмен-та ST, переходят ко второму этапу.
Таблица 12. Начальные лечебные меры
 Второй этап: подтверждение диагноза и оценкарискаПациентам с диагнозом ОКС без подъема сегментаST назначают антитромботические препараты внутри-венно и внутрь (табл. 13). Тактику дальнейшего веде-ния определяют с учетом дополнительной информации:• ответ на антиангинальную терапию;• биохимические показатели, особенно уровнитропонинов (при поступлении и через 6-9 ч) и другиебиомаркеры с учетом рабочих диагнозов (например,D-димер, МНП, NT-проМНП); если возможно приме-нение высокочувствительного метода анализа тропо-нинов, может быть внедрен протокол быстрого исклю-чения ОКС (3 ч) (рис. 5);• повторное или постоянное (если возможно) мо-ниторирование сегмента ST; • оценка риска ишемических исходов (индексGRACE);• эхокардиография;• дополнительные методы: рентгенография груднойклетки, КТ, МРТ или сцинтиграфия для дифференци-альной диагностики (например, расслоение стенкиаорты, тромбоэмболия легочной артерии и др.);• оценка риска кровотечений (индекс CRUSADE).На втором этапе подтверждают или исключаютдругие диагнозы, такие как тромбоэмболия легочнойартерии или аневризма аорты (см. табл. 4 и раздел 3.3.).Лечение выбирают индивидуально с учетом рисканеблагоприятных исходов, который оценивали при по-ступлении, а также в динамике с учетом клиническихсимптомов и результатов биохимических исследованийи визуализирующих методов.Оценка риска является важным компонентом про-цесса принятия решения. Риск следует постоянно оце-нивать в динамике. Необходимо определять рискишемических исходов и геморрагических осложнений.Факторы риска часто перекрещиваются, поэтому у па-циентов с высоким риском ишемических исходов рисккровотечений часто также высокий. Важное значениеимеет выбор адекватной терапии (двойная или трой-ная антитромбоцитарная терапия или антикоагулянты),а также доз лекарственных препаратов и доступа для ан-гиографии. Особое внимание следует уделять дисфунк-ции почек, которая особенно часто встречается у пожи-лых людей и пациентов с диабетом. Методы медика-ментозной терапии суммированы в табл. 13.
Таблица 13. Методы лечения, которые рекомендуютсяв тех случаях, когда диагноз ОКСпредставляется вероятным
Второй этап: подтверждение диагноза и оценкарискаПациентам с диагнозом ОКС без подъема сегментаST назначают антитромботические препараты внутри-венно и внутрь (табл. 13). Тактику дальнейшего веде-ния определяют с учетом дополнительной информации:• ответ на антиангинальную терапию;• биохимические показатели, особенно уровнитропонинов (при поступлении и через 6-9 ч) и другиебиомаркеры с учетом рабочих диагнозов (например,D-димер, МНП, NT-проМНП); если возможно приме-нение высокочувствительного метода анализа тропо-нинов, может быть внедрен протокол быстрого исклю-чения ОКС (3 ч) (рис. 5);• повторное или постоянное (если возможно) мо-ниторирование сегмента ST; • оценка риска ишемических исходов (индексGRACE);• эхокардиография;• дополнительные методы: рентгенография груднойклетки, КТ, МРТ или сцинтиграфия для дифференци-альной диагностики (например, расслоение стенкиаорты, тромбоэмболия легочной артерии и др.);• оценка риска кровотечений (индекс CRUSADE).На втором этапе подтверждают или исключаютдругие диагнозы, такие как тромбоэмболия легочнойартерии или аневризма аорты (см. табл. 4 и раздел 3.3.).Лечение выбирают индивидуально с учетом рисканеблагоприятных исходов, который оценивали при по-ступлении, а также в динамике с учетом клиническихсимптомов и результатов биохимических исследованийи визуализирующих методов.Оценка риска является важным компонентом про-цесса принятия решения. Риск следует постоянно оце-нивать в динамике. Необходимо определять рискишемических исходов и геморрагических осложнений.Факторы риска часто перекрещиваются, поэтому у па-циентов с высоким риском ишемических исходов рисккровотечений часто также высокий. Важное значениеимеет выбор адекватной терапии (двойная или трой-ная антитромбоцитарная терапия или антикоагулянты),а также доз лекарственных препаратов и доступа для ан-гиографии. Особое внимание следует уделять дисфунк-ции почек, которая особенно часто встречается у пожи-лых людей и пациентов с диабетом. Методы медика-ментозной терапии суммированы в табл. 13.
Таблица 13. Методы лечения, которые рекомендуютсяв тех случаях, когда диагноз ОКСпредставляется вероятным
 Рис. 5. Алгоритм быстрого исключения ОКС с помощью высокочувствительного метода определения тропонина
Рис. 5. Алгоритм быстрого исключения ОКС с помощью высокочувствительного метода определения тропонина
 Третий этап: инвазивная стратегия• Катетеризация сердца с последующей реваскуля-ризацией предупреждали развитие рецидивирующейишемии и/или улучшали ближайший или отдаленныйпрогноз. Выделены несколько факторов риска (повы-шение уровня тропонина, депрессия сегмента ST, по-чечная недостаточность и др.), которые позволяютпредсказать отдаленную эффективность инвазивнойстратегии. В зависимости от степени повышения рис-ка ангиография может быть проведена в следующиесроки (рис. 6):• Инвазивное лечение (<72 ч)— неотложное (<120 мин);— раннее (<24 ч).• Первичная консервативная стратегия.Оптимальные сроки вмешательства зависят от про-филя риска конкретного пациента и могут быть выбра-ны на основании нескольких показателей.Неотложная инвазивная стратегия (в течение первых 120 минпосле первого контакта с врачом)Эта стратегия обоснованна у пациентов с оченьвысоким риском:• Рефрактерная стенокардия (включая формирую-щийся ИМ без отклонений сегмента ST).• Рецидивирующая стенокардия, несмотря на анти-ангинальную терапию, в сочетании с депрессией сег-мента ST (2 мм) или глубокими отрицательными зуб-цами Т.• Клинические симптомы сердечной недостаточно-сти или нестабильная гемодинамика (шок). • Угрожающие жизни аритмии (желудочковая тахи-кардия или фибрилляция желудочков).Перед катетеризацией таким пациентам можноввести блокатор GP IIb/IIIa рецепторов (эптифибатидили тирофибан). Список антитромботических препа-ратов, которые применяют перед ЧКВ, приведен втабл. 14.
Рис. 6. Алгоритм принятия решения при ОКС
Третий этап: инвазивная стратегия• Катетеризация сердца с последующей реваскуля-ризацией предупреждали развитие рецидивирующейишемии и/или улучшали ближайший или отдаленныйпрогноз. Выделены несколько факторов риска (повы-шение уровня тропонина, депрессия сегмента ST, по-чечная недостаточность и др.), которые позволяютпредсказать отдаленную эффективность инвазивнойстратегии. В зависимости от степени повышения рис-ка ангиография может быть проведена в следующиесроки (рис. 6):• Инвазивное лечение (<72 ч)— неотложное (<120 мин);— раннее (<24 ч).• Первичная консервативная стратегия.Оптимальные сроки вмешательства зависят от про-филя риска конкретного пациента и могут быть выбра-ны на основании нескольких показателей.Неотложная инвазивная стратегия (в течение первых 120 минпосле первого контакта с врачом)Эта стратегия обоснованна у пациентов с оченьвысоким риском:• Рефрактерная стенокардия (включая формирую-щийся ИМ без отклонений сегмента ST).• Рецидивирующая стенокардия, несмотря на анти-ангинальную терапию, в сочетании с депрессией сег-мента ST (2 мм) или глубокими отрицательными зуб-цами Т.• Клинические симптомы сердечной недостаточно-сти или нестабильная гемодинамика (шок). • Угрожающие жизни аритмии (желудочковая тахи-кардия или фибрилляция желудочков).Перед катетеризацией таким пациентам можноввести блокатор GP IIb/IIIa рецепторов (эптифибатидили тирофибан). Список антитромботических препа-ратов, которые применяют перед ЧКВ, приведен втабл. 14.
Рис. 6. Алгоритм принятия решения при ОКС
 Таблица 14. Антитромботические препаратыперед ЧКВ
Таблица 14. Антитромботические препаратыперед ЧКВ
 Ранняя инвазивная стратегия (в течение первых 24 ч послепервого контакта с врачом)Большинство пациентов первоначально отвечают наантиангинальную терапию, однако у них отмечается повышенный риск и необходима ангиография с реваску-ляризацией. Пациентам с высоким риском (индексGRACE>140 и/или наличие по крайней мере одногокритерия высокого риска; табл. 9) инвазивное обсле-дование следует провести в течение 24 ч.Инвазивная стратегия (в течение 72 ч после первого контакта сврачом)У пациентов с более низким риском, у которых нерецидивируют симптомы, ангиография может быть про-ведена в течение 72 ч. Таким образом, им следует про-вести плановое инвазивное обследование при первойвозможности с учетом локальных условий.Консервативная стратегия (ангиография не проводится иливыполняется в плановом порядке)При отсутствии перечисленных ниже критериевриск является низким, поэтому раннее инвазивноеобследование не требуется:• отсутствие рецидивирующей боли в груди;• отсутствие сердечной недостаточности;• отсутствие изменений на первой или второй(через 6-9 ч) ЭКГ;• нормальный уровень тропонина (при поступлениии через 6-9 ч);• отсутствие стресс-индуцированной ишемии.Пациентам с низким риском (см. раздел 4.4.) пока-зано консервативное ведение. Последующее лечениевыбирают с учетом тактики ведения пациентов со ста-бильной ИБС [319]. Перед выпиской из стационара не-обходимо провести стресс-пробу с целью планирова-ния дальнейшего ведения и оценки необходимости вплановой ангиографии.
Таблица 15. Рекомендуемые методы леченияперед выпиской
Ранняя инвазивная стратегия (в течение первых 24 ч послепервого контакта с врачом)Большинство пациентов первоначально отвечают наантиангинальную терапию, однако у них отмечается повышенный риск и необходима ангиография с реваску-ляризацией. Пациентам с высоким риском (индексGRACE>140 и/или наличие по крайней мере одногокритерия высокого риска; табл. 9) инвазивное обсле-дование следует провести в течение 24 ч.Инвазивная стратегия (в течение 72 ч после первого контакта сврачом)У пациентов с более низким риском, у которых нерецидивируют симптомы, ангиография может быть про-ведена в течение 72 ч. Таким образом, им следует про-вести плановое инвазивное обследование при первойвозможности с учетом локальных условий.Консервативная стратегия (ангиография не проводится иливыполняется в плановом порядке)При отсутствии перечисленных ниже критериевриск является низким, поэтому раннее инвазивноеобследование не требуется:• отсутствие рецидивирующей боли в груди;• отсутствие сердечной недостаточности;• отсутствие изменений на первой или второй(через 6-9 ч) ЭКГ;• нормальный уровень тропонина (при поступлениии через 6-9 ч);• отсутствие стресс-индуцированной ишемии.Пациентам с низким риском (см. раздел 4.4.) пока-зано консервативное ведение. Последующее лечениевыбирают с учетом тактики ведения пациентов со ста-бильной ИБС [319]. Перед выпиской из стационара не-обходимо провести стресс-пробу с целью планирова-ния дальнейшего ведения и оценки необходимости вплановой ангиографии.
Таблица 15. Рекомендуемые методы леченияперед выпиской
 Четвертый этап: методы реваскуляризацииЕсли при ангиографии выявлены атероматозныеизменения, однако отсутствует критический стеноз ко-ронарных артерий, показана медикаментозная терапия.Необходимо пересмотреть диагноз ОКС без подъема сег-мента ST с учетом других возможных причин появлениясимптомов. Однако отсутствие критического стеноза неисключает диагноз ОКС, если клинические симптомы ука-зывают на ишемическую боль в груди и определяютсябиомаркеры. В этом случае пациенты должны получатьлечение в соответствии с рекомендациями по ведениюпациентов с ОКС без подъема сегмента ST.Рекомендации по выбору метода реваскуляризацииу пациентов с ОКС без подъема сегмента ST соответ-ствуют рекомендациям по выбору метода плановоговмешательства. У пациента со стенозом одной коронар-ной артерии методом выбора является ЧКВ. У пациен-тов с поражением нескольких сосудов выбор между ЧКВи КШ должен быть индивидуальным в соответствии спротоколом лечебного учреждения. В некоторых слу-чаях оправданно ЧКВ на ведущей артерии и последую-щее плановое шунтирование других пораженных со-судов с учетом результатов оценки ишемии и/илифункционального резерва кровотока.Во время ЧКВ не следует менять антикоагулянты. Па-циентам, получавшим фондапаринукс, перед ЧКВ сле-дует добавить НФГ. Применение блокатора GP IIb/IIIaрецепторов оправданно при повышенном уровне тро-понинов или наличии ангиографических признаковтромба. Если планируется КШ, следует отменить бло-каторы P2Y12 рецепторов и отложить операцию, еслиэто позволяют клиническое состояние и ангиографиче-ские данные.Если ангиография указывает на невозможность ре-васкуляризации в связи с распространенностью и/илилокализацией поражений, необходимо усилить меди-каментозную терапию и назначить меры вторичной про-филактики.
Пятый этап: выписка из стационара и наблюдениепосле выпискиХотя большинство нежелательных событий у паци-ентов с ОКС без подъема сегмента ST наблюдают на ран-нем этапе, риск ИМ или смерти остается повышеннымв течение нескольких мес. После ранней реваскуляри-зации риск развития угрожающих жизни аритмийнизкий (2,5%); 80% из них развиваются в течение пер-вых 12 ч после появления симптомов [320]. Соответ-ственно, продолжение мониторирования после24-48 ч обычно не требуется. Пациенты с ОКС безподъема сегмента ST должны находиться в стациона-ре в течение по крайней мере 24 ч после успешного стен-тирования ведущего стеноза. Всем пациентам показа-ны интенсивная модификация риска и улучшение об-раза жизни (см. раздел 5.6.). Включение пациента в про-грамму реабилитации после выписки повышает при-верженность и может способствовать модификациифакторов риска. Необходимые меры профилактикипосле выписки из стационара указаны в табл. 15.
Литература
1. Murray CJ, Lopez AD. Alternative projections of mortality and disability by cause 1990–2020: Global Burden ofDisease Study. Lancet 1997;349:1498–1504. 2. Van deWerf F, Bax J, Betriu A, Blomstrom-Lundqvist C, Crea F, Falk V, Filippatos G, Fox K, Huber K, Kastrati A,Rosengren A, Steg PG, Tubaro M, Verheugt F, Weidinger F, Weis M. Management of acute myocardial infarctionin patients presenting with persistent ST-segment elevation: the Task Force on the Management of ST-SegmentElevation Acute Myocardial Infarction of the European Society of Cardiology. Eur Heart J 2008;29:2909–2945.3. Bassand JP, Hamm CW, Ardissino D, Boersma E, Budaj A, Fernandez-Aviles F, Fox KA, Hasdai D, Ohman EM,Wallentin L, Wijns W. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronarysyndromes. Eur Heart J 2007;28:1598–1660.4. Yeh RW, Sidney S, Chandra M, Sorel M, Selby JV, Go AS. Population trends in the incidence and outcomes of acutemyocardial infarction. N Engl J Med 2010;362:2155–2165.5. Fox KA, Eagle KA, Gore JM, Steg PG, Anderson FA. The Global Registry of Acute Coronary Events, 1999 to 2009—GRACE. Heart 2010;96:1095–1101.6. Savonitto S, Ardissino D, Granger CB, Morando G, Prando MD, Mafrici A, Cavallini C, Melandri G, Thompson TD,Vahanian A, Ohman EM, Califf RM, Van de Werf F, Topol EJ. Prognostic value of the admission electrocardiogramin acute coronary syndromes. JAMA 1999;281:707–713.7. Mandelzweig L, Battler A, Boyko V, Bueno H, Danchin N, Filippatos G, Gitt A, Hasdai D, Hasin Y, Marrugat J,Van de Werf F, Wallentin L, Behar S. The second Euro Heart Survey on acute coronary syndromes: characteristics,treatment, and outcome of patients with ACS in Europe and the Mediterranean Basin in 2004. Eur Heart J2006;27:2285–2293.8. Terkelsen CJ, Lassen JF, Norgaard BL, Gerdes JC, Jensen T, Gotzsche LB, Nielsen TT, Andersen HR. Mortality ratesin patients with ST-elevation vs. non-ST-elevation acute myocardial infarction: observations from an unselectedcohort. Eur Heart J 2005;26:18–26.9. Hamm CW, Mo¨llmann H, Bassand JP, Van deWerf F. Acute coronary syndrome. In: Camm AJ, Lu¨scher TF, SerruysPW, eds. The ESC Textbook of Cardiovascular Medicine. 2nd ed. Oxford: Oxford University Press; 2009.10. Stone GW, Maehara A, Lansky AJ, de Bruyne B, Cristea E, Mintz GS, Mehran R, McPherson J, Farhat N, MarsoSP, Parise H, Templin B, White R, Zhang Z, Serruys PW. A prospective natural-history study of coronary atherosclerosis.N Engl J Med 2011;364:226–235.11. Campeau L. Grading of angina pectoris. Circulation 1976;54:522–523.12. van Domburg RT, van Miltenburg-van Zijl AJ, Veerhoek RJ, Simoons ML. Unstable angina: good long-term outcomeafter a complicated early course. J Am Coll Cardiol 1998;31:1534–1539.13. Canto JG, Fincher C, Kiefe CI, Allison JJ, Li Q, Funkhouser E, Centor RM, Selker HP,Weissman NW. Atypical presentationsamong Medicare beneficiaries with unstable angina pectoris. Am J Cardiol 2002;90:248–253.14. Culic V, Eterovic D, Miric D, Silic N. Symptom presentation of acute myocardial infarction: influence of sex, age,and risk factors. Am Heart J 2002;144:1012–1017.15. Brieger D, Eagle KA, Goodman SG, Steg PG, Budaj A, White K, Montalescot G. Acute coronary syndromeswithout chest pain, an underdiagnosed and undertreated high-risk group: insights from the Global Registry ofAcute Coronary Events. Chest 2004;126:461–469.16. Lev EI, Battler A, Behar S, Porter A, Haim M, Boyko V, Hasdai D. Frequency, characteristics, and outcome of patientshospitalized with acute coronary syndromes with undetermined electrocardiographic patterns. Am J Cardiol2003;91:224–227.17. Diercks DB, Peacock WF, Hiestand BC, Chen AY, Pollack CV Jr., Kirk JD, Smith SC Jr., Gibler WB, Ohman EM,Blomkalns AL, Newby LK, Hochman JS, Peterson ED, Roe MT. Frequency and consequences of recording an electrocardiogram.10 min after arrival in an emergency room in non-ST-segment elevation acute coronary syndromes(from the CRUSADE Initiative). Am J Cardiol 2006;97:437–442.18. Thygesen K, Alpert JS, White HD, Jaffe AS, Apple FS, Galvani M, Katus HA, Newby LK, Ravkilde J, Chaitman B,Clemmensen PM, Dellborg M, Hod H, Porela P, Underwood R, Bax JJ, Beller GA, Bonow R, Van der Wall EE, BassandJP, Wijns W, Ferguson TB, Steg PG, Uretsky BF, Williams DO, Armstrong PW, Antman EM, Fox KA, HammCW, Ohman EM, Simoons ML, Poole-Wilson PA, Gurfinkel EP, Lopez-Sendon JL, Pais P, Mendis S, Zhu JR, WallentinLC, Fernandez-Aviles F, Fox KM, Parkhomenko AN, Priori SG, Tendera M, Voipio-Pulkki LM, Vahanian A,Camm AJ, De Caterina R, Dean V, Dickstein K, Filippatos G, Funck-Brentano C, Hellemans I, Kristensen SD, Mc-Gregor K, Sechtem U, Silber S, Widimsky P, Zamorano JL, Morais J, Brener S, Harrington R, Morrow D, Lim M,Martinez-Rios MA, Steinhubl S, Levine GN, Gibler WB, Goff D, Tubaro M, Dudek D, Al-Attar N. Universal definitionof myocardial infarction. Circulation 2007;116:2634–2653.19. Okamatsu K, Takano M, Sakai S, Ishibashi F, Uemura R, Takano T, Mizuno K. Elevated troponin T levels and lesioncharacteristics in non-ST-elevation acute coronary syndromes. Circulation 2004;109:465–470.20. Keller T, Zeller T, Peetz D, Tzikas S, Roth A, Czyz E, Bickel C, Baldus S, Warnholtz A, Frohlich M, Sinning CR,Eleftheriadis MS, Wild PS, Schnabel RB, Lubos E, Jachmann N, Genth-Zotz S, Post F, Nicaud V, Tiret L, LacknerKJ, Munzel TF, Blankenberg S. Sensitive troponin I assay in early diagnosis of acute myocardial infarction. N EnglJ Med 2009;361:868–877.21. Reichlin T, Hochholzer W, Bassetti S, Steuer S, Stelzig C, Hartwiger S, Biedert S, Schaub N, Buerge C, Potocki M,Noveanu M, Breidthardt T, Twerenbold R, Winkler K, Bingisser R, Mueller C. Early diagnosis of myocardial infarctionwith sensitive cardiac troponin assays. N Engl J Med 2009;361:858–867.22. Giannitsis E, Becker M, Kurz K, Hess G, Zdunek D, Katus HA. High-sensitivity cardiac troponin T for early predictionof evolving non-ST-segment elevation myocardial infarction in patients with suspected acute coronarysyndrome and negative troponin results on admission. Clin Chem 2010;56:642–650.23. Weber M, Bazzino O, Estrada JJN, Miguel R, Salzberg S, Fuselli JJ, Liebetrau C, Woelken M, Moellmann H, NefH, Hamm C. Improved diagnostic and prognostic performance of a new high-sensitive troponin T assay in patientswith acute coronary syndrome. Am Heart J 2011;162:81–88.24. Omland T, de Lemos JA, Sabatine MS, Christophi CA, Rice MM, Jablonski KA, Tjora S, Domanski MJ, Gersh BJ,Rouleau JL, Pfeffer MA, Braunwald E. A sensitive cardiac troponin T assay in stable coronary artery disease. NEngl J Med 2009;361:2538–2547.25. de Lemos JA, Drazner MH, Omland T, Ayers CR, Khera A, Rohatgi A, Hashim I, Berry JD, Das SR, Morrow DA,McGuire DK. Association of troponin T detected with a highly sensitive assay and cardiac structure and mortalityrisk in the general population. JAMA 2010;304:2503–2512.26. Otsuka T, Kawada T, Ibuki C, Seino Y. Association between high-sensitivity cardiac troponin T levels and thepredicted cardiovascular risk in middle-aged men without overt cardiovascular disease. Am Heart J2010;159:972–978.27. Thygesen K, Mair J, Katus H, Plebani M, Venge P, Collinson P, Lindahl B, Giannitsis E, Hasin Y, Galvani M, TubaroM, Alpert JS, Biasucci LM, Koenig W, Mueller C, Huber K, Hamm C, Jaffe AS. Recommendations for the use ofcardiac troponin measurement in acute cardiac care. Eur Heart J 2010;31:2197–2204.28. Apple FS, Murakami MM, Pearce LA, Herzog CA. Predictive value of cardiac troponin I and T for subsequentdeath in end-stage renal disease. Circulation 2002;106:2941–2945.29. Aviles RJ, Askari AT, Lindahl B, Wallentin L, Jia G, Ohman EM, Mahaffey KW, Newby LK, Califf RM, Simoons ML,Topol EJ, Berger P, Lauer MS. Troponin T levels in patients with acute coronary syndromes, with or without renaldysfunction. N Engl J Med 2002;346:2047–2052.30. Hamm CW, Goldmann BU, Heeschen C, Kreymann G, Berger J, Meinertz T. Emergency room triage of patientswith acute chest pain by means of rapid testing for cardiac troponin T or troponin I. N Engl J Med1997;337:1648–1653.31. Wu AH, Apple FS, Gibler WB, Jesse RL, Warshaw MM, Valdes R Jr. National Academy of Clinical BiochemistryStandards of Laboratory Practice: recommendations for the use of cardiac markers in coronary artery diseases.Clin Chem 1999;45:1104–1121.32. Than M, Cullen L, Reid CM, Lim SH, Aldous S, Ardagh MW, Peacock WF, Parsonage WA, Ho HF, Ko HF, KasliwalRR, Bansal M, Soerianata S, Hu D, Ding R, Hua Q, Seok-Min K, Sritara P, Sae-Lee R, Chiu TF, Tsai KC, Chu FY, ChenWK, Chang WH, Flaws DF, George PM, Richards AM. A 2-h diagnostic protocol to assess patients with chestpain symptoms in the Asia-Pacific region (ASPECT): a prospective observational validation study. Lancet2011;377:1077–1084.33. Cheitlin MD, Armstrong WF, Aurigemma GP, Beller GA, Bierman FZ, Davis JL, Douglas PS, Faxon DP, Gillam LD,Kimball TR, Kussmaul WG, Pearlman AS, Philbrick JT, Rakowski H, Thys DM, Antman EM, Smith SC Jr., AlpertJS, Gregoratos G, Anderson JL, Hiratzka LF, Hunt SA, Fuster V, Jacobs AK, Gibbons RJ, Russell RO. ACC/AHA/ASE2003 guideline update for the clinical application of echocardiography: summary article: a report of the AmericanCollege of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASE Committeeto Update the 1997 Guidelines for the Clinical Application of Echocardiography). Circulation2003;108:1146–1162.34. Nucifora G, Badano LP, Sarraf-Zadegan N, Karavidas A, Trocino G, Scaffidi G, Pettinati G, Astarita C, VysniauskasV, Gregori D, Ilerigelen B, Marinigh R, Fioretti PM. Comparison of early dobutamine stress echocardiography andexercise electrocardiographic testing for management of patients presenting to the emergency departmentwith chest pain. Am J Cardiol 2007;100:1068–1073.35. Kwong RY, Schussheim AE, Rekhraj S, Aletras AH, Geller N, Davis J, Christian TF, Balaban RS, Arai AE. Detectingacute coronary syndrome in the emergency department with cardiac magnetic resonance imaging. Circulation2003;107:531–537.36. Udelson JE, Beshansky JR, Ballin DS, Feldman JA, Griffith JL, Handler J, Heller GV, Hendel RC, Pope JH, RuthazerR, Spiegler EJ, Woolard RH, Selker HP. Myocardial perfusion imaging for evaluation and triage of patientswith suspected acute cardiac ischemia: a randomized controlled trial. JAMA 2002;288:2693–2700.37. Hoffmann U, Bamberg F, Chae CU, Nichols JH, Rogers IS, Seneviratne SK, Truong QA, Cury RC, Abbara S, ShapiroMD, Moloo J, Butler J, Ferencik M, Lee H, Jang IK, Parry BA, Brown DF, Udelson JE, Achenbach S, Brady TJ,Nagurney JT. Coronary computed tomography angiography for early triage of patients with acute chest pain:the ROMICAT (Rule Out Myocardial Infarction using Computer Assisted Tomography) trial. J Am Coll Cardiol2009;53:1642–1650.38. Rubinshtein R, Halon DA, Gaspar T, Jaffe R, Karkabi B, Flugelman MY, Kogan A, Shapira R, Peled N, Lewis BS.Usefulness of 64-slice cardiac computed tomographic angiography for diagnosing acute coronary syndromesand predicting clinical outcome in emergency department patients with chest pain of uncertain origin. Circulation2007;115:1762–1768.39. Meijboom WB, Mollet NR, Van Mieghem CA, Weustink AC, Pugliese F, van Pelt N, Cademartiri F, Vourvouri E,de Jaegere P, Krestin GP, de Feyter PJ 64-Slice CT coronary angiography in patients with non-ST elevation acutecoronary syndrome. Heart 2007;93:1386–1392.40. Hollander JE, Chang AM, Shofer FS, Collin MJ, Walsh KM, McCusker CM, Baxt WG, Litt HI. One-year outcomesfollowing coronary computerized tomographic angiography for evaluation of emergency department patientswith potential acute coronary syndrome. Acad Emerg Med 2009;16:693–698.41. Chang SA, Choi SI, Choi EK, Kim HK, Jung JW, Chun EJ, Kim KS, Cho YS, Chung WY, Youn TJ, Chae IH, Choi DJ,Chang HJ. Usefulness of 64-slice multidetector computed tomography as an initial diagnostic approach in patientswith acute chest pain. Am Heart J 2008;156:375–383.42. Effects of tissue plasminogen activator and a comparison of early invasive and conservative strategies in unstableangina and non-Q-wave myocardial infarction. Results of the TIMI IIIB Trial. Thrombolysis in Myocardial Ischemia.Circulation 1994;89:1545–1556.43. Invasive compared with non-invasive treatment in unstable coronary-artery disease: FRISC II prospective randomisedmulticentre study. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators.Lancet 1999;354:708–715.44. Tonino PA, De Bruyne B, Pijls NH, Siebert U, Ikeno F, van’ t Veer M, Klauss V, Manoharan G, Engstrom T, OldroydKG, Ver Lee PN, MacCarthy PA, Fearon WF. Fractional flow reserve versus angiography for guiding percutaneouscoronary intervention. N Engl J Med 2009;360:213–224.45. Jolly SS, Yusuf S, Cairns J, Niemela K, Xavier D, Widimsky P, Budaj A, Niemela M, Valentin V, Lewis BS, AvezumA, Steg PG, Rao SV, Gao P, Afzal R, Joyner CD, Chrolavicius S, Mehta SR. Radial versus femoral access for coronaryangiography and intervention in patients with acute coronary syndromes (RIVAL): a randomised, parallelgroup, multicentre trial. Lancet 2011;377:1409–1420.46. Hasdai D, Lev EI, Behar S, Boyko V, Danchin N, Vahanian A, Battler A. Acute coronary syndromes in patients withpre-existing moderate to severe valvular disease of the heart: lessons from the Euro-Heart Survey of acute coronarysyndromes. Eur Heart J 2003;24:623–629.47. Hasin Y, Danchin N, Filippatos GS, Heras M, Janssens U, Leor J, Nahir M, Parkhomenko A, Thygesen K, TubaroM, Wallentin LC, Zakke I. Recommendations for the structure, organization, and operation of intensive cardiaccare units. Eur Heart J 2005;26:1676–1682.48. Granger CB, Goldberg RJ, Dabbous O, Pieper KS, Eagle KA, Cannon CP, Van De Werf F, Avezum A, GoodmanSG, Flather MD, Fox KA. Predictors of hospital mortality in the global registry of acute coronary events. Arch InternMed 2003;163:2345–2353.49. Antman EM, Cohen M, Bernink PJ, McCabe CH, Horacek T, Papuchis G, Mautner B, Corbalan R, Radley D,Braunwald E. The TIMI risk score for unstable angina/non-ST elevation MI: a method for prognostication andtherapeutic decision making. JAMA 2000;284:835–842.50. Fox KA, Dabbous OH, Goldberg RJ, Pieper KS, Eagle KA, Van de Werf F, Avezum A, Goodman SG, Flather MD,Anderson FA Jr., Granger CB. Prediction of risk of death and myocardial infarction in the six months after presentationwith acute coronary syndrome: prospective multinational observational study (GRACE). BMJ2006;333:1091. 51. Carrillo X, Curos A, Muga R, Serra J, Sanvisens A, Bayes-Genis A. Acute coronary syndrome and cocaine use:8-year prevalence and inhospital outcomes. Eur Heart J 2011;32:1244–1250.52. Holmvang L, Clemmensen P, Lindahl B, Lagerqvist B, Venge P, Wagner G, Wallentin L, Grande P. Quantitativeanalysis of the admission electrocardiogram identifies patients with unstable coronary artery disease who benefitthe most from early invasive treatment. J Am Coll Cardiol 2003;41:905–915.53. Kaul P, Fu Y, Chang WC, Harrington RA, Wagner GS, Goodman SG, Granger CB, Moliterno DJ, Van de Werf F,Califf RM, Topol EJ, Armstrong PW. Prognostic value of ST segment depression in acute coronary syndromes:insights from PARAGON-A applied to GUSTO-IIb. PARAGON-A and GUSTO IIb Investigators. Platelet IIb/IIIa Antagonismfor the Reduction of Acute Global Organization Network. J Am Coll Cardiol 2001;38:64–71.54. Nyman I, Wallentin L, Areskog M, Areskog NH, Swahn E. Risk stratification by early exercise testing after anepisode of unstable coronary artery disease. The RISC Study Group. Int J Cardiol 1993;39:131–142.55. Amsterdam EA, Kirk JD, Diercks DB, Lewis WR, Turnipseed SD. Immediate exercise testing to evaluate low-riskpatients presenting to the emergency department with chest pain. J Am Coll Cardiol 2002;40:251–256.56. Scirica BM, Morrow DA, Budaj A, Dalby AJ, Mohanavelu S, Qin J, Aroesty J, Hedgepeth CM, Stone PH, BraunwaldE. Ischemia detected on continuous electrocardiography after acute coronary syndrome: observationsfrom the MERLIN-TIMI 36 (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST-Elevation AcuteCoronary Syndrome-Thrombolysis In Myocardial Infarction 36) trial. J Am Coll Cardiol 2009;53:1411–1421.57. Akkerhuis KM, Klootwijk PA, Lindeboom W, Umans VA, Meij S, Kint PP, Simoons ML. Recurrent ischaemia duringcontinuous multilead ST-segment monitoring identifies patients with acute coronary syndromes at highrisk of adverse cardiac events; meta-analysis of three studies involving 995 patients. Eur Heart J2001;22:1997–2006.58. Antman EM, Tanasijevic MJ, Thompson B, Schactman M, McCabe CH, Cannon CP, Fischer GA, Fung AY, ThompsonC, Wybenga D, Braunwald E. Cardiac-specific troponin I levels to predict the risk of mortality in patients withacute coronary syndromes. N Engl J Med 1996;335:1342–1349.59. Kontos MC, de Lemos JA, Ou FS, Wiviott SD, Foody JM, Newby LK, Chen A, Roe MT. Troponin-positive, MBnegativepatients with non-ST-elevation myocardial infarction: an undertreated but high-risk patient group:results from the National Cardiovascular Data Registry Acute Coronary Treatment and Intervention OutcomesNetwork—Get With The Guidelines (NCDR ACTION-GWTG) Registry. Am Heart J 2010;160:819–825.60. James SK, Lindahl B, Siegbahn A, Stridsberg M, Venge P, Armstrong P, Barnathan ES, Califf R, Topol EJ, SimoonsML, Wallentin L. N-terminal pro-brain natriuretic peptide and other risk markers for the separate prediction ofmortality and subsequent myocardial infarction in patients with unstable coronary artery disease: a Global Utilizationof Strategies To Open occluded arteries (GUSTO)-IV substudy. Circulation 2003;108:275–281.61. Steg PG, FitzGerald G, Fox KA. Risk stratification in non-ST-segment elevation acute coronary syndromes: troponinalone is not enough. Am J Med 2009;122: 107–108.62. Thygesen K, Mair J, Mueller C, Huber K, Weber M, Plebani M, Hasin Y, Biasucci LM, Giannitsis E, Lindahl B,Koenig W, Tubaro M, Collinson P, Katus H, Galvani M, Venge P, Alpert JS, Hamm C, Jaffe AS. Recommendationsfor the use of natriuretic peptides in acute cardiac care: a position statement from the Study Group on Biomarkersin Cardiology of the ESC Working Group on Acute Cardiac Care. Eur Heart J 2011;10.1093/eurheartj/ehq509.63. Heeschen C, Hamm CW, Bruemmer J, Simoons ML. Predictive value of Creactive protein and troponin T in patientswith unstable angina: a comparative analysis. CAPTURE Investigators. Chimeric c7E3 AntiPlatelet Therapyin Unstable angina REfractory to standard treatment trial. J Am Coll Cardiol 2000;35:1535–1542.64. Morrow DA, Rifai N, Antman EM, Weiner DL, McCabe CH, Cannon CP, Braunwald E. C-reactive protein is a potentpredictor of mortality independently of and in combination with troponin T in acute coronary syndromes:a TIMI 11A substudy. Thrombolysis in Myocardial Infarction. J Am Coll Cardiol 1998;31:1460–1465.65. Lindahl B, Toss H, Siegbahn A, Venge P, Wallentin L. Markers of myocardial damage and inflammation in relationto long-term mortality in unstable coronary artery disease. FRISC Study Group. Fragmin during Instabilityin Coronary Artery Disease. N Engl J Med 2000;343:1139–1147.66. Currie CJ, Poole CD, Conway P. Evaluation of the association between the first observation and the longitudinalchange in C-reactive protein, and all-cause mortality. Heart 2008;94:457–462.67. Aronson D, Hammerman H, Suleiman M, Markiewicz W. Usefulness of changes in fasting glucose during hospitalizationto predict long-term mortality in patients with acute myocardial infarction. Am J Cardiol2009;104:1013–1017.68. Suleiman M, Hammerman H, Boulos M, Kapeliovich MR, Suleiman A, Agmon Y, Markiewicz W, Aronson D. Fastingglucose is an important independent risk factor for 30-day mortality in patients with acute myocardial infarction:a prospective study. Circulation 2005;111:754–760.69. Sabatine MS, Morrow DA, Giugliano RP, Burton PB, Murphy SA, McCabe CH, Gibson CM, Braunwald E. Associationof hemoglobin levels with clinical outcomes in acute coronary syndromes. Circulation2005;111:2042–2049.70. Mahaffey KW, Yang Q, Pieper KS, Antman EM, White HD, Goodman SG, Cohen M, Kleiman NS, Langer A,Aylward PE, Col JJ, Reist C, Ferguson JJ, Califf RM. Prediction of one-year survival in high-risk patients withacute coronary syndromes: results from the SYNERGY trial. J Gen Intern Med 2008;23:310–316.71. Al Suwaidi J, Reddan DN, Williams K, Pieper KS, Harrington RA, Califf RM, Granger CB, Ohman EM, Holmes DRJr. Prognostic implications of abnormalities in renal function in patients with acute coronary syndromes. Circulation2002;106:974–980.72. Baldus S, Heeschen C, Meinertz T, Zeiher AM, Eiserich JP, Munzel T, Simoons ML, Hamm CW. Myeloperoxidaseserum levels predict risk in patients with acute coronary syndromes. Circulation 2003;108:1440–1445.73. Brennan ML, Penn MS, Van Lente F, Nambi V, Shishehbor MH, Aviles RJ, Goormastic M, Pepoy ML, McErleanES, Topol EJ, Nissen SE, Hazen SL. Prognostic value of myeloperoxidase in patients with chest pain. N Engl JMed 2003;349:1595–1604.74. Wollert KC, Kempf T, Peter T, Olofsson S, James S, Johnston N, Lindahl B, Horn-Wichmann R, Brabant G, SimoonsML, Armstrong PW, Califf RM, Drexler H, Wallentin L. Prognostic value of growth-differentiation factor-15 inpatients with non-ST-elevation acute coronary syndrome. Circulation 2007;115:962–971.75. Morrow DA, Sabatine MS, Brennan ML, de Lemos JA, Murphy SA, Ruff CT, Rifai N, Cannon CP, Hazen SL. Concurrentevaluation of novel cardiac biomarkers in acute coronary syndrome: myeloperoxidase and soluble CD40ligand and the risk of recurrent ischaemic events in TACTICS-TIMI 18. Eur Heart J 2008;29:1096–1102.76. Viswanathan K, Kilcullen N, Morrell C, Thistlethwaite SJ, Sivananthan MU, Hassan TB, Barth JH, Hall AS. Hearttypefatty acid-binding protein predicts long-term mortality and re-infarction in consecutive patients with suspectedacute coronary syndrome who are troponin-negative. J Am Coll Cardiol 2010;55:2590–2598.77. Van Belle E, Dallongeville J, Vicaut E, Degrandsart A, Baulac C, Montalescot G. Ischemia-modified albumin levelspredict long-term outcome in patients with acute myocardial infarction. The French Nationwide OPERAstudy. Am Heart J 2010;159:570–576.78. Reichlin T, Hochholzer W, Stelzig C, Laule K, Freidank H, Morgenthaler NG, Bergmann A, Potocki M, NoveanuM, Breidthardt T, Christ A, Boldanova T, Merki R, Schaub N, Bingisser R, Christ M, Mueller C. Incremental valueof copeptin for rapid rule out of acute myocardial infarction. J Am Coll Cardiol 2009;54:60–68.79. de Araujo Goncalves P, Ferreira J, Aguiar C, Seabra-Gomes R. TIMI, PURSUIT, and GRACE risk scores: sustainedprognostic value and interaction with revascularization in NSTE-ACS. Eur Heart J 2005;26:865–872.80. Aragam KG, Tamhane UU, Kline-Rogers E, Li J, Fox KA, Goodman SG, Eagle KA, Gurm HS. Does simplicitycompromise accuracy in ACS risk prediction? A retrospective analysis of the TIMI and GRACE risk scores. PLoSOne 2009;4:e7947.81. Eggers KM, Kempf T, Venge P, Wallentin L, Wollert KC, Lindahl B. Improving long-term risk prediction in patientswith acute chest pain: the Global Registry of Acute Coronary Events (GRACE) risk score is enhanced by selectednonnecrosis biomarkers. Am Heart J 2010;160:88–94.82. Khot UN, Jia G, Moliterno DJ, Lincoff AM, Khot MB, Harrington RA, Topol EJ. Prognostic importance of physicalexamination for heart failure in non-ST-elevation acute coronary syndromes: the enduring value of Killip classification.JAMA 2003;290:2174–2181.83. Subherwal S, Bach RG, Chen AY, Gage BF, Rao SV, Newby LK, Wang TY, Gibler WB, Ohman EM, Roe MT, PollackCV Jr., Peterson ED, Alexander KP. Baseline risk of major bleeding in non-ST-segment-elevation myocardialinfarction: the CRUSADE (Can Rapid risk stratification of Unstable angina patients Suppress ADverseoutcomes with Early implementation of the ACC/AHA Guidelines) Bleeding Score. Circulation2009;119:1873–1882.84. Mehran R, Pocock SJ, Nikolsky E, Clayton T, Dangas GD, Kirtane AJ, Parise H, Fahy M, Manoukian SV, Feit F,Ohman ME, Witzenbichler B, Guagliumi G, Lansky AJ, Stone GW. A risk score to predict bleeding in patients withacute coronary syndromes. J Am Coll Cardiol 2010;55:2556–2566.85. Yusuf S, Peto R, Lewis J, Collins R, Sleight P. Beta blockade during and after myocardial infarction: an overviewof the randomized trials. Prog Cardiovasc Dis 1985;27:335–371.86. Randomised trial of intravenous atenolol among 16 027 cases of suspected acute myocardial infarction: ISIS-1. First International Study of Infarct Survival Collaborative Group. Lancet 1986;2:57–66.87. Telford AM, Wilson C. Trial of heparin versus atenolol in prevention of myocardial infarction in intermediatecoronary syndrome. Lancet 1981;1:1225–1228.88. Lubsen J, Tijssen JG. Efficacy of nifedipine and metoprolol in the early treatment of unstable angina in the coronarycare unit: findings from the Holland Interuniversity Nifedipine/metoprolol Trial (HINT). Am J Cardiol1987;60:18A–25A.89. Yusuf S, Wittes J, Friedman L. Overview of results of randomized clinical trials in heart disease. I. Treatments followingmyocardial infarction. JAMA 1988;260:2088–2093.90. Metoprolol in acute myocardial infarction (MIAMI). A randomised placebocontrolled international trial. TheMIAMI Trial Research Group. Eur Heart J 1985;6:199–226.91. Miller CD, Roe MT, Mulgund J, Hoekstra JW, Santos R, Pollack CV Jr., Ohman EM, Gibler WB, Peterson ED. Impactof acute beta-blocker therapy for patients with non-ST-segment elevation myocardial infarction. Am JMed 2007;120:685–692.92. Brandler E, Paladino L, Sinert R. Does the early administration of beta-blockers improve the in-hospital mortalityrate of patients admitted with acute coronary syndrome? Acad Emerg Med 2010;17:1–10.93. Chen ZM, Pan HC, Chen YP, Peto R, Collins R, Jiang LX, Xie JX, Liu LS. Early intravenous then oral metoprolol in45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet2005;366:1622–1632.94. Borzak S, Cannon CP, Kraft PL, Douthat L, Becker RC, Palmeri ST, Henry T, Hochman JS, Fuchs J, Antman EM,McCabe C, Braunwald E. Effects of prior aspirin and anti-ischemic therapy on outcome of patients with unstableangina. TIMI 7 Investigators. Thrombin Inhibition in Myocardial Ischemia. Am J Cardiol 1998;81:678–681.95. Ambrosio G, Del Pinto M, Tritto I, Agnelli G, Bentivoglio M, Zuchi C, Anderson FA, Gore JM, Lopez-Sendon J,Wyman A, Kennelly BM, Fox KA. Chronic nitrate therapy is associated with different presentation and evolutionof acute coronary syndromes: insights from 52,693 patients in the Global Registry of Acute Coronary Events.Eur Heart J 2010;31:430–438.96. Cotter G, Faibel H, Barash P, Shemesh E, Moshkovitz Y, Metzkor E, Simovitz A, Miller R, Schlezinger Z, Golik A.High-dose nitrates in the immediate management of unstable angina: optimal dosage, route of administration,and therapeutic goals. Am J Emerg Med 1998;16:219–224.97. Theroux P, Taeymans Y, Morissette D, Bosch X, Pelletier GB, Waters DD. A randomized study comparing propranololand diltiazem in the treatment of unstable angina. J Am Coll Cardiol 1985;5:717–722.98. Parodi O, Simonetti I, Michelassi C, Carpeggiani C, Biagini A, L’Abbate A, Maseri A. Comparison of verapamiland propranolol therapy for angina pectoris at rest: a randomized, multiple-crossover, controlled trial in thecoronary care unit. Am J Cardiol 1986;57:899–906.99. Hansen JF. Treatment with verapamil after an acute myocardial infarction. Review of the Danish studies on verapamilin myocardial infarction (DAVIT I and II). Drugs 1991;42 Suppl 2:43–53.100. Moss AJ, Oakes D, Rubison M, McDermott M, Carleen E, Eberly S, Brown M. Effects of diltiazem on long-termoutcome after acute myocardial infarction in patients with and without a history of systemic hypertension.The Multicenter Diltiazem Postinfarction Trial Research Group. Am J Cardiol 1991;68:429–433.101. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina(IONA) randomised trial. Lancet 2002;359:1269–1275.102. Borer JS. Therapeutic effects of I(f) blockade: evidence and perspective. Pharmacol Res 2006;53:440–445.103. Morrow DA, Scirica BM, Karwatowska-Prokopczuk E, Murphy SA, Budaj A, Varshavsky S, Wolff AA, Skene A,McCabe CH, Braunwald E. Effects of ranolazine on recurrent cardiovascular events in patients with non-ST-elevationacute coronary syndromes: the MERLIN-TIMI 36 randomized trial. JAMA 2007;297:1775–1783.104. Theroux P, Ouimet H, McCans J, Latour JG, Joly P, Levy G, Pelletier E, Juneau M, Stasiak J, de Guise P, PelletierG, Rinzler D, Waters D. Aspirin, heparin, or both to treat acute unstable angina. N Engl J Med1988;319:1105–1111.105. Theroux P, Waters D, Qiu S, McCans J, de Guise P, Juneau M. Aspirin versus heparin to prevent myocardial infarctionduring the acute phase of unstable angina. Circulation 1993;88:2045–2048.106. Cairns JA, Gent M, Singer J, Finnie KJ, Froggatt GM, Holder DA, Jablonsky G, Kostok WJ, Melendez LJ, MyersMG, Sackett DL, Staley BJ, Tanser PH. Aspirin, sulfinpyrazone, or both in unstable angina. Results of a Canadianmulticenter trial. N Engl J Med 1985;313:1369–1375.107. Baigent C, Blackwell L, Collins R, Emberson J, Godwin J, Peto R, Buring J, Hennekens C, Kearney P, Meade T,Patrono C, Roncaglioni MC, Zanchetti A. Aspirin in the primary and secondary prevention of vascular disease:collaborative meta-analysis 108. Mehta SR, Tanguay JF, Eikelboom JW, Jolly SS, Joyner CD, Granger CB, Faxon DP, Rupprecht HJ, Budaj A,Avezum A, Widimsky P, Steg PG, Bassand JP, Montalescot G, Macaya C, Di Pasquale G, Niemela K, Ajani AE,White HD, Chrolavicius S, Gao P, Fox KA, Yusuf S. Double-dose versus standard-dose clopidogrel and highdoseversus low-dose aspirin in individuals undergoing percutaneous coronary intervention for acute coronarysyndromes (CURRENT-OASIS 7): a randomised factorial trial. Lancet 2010;376:1233–1243.109. Gislason GH, Jacobsen S, Rasmussen JN, Rasmussen S, Buch P, Friberg J, Schramm TK, Abildstrom SZ, KoberL, Madsen M, Torp-Pedersen C. Risk of death or reinfarction associated with the use of selective cyclooxygenase-2 inhibitors and nonselective nonsteroidal antiinflammatory drugs after acute myocardial infarction. Circulation2006;113:2906–2913.110. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Effects of clopidogrel in addition to aspirin inpatients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345:494–502.111. Yusuf S, Mehta SR, Zhao F, Gersh BJ, Commerford PJ, Blumenthal M, Budaj A, Wittlinger T, Fox KA. Early andlate effects of clopidogrel in patients with acute coronary syndromes. Circulation 2003;107:966–972.112. Ho PM, Peterson ED, Wang L, Magid DJ, Fihn SD, Larsen GC, Jesse RA, Rumsfeld JS. Incidence of death andacute myocardial infarction associated with stopping clopidogrel after acute coronary syndrome. JAMA2008;299:532–539.113. Fox KA, Mehta SR, Peters R, Zhao F, Lakkis N, Gersh BJ, Yusuf S. Benefits and risks of the combination of clopidogreland aspirin in patients undergoing surgical revascularization for non-ST-elevation acute coronary syndrome:the Clopidogrel in Unstable angina to prevent Recurrent ischemic Events (CURE) Trial. Circulation2004;110:1202–1208.114. Montalescot G, Sideris G, Meuleman C, Bal-dit-Sollier C, Lellouche N, Steg PG, Slama M, Milleron O, ColletJ-P, Henry P, Beygui F, Drouet L. A randomized comparison of high clopidogrel loading doses in patients withnon-ST-segment elevation acute coronary syndromes: the ALBION (Assessment of the Best Loading Dose ofClopidogrel to Blunt Platelet Activation, Inflammation and Ongoing Necrosis) Trial. J Am Coll Cardiol2006;48:931–938.115. Snoep JD, Hovens MM, Eikenboom JC, van der Bom JG, Jukema JW, Huisman MV. Clopidogrel nonresponsivenessin patients undergoing percutaneous coronary intervention with stenting: a systematic review andmeta-analysis. Am Heart J 2007;154:221–231.116. Aleil B, Jacquemin L, De Poli F, Zaehringer M, Collet J-P, Montalescot G, Cazenave J-P, Dickele M-C, MonassierJ-P, Gachet C. Clopidogrel 150 mg/day to overcome low responsiveness in patients undergoing elective percutaneouscoronary intervention: results from the VASP-02 (Vasodilator-Stimulated Phosphoprotein-02)Randomized Study. JACC Cardiovasc Interv 2008;1:631–638.117. The CURRENT-OASIS 7 Investigators. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes.N Engl J Med 2010;363:930–942.118. Taubert D, von Beckerath N, Grimberg G, Lazar A, Jung N, Goeser T, Kastrati A, Schomig A, Schomig E. Impactof P-glycoprotein on clopidogrel absorption. Clin Pharmacol Ther 2006;80:486–501.119. Mega JL, Close SL, Wiviott SD, Shen L, Walker JR, Simon T, Antman EM, Braunwald E, Sabatine MS. Geneticvariants in ABCB1 and CYP2C19 and cardiovascular outcomes after treatment with clopidogrel and prasugrelin the TRITON-TIMI 38 trial: a pharmacogenetic analysis. Lancet 2010;376:1312–1319.120. Mega JL, Simon T, Collet JP, Anderson JL, Antman EM, Bliden K, Cannon CP, Danchin N, Giusti B, Gurbel P,Horne BD, Hulot JS, Kastrati A, Montalescot G, Neumann FJ, Shen L, Sibbing D, Steg PG, Trenk D, Wiviott SD,Sabatine MS. Reduced-function CYP2C19 genotype and risk of adverse clinical outcomes among patientstreated with clopidogrel predominantly for PCI: a meta-analysis. JAMA 2010;304:1821–1830.121. Breet N, van Werkum J, Bouman H, Kelder J, Ruven H, Bal E, Deneer V, Harmsze A, van der Heyden J, RensingB, Suttorp M, Hackeng C, ten Berg J. Comparison of platelet function tests in predicting clinical outcomein patients undergoing coronary stent implantation. JAMA 2010;303:754–762.122. Geisler T, Langer H, Wydymus M, Gohring K, Zurn C, Bigalke B, Stellos K, May AE, Gawaz M. Low responseto clopidogrel is associated with cardiovascular outcome after coronary stent implantation. Eur Heart J2006;27:2420–2425.123. Trenk D, Hochholzer W, Fromm MF, Chialda LE, Pahl A, Valina CM, Stratz C, Schmiebusch P, Bestehorn HP,Buttner HJ, Neumann FJ. Cytochrome P450 2C19 681G.A polymorphism and high on-clopidogrel platelet reactivityassociated with adverse 1-year clinical outcome of elective percutaneous coronary intervention withdrug-eluting or bare-metal stents. J Am Coll Cardiol 2008;51:1925–1934.124. Price MJ, Berger PB, Teirstein PS, Tanguay JF, Angiolillo DJ, Spriggs D, Puri S, Robbins M, Garratt KN, BertrandOF, Stillablower ME, Aragon JR, Kandzari DE, Stinis CT, Lee MS, Manoukian SV, Cannon CP, Schork NJ, TopolEJ. Standard- vs high-dose clopidogrel based on platelet function testing after percutaneous coronary intervention:the GRAVITAS randomized trial. JAMA 2011;305:1097–1105.125. O’Donoghue ML, Braunwald E, Antman EM, Murphy SA, Bates ER, Rozenman Y, Michelson AD, HautvastRW, Ver Lee PN, Close SL, Shen L, Mega JL, Sabatine MS, Wiviott SD. Pharmacodynamic effect and clinical efficacyof clopidogrel and prasugrel with or without a proton-pump inhibitor: an analysis of two randomisedtrials. Lancet 2009;374:989–997.126. Abraham NS, Hlatky MA, Antman EM, Bhatt DL, Bjorkman DJ, Clark CB, Furberg CD, Johnson DA, Kahi CJ,Laine L, Mahaffey KW, Quigley EM, Scheiman J, Sperling LS, Tomaselli GF. ACCF/ACG/AHA 2010 Expert ConsensusDocument on the concomitant use of proton pump inhibitors and thienopyridines: a focused updateof the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelettherapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Expert ConsensusDocuments. Circulation 2010;122:2619–2633.127. Bhatt DL, Cryer BL, Contant CF, Cohen M, Lanas A, Schnitzer TJ, Shook TL, Lapuerta P, Goldsmith MA, LaineL, Scirica BM, Murphy SA, Cannon CP. Clopidogrel with or without omeprazole in coronary artery disease. NEngl J Med 2010;363:1909–1917.128. Wiviott SD, Trenk D, Frelinger AL, O’Donoghue M, Neumann F-J, Michelson AD, Angiolillo DJ, Hod H, MontalescotG, Miller DL, Jakubowski JA, Cairns R, Murphy SA, McCabe CH, Antman EM, Braunwald E, PRINCIPLE-TIMI 44 Investigators. Prasugrel compared with high loading- and maintenance-dose clopidogrel inpatients with planned percutaneous coronary intervention: the Prasugrel in Comparison to Clopidogrel for Inhibitionof Platelet Activation and Aggregation Thrombolysis in Myocardial Infarction 44 Trial. Circulation2007;116:2923–2932.129. Small DS, Farid NA, Payne CD, Weerakkody GJ, Li YG, Brandt JT, Salazar DE, Winters KJ. Effects of the protonpump inhibitor lansoprazole on the pharmacokinetics and pharmacodynamics of prasugrel and clopidogrel.J Clin Pharmacol 2008;48:475–484.130. Wiviott S, Braunwald E, McCabe C, Montalescot G, Ruzyllo W, Gottlieb S, Neumann F-J, Ardissino D, De ServiS, Murphy S, Riesmeyer J, Weerakkody G, Gibson C, Antman E. Prasugrel versus clopidogrel in patients withacute coronary syndromes. N Engl J Med 2007;357:2001–2015.131. Gurbel PA, Bliden KP, Butler K, Tantry US, Gesheff T, Wei C, Teng R, Antonino MJ, Patil SB, Karunakaran A,Kereiakes DJ, Paris C, Purdy D, Wilson V, Ledley GS, Storey RF. Randomized double-blind assessment of theONSET and OFFSet of the antiplatelet effects of ticagrelor versus clopidogrel in patients with stable coronaryartery disease: the ONSET/OFFSET Study. Circulation 2009;120:2577–2585.132. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C, Horrow J, Husted S, James S, Katus H,Mahaffey KW, Scirica BM, Skene A, Steg PG, Storey RF, Harrington RA, for the PLATO Investigators. Ticagrelorversus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361:1045–1057.133. Cannon C, Harrington R, James S, Ardissino D, Becker R, Emanuelsson H, Husted S, Katus H, Keltaih M, KhurmiN, Kontny F, Lewis B, Steg P, Storey R, Wojdyla D, Wallentin L, the PLATelet inhibition and patient Outcomes(PLATO) investigators. Ticagrelor compared with clopidogrel in acute coronary syndromes patients with aplanned invasive strategy (PLATO): a randomised double-blind study. Lancet 2010;375:283–293.134. Held C, Asenblad N, Bassand JP, Becker RC, Cannon CP, Claeys MJ, Harrington RA, Horrow J, Husted S, JamesSK, Mahaffey KW, Nicolau JC, Scirica BM, Storey RF, Vintila M, Ycas J, Wallentin L. Ticagrelor versus clopidogrelin patients with acute coronary syndromes undergoing coronary artery bypass surgery results from thePLATO (Platelet Inhibition and Patient Outcomes) Trial. J Am Coll Cardiol 2011;57:672–684.135. Husted S, Emanuelsson H, Heptinstall S, Sandset PM, Wickens M, Peters G. Pharmacodynamics, pharmacokinetics,and safety of the oral reversible P2Y12 antagonist AZD6140 with aspirin in patients with atherosclerosis:a double-blind comparison to clopidogrel with aspirin. Eur Heart J 2006;27:1038–1047.136. Cannon CP, Husted S, Harrington RA, Scirica BM, Emanuelsson H, Peters G, Storey RF. Safety, tolerability, andinitial efficacy of AZD6140, the First reversible oral adenosine diphosphate receptor antagonist, comparedwith clopidogrel, in patients with non-ST-segment elevation acute coronary syndrome: primary results of theDISPERSE-2 Trial. J Am Coll Cardiol 2007;50:1844–1851.137. Storey RF, Bliden K, Patil SB, Karunakaran A, Ecob R, Butler K, Teng R, Wei C, Tantry US, Gurbel P. Incidence ofdyspnea and assessment of cardiac and pulmonary function in patients with stable coronary artery disease receivingticagrelor, clopidogrel or placebo in the ONSET/OFFSET Study. J Am Coll Cardiol 2010;56:185–193.138. Berger JS, Frye CB, Harshaw Q, Edwards FH, Steinhubl SR, Becker RC. Impact of clopidogrel in patients withacute coronary syndromes requiring coronary artery bypass surgery: a multicenter analysis. J Am Coll Cardiol2008;52:1693–1701.139. Kapetanakis EI, Medlam DA, Boyce SW, Haile E, Hill PC, Dullum MK, Bafi AS, Petro KR, Corso PJ. Clopidogreladministration prior to coronary artery bypass grafting surgery: the cardiologist’s panacea or the surgeon’sheadache? Eur Heart J 2005;26:576–583.140. Mehta RH, Roe MT, Mulgund J, Ohman EM, Cannon CP, Gibler WB, Pollack CV Jr., Smith SC Jr., Ferguson TB,Peterson ED. Acute clopidogrel use and outcomes in patients with non-ST-segment elevation acute coronarysyndromes undergoing coronary artery bypass surgery. J Am Coll Cardiol 2006;48:281–286.141. Ebrahimi R, Dyke C, Mehran R, Manoukian SV, Feit F, Cox DA, Gersh BJ, Ohman EM, White HD, Moses JW,WareJH, Lincoff AM, Stone GW. Outcomes following pre-operative clopidogrel administration in patients with acutecoronary syndromes undergoing coronary artery bypass surgery: the ACUITY (Acute Catheterization and UrgentIntervention Triage strategY) Trial. J Am Coll Cardiol 2009;53:1965–1972.142. Kim JH, Newby LK, Clare RM, Shaw LK, Lodge AJ, Smith PK, Jolicoeur EM, Rao SV, Becker RC, Mark DB,Granger CB. Clopidogrel use and bleeding after coronary artery bypass graft surgery. Am Heart J2008;156:886–892.143. Fitchett D, Eikelboom J, Fremes S, Mazer D, Singh S, Bittira B, Brister S, Graham JJ, Gupta M, Karkouti K, LeeA, Love M, McArthur R, Peterson M, Verma S, Yau TM. Dual antiplatelet therapy in patients requiring urgentcoronary artery bypass grafting surgery: a position statement of the Canadian Cardiovascular Society. Can J Cardiol2009;25:683–689.144. Collet JP, Montalescot G, Blanchet B, Tanguy ML, Golmard JL, Choussat R, Beygui F, Payot L, Vignolles N, MetzgerJP, Thomas D. Impact of prior use or recent withdrawal of oral antiplatelet agents on acute coronary syndromes.Circulation 2004;110:2361–2367.145. Grines CL, Bonow RO, Casey DE Jr., Gardner TJ, Lockhart PB, Moliterno DJ, O’Gara P, Whitlow P. Prevention ofpremature discontinuation of dual antiplatelet therapy in patients with coronary artery stents: a science advisoryfrom the American Heart Association, American College of Cardiology, Society for Cardiovascular Angiographyand Interventions, American College of Surgeons, and American Dental Association, withrepresentation from the American College of Physicians. Circulation 2007;115:813–818.146. Mehta SR, Yusuf S, Peters RJ, Bertrand ME, Lewis BS, Natarajan MK, Malmberg K, Rupprecht H, Zhao F,Chrolavicius S, Copland I, Fox KA. Effects of pretreatment with clopidogrel and aspirin followed by long-termtherapy in patients undergoing percutaneous coronary intervention: the PCI-CURE study. Lancet2001;358:527–533.147. Steinhubl SR, Berger PB, Mann JT 3rd, Fry ET, DeLago A, Wilmer C, Topol EJ. Early and sustained dual oral antiplatelettherapy following percutaneous coronary intervention: a randomized controlled trial. JAMA2002;288:2411–2420.148. Wijns W, Kolh P, Danchin N, Di Mario C, Falk V, Folliguet T, Garg S, Huber K, James S, Knuuti J, Lopez-SendonJ, Marco J, Menicanti L, Ostojic M, Piepoli MF, Pirlet C, Pomar JL, Reifart N, Ribichini FL, Schalij MJ, SergeantP, Serruys PW, Silber S, Sousa Uva M, Taggart D. Guidelines on myocardial revascularization: the Task Force onMyocardial Revascularization of the European Society of Cardiology (ESC) and the European Association forCardio-Thoracic Surgery (EACTS). Eur Heart J 2010;31:2501–2555.149. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Moliterno DJ, Heeschen C, Hamm CW, Robbins MA,Kleiman NS, Theroux P, White HD, Topol EJ. Platelet glycoprotein IIb/IIIa inhibition in acute coronary syndromes.Gradient of benefit related to the revascularisation strategy. Eur Heart J 2002; 23:1441–1448.150. Stone GW, Bertrand ME, Moses JW, Ohman EM, Lincoff AM, Ware JH, Pocock SJ, McLaurin BT, Cox DA, JafarMZ, Chandna H, Hartmann F, Leisch F, Strasser RH, Desaga M, Stuckey TD, Zelman RB, Lieber IH, Cohen DJ,Mehran R, White HD. Routine upstream initiation vs deferred selective use of glycoprotein IIb/IIIa inhibitorsin acute coronary syndromes: the ACUITY Timing trial. JAMA 2007;297:591–602.151. Giugliano RP, White JA, Bode C, Armstrong PW, Montalescot G, Lewis BS, van’t Hof A, Berdan LG, Lee KL,Strony JT, Hildemann S, Veltri E, Van de Werf F, Braunwald E, Harrington RA, Califf RM, Newby LK, the EARLYACS Investigators. Early versus delayed, provisional eptifibatide in acute coronary syndromes. N Engl J Med2009;360:2176–2190.152. Kastrati A, Mehilli J, Neumann F-J, Dotzer F, ten Berg J, Bollwein H, Graf I, Ibrahim M, Pache J, Seyfarth M,Schuhlen H, Dirschinger J, Berger PB, Schomig A, for the Intracoronary Stenting, Antithrombotic Regimen:Rapid Early Action for Coronary Treatment 2 Trial I. Abciximab in patients with acute coronary syndromes undergoingpercutaneous coronary intervention after clopidogrel pretreatment: the ISAR-REACT 2 RandomizedTrial. JAMA 2006;295:1531–1538. 153. Dasgupta H, Blankenship JC, Wood GC, Frey CM, Demko SL, Menapace FJ. Thrombocytopenia complicatingtreatment with intravenous glycoprotein IIb/IIIa receptor inhibitors: a pooled analysis. Am Heart J2000;140:206–211.154. Jubelirer SJ, Koenig BA, Bates MC. Acute profound thrombocytopenia following C7E3 Fab (Abciximab) therapy:case reports, review of the literature and implications for therapy. Am J Hematol 1999;61:205–208.155. Lajus S, Clofent-Sanchez G, Jais C, Coste P, Nurden P, Nurden AT. Thrombocytopenia after abciximab use resultsfrom different mechanisms. Thromb Haemost 2010;103 651–661.156. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute coronary syndromes. ThePURSUIT Trial Investigators. Platelet glycoprotein IIb/IIIa in unstable angina: receptor suppression using integrilintherapy. N Engl J Med 1998;339:436–443.157. Merlini PA, Rossi M, Menozzi A, Buratti S, Brennan DM, Moliterno DJ, Topol EJ, Ardissino D. Thrombocytopeniacaused by abciximab or tirofiban and its association with clinical outcome in patients undergoing coronarystenting. Circulation 2004;109:2203–2206.158. Topol EJ, Moliterno DJ, Herrmann HC, Powers ER, Grines CL, Cohen DJ, Cohen EA, Bertrand M, Neumann FJ,Stone GW, DiBattiste PM, Yakubov SJ, DeLucca PT, Demopoulos L, the TARGET Investigators. Comparisonof two platelet glycoprotein IIb/IIIa inhibitors, tirofiban and abciximab, for the prevention of ischemic eventswith percutaneous coronary revascularization. N Engl J Med 2001;344:1888–1894.159. Moliterno DJ, Yakubov SJ, DiBattiste PM, Herrmann HC, Stone GW, Macaya C, Neumann F-J, Ardissino D,Bassand J-P, Borzi L. Outcomes at 6 months for the direct comparison of tirofiban and abciximab during percutaneouscoronary revascularisation with stent placement: the TARGET follow-up study. Lancet2002;360:355–360.160. De Luca G, Ucci G, Cassetti E, Marino P. Benefits from small molecule administration as compared with abciximabamong patients with ST-segment elevation myocardial infarction treated with primary angioplasty: ameta-analysis. J Am Coll Cardiol 2009;53:1668–1673.161. Valgimigli M, Biondi-Zoccai G, Tebaldi M, van’t Hof AWJ, Campo G, Hamm C, ten Berg J, Bolognese L, Saia F,Danzi GB, Briguori C, Okmen E, King SB, Moliterno DJ, Topol EJ. Tirofiban as adjunctive therapy for acutecoronary syndromes and percutaneous coronary intervention: a meta-analysis of randomized trials. Eur HeartJ 2010;31:35–49.162. O’Donoghue M, Antman EM, Braunwald E, Murphy SA, Steg PG, Finkelstein A, Penny WF, Fridrich V, McCabeCH, Sabatine MS, Wiviott SD. The efficacy and safety of prasugrel with and without a glycoprotein IIb/IIIa inhibitorin patients with acute coronary syndromes undergoing percutaneous intervention: a TRITON-TIMI 38(Trial to Assess Improvement in Therapeutic Outcomes by Optimizing Platelet Inhibition With Prasugrel-ThrombolysisIn Myocardial Infarction 38) analysis. J Am Coll Cardiol 2009;54:678–685.163. Buller C, Pate G, Armstrong P, O’Neill B, Webb J, Gallo R, Welsh R. Catheter thrombosis during primary percutaneouscoronary intervention for acute ST elevation myocardial infarction despite subcutaneous low-molecular-weight heparin, acetylsalicylic acid, clopidogrel and abciximab pretreatment. Can J Cardiol2006;22:511–515.164. Jolly SS, Faxon DP, Fox KA, Afzal R, Boden WE, Widimsky P, Steg PG, Valentin V, Budaj A, Granger CB, JoynerCD, Chrolavicius S, Yusuf S, Mehta SR. Efficacy and safety of fondaparinux versus enoxaparin in patients withacute coronary syndromes treated with glycoprotein IIb/IIIa inhibitors or thienopyridines: results from theOASIS 5 (Fifth Organization to Assess Strategies in Ischemic Syndromes) trial. J Am Coll Cardiol2009;54:468–476.165. White HD, Ohman EM, Lincoff AM, Bertrand ME, Colombo A, McLaurin BT, Cox DA, Pocock SJ, Ware JA,Manoukian SV, Lansky AJ, Mehran R, Moses JW, Stone GW. Safety and efficacy of bivalirudin with and withoutglycoprotein IIb/IIIa inhibitors in patients with acute coronary syndromes undergoing percutaneous coronaryintervention: 1-year results from the ACUITY (Acute Catheterization and Urgent Intervention TriagestrategY) trial. J Am Coll Cardiol 2008;52:807–814.166. Lincoff AM, Steinhubl SR, Manoukian SV, Chew D, Pollack CV Jr, Feit F,Ware JH, Bertrand ME, Ohman EM,DesmetW, Cox DA, Mehran R, Stone GW. Influence of timing of clopidogrel treatment on the efficacy andsafety of bivalirudin in patients with non-ST-segment elevation acute coronary syndromes undergoing percutaneouscoronary intervention: an analysis of the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. JACC Cardiovasc Interv 2008;1:639–648.167. Brieger D, Van de Werf F, Avezum A, Montalescot G, Kennelly B, Granger CB, Goodman SG, Dabbous O, AgnelliG. Interactions between heparins, glycoprotein IIb/IIIa antagonists, and coronary intervention. The GlobalRegistry of Acute Coronary Events (GRACE). Am Heart J 2007;153:960–969.168. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED, for the CRUSADE Investigators. Excess dosing of antiplatelet and antithrombin agents in thetreatment of non-ST-segment elevation acute coronary syndromes. JAMA 2005;294:3108–3116.169. Li Y, Spencer F, Becker R. Comparative efficacy of fibrinogen and platelet supplementation on the in vitro reversibilityof competitive glycoprotein IIb/IIIa receptor-directed platelet inhibition. Am Heart J2002;143:725–732.170. Neumann FJ, Kastrati A, Pogatsa-Murray G, Mehilli J, Bollwein H, Bestehorn HP, Schmitt C, Seyfarth M,Dirschinger J, Schomig A. Evaluation of prolonged antithrombotic pretreatment (‘cooling-off’ strategy) beforeintervention in patients with unstable coronary syndromes: a randomized controlled trial. JAMA2003;290:1593–1599.171. Harrington RA, Becker RC, Cannon CP, Gutterman D, Lincoff AM, Popma JJ, Steg G, Guyatt GH, Goodman SG.Antithrombotic therapy for non-ST-segment elevation acute coronary syndromes: American College of ChestPhysicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008;133:670S–707S.172. Eikelboom JW, Anand SS, Malmberg K, Weitz JI, Ginsberg JS, Yusuf S. Unfractionated heparin and low-molecular-weight heparin in acute coronary syndrome without ST elevation: a meta-analysis. Lancet2000;355:1936–1942.173. Simoons ML, Bobbink IW, Boland J, Gardien M, Klootwijk P, Lensing AW, Ruzyllo W, Umans VA, Vahanian A,Van De Werf F, Zeymer U; PENTUA Investigators. A dose-finding study of fondaparinux in patients with non-ST-segment elevation acute coronary syndromes: the Pentasaccharide in Unstable Angina (PENTUA) Study.J Am Coll Cardiol 2004;43:2183–2190.174. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Effects of fondaparinux on mortality and reinfarction in patients with acute ST-segment elevationmyocardial infarction: the OASIS-6 randomized trial. JAMA 2006;295:1519–1530.175. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Comparison of fondaparinux and enoxaparin in acute coronary syndromes. N Engl J Med2006;354:1464–1476.176. Mehta SR, Steg PG, Granger CB, Bassand JP, Faxon DP,Weitz JI, Afzal R, Rush B, Peters RJ, Natarajan MK,Velianou JL, Goodhart DM, Labinaz M, Tanguay JF, Fox KA, Yusuf S. Randomized, blinded trial comparingfondaparinux with unfractionated heparin in patients undergoing contemporary percutaneous coronary intervention:Arixtra Study in Percutaneous Coronary Intervention: a Randomized Evaluation (ASPIRE) pilot trial.Circulation 2005;111:1390–1397.177. Anderson JA, Hirsh J, Yusuf S, Johnston M, Afzal R, Mehta SR, Fox KA, Budaj A, Eikelboom JW. Comparisonof the anticoagulant intensities of fondaparinux and enoxaparin in the Organization to Assess Strategies inAcute Ischemic Syndromes (OASIS)-5 trial. J Thromb Haemost 2010;8:243–249.178. Steg PG, Jolly SS, Mehta SR, Afzal R, Xavier D, Rupprecht HJ, Lopez-Sendon JL, Budaj A, Diaz R, Avezum A,Widimsky P, Rao SV, Chrolavicius S, Meeks B, Joyner C, Pogue J, Yusuf S. Low-dose vs standard-dose unfractionatedheparin for percutaneous coronary intervention in acute coronary syndromes treated with fondaparinux:the FUTURA/OASIS-8 randomized trial. JAMA 2010;304:1339–1349.179. Antman EM, McCabe CH, Gurfinkel EP, Turpie AG, Bernink PJ, Salein D, Bayes De Luna A, Fox K, Lablanche JM,Radley D, Premmereur J, Braunwald E. Enoxaparin prevents death and cardiac ischemic events in unstableangina/non-Q-wave myocardial infarction. Results of the thrombolysis in myocardial infarction (TIMI) 11Btrial. Circulation 1999;100:1593–1601.180. Cohen M, Demers C, Gurfinkel EP, Turpie AG, Fromell GJ, Goodman S, Langer A, Califf RM, Fox KA, PremmereurJ, Bigonzi F. A comparison of low-molecular-weight heparin with unfractionated heparin for unstablecoronary artery disease. Efficacy and Safety of Subcutaneous Enoxaparin in Non-Q-Wave Coronary EventsStudy Group. N Engl J Med 1997;337:447–452.181. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators. Long-term lowmolecular-mass heparin in unstable coronary-artery disease: FRISC II prospective randomised multicentrestudy. Lancet 1999;354:701–707.182. Fragmin during Instability in Coronary Artery Disease (FRISC) study group. Low-molecular-weight heparinduring instability in coronary artery disease Lancet 1996;347:561–568.183. Hirsh J, Raschke R. Heparin and low-molecular-weight heparin: the Seventh ACCP Conference on Antithromboticand Thrombolytic Therapy. Chest 2004;126:188S–203S.184. TIMI 11A Investigators. Dose-ranging trial of enoxaparin for unstable angina: results of TIMI 11A. The Thrombolysisin Myocardial Infarction (TIMI) 11A Trial Investigators. J Am Coll Cardiol 1997;29:1474–1482.185. Montalescot G, Collet JP, Tanguy ML, Ankri A, Payot L, Dumaine R, Choussat R, Beygui F, Gallois V, Thomas D.Anti-Xa activity relates to survival and efficacy in unselected acute coronary syndrome patients treated withenoxaparin. Circulation 2004;110:392–398.186. Choussat R, Montalescot G, Collet JP, Vicaut E, Ankri A, Gallois V, Drobinski G, Sotirov I, Thomas D. A unique,low dose of intravenous enoxaparin in elective percutaneous coronary intervention. J Am Coll Cardiol2002;40:1943–1950.187. Collet JP, Montalescot G, Lison L, Choussat R, Ankri A, Drobinski G, Sotirov I, Thomas D. Percutaneous coronaryintervention after subcutaneous enoxaparin pretreatment in patients with unstable angina pectoris. Circulation2001;103:658–663.188. Murphy S, Gibson C, Morrow D, Van de Werf F, Menown I, Goodman S, Mahaffey K, Cohen M, McCabe C,Antman EM, Braunwald E. Efficacy and safety of the low-molecular weight heparin enoxaparin comparedwith unfractionated heparin across the acute coronary syndrome spectrum: a meta-analysis.Eur Heart J2007;28:2077–2086.189. Blazing MA, de Lemos JA, White HD, Fox KA, Verheugt FW, Ardissino D, DiBattiste PM, Palmisano J, BilheimerDW, Snapinn SM, Ramsey KE, Gardner LH, Hasselblad V, Pfeffer MA, Lewis EF, Braunwald E, Califf RM. Safetyand efficacy of enoxaparin vs unfractionated heparin in patients with non-ST-segment elevation acute coronarysyndromes who receive tirofiban and aspirin: a randomized controlled trial. JAMA 2004;292:55–64.190. Cohen M, Theroux P, Borzak S, Frey MJ, White HD, Van Mieghem W, Senatore F, Lis J, Mukherjee R, Harris K,Bigonzi F. Randomized double-blind safety study of enoxaparin versus unfractionated heparin in patients withnon-ST-segment elevation acute coronary syndromes treated with tirofiban and aspirin: the ACUTE II study.The Antithrombotic Combination Using Tirofiban and Enoxaparin. Am Heart J 2002;144:470–477.191. Goodman SG, Fitchett D, Armstrong PW, Tan M, Langer A. Randomized evaluation of the safety and efficacyof enoxaparin versus unfractionated heparin in high-risk patients with non-ST-segment elevation acute coronarysyndromes receiving the glycoprotein IIb/IIIa inhibitor eptifibatide. Circulation 2003;107:238–244.192. Ferguson JJ, Califf RM, Antman EM, Cohen M, Grines CL, Goodman S, Kereiakes DJ, Langer A, Mahaffey KW,Nessel CC, Armstrong PW, Avezum A, Aylward P, Becker RC, Biasucci L, Borzak S, Col J, Frey MJ, Fry E, GulbaDC, Guneri S, Gurfinkel E, Harrington R, Hochman JS, Kleiman NS, Leon MB, Lopez-Sendon JL, Pepine CJ,Ruzyllo W, Steinhubl SR, Teirstein PS, Toro-Figueroa L, White H. Enoxaparin vs unfractionated heparin in highriskpatients with non-ST-segment elevation acute coronary syndromes managed with an intended early invasivestrategy: primary results of the SYNERGY randomized trial. JAMA 2004;292:45–54.193. Petersen JL, Mahaffey KW, Hasselblad V, Antman EM, Cohen M, Goodman SG, Langer A, Blazing MA, Le-Moigne-Amrani A, de Lemos JA, Nessel CC, Harrington RA, Ferguson JJ, Braunwald E, Califf RM. Efficacy andbleeding complications among patients randomized to enoxaparin or unfractionated heparin for antithrombintherapy in non-ST-Segment elevation acute coronary syndromes: a systematic overview. JAMA2004;292:89–96.194. Sanchez-Pena P, Hulot JS, Urien S, Ankri A, Collet JP, Choussat R, Lechat P, Montalescot G. Anti-factor Xa kineticsafter intravenous enoxaparin in patients undergoing percutaneous coronary intervention: a populationmodel analysis. Br J Clin Pharmacol 2005;60:364–373.195. Montalescot G, White HD, Gallo R, Cohen M, Steg PG, Aylward PE, Bode C, Chiariello M, King SB 3rd, HarringtonRA, Desmet WJ, Macaya C, Steinhubl SR. Enoxaparin versus unfractionated heparin in elective percutaneouscoronary intervention. N Engl J Med 2006;355:1006–1017.196. Stone GW, McLaurin BT, Cox DA, Bertrand ME, Lincoff AM, Moses JW, White HD, Pocock SJ, Ware JH, Feit F,Colombo A, Aylward PE, Cequier AR, Darius H, Desmet W, Ebrahimi R, Hamon M, Rasmussen LH, RupprechtHJ, Hoekstra J, Mehran R, Ohman EM; ACUITY Investigators. Bivalirudin for patients with acute coronary syndromes.N Engl J Med 2006;355:2203–2216.197. Stone GW, White HD, Ohman EM, Bertrand ME, Lincoff AM, McLaurin BT, Cox DA, Pocock SJ, Ware JH, FeitF, Colombo A, Manoukian SV, Lansky AJ, Mehran R, Moses JW. Acute Catheterization and Urgent InterventionTriage strategy (ACUITY) trial investigators. Bivalirudin in patients with acute coronary syndromes undergoingpercutaneous coronary intervention: a subgroup analysis from the Acute Catheterization and UrgentIntervention Triage strategy (ACUITY) trial. Lancet 2007;369:907–919.198. Stone G, Ware J, Bertrand M, Lincoff A, Moses J, Ohman E, White H, Feit F, Colombo A, McLaurin B, Cox D,Manoukian S, Fahy M, Clayton T, Mehran R, Pocock S. For the ACUITY Investigators. Antithrombotic strategiesin patients with acute coronary syndromes undergoing early invasive management: one-year results fromthe ACUITY trial. JAMA 2007;298:2497–2506. 199. White HD, Chew DP, Hoekstra JW, Miller CD, Pollack CV Jr., Feit F, Lincoff AM, Bertrand M, Pocock S, Ware J,Ohman EM, Mehran R, Stone GW. Safety and efficacy of switching from either unfractionated heparin orenoxaparin to bivalirudin in patients with non-ST-segment elevation acute coronary syndromes managedwith an invasive strategy: results from the ACUITY (Acute Catheterization and Urgent Intervention Triage strategY)trial. J Am Coll Cardiol 2008;51:1734–1741.200. Alexander JH, Becker RC, Bhatt DL, Cools F, Crea F, Dellborg M, Fox KA, Goodman SG, Harrington RA, HuberK, Husted S, Lewis BS, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, WallentinL. Apixaban, an oral, direct, selective factor Xa inhibitor, in combination with antiplatelet therapy after acutecoronary syndrome: results of the Apixaban for Prevention of Acute Ischemic and Safety Events (APPRAISE)trial. Circulation 2009;119:2877–2885.201. Mega JL, Braunwald E, Mohanavelu S, Burton P, Poulter R, Misselwitz F, Hricak V, Barnathan ES, Bordes P,Witkowski A, Markov V, Oppenheimer L, Gibson CM. Rivaroxaban versus placebo in patients with acute coronarysyndromes (ATLAS ACS-TIMI 46): a randomised, double-blind, phase II trial. Lancet 2009;374:29–38.202. Alexander J, Becker R, Bhatt D, Cools F, Crea F, Dellborg M, Fox K, Goodman S, Harrington R, Huber K, HustedS, Lewis B, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, Wallentin L. For the APPRAISESteering Committee and Investigators. Apixaban, an oral, direct, selective factor Xa inhibitor, in combinationwith antiplatelet therapy after acute coronary syndrome: results of the Apixaban for Prevention ofAcute Ischemic and Safety Events (APPRAISE) trial. Circulation 2009;119:2877–2885.203. Sabatine MS, Antman EM, Widimsky P, Ebrahim IO, Kiss RG, Saaiman A, Polasek R, Contant CF, McCabe CH,Braunwald E. Otamixaban for the treatment of patients with non-ST-elevation acute coronary syndromes(SEPIA-ACS1 TIMI 42): a randomised, double-blind, active-controlled, phase 2 trial. Lancet2009;374:787–795.204. Lip GY, Huber K, Andreotti F, Arnesen H, Airaksinen JK, Cuisset T, Kirchhof P, Marin F. Antithrombotic managementof atrial fibrillation patients presenting with acute coronary syndrome and/or undergoing coronarystenting: executive summary—a Consensus Document of the European Society of Cardiology Working Groupon Thrombosis, endorsed by the European Heart Rhythm Association (EHRA) and the European Associationof Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2010;31:1311–1318.205. Yan AT, Yan RT, Tan M, Eagle KA, Granger CB, Dabbous OH, Fitchett D, Grima E, Langer A, Goodman SG. Inhospitalrevascularization and one-year outcome of acute coronary syndrome patients stratified by the GRACErisk score. Am J Cardiol 2005;96:913–916.206. Mehta SR, Cannon CP, Fox KA, Wallentin L, Boden WE, Spacek R, Widimsky P, McCullough PA, Hunt D, BraunwaldE, Yusuf S. Routine vs selective invasive strategies in patients with acute coronary syndromes: a collaborativemeta-analysis of randomized trials. JAMA 2005;293:2908–2917.207. Bavry AA, Kumbhani DJ, Rassi AN, Bhatt DL, Askari AT. Benefit of early invasive therapy in acute coronary syndromes:a meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006;48:1319–1325.208. O’Donoghue M, Boden WE, Braunwald E, Cannon CP, Clayton TC, de Winter RJ, Fox KA, Lagerqvist B, McCulloughPA, Murphy SA, Spacek R, Swahn E,Wallentin L, Windhausen F, Sabatine MS. Early invasive vs conservativetreatment strategies in women and men with unstable angina and non-ST-segment elevation myocardialinfarction: a meta-analysis. JAMA 2008; 300:71–80.209. Fox KA, Clayton TC, Damman P, Pocock SJ, de Winter RJ, Tijssen JG, Lagerqvist B,Wallentin L. Long-term outcomeof a routine versus selective invasive strategy in patients with non-ST-segment elevation acute coronarysyndrome a meta-analysis of individual patient data. J Am Coll Cardiol 2010;55:2435–2445.210. Montalescot G, Cayla G, Collet JP, Elhadad S, Beygui F, Le Breton H, Choussat R, Leclercq F, Silvain J, Duclos F,Aout M, Dubois-Rande JL, Barthelemy O, Ducrocq G, Bellemain-Appaix A, Payot L, Steg PG, Henry P, SpauldingC, Vicaut E. Immediate vs delayed intervention for acute coronary syndromes: a randomized clinical trial.JAMA 2009;302:947–954.211. van’t Hof AW, de Vries ST, Dambrink JH, Miedema K, Suryapranata H, Hoorntje JC, Gosselink AT, Zijlstra F, deBoer MJ. A comparison of two invasive strategies in patients with non-ST elevation acute coronary syndromes:results of the Early or Late Intervention in unStable Angina (ELISA) pilot study. 2b/3a upstream therapy andacute coronary syndromes. Eur Heart J 2003;24:1401–1405.212. Mehta SR, Granger CB, Boden WE, Steg PG, Bassand JP, Faxon DP, Afzal R, Chrolavicius S, Jolly SS, WidimskyP, Avezum A, Rupprecht HJ, Zhu J, Col J, Natarajan MK, Horsman C, Fox KA, Yusuf S. Early versus delayed invasiveintervention in acute coronary syndromes. N Engl J Med 2009;360:2165–2175.213. Katritsis DG, Siontis GC, Kastrati A, van’t Hof AW, Neumann FJ, Siontis KC, Ioannidis JP. Optimal timing ofcoronary angiography and potential intervention in non-ST-elevation acute coronary syndromes. Eur Heart J2010;32:32–40.214. Riezebos RK, Ronner E, Ter Bals E, Slagboom T, Smits PC, ten Berg JM, Kiemeneij F, Amoroso G, Patterson MS,Suttorp MJ, Tijssen JG, Laarman GJ. Immediate versus deferred coronary angioplasty in non-ST-segment elevationacute coronary syndromes. Heart 2009;95:807–812.215. Sorajja P, Gersh BJ, Cox DA, McLaughlin MG, Zimetbaum P, Costantini C, Stuckey T, Tcheng JE, Mehran R,Lansky AJ, Grines CL, Stone GW. Impact of delay to angioplasty in patients with acute coronary syndromes undergoinginvasive management: analysis from the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. J Am Coll Cardiol 2010;55:1416–1424.216. Brener SJ, Milford-Beland S, Roe MT, Bhatt DL, Weintraub WS, Brindis RG. Culprit-only or multivessel revascularizationin patients with acute coronary syndromes: an American College of Cardiology National CardiovascularDatabase Registry report. Am Heart J 2008;155:140–146.217. Ben-Gal Y, Moses JW, Mehran R, Lansky AJ,Weisz G, Nikolsky E, Argenziano M, Williams MR, Colombo A, AylwardPE, Stone GW. Surgical versus percutaneous revascularization for multivessel disease in patients withacute coronary syndromes: analysis from the ACUITY (Acute Catheterization and Urgent Intervention TriageStrategy) trial. JACC Cardiovasc Interv 2010;3:1059–1067.218. Serruys PW, Morice MC, Kappetein AP, Colombo A, Holmes DR, Mack MJ, Stahle E, Feldman TE, van denBrand M, Bass EJ, Van Dyck N, Leadley K, Dawkins KD, Mohr FW. Percutaneous coronary intervention versuscoronary-artery bypass grafting for severe coronary artery disease. N Engl J Med 2009;360:961–972.219. Sianos G, Morel MA, Kappetein AP, Morice MC, Colombo A, Dawkins K, van den Brand M, Van Dyck N, RussellME, Mohr FW, Serruys PW. The SYNTAX Score: an angiographic tool grading the complexity of coronaryartery disease. EuroIntervention 2005;1:219–227.220. de Winter RJ, Windhausen F, Cornel JH, Dunselman PH, Janus CL, Bendermacher PE, Michels HR, Sanders GT,Tijssen JG, Verheugt FW. Early invasive versus selectively invasive management for acute coronary syndromes.N Engl J Med 2005;353:1095–1104.221. Monteiro P. Impact of early coronary artery bypass graft in an unselected acute coronary syndrome patient population.Circulation 2006;114:I467–I472.222. Parikh SV, de Lemos JA, Jessen ME, Brilakis ES, Ohman EM, Chen AY, Wang TY, Peterson ED, Roe MT, HolperEM. Timing of in-hospital coronary artery bypass graft surgery for non-ST-segment elevation myocardial infarctionpatients results from the National Cardiovascular Data Registry ACTION Registry-GWTG (Acute CoronaryTreatment and Intervention Outcomes Network Registry-Get With The Guidelines). JACC CardiovascInterv 2010;3:419–427.223. Chu MW, Wilson SR, Novick RJ, Stitt LW, Quantz MA. Does clopidogrel increase blood loss following coronaryartery bypass surgery? Ann Thorac Surg 2004;78:1536–1541.224. Solodky A, Behar S, Boyko V, Battler A, Hasdai D. The outcome of coronary artery bypass grafting surgeryamong patients hospitalized with acute coronary syndrome: the Euro Heart Survey of acute coronary syndromeexperience. Cardiology 2005;103:44–47.225. Kaiser C, Galatius S, Erne P, Eberli F, Alber H, Rickli H, Pedrazzini G, Hornig B, Bertel O, Bonetti P, De Servi S,Brunner-La Rocca HP, Ricard I, Pfisterer M. Drug-eluting versus bare-metal stents in large coronary arteries. NEngl J Med 2010;363:2310–2319.226. Greenhalgh J, Hockenhull J, Rao N, Dundar Y, Dickson RC, Bagust A. Drug-eluting stents versus bare metalstents for angina or acute coronary syndromes. Cochrane Database Syst Rev 2010;5:CD004587.227. Vlaar PJ, Diercks GF, Svilaas T, Vogelzang M, de Smet BJ, van den Heuvel AF, Anthonio RL, Jessurun GA, TanES, Suurmeijer AJ, Zijlstra F. The feasibility and safety of routine thrombus aspiration in patients with non-STelevationmyocardial infarction. Catheter Cardiovasc Interv 2008;72:937–942.228. Rosengren A, Wallentin L, Simoons M, Gitt AK, Behar S, Battler A, Hasdai D. Age, clinical presentation, andoutcome of acute coronary syndromes in the Euroheart acute coronary syndrome survey. Eur Heart J2006;27:789–795.229. Bauer T, Koeth O, Junger C, Heer T, Wienbergen H, Gitt A, Zahn R, Senges J, Zeymer U. Effect of an invasivestrategy on in-hospital outcome in elderly patients with non-ST-elevation myocardial infarction. Eur Heart J2007;28:2873–2878.230. Alexander KP, Newby LK, Cannon CP, Armstrong PW, Gibler WB, Rich MW, Van de Werf F, White HD, WeaverWD, Naylor MD, Gore JM, Krumholz HM, Ohman EM. Acute coronary care in the elderly, part I: non-ST-segment-elevation acute coronary syndromes: a scientific statement for healthcare professionals from the AmericanHeart Association Council on Clinical Cardiology: in collaboration with the Society of Geriatric Cardiology.Circulation 2007;115:2549–2569.231. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED. Excess dosing of antiplatelet and antithrombin agents in the treatment of non-ST-segment elevationacute coronary syndromes. JAMA 2005;294:3108–3116.232. Lopes RD, Alexander KP, Marcucci G, White HD, Spinler S, Col J, Aylward PE, Califf RM, Mahaffey KW. Outcomesin elderly patients with acute coronary syndromes randomized to enoxaparin vs. unfractionated heparin:results from the SYNERGY trial. Eur Heart J 2008;29:1827–1833.233. Wallentin L, Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E. Outcome at 1 year after an invasive comparedwith a non-invasive strategy in unstable coronary-artery disease: the FRISC II invasive randomised trial. FRISCII Investigators. Fast Revascularisation during Instability in Coronary artery disease. Lancet 2000;356:9–16.234. Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E, Wallentin L. 5-Year outcomes in the FRISC-II randomisedtrial of an invasive versus a non-invasive strategy in non-ST-elevation acute coronary syndrome: a follow-upstudy. Lancet 2006;368:998–1004.235. Bach RG, Cannon CP, Weintraub WS, DiBattiste PM, Demopoulos LA, Anderson HV, DeLucca PT, Mahoney EM,Murphy SA, Braunwald E. The effect of routine, early invasive management on outcome for elderly patientswith non-ST-segment elevation acute coronary syndromes. Ann Intern Med 2004;141:186–195.236. Rosengren A, Wallentin L, Gitt AK, Behar S, Battler A, Hasdai D. Sex, age, and clinical presentation of acutecoronary syndromes. Eur Heart J 2004;25:663–670.237. Alfredsson J, Stenestrand U, Wallentin L, Swahn E. Gender differences in management and outcome in non-ST-elevation acute coronary syndrome. Heart 2007;93:1357–1362.238. Hvelplund A, Galatius S, Madsen M, Rasmussen JN, Rasmussen S, Madsen JK, Sand NP, Tilsted HH, ThayssenP, Sindby E, Hojbjerg S, Abildstrom SZ. Women with acute coronary syndrome are less invasively examined andsubsequently less treated than men. Eur Heart J 2010;31:684–690.239. Diercks DB, Owen KP, Kontos MC, Blomkalns A, Chen AY, Miller C, Wiviott S, Peterson ED. Gender differencesin time to presentation for myocardial infarction before and after a national women’s cardiovascular awarenesscampaign: a temporal analysis from the Can Rapid Risk Stratification of Unstable Angina Patients SuppressADverse Outcomes with Early Implementation (CRUSADE) and the National Cardiovascular Data RegistryAcute Coronary Treatment and Intervention Outcomes Network-Get with the Guidelines (NCDR ACTION Registry-GWTG). Am Heart J 2010;160:80–87 e83.240. Heer T, Gitt AK, Juenger C, Schiele R, Wienbergen H, Towae F, Gottwitz M, Zahn R, Zeymer U, Senges J. Genderdifferences in acute non-ST-segment elevation myocardial infarction. Am J Cardiol 2006;98:160–166.241. Bavry AA, Kumbhani DJ, Quiroz R, Ramchandani SR, Kenchaiah S, Antman EM. Invasive therapy along withglycoprotein IIb/IIIa inhibitors and intracoronary stents improves survival in non-ST-segment elevation acutecoronary syndromes: a meta-analysis and review of the literature. Am J Cardiol 2004;93:830–835.242. Fox KA, Poole-Wilson PA, Henderson RA, Clayton TC, Chamberlain DA, Shaw TR, Wheatley DJ, Pocock SJ. Interventionalversus conservative treatment for patients with unstable angina or non-ST-elevation myocardialinfarction: the British Heart Foundation RITA 3 randomised trial. Randomized Intervention Trial of unstableAngina. Lancet 2002;360:743–751.243. Hoenig MR, Doust JA, Aroney CN, Scott IA. Early invasive versus conservative strategies for unstable angina& non-ST-elevation myocardial infarction in the stent era. Cochrane Database Syst Rev 2006;3:CD004815.244. Glaser R, Herrmann HC, Murphy SA, Demopoulos LA, DiBattiste PM, Cannon CP, Braunwald E. Benefit of anearly invasive management strategy in women with acute coronary syndromes. JAMA2002;288:3124–3129.245. Boersma E, Harrington RA, Moliterno DJ, White H, Simoons ML. Platelet glycoprotein IIb/IIIa inhibitors inacute coronary syndromes. Lancet 2002;360:342–343.246. Berger JS, Elliott L, Gallup D, Roe M, Granger CB, Armstrong PW, Simes RJ, White HD, Van de Werf F, TopolEJ, Hochman JS, Newby LK, Harrington RA, Califf RM, Becker RC, Douglas PS. Sex differences in mortalityfollowing acute coronary syndromes. JAMA 2009;302:874–882.247. Bartnik M, Malmberg K, Norhammar A, Tenerz A, Ohrvik J, Ryden L. Newly detected abnormal glucose tolerance:an important predictor of long-term outcome after myocardial infarction. Eur Heart J2004;25:1990–1997.248. Dotevall A, Hasdai D, Wallentin L, Battler A, Rosengren A. Diabetes mellitus: clinical presentation and outcomein men and women with acute coronary syndromes. Data from the Euro Heart Survey ACS. Diabet Med2005;22:1542–1550. 249. Donahoe SM, Stewart GC, McCabe CH, Mohanavelu S, Murphy SA, Cannon CP, Antman EM. Diabetes andmortality following acute coronary syndromes. JAMA 2007;298:765–775.250. Hasin T, Hochadel M, Gitt AK, Behar S, Bueno H, Hasin Y. Comparison of treatment and outcome of acute coronarysyndrome in patients with versus patients without diabetes mellitus. Am J Cardiol 2009;103:772–778.251. De Caterina R, Madonna R, Sourij H, Wascher T. Glycaemic control in acute coronary syndromes: prognosticvalue and therapeutic options. Eur Heart J 2010;31:1557–1564.252. Graham I, Atar D, Borch-Johnsen K, Boysen G, Burell G, Cifkova R, Dallongeville J, De Backer G, Ebrahim S,Gjelsvik B, Herrmann-Lingen C, Hoes A, Humphries S, Knapton M, Perk J, Priori SG, Pyorala K, Reiner Z, RuilopeL, Sans-Menendez S, Scholte op Reimer W, Weissberg P, Wood D, Yarnell J, Zamorano JL, Walma E,Fitzgerald T, Cooney MT, Dudina A. European guidelines on cardiovascular disease prevention in clinical practice:executive summary: Fourth Joint Task Force of the European Society of Cardiology and Other Societies onCardiovascular Disease Prevention in Clinical Practice (Constituted by representatives of nine societies and byinvited experts). Eur Heart J 2007;28:2375–2414.253. Finfer S, Chittock DR, Su SY, Blair D, Foster D, Dhingra V, Bellomo R, Cook D, Dodek P, Henderson WR, HebertPC, Heritier S, Heyland DK, McArthur C, McDonald E, Mitchell I, Myburgh JA, Norton R, Potter J, RobinsonBG, Ronco JJ. Intensive versus conventional glucose control in critically ill patients. N Engl J Med2009;360:1283–1297.254. Diaz R, Goyal A, Mehta SR, Afzal R, Xavier D, Pais P, Chrolavicius S, Zhu J, Kazmi K, Liu L, Budaj A, Zubaid M,Avezum A, Ruda M, Yusuf S. Glucose–insulin–potassium therapy in patients with ST-segment elevation myocardialinfarction. JAMA 2007;298:2399–2405.255. Cannon CP, Weintraub WS, Demopoulos LA, Vicari R, Frey MJ, Lakkis N, Neumann FJ, Robertson DH, DeLuccaPT, DiBattiste PM, Gibson CM, Braunwald E. Comparison of early invasive and conservative strategies in patientswith unstable coronary syndromes treated with the glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med2001;344:1879–1887.256. Hlatky MA, Boothroyd DB, Bravata DM, Boersma E, Booth J, Brooks MM, Carrie D, Clayton TC, Danchin N,Flather M, Hamm CW, Hueb WA, Kahler J, Kelsey SF, King SB, Kosinski AS, Lopes N, McDonald KM, RodriguezA, Serruys P, Sigwart U, Stables RH, Owens DK, Pocock SJ. Coronary artery bypass surgery compared withpercutaneous coronary interventions for multivessel disease: a collaborative analysis of individual patient datafrom ten randomised trials. Lancet 2009;373:1190–1197.257. Chaitman BR, Hardison RM, Adler D, Gebhart S, Grogan M, Ocampo S, Sopko G, Ramires JA, Schneider D,Frye RL. The Bypass Angioplasty Revascularization Investigation 2 Diabetes randomized trial of different treatmentstrategies in type 2 diabetes mellitus with stable ischemic heart disease: impact of treatment strategy oncardiac mortality and myocardial infarction. Circulation 2009;120:2529–2540.258. Frye RL, August P, Brooks MM, Hardison RM, Kelsey SF, MacGregor JM, Orchard TJ, Chaitman BR, Genuth SM,Goldberg SH, Hlatky MA, Jones TL, Molitch ME, Nesto RW, Sako EY, Sobel BE. A randomized trial of therapiesfor type 2 diabetes and coronary artery disease. N Engl J Med 2009;360:2503–2515.259. Banning AP, Westaby S, Morice MC, Kappetein AP, Mohr FW, Berti S, Glauber M, Kellett MA, Kramer RS,Leadley K, Dawkins KD, Serruys PW. Diabetic and nondiabetic patients with left main and/or 3-vessel coronaryartery disease: comparison of outcomes with cardiac surgery and paclitaxel-eluting stents. J Am Coll Cardiol2010;55:1067–1075.260. Hannan EL, Wu C, Walford G, Culliford AT, Gold JP, Smith CR, Higgins RS, Carlson RE, Jones RH. Drug-elutingstents vs. coronary-artery bypass grafting in multivessel coronary disease. N Engl J Med 2008;358:331–341.261. Stettler C, Allemann S, Wandel S, Kastrati A, Morice MC, Schomig A, Pfisterer ME, Stone GW, Leon MB, de LezoJS, Goy JJ, Park SJ, Sabate M, Suttorp MJ, Kelbaek H, Spaulding C, Menichelli M, Vermeersch P, Dirksen MT,Cervinka P, De Carlo M, Erglis A, Chechi T, Ortolani P, Schalij MJ, Diem P, Meier B, Windecker S, Juni P. Drugeluting and bare metal stents in people with and without diabetes: collaborative network meta-analysis. BMJ2008;337:a1331.262. Wiviott SD, Braunwald E, Angiolillo DJ, Meisel S, Dalby AJ, Verheugt FW, Goodman SG, Corbalan R, PurdyDA, Murphy SA, McCabe CH, Antman EM. Greater clinical benefit of more intensive oral antiplatelet therapywith prasugrel in patients with diabetes mellitus in the trial to assess improvement in therapeutic outcomes byoptimizing platelet inhibition with prasugrel-Thrombolysis in Myocardial Infarction 38. Circulation2008;118:1626–1636.263. James S, Angiolillo DJ, Cornel JH, Erlinge D, Husted S, Kontny F, Maya J, Nicolau JC, Spinar J, Storey RF, StevensSR, Wallentin L. Ticagrelor vs. clopidogrel in patients with acute coronary syndromes and diabetes: a substudyfrom the PLATelet inhibition and patient Outcomes (PLATO) trial. Eur Heart J 2010;31:3006–3016.264. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Heeschen C, Hamm CW, Moliterno DJ, Califf RM, WhiteHD, Kleiman NS, Theroux P, Topol EJ. Platelet glycoprotein IIb/IIIa inhibitors reduce mortality in diabetic patientswith non-ST-segment-elevation acute coronary syndromes. Circulation 2001;104:2767–2771.265. Salpeter SR, Greyber E, Pasternak GA, Salpeter EE. Risk of fatal and nonfatal lactic acidosis with metformin usein type 2 diabetes mellitus. Cochrane Database Syst Rev 2010;4:CD002967.266. Hasdai D, Behar S, Wallentin L, Danchin N, Gitt AK, Boersma E, Fioretti PM, Simoons ML, Battler A. A prospectivesurvey of the characteristics, treatments and outcomes of patients with acute coronary syndromes in Europeand the Mediterranean basin; the Euro Heart Survey of Acute Coronary Syndromes (Euro Heart SurveyACS). Eur Heart J 2002;23:1190–1201.267. Goldenberg I, Subirana I, Boyko V, Vila J, Elosua R, Permanyer-Miralda G, Ferreira-Gonzalez I, Benderly M,Guetta V, Behar S, Marrugat J. Relation between renal function and outcomes in patients with non-ST-segmentelevation acute coronary syndrome: real-world data from the European Public Health Outcome Researchand Indicators Collection Project. Arch Intern Med 2010;170:888–895.268. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Relationbetween renal function, presentation, use of therapies and in-hospital complications in acute coronary syndrome:data from the SWEDEHEART register. J Intern Med 2010;268:40–49.269. Collet JP, Montalescot G, Agnelli G, Van de Werf F, Gurfinkel EP, Lopez-Sendon J, Laufenberg CV, Klutman M,Gowda N, Gulba D. Non-ST-segment elevation acute coronary syndrome in patients with renal dysfunction:benefit of low-molecular-weight heparin alone or with glycoprotein IIb/IIIa inhibitors on outcomes. The GlobalRegistry of Acute Coronary Events. Eur Heart J 2005;26:2285–2293.270. Fox KA, Bassand JP, Mehta SR, Wallentin L, Theroux P, Piegas LS, Valentin V, Moccetti T, Chrolavicius S, AfzalR, Yusuf S. Influence of renal function on the efficacy and safety of fondaparinux relative to enoxaparin in nonST-segment elevation acute coronary syndromes. Ann Intern Med 2007;147:304–310.271. James S, Budaj A, Aylward P, Buck KK, Cannon CP, Cornel JH, Harrington RA, Horrow J, Katus H, Keltai M, LewisBS, Parikh K, Storey RF, Szummer K, Wojdyla D, Wallentin L. Ticagrelor versus clopidogrel in acute coronary syndromesin relation to renal function: results from the Platelet Inhibition and Patient Outcomes (PLATO) trial.Circulation 2010;122:1056–1067.272. Pannu N, Wiebe N, Tonelli M. Prophylaxis strategies for contrast-induced nephropathy. JAMA2006;295:2765–2779.273. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Influenceof renal function on the effects of early revascularization in non-ST-elevation myocardial infarction: data fromthe Swedish Web-System for Enhancement and Development of Evidence-Based Care in Heart Disease EvaluatedAccording to Recommended Therapies (SWEDEHEART). Circulation 2009;120:851–858.274. Steg PG, Dabbous OH, Feldman LJ, Cohen-Solal A, Aumont MC, Lopez-Sendon J, Budaj A, Goldberg RJ, KleinW, Anderson FA Jr. Determinants and prognostic impact of heart failure complicating acute coronary syndromes:observations from the Global Registry of Acute Coronary Events (GRACE). Circulation2004;109:494–499.275. Dickstein K, Vardas PE, Auricchio A, Daubert JC, Linde C, McMurray J, Ponikowski P, Priori SG, Sutton R, vanVeldhuisen DJ, Vahanian A, Bax J, Ceconi C, Dean V, Filippatos G, Funck-Brentano C, Hobbs R, Kearney P, Mc-Donagh T, Popescu BA, Reiner Z, Sechtem U, Sirnes PA, Tendera M, Vardas P, Widimsky P, Anker SD, Blanc JJ,Gasparini M, Hoes AW, Israel CW, Kalarus Z, Merkely B, Swedberg K, Camm AJ. 2010 Focused Update of ESCGuidelines on device therapy in heart failure: an update of the 2008 ESC Guidelines for the diagnosis andtreatment of acute and chronic heart failure and the 2007 ESC guidelines for cardiac and resynchronizationtherapy. Developed with the special contribution of the Heart Failure Association and the European HeartRhythm Association. Eur Heart J 2010;31:2677–2687.276. Pitt B, Remme W, Zannad F, Neaton J, Martinez F, Roniker B, Bittman R, Hurley S, Kleiman J, Gatlin M.Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction.N Engl J Med 2003;348:1309–1321.277. Zannad F, McMurray JJ, Krum H, van Veldhuisen DJ, Swedberg K, Shi H, Vincent J, Pocock SJ, Pitt B. Eplerenonein patients with systolic heart failure and mild symptoms. N Engl J Med 2011;364:11–21.278. Moss AJ, Zareba W, Hall WJ, Klein H, Wilber DJ, Cannom DS, Daubert JP, Higgins SL, Brown MW, Andrews ML.Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction.N Engl J Med 2002;346:877–883.279. Diercks DB, Roe MT, Mulgund J, Pollack CV Jr., Kirk JD, Gibler WB, Ohman EM, Smith SC Jr., Boden WE, PetersonED. The obesity paradox in non-ST-segment elevation acute coronary syndromes: results from the CanRapid risk stratification of Unstable angina patients Suppress ADverse outcomes with Early implementation ofthe American College of Cardiology/American Heart Association Guidelines Quality Improvement Initiative.Am Heart J 2006;152:140–148.280. Steinberg BA, Cannon CP, Hernandez AF, Pan W, Peterson ED, Fonarow GC. Medical therapies and invasivetreatments for coronary artery disease by body mass: the ‘obesity paradox’ in the Get With The Guidelines database.Am J Cardiol 2007;100:1331–1335.281. Ong P, Athanasiadis A, Borgulya G, Voehringer M, Sechtem U. 3-Year follow-up of patients with coronary arteryspasm as cause of acute coronary syndrome: the CASPAR (coronary artery spasm in patients with acutecoronary syndrome) study follow-up. J Am Coll Cardiol 2011;57:147–152.282. Hasin T, Sorkin A, Markiewicz W, Hammerman H, Aronson D. Prevalence and prognostic significance of transient,persistent, and new-onset anemia after acute myocardial infarction. Am J Cardiol 2009;104:486–491.283. Bassand JP, Afzal R, Eikelboom J, Wallentin L, Peters R, Budaj A, Fox KA, Joyner CD, Chrolavicius S, GrangerCB, Mehta S, Yusuf S. Relationship between baseline haemoglobin and major bleeding complications in acutecoronary syndromes. Eur Heart J 2010;31:50–58.284. Chase AJ, Fretz EB, Warburton WP, Klinke WP, Carere RG, Pi D, Berry B, Hilton JD. Association of the arterialaccess site at angioplasty with transfusion and mortality: the M.O.R.T.A.L study (Mortality benefit Of ReducedTransfusion after percutaneous coronary intervention via the Arm or Leg). Heart 2008;94:1019–1025.285. Agostoni P, Biondi-Zoccai GG, de Benedictis ML, Rigattieri S, Turri M, Anselmi M, Vassanelli C, Zardini P, LouvardY, Hamon M. Radial versus femoral approach for percutaneous coronary diagnostic and interventional procedures;systematic overview and meta-analysis of randomized trials. J Am Coll Cardiol 2004;44:349–356.286. Alexander KP, Chen AY, Wang TY, Rao SV, Newby LK, LaPointe NM, Ohman EM, Roe MT, Boden WE, HarringtonRA, Peterson ED. Transfusion practice and outcomes in non-ST-segment elevation acute coronary syndromes.Am Heart J 2008;155:1047–1053.287. Hill SR, Carless PA, Henry DA, Carson JL, Hebert PC, McClelland DB, Henderson KM. Transfusion thresholdsand other strategies for guiding allogeneic red blood cell transfusion. Cochrane Database Syst Rev2002;2:CD002042.288. Mehran R, Rao SV, Bhatt DL, Gibson CM, Caixeta A, Eikelboom J, Kaul S, Wiviott SD, Menon V, Nikolsky E, SerebruanyV, Valgimigli M, Vranckx P, Taggart D, Sabik JF, Cutlip DE, Krucoff MW, Ohman EM, Steg PG, White H.Standardized bleeding definitions for cardiovascular clinical trials: a consensus report from the Bleeding AcademicResearch Consortium (BARC). Circulation 2011;123:2736–2747.289. Fox KA, Carruthers K, Steg PG, Avezum A, Granger CB, Montalescot G, Goodman SG, Gore JM, Quill AL,Eagle KA. Has the frequency of bleeding changed over time for patients presenting with an acute coronary syndrome?The global registry of acute coronary events. Eur Heart J 2010;31:667–675.290. Eikelboom JW, Mehta SR, Anand SS, Xie C, Fox KA, Yusuf S. Adverse impact of bleeding on prognosis in patientswith acute coronary syndromes. Circulation 2006;114:774–782.291. Budaj A, Eikelboom JW, Mehta SR, Afzal R, Chrolavicius S, Bassand JP, Fox KA, Wallentin L, Peters RJ, GrangerCB, Joyner CD, Yusuf S. Improving clinical outcomes by reducing bleeding in patients with non-ST-elevationacute coronary syndromes. Eur Heart J 2009;30:655–661.292. Mehran R, Pocock SJ, Stone GW, Clayton TC, Dangas GD, Feit F, Manoukian SV, Nikolsky E, Lansky AJ, KirtaneA, White HD, Colombo A, Ware JH, Moses JW, Ohman EM. Associations of major bleeding and myocardialinfarction with the incidence and timing of mortality in patients presenting with non-ST-elevation acute coronarysyndromes: a risk model from the ACUITY trial. Eur Heart J 2009;30:1457–1466.293. Antman EM, Wiviott SD, Murphy SA, Voitk J, Hasin Y, Widimsky P, Chandna H, Macias W, McCabe CH, BraunwaldE. Early and late benefits of prasugrel in patients with acute coronary syndromes undergoing percutaneouscoronary intervention: a TRITON-TIMI 38 (TRial to Assess Improvement in Therapeutic Outcomes byOptimizing Platelet InhibitioN with Prasugrel-Thrombolysis In Myocardial Infarction) analysis. J Am Coll Cardiol2008;51:2028–2033.294. Berger PB, Bhatt DL, Fuster V, Steg PG, Fox KA, Shao M, Brennan DM, Hacke W, Montalescot G, Steinhubl SR,Topol EJ. Bleeding complications with dual antiplatelet therapy among patients with stable vascular disease orrisk factors for vascular disease: results from the Clopidogrel for High Atherothrombotic Risk and IschemicStabilization, Management, and Avoidance (CHARISMA) trial. Circulation 2010;121:2575–2583.295. Sorensen R, Hansen ML, Abildstrom SZ, Hvelplund A, Andersson C, Jorgensen C, Madsen JK, Hansen PR,Kober L, Torp-Pedersen C, Gislason GH. Risk of bleeding in patients with acute myocardial infarction treatedwith different combinations of aspirin, clopidogrel, and vitamin K antagonists in Denmark: a retrospectiveanalysis of nationwide registry data. Lancet 2009;374:1967–1974. 296. Joyner CD, Peters RJ, Afzal R, Chrolavicius S, Mehta SR, Fox KA, Granger CB, Franzosi MG, Flather M, BudajA, Bassand JP, Yusuf S. Fondaparinux compared to enoxaparin in patients with acute coronary syndromeswithout ST-segment elevation: outcomes and treatment effect across different levels of risk. Am Heart J2009;157:502–508.297. Spencer FA, Moscucci M, Granger CB, Gore JM, Goldberg RJ, Steg PG, Goodman SG, Budaj A, FitzGerald G,Fox KA. Does comorbidity account for the excess mortality in patients with major bleeding in acute myocardialinfarction? Circulation 2007;116:2793–2801.298. Rao SV, Jollis JG, Harrington RA, Granger CB, Newby LK, Armstrong PW, Moliterno DJ, Lindblad L, Pieper K,Topol EJ, Stamler JS, Califf RM. Relationship of blood transfusion and clinical outcomes in patients with acutecoronary syndromes. JAMA 2004;292:1555–1562.299. Alexander KP, Peterson ED. Minimizing the risks of anticoagulants and platelet inhibitors. Circulation2010;121:1960–1970.300. Marso SP, Amin AP, House JA, Kennedy KF, Spertus JA, Rao SV, Cohen DJ, Messenger JC, Rumsfeld JS. Associationbetween use of bleeding avoidance strategies and risk of periprocedural bleeding among patients undergoingpercutaneous coronary intervention. JAMA 2010;303:2156–2164.301. Yank V, Tuohy CV, Logan AC, Bravata DM, Staudenmayer K, Eisenhut R, Sundaram V, McMahon D, Olkin I,McDonald KM, Owens DK, Stafford RS. Systematic review: benefits and harms of in-hospital use of recombinantfactor VIIa for off-label indications. Ann Intern Med 2011;154:529–540.302. Hebert PC, Wells G, Blajchman MA, Marshall J, Martin C, Pagliarello G, Tweeddale M, Schweitzer I, Yetisir E.A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. Transfusion Requirementsin Critical Care Investigators, Canadian Critical Care Trials Group. N Engl J Med1999;340:409–417.303. Singh AK, Szczech L, Tang KL, Barnhart H, Sapp S, Wolfson M, Reddan D. Correction of anemia with epoetinalfa in chronic kidney disease. N Engl J Med 2006;355:2085–2098.304. Menzin J, Wygant G, Hauch O, Jackel J, Friedman M. One-year costs of ischemic heart disease among patientswith acute coronary syndromes: findings from a multi-employer claims database. Curr Med Res Opin2008;24:461–468.305. Smith SC Jr., Allen J, Blair SN, Bonow RO, Brass LM, Fonarow GC, Grundy SM, Hiratzka L, Jones D, KrumholzHM, Mosca L, Pasternak RC, Pearson T, Pfeffer MA, Taubert KA. AHA/ACC guidelines for secondary preventionfor patients with coronary and other atherosclerotic vascular disease: 2006 update: endorsed by the NationalHeart, Lung, and Blood Institute. Circulation 2006;113:2363–2372.306. Chow CK, Jolly S, Rao-Melacini P, Fox KA, Anand SS, Yusuf S. Association of diet, exercise, and smoking modificationwith risk of early cardiovascular events after acute coronary syndromes. Circulation2010;121:750–758.307. Chew DP, Huynh LT, Liew D, Astley C, Soman A, Brieger D. Potential survival gains in the treatment of myocardialinfarction. Heart 2009;95:1844–1850.308. Ford ES, Ajani UA, Croft JB, Critchley JA, Labarthe DR, Kottke TE, Giles WH, Capewell S. Explaining the decreasein U.S. deaths from coronary disease, 1980–2000. N Engl J Med 2007;356:2388–2398.309. Dagenais GR, Pogue J, Fox K, Simoons ML, Yusuf S. Angiotensinconverting-enzyme inhibitors in stable vasculardisease without left ventricular systolic dysfunction or heart failure: a combined analysis of three trials.Lancet 2006;368:581–588.310. Danchin N, Cucherat M, Thuillez C, Durand E, Kadri Z, Steg PG. Angiotensinconverting enzyme inhibitors inpatients with coronary artery disease and absence of heart failure or left ventricular systolic dysfunction: anoverview of long-term randomized controlled trials. Arch Intern Med 2006;166:787–796.311. Yusuf S, Teo KK, Pogue J, Dyal L, Copland I, Schumacher H, Dagenais G, Sleight P, Anderson C. Telmisartan,ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008;358:1547–1559.312. Hulten E, Jackson JL, Douglas K, George S, Villines TC. The effect of early, intensive statin therapy on acute coronarysyndrome: a meta-analysis of randomized controlled trials. Arch Intern Med 2006;166:1814–1821.313. Cannon CP, Braunwald E, McCabe CH, Rader DJ, Rouleau JL, Belder R, Joyal SV, Hill KA, Pfeffer MA, Skene AM.Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med2004;350:1495–1504.314. Lopez-Sendon J, Swedberg K, McMurray J, Tamargo J, Maggioni AP, Dargie H, Tendera M, Waagstein F, KjekshusJ, Lechat P, Torp-Pedersen C. Expert consensus document on beta-adrenergic receptor blockers. Eur HeartJ 2004;25:1341–1362.315. Pfeffer MA, Braunwald E, Moye LA, Basta L, Brown EJ Jr., Cuddy TE, Davis BR, Geltman EM, Goldman S, FlakerGC, Klein M, Lamas GA, Packer M, Rouleau J, Rouleau JL, Rutherford J, Wertheimer JH, Hawkins CM. Effectof captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction.Results of the survival and ventricular enlargement trial. The SAVE Investigators. N Engl J Med1992;327:669–677.316. Torp-Pedersen C, Kober L. Effect of ACE inhibitor trandolapril on life expectancy of patients with reduced leftventricularfunction after acute myocardial infarction. TRACE Study Group. Trandolapril Cardiac Evaluation.Lancet 1999;354:9–12.317. Pfeffer MA, McMurray JJ, Velazquez EJ, Rouleau JL, Kober L, Maggioni AP, Solomon SD, Swedberg K, Van deWerf F, White H, Leimberger JD, Henis M, Edwards S, Zelenkofske S, Sellers MA, Califf RM. Valsartan, captopril,or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N EnglJ Med 2003;349:1893–1906.318. Fox KA, Steg PG, Eagle KA, Goodman SG, Anderson FA Jr., Granger CB, Flather MD, Budaj A, Quill A, GoreJM. Decline in rates of death and heart failure in acute coronary syndromes, 1999–2006. JAMA2007;297:1892–1900.319. Fox K, Garcia MA, Ardissino D, Buszman P, Camici PG, Crea F, Daly C, De Backer G, Hjemdahl P, Lopez-SendonJ, Marco J, Morais J, Pepper J, Sechtem U, Simoons M, Thygesen K, Priori SG, Blanc JJ, Budaj A, Camm J,Dean V, Deckers J, Dickstein K, Lekakis J, McGregor K, Metra M, Osterspey A, Tamargo J, Zamorano JL. Guidelineson the management of stable angina pectoris: executive summary: the Task Force on the Managementof Stable Angina Pectoris of the European Society of Cardiology. Eur Heart J 2006;27:1341–1381.320. Rahimi K, Watzlawek S, Thiele H, Secknus MA, Hayerizadeh BF, Niebauer J, Schuler G. Incidence, time course,and predictors of early malignant ventricular arrhythmias after non-ST-segment elevation myocardial infarctionin patients with early invasive treatment. Eur Heart J 2006;27:1706–1711.
Цели вторичной профилактики после ОКС/ИМ без подъема сегмента ST
Четвертый этап: методы реваскуляризацииЕсли при ангиографии выявлены атероматозныеизменения, однако отсутствует критический стеноз ко-ронарных артерий, показана медикаментозная терапия.Необходимо пересмотреть диагноз ОКС без подъема сег-мента ST с учетом других возможных причин появлениясимптомов. Однако отсутствие критического стеноза неисключает диагноз ОКС, если клинические симптомы ука-зывают на ишемическую боль в груди и определяютсябиомаркеры. В этом случае пациенты должны получатьлечение в соответствии с рекомендациями по ведениюпациентов с ОКС без подъема сегмента ST.Рекомендации по выбору метода реваскуляризацииу пациентов с ОКС без подъема сегмента ST соответ-ствуют рекомендациям по выбору метода плановоговмешательства. У пациента со стенозом одной коронар-ной артерии методом выбора является ЧКВ. У пациен-тов с поражением нескольких сосудов выбор между ЧКВи КШ должен быть индивидуальным в соответствии спротоколом лечебного учреждения. В некоторых слу-чаях оправданно ЧКВ на ведущей артерии и последую-щее плановое шунтирование других пораженных со-судов с учетом результатов оценки ишемии и/илифункционального резерва кровотока.Во время ЧКВ не следует менять антикоагулянты. Па-циентам, получавшим фондапаринукс, перед ЧКВ сле-дует добавить НФГ. Применение блокатора GP IIb/IIIaрецепторов оправданно при повышенном уровне тро-понинов или наличии ангиографических признаковтромба. Если планируется КШ, следует отменить бло-каторы P2Y12 рецепторов и отложить операцию, еслиэто позволяют клиническое состояние и ангиографиче-ские данные.Если ангиография указывает на невозможность ре-васкуляризации в связи с распространенностью и/илилокализацией поражений, необходимо усилить меди-каментозную терапию и назначить меры вторичной про-филактики.
Пятый этап: выписка из стационара и наблюдениепосле выпискиХотя большинство нежелательных событий у паци-ентов с ОКС без подъема сегмента ST наблюдают на ран-нем этапе, риск ИМ или смерти остается повышеннымв течение нескольких мес. После ранней реваскуляри-зации риск развития угрожающих жизни аритмийнизкий (2,5%); 80% из них развиваются в течение пер-вых 12 ч после появления симптомов [320]. Соответ-ственно, продолжение мониторирования после24-48 ч обычно не требуется. Пациенты с ОКС безподъема сегмента ST должны находиться в стациона-ре в течение по крайней мере 24 ч после успешного стен-тирования ведущего стеноза. Всем пациентам показа-ны интенсивная модификация риска и улучшение об-раза жизни (см. раздел 5.6.). Включение пациента в про-грамму реабилитации после выписки повышает при-верженность и может способствовать модификациифакторов риска. Необходимые меры профилактикипосле выписки из стационара указаны в табл. 15.
Литература
1. Murray CJ, Lopez AD. Alternative projections of mortality and disability by cause 1990–2020: Global Burden ofDisease Study. Lancet 1997;349:1498–1504. 2. Van deWerf F, Bax J, Betriu A, Blomstrom-Lundqvist C, Crea F, Falk V, Filippatos G, Fox K, Huber K, Kastrati A,Rosengren A, Steg PG, Tubaro M, Verheugt F, Weidinger F, Weis M. Management of acute myocardial infarctionin patients presenting with persistent ST-segment elevation: the Task Force on the Management of ST-SegmentElevation Acute Myocardial Infarction of the European Society of Cardiology. Eur Heart J 2008;29:2909–2945.3. Bassand JP, Hamm CW, Ardissino D, Boersma E, Budaj A, Fernandez-Aviles F, Fox KA, Hasdai D, Ohman EM,Wallentin L, Wijns W. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronarysyndromes. Eur Heart J 2007;28:1598–1660.4. Yeh RW, Sidney S, Chandra M, Sorel M, Selby JV, Go AS. Population trends in the incidence and outcomes of acutemyocardial infarction. N Engl J Med 2010;362:2155–2165.5. Fox KA, Eagle KA, Gore JM, Steg PG, Anderson FA. The Global Registry of Acute Coronary Events, 1999 to 2009—GRACE. Heart 2010;96:1095–1101.6. Savonitto S, Ardissino D, Granger CB, Morando G, Prando MD, Mafrici A, Cavallini C, Melandri G, Thompson TD,Vahanian A, Ohman EM, Califf RM, Van de Werf F, Topol EJ. Prognostic value of the admission electrocardiogramin acute coronary syndromes. JAMA 1999;281:707–713.7. Mandelzweig L, Battler A, Boyko V, Bueno H, Danchin N, Filippatos G, Gitt A, Hasdai D, Hasin Y, Marrugat J,Van de Werf F, Wallentin L, Behar S. The second Euro Heart Survey on acute coronary syndromes: characteristics,treatment, and outcome of patients with ACS in Europe and the Mediterranean Basin in 2004. Eur Heart J2006;27:2285–2293.8. Terkelsen CJ, Lassen JF, Norgaard BL, Gerdes JC, Jensen T, Gotzsche LB, Nielsen TT, Andersen HR. Mortality ratesin patients with ST-elevation vs. non-ST-elevation acute myocardial infarction: observations from an unselectedcohort. Eur Heart J 2005;26:18–26.9. Hamm CW, Mo¨llmann H, Bassand JP, Van deWerf F. Acute coronary syndrome. In: Camm AJ, Lu¨scher TF, SerruysPW, eds. The ESC Textbook of Cardiovascular Medicine. 2nd ed. Oxford: Oxford University Press; 2009.10. Stone GW, Maehara A, Lansky AJ, de Bruyne B, Cristea E, Mintz GS, Mehran R, McPherson J, Farhat N, MarsoSP, Parise H, Templin B, White R, Zhang Z, Serruys PW. A prospective natural-history study of coronary atherosclerosis.N Engl J Med 2011;364:226–235.11. Campeau L. Grading of angina pectoris. Circulation 1976;54:522–523.12. van Domburg RT, van Miltenburg-van Zijl AJ, Veerhoek RJ, Simoons ML. Unstable angina: good long-term outcomeafter a complicated early course. J Am Coll Cardiol 1998;31:1534–1539.13. Canto JG, Fincher C, Kiefe CI, Allison JJ, Li Q, Funkhouser E, Centor RM, Selker HP,Weissman NW. Atypical presentationsamong Medicare beneficiaries with unstable angina pectoris. Am J Cardiol 2002;90:248–253.14. Culic V, Eterovic D, Miric D, Silic N. Symptom presentation of acute myocardial infarction: influence of sex, age,and risk factors. Am Heart J 2002;144:1012–1017.15. Brieger D, Eagle KA, Goodman SG, Steg PG, Budaj A, White K, Montalescot G. Acute coronary syndromeswithout chest pain, an underdiagnosed and undertreated high-risk group: insights from the Global Registry ofAcute Coronary Events. Chest 2004;126:461–469.16. Lev EI, Battler A, Behar S, Porter A, Haim M, Boyko V, Hasdai D. Frequency, characteristics, and outcome of patientshospitalized with acute coronary syndromes with undetermined electrocardiographic patterns. Am J Cardiol2003;91:224–227.17. Diercks DB, Peacock WF, Hiestand BC, Chen AY, Pollack CV Jr., Kirk JD, Smith SC Jr., Gibler WB, Ohman EM,Blomkalns AL, Newby LK, Hochman JS, Peterson ED, Roe MT. Frequency and consequences of recording an electrocardiogram.10 min after arrival in an emergency room in non-ST-segment elevation acute coronary syndromes(from the CRUSADE Initiative). Am J Cardiol 2006;97:437–442.18. Thygesen K, Alpert JS, White HD, Jaffe AS, Apple FS, Galvani M, Katus HA, Newby LK, Ravkilde J, Chaitman B,Clemmensen PM, Dellborg M, Hod H, Porela P, Underwood R, Bax JJ, Beller GA, Bonow R, Van der Wall EE, BassandJP, Wijns W, Ferguson TB, Steg PG, Uretsky BF, Williams DO, Armstrong PW, Antman EM, Fox KA, HammCW, Ohman EM, Simoons ML, Poole-Wilson PA, Gurfinkel EP, Lopez-Sendon JL, Pais P, Mendis S, Zhu JR, WallentinLC, Fernandez-Aviles F, Fox KM, Parkhomenko AN, Priori SG, Tendera M, Voipio-Pulkki LM, Vahanian A,Camm AJ, De Caterina R, Dean V, Dickstein K, Filippatos G, Funck-Brentano C, Hellemans I, Kristensen SD, Mc-Gregor K, Sechtem U, Silber S, Widimsky P, Zamorano JL, Morais J, Brener S, Harrington R, Morrow D, Lim M,Martinez-Rios MA, Steinhubl S, Levine GN, Gibler WB, Goff D, Tubaro M, Dudek D, Al-Attar N. Universal definitionof myocardial infarction. Circulation 2007;116:2634–2653.19. Okamatsu K, Takano M, Sakai S, Ishibashi F, Uemura R, Takano T, Mizuno K. Elevated troponin T levels and lesioncharacteristics in non-ST-elevation acute coronary syndromes. Circulation 2004;109:465–470.20. Keller T, Zeller T, Peetz D, Tzikas S, Roth A, Czyz E, Bickel C, Baldus S, Warnholtz A, Frohlich M, Sinning CR,Eleftheriadis MS, Wild PS, Schnabel RB, Lubos E, Jachmann N, Genth-Zotz S, Post F, Nicaud V, Tiret L, LacknerKJ, Munzel TF, Blankenberg S. Sensitive troponin I assay in early diagnosis of acute myocardial infarction. N EnglJ Med 2009;361:868–877.21. Reichlin T, Hochholzer W, Bassetti S, Steuer S, Stelzig C, Hartwiger S, Biedert S, Schaub N, Buerge C, Potocki M,Noveanu M, Breidthardt T, Twerenbold R, Winkler K, Bingisser R, Mueller C. Early diagnosis of myocardial infarctionwith sensitive cardiac troponin assays. N Engl J Med 2009;361:858–867.22. Giannitsis E, Becker M, Kurz K, Hess G, Zdunek D, Katus HA. High-sensitivity cardiac troponin T for early predictionof evolving non-ST-segment elevation myocardial infarction in patients with suspected acute coronarysyndrome and negative troponin results on admission. Clin Chem 2010;56:642–650.23. Weber M, Bazzino O, Estrada JJN, Miguel R, Salzberg S, Fuselli JJ, Liebetrau C, Woelken M, Moellmann H, NefH, Hamm C. Improved diagnostic and prognostic performance of a new high-sensitive troponin T assay in patientswith acute coronary syndrome. Am Heart J 2011;162:81–88.24. Omland T, de Lemos JA, Sabatine MS, Christophi CA, Rice MM, Jablonski KA, Tjora S, Domanski MJ, Gersh BJ,Rouleau JL, Pfeffer MA, Braunwald E. A sensitive cardiac troponin T assay in stable coronary artery disease. NEngl J Med 2009;361:2538–2547.25. de Lemos JA, Drazner MH, Omland T, Ayers CR, Khera A, Rohatgi A, Hashim I, Berry JD, Das SR, Morrow DA,McGuire DK. Association of troponin T detected with a highly sensitive assay and cardiac structure and mortalityrisk in the general population. JAMA 2010;304:2503–2512.26. Otsuka T, Kawada T, Ibuki C, Seino Y. Association between high-sensitivity cardiac troponin T levels and thepredicted cardiovascular risk in middle-aged men without overt cardiovascular disease. Am Heart J2010;159:972–978.27. Thygesen K, Mair J, Katus H, Plebani M, Venge P, Collinson P, Lindahl B, Giannitsis E, Hasin Y, Galvani M, TubaroM, Alpert JS, Biasucci LM, Koenig W, Mueller C, Huber K, Hamm C, Jaffe AS. Recommendations for the use ofcardiac troponin measurement in acute cardiac care. Eur Heart J 2010;31:2197–2204.28. Apple FS, Murakami MM, Pearce LA, Herzog CA. Predictive value of cardiac troponin I and T for subsequentdeath in end-stage renal disease. Circulation 2002;106:2941–2945.29. Aviles RJ, Askari AT, Lindahl B, Wallentin L, Jia G, Ohman EM, Mahaffey KW, Newby LK, Califf RM, Simoons ML,Topol EJ, Berger P, Lauer MS. Troponin T levels in patients with acute coronary syndromes, with or without renaldysfunction. N Engl J Med 2002;346:2047–2052.30. Hamm CW, Goldmann BU, Heeschen C, Kreymann G, Berger J, Meinertz T. Emergency room triage of patientswith acute chest pain by means of rapid testing for cardiac troponin T or troponin I. N Engl J Med1997;337:1648–1653.31. Wu AH, Apple FS, Gibler WB, Jesse RL, Warshaw MM, Valdes R Jr. National Academy of Clinical BiochemistryStandards of Laboratory Practice: recommendations for the use of cardiac markers in coronary artery diseases.Clin Chem 1999;45:1104–1121.32. Than M, Cullen L, Reid CM, Lim SH, Aldous S, Ardagh MW, Peacock WF, Parsonage WA, Ho HF, Ko HF, KasliwalRR, Bansal M, Soerianata S, Hu D, Ding R, Hua Q, Seok-Min K, Sritara P, Sae-Lee R, Chiu TF, Tsai KC, Chu FY, ChenWK, Chang WH, Flaws DF, George PM, Richards AM. A 2-h diagnostic protocol to assess patients with chestpain symptoms in the Asia-Pacific region (ASPECT): a prospective observational validation study. Lancet2011;377:1077–1084.33. Cheitlin MD, Armstrong WF, Aurigemma GP, Beller GA, Bierman FZ, Davis JL, Douglas PS, Faxon DP, Gillam LD,Kimball TR, Kussmaul WG, Pearlman AS, Philbrick JT, Rakowski H, Thys DM, Antman EM, Smith SC Jr., AlpertJS, Gregoratos G, Anderson JL, Hiratzka LF, Hunt SA, Fuster V, Jacobs AK, Gibbons RJ, Russell RO. ACC/AHA/ASE2003 guideline update for the clinical application of echocardiography: summary article: a report of the AmericanCollege of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASE Committeeto Update the 1997 Guidelines for the Clinical Application of Echocardiography). Circulation2003;108:1146–1162.34. Nucifora G, Badano LP, Sarraf-Zadegan N, Karavidas A, Trocino G, Scaffidi G, Pettinati G, Astarita C, VysniauskasV, Gregori D, Ilerigelen B, Marinigh R, Fioretti PM. Comparison of early dobutamine stress echocardiography andexercise electrocardiographic testing for management of patients presenting to the emergency departmentwith chest pain. Am J Cardiol 2007;100:1068–1073.35. Kwong RY, Schussheim AE, Rekhraj S, Aletras AH, Geller N, Davis J, Christian TF, Balaban RS, Arai AE. Detectingacute coronary syndrome in the emergency department with cardiac magnetic resonance imaging. Circulation2003;107:531–537.36. Udelson JE, Beshansky JR, Ballin DS, Feldman JA, Griffith JL, Handler J, Heller GV, Hendel RC, Pope JH, RuthazerR, Spiegler EJ, Woolard RH, Selker HP. Myocardial perfusion imaging for evaluation and triage of patientswith suspected acute cardiac ischemia: a randomized controlled trial. JAMA 2002;288:2693–2700.37. Hoffmann U, Bamberg F, Chae CU, Nichols JH, Rogers IS, Seneviratne SK, Truong QA, Cury RC, Abbara S, ShapiroMD, Moloo J, Butler J, Ferencik M, Lee H, Jang IK, Parry BA, Brown DF, Udelson JE, Achenbach S, Brady TJ,Nagurney JT. Coronary computed tomography angiography for early triage of patients with acute chest pain:the ROMICAT (Rule Out Myocardial Infarction using Computer Assisted Tomography) trial. J Am Coll Cardiol2009;53:1642–1650.38. Rubinshtein R, Halon DA, Gaspar T, Jaffe R, Karkabi B, Flugelman MY, Kogan A, Shapira R, Peled N, Lewis BS.Usefulness of 64-slice cardiac computed tomographic angiography for diagnosing acute coronary syndromesand predicting clinical outcome in emergency department patients with chest pain of uncertain origin. Circulation2007;115:1762–1768.39. Meijboom WB, Mollet NR, Van Mieghem CA, Weustink AC, Pugliese F, van Pelt N, Cademartiri F, Vourvouri E,de Jaegere P, Krestin GP, de Feyter PJ 64-Slice CT coronary angiography in patients with non-ST elevation acutecoronary syndrome. Heart 2007;93:1386–1392.40. Hollander JE, Chang AM, Shofer FS, Collin MJ, Walsh KM, McCusker CM, Baxt WG, Litt HI. One-year outcomesfollowing coronary computerized tomographic angiography for evaluation of emergency department patientswith potential acute coronary syndrome. Acad Emerg Med 2009;16:693–698.41. Chang SA, Choi SI, Choi EK, Kim HK, Jung JW, Chun EJ, Kim KS, Cho YS, Chung WY, Youn TJ, Chae IH, Choi DJ,Chang HJ. Usefulness of 64-slice multidetector computed tomography as an initial diagnostic approach in patientswith acute chest pain. Am Heart J 2008;156:375–383.42. Effects of tissue plasminogen activator and a comparison of early invasive and conservative strategies in unstableangina and non-Q-wave myocardial infarction. Results of the TIMI IIIB Trial. Thrombolysis in Myocardial Ischemia.Circulation 1994;89:1545–1556.43. Invasive compared with non-invasive treatment in unstable coronary-artery disease: FRISC II prospective randomisedmulticentre study. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators.Lancet 1999;354:708–715.44. Tonino PA, De Bruyne B, Pijls NH, Siebert U, Ikeno F, van’ t Veer M, Klauss V, Manoharan G, Engstrom T, OldroydKG, Ver Lee PN, MacCarthy PA, Fearon WF. Fractional flow reserve versus angiography for guiding percutaneouscoronary intervention. N Engl J Med 2009;360:213–224.45. Jolly SS, Yusuf S, Cairns J, Niemela K, Xavier D, Widimsky P, Budaj A, Niemela M, Valentin V, Lewis BS, AvezumA, Steg PG, Rao SV, Gao P, Afzal R, Joyner CD, Chrolavicius S, Mehta SR. Radial versus femoral access for coronaryangiography and intervention in patients with acute coronary syndromes (RIVAL): a randomised, parallelgroup, multicentre trial. Lancet 2011;377:1409–1420.46. Hasdai D, Lev EI, Behar S, Boyko V, Danchin N, Vahanian A, Battler A. Acute coronary syndromes in patients withpre-existing moderate to severe valvular disease of the heart: lessons from the Euro-Heart Survey of acute coronarysyndromes. Eur Heart J 2003;24:623–629.47. Hasin Y, Danchin N, Filippatos GS, Heras M, Janssens U, Leor J, Nahir M, Parkhomenko A, Thygesen K, TubaroM, Wallentin LC, Zakke I. Recommendations for the structure, organization, and operation of intensive cardiaccare units. Eur Heart J 2005;26:1676–1682.48. Granger CB, Goldberg RJ, Dabbous O, Pieper KS, Eagle KA, Cannon CP, Van De Werf F, Avezum A, GoodmanSG, Flather MD, Fox KA. Predictors of hospital mortality in the global registry of acute coronary events. Arch InternMed 2003;163:2345–2353.49. Antman EM, Cohen M, Bernink PJ, McCabe CH, Horacek T, Papuchis G, Mautner B, Corbalan R, Radley D,Braunwald E. The TIMI risk score for unstable angina/non-ST elevation MI: a method for prognostication andtherapeutic decision making. JAMA 2000;284:835–842.50. Fox KA, Dabbous OH, Goldberg RJ, Pieper KS, Eagle KA, Van de Werf F, Avezum A, Goodman SG, Flather MD,Anderson FA Jr., Granger CB. Prediction of risk of death and myocardial infarction in the six months after presentationwith acute coronary syndrome: prospective multinational observational study (GRACE). BMJ2006;333:1091. 51. Carrillo X, Curos A, Muga R, Serra J, Sanvisens A, Bayes-Genis A. Acute coronary syndrome and cocaine use:8-year prevalence and inhospital outcomes. Eur Heart J 2011;32:1244–1250.52. Holmvang L, Clemmensen P, Lindahl B, Lagerqvist B, Venge P, Wagner G, Wallentin L, Grande P. Quantitativeanalysis of the admission electrocardiogram identifies patients with unstable coronary artery disease who benefitthe most from early invasive treatment. J Am Coll Cardiol 2003;41:905–915.53. Kaul P, Fu Y, Chang WC, Harrington RA, Wagner GS, Goodman SG, Granger CB, Moliterno DJ, Van de Werf F,Califf RM, Topol EJ, Armstrong PW. Prognostic value of ST segment depression in acute coronary syndromes:insights from PARAGON-A applied to GUSTO-IIb. PARAGON-A and GUSTO IIb Investigators. Platelet IIb/IIIa Antagonismfor the Reduction of Acute Global Organization Network. J Am Coll Cardiol 2001;38:64–71.54. Nyman I, Wallentin L, Areskog M, Areskog NH, Swahn E. Risk stratification by early exercise testing after anepisode of unstable coronary artery disease. The RISC Study Group. Int J Cardiol 1993;39:131–142.55. Amsterdam EA, Kirk JD, Diercks DB, Lewis WR, Turnipseed SD. Immediate exercise testing to evaluate low-riskpatients presenting to the emergency department with chest pain. J Am Coll Cardiol 2002;40:251–256.56. Scirica BM, Morrow DA, Budaj A, Dalby AJ, Mohanavelu S, Qin J, Aroesty J, Hedgepeth CM, Stone PH, BraunwaldE. Ischemia detected on continuous electrocardiography after acute coronary syndrome: observationsfrom the MERLIN-TIMI 36 (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST-Elevation AcuteCoronary Syndrome-Thrombolysis In Myocardial Infarction 36) trial. J Am Coll Cardiol 2009;53:1411–1421.57. Akkerhuis KM, Klootwijk PA, Lindeboom W, Umans VA, Meij S, Kint PP, Simoons ML. Recurrent ischaemia duringcontinuous multilead ST-segment monitoring identifies patients with acute coronary syndromes at highrisk of adverse cardiac events; meta-analysis of three studies involving 995 patients. Eur Heart J2001;22:1997–2006.58. Antman EM, Tanasijevic MJ, Thompson B, Schactman M, McCabe CH, Cannon CP, Fischer GA, Fung AY, ThompsonC, Wybenga D, Braunwald E. Cardiac-specific troponin I levels to predict the risk of mortality in patients withacute coronary syndromes. N Engl J Med 1996;335:1342–1349.59. Kontos MC, de Lemos JA, Ou FS, Wiviott SD, Foody JM, Newby LK, Chen A, Roe MT. Troponin-positive, MBnegativepatients with non-ST-elevation myocardial infarction: an undertreated but high-risk patient group:results from the National Cardiovascular Data Registry Acute Coronary Treatment and Intervention OutcomesNetwork—Get With The Guidelines (NCDR ACTION-GWTG) Registry. Am Heart J 2010;160:819–825.60. James SK, Lindahl B, Siegbahn A, Stridsberg M, Venge P, Armstrong P, Barnathan ES, Califf R, Topol EJ, SimoonsML, Wallentin L. N-terminal pro-brain natriuretic peptide and other risk markers for the separate prediction ofmortality and subsequent myocardial infarction in patients with unstable coronary artery disease: a Global Utilizationof Strategies To Open occluded arteries (GUSTO)-IV substudy. Circulation 2003;108:275–281.61. Steg PG, FitzGerald G, Fox KA. Risk stratification in non-ST-segment elevation acute coronary syndromes: troponinalone is not enough. Am J Med 2009;122: 107–108.62. Thygesen K, Mair J, Mueller C, Huber K, Weber M, Plebani M, Hasin Y, Biasucci LM, Giannitsis E, Lindahl B,Koenig W, Tubaro M, Collinson P, Katus H, Galvani M, Venge P, Alpert JS, Hamm C, Jaffe AS. Recommendationsfor the use of natriuretic peptides in acute cardiac care: a position statement from the Study Group on Biomarkersin Cardiology of the ESC Working Group on Acute Cardiac Care. Eur Heart J 2011;10.1093/eurheartj/ehq509.63. Heeschen C, Hamm CW, Bruemmer J, Simoons ML. Predictive value of Creactive protein and troponin T in patientswith unstable angina: a comparative analysis. CAPTURE Investigators. Chimeric c7E3 AntiPlatelet Therapyin Unstable angina REfractory to standard treatment trial. J Am Coll Cardiol 2000;35:1535–1542.64. Morrow DA, Rifai N, Antman EM, Weiner DL, McCabe CH, Cannon CP, Braunwald E. C-reactive protein is a potentpredictor of mortality independently of and in combination with troponin T in acute coronary syndromes:a TIMI 11A substudy. Thrombolysis in Myocardial Infarction. J Am Coll Cardiol 1998;31:1460–1465.65. Lindahl B, Toss H, Siegbahn A, Venge P, Wallentin L. Markers of myocardial damage and inflammation in relationto long-term mortality in unstable coronary artery disease. FRISC Study Group. Fragmin during Instabilityin Coronary Artery Disease. N Engl J Med 2000;343:1139–1147.66. Currie CJ, Poole CD, Conway P. Evaluation of the association between the first observation and the longitudinalchange in C-reactive protein, and all-cause mortality. Heart 2008;94:457–462.67. Aronson D, Hammerman H, Suleiman M, Markiewicz W. Usefulness of changes in fasting glucose during hospitalizationto predict long-term mortality in patients with acute myocardial infarction. Am J Cardiol2009;104:1013–1017.68. Suleiman M, Hammerman H, Boulos M, Kapeliovich MR, Suleiman A, Agmon Y, Markiewicz W, Aronson D. Fastingglucose is an important independent risk factor for 30-day mortality in patients with acute myocardial infarction:a prospective study. Circulation 2005;111:754–760.69. Sabatine MS, Morrow DA, Giugliano RP, Burton PB, Murphy SA, McCabe CH, Gibson CM, Braunwald E. Associationof hemoglobin levels with clinical outcomes in acute coronary syndromes. Circulation2005;111:2042–2049.70. Mahaffey KW, Yang Q, Pieper KS, Antman EM, White HD, Goodman SG, Cohen M, Kleiman NS, Langer A,Aylward PE, Col JJ, Reist C, Ferguson JJ, Califf RM. Prediction of one-year survival in high-risk patients withacute coronary syndromes: results from the SYNERGY trial. J Gen Intern Med 2008;23:310–316.71. Al Suwaidi J, Reddan DN, Williams K, Pieper KS, Harrington RA, Califf RM, Granger CB, Ohman EM, Holmes DRJr. Prognostic implications of abnormalities in renal function in patients with acute coronary syndromes. Circulation2002;106:974–980.72. Baldus S, Heeschen C, Meinertz T, Zeiher AM, Eiserich JP, Munzel T, Simoons ML, Hamm CW. Myeloperoxidaseserum levels predict risk in patients with acute coronary syndromes. Circulation 2003;108:1440–1445.73. Brennan ML, Penn MS, Van Lente F, Nambi V, Shishehbor MH, Aviles RJ, Goormastic M, Pepoy ML, McErleanES, Topol EJ, Nissen SE, Hazen SL. Prognostic value of myeloperoxidase in patients with chest pain. N Engl JMed 2003;349:1595–1604.74. Wollert KC, Kempf T, Peter T, Olofsson S, James S, Johnston N, Lindahl B, Horn-Wichmann R, Brabant G, SimoonsML, Armstrong PW, Califf RM, Drexler H, Wallentin L. Prognostic value of growth-differentiation factor-15 inpatients with non-ST-elevation acute coronary syndrome. Circulation 2007;115:962–971.75. Morrow DA, Sabatine MS, Brennan ML, de Lemos JA, Murphy SA, Ruff CT, Rifai N, Cannon CP, Hazen SL. Concurrentevaluation of novel cardiac biomarkers in acute coronary syndrome: myeloperoxidase and soluble CD40ligand and the risk of recurrent ischaemic events in TACTICS-TIMI 18. Eur Heart J 2008;29:1096–1102.76. Viswanathan K, Kilcullen N, Morrell C, Thistlethwaite SJ, Sivananthan MU, Hassan TB, Barth JH, Hall AS. Hearttypefatty acid-binding protein predicts long-term mortality and re-infarction in consecutive patients with suspectedacute coronary syndrome who are troponin-negative. J Am Coll Cardiol 2010;55:2590–2598.77. Van Belle E, Dallongeville J, Vicaut E, Degrandsart A, Baulac C, Montalescot G. Ischemia-modified albumin levelspredict long-term outcome in patients with acute myocardial infarction. The French Nationwide OPERAstudy. Am Heart J 2010;159:570–576.78. Reichlin T, Hochholzer W, Stelzig C, Laule K, Freidank H, Morgenthaler NG, Bergmann A, Potocki M, NoveanuM, Breidthardt T, Christ A, Boldanova T, Merki R, Schaub N, Bingisser R, Christ M, Mueller C. Incremental valueof copeptin for rapid rule out of acute myocardial infarction. J Am Coll Cardiol 2009;54:60–68.79. de Araujo Goncalves P, Ferreira J, Aguiar C, Seabra-Gomes R. TIMI, PURSUIT, and GRACE risk scores: sustainedprognostic value and interaction with revascularization in NSTE-ACS. Eur Heart J 2005;26:865–872.80. Aragam KG, Tamhane UU, Kline-Rogers E, Li J, Fox KA, Goodman SG, Eagle KA, Gurm HS. Does simplicitycompromise accuracy in ACS risk prediction? A retrospective analysis of the TIMI and GRACE risk scores. PLoSOne 2009;4:e7947.81. Eggers KM, Kempf T, Venge P, Wallentin L, Wollert KC, Lindahl B. Improving long-term risk prediction in patientswith acute chest pain: the Global Registry of Acute Coronary Events (GRACE) risk score is enhanced by selectednonnecrosis biomarkers. Am Heart J 2010;160:88–94.82. Khot UN, Jia G, Moliterno DJ, Lincoff AM, Khot MB, Harrington RA, Topol EJ. Prognostic importance of physicalexamination for heart failure in non-ST-elevation acute coronary syndromes: the enduring value of Killip classification.JAMA 2003;290:2174–2181.83. Subherwal S, Bach RG, Chen AY, Gage BF, Rao SV, Newby LK, Wang TY, Gibler WB, Ohman EM, Roe MT, PollackCV Jr., Peterson ED, Alexander KP. Baseline risk of major bleeding in non-ST-segment-elevation myocardialinfarction: the CRUSADE (Can Rapid risk stratification of Unstable angina patients Suppress ADverseoutcomes with Early implementation of the ACC/AHA Guidelines) Bleeding Score. Circulation2009;119:1873–1882.84. Mehran R, Pocock SJ, Nikolsky E, Clayton T, Dangas GD, Kirtane AJ, Parise H, Fahy M, Manoukian SV, Feit F,Ohman ME, Witzenbichler B, Guagliumi G, Lansky AJ, Stone GW. A risk score to predict bleeding in patients withacute coronary syndromes. J Am Coll Cardiol 2010;55:2556–2566.85. Yusuf S, Peto R, Lewis J, Collins R, Sleight P. Beta blockade during and after myocardial infarction: an overviewof the randomized trials. Prog Cardiovasc Dis 1985;27:335–371.86. Randomised trial of intravenous atenolol among 16 027 cases of suspected acute myocardial infarction: ISIS-1. First International Study of Infarct Survival Collaborative Group. Lancet 1986;2:57–66.87. Telford AM, Wilson C. Trial of heparin versus atenolol in prevention of myocardial infarction in intermediatecoronary syndrome. Lancet 1981;1:1225–1228.88. Lubsen J, Tijssen JG. Efficacy of nifedipine and metoprolol in the early treatment of unstable angina in the coronarycare unit: findings from the Holland Interuniversity Nifedipine/metoprolol Trial (HINT). Am J Cardiol1987;60:18A–25A.89. Yusuf S, Wittes J, Friedman L. Overview of results of randomized clinical trials in heart disease. I. Treatments followingmyocardial infarction. JAMA 1988;260:2088–2093.90. Metoprolol in acute myocardial infarction (MIAMI). A randomised placebocontrolled international trial. TheMIAMI Trial Research Group. Eur Heart J 1985;6:199–226.91. Miller CD, Roe MT, Mulgund J, Hoekstra JW, Santos R, Pollack CV Jr., Ohman EM, Gibler WB, Peterson ED. Impactof acute beta-blocker therapy for patients with non-ST-segment elevation myocardial infarction. Am JMed 2007;120:685–692.92. Brandler E, Paladino L, Sinert R. Does the early administration of beta-blockers improve the in-hospital mortalityrate of patients admitted with acute coronary syndrome? Acad Emerg Med 2010;17:1–10.93. Chen ZM, Pan HC, Chen YP, Peto R, Collins R, Jiang LX, Xie JX, Liu LS. Early intravenous then oral metoprolol in45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet2005;366:1622–1632.94. Borzak S, Cannon CP, Kraft PL, Douthat L, Becker RC, Palmeri ST, Henry T, Hochman JS, Fuchs J, Antman EM,McCabe C, Braunwald E. Effects of prior aspirin and anti-ischemic therapy on outcome of patients with unstableangina. TIMI 7 Investigators. Thrombin Inhibition in Myocardial Ischemia. Am J Cardiol 1998;81:678–681.95. Ambrosio G, Del Pinto M, Tritto I, Agnelli G, Bentivoglio M, Zuchi C, Anderson FA, Gore JM, Lopez-Sendon J,Wyman A, Kennelly BM, Fox KA. Chronic nitrate therapy is associated with different presentation and evolutionof acute coronary syndromes: insights from 52,693 patients in the Global Registry of Acute Coronary Events.Eur Heart J 2010;31:430–438.96. Cotter G, Faibel H, Barash P, Shemesh E, Moshkovitz Y, Metzkor E, Simovitz A, Miller R, Schlezinger Z, Golik A.High-dose nitrates in the immediate management of unstable angina: optimal dosage, route of administration,and therapeutic goals. Am J Emerg Med 1998;16:219–224.97. Theroux P, Taeymans Y, Morissette D, Bosch X, Pelletier GB, Waters DD. A randomized study comparing propranololand diltiazem in the treatment of unstable angina. J Am Coll Cardiol 1985;5:717–722.98. Parodi O, Simonetti I, Michelassi C, Carpeggiani C, Biagini A, L’Abbate A, Maseri A. Comparison of verapamiland propranolol therapy for angina pectoris at rest: a randomized, multiple-crossover, controlled trial in thecoronary care unit. Am J Cardiol 1986;57:899–906.99. Hansen JF. Treatment with verapamil after an acute myocardial infarction. Review of the Danish studies on verapamilin myocardial infarction (DAVIT I and II). Drugs 1991;42 Suppl 2:43–53.100. Moss AJ, Oakes D, Rubison M, McDermott M, Carleen E, Eberly S, Brown M. Effects of diltiazem on long-termoutcome after acute myocardial infarction in patients with and without a history of systemic hypertension.The Multicenter Diltiazem Postinfarction Trial Research Group. Am J Cardiol 1991;68:429–433.101. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina(IONA) randomised trial. Lancet 2002;359:1269–1275.102. Borer JS. Therapeutic effects of I(f) blockade: evidence and perspective. Pharmacol Res 2006;53:440–445.103. Morrow DA, Scirica BM, Karwatowska-Prokopczuk E, Murphy SA, Budaj A, Varshavsky S, Wolff AA, Skene A,McCabe CH, Braunwald E. Effects of ranolazine on recurrent cardiovascular events in patients with non-ST-elevationacute coronary syndromes: the MERLIN-TIMI 36 randomized trial. JAMA 2007;297:1775–1783.104. Theroux P, Ouimet H, McCans J, Latour JG, Joly P, Levy G, Pelletier E, Juneau M, Stasiak J, de Guise P, PelletierG, Rinzler D, Waters D. Aspirin, heparin, or both to treat acute unstable angina. N Engl J Med1988;319:1105–1111.105. Theroux P, Waters D, Qiu S, McCans J, de Guise P, Juneau M. Aspirin versus heparin to prevent myocardial infarctionduring the acute phase of unstable angina. Circulation 1993;88:2045–2048.106. Cairns JA, Gent M, Singer J, Finnie KJ, Froggatt GM, Holder DA, Jablonsky G, Kostok WJ, Melendez LJ, MyersMG, Sackett DL, Staley BJ, Tanser PH. Aspirin, sulfinpyrazone, or both in unstable angina. Results of a Canadianmulticenter trial. N Engl J Med 1985;313:1369–1375.107. Baigent C, Blackwell L, Collins R, Emberson J, Godwin J, Peto R, Buring J, Hennekens C, Kearney P, Meade T,Patrono C, Roncaglioni MC, Zanchetti A. Aspirin in the primary and secondary prevention of vascular disease:collaborative meta-analysis 108. Mehta SR, Tanguay JF, Eikelboom JW, Jolly SS, Joyner CD, Granger CB, Faxon DP, Rupprecht HJ, Budaj A,Avezum A, Widimsky P, Steg PG, Bassand JP, Montalescot G, Macaya C, Di Pasquale G, Niemela K, Ajani AE,White HD, Chrolavicius S, Gao P, Fox KA, Yusuf S. Double-dose versus standard-dose clopidogrel and highdoseversus low-dose aspirin in individuals undergoing percutaneous coronary intervention for acute coronarysyndromes (CURRENT-OASIS 7): a randomised factorial trial. Lancet 2010;376:1233–1243.109. Gislason GH, Jacobsen S, Rasmussen JN, Rasmussen S, Buch P, Friberg J, Schramm TK, Abildstrom SZ, KoberL, Madsen M, Torp-Pedersen C. Risk of death or reinfarction associated with the use of selective cyclooxygenase-2 inhibitors and nonselective nonsteroidal antiinflammatory drugs after acute myocardial infarction. Circulation2006;113:2906–2913.110. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Effects of clopidogrel in addition to aspirin inpatients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345:494–502.111. Yusuf S, Mehta SR, Zhao F, Gersh BJ, Commerford PJ, Blumenthal M, Budaj A, Wittlinger T, Fox KA. Early andlate effects of clopidogrel in patients with acute coronary syndromes. Circulation 2003;107:966–972.112. Ho PM, Peterson ED, Wang L, Magid DJ, Fihn SD, Larsen GC, Jesse RA, Rumsfeld JS. Incidence of death andacute myocardial infarction associated with stopping clopidogrel after acute coronary syndrome. JAMA2008;299:532–539.113. Fox KA, Mehta SR, Peters R, Zhao F, Lakkis N, Gersh BJ, Yusuf S. Benefits and risks of the combination of clopidogreland aspirin in patients undergoing surgical revascularization for non-ST-elevation acute coronary syndrome:the Clopidogrel in Unstable angina to prevent Recurrent ischemic Events (CURE) Trial. Circulation2004;110:1202–1208.114. Montalescot G, Sideris G, Meuleman C, Bal-dit-Sollier C, Lellouche N, Steg PG, Slama M, Milleron O, ColletJ-P, Henry P, Beygui F, Drouet L. A randomized comparison of high clopidogrel loading doses in patients withnon-ST-segment elevation acute coronary syndromes: the ALBION (Assessment of the Best Loading Dose ofClopidogrel to Blunt Platelet Activation, Inflammation and Ongoing Necrosis) Trial. J Am Coll Cardiol2006;48:931–938.115. Snoep JD, Hovens MM, Eikenboom JC, van der Bom JG, Jukema JW, Huisman MV. Clopidogrel nonresponsivenessin patients undergoing percutaneous coronary intervention with stenting: a systematic review andmeta-analysis. Am Heart J 2007;154:221–231.116. Aleil B, Jacquemin L, De Poli F, Zaehringer M, Collet J-P, Montalescot G, Cazenave J-P, Dickele M-C, MonassierJ-P, Gachet C. Clopidogrel 150 mg/day to overcome low responsiveness in patients undergoing elective percutaneouscoronary intervention: results from the VASP-02 (Vasodilator-Stimulated Phosphoprotein-02)Randomized Study. JACC Cardiovasc Interv 2008;1:631–638.117. The CURRENT-OASIS 7 Investigators. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes.N Engl J Med 2010;363:930–942.118. Taubert D, von Beckerath N, Grimberg G, Lazar A, Jung N, Goeser T, Kastrati A, Schomig A, Schomig E. Impactof P-glycoprotein on clopidogrel absorption. Clin Pharmacol Ther 2006;80:486–501.119. Mega JL, Close SL, Wiviott SD, Shen L, Walker JR, Simon T, Antman EM, Braunwald E, Sabatine MS. Geneticvariants in ABCB1 and CYP2C19 and cardiovascular outcomes after treatment with clopidogrel and prasugrelin the TRITON-TIMI 38 trial: a pharmacogenetic analysis. Lancet 2010;376:1312–1319.120. Mega JL, Simon T, Collet JP, Anderson JL, Antman EM, Bliden K, Cannon CP, Danchin N, Giusti B, Gurbel P,Horne BD, Hulot JS, Kastrati A, Montalescot G, Neumann FJ, Shen L, Sibbing D, Steg PG, Trenk D, Wiviott SD,Sabatine MS. Reduced-function CYP2C19 genotype and risk of adverse clinical outcomes among patientstreated with clopidogrel predominantly for PCI: a meta-analysis. JAMA 2010;304:1821–1830.121. Breet N, van Werkum J, Bouman H, Kelder J, Ruven H, Bal E, Deneer V, Harmsze A, van der Heyden J, RensingB, Suttorp M, Hackeng C, ten Berg J. Comparison of platelet function tests in predicting clinical outcomein patients undergoing coronary stent implantation. JAMA 2010;303:754–762.122. Geisler T, Langer H, Wydymus M, Gohring K, Zurn C, Bigalke B, Stellos K, May AE, Gawaz M. Low responseto clopidogrel is associated with cardiovascular outcome after coronary stent implantation. Eur Heart J2006;27:2420–2425.123. Trenk D, Hochholzer W, Fromm MF, Chialda LE, Pahl A, Valina CM, Stratz C, Schmiebusch P, Bestehorn HP,Buttner HJ, Neumann FJ. Cytochrome P450 2C19 681G.A polymorphism and high on-clopidogrel platelet reactivityassociated with adverse 1-year clinical outcome of elective percutaneous coronary intervention withdrug-eluting or bare-metal stents. J Am Coll Cardiol 2008;51:1925–1934.124. Price MJ, Berger PB, Teirstein PS, Tanguay JF, Angiolillo DJ, Spriggs D, Puri S, Robbins M, Garratt KN, BertrandOF, Stillablower ME, Aragon JR, Kandzari DE, Stinis CT, Lee MS, Manoukian SV, Cannon CP, Schork NJ, TopolEJ. Standard- vs high-dose clopidogrel based on platelet function testing after percutaneous coronary intervention:the GRAVITAS randomized trial. JAMA 2011;305:1097–1105.125. O’Donoghue ML, Braunwald E, Antman EM, Murphy SA, Bates ER, Rozenman Y, Michelson AD, HautvastRW, Ver Lee PN, Close SL, Shen L, Mega JL, Sabatine MS, Wiviott SD. Pharmacodynamic effect and clinical efficacyof clopidogrel and prasugrel with or without a proton-pump inhibitor: an analysis of two randomisedtrials. Lancet 2009;374:989–997.126. Abraham NS, Hlatky MA, Antman EM, Bhatt DL, Bjorkman DJ, Clark CB, Furberg CD, Johnson DA, Kahi CJ,Laine L, Mahaffey KW, Quigley EM, Scheiman J, Sperling LS, Tomaselli GF. ACCF/ACG/AHA 2010 Expert ConsensusDocument on the concomitant use of proton pump inhibitors and thienopyridines: a focused updateof the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelettherapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Expert ConsensusDocuments. Circulation 2010;122:2619–2633.127. Bhatt DL, Cryer BL, Contant CF, Cohen M, Lanas A, Schnitzer TJ, Shook TL, Lapuerta P, Goldsmith MA, LaineL, Scirica BM, Murphy SA, Cannon CP. Clopidogrel with or without omeprazole in coronary artery disease. NEngl J Med 2010;363:1909–1917.128. Wiviott SD, Trenk D, Frelinger AL, O’Donoghue M, Neumann F-J, Michelson AD, Angiolillo DJ, Hod H, MontalescotG, Miller DL, Jakubowski JA, Cairns R, Murphy SA, McCabe CH, Antman EM, Braunwald E, PRINCIPLE-TIMI 44 Investigators. Prasugrel compared with high loading- and maintenance-dose clopidogrel inpatients with planned percutaneous coronary intervention: the Prasugrel in Comparison to Clopidogrel for Inhibitionof Platelet Activation and Aggregation Thrombolysis in Myocardial Infarction 44 Trial. Circulation2007;116:2923–2932.129. Small DS, Farid NA, Payne CD, Weerakkody GJ, Li YG, Brandt JT, Salazar DE, Winters KJ. Effects of the protonpump inhibitor lansoprazole on the pharmacokinetics and pharmacodynamics of prasugrel and clopidogrel.J Clin Pharmacol 2008;48:475–484.130. Wiviott S, Braunwald E, McCabe C, Montalescot G, Ruzyllo W, Gottlieb S, Neumann F-J, Ardissino D, De ServiS, Murphy S, Riesmeyer J, Weerakkody G, Gibson C, Antman E. Prasugrel versus clopidogrel in patients withacute coronary syndromes. N Engl J Med 2007;357:2001–2015.131. Gurbel PA, Bliden KP, Butler K, Tantry US, Gesheff T, Wei C, Teng R, Antonino MJ, Patil SB, Karunakaran A,Kereiakes DJ, Paris C, Purdy D, Wilson V, Ledley GS, Storey RF. Randomized double-blind assessment of theONSET and OFFSet of the antiplatelet effects of ticagrelor versus clopidogrel in patients with stable coronaryartery disease: the ONSET/OFFSET Study. Circulation 2009;120:2577–2585.132. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C, Horrow J, Husted S, James S, Katus H,Mahaffey KW, Scirica BM, Skene A, Steg PG, Storey RF, Harrington RA, for the PLATO Investigators. Ticagrelorversus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361:1045–1057.133. Cannon C, Harrington R, James S, Ardissino D, Becker R, Emanuelsson H, Husted S, Katus H, Keltaih M, KhurmiN, Kontny F, Lewis B, Steg P, Storey R, Wojdyla D, Wallentin L, the PLATelet inhibition and patient Outcomes(PLATO) investigators. Ticagrelor compared with clopidogrel in acute coronary syndromes patients with aplanned invasive strategy (PLATO): a randomised double-blind study. Lancet 2010;375:283–293.134. Held C, Asenblad N, Bassand JP, Becker RC, Cannon CP, Claeys MJ, Harrington RA, Horrow J, Husted S, JamesSK, Mahaffey KW, Nicolau JC, Scirica BM, Storey RF, Vintila M, Ycas J, Wallentin L. Ticagrelor versus clopidogrelin patients with acute coronary syndromes undergoing coronary artery bypass surgery results from thePLATO (Platelet Inhibition and Patient Outcomes) Trial. J Am Coll Cardiol 2011;57:672–684.135. Husted S, Emanuelsson H, Heptinstall S, Sandset PM, Wickens M, Peters G. Pharmacodynamics, pharmacokinetics,and safety of the oral reversible P2Y12 antagonist AZD6140 with aspirin in patients with atherosclerosis:a double-blind comparison to clopidogrel with aspirin. Eur Heart J 2006;27:1038–1047.136. Cannon CP, Husted S, Harrington RA, Scirica BM, Emanuelsson H, Peters G, Storey RF. Safety, tolerability, andinitial efficacy of AZD6140, the First reversible oral adenosine diphosphate receptor antagonist, comparedwith clopidogrel, in patients with non-ST-segment elevation acute coronary syndrome: primary results of theDISPERSE-2 Trial. J Am Coll Cardiol 2007;50:1844–1851.137. Storey RF, Bliden K, Patil SB, Karunakaran A, Ecob R, Butler K, Teng R, Wei C, Tantry US, Gurbel P. Incidence ofdyspnea and assessment of cardiac and pulmonary function in patients with stable coronary artery disease receivingticagrelor, clopidogrel or placebo in the ONSET/OFFSET Study. J Am Coll Cardiol 2010;56:185–193.138. Berger JS, Frye CB, Harshaw Q, Edwards FH, Steinhubl SR, Becker RC. Impact of clopidogrel in patients withacute coronary syndromes requiring coronary artery bypass surgery: a multicenter analysis. J Am Coll Cardiol2008;52:1693–1701.139. Kapetanakis EI, Medlam DA, Boyce SW, Haile E, Hill PC, Dullum MK, Bafi AS, Petro KR, Corso PJ. Clopidogreladministration prior to coronary artery bypass grafting surgery: the cardiologist’s panacea or the surgeon’sheadache? Eur Heart J 2005;26:576–583.140. Mehta RH, Roe MT, Mulgund J, Ohman EM, Cannon CP, Gibler WB, Pollack CV Jr., Smith SC Jr., Ferguson TB,Peterson ED. Acute clopidogrel use and outcomes in patients with non-ST-segment elevation acute coronarysyndromes undergoing coronary artery bypass surgery. J Am Coll Cardiol 2006;48:281–286.141. Ebrahimi R, Dyke C, Mehran R, Manoukian SV, Feit F, Cox DA, Gersh BJ, Ohman EM, White HD, Moses JW,WareJH, Lincoff AM, Stone GW. Outcomes following pre-operative clopidogrel administration in patients with acutecoronary syndromes undergoing coronary artery bypass surgery: the ACUITY (Acute Catheterization and UrgentIntervention Triage strategY) Trial. J Am Coll Cardiol 2009;53:1965–1972.142. Kim JH, Newby LK, Clare RM, Shaw LK, Lodge AJ, Smith PK, Jolicoeur EM, Rao SV, Becker RC, Mark DB,Granger CB. Clopidogrel use and bleeding after coronary artery bypass graft surgery. Am Heart J2008;156:886–892.143. Fitchett D, Eikelboom J, Fremes S, Mazer D, Singh S, Bittira B, Brister S, Graham JJ, Gupta M, Karkouti K, LeeA, Love M, McArthur R, Peterson M, Verma S, Yau TM. Dual antiplatelet therapy in patients requiring urgentcoronary artery bypass grafting surgery: a position statement of the Canadian Cardiovascular Society. Can J Cardiol2009;25:683–689.144. Collet JP, Montalescot G, Blanchet B, Tanguy ML, Golmard JL, Choussat R, Beygui F, Payot L, Vignolles N, MetzgerJP, Thomas D. Impact of prior use or recent withdrawal of oral antiplatelet agents on acute coronary syndromes.Circulation 2004;110:2361–2367.145. Grines CL, Bonow RO, Casey DE Jr., Gardner TJ, Lockhart PB, Moliterno DJ, O’Gara P, Whitlow P. Prevention ofpremature discontinuation of dual antiplatelet therapy in patients with coronary artery stents: a science advisoryfrom the American Heart Association, American College of Cardiology, Society for Cardiovascular Angiographyand Interventions, American College of Surgeons, and American Dental Association, withrepresentation from the American College of Physicians. Circulation 2007;115:813–818.146. Mehta SR, Yusuf S, Peters RJ, Bertrand ME, Lewis BS, Natarajan MK, Malmberg K, Rupprecht H, Zhao F,Chrolavicius S, Copland I, Fox KA. Effects of pretreatment with clopidogrel and aspirin followed by long-termtherapy in patients undergoing percutaneous coronary intervention: the PCI-CURE study. Lancet2001;358:527–533.147. Steinhubl SR, Berger PB, Mann JT 3rd, Fry ET, DeLago A, Wilmer C, Topol EJ. Early and sustained dual oral antiplatelettherapy following percutaneous coronary intervention: a randomized controlled trial. JAMA2002;288:2411–2420.148. Wijns W, Kolh P, Danchin N, Di Mario C, Falk V, Folliguet T, Garg S, Huber K, James S, Knuuti J, Lopez-SendonJ, Marco J, Menicanti L, Ostojic M, Piepoli MF, Pirlet C, Pomar JL, Reifart N, Ribichini FL, Schalij MJ, SergeantP, Serruys PW, Silber S, Sousa Uva M, Taggart D. Guidelines on myocardial revascularization: the Task Force onMyocardial Revascularization of the European Society of Cardiology (ESC) and the European Association forCardio-Thoracic Surgery (EACTS). Eur Heart J 2010;31:2501–2555.149. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Moliterno DJ, Heeschen C, Hamm CW, Robbins MA,Kleiman NS, Theroux P, White HD, Topol EJ. Platelet glycoprotein IIb/IIIa inhibition in acute coronary syndromes.Gradient of benefit related to the revascularisation strategy. Eur Heart J 2002; 23:1441–1448.150. Stone GW, Bertrand ME, Moses JW, Ohman EM, Lincoff AM, Ware JH, Pocock SJ, McLaurin BT, Cox DA, JafarMZ, Chandna H, Hartmann F, Leisch F, Strasser RH, Desaga M, Stuckey TD, Zelman RB, Lieber IH, Cohen DJ,Mehran R, White HD. Routine upstream initiation vs deferred selective use of glycoprotein IIb/IIIa inhibitorsin acute coronary syndromes: the ACUITY Timing trial. JAMA 2007;297:591–602.151. Giugliano RP, White JA, Bode C, Armstrong PW, Montalescot G, Lewis BS, van’t Hof A, Berdan LG, Lee KL,Strony JT, Hildemann S, Veltri E, Van de Werf F, Braunwald E, Harrington RA, Califf RM, Newby LK, the EARLYACS Investigators. Early versus delayed, provisional eptifibatide in acute coronary syndromes. N Engl J Med2009;360:2176–2190.152. Kastrati A, Mehilli J, Neumann F-J, Dotzer F, ten Berg J, Bollwein H, Graf I, Ibrahim M, Pache J, Seyfarth M,Schuhlen H, Dirschinger J, Berger PB, Schomig A, for the Intracoronary Stenting, Antithrombotic Regimen:Rapid Early Action for Coronary Treatment 2 Trial I. Abciximab in patients with acute coronary syndromes undergoingpercutaneous coronary intervention after clopidogrel pretreatment: the ISAR-REACT 2 RandomizedTrial. JAMA 2006;295:1531–1538. 153. Dasgupta H, Blankenship JC, Wood GC, Frey CM, Demko SL, Menapace FJ. Thrombocytopenia complicatingtreatment with intravenous glycoprotein IIb/IIIa receptor inhibitors: a pooled analysis. Am Heart J2000;140:206–211.154. Jubelirer SJ, Koenig BA, Bates MC. Acute profound thrombocytopenia following C7E3 Fab (Abciximab) therapy:case reports, review of the literature and implications for therapy. Am J Hematol 1999;61:205–208.155. Lajus S, Clofent-Sanchez G, Jais C, Coste P, Nurden P, Nurden AT. Thrombocytopenia after abciximab use resultsfrom different mechanisms. Thromb Haemost 2010;103 651–661.156. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute coronary syndromes. ThePURSUIT Trial Investigators. Platelet glycoprotein IIb/IIIa in unstable angina: receptor suppression using integrilintherapy. N Engl J Med 1998;339:436–443.157. Merlini PA, Rossi M, Menozzi A, Buratti S, Brennan DM, Moliterno DJ, Topol EJ, Ardissino D. Thrombocytopeniacaused by abciximab or tirofiban and its association with clinical outcome in patients undergoing coronarystenting. Circulation 2004;109:2203–2206.158. Topol EJ, Moliterno DJ, Herrmann HC, Powers ER, Grines CL, Cohen DJ, Cohen EA, Bertrand M, Neumann FJ,Stone GW, DiBattiste PM, Yakubov SJ, DeLucca PT, Demopoulos L, the TARGET Investigators. Comparisonof two platelet glycoprotein IIb/IIIa inhibitors, tirofiban and abciximab, for the prevention of ischemic eventswith percutaneous coronary revascularization. N Engl J Med 2001;344:1888–1894.159. Moliterno DJ, Yakubov SJ, DiBattiste PM, Herrmann HC, Stone GW, Macaya C, Neumann F-J, Ardissino D,Bassand J-P, Borzi L. Outcomes at 6 months for the direct comparison of tirofiban and abciximab during percutaneouscoronary revascularisation with stent placement: the TARGET follow-up study. Lancet2002;360:355–360.160. De Luca G, Ucci G, Cassetti E, Marino P. Benefits from small molecule administration as compared with abciximabamong patients with ST-segment elevation myocardial infarction treated with primary angioplasty: ameta-analysis. J Am Coll Cardiol 2009;53:1668–1673.161. Valgimigli M, Biondi-Zoccai G, Tebaldi M, van’t Hof AWJ, Campo G, Hamm C, ten Berg J, Bolognese L, Saia F,Danzi GB, Briguori C, Okmen E, King SB, Moliterno DJ, Topol EJ. Tirofiban as adjunctive therapy for acutecoronary syndromes and percutaneous coronary intervention: a meta-analysis of randomized trials. Eur HeartJ 2010;31:35–49.162. O’Donoghue M, Antman EM, Braunwald E, Murphy SA, Steg PG, Finkelstein A, Penny WF, Fridrich V, McCabeCH, Sabatine MS, Wiviott SD. The efficacy and safety of prasugrel with and without a glycoprotein IIb/IIIa inhibitorin patients with acute coronary syndromes undergoing percutaneous intervention: a TRITON-TIMI 38(Trial to Assess Improvement in Therapeutic Outcomes by Optimizing Platelet Inhibition With Prasugrel-ThrombolysisIn Myocardial Infarction 38) analysis. J Am Coll Cardiol 2009;54:678–685.163. Buller C, Pate G, Armstrong P, O’Neill B, Webb J, Gallo R, Welsh R. Catheter thrombosis during primary percutaneouscoronary intervention for acute ST elevation myocardial infarction despite subcutaneous low-molecular-weight heparin, acetylsalicylic acid, clopidogrel and abciximab pretreatment. Can J Cardiol2006;22:511–515.164. Jolly SS, Faxon DP, Fox KA, Afzal R, Boden WE, Widimsky P, Steg PG, Valentin V, Budaj A, Granger CB, JoynerCD, Chrolavicius S, Yusuf S, Mehta SR. Efficacy and safety of fondaparinux versus enoxaparin in patients withacute coronary syndromes treated with glycoprotein IIb/IIIa inhibitors or thienopyridines: results from theOASIS 5 (Fifth Organization to Assess Strategies in Ischemic Syndromes) trial. J Am Coll Cardiol2009;54:468–476.165. White HD, Ohman EM, Lincoff AM, Bertrand ME, Colombo A, McLaurin BT, Cox DA, Pocock SJ, Ware JA,Manoukian SV, Lansky AJ, Mehran R, Moses JW, Stone GW. Safety and efficacy of bivalirudin with and withoutglycoprotein IIb/IIIa inhibitors in patients with acute coronary syndromes undergoing percutaneous coronaryintervention: 1-year results from the ACUITY (Acute Catheterization and Urgent Intervention TriagestrategY) trial. J Am Coll Cardiol 2008;52:807–814.166. Lincoff AM, Steinhubl SR, Manoukian SV, Chew D, Pollack CV Jr, Feit F,Ware JH, Bertrand ME, Ohman EM,DesmetW, Cox DA, Mehran R, Stone GW. Influence of timing of clopidogrel treatment on the efficacy andsafety of bivalirudin in patients with non-ST-segment elevation acute coronary syndromes undergoing percutaneouscoronary intervention: an analysis of the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. JACC Cardiovasc Interv 2008;1:639–648.167. Brieger D, Van de Werf F, Avezum A, Montalescot G, Kennelly B, Granger CB, Goodman SG, Dabbous O, AgnelliG. Interactions between heparins, glycoprotein IIb/IIIa antagonists, and coronary intervention. The GlobalRegistry of Acute Coronary Events (GRACE). Am Heart J 2007;153:960–969.168. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED, for the CRUSADE Investigators. Excess dosing of antiplatelet and antithrombin agents in thetreatment of non-ST-segment elevation acute coronary syndromes. JAMA 2005;294:3108–3116.169. Li Y, Spencer F, Becker R. Comparative efficacy of fibrinogen and platelet supplementation on the in vitro reversibilityof competitive glycoprotein IIb/IIIa receptor-directed platelet inhibition. Am Heart J2002;143:725–732.170. Neumann FJ, Kastrati A, Pogatsa-Murray G, Mehilli J, Bollwein H, Bestehorn HP, Schmitt C, Seyfarth M,Dirschinger J, Schomig A. Evaluation of prolonged antithrombotic pretreatment (‘cooling-off’ strategy) beforeintervention in patients with unstable coronary syndromes: a randomized controlled trial. JAMA2003;290:1593–1599.171. Harrington RA, Becker RC, Cannon CP, Gutterman D, Lincoff AM, Popma JJ, Steg G, Guyatt GH, Goodman SG.Antithrombotic therapy for non-ST-segment elevation acute coronary syndromes: American College of ChestPhysicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008;133:670S–707S.172. Eikelboom JW, Anand SS, Malmberg K, Weitz JI, Ginsberg JS, Yusuf S. Unfractionated heparin and low-molecular-weight heparin in acute coronary syndrome without ST elevation: a meta-analysis. Lancet2000;355:1936–1942.173. Simoons ML, Bobbink IW, Boland J, Gardien M, Klootwijk P, Lensing AW, Ruzyllo W, Umans VA, Vahanian A,Van De Werf F, Zeymer U; PENTUA Investigators. A dose-finding study of fondaparinux in patients with non-ST-segment elevation acute coronary syndromes: the Pentasaccharide in Unstable Angina (PENTUA) Study.J Am Coll Cardiol 2004;43:2183–2190.174. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Effects of fondaparinux on mortality and reinfarction in patients with acute ST-segment elevationmyocardial infarction: the OASIS-6 randomized trial. JAMA 2006;295:1519–1530.175. Yusuf S, Mehta SR, Chrolavicius S, Afzal R, Pogue J, Granger CB, Budaj A, Peters RJ, Bassand JP, Wallentin L,Joyner C, Fox KA. Comparison of fondaparinux and enoxaparin in acute coronary syndromes. N Engl J Med2006;354:1464–1476.176. Mehta SR, Steg PG, Granger CB, Bassand JP, Faxon DP,Weitz JI, Afzal R, Rush B, Peters RJ, Natarajan MK,Velianou JL, Goodhart DM, Labinaz M, Tanguay JF, Fox KA, Yusuf S. Randomized, blinded trial comparingfondaparinux with unfractionated heparin in patients undergoing contemporary percutaneous coronary intervention:Arixtra Study in Percutaneous Coronary Intervention: a Randomized Evaluation (ASPIRE) pilot trial.Circulation 2005;111:1390–1397.177. Anderson JA, Hirsh J, Yusuf S, Johnston M, Afzal R, Mehta SR, Fox KA, Budaj A, Eikelboom JW. Comparisonof the anticoagulant intensities of fondaparinux and enoxaparin in the Organization to Assess Strategies inAcute Ischemic Syndromes (OASIS)-5 trial. J Thromb Haemost 2010;8:243–249.178. Steg PG, Jolly SS, Mehta SR, Afzal R, Xavier D, Rupprecht HJ, Lopez-Sendon JL, Budaj A, Diaz R, Avezum A,Widimsky P, Rao SV, Chrolavicius S, Meeks B, Joyner C, Pogue J, Yusuf S. Low-dose vs standard-dose unfractionatedheparin for percutaneous coronary intervention in acute coronary syndromes treated with fondaparinux:the FUTURA/OASIS-8 randomized trial. JAMA 2010;304:1339–1349.179. Antman EM, McCabe CH, Gurfinkel EP, Turpie AG, Bernink PJ, Salein D, Bayes De Luna A, Fox K, Lablanche JM,Radley D, Premmereur J, Braunwald E. Enoxaparin prevents death and cardiac ischemic events in unstableangina/non-Q-wave myocardial infarction. Results of the thrombolysis in myocardial infarction (TIMI) 11Btrial. Circulation 1999;100:1593–1601.180. Cohen M, Demers C, Gurfinkel EP, Turpie AG, Fromell GJ, Goodman S, Langer A, Califf RM, Fox KA, PremmereurJ, Bigonzi F. A comparison of low-molecular-weight heparin with unfractionated heparin for unstablecoronary artery disease. Efficacy and Safety of Subcutaneous Enoxaparin in Non-Q-Wave Coronary EventsStudy Group. N Engl J Med 1997;337:447–452.181. FRagmin and Fast Revascularisation during InStability in Coronary artery disease Investigators. Long-term lowmolecular-mass heparin in unstable coronary-artery disease: FRISC II prospective randomised multicentrestudy. Lancet 1999;354:701–707.182. Fragmin during Instability in Coronary Artery Disease (FRISC) study group. Low-molecular-weight heparinduring instability in coronary artery disease Lancet 1996;347:561–568.183. Hirsh J, Raschke R. Heparin and low-molecular-weight heparin: the Seventh ACCP Conference on Antithromboticand Thrombolytic Therapy. Chest 2004;126:188S–203S.184. TIMI 11A Investigators. Dose-ranging trial of enoxaparin for unstable angina: results of TIMI 11A. The Thrombolysisin Myocardial Infarction (TIMI) 11A Trial Investigators. J Am Coll Cardiol 1997;29:1474–1482.185. Montalescot G, Collet JP, Tanguy ML, Ankri A, Payot L, Dumaine R, Choussat R, Beygui F, Gallois V, Thomas D.Anti-Xa activity relates to survival and efficacy in unselected acute coronary syndrome patients treated withenoxaparin. Circulation 2004;110:392–398.186. Choussat R, Montalescot G, Collet JP, Vicaut E, Ankri A, Gallois V, Drobinski G, Sotirov I, Thomas D. A unique,low dose of intravenous enoxaparin in elective percutaneous coronary intervention. J Am Coll Cardiol2002;40:1943–1950.187. Collet JP, Montalescot G, Lison L, Choussat R, Ankri A, Drobinski G, Sotirov I, Thomas D. Percutaneous coronaryintervention after subcutaneous enoxaparin pretreatment in patients with unstable angina pectoris. Circulation2001;103:658–663.188. Murphy S, Gibson C, Morrow D, Van de Werf F, Menown I, Goodman S, Mahaffey K, Cohen M, McCabe C,Antman EM, Braunwald E. Efficacy and safety of the low-molecular weight heparin enoxaparin comparedwith unfractionated heparin across the acute coronary syndrome spectrum: a meta-analysis.Eur Heart J2007;28:2077–2086.189. Blazing MA, de Lemos JA, White HD, Fox KA, Verheugt FW, Ardissino D, DiBattiste PM, Palmisano J, BilheimerDW, Snapinn SM, Ramsey KE, Gardner LH, Hasselblad V, Pfeffer MA, Lewis EF, Braunwald E, Califf RM. Safetyand efficacy of enoxaparin vs unfractionated heparin in patients with non-ST-segment elevation acute coronarysyndromes who receive tirofiban and aspirin: a randomized controlled trial. JAMA 2004;292:55–64.190. Cohen M, Theroux P, Borzak S, Frey MJ, White HD, Van Mieghem W, Senatore F, Lis J, Mukherjee R, Harris K,Bigonzi F. Randomized double-blind safety study of enoxaparin versus unfractionated heparin in patients withnon-ST-segment elevation acute coronary syndromes treated with tirofiban and aspirin: the ACUTE II study.The Antithrombotic Combination Using Tirofiban and Enoxaparin. Am Heart J 2002;144:470–477.191. Goodman SG, Fitchett D, Armstrong PW, Tan M, Langer A. Randomized evaluation of the safety and efficacyof enoxaparin versus unfractionated heparin in high-risk patients with non-ST-segment elevation acute coronarysyndromes receiving the glycoprotein IIb/IIIa inhibitor eptifibatide. Circulation 2003;107:238–244.192. Ferguson JJ, Califf RM, Antman EM, Cohen M, Grines CL, Goodman S, Kereiakes DJ, Langer A, Mahaffey KW,Nessel CC, Armstrong PW, Avezum A, Aylward P, Becker RC, Biasucci L, Borzak S, Col J, Frey MJ, Fry E, GulbaDC, Guneri S, Gurfinkel E, Harrington R, Hochman JS, Kleiman NS, Leon MB, Lopez-Sendon JL, Pepine CJ,Ruzyllo W, Steinhubl SR, Teirstein PS, Toro-Figueroa L, White H. Enoxaparin vs unfractionated heparin in highriskpatients with non-ST-segment elevation acute coronary syndromes managed with an intended early invasivestrategy: primary results of the SYNERGY randomized trial. JAMA 2004;292:45–54.193. Petersen JL, Mahaffey KW, Hasselblad V, Antman EM, Cohen M, Goodman SG, Langer A, Blazing MA, Le-Moigne-Amrani A, de Lemos JA, Nessel CC, Harrington RA, Ferguson JJ, Braunwald E, Califf RM. Efficacy andbleeding complications among patients randomized to enoxaparin or unfractionated heparin for antithrombintherapy in non-ST-Segment elevation acute coronary syndromes: a systematic overview. JAMA2004;292:89–96.194. Sanchez-Pena P, Hulot JS, Urien S, Ankri A, Collet JP, Choussat R, Lechat P, Montalescot G. Anti-factor Xa kineticsafter intravenous enoxaparin in patients undergoing percutaneous coronary intervention: a populationmodel analysis. Br J Clin Pharmacol 2005;60:364–373.195. Montalescot G, White HD, Gallo R, Cohen M, Steg PG, Aylward PE, Bode C, Chiariello M, King SB 3rd, HarringtonRA, Desmet WJ, Macaya C, Steinhubl SR. Enoxaparin versus unfractionated heparin in elective percutaneouscoronary intervention. N Engl J Med 2006;355:1006–1017.196. Stone GW, McLaurin BT, Cox DA, Bertrand ME, Lincoff AM, Moses JW, White HD, Pocock SJ, Ware JH, Feit F,Colombo A, Aylward PE, Cequier AR, Darius H, Desmet W, Ebrahimi R, Hamon M, Rasmussen LH, RupprechtHJ, Hoekstra J, Mehran R, Ohman EM; ACUITY Investigators. Bivalirudin for patients with acute coronary syndromes.N Engl J Med 2006;355:2203–2216.197. Stone GW, White HD, Ohman EM, Bertrand ME, Lincoff AM, McLaurin BT, Cox DA, Pocock SJ, Ware JH, FeitF, Colombo A, Manoukian SV, Lansky AJ, Mehran R, Moses JW. Acute Catheterization and Urgent InterventionTriage strategy (ACUITY) trial investigators. Bivalirudin in patients with acute coronary syndromes undergoingpercutaneous coronary intervention: a subgroup analysis from the Acute Catheterization and UrgentIntervention Triage strategy (ACUITY) trial. Lancet 2007;369:907–919.198. Stone G, Ware J, Bertrand M, Lincoff A, Moses J, Ohman E, White H, Feit F, Colombo A, McLaurin B, Cox D,Manoukian S, Fahy M, Clayton T, Mehran R, Pocock S. For the ACUITY Investigators. Antithrombotic strategiesin patients with acute coronary syndromes undergoing early invasive management: one-year results fromthe ACUITY trial. JAMA 2007;298:2497–2506. 199. White HD, Chew DP, Hoekstra JW, Miller CD, Pollack CV Jr., Feit F, Lincoff AM, Bertrand M, Pocock S, Ware J,Ohman EM, Mehran R, Stone GW. Safety and efficacy of switching from either unfractionated heparin orenoxaparin to bivalirudin in patients with non-ST-segment elevation acute coronary syndromes managedwith an invasive strategy: results from the ACUITY (Acute Catheterization and Urgent Intervention Triage strategY)trial. J Am Coll Cardiol 2008;51:1734–1741.200. Alexander JH, Becker RC, Bhatt DL, Cools F, Crea F, Dellborg M, Fox KA, Goodman SG, Harrington RA, HuberK, Husted S, Lewis BS, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, WallentinL. Apixaban, an oral, direct, selective factor Xa inhibitor, in combination with antiplatelet therapy after acutecoronary syndrome: results of the Apixaban for Prevention of Acute Ischemic and Safety Events (APPRAISE)trial. Circulation 2009;119:2877–2885.201. Mega JL, Braunwald E, Mohanavelu S, Burton P, Poulter R, Misselwitz F, Hricak V, Barnathan ES, Bordes P,Witkowski A, Markov V, Oppenheimer L, Gibson CM. Rivaroxaban versus placebo in patients with acute coronarysyndromes (ATLAS ACS-TIMI 46): a randomised, double-blind, phase II trial. Lancet 2009;374:29–38.202. Alexander J, Becker R, Bhatt D, Cools F, Crea F, Dellborg M, Fox K, Goodman S, Harrington R, Huber K, HustedS, Lewis B, Lopez-Sendon J, Mohan P, Montalescot G, Ruda M, Ruzyllo W, Verheugt F, Wallentin L. For the APPRAISESteering Committee and Investigators. Apixaban, an oral, direct, selective factor Xa inhibitor, in combinationwith antiplatelet therapy after acute coronary syndrome: results of the Apixaban for Prevention ofAcute Ischemic and Safety Events (APPRAISE) trial. Circulation 2009;119:2877–2885.203. Sabatine MS, Antman EM, Widimsky P, Ebrahim IO, Kiss RG, Saaiman A, Polasek R, Contant CF, McCabe CH,Braunwald E. Otamixaban for the treatment of patients with non-ST-elevation acute coronary syndromes(SEPIA-ACS1 TIMI 42): a randomised, double-blind, active-controlled, phase 2 trial. Lancet2009;374:787–795.204. Lip GY, Huber K, Andreotti F, Arnesen H, Airaksinen JK, Cuisset T, Kirchhof P, Marin F. Antithrombotic managementof atrial fibrillation patients presenting with acute coronary syndrome and/or undergoing coronarystenting: executive summary—a Consensus Document of the European Society of Cardiology Working Groupon Thrombosis, endorsed by the European Heart Rhythm Association (EHRA) and the European Associationof Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2010;31:1311–1318.205. Yan AT, Yan RT, Tan M, Eagle KA, Granger CB, Dabbous OH, Fitchett D, Grima E, Langer A, Goodman SG. Inhospitalrevascularization and one-year outcome of acute coronary syndrome patients stratified by the GRACErisk score. Am J Cardiol 2005;96:913–916.206. Mehta SR, Cannon CP, Fox KA, Wallentin L, Boden WE, Spacek R, Widimsky P, McCullough PA, Hunt D, BraunwaldE, Yusuf S. Routine vs selective invasive strategies in patients with acute coronary syndromes: a collaborativemeta-analysis of randomized trials. JAMA 2005;293:2908–2917.207. Bavry AA, Kumbhani DJ, Rassi AN, Bhatt DL, Askari AT. Benefit of early invasive therapy in acute coronary syndromes:a meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006;48:1319–1325.208. O’Donoghue M, Boden WE, Braunwald E, Cannon CP, Clayton TC, de Winter RJ, Fox KA, Lagerqvist B, McCulloughPA, Murphy SA, Spacek R, Swahn E,Wallentin L, Windhausen F, Sabatine MS. Early invasive vs conservativetreatment strategies in women and men with unstable angina and non-ST-segment elevation myocardialinfarction: a meta-analysis. JAMA 2008; 300:71–80.209. Fox KA, Clayton TC, Damman P, Pocock SJ, de Winter RJ, Tijssen JG, Lagerqvist B,Wallentin L. Long-term outcomeof a routine versus selective invasive strategy in patients with non-ST-segment elevation acute coronarysyndrome a meta-analysis of individual patient data. J Am Coll Cardiol 2010;55:2435–2445.210. Montalescot G, Cayla G, Collet JP, Elhadad S, Beygui F, Le Breton H, Choussat R, Leclercq F, Silvain J, Duclos F,Aout M, Dubois-Rande JL, Barthelemy O, Ducrocq G, Bellemain-Appaix A, Payot L, Steg PG, Henry P, SpauldingC, Vicaut E. Immediate vs delayed intervention for acute coronary syndromes: a randomized clinical trial.JAMA 2009;302:947–954.211. van’t Hof AW, de Vries ST, Dambrink JH, Miedema K, Suryapranata H, Hoorntje JC, Gosselink AT, Zijlstra F, deBoer MJ. A comparison of two invasive strategies in patients with non-ST elevation acute coronary syndromes:results of the Early or Late Intervention in unStable Angina (ELISA) pilot study. 2b/3a upstream therapy andacute coronary syndromes. Eur Heart J 2003;24:1401–1405.212. Mehta SR, Granger CB, Boden WE, Steg PG, Bassand JP, Faxon DP, Afzal R, Chrolavicius S, Jolly SS, WidimskyP, Avezum A, Rupprecht HJ, Zhu J, Col J, Natarajan MK, Horsman C, Fox KA, Yusuf S. Early versus delayed invasiveintervention in acute coronary syndromes. N Engl J Med 2009;360:2165–2175.213. Katritsis DG, Siontis GC, Kastrati A, van’t Hof AW, Neumann FJ, Siontis KC, Ioannidis JP. Optimal timing ofcoronary angiography and potential intervention in non-ST-elevation acute coronary syndromes. Eur Heart J2010;32:32–40.214. Riezebos RK, Ronner E, Ter Bals E, Slagboom T, Smits PC, ten Berg JM, Kiemeneij F, Amoroso G, Patterson MS,Suttorp MJ, Tijssen JG, Laarman GJ. Immediate versus deferred coronary angioplasty in non-ST-segment elevationacute coronary syndromes. Heart 2009;95:807–812.215. Sorajja P, Gersh BJ, Cox DA, McLaughlin MG, Zimetbaum P, Costantini C, Stuckey T, Tcheng JE, Mehran R,Lansky AJ, Grines CL, Stone GW. Impact of delay to angioplasty in patients with acute coronary syndromes undergoinginvasive management: analysis from the ACUITY (Acute Catheterization and Urgent InterventionTriage strategY) trial. J Am Coll Cardiol 2010;55:1416–1424.216. Brener SJ, Milford-Beland S, Roe MT, Bhatt DL, Weintraub WS, Brindis RG. Culprit-only or multivessel revascularizationin patients with acute coronary syndromes: an American College of Cardiology National CardiovascularDatabase Registry report. Am Heart J 2008;155:140–146.217. Ben-Gal Y, Moses JW, Mehran R, Lansky AJ,Weisz G, Nikolsky E, Argenziano M, Williams MR, Colombo A, AylwardPE, Stone GW. Surgical versus percutaneous revascularization for multivessel disease in patients withacute coronary syndromes: analysis from the ACUITY (Acute Catheterization and Urgent Intervention TriageStrategy) trial. JACC Cardiovasc Interv 2010;3:1059–1067.218. Serruys PW, Morice MC, Kappetein AP, Colombo A, Holmes DR, Mack MJ, Stahle E, Feldman TE, van denBrand M, Bass EJ, Van Dyck N, Leadley K, Dawkins KD, Mohr FW. Percutaneous coronary intervention versuscoronary-artery bypass grafting for severe coronary artery disease. N Engl J Med 2009;360:961–972.219. Sianos G, Morel MA, Kappetein AP, Morice MC, Colombo A, Dawkins K, van den Brand M, Van Dyck N, RussellME, Mohr FW, Serruys PW. The SYNTAX Score: an angiographic tool grading the complexity of coronaryartery disease. EuroIntervention 2005;1:219–227.220. de Winter RJ, Windhausen F, Cornel JH, Dunselman PH, Janus CL, Bendermacher PE, Michels HR, Sanders GT,Tijssen JG, Verheugt FW. Early invasive versus selectively invasive management for acute coronary syndromes.N Engl J Med 2005;353:1095–1104.221. Monteiro P. Impact of early coronary artery bypass graft in an unselected acute coronary syndrome patient population.Circulation 2006;114:I467–I472.222. Parikh SV, de Lemos JA, Jessen ME, Brilakis ES, Ohman EM, Chen AY, Wang TY, Peterson ED, Roe MT, HolperEM. Timing of in-hospital coronary artery bypass graft surgery for non-ST-segment elevation myocardial infarctionpatients results from the National Cardiovascular Data Registry ACTION Registry-GWTG (Acute CoronaryTreatment and Intervention Outcomes Network Registry-Get With The Guidelines). JACC CardiovascInterv 2010;3:419–427.223. Chu MW, Wilson SR, Novick RJ, Stitt LW, Quantz MA. Does clopidogrel increase blood loss following coronaryartery bypass surgery? Ann Thorac Surg 2004;78:1536–1541.224. Solodky A, Behar S, Boyko V, Battler A, Hasdai D. The outcome of coronary artery bypass grafting surgeryamong patients hospitalized with acute coronary syndrome: the Euro Heart Survey of acute coronary syndromeexperience. Cardiology 2005;103:44–47.225. Kaiser C, Galatius S, Erne P, Eberli F, Alber H, Rickli H, Pedrazzini G, Hornig B, Bertel O, Bonetti P, De Servi S,Brunner-La Rocca HP, Ricard I, Pfisterer M. Drug-eluting versus bare-metal stents in large coronary arteries. NEngl J Med 2010;363:2310–2319.226. Greenhalgh J, Hockenhull J, Rao N, Dundar Y, Dickson RC, Bagust A. Drug-eluting stents versus bare metalstents for angina or acute coronary syndromes. Cochrane Database Syst Rev 2010;5:CD004587.227. Vlaar PJ, Diercks GF, Svilaas T, Vogelzang M, de Smet BJ, van den Heuvel AF, Anthonio RL, Jessurun GA, TanES, Suurmeijer AJ, Zijlstra F. The feasibility and safety of routine thrombus aspiration in patients with non-STelevationmyocardial infarction. Catheter Cardiovasc Interv 2008;72:937–942.228. Rosengren A, Wallentin L, Simoons M, Gitt AK, Behar S, Battler A, Hasdai D. Age, clinical presentation, andoutcome of acute coronary syndromes in the Euroheart acute coronary syndrome survey. Eur Heart J2006;27:789–795.229. Bauer T, Koeth O, Junger C, Heer T, Wienbergen H, Gitt A, Zahn R, Senges J, Zeymer U. Effect of an invasivestrategy on in-hospital outcome in elderly patients with non-ST-elevation myocardial infarction. Eur Heart J2007;28:2873–2878.230. Alexander KP, Newby LK, Cannon CP, Armstrong PW, Gibler WB, Rich MW, Van de Werf F, White HD, WeaverWD, Naylor MD, Gore JM, Krumholz HM, Ohman EM. Acute coronary care in the elderly, part I: non-ST-segment-elevation acute coronary syndromes: a scientific statement for healthcare professionals from the AmericanHeart Association Council on Clinical Cardiology: in collaboration with the Society of Geriatric Cardiology.Circulation 2007;115:2549–2569.231. Alexander KP, Chen AY, Roe MT, Newby LK, Gibson CM, Allen-LaPointe NM, Pollack C, Gibler WB, Ohman EM,Peterson ED. Excess dosing of antiplatelet and antithrombin agents in the treatment of non-ST-segment elevationacute coronary syndromes. JAMA 2005;294:3108–3116.232. Lopes RD, Alexander KP, Marcucci G, White HD, Spinler S, Col J, Aylward PE, Califf RM, Mahaffey KW. Outcomesin elderly patients with acute coronary syndromes randomized to enoxaparin vs. unfractionated heparin:results from the SYNERGY trial. Eur Heart J 2008;29:1827–1833.233. Wallentin L, Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E. Outcome at 1 year after an invasive comparedwith a non-invasive strategy in unstable coronary-artery disease: the FRISC II invasive randomised trial. FRISCII Investigators. Fast Revascularisation during Instability in Coronary artery disease. Lancet 2000;356:9–16.234. Lagerqvist B, Husted S, Kontny F, Stahle E, Swahn E, Wallentin L. 5-Year outcomes in the FRISC-II randomisedtrial of an invasive versus a non-invasive strategy in non-ST-elevation acute coronary syndrome: a follow-upstudy. Lancet 2006;368:998–1004.235. Bach RG, Cannon CP, Weintraub WS, DiBattiste PM, Demopoulos LA, Anderson HV, DeLucca PT, Mahoney EM,Murphy SA, Braunwald E. The effect of routine, early invasive management on outcome for elderly patientswith non-ST-segment elevation acute coronary syndromes. Ann Intern Med 2004;141:186–195.236. Rosengren A, Wallentin L, Gitt AK, Behar S, Battler A, Hasdai D. Sex, age, and clinical presentation of acutecoronary syndromes. Eur Heart J 2004;25:663–670.237. Alfredsson J, Stenestrand U, Wallentin L, Swahn E. Gender differences in management and outcome in non-ST-elevation acute coronary syndrome. Heart 2007;93:1357–1362.238. Hvelplund A, Galatius S, Madsen M, Rasmussen JN, Rasmussen S, Madsen JK, Sand NP, Tilsted HH, ThayssenP, Sindby E, Hojbjerg S, Abildstrom SZ. Women with acute coronary syndrome are less invasively examined andsubsequently less treated than men. Eur Heart J 2010;31:684–690.239. Diercks DB, Owen KP, Kontos MC, Blomkalns A, Chen AY, Miller C, Wiviott S, Peterson ED. Gender differencesin time to presentation for myocardial infarction before and after a national women’s cardiovascular awarenesscampaign: a temporal analysis from the Can Rapid Risk Stratification of Unstable Angina Patients SuppressADverse Outcomes with Early Implementation (CRUSADE) and the National Cardiovascular Data RegistryAcute Coronary Treatment and Intervention Outcomes Network-Get with the Guidelines (NCDR ACTION Registry-GWTG). Am Heart J 2010;160:80–87 e83.240. Heer T, Gitt AK, Juenger C, Schiele R, Wienbergen H, Towae F, Gottwitz M, Zahn R, Zeymer U, Senges J. Genderdifferences in acute non-ST-segment elevation myocardial infarction. Am J Cardiol 2006;98:160–166.241. Bavry AA, Kumbhani DJ, Quiroz R, Ramchandani SR, Kenchaiah S, Antman EM. Invasive therapy along withglycoprotein IIb/IIIa inhibitors and intracoronary stents improves survival in non-ST-segment elevation acutecoronary syndromes: a meta-analysis and review of the literature. Am J Cardiol 2004;93:830–835.242. Fox KA, Poole-Wilson PA, Henderson RA, Clayton TC, Chamberlain DA, Shaw TR, Wheatley DJ, Pocock SJ. Interventionalversus conservative treatment for patients with unstable angina or non-ST-elevation myocardialinfarction: the British Heart Foundation RITA 3 randomised trial. Randomized Intervention Trial of unstableAngina. Lancet 2002;360:743–751.243. Hoenig MR, Doust JA, Aroney CN, Scott IA. Early invasive versus conservative strategies for unstable angina& non-ST-elevation myocardial infarction in the stent era. Cochrane Database Syst Rev 2006;3:CD004815.244. Glaser R, Herrmann HC, Murphy SA, Demopoulos LA, DiBattiste PM, Cannon CP, Braunwald E. Benefit of anearly invasive management strategy in women with acute coronary syndromes. JAMA2002;288:3124–3129.245. Boersma E, Harrington RA, Moliterno DJ, White H, Simoons ML. Platelet glycoprotein IIb/IIIa inhibitors inacute coronary syndromes. Lancet 2002;360:342–343.246. Berger JS, Elliott L, Gallup D, Roe M, Granger CB, Armstrong PW, Simes RJ, White HD, Van de Werf F, TopolEJ, Hochman JS, Newby LK, Harrington RA, Califf RM, Becker RC, Douglas PS. Sex differences in mortalityfollowing acute coronary syndromes. JAMA 2009;302:874–882.247. Bartnik M, Malmberg K, Norhammar A, Tenerz A, Ohrvik J, Ryden L. Newly detected abnormal glucose tolerance:an important predictor of long-term outcome after myocardial infarction. Eur Heart J2004;25:1990–1997.248. Dotevall A, Hasdai D, Wallentin L, Battler A, Rosengren A. Diabetes mellitus: clinical presentation and outcomein men and women with acute coronary syndromes. Data from the Euro Heart Survey ACS. Diabet Med2005;22:1542–1550. 249. Donahoe SM, Stewart GC, McCabe CH, Mohanavelu S, Murphy SA, Cannon CP, Antman EM. Diabetes andmortality following acute coronary syndromes. JAMA 2007;298:765–775.250. Hasin T, Hochadel M, Gitt AK, Behar S, Bueno H, Hasin Y. Comparison of treatment and outcome of acute coronarysyndrome in patients with versus patients without diabetes mellitus. Am J Cardiol 2009;103:772–778.251. De Caterina R, Madonna R, Sourij H, Wascher T. Glycaemic control in acute coronary syndromes: prognosticvalue and therapeutic options. Eur Heart J 2010;31:1557–1564.252. Graham I, Atar D, Borch-Johnsen K, Boysen G, Burell G, Cifkova R, Dallongeville J, De Backer G, Ebrahim S,Gjelsvik B, Herrmann-Lingen C, Hoes A, Humphries S, Knapton M, Perk J, Priori SG, Pyorala K, Reiner Z, RuilopeL, Sans-Menendez S, Scholte op Reimer W, Weissberg P, Wood D, Yarnell J, Zamorano JL, Walma E,Fitzgerald T, Cooney MT, Dudina A. European guidelines on cardiovascular disease prevention in clinical practice:executive summary: Fourth Joint Task Force of the European Society of Cardiology and Other Societies onCardiovascular Disease Prevention in Clinical Practice (Constituted by representatives of nine societies and byinvited experts). Eur Heart J 2007;28:2375–2414.253. Finfer S, Chittock DR, Su SY, Blair D, Foster D, Dhingra V, Bellomo R, Cook D, Dodek P, Henderson WR, HebertPC, Heritier S, Heyland DK, McArthur C, McDonald E, Mitchell I, Myburgh JA, Norton R, Potter J, RobinsonBG, Ronco JJ. Intensive versus conventional glucose control in critically ill patients. N Engl J Med2009;360:1283–1297.254. Diaz R, Goyal A, Mehta SR, Afzal R, Xavier D, Pais P, Chrolavicius S, Zhu J, Kazmi K, Liu L, Budaj A, Zubaid M,Avezum A, Ruda M, Yusuf S. Glucose–insulin–potassium therapy in patients with ST-segment elevation myocardialinfarction. JAMA 2007;298:2399–2405.255. Cannon CP, Weintraub WS, Demopoulos LA, Vicari R, Frey MJ, Lakkis N, Neumann FJ, Robertson DH, DeLuccaPT, DiBattiste PM, Gibson CM, Braunwald E. Comparison of early invasive and conservative strategies in patientswith unstable coronary syndromes treated with the glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med2001;344:1879–1887.256. Hlatky MA, Boothroyd DB, Bravata DM, Boersma E, Booth J, Brooks MM, Carrie D, Clayton TC, Danchin N,Flather M, Hamm CW, Hueb WA, Kahler J, Kelsey SF, King SB, Kosinski AS, Lopes N, McDonald KM, RodriguezA, Serruys P, Sigwart U, Stables RH, Owens DK, Pocock SJ. Coronary artery bypass surgery compared withpercutaneous coronary interventions for multivessel disease: a collaborative analysis of individual patient datafrom ten randomised trials. Lancet 2009;373:1190–1197.257. Chaitman BR, Hardison RM, Adler D, Gebhart S, Grogan M, Ocampo S, Sopko G, Ramires JA, Schneider D,Frye RL. The Bypass Angioplasty Revascularization Investigation 2 Diabetes randomized trial of different treatmentstrategies in type 2 diabetes mellitus with stable ischemic heart disease: impact of treatment strategy oncardiac mortality and myocardial infarction. Circulation 2009;120:2529–2540.258. Frye RL, August P, Brooks MM, Hardison RM, Kelsey SF, MacGregor JM, Orchard TJ, Chaitman BR, Genuth SM,Goldberg SH, Hlatky MA, Jones TL, Molitch ME, Nesto RW, Sako EY, Sobel BE. A randomized trial of therapiesfor type 2 diabetes and coronary artery disease. N Engl J Med 2009;360:2503–2515.259. Banning AP, Westaby S, Morice MC, Kappetein AP, Mohr FW, Berti S, Glauber M, Kellett MA, Kramer RS,Leadley K, Dawkins KD, Serruys PW. Diabetic and nondiabetic patients with left main and/or 3-vessel coronaryartery disease: comparison of outcomes with cardiac surgery and paclitaxel-eluting stents. J Am Coll Cardiol2010;55:1067–1075.260. Hannan EL, Wu C, Walford G, Culliford AT, Gold JP, Smith CR, Higgins RS, Carlson RE, Jones RH. Drug-elutingstents vs. coronary-artery bypass grafting in multivessel coronary disease. N Engl J Med 2008;358:331–341.261. Stettler C, Allemann S, Wandel S, Kastrati A, Morice MC, Schomig A, Pfisterer ME, Stone GW, Leon MB, de LezoJS, Goy JJ, Park SJ, Sabate M, Suttorp MJ, Kelbaek H, Spaulding C, Menichelli M, Vermeersch P, Dirksen MT,Cervinka P, De Carlo M, Erglis A, Chechi T, Ortolani P, Schalij MJ, Diem P, Meier B, Windecker S, Juni P. Drugeluting and bare metal stents in people with and without diabetes: collaborative network meta-analysis. BMJ2008;337:a1331.262. Wiviott SD, Braunwald E, Angiolillo DJ, Meisel S, Dalby AJ, Verheugt FW, Goodman SG, Corbalan R, PurdyDA, Murphy SA, McCabe CH, Antman EM. Greater clinical benefit of more intensive oral antiplatelet therapywith prasugrel in patients with diabetes mellitus in the trial to assess improvement in therapeutic outcomes byoptimizing platelet inhibition with prasugrel-Thrombolysis in Myocardial Infarction 38. Circulation2008;118:1626–1636.263. James S, Angiolillo DJ, Cornel JH, Erlinge D, Husted S, Kontny F, Maya J, Nicolau JC, Spinar J, Storey RF, StevensSR, Wallentin L. Ticagrelor vs. clopidogrel in patients with acute coronary syndromes and diabetes: a substudyfrom the PLATelet inhibition and patient Outcomes (PLATO) trial. Eur Heart J 2010;31:3006–3016.264. Roffi M, Chew DP, Mukherjee D, Bhatt DL, White JA, Heeschen C, Hamm CW, Moliterno DJ, Califf RM, WhiteHD, Kleiman NS, Theroux P, Topol EJ. Platelet glycoprotein IIb/IIIa inhibitors reduce mortality in diabetic patientswith non-ST-segment-elevation acute coronary syndromes. Circulation 2001;104:2767–2771.265. Salpeter SR, Greyber E, Pasternak GA, Salpeter EE. Risk of fatal and nonfatal lactic acidosis with metformin usein type 2 diabetes mellitus. Cochrane Database Syst Rev 2010;4:CD002967.266. Hasdai D, Behar S, Wallentin L, Danchin N, Gitt AK, Boersma E, Fioretti PM, Simoons ML, Battler A. A prospectivesurvey of the characteristics, treatments and outcomes of patients with acute coronary syndromes in Europeand the Mediterranean basin; the Euro Heart Survey of Acute Coronary Syndromes (Euro Heart SurveyACS). Eur Heart J 2002;23:1190–1201.267. Goldenberg I, Subirana I, Boyko V, Vila J, Elosua R, Permanyer-Miralda G, Ferreira-Gonzalez I, Benderly M,Guetta V, Behar S, Marrugat J. Relation between renal function and outcomes in patients with non-ST-segmentelevation acute coronary syndrome: real-world data from the European Public Health Outcome Researchand Indicators Collection Project. Arch Intern Med 2010;170:888–895.268. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Relationbetween renal function, presentation, use of therapies and in-hospital complications in acute coronary syndrome:data from the SWEDEHEART register. J Intern Med 2010;268:40–49.269. Collet JP, Montalescot G, Agnelli G, Van de Werf F, Gurfinkel EP, Lopez-Sendon J, Laufenberg CV, Klutman M,Gowda N, Gulba D. Non-ST-segment elevation acute coronary syndrome in patients with renal dysfunction:benefit of low-molecular-weight heparin alone or with glycoprotein IIb/IIIa inhibitors on outcomes. The GlobalRegistry of Acute Coronary Events. Eur Heart J 2005;26:2285–2293.270. Fox KA, Bassand JP, Mehta SR, Wallentin L, Theroux P, Piegas LS, Valentin V, Moccetti T, Chrolavicius S, AfzalR, Yusuf S. Influence of renal function on the efficacy and safety of fondaparinux relative to enoxaparin in nonST-segment elevation acute coronary syndromes. Ann Intern Med 2007;147:304–310.271. James S, Budaj A, Aylward P, Buck KK, Cannon CP, Cornel JH, Harrington RA, Horrow J, Katus H, Keltai M, LewisBS, Parikh K, Storey RF, Szummer K, Wojdyla D, Wallentin L. Ticagrelor versus clopidogrel in acute coronary syndromesin relation to renal function: results from the Platelet Inhibition and Patient Outcomes (PLATO) trial.Circulation 2010;122:1056–1067.272. Pannu N, Wiebe N, Tonelli M. Prophylaxis strategies for contrast-induced nephropathy. JAMA2006;295:2765–2779.273. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, Stenestrand U, Wallentin L, Jernberg T. Influenceof renal function on the effects of early revascularization in non-ST-elevation myocardial infarction: data fromthe Swedish Web-System for Enhancement and Development of Evidence-Based Care in Heart Disease EvaluatedAccording to Recommended Therapies (SWEDEHEART). Circulation 2009;120:851–858.274. Steg PG, Dabbous OH, Feldman LJ, Cohen-Solal A, Aumont MC, Lopez-Sendon J, Budaj A, Goldberg RJ, KleinW, Anderson FA Jr. Determinants and prognostic impact of heart failure complicating acute coronary syndromes:observations from the Global Registry of Acute Coronary Events (GRACE). Circulation2004;109:494–499.275. Dickstein K, Vardas PE, Auricchio A, Daubert JC, Linde C, McMurray J, Ponikowski P, Priori SG, Sutton R, vanVeldhuisen DJ, Vahanian A, Bax J, Ceconi C, Dean V, Filippatos G, Funck-Brentano C, Hobbs R, Kearney P, Mc-Donagh T, Popescu BA, Reiner Z, Sechtem U, Sirnes PA, Tendera M, Vardas P, Widimsky P, Anker SD, Blanc JJ,Gasparini M, Hoes AW, Israel CW, Kalarus Z, Merkely B, Swedberg K, Camm AJ. 2010 Focused Update of ESCGuidelines on device therapy in heart failure: an update of the 2008 ESC Guidelines for the diagnosis andtreatment of acute and chronic heart failure and the 2007 ESC guidelines for cardiac and resynchronizationtherapy. Developed with the special contribution of the Heart Failure Association and the European HeartRhythm Association. Eur Heart J 2010;31:2677–2687.276. Pitt B, Remme W, Zannad F, Neaton J, Martinez F, Roniker B, Bittman R, Hurley S, Kleiman J, Gatlin M.Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction.N Engl J Med 2003;348:1309–1321.277. Zannad F, McMurray JJ, Krum H, van Veldhuisen DJ, Swedberg K, Shi H, Vincent J, Pocock SJ, Pitt B. Eplerenonein patients with systolic heart failure and mild symptoms. N Engl J Med 2011;364:11–21.278. Moss AJ, Zareba W, Hall WJ, Klein H, Wilber DJ, Cannom DS, Daubert JP, Higgins SL, Brown MW, Andrews ML.Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction.N Engl J Med 2002;346:877–883.279. Diercks DB, Roe MT, Mulgund J, Pollack CV Jr., Kirk JD, Gibler WB, Ohman EM, Smith SC Jr., Boden WE, PetersonED. The obesity paradox in non-ST-segment elevation acute coronary syndromes: results from the CanRapid risk stratification of Unstable angina patients Suppress ADverse outcomes with Early implementation ofthe American College of Cardiology/American Heart Association Guidelines Quality Improvement Initiative.Am Heart J 2006;152:140–148.280. Steinberg BA, Cannon CP, Hernandez AF, Pan W, Peterson ED, Fonarow GC. Medical therapies and invasivetreatments for coronary artery disease by body mass: the ‘obesity paradox’ in the Get With The Guidelines database.Am J Cardiol 2007;100:1331–1335.281. Ong P, Athanasiadis A, Borgulya G, Voehringer M, Sechtem U. 3-Year follow-up of patients with coronary arteryspasm as cause of acute coronary syndrome: the CASPAR (coronary artery spasm in patients with acutecoronary syndrome) study follow-up. J Am Coll Cardiol 2011;57:147–152.282. Hasin T, Sorkin A, Markiewicz W, Hammerman H, Aronson D. Prevalence and prognostic significance of transient,persistent, and new-onset anemia after acute myocardial infarction. Am J Cardiol 2009;104:486–491.283. Bassand JP, Afzal R, Eikelboom J, Wallentin L, Peters R, Budaj A, Fox KA, Joyner CD, Chrolavicius S, GrangerCB, Mehta S, Yusuf S. Relationship between baseline haemoglobin and major bleeding complications in acutecoronary syndromes. Eur Heart J 2010;31:50–58.284. Chase AJ, Fretz EB, Warburton WP, Klinke WP, Carere RG, Pi D, Berry B, Hilton JD. Association of the arterialaccess site at angioplasty with transfusion and mortality: the M.O.R.T.A.L study (Mortality benefit Of ReducedTransfusion after percutaneous coronary intervention via the Arm or Leg). Heart 2008;94:1019–1025.285. Agostoni P, Biondi-Zoccai GG, de Benedictis ML, Rigattieri S, Turri M, Anselmi M, Vassanelli C, Zardini P, LouvardY, Hamon M. Radial versus femoral approach for percutaneous coronary diagnostic and interventional procedures;systematic overview and meta-analysis of randomized trials. J Am Coll Cardiol 2004;44:349–356.286. Alexander KP, Chen AY, Wang TY, Rao SV, Newby LK, LaPointe NM, Ohman EM, Roe MT, Boden WE, HarringtonRA, Peterson ED. Transfusion practice and outcomes in non-ST-segment elevation acute coronary syndromes.Am Heart J 2008;155:1047–1053.287. Hill SR, Carless PA, Henry DA, Carson JL, Hebert PC, McClelland DB, Henderson KM. Transfusion thresholdsand other strategies for guiding allogeneic red blood cell transfusion. Cochrane Database Syst Rev2002;2:CD002042.288. Mehran R, Rao SV, Bhatt DL, Gibson CM, Caixeta A, Eikelboom J, Kaul S, Wiviott SD, Menon V, Nikolsky E, SerebruanyV, Valgimigli M, Vranckx P, Taggart D, Sabik JF, Cutlip DE, Krucoff MW, Ohman EM, Steg PG, White H.Standardized bleeding definitions for cardiovascular clinical trials: a consensus report from the Bleeding AcademicResearch Consortium (BARC). Circulation 2011;123:2736–2747.289. Fox KA, Carruthers K, Steg PG, Avezum A, Granger CB, Montalescot G, Goodman SG, Gore JM, Quill AL,Eagle KA. Has the frequency of bleeding changed over time for patients presenting with an acute coronary syndrome?The global registry of acute coronary events. Eur Heart J 2010;31:667–675.290. Eikelboom JW, Mehta SR, Anand SS, Xie C, Fox KA, Yusuf S. Adverse impact of bleeding on prognosis in patientswith acute coronary syndromes. Circulation 2006;114:774–782.291. Budaj A, Eikelboom JW, Mehta SR, Afzal R, Chrolavicius S, Bassand JP, Fox KA, Wallentin L, Peters RJ, GrangerCB, Joyner CD, Yusuf S. Improving clinical outcomes by reducing bleeding in patients with non-ST-elevationacute coronary syndromes. Eur Heart J 2009;30:655–661.292. Mehran R, Pocock SJ, Stone GW, Clayton TC, Dangas GD, Feit F, Manoukian SV, Nikolsky E, Lansky AJ, KirtaneA, White HD, Colombo A, Ware JH, Moses JW, Ohman EM. Associations of major bleeding and myocardialinfarction with the incidence and timing of mortality in patients presenting with non-ST-elevation acute coronarysyndromes: a risk model from the ACUITY trial. Eur Heart J 2009;30:1457–1466.293. Antman EM, Wiviott SD, Murphy SA, Voitk J, Hasin Y, Widimsky P, Chandna H, Macias W, McCabe CH, BraunwaldE. Early and late benefits of prasugrel in patients with acute coronary syndromes undergoing percutaneouscoronary intervention: a TRITON-TIMI 38 (TRial to Assess Improvement in Therapeutic Outcomes byOptimizing Platelet InhibitioN with Prasugrel-Thrombolysis In Myocardial Infarction) analysis. J Am Coll Cardiol2008;51:2028–2033.294. Berger PB, Bhatt DL, Fuster V, Steg PG, Fox KA, Shao M, Brennan DM, Hacke W, Montalescot G, Steinhubl SR,Topol EJ. Bleeding complications with dual antiplatelet therapy among patients with stable vascular disease orrisk factors for vascular disease: results from the Clopidogrel for High Atherothrombotic Risk and IschemicStabilization, Management, and Avoidance (CHARISMA) trial. Circulation 2010;121:2575–2583.295. Sorensen R, Hansen ML, Abildstrom SZ, Hvelplund A, Andersson C, Jorgensen C, Madsen JK, Hansen PR,Kober L, Torp-Pedersen C, Gislason GH. Risk of bleeding in patients with acute myocardial infarction treatedwith different combinations of aspirin, clopidogrel, and vitamin K antagonists in Denmark: a retrospectiveanalysis of nationwide registry data. Lancet 2009;374:1967–1974. 296. Joyner CD, Peters RJ, Afzal R, Chrolavicius S, Mehta SR, Fox KA, Granger CB, Franzosi MG, Flather M, BudajA, Bassand JP, Yusuf S. Fondaparinux compared to enoxaparin in patients with acute coronary syndromeswithout ST-segment elevation: outcomes and treatment effect across different levels of risk. Am Heart J2009;157:502–508.297. Spencer FA, Moscucci M, Granger CB, Gore JM, Goldberg RJ, Steg PG, Goodman SG, Budaj A, FitzGerald G,Fox KA. Does comorbidity account for the excess mortality in patients with major bleeding in acute myocardialinfarction? Circulation 2007;116:2793–2801.298. Rao SV, Jollis JG, Harrington RA, Granger CB, Newby LK, Armstrong PW, Moliterno DJ, Lindblad L, Pieper K,Topol EJ, Stamler JS, Califf RM. Relationship of blood transfusion and clinical outcomes in patients with acutecoronary syndromes. JAMA 2004;292:1555–1562.299. Alexander KP, Peterson ED. Minimizing the risks of anticoagulants and platelet inhibitors. Circulation2010;121:1960–1970.300. Marso SP, Amin AP, House JA, Kennedy KF, Spertus JA, Rao SV, Cohen DJ, Messenger JC, Rumsfeld JS. Associationbetween use of bleeding avoidance strategies and risk of periprocedural bleeding among patients undergoingpercutaneous coronary intervention. JAMA 2010;303:2156–2164.301. Yank V, Tuohy CV, Logan AC, Bravata DM, Staudenmayer K, Eisenhut R, Sundaram V, McMahon D, Olkin I,McDonald KM, Owens DK, Stafford RS. Systematic review: benefits and harms of in-hospital use of recombinantfactor VIIa for off-label indications. Ann Intern Med 2011;154:529–540.302. Hebert PC, Wells G, Blajchman MA, Marshall J, Martin C, Pagliarello G, Tweeddale M, Schweitzer I, Yetisir E.A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. Transfusion Requirementsin Critical Care Investigators, Canadian Critical Care Trials Group. N Engl J Med1999;340:409–417.303. Singh AK, Szczech L, Tang KL, Barnhart H, Sapp S, Wolfson M, Reddan D. Correction of anemia with epoetinalfa in chronic kidney disease. N Engl J Med 2006;355:2085–2098.304. Menzin J, Wygant G, Hauch O, Jackel J, Friedman M. One-year costs of ischemic heart disease among patientswith acute coronary syndromes: findings from a multi-employer claims database. Curr Med Res Opin2008;24:461–468.305. Smith SC Jr., Allen J, Blair SN, Bonow RO, Brass LM, Fonarow GC, Grundy SM, Hiratzka L, Jones D, KrumholzHM, Mosca L, Pasternak RC, Pearson T, Pfeffer MA, Taubert KA. AHA/ACC guidelines for secondary preventionfor patients with coronary and other atherosclerotic vascular disease: 2006 update: endorsed by the NationalHeart, Lung, and Blood Institute. Circulation 2006;113:2363–2372.306. Chow CK, Jolly S, Rao-Melacini P, Fox KA, Anand SS, Yusuf S. Association of diet, exercise, and smoking modificationwith risk of early cardiovascular events after acute coronary syndromes. Circulation2010;121:750–758.307. Chew DP, Huynh LT, Liew D, Astley C, Soman A, Brieger D. Potential survival gains in the treatment of myocardialinfarction. Heart 2009;95:1844–1850.308. Ford ES, Ajani UA, Croft JB, Critchley JA, Labarthe DR, Kottke TE, Giles WH, Capewell S. Explaining the decreasein U.S. deaths from coronary disease, 1980–2000. N Engl J Med 2007;356:2388–2398.309. Dagenais GR, Pogue J, Fox K, Simoons ML, Yusuf S. Angiotensinconverting-enzyme inhibitors in stable vasculardisease without left ventricular systolic dysfunction or heart failure: a combined analysis of three trials.Lancet 2006;368:581–588.310. Danchin N, Cucherat M, Thuillez C, Durand E, Kadri Z, Steg PG. Angiotensinconverting enzyme inhibitors inpatients with coronary artery disease and absence of heart failure or left ventricular systolic dysfunction: anoverview of long-term randomized controlled trials. Arch Intern Med 2006;166:787–796.311. Yusuf S, Teo KK, Pogue J, Dyal L, Copland I, Schumacher H, Dagenais G, Sleight P, Anderson C. Telmisartan,ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008;358:1547–1559.312. Hulten E, Jackson JL, Douglas K, George S, Villines TC. The effect of early, intensive statin therapy on acute coronarysyndrome: a meta-analysis of randomized controlled trials. Arch Intern Med 2006;166:1814–1821.313. Cannon CP, Braunwald E, McCabe CH, Rader DJ, Rouleau JL, Belder R, Joyal SV, Hill KA, Pfeffer MA, Skene AM.Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med2004;350:1495–1504.314. Lopez-Sendon J, Swedberg K, McMurray J, Tamargo J, Maggioni AP, Dargie H, Tendera M, Waagstein F, KjekshusJ, Lechat P, Torp-Pedersen C. Expert consensus document on beta-adrenergic receptor blockers. Eur HeartJ 2004;25:1341–1362.315. Pfeffer MA, Braunwald E, Moye LA, Basta L, Brown EJ Jr., Cuddy TE, Davis BR, Geltman EM, Goldman S, FlakerGC, Klein M, Lamas GA, Packer M, Rouleau J, Rouleau JL, Rutherford J, Wertheimer JH, Hawkins CM. Effectof captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction.Results of the survival and ventricular enlargement trial. The SAVE Investigators. N Engl J Med1992;327:669–677.316. Torp-Pedersen C, Kober L. Effect of ACE inhibitor trandolapril on life expectancy of patients with reduced leftventricularfunction after acute myocardial infarction. TRACE Study Group. Trandolapril Cardiac Evaluation.Lancet 1999;354:9–12.317. Pfeffer MA, McMurray JJ, Velazquez EJ, Rouleau JL, Kober L, Maggioni AP, Solomon SD, Swedberg K, Van deWerf F, White H, Leimberger JD, Henis M, Edwards S, Zelenkofske S, Sellers MA, Califf RM. Valsartan, captopril,or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N EnglJ Med 2003;349:1893–1906.318. Fox KA, Steg PG, Eagle KA, Goodman SG, Anderson FA Jr., Granger CB, Flather MD, Budaj A, Quill A, GoreJM. Decline in rates of death and heart failure in acute coronary syndromes, 1999–2006. JAMA2007;297:1892–1900.319. Fox K, Garcia MA, Ardissino D, Buszman P, Camici PG, Crea F, Daly C, De Backer G, Hjemdahl P, Lopez-SendonJ, Marco J, Morais J, Pepper J, Sechtem U, Simoons M, Thygesen K, Priori SG, Blanc JJ, Budaj A, Camm J,Dean V, Deckers J, Dickstein K, Lekakis J, McGregor K, Metra M, Osterspey A, Tamargo J, Zamorano JL. Guidelineson the management of stable angina pectoris: executive summary: the Task Force on the Managementof Stable Angina Pectoris of the European Society of Cardiology. Eur Heart J 2006;27:1341–1381.320. Rahimi K, Watzlawek S, Thiele H, Secknus MA, Hayerizadeh BF, Niebauer J, Schuler G. Incidence, time course,and predictors of early malignant ventricular arrhythmias after non-ST-segment elevation myocardial infarctionin patients with early invasive treatment. Eur Heart J 2006;27:1706–1711.
Цели вторичной профилактики после ОКС/ИМ без подъема сегмента ST



