СИСТЕМНАЯ СКЛЕРОДЕРМИЯ (ССД)
Ирина Александровна Зборовская – д.м.н., профессор, профессор кафедры госпитальной терапии с курсом клинической ревматологии факультета усовершенствования врачей Волгоградского государственного медицинского университета, директор Федерального Бюджетного Государственного Учреждения «Научно-исследовательский институт клинической и экспериментальной ревматологии» РАМН, руководитель регионального Центра по проблемам остеопороза, член президиума Ассоциации ревматологов России, член редакционных советов журналов «Научно – практическая ревматология» и «Современная ревматология»
Определение
ССД – тяжёлое системное заболевание из группы диффузных заболеваний соединительной ткани. Характеризуется генерализованным, дегенеративно-склеротическим изменением соединительной ткани с облитерацией мелких сосудов, своеобразным поражением кожи (фиброз), опорно-двигательного аппарата, внутренних органов, вазоспастическими нарушениями типа синдрома Рейно.
Эпидемиология
I. Системная склеродермия распространена повсеместно и поражает представителей всех рас. У детей и молодых мужчин она бывает редко. С возрастом заболеваемость ею увеличивается, достигая максимума к 20 — 40 годам. Женщины болеют в 3 раза чаще, а женщины детородного возраста — в 15 раз чаще, чем мужчины. Чаще и тяжелее всех болеют молодые негритянки.
II. Распространенность заболевания, по данным разных исследований, колеблется от 19 до 75 случаев на 100 000 человек. Не исключено, что на самом деле распространенность и заболеваемость несколько выше, поскольку на ранних стадиях и при атипичном течении системная склеродермия нередко остается недиагностированной. Роль генетических факторов неясна.
III. О наследственной предрасположенности свидетельствуют семейные случаи заболевания, а также повышенная распространенность других заболеваний соединительной ткани и частое выявление аутоантител у родственников больных системной склеродермией. Однако у супругов больных тоже нередко выявляют антинуклеарные антитела, следовательно, факторы окружающей среды также имеют патогенетическое значение. Хотя иммуногенетические исследования не выявили четкой связи между НLА и системной склеродермией, существуют данные о том, что ее риск повышен у носителей НLА-DR1, НLА-DR2, HLA-DR3, HLA-DR5, HLA-DQA2 и нулевого аллеля гена С4А. Кроме того, обнаружена связь между НLА и выработкой аутоантител, характерных для системной склеродермии.
Этиология
В этиологии заболевания могут иметь значение:
- вирусы;
- токсины;
- факторы окружающей среды (длительный контакт с поливинилхлоридом, кремниевой пылью);
- ЛС (блеомицин, L-триптофан) и продукты питания (“испанское токсическое масло”).
1. Большую роль в развитии системной склеродермии и склеродермических состояний играют факторы внешней среды. Показано, например, что риск системной склеродермии повышен у шахтеров и строителей, особенно у тех, кто работает уже давно. Это говорит о том, что предрасполагающим фактором может быть контакт с кремниевой пылью.
2. Частый контакт с поливинилхлоридом может приводить к синдрому Рейно, акроостеолизу, поражению кожи и изменениям капилляров ногтевых валиков, напоминающим склеродермию, а также к фиброзу печени и гемангиосаркоме.
3. К развитию склеродермии может приводить контакт с такими веществами, как винилхлорид, эпоксидные смолы, ароматические углеводороды (например, бензол и толуол).
4. В 1981 г. в Испании было зарегистрировано около 20 000 случаев заболевания, напоминающего системную склеродермию, причиной которого послужило употребление в пищу фальсифицированного рапсового масла. Заболевание начиналось с интерстициального пневмонита, эозинофилии, артралгии, артрита и миозита, а потом развивались контрактуры суставов, утолщение кожи, синдром Рейно, легочная гипертензия, синдром Шегрена и акроостеолиз.
5. Применение наркотического анальгетика пентазоцина может приводить к выраженному фиброзу дермы и подкожной клетчатки, а лечение противоопухолевым препаратом блеомицином – к появлению фиброзных узлов и гиперпигментированных полос на коже, алопеции, гангрене пальцев и пневмосклерозу с преимущественным поражением нижних долей легких.
6. Описаны случаи склеродермии и других заболеваний соединительной ткани у женщин с силиконовыми протезами молочных желез. Однако данные об этиологической роли силикона пока неубедительны. Известно лишь, что вокруг протезов может развиться фиброз. Прием определенных препаратов триптофана послужил причиной синдрома эозинофилии-миалгии, также напоминающего системную склеродермию.
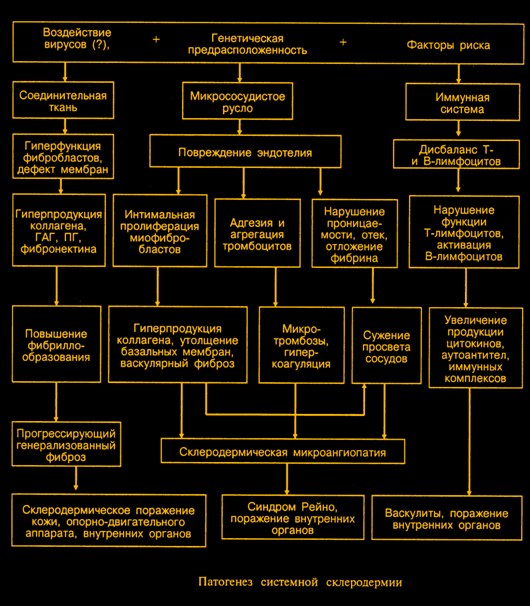
Патогенез
I.Основные этапы патогенеза
1. Вне зависимости от природы этиологического фактора локализация первичных повреждений – эндотелий сосудов, особенно малых.
1) На самых ранних стадиях болезни развивается гиперплазия интимы небольших сосудов.
2) Сужение просвета сосудов приводит к ишемии тканей.
3) Физиологические вазоконстрикторные стимулы (холод, эмоции, тромбоксан А2, серотонин) вызывают дальнейшее сужение сосудов и формирование феномена Рейно в коже и внутренних органах.
4) При поражении сосудов почек стимуляция ренинангиотензинового механизма приводит к порочному кругу вазоконстрикции, что считают причиной почечных кризов при ССД.
2. Инфильтрация пораженной кожи активированными (экспрессирующими DR антиген) Т-лимфоцитами.
3. Синтез цитокинов (ИЛ-1, ИЛ-4, ИЛ-6 и др.)
4. Пролиферация фибробластов и синтез коллагена типа I и III.
5. Высвобождение из тромбоцитов тромбоцитарного фактора роста и трансформирующего фактора роста — В.
6. Селекция популяции фибробластов, устойчивых к апоптозу и функционирующих в автономном режиме максимальной синтетической активности.
7. Активация тучных клеток, синтезирующих триптазу (активирует трансформирующий фактор роста – бета), выделение гистамина (стимулирует пролиферацию фибробластов и синтез компонентов матрикса) и эозинофильного катионного белка. Не исключено, что в некоторых случаях развитие ССД является своеобразным проявлением хронической реакции трансплантата против хозяина, что подтверждается:
- развитием “склеродермоподобных” проявлений у некоторых пациентов после пересадки костного мозга,
- длительная персистенция после рождения ребенка в организме женщин, у которых в последующем развивалась ССД, клеток плода (“фетальный микрохимеризм”). Развитие феномена Рейно определяется сложным иммунологически обусловленным взаимодействием:
- эндотелиальных медиаторов (оксид азота, эндотелин-1, простагландины),
- тромбоцитарных медиаторов (серотонин, бета-тромбоглобулин),
- нейропептидов (пептид, связанный с геном кальцитонина; вазоактивный интестинальный полипептид).
8. Разрегулированный иммунный процесс приводит к хронизации сосудистых поражений и возникает распространённый фиброз кожи и внутренних органов.
1) Фиброз тканей может быть результатом компенсаторных механизмов в ответ на повреждение интимы или иммуноопосредованной повышенной активности фибробластов с повышенной выработкой коллагена.
Поражение чувствительных нервов также способствует спазму сосудов, поскольку приводит к дефициту сосудорасширяющих нейропептидов.
У многих больных поражение эндотелия сопровождается повышением уровня фактора свертывания VIII и фактора фон Виллебранда в сыворотке. Связывание фактора фон Виллебранда с субэндотелиальным слоем способствует активации тромбоцитов, выбросу веществ, повышающих проницаемость сосудов, и развитию отека.
2) Цитокины и факторы роста, секретируемые лимфоцитами, моноцитами и тромбоцитами (например, фактор роста из тромбоцитов, трансформирующий фактор роста В), приводят к гиперпродукции коллагена и макромолекул основного вещества соединительной ткани с последующим развитием участков фиброза.
Повреждение эндотелия и недостаточность тканевого активатора плазминогена способствуют внутрисосудистому свертыванию крови и в тяжелых случаях могут приводить к микроангиопатической гемолитической анемии, которая сопряжена с высоким риском ОПН.
II. Существуют данные о важной роли нарушений клеточного иммунитета в развитии фиброза при системной склеродермии. Так, при биопсии на первый взгляд здоровой кожи вокруг очагов склероза обнаруживают ее периваскулярную и диффузную инфильтрацию, преимущественно Т-лимфоцитами и макрофагами. Т-лимфоциты представлены в основном Т-хелперами. Повышение уровня ИЛ-2, свободных рецепторов ИЛ-2, свободных молекул СD4 и активности аденозиндезаминазы в сыворотке больных свидетельствует об активации Т-хелперов. Кроме того, повышенный уровень ИЛ-2 и свободных рецепторов ИЛ-2 на ранних стадиях заболевания — признак его прогрессирования. В сыворотке больных обнаруживают также ИЛ-4 и ИЛ-6. ИЛ-4, вырабатываемый активированными Т-хелперами и тучными клетками, стимулирует пролиферацию фибробластов и синтез коллагена, а также усиливает адгезию Т-лимфоцитов к эндотелию. Взаимодействуя с фибробластами, Т-лимфоциты могут секретировать цитокины, стимулирующие фиброз.
В исследованиях in vitro показано, что компоненты базальной мембраны сосудов — ламинин и коллаген IV типа — вызывают пролиферацию Т-лимфоцитов больных системной склеродермией. Эти данные говорят о том, что базальная мембрана сосудов может служить мишенью клеточных иммунных реакций, развивающихся при этом заболевании. Определенную роль в патогенезе заболевания играют молекулы адгезии, опосредующие взаимодействие Т-лимфоцитов с эндотелием.
Кроме того, в сыворотке больных повышаются уровни ИЛ-1 и ФНО-альфа, что может свидетельствовать об активации моноцитов. Наряду с множеством других функций эти цитокины обладают способностью активировать фибробласты. Еще одно подтверждение важной роли клеточного иммунитета в патогенезе заболевания — сходство кожных проявлений системной склеродермии и хронической реакции «трансплантат против хозяина», которая, как известно, опосредована активированными Т-лимфоцитами. В развитии фиброза кожи могут также участвовать тучные клетки; об этом говорит их повышенное содержание в дерме, как очаге поражения, так и за его пределами. При этом показано, что в участках кожи, содержащих дегранулированные тучные клетки, впоследствии развивается фиброз. Одной из причин дегрануляции тучных клеток может быть их взаимодействие с активированными Т-лимфоцитами. Некоторые медиаторы тучных клеток стимулируют синтез коллагена фибробластами, а другие, например гистамин, вызывают отек кожи на ранних стадиях заболевания.
III. У больных системной склеродермией нарушен не только клеточный, но и гуморальный иммунитет. Так, примерно у 95% из них в сыворотке присутствуют антинуклеарные антитела, у некоторых больных обнаруживают также антитела к ламинину и коллагену IV типа. Однако роль аутоантител в патогенезе заболевания пока не ясна.
По-видимому, при системной склеродермии нарушены механизмы регуляции роста фибробластов и синтеза ими коллагена, фибронектина и гликозаминогликанов.
IV. Имеется семейно-генетическое предрасположение: в семьях больных ССД у родственников отмечается синдром Рейно, реже — ССД и другие ревматические болезни. При хроническом течении имеется связь с НLА антигеном DR3, при подострой — с DR5.
Недавно был идентифицирован мутантный ген, детерминирующий синтез фибронектина фибробластами пораженной кожи больных ССД, однако роль фибронектина в патологическом процессе неясна.
В культуре фибробластов, выделенных из пораженных участков кожи, продолжается избыточный синтез коллагена. При этом структура коллагена и соотношение коллагена I и III типов остаются такими же, как и в здоровой коже. Полагают, что значительная часть фибробластов больных все время находится в состоянии активации, скорее всего обусловленной действием цитокинов. Этим фибробластам свойственна повышенная экспрессия генов, кодирующих белки межклеточного вещества. Показано, что при системной склеродермии некоторые фибробласты вырабатывают в 2—3 раза больше коллагена, чем остальные.
В норме коллаген VII типа служит основным компонентом крепящих фибрилл, стабилизирующих связь между эпидермисом и дермой. У больных системной склеродермией коллаген VII типа располагается по всей толще дермы. Возможно, именно поэтому кожа, у них уплотнена и спаяна с глубжележащими тканями.
Более чем у 90% больных системной склеродермией возникают хромосомные аномалии; эти аномалии обнаруживают примерно в 30% клеток в митозе. В сыворотке больных и их близких родственников обнаружены вещества, вызывающие разрывы хромосом в культивируемых нормальных клетках. Однако роль хромосомных аномалий в патогенезе заболевания пока не ясна.
КЛИНИЧЕСКАЯ КЛАССИФИКАЦИЯ СИСТЕМНОЙ СКЛЕРОДЕРМИИ (Гусева Н.Г., 1994)
| Характер течения | Стадия развития | Степень активности | Клинико-морфологическая характеристика поражений | ||||||
| кожи и перифери-ческих сосудов | локомо-торного аппарата | сердца | легких | пищеварительного тракта | почек | нервной системы | |||
| Острое
Подострое
Хроничес-кое |
I (начальная)
II (генера-лизован-ная) III (терми-нальная) |
I (мини-мальная)
II (умерен-ная)
III (высокая) |
Плотный отёк, индурация, атрофия, гиперпигментация, телеангиоэктазии, синдром Рейно, очаговое поражение | Артралгии, полиартрит (экссудативный или фиброзно-индуративный), псевдоартрит, полимиозит, кальциноз, остеолиз | Миокардоз, кардиосклероз, порок сердца (чаще недостаточность митрального клапана) | Интерстициальная пневмония, пневмосклероз (компактный или кистозный), адгезивный плеврит) | Эзофагит, дуоденит, колит, спруподобный синдром | Истинная склеродермическая почка, хроничес-кий диффузный нефрит, очаговый нефрит | Полиневрит, нейропсихические расстройства, вегетативные сдвиги |
Клинические формы
С очаговым поражением кожи; Преимущественно висцеральная; Суставная; Мышечная; Сосудистая |
|||||||||
Классификация
I. По течению: острое, подострое и хроническое.
Они отличаются друг от друга активностью и быстротой прогрессирования процесса, степенью выраженности и характером “периферических” и висцеральных проявлений в большинстве случаев различием лабораторных и морфологических тестов.
1. Острое течение.
1) Острое течение отличается быстрым прогрессированием как поражений кожи, так и особенно внутренних органов: лёгких (интерстициальные пневмонии с исходом в пневмосклероз), сердца (с формированием кардиосклероза), почек (по типу “истинной склеродермической почки”).
2) Как правило, увеличение СОЭ, повышение содержания оксипролина в плазме и моче, фибриногена и a2 -глобулинов, а также иммунологические сдвиги (гипергаммаглобулинемия, наличие ревматоидного и антиядерного факторов, волчаночных клеток).
3) Летальный исход наступает уже в первый год заболевания, чаще от прогрессирующей почечной недостаточности.
2. Подострое течение.
1) При подостром течении заболевание развивается более постепенно.
2) Наблюдаются поражения кожи с её плотным отёком и последующей индурацией, рецидивирующий полиартрит, миозит с миастеническим синдромом.
3) Поражения внутренних органов. Интерстициальные пневмонии с постепенным развитием пневмофиброза, серозиты, эзофагит, хроническая нефропатия. Нередки перекрестные синдромы. Преобладает также высокая воспалительная и иммунологическая активность.
4) Вазомоторные трофические нарушения.
3. Хроническое течение.
1) Для наиболее известного хронического течения характерныпрогрессирующие вазомоторные нарушения по типу синдрома Рейно и обусловленные им выраженные трофические расстройства, которые нередко являются единственным признаком заболевания на протяжении ряда лет и в дальнейшем превалируют в картине болезни.
2) Постепенно развивается наряду с этим уплотнение кожи и периартикулярных тканей с образованием контрактур, остеолизом.
3) Характерны медленно прогрессирующие склеротические изменения внутренних органов (пищевода, легких, сердца) , иногда CREST –синдром.
4) Лабораторные тесты остаются в пределах нормы или близки к ней, за исключением умеренной гипергаммаглобулинемии, гиперпротеинемии, наличия антинуклеарных антител (антицентромерных ).
II По степени активности.
- 1. Максимальная ( IIIстепень ).
1) Свойственна острому и подострому вариантам течения заболевания.
2) Выраженное поражение кожи, полисерозиты.
3) Температура – 37,5-38° С и выше.
4) Лабораторные данные.
– СОЭ – 35 мм/час и выше.
– Фибриноген – 0,6 и выше.
– Общий белок – 9 г% и выше.
– a2-глобулин свыше 30.
– СРП – ++++ .
- 2. Умеренная (II степень ).
1) Температура – 37,5 – 38° С.
2) Экссудативный полиартрит. Интерстициальная пневмония
3) Отек кожи.
4) Склеротические изменения внутренних органов.
5) Лабораторные данные.
– СОЭ – 35 мм-час.
– Фибриноген – 0,5 – 0,6.
– Увеличение общего белка до 9 г%.
– СРП – ++ , +++.
3. Минимальная (I степень ).
1) I степень активности в основном свойственна хроническому течению.
2) Температура – до 37° С.
3) Атрофия кожи.
4) Фиброзно-индуративные изменения в суставах, псевдоартроз, артралгии.
5) Лабораторные данные.
– СОЭ – 15мм/час и менее
– Фибриноген – до 0,5
– Общий белок – до 8 г%
– СРП – + или –
Необходимо также отметить, что на фоне проводимой терапии степень активности заболевания изменяется от большей к меньшей.
III. По стадиям
1-я стадия. Это стадия начальных проявлений (Синдром Рейно, полиартралгии, артрит, реже кожные, висцеральные или общие проявления).
2-я стадия. Стадия генералилизованная или диффузная (полисиндромность клинической картины).
3-я стадия. Она называется терминальной и характеризуется склеротическими, дистрофическими и сосудисто-некротическими изменениями органов с недостаточностью их функции.
IV. Выделяют следующие основные клинические формы ССД:
- Пресклеродермия.
- Диффузная кожная склеродермия.
- Лимитированная кожная склеродермия.
- Склеродермия без склеродермы.
- Перекрестный синдром.
Характеристика клинических форм
1. Пресклеродермия характеризуется сочетанием феномена Рейно со следующими признаками:
– изменениями капилляров ногтевого ложа,
– дигитальной ишемией,
– иммунологическими нарушениями, характерными для ССД.
2. Диффузная форма склеродермии (с диффузным поражением кожи).
– Быстрое прогрессирование.
– Характерно поражение кожи проксимальнее лучезапястных суставов
– Наличие антинуклеарных антител.
– Поражение внутренних органов происходит раньше, чем при акросклеротической форме.
– Чаще страдают почки, и развивается фиброз легких.
- Акросклеротическая или лимитированная форма склеродермии (с очаговым поражением кожи) – симметричное поражение кожи с ограниченным вовлечением дистальных отделов конечностей, лица и (позднее) висцеральных органов, включая частый вариант этой формы – синдром CREST.
1) Синдром CREST, назван в соответствии с начальными буквами основных его проявлений:
– подкожный кальциноз (кожа изменяется на конечностях и лице),
– феномен Рейно,
– нарушения моторики пищевода (эзофагит),
– склеродактилия,
– телеангиэктазы
2) Часто находят антицентромерные антитела.
3) Поражения внутренних органов развиваются и протекают мягче.
4) Фиброзирование легких или первичный биллиарный цирроз печени может появиться даже после нескольких десятилетий болезни.
5) Исключение – рано развивающаяся легочная гипертензия вследствие облитерации легочных артерий.
6) Системный феномен Рейно (генерализованный вазоспазм артерий, кровоснабжающих почки, сердце и, возможно, другие висцеральные органы).
4. Склеродермия без склеродермы.
Иногда ССД поражает только внутренние органы – так называемая висцеральная форма ССД. В этом случае прогноз зависит от тяжести поражения внутренних органов ( сердца, легких, почек).
5. Смешанное заболевание соединительной ткани или перекрестная форма (OVERLAP).
1) Перекрестную форму считают ревматическим синдромом.
2) который может включать в себя признаки ССД, РА, СКВ и полимиозита.
3) Обнаруживают высокие титры антител к рибонуклеопротеину.
4) Со временем в большинстве случаев происходит трансформация этого синдрома в ССД или СКВ.
РАЗЛИЧИЯ МЕЖДУ ФОРМАМИ СИСТЕМНОЙ СКЛЕРОДЕРМИИ
| Диффузная форма | Акросклеротическая формаа | |
| Поражение кожи | Дистальные и проксимальные отделы конечностей, лицо, туловище | Дистальные отделы конечностей, лицо |
| Синдром Рейно | Появляется за год до поражения кожи или одновременно с ним | Может появиться за несколько лет до поражения кожи |
| Поражения внутренних органов | Легкие, почки, ЖКТ, сердце | ЖКТ, легочная гипертензия, первичный билиарный цирроз печени |
| Капилляроскопия | Расширение капилляров и уменьшение их количества | Расширение капилляров без уменьшения их количества |
| Антинуклеарные антитела | Антитела к антигену Scl -70 | Антитела к центромерам |
а – Включая синдром CREST
Клиника
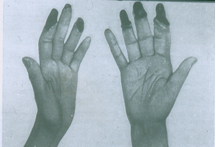
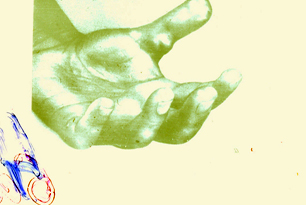
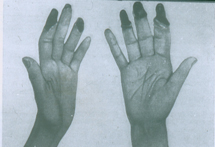
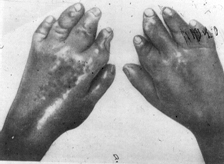
I. Поражение кожи. Находят у 95% больных.
1. Распределение поражений на коже.
1) Изменения чаще возникают на пальцах и руках, позднее распространяясь проксимально на туловище и лицо, больной ощущает чувство сдавления как бы корсетом, панцирем.
2) Поражения нижних конечностей выражены слабее.
2. Фазы поражения кожи.
1) Ранняя ( отечная ) фаза.
– Отек может быть плотным или оставляет ямку при надавливании, или эритему.
– Повышается проницаемость сосудистой стенки.
– Повреждается эндотелий мелких сосудов.
2) Индуративная фаза. Характеризуется повышенным синтезом коллагена.
3) Атрофическая фаза.
– Возникает атрофия кожи и ее придатков, ее сухость.
– Характерна «спаянность» кожи с подлежащими тканями.
3. Сопутствующие поражению кожи признаки.
1) Феномен (синдром) Рейно наблюдают у 95 % больных. Может появиться задолго до возникновения других типичных проявлений ССД, при этом его проявления бывают стертыми (зябкость кистей рук, без изменения цвета).
– Эпизодический спазм пораженных сосудов пальцев вызывает трехфазные изменения цвета кожи: при остановке кровотока – белый цвет, медленном восстановлении – синий, цианотичный, полном восстановлении – реактивная гиперемия.
– Следует подчеркнуть большую распространенность вазомоторных нарушений при ССД, чем при классическом синдроме Рейно, когда поражаются лишь пальцы.
– По мере прогрессирования приступы становятся более продолжительными и мучительно болезненными.
– При ССД вазоспастические нарушения распространяются на кисти, стопы; нередко чувство онемения и побеления отмечается и в области губ, части лица, кончика языка.
Возможна и висцеральная локализация вазоспастических нарушений (головной мозг, сердце, легкие). В межприступный период кожные покровы цианотичные, могут сохраняться парестезии и болевой синдром. В редких случаях может быть криз, приводящий к некрозу и гангрене пальцев
– Может быть спровоцирован холодом, вибрацией, волнением.
– Отсутствие феномена Рейно ассоциируется с риском поражения почек.
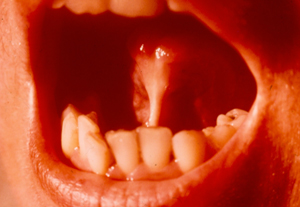
2) Телеангиэктазии возникают в коже и/или слизистых оболочках.
Это — локальное расширение капилляров и мелких сосудов, с напоминающее по форме звездочку, наблюдаются у 30% пациентов диффузной и 80% лимитированной формами ССД, появляются на поздней стадии болезни.
1) Подкожный кальциноз.
Кальцинаты могут вскрываться. Чаще появляются на концах пальцев,
локтях, коленях (R-ки – синдром Тибьержа-Вейссенбаха), т.е. в местах повторяющейся травматизации.
Может возникнуть кальциноз надгортанника,
голосовых связок, перикарда, клапанного аппарата и мышцы сердца, капсулы печени и селезенки.
4) Изменения типа «соль с перцем».
– Кожа становится натянутой, блестящей, «спаянной» с подлежащими тканями.
– Она ригидная и не собирается в складку.
– Участки гипер- и депигментации могут чередоваться и переходить один в другой.
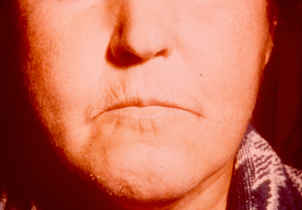
– Вследствие этих изменений меняется выражение лица, оно становится маскообразным и амимичным,
нос и уши истончены, ротовая щель сужена с “кисетообразными” морщинами вокруг, веки могут смыкаться не полностью.
5) Патология микрососудов.
– Характеризуется пролиферацией капиллярного ложа ногтевых пластин. Утолщение и расслоение базальной мембраны мышечных капилляров – характерные признаки ССД.
– Биомикроскопически определяют дилятацию, извитость и уменьшение количества функционирующих микрососудов.
– Для диагностики используют тепловидение, артериографию.
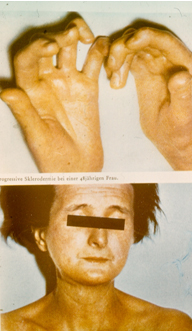
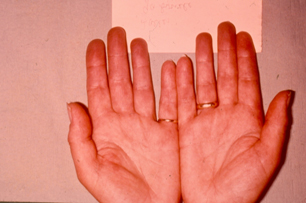
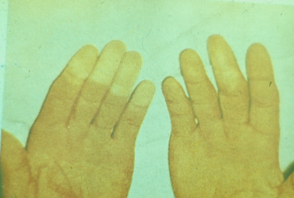
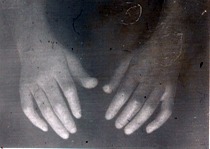
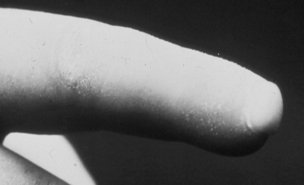
1) Характерны и изменения кистей.
– Вследствие отёка и индурации, пальцы напоминают “муляжные”.
– Кисть трудно сжать в кулак.
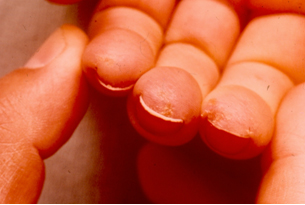
– Развивается истончение, остеолиз концевых фаланг, укорочение пальцев. По мере прогрессирования происходит рассасывание большой части ногтевых пластинок.
7) Изъязвления кожи.
Над костными выступами, но чаще всего возникает на кончиках пальцев вследствие нарушения кровообращения.
– В данном случае опасно присоединение вторичной инфекции.
– Редко могут возникать изъязвления в области ушных раковин и даже век.
8) Гиперпигментация кожи, даже в отсутствии инсоляции, чередуется с участками гипопигментации. Иногда кожа приобретает бронзовый оттенок. Волосы истончаются, нередко наблюдается алопеция.
II. Поражение ЖКТ.
Это самое частое из всех поражений внутренних органов при ССД.
Поражение ЖКТ при ССД имеет столь чётко очерченную и своеобразную клинико-рентгенологическую картину, что по своей диагностической значимости выходит на первый план среди других висцеральных проявлений ССД.
1. Дисфункция пищевода.
1) нарушения моторики пищевода и рефлюкс.
– Нарушение моторики пищевода наблюдается даже у больных, страдающих только синдромом Рейно.
– Возникают в результате замещения коллагеном гладких мышц нижней трети пищевода. Снижается тонус нижнего пищеводного сфинктера.
– Поперечно-полосатая мускулатура верхней трети пищевода обычно не повреждается. При этом определяется снижение амплитуды или полное отсутствие перистальтики нижней трети пищевода.
– Характеризуется картиной своеобразного рефлюкс – эзофагита, который проявляется: дисфагией, нарушением глотания твёрдой и даже жидкой пищи, болезненными срыгиваниями, жжение в эпигастрии и за грудиной.
– Дисфагия (особенно при глотании твердой пищи) может возникать в отсутствие других симптомов поражения пищевода. Её причиной служит снижение моторики пищевода, обусловленное нервно – мышечными нарушениями.
2) Стриктуры пищевода.
– Возникают вследствие постоянного рефлюкса.
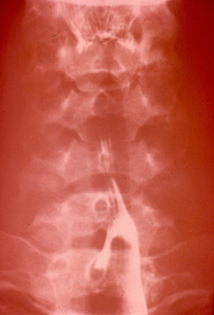
При этом рентгенологически в положении больного лёжа отмечают значительное расширение пищевода в верхних отделах и сужение в нижней трети, значительную задержку пассажа бариевой взвеси по пищеводу, замедление перистальтики
В зависимости от выраженности симптомов нарушений перистальтики и тонуса пищевода выделяют три степени склеродермического поражения пищевода, отражающее эволюцию патологического процесса:
I степень – умеренная, характеризующая незначительным замедлением продвижения бария сульфата от краниального до каудального отдела пищевода.
II степень – выраженная, характеризующая отчетливым замедлением продвижения бария по пищеводу, длительной задержкой взвеси бария в пищеводе, зиянием, расширением просвета пищевода, изменением рельефа слизистой оболочки.
III степень – максимальная, характеризуется значительным замедлением, вплоть до прекращения, продвижения бария, длительной его задержкой в пищеводе, выраженным расширением просвета пищевода, изменением рельефа слизистой оболочки, признаками рефлюкс – эзофагита и его вторичных осложнений.
3) Язвы пищевода.
Чаще всего образуются в месте соединения пищевода с желудком. Иногда могут привести к кровотечению из пищевода.
Кроме того, рефлюкс – эзофагит может стать причиной цилиндроклеточной метаплазии эпителия пищевода, однако, аденокарцинома при этом развивается редко. Иногда – склероз уздечки языка.
2. Поражение желудка.
R-ки проявляется его расширением, атонией и замедленными опорожнениями.
3. Изменения в кишечнике – подобны изменению в пищеводе.
1) Признаки склеродермического дуоденита: нарушение моторики кишечника, спазмы, диарея, боли.
Боли иногда настолько сильные, что больному ставят диагноз механической или паралитической кишечной непроходимости.
2) Синдром нарушения всасывания и бактериального роста.
– Это происходит при преимущественном поражении тонкого кишечника – спруподобный синдром (похудание, понос, анемия).
– При поражении толстого кишечника – упорные запоры, иногда с признаками частичной рецидивирующей непроходимости, саккуляции.
– Атония какого-либо участка кишки может привести к инвагинации.
– Снижение тонуса внутреннего сфинктера заднего прохода может приводить к недержанию кала и изредка – к выпадению прямой кишки. Инфаркты, язвы, некроз, перфорация.
3) Дивертикулы.
Могут возникать дивертикулы поперечной ободочной и нисходящей кишок. У некоторых больных развивается кистозный пневматоз кишечника, при этом на R-ах в стенке тонкой кишки видны округлые или линейные просветления. При разрыве кист может развиться пневмоперитонеум без признаков перитонита.
Телеангиэктазии желудка и кишечника могут стать источником желудочно-кишечного кровотечения.
Для диагностики используют контрастную рентгенографию и исследование всасывающей способности кишечника.
При R-контрастном исследовании выявляют расширение нисходящей и горизонтальной частей 12-перстной и тощей кишок, сглаживание круговых складок и замедление пассажа бариевой взвеси. При R-контрастном исследовании толстой кишки иногда выявляют ее расширение и атонию, а также дивертикулы с широким устьем.
4. Первичный биллиарный цирроз печени
При акросклеротической форме ССД иногда развивается первичный биллиарный цирроз печени (гепатомегалия, гепатолиенальный синдром).
III. Поражение слизистых оболочек.
При ССД нередко наблюдается поражение слизистых оболочек по типу синдрома Шегрена. При этом вследствие хронического воспалительного процесса преимущественно в экзокринных железах развивается их секреторная недостаточность: увеличение околоушных слюнных желез (фиброз), сухость слизистых оболочек глаз (ксерофтальмия), рта (ксеростомия), склеродермическая пародонтонатия, трахеи и бронхов, желудка, влагалища, кожи.
IV. Поражение эндокринных желез.
1. Часто развивается гипотиреоз, которому может сопутствовать резкое повышение уровня антитиреоидньгх антител в сыворотке. Причиной гипотиреоза может быть не только хронический лимфоцитарный тиреоидит, но и фиброз щитовидной железы. У некоторых больных развивается импотенция. Уровень тестостерона и гонадотропных гормонов у них нормальный; вероятно, причиной импотенции служат сосудистые и вегетативные нарушения.
2. Нарушение функции коры надпочечников.
При ССД нередко отмечается нарушение функции коры надпочечников, снижение или истощение функциональных резервов коры надпочечников, что, возможно, и обуславливает некоторые клинические черты аддисонизма (гипотонию, слабость, пигментацию).
3. Сахарный диабет.
При ССД может развиваться первичный и вторичный сахарный диабет, в основе которого могут лежать интерстициальный фиброз поджелудочной железы, сходство отдельных патогенетических признаков и реализация генетической предрасположенности к заболеванию. Возможна связь с иммунной и сосудистой патологией.
V. Суставы и сухожилия.
1. Суставной синдром выходит на первый план по частоте и нередко становится одним из начальных признаков заболевания (уступая в этом отношении лишь синдрому Рейно), а поэтому играет важную роль в ранней диагностике ССД.
Выделяют 3 основных его варианта:
1) Полиартралгии.
2) Склеродермический полиартрит е преобладанием экссудативно-пролиферативных или фиброэно – индуративных изменений. Более 50% больных ССД предъявляют жалобы на отёчность, скованность и боли в суставах пальцев, лучезапястных и коленных суставах. Мягкий воспалительный артрит на ранних стадиях болезни.
3) Периартрит (иногда безболевой) с развитием фиброзных контрактур, преимущественно вследствие поражения периартикулярных тканей. Типичным для ССД считают фибризирующий суставной процесс с выраженными ограничениями подвижности.
2. Сухожилия.
1) Сухожильно-мышечный синдром.
Сгибательные контрактуры – возникают вследствие поражения связок и прогрессирующего уплотнения кожи (склеродактилия и акросклероз).
2) Синдром “карпального канала”.
Теносиновит – приводит к синдрому запястного канала и иногда проявляется «шумом трения связок» при движении.
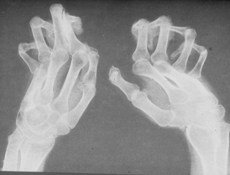
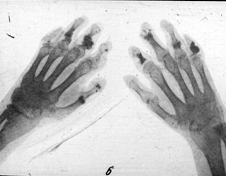
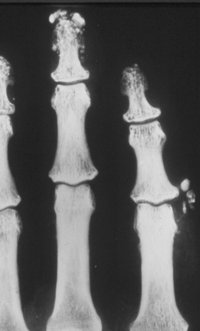
VI. Изменения костей (иногда).
- 1. Остеолиз, чаще ногтевых фаланг.
– Остеолиз обусловлен, главным образом, сосудисто-трофическими нарушениями (не исключены изменения и собственно коллагеновой матрицы кости) и проявляется клинически в виде укорочения и деформации пальцев рук и ног.
Причем, резорбции могут подвергнуться не только дистальные фаланги пальцев рук, но и ребра, ключицы и угол нижней челюсти (иногда атрофия нижней челюсти).
– Остеолиз практически не наблюдается при других коллагеновых заболеваниях и очень редок в общей патологии, что позволяет высоко оценить его диагностическое и дифференциально-диагностическое значение.
2. Остеопороз.
3. Остеосклероз.
VII. Поражения мышц.
1. При ССД поражение мышц обычно протекает в мягкой форме с незначительным повышением активности ферментов и обычно не требует специального лечения.
2. Фиброзный интерстициальный миозит
В редких случаях может возникнуть фиброзный интерстициальный миозит с развитием соединительной ткани и атрофией собственно мышечных волокон. Проявляется нарастающей мышечной слабостью, реже миалгиями.
Мышцы уплотняются, становятся ригидными, что приводит к развитию мышечно-сухожильных контрактур. Развивающиеся контрактуры столь устойчивы, что может возникнуть анкилозирование суставов, приводящее к инвалидизации больного.
3.Истинный миозит (воспалительная миопатия). Overlap-синдром.
– Возникает значительно реже.
– Первичные дегенеративные и некротические изменения в мышечных волокнах с последующим склерозом.
– Для него характерен миастенический синдром и нарушения движений, свойственные полимиозиту или дерматомиозиту, с мышечной слабостью, повышением КФК, изменениями на ЭМГ и мышечной биопсии. Поражение мышц губ, носа (нарушается мимика, дизартрия). Поражение глазных мышц (нарушается подвижность глазного яблока).
VIII. Нервы
Поражение нервной системы могут проявляться как периферическими, так и центральными нарушениями.
1. Полиневритический синдром – наиболее характерен.
1) Вторичный (ишемический).
– При выраженном синдроме Рейно и преимущественно хроническом течении заболевания.
– Невропатия за счёт ущемления срединного и тройничного нервов.
2) Истинный.
В случаях тяжёлого полиневрита преимущественно при остром и подостром течении болезни.
2.Поражение ЦНС (очень редко).
Тригиминальная сенсорная невропатия и другие краниальные невропатии наблюдаются при лимитированной форме ССД.
IX. Легкие
Характер поражения легких при ССД сложен и включает по крайней мере 4 компонента:
1. Интерстициальный фиброз или фиброзирующий альвеолит с преимущественным поражением нижних отделов легких.
2. Изменения по типу «болезни малых дыхательных путей». Диффузный фиброз легких (компактного или кистозного типа) чаще развивается в первые 5 лет заболевания при диффузной форме.
3. Патология (функциональная и органическая) сосудистого ложа легких с развитием легочной гипертензии.
4. Легочные осложнения.
Легочная гипертензия первичная или вторичная (ассоциированная с фиброзом легких). Первичная легочная гипертензия характеризуется изолированным снижением диффузионной способности легких, встречается преимущественно на поздних стадиях при лимитированной форме.
Эти изменения далеко не всегда развиваются параллельно и лишь в поздней стадии они сочетаются, углубляя тяжесть легочной патологии и состояния больных.
У большинства больных легочная патология выявляется на фоне уже развернутой картины болезни (II—III стадия), но у некоторых больных может быть первым или одним из первых проявлений ССД.
Уменьшается величина объема сосудистого ложа легких.
Утолщение альвеолярных стенок и нарушение диффузии газов через измененную мембрану.
Поражения легких отмечаются примерно у 2/3 больных.
Характерно:
1) В начале заболевания постепенное развитие фиброзирующего альвеолита и затем диффузного фиброза (компактного, реже – кистозного) с преимущественной локализацией в базальных отделах лёгких.
2) Наличие спаечного процесса и утолщение плевры.
Начальный пневмосклероз.
1. Клинические признаки пневмосклероза в начальной стадии незначительны или отсутствуют.
2. У некоторых больных (10%), однако, уже до рентгенологических признаков фиброза выявляется изолированная легочная гипертензия, которая развивается вследствие диффузного сужения просвета небольших лёгочных сосудов и фиброзных изменений в них.
Развитие легочной гипертензии обычно сопровождается изменениями на ЭКГ. Клинически она проявляется нарастающей одышкой с последующим развитием правожелудочковой недостаточности. Прогноз при легочной гипертензии крайне неблагоприятный, средняя продолжительность жизни составляет примерно 2 года.
3. Уже могут иметься функциональные изменения, поэтому рекомендуется использование этих методов исследования для ранней диагностики склеродермического пневмофиброза. Это: снижение ЖЕЛ, увеличение остаточного объема легких.
Снижение диффузионной способности легких и низкое РаО2 при физической нагрузке свидетельствуют о нарушении газообмена. При этом рентгенологических признаков поражения легких может и не быть.
4. Нередко выявляющееся у больных ССД увеличение остаточного объема легких при отсутствии признаков обструктивного или рестриктивного поражения позволяет предположить вовлечение в процесс терминальных отделов дыхательных путей, которое предшествует нарушению диффузионной способности легких (аналогичным изменениям при «болезни малых дыхательных путей» «асимптомных» курильщиков).
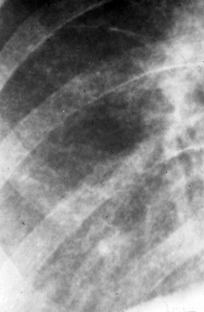
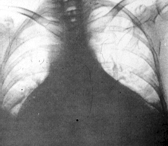
Выраженный пневмосклероз.
1. Намного чаще возникают интерстициальные поражения легких, вследствие фиброзирования перибронхиальных и периальвеолярных тканей (в основном в базальных отделах легких).
2. При выраженном пневмосклерозе развиваются бронхоэктазы, элефизема, перифокальные пневмонии, кистозный пневмосклероз (на рентгенограмме – по типу «медовых сот»).
3. Больные жалуются на прогрессирующую одышку при физической нагрузке, особенно затруднение глубокого вдоха; сухой кашель, удушье, особенно на холоде; а при исследовании функции внешнего дыхания выявляют рестриктивные изменения – один из важных диагностических признаков.
На рентгенограммах грудной клетки (особенно в средних и нижних отделах легочных полей) могут обнаруживаться линейные или множественные мелкоочаговые тени и картина сотового легкого. Для выявления ранних изменений в легких используют КТ с высоким разрешением и бронхоальвеолярный лаваж. При альвеолите в жидкости, полученной при бронхоальвеолярном лаваже, обнаруживают большое количество альвеолярных макрофагов, нейтрофилов и эозинофилов.
4. Плевриты при ССД встречаются значительно реже, чем при других ревматических заболеваниях (РА, СКВ) (слипчивый плеврит, заращение синусов, сужение плевральных полостей).
Легочные осложнения.
- Вирусные и бактериальные пневмонии.
- Разрыв субплевральных кист с развитием пневмоторакса.
- Абсцедирование
- Рак лёгких на фоне склеродермического пневмофиброза.
Необходимо отметить, что степень выраженности и тяжести пневмосклероза обусловлена в первую очередь активностью склеродермического процесса.
X. Сердце.
Поражение сердца при ССД занимает ведущее место среди висцеральных признаков склеродермии, как по частоте, так и по значимости, обусловливая в некоторых случаях смертельный исход.
1. Поражение миокарда.
Н. Г. Гусева выделяет раннюю, более обратимую фазу поражения миокарда, предшествующую развитию фиброза, когда морфологически выявляются отек, элементы воспаления и разрастание молодой рыхлой соединительной ткани, иногда участки некробиоза мышечных волокон.
Более выраженное поражение миокарда с выраженным кардиосклерозом, фиброзно-склеротическими рубцовыми изменениями мышцы сердца носят название «миокардоз» или интерстициальный миокардит.
1) Итак, в основе поражения лежат свойственные заболеванию процессы фиброзирования и склероза, усугубляющиеся нарушением микроциркуляции и приводящие к развитию некоронарогеннрго кардиосклероза с характерным увеличением сердца – застойная кардиомиопатия с нарушениями ритма, проводимости и недостаточностью кровообращения (снижение сократительной функции миокарда с зонами адинамии; при рентгенологическом исследовании).
2) Крупноочаговый фиброз миокарда обусловливает «инфарктоподобные» изменения на ЭКГ и в отдельных случаях может вести к развитию своеобразной “мозолистой” аневризмы сердца. Может возникнуть кальциноз отдельных участков мышцы сердца.
3) При фиброзном повреждении венечных артерий появляется стенокардия. Электрокардиографический мониторинг при этом позволяет выявить эпизоды ишемии, опасные аритмии и назначить адекватную терапию.
2. Поражение эндокарда.
1). Поражение клапанного эндокарда ведет к образованию склеродермического, чаще митрального порока сердца (кальциноз клапанов), который отличается от ревматического менее выраженным обезображиванием клапанов и, как следствие этого, известной “доброкачественностью” течения с редким развитием декомпенсации. Чаще поражаются митральный и 3-х створчатый клапан.
2). Клиническая и рентгенологическая картина порока не всегда отчётлива в связи с одновременным поражением миокарда, реже – перикарда.
3) Пролапс митрального клапана.
У отдельных больных выявляется пролапс митрального клапана.
3. Поражение перикарда.
Перикардит, как проявление полисерозита имеет адгезивно-экссудативный характер и нерезко выражен. В этих случаях рентгенологически у некоторых больных обнаруживаются плевроперикардиальные спайки; при эхокардиографии – утолщение оболочки и наличие небольшого количества жидкости, которая обычно не содержит элементов воспаления и чаще отражает нарушения транссудаций.
Часто, в настоящее время, выпот в сердечной сорочке связывают с поражением миокарда.
Итак, если обобщить поражения сердца при ССД:
- миокардиопатия с ЭКГ- признаками очагового кардиосклероза;
- аритмия и нарушения проводимости сердца;
- адгезивный или экссудативный перикардит;
- нарушение функции левого желудочка при специальном исследовании выявляют у большинства пациентов;
- эндокардит с формированием пороков сердца — очень редко;
- ЭКГ признаки миокардиального фиброза встречаются редко (преимущественно у пациентов с диффузной формой);
- признаки миокардита наблюдаются почти исключительно у пациентов с симптоматикой полимиозита;
- застойная сердечная недостаточность развивается редко, отличается рефрактерностью к проводимому лечению;
- типичное легочное сердце, несмотря на частое поражение легких, наблюдается относительно редко.
XI. Поражение почек.
Поражение почек при морфологическом исследовании выявляется примерно у 80% пациентов и характеризуется преимущественным поражением почечных сосудов, а не развитием фиброза.
Степень поражения почек при ССД часто определяет прогноз заболевания в целом.
1. Истинная склеродермическая почка.
– Склеродермическая нефропатия.
– Поражение сосудов с множественными кортикальными некрозами – ведущий и первичный процесс при склеродермической нефропатии.
– Быстро нарастает протеинурия, повышается АД, развиваются олигурия, азотемия и, наконец, терминальная анурия.
2. Склеродермический почечный криз.
– Развивается обычно в первые 5 лет болезни у пациентов с диффузной формой ССД и протекает по типу диффузного гломерулонефрита.
– Быстро прогрессирующая олигурическая острая почечная недостаточность развивается как результат фиброза междольковых артерий в комбинации с каким-либо сосудосуживающим стимулом (значительный диурез, кровопотеря, хирургическое вмешательство).
– Активация ренин-ангиотензинового механизма приводит к усилению вазоконстрикации – возникает острая почечная недостаточность. У 90% пациентов – гиперренинемия.
– Подобные изменения в почках обычно сопровождают злокачественная гипертензия более 170/130 мм.рт.ст., (хотя примерно у 10% пациенто АД сохраняется в пределах нормы) и микроангиопатическая гемолитическая анемия, тромбоцитопения гипертоническая энцефалопатия с сильной головной болью с судорогами, эпилептическими признаками, ретинопатией и левожелудочковой недостаточностью.
– Если не восстанавливается почечный кровоток, возникает хроническая почечная недостаточность, приводящая к смерти больных.
Кстати, предвестниками почечной недостаточности могут быть микроангиопатическая гемолитическая анемия, которая может возникать и в отсутствие артериальной гипертензии, и длительно сохраняющийся перикардиальный выпот.
Кроме того, необходимо подчеркнуть, что у некоторых больных незадолго до возникновения склеродермического почечного криза наблюдают артериальную гипертензию, протеинурию, гематурию или повышение уровня креатинина в моче. Поэтому мониторинг этих показателей позволяет прогнозировать наступление криза и предотвратить его.
3. Хронический вариант нефропатии при ССД целесообразно подразделять на три группы:
- субклиническая хроническая склеродермическая нефропатия (ХСН1);
- умеренная (ХСН2);
- выраженная (ХСН3).
При минимальной, субклинически протекающей ХСН отмечаются незначительные и нестойкие изменения в моче и (или) функциональные нарушения (снижение клубочковой фильтрации).
Умеренная ХСН характеризуется небольшими, но стойкими изменениями в моче в сочетании с нарушениями функции почек.
При выраженной ХСН, помимо мочевого синдрома и функциональных нарушений, у больных отмечаются гипертензия, контролируемая гипотензивными препаратами, отеки, повышение уровня серомукоида мочи, гиперренинемия. ХСН развивается в течение ряда месяцев и лет и протекает более доброкачественно.
В каждом конкретном случае склеродермической нефропатии следует конкретизировать ее варианты. Наиболее важными признаками для выделения вариантов склеродермической нефропатии являются характер и стойкость мочевого синдрома, количество серомукоида мочи и снижение клубочковой фильтрации, отражающие степень вовлечения почек в патологический процесс.
4. Очаговый или латентный нефрит.
В большинстве случаев встречается более лёгкий вариант поражения почек – по типу очагового или латентного нефрита с умеренной преходящей протеинурией.
Надо помнить, что сердечная недостаточность или гиповолемия при передозировке диуретиков могут приводить к снижению почечного кровотока и, как следствие, к развитию почечного склеродермического криза, даже если до этого признаков поражения почек не было.
XII. Общие проявления
1. Потеря массы тела.
Наиболее характерна значительная, иногда катастрофическая, потеря массы тела, наблюдающаяся в основном в период генерализации или быстрого прогрессирования болезни.
2. Лихорадочная реакция.
Обычно мало выражена и отражает в некоторой степени остроту патологического процесса.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ СИСТЕМНОЙ СКЛЕРОДЕРМИИ
| Частота, % | ||
| Клинические проявления | Акрокросклероти-ческая форма | Диффузная форма |
| Синдром Рейно
Утолщение кожи Обызвествление подкожной клетчатки Телеангиоэктазии Артралгия, артрит Миопатия Нарушение моторики пищевода Пневмосклероз Легочная гипертензия Сердечная недостаточность Почечный склеродермический криз |
95-100
98а 50 85 40 5 80 35 < 10 < 1 < 1 |
0-95
100 10 40 70 50 80 40 < 1 30 15 |
КЛИНИКО-ЛАБОРАТОРНАЯ ХАРАКТЕРИСТИКА СИСТЕМНОЙ СКЛЕРОДЕРМИИ
(Гусева Н.Г., 1994)
| Проявления болезни | % |
| Синдром Рейно
Лихорадка Потеря массы (на 10 кг и более) Трофические нарушения Поражения кожи Поражения мышц Поражения суставов Поражения костей (остеолиз) Поражения лимфатических узлов Поражения серозных оболочек Поражения лёгких Поражения сердца Поражения желудочно-кишечного тракта Поражения почек Поражения нервной системы Увеличенная СОЭ (более 20 мм/час) Гиперпротеинемия (более 8,5 г%) Гипергаммаглобулинемия (более 1,9 г%) АНФ (на 71 обследованного) Ревматоидный фактор (на 125 обследованных) |
84,5
64,5 50,5 64,5 90,0 64,0 91,0 14,0 40,0 59,0 79,0 87,0 69,5 39,0 46,5 71,5 60,5 64,0 55,0 40,0 |
Лабораторные показатели
1. Как правило, неспецифичны и в основном отражают степень активности воспалительного процесса и глубину иммунных нарушений.
2. Периферическая кровь при ССД изменена мало: лишь у отдельных больных отмечаются:
– гипохромная анемия, иногда В12 – деф.- и фолиево-деф. анемия;
– лейкоцитоз;
– реже – лейкопения;
– увеличение СОЭ.
3 Повышение содержания:
– фибриногена;
– серомукоида;
– альфа2 – глобулинов, повышение IgG;
– гиперпротеинемия (гипер гамма-глобулинемия).
4. Некоторые признаки с иммунологических позиций сближает ССД с РА и СКВ:
1) Обнаружение РФ (в 40-50% случаев), ЦИК.
2) При диффузных формах выявляют антинуклеарные антитела и антитела к ScL-70 (это антитела к топоизомеразе-1), а при акросклеротических – антицентромерные антитела при CREST-синдроме.
3) Обнаружение волчаночных клеток (2-7%).
4) Обнаружение антител к эндотелию.
5) У больных ССД выявлено снижение активности СОД, ГП и ГР в эритроцитах крови и повышение активности СОД и ГР в плазме, увеличение малонового диальдегида. С повышением активности патологического процесса отмечается еще большее увеличение изоэнзимов СОД-1.
5. При поражении почек – микрогематурия, протеинурия, цилиндрурия, лейкоцитурия.
6. В костном мозге выявляется плазмоцитарная и ретикулоцитарная реакция.
7. Нарушение метаболизма коллагена.
Определение оксипролина в моче и крови отражает лишь суммарные изменения «коллагенового» профиля. Поэтому определяют отдельные фрагменты коллагена IV типа и ламинина в сыворотке крови.
АУТОАНТИТЕЛА, ВЫЯВЛЯЕМЫЕ ПРИ СИСТЕМНОЙ СКЛЕРОДЕРМИИ
| Аутоантитела | Форма заболевания | Частота выявления, %а |
| Антитела к антигену Scl-70
Антитела к центромерам Антитела к РНК-полимеразам I, II и III Антитела к Th-рибонуклеопротеиду Антитела к U1-рибонуклеопротеиду Антитела к антигену РМ-1 |
Диффузная
Акросклеротическая Диффузная Акросклеротическая Акросклеротическая. Смешанное заболевание соединительной ткани Перекрестный синдром с признаками полимиозита и акросклеротической формы системной склеродермии |
40
60-80 5-40 14 5-10 95-100 25 |
а Цифры отражают приблизительную частоту выявления аутоантител при данной форме заболевания.
Диагноз
Диагностические критерии надежности диагноза.
Для диагностики ССД применяют критерии Американской ревматологической ассоциации (1980), которые позволяют исключить пациентов с локальными формами склеродермии, эозинофильным фасциитом, и различными типами псевдосклеродермы:
«Большие» критерии
1. Феномен Рейно.
1) Аномальную сосудистую реакцию на холодовые или эмоциональные стимулы встречают у большинства больных диффузной и ограниченной ССД, но многие больные с феноменом Рейно не страдают склеродермией или каким-либо другим ревматическим заболеванием.
2) До 5-10% некурящих здоровых людей могут проявлять феномен Рейно.
3) Скрининг на ССД должен включать осмотр пальцев рук для выявления:
а) отёчности,
б) биомикроскопию капилляров,
в) выявление АНАТ.
4) Если у больного нет хотя бы одного из этих признаков, вероятность склеродермии мала.
5) А так как феномен Рейно встречают и при других ревматических заболеваниях (СКВ, полимиозит), врач должен тщательно провести дифференциальную диагностику.
2. Характерное поражение кожи.
Проксимальная склеродерма — симметричное утолщение, уплотнение и индурация кожи пальцев проксимально от пястно-фаланговых и плюснефаланговых суставов. Изменения могут локализоваться на лице, шее, грудной клетке и животе.
1) Склеродерма или акросклероз – утолщение дистальных участков коки – это диагностический признак обеих форм ССД.
2) У больных с диффузной формой заболевания происходит дальнейшее проксимальное распространение поражений кожи на руки, бедра и туловище. В сомнительных случаях существенную помощь оказывает морфологическое исследование биоптата кожи.
«Малые» критерии
1 Лабораторные данные.
1) Представляет интерес выявление при диффузных формах склеродермии антинуклеарных антител и антител к ScL-70, а при лимитированных формах ССД – антицентромерных антител.
2) Антитела ScL-70 чаще выявляются при диффузной, форме ССД, обнаружение антител ScL-70 у пациентов с изолированным феноменом Рейно коррелирует с последующим развитием ССД. Антитела к центромерам обнаруживают у 20% пациентов ССД, большинство из которых имеют признаки CREST-синдрома, рассматривают в качестве прогностического маркера развития ССД.
2 Склеродактилия — перечисленные выше изменения, локализованные на пальцах.
3. Рубцы на кончиках пальцев или потеря вещества подушек пальцев.
4 Характерные поражения внутренних органов
1) Дисфагия с нарушением функции пищевода (рентгенологически).
2) Фиброз лёгких (рентгенологически).
Двухсторонний базальный легочный фиброз — при стандартном рентгенологическом исследовании определяются двухсторонние сетчатые или линейнонодулярные тени, наиболее выраженные в базальных участках легких, или проявления по типу «сотового легкого» (изменения не должны быть связаны с первичным поражением легких).
3) Поражение сердца (кардиомегалия, нарушения проводимости).
4) Нефропатия.
5) Артралгии и артриты.
6) Остеолиз, кальциноз.
7) Полимиозит.
При наличии одного большого или двух малых критериев чувствительность составляет 97%, а специфичность 98%.
Чаще пользуемся Российской классификацией Гусевой
ДИАГНОСТИЧЕСКИЕ ПРИЗНАКИ ССД (Н.Г.ГУСЕВА, 1993)
ОСНОВНЫЕ:
Периферические:
1. Синдром Рейно.
2. Склеродермическое поражение кожи.
3. Суставно-мышечный синдром (с контрактурами).
4. Остеолиз.
5.Кальциноз.
Висцеральные:
6. Базальный пневмосклероз.
7. Крупноочаговый кардиосклероз.
8. Склеродермическое поражение пищеварительного тракта.
9. Острая склеродермическая нефропатия.
Лабораторные:
Специфические АНА (анти-СКЛ-70 и антицентромерные антитела).
ДОПОЛНИТЕЛЬНЫЕ
Периферические:
1. Гиперпигментация кожи.
2. Телеангиоэктазии.
3. Трофические нарушения.
4. Полиартралгии.
5.Полимиалгии, полимиозит.
Висцеральные:
1. Лимфаденопатия.
2. Полисерозит (чаще адгезивный).
3. Хроническая нефропатия.
4.Полиневрит, поражение ЦНС.
Общие:
1. Потеря массы тела (более 10 кг).
2. Лихорадка (чаще субфебрильная).
Лабораторные:
1. Увеличение СОЭ (более 20 мм/ч).
2. Гиперпротеинемия (более 5 г/л).
3. Гипергаммаглобулинемия (более 23%).
4. Антитела к ДНК или АНФ.
5. Ревматоидный фактор.
Дифференциальный диагноз
В типичных случаях диагноз не вызывает значительных затруднений, трудности возникают обычно при диагностике атипичных форм заболевания, особенно протекающих с преимущественным поражением внутренних органов и невыраженными кожными изменениями.
Дифференциальную диагностикуССД проводят с другими СЗСТ и заболеваниями склеродермической группы. Подавляющее большинство заболеваний “склеродермической” группы отличаются от ССД в первую очередь отсутствием феномена Рейно (а также других сосудистых и висцеральных проявлений).
Выделяют 2 основные формы феномена Рейно – первичный и вторичный.
Наличие вторичного феномена Рейно диктует необходимость проводить дифференциальную диагностику ССД с другими СЗСТ (в % указана частота встречаемости вторичного феномена Рейно).
1. РА – около 5%.
Преобладающее поражение суставов требует дифференциальной диагностики в первую очередь с РА. Полиартрит при ССД отличается от полиартрита при РА преобладанием фиброзных, а не деструктивных изменений.
2. Полимиозит (дерматомиозит) –20-30%.
Уровень активности ферментов при ССД – менее выражен при ССД в отличие от ДМ, уровень альдолазы чаще выше, чем КФК.
При ведущем в клинической картине мышечном синдроме заболевания дифференцируют с полимиозитом.
3. Васкулиты.
При преобладании сосудистых поражений ССД необходимо дифференцировать с различными первичными васкулитами (облитерирующий тромбангиит, артериит Такаясу, атеросклероз).
4. СКВ — 20-40% случаев, нередко в сочетании с АФС и синдромом Шегрена.
5. Первичный синдром Шегрена — до 80%.
6. Антисинтетазный синдром в рамках ПМ/ ДМ — 20-30%.
7. Смешанные заболевания соединительной ткани (перекрестный синдром с клиническими признаками СКВ, ССД и ПМ) — более 80%. Однако в настоящее время существование смешанного заболевания соединительной ткани подвергается сомнению, предполагают, что это заболевание является вариантом дебюта лимитированной формы ССД,
8. Заболевания, сопровождающиеся повышением вязкости крови (криоглобулинемия, полицитемия, макроглобулинемия Вальденстрема).
9. Туннельные синдромы.
10. Эндокринная патология.
11. Последствия лечения некоторыми ЛС (бета-адреноблокаторы, блеомицин, винбластин, клофелин, эрготамин и др.).
При отсутствии вышеперечисленных заболеваний и факторов, феномен Рейно рассматривают как первичный (встречается у 4-15% населения, преимущественно женщин). Первичный феномен Рейно отличается от вторичного:
- более ранним возрастом дебюта болезни;
- более высокой частотой приступов (провоцируются охлаждением и эмоциональным стрессом);
- более мягким течением без признаков развития стойкой дигитальной ишемии и трофических нарушений;
- отсутствием изменений при капилляроскопии, АНФ и “склеродермических” антител.
12. Псевдосклеродермический синдром.
При этом синдроме изменения, сходные с ССД, являются вторичными и связаны со злокачественной опухолью, особенно у больных среднего и пожилого возраста.
У страдающих инсулино-зависимым СД может развиться утолщение кожи пальцев рук и их контрактуры (диабетическая нейропатия).
13. Очаговая склеродермия.
1) При ней не наблюдается феномена Рейно и поражений внутренних органов.
2) Существуют 2 формы очаговой или ограниченной склеродермии. При них наблюдают только характерные для ССД поражения кожи.
1-я форма – кольцевидная склеродермия
а) Возникает в любом возрасте (чаще в детском) и характеризуется небольшими округлыми поражениями кожи (каплевидная склеродермия) или более крупными (кольцевидные бляшки).
б) Подобные же изменения встречают и при хронической форме болезни Лайма, поэтому в подозрительных случаях рекомендуют проводить серодиагностику этого заболевания.
2-я форма – линейная склеродермия
а) Чаще возникает у детей и подростков.
б) Могут развиваться тяжёлые деформации лица (“сабельный удар”).
в) Иногда при ней развивается гемиатрофия лица.
14. Эозинофильный фасциит.
Это заболевание неясной этиологии, входит в группу склеродермических состояний.
1) Характерна боль и припухлость одной или нескольких конечностей, иногда после тяжёлой физической нагрузки.
2) Вскоре отек сменяется уплотнением кожи по типу “апельсиновой корки” и подкожной клетчатки, но феномена Рейно и склеродактилии, поражений внутренних органов нет.
В начале заболевания может развиться синдром «карпального канала», легкий миозит, в более поздних стадиях возможны сгибательные контрактуры. Через 2-5 лет может наступить спонтанное улучшение, и даже выздоровление. Иногда заболевание приобретает затяжной характер.
3) При исследовании периферической крови больных всегда определяют эозинофилию, иногда апластическую анемию, тромбоцитопению и другие гематологические осложнения.
4) Диагностику основывают на результатах биопсии кожи и подлежащих тканей (глубокая инфильтрация фасций эозинофилами и воспалительными клетками), на поздних стадиях – склеротические изменения.
5) Характерна гипергаммаглубулинемия и увеличение СОЭ, ↑ ЦИК
6) Отмечаются обычно положительное действие кортикостероидов и относительно благоприятный прогноз. Имеются сообщения об успешном применении Н2 блокатора циметидина.
7) В отличие от ССД эозинофильным фасциитом чаще поражаются мужчины.
15 Синдром эозинофильной миалгии.
В 1989 г. появились многочисленные сообщения о заболевании, проявляющемся склеродермоподобным поражением кожи, миалгией и эозинофилией. Хотя патогенез заболевания до сих пор неизвестен, установлено, что в большинстве случаев оно было связано с приемом триптофана, производимого одной японской фирмой. В партиях препарата, вызвавших это заболевание, была обнаружена незначительная примесь димеров триптофана. Впоследствии установили, что причиной такого загрязнения послужили изменения, внесенные в технологию получения триптофана в 1988 г. Однако этиологическая роль димеров триптофана до сих пор не доказана. Возможно, заболевание обусловлено какими-то другими примесями. В 1990 г. продажа триптофана в США была запрещена.
1) Это патология, связанная с приёмом L-триптофана (пищевая добавка).
2) Начало внезапное или постепенное. В первые 2-3 месяца развивается склеродермоподобное утолщение кожи, у больных возникают признаки эозинофильного фасциита.
3) Возможно, заболевание связано с токсическими продуктами распада L-триптофана или аномальным метаболизмом вещества. Его ранние проявления: субфебрильная температура, утомляемость, одышка, кашель, артралгия или артрит.
4) Диагностические признаки:
– эозинофилия (более 1000/мм3)
– тяжёлая миалгия, мышечные спазмы.
5) Возможны:
– кожная сыпь,
– индурация,
– интерстициальные инфильтраты в лёгких,
– полиневропатия, которая может приводить к параличам и дыхательной недостаточности, при которой может потребоваться ИВЛ. Иногда возникают миокардит, аритмии, легочная гипертензия. Возможно снижение памяти и внимания.
Когда заболевание принимает хронический характер, эффективность лечения может быть невысокой. Для лечения используют ГК, противомалярийные средства, иммунодепрессанты и плазмаферез.
6) В сыворотке крови повышена активность альдолазы и трансаминаз.
16. При синдроме Вернера – наследственной общей кожной атрофии у больных обнаруживается тонкая напряженная кожа, заостренность носа, застывшая мимика, множественные телеангиэктазии, ограничение подвижности суставов с изъязвлением кожи над костными выступами. Однако, в отличие от ССД, при данном заболевании отмечается снижение интеллекта, карликовый рост больных, инсулинозависимый диабет. В то же время отсутствуют висцериты, типичные для ССД. Болезнь обычно встречается в более раннем возрасте и у нескольких членов семьи (аутосомно – рецессивное наследование).
17. Склеродерма Бушке.
Для неё характерны индуративные изменения преимущественно области лица и шеи, волосистой части головы, туловища и проксимальных отделов конечностей. Кисти и стопы обычно не изменены. Ее развитию обычно предшествует стрептококковая инфекция. Как правило, болезнь проходит самостоятельно через 6-12 месяцев.
18. Склеромикседема Арндта—Готтрона — редкое заболевание, для которого характерны появление желтоватых или розовых папул и диффузное утолщение кожи на кистях и лице. При гистологическом исследовании в дерме обнаруживают отложение кислых гликозаминогликанов. У некоторых больных в сыворотке повышено содержание моноклональных IgG.
19. При наличии множественных телеангиэктазий проводится дифференциальная диагностика между ССД и наследственными гемморрагическими телеангиэктазиями, а также болезнью Рандю-Ослера-Вебера. Для ССД, в отличие от данных заболеваний, характерно позднее появление телеангиэктазий, редкое развитие геморрагий, а также отсутствие в анамнезе сведений о наличии у родственников данных симптомов.
КЛАССИФИКАЦИЯ СКЛЕРОДЕРМИИ И СКЛЕРОДЕРМИЧЕСКИХ СОСТОЯНИЙ
Системная склеродермия
– Акросклеротическая форма
– Диффузная форма
– Висцеральная форма
– Смешанное заболевание соединительной ткани
– Другие перекрестные синдромы
Ограниченная склеродермия
– Бляшечная склеродермия
– Линейная склеродермия
– Лобно-теменная склеродермия
Склеродермические состояния, вызванные лекарственными средствами и химическими веществами
– Отравление фальсифицированным рапсовым маслом
– Отравление винилхлоридом
– Побочное действие блеомицина
– Побочное действие пентазоцина
– Интоксикация эпоксидными смолами и ароматическими углеводородами
– Синдром эозинофилии-миалгии
Другие заболевания, с которыми дифференцируют системную склеродермию
– Склередема
– Склеромикседема Арндта-Готтрона
– Хроническая реакция «трансплантат против хозяина»
– Эозинофильный фасциит
– Диабетическая хейропатия
– AL-амилоидоз
Лечение ССД.
Хотя системная склеродермия неизлечима, лечение отдельных ее проявлений позволяет улучшить функцию пораженных органов и облегчить состояние больного. Как и при любом тяжелом хроническом заболевании, очень важно взаимопонимание между врачом и больным. Как только будет поставлен диагноз, нужно рассказать о заболевания больному и членам его семьи, а потом все время подбадривать больного и давать ему необходимые разъяснения. В зависимости от течения болезни необходимо регулярно измерять АД, проводить общие анализы крови и мочи, оценивать функцию почек и легких.
Лечение ССД представляет сложную и нерешенную в полной мере задачу современной медицины. Оно должно проводиться с учетом стадии и характера течения заболевания. При первичной диагностике или при подозрении на ССД больной должен быть госпитализирован в специализированный стационар.
Режим больных определяется функциональным состоянием различных органов и систем, в первую очередь желудочно-кишечного тракта и почек. Специальной диеты больным ССД не требуется. Пища должна быть разнообразной, калорийной, богатой витаминами, легко усвояемой. При возникновении артериальной гипертензии, поражении сердца и желудочно-кишечного тракта производится соответствующая коррекция диеты.
Сложный патогенез заболевания обуславливает необходимость комплексной терапии.
Лечение в первую очередь определяется вариантом течения ССД и активностью процесса.
Основные цели современной дифференцированной терапии ССД:
- Своевременность.
- Комплексность.
- Длительность.
- Этапность (стационар-диспансер-курорт).
Основные направления фармакотерапии при ССД:
- профилактика и лечение сосудистых осложнений;
- подавление прогрессирования фиброза;
- воздействие на иммуновоспалительные механизмы ССД;
- профилактика и лечение поражения внутренних органов.
Существует 3 группы препаратов, которые воздействуют на основные патогенетические механизмы ССД:
1) антифиброзные;
2) сосудистые;
3) противовоспалительные.
При преобладающем поражении кожи.
1. D-пеницилламин.
Одним из важнейших медикаментозных, по существу базисных средств в лечении ССД считают D-пеницилламин.
1) Особенно на ранних стадиях болезни он может привести к замедлению прогрессирования, регрессированию кожных проявлений при диффузной форме ССД, обладает иммуносупрессивным действием.
2) D-пеницилламин тормозит избыточное фиброзообразование, ускоряет распад коллагена. Препятствует образованию внутримолекулярных и межмолекулярных поперечных сшивок в коллагеновых волокнах. Удаляет Сu из организма, а медь является ингибитором коллагеназы.
3) Назначают при всех вариантах течения, особенно при остром, быстро прогрессирующем течении.
4) В первые сутки препарат дают в половинной дозе, затем в течение нескольких месяцев (1-3 мес.) до достижения отчётливого улучшения) D-пеницилламин назначают в дозе 450-900 мг/сутки, дозу увеличивают каждые 2 недели на 300 мг, а при необходимости и до 1500 мг. Эффект оценивают не ранее, чем через 1,5 – 2 месяца от начала терапии.
– В последующем переходят на поддерживающую дозу – 300-450 мг/сутки за 1 час до еды или через 2 часа после еды, и продолжают лечение несколько лет.
– Однако, в настоящее время чаще – D-пеницилламин внутрь по 125-500 мг через сутки натощак.
– При применении рекомендовавшихся ранее высоких доз (750-1000 мг/сут) эффективность терапии существенно не увеличивается, но значительно возрастает частота побочных эффектов, требующих прерывания лечения.
5) Препарат противопоказан при поражениях печени и почек, тромбоцито- и лейкопении.
6) В процессе лечения возможны аллергические реакции, диспепсические явления, апластическая анемия, лейко- и тромбоцитопения, маточные и носовые кровотечения, синдром миастении, головокружения, изменения осадка мочи, выпадение волос, что требует уменьшения дозы препарата или временной его отмены.
7) Однако самое тяжелое его осложнение – гломерулонефрит с нефротическим синдромом. Он развивается примерно через полгода после начала приема препарата (при протеинурии > 1-2 г/сутки лекарство отменяют)
Те или иные осложнения наблюдаются у 1/3 больных, поэтому лечение D-пеницилламином следует начинать в стационаре и тщательно контролировать его переносимость.
2. Унитиол также препятствует созреванию коллагена и фиброзообразованию – 5% 5-10 мл в/м через день – 20-25 инъекций (2 раза в год).
3. Аппликации нитроглицериновой мази:
Эти аппликации на кончики пальцев помогают залечить язвы.
4. Аппликации 50% раствора димексида (на участки пораженной кожи). Увеличивают проницаемость тканей, ингибируют пролиферацию фибробластов. Служит проводником через кожу многих других сосудорасширяющих средств, поэтому:
– Эффективны особенно с добавлением сосудорасширяющих препаратов.
– На курс – 10-20-30 аппликаций по 20-30 минут, при хорошей переносимости – повторные курсы.
5. Колхицин.
– Колхицин предотвращает острую боль, связанную с подкожным кальцинозом.
– Этот препарат способен подавлять накопление коллагена, блокируя конверсию проколлагена в коллаген. Кроме того, колхицин усиливает синтез коллагеназы.
– Имеются единичные данные о положительном влиянии колхицина именно на кожные проявления при ССД. Но контролируемые испытания не проводились.
6. Мадекассол
Положительным сосудистым эффектом наряду с умеренным антифиброзным действием обладает мадекассол, который может применяться per os (1-2 таблетки 3 раза в день) и локально – в виде мази при системной и очаговой СД. Следует подчеркнуть эффективность локального применения мадекассола у больных с длительно существующими болезненными длительными язвочками и другими сосудисто-трофическими изменениями.
7. Лидаза или гиалуронидаза.
– Применяют при хроническом течении или очаговой склеродермии.
– В виде повторных курсов (12-14 инъекций) по 64-128 ЕД подкожно или электрофоретически.
8. Дапсон – 0,1-0,2 г. 3 раза в день или 4,0 мл – 5% раствора в/м.
9. Метотрексат.
Недавно появились сообщения об эффективности метотрексата, особенно при кожных проявлениях у больных ССД, при поражении суставов и мышц (10-7,5 мл/нед).
10. Циклоспорин – А.
– Некоторые исследования в настоящее время подтверждают положительное влияние ЦсА на кожные проявления при ССД.
– Желательно использование вначале небольших доз (2,5 мг/кг день) с последующим медленным увеличением до оптимальных при удовлетворительной переносимости препарата.
11. Рекомбинантный гамма-интерферон и интерферон-альфа препятствует фиброзообразованию.
12. Экстракорпоральная фотохимиотерапия (фотаферез).
– Это новый метод иммунотерапии, при котором лейкоциты периферической крови, сенсибилизированные 8-метоксипрозаленом, подвергаются длинноволновому ультрафиолетовому облучению, а затем возвращаются больному.
– Отмечают существенное уменьшение выраженности кожных проявлений.
13. Плазмаферез, карбогемосорбция.
Особенно при высокой активности процесса.
14. Уменьшение сухости кожи – мытье мягкими средствами, не содержащими мыла, принимать ванны с масляными добавками и использование кремов и мазей на гидрофильной основе.
15. Ежедневные физические упражнения, а также частый (несколько раз в день) массаж помогают сохранить объем движений в конечностях и делают кожу более эластичной.
16. Ускорение заживления неинфицированных язв на кончиках пальцев и предотвращение образования новых. На дистальные фаланги можно наложить окклюзионную повязку или синтетическое покрытие, например из гидроколлоида.
17. Хирургическая обработка и промывание язв.
Необходимо регулярно промывать язвы, проводить их хирургическую обработку или удалять некротизированные ткани с помощью ферментных препаратов.
18. Симпатолитики.
Язвы быстрее заживают, если применять симпатолитики.
19. Антимикробное лечение.
При инфицировании язв обычно проводят местное антимикробное лечение. Однако в некоторых случаях (особенно при подозрении на остеомиелит) приходится использовать антимикробные средства для системного применения.
20. Варфарин, дилтиазем.
Средства, позволяющего предупредить обызвествление кожи и способствующего рассасыванию кальцификатов, не существует. Однако имеются сообщения о том, что у отдельных больных объем кальцификатов уменьшился при лечении варфарином, дилтиаземом внутрь по 120-300 мг/сутки.
При поражении лёгких.
1. Гормональная терапия – особенно эффективна на ранних стадиях интерстициального поражения легких.
1) Основные показания к применению кортикостероидов:
– высокая активность склеродермического процесса,
– наличие иммунных сдвигов, обычно наблюдающихся при подостром течении ССД.
2) Предпочтителен преднизолон 20-30 мг в день до достижения терапевтического эффекта, а затем доза его постепенно снижается до поддерживающей (15-10-5 мг). Но при фиброзирующем альвеолите она повышается до 40 мг/день, а при поражении мышц по типу полимиозита –50-60 мл/день.
3) При остром и подостром течении целесообразна длительная (не менее 1 года), чаще многолетняя, терапия преднизолоном.
4) Возможна замена преднизолона другим стероидным препаратом, но следует учитывать, что триамцинолон может вызвать миопатию, а дексаметазон – быстрое развитие синдрома Иценко- Кушинга.
5) Противопоказания к применению кортикостероидов при ССД соответствуют общепринятым. Кроме того, существует предположение, что ГК в высоких дозах способствуют развитию ОПН именно у больных ССД.
2. Иммунодепрессанты.
1) Применяют для лечения больных ССД сравнительно редко и лишь по показаниям: отчётливые иммунные нарушения и высокая активность процесса, не поддающиеся воздействию кортикостероидов, или наличие противопоказаний к ним.
2) Циклофосфамид
Было показано, что циклофосфамид в дозе 2,0-2,5 мг/кг в день перорально (200-400 в/м мл/нед) в сочетании с низкими дозами преднизолона вызывает достоверное улучшение функционального состояния лёгких у больных ССД с лёгочным фиброзом.
Редко – пульс-терапия.
3. D-пеницилламин (о котором уже было сказано выше). По 125 мг через сутки натощак.
4. Ингибиторы ангиотензин – превращающего фермента (АПФ). Малоэффективны.
5. Фотаферез.
6. Антимикробная терапия.
При развитии легочных инфекций – антимикробная терапия.
Однако необходимо подчеркнуть, что ни один из видов терапии при лечении поражения лёгких у больных ССД не отличается эффективностью.
В США всем больным ССД с поражением легких показаны иммунизация пневмококковой вакциной и ежегодная иммунизация противогриппозной вакциной.
В США при отсутствии тяжелого поражения других органов прибегают к трансплантации комплекса сердце-легкие или одного легкого.
При поражении почек.
1. Стероиды.
При поражении почек применение стероидов должно быть строго дифференцировано:
- Наличие активного гломерулонефрита является показанием к использованию сравнительно высоких доз кортикостероидов (30-40 мг преднизолона).
- Развитие острой склеродермической почки с гипертензией и быстрым нарастанием уремии, по мнению большинства авторов, требует резкого ограничения и даже исключения стероидной терапии, т.к. прием доз глюкокортикоидов более 15-20 мг/сут увеличивает риск развития нормотензивного почечного криза.
2. Иммунодепрессанты.
- При поражении почек предпочтительнее азатиоприн.
- Его назначают по 1-3 мг/кг массы тела больного (50-200 мг в день) в течение 2-3 месяцев и более под контролем анализов крови.
- Лучше в сочетании с кортикостероидами.
3. Гипотензивные средства: пропранолол, клонидин, миноксидил – ↓ АД и восстанавливают функцию почек.
4. Ингибиторы ангиотензин – превращающего фермента (АПФ).
Ингибиторы АПФ следует назначать как можно раньше (желательно в течение первых трех дней после появления первых признаков поражения почек).
Их эффективность связана с тем, что данная АГ протекает с высоким содержанием ренина, а ингибиторы АПФ прерывают цепочку синтеза прессорных соединений.
1) Каптоприл (капотен, и др.) – является препаратом выбора при развитии острой склеродермической почки и ренинзависимой гипертензии. Препарат назначают по 50-250 мг в день длительно (6-12 месяцев); подбирают минимальную дозу, позволяющую корректировать АД (при необходимости дозу увеличивают). Эналаприл (10-40 мг/сут) и лизиноприл.
2) При острой склеродермической нефропатии рекомендуется сочетание ингибиторов конвертирующего энзима с блокаторами ионов кальция, дезагрегантами. Однако блокаторы кальциевых каналов уступают по эффективности ингибиторам АПФ.
3) При нарастании почечной недостаточности – их сочетают с гемодиализом.
Плазмаферез, ГК и цитотоксические препараты противопоказаны, так как они не только не предупреждают прогрессирование почечной патологии, а, напротив, могут способствовать обострению процесса.
При синдроме Рейно.
1. Устраненение провоцирующих факторов.
Пациентов предупреждают о необходимости укутывания головы, рук и туловища в холодную погоду, отказа от курения, избегать эмоциональных перегрузок, воздействия вибрации, избыточного приема кофеина, и применения некоторых лекарственных средств, индуцирующих вазоспазм (эрготамина, амфетаминов и В-адреноблокаторов).
Фармакотерапия феномена Рейно нередко затруднена из-за развития устойчивости при длительном применении препаратов и побочных эффектов.
Ее рекомендуют в первую очередь при:
- Тяжелых проявлениях феномена Рейно, снижающих качество жизни,
- Высоком риске тяжелых сосудистых осложнений.
2. Блокаторы кальциевых каналов. Эффективность подтверждена в плацебо-контролируемых исследованиях.
Внутрь дигидропиридиновые производные:
Амлодипин 5—20 мг/сут
Фелодипин по 2,5—10 мг 2р/сут;
Исрадипин по 2,5—5.0 мг 2 р/сут;
Нифедипин (коринфар) (может быть дурнота и сердцебиение).
Назначают в дозе 30-90 мг в день отдельными курсами или длительно в течение 1 года (при условии хорошей переносимости). Лучше препараты нифедипина продленного действия – нифедипин пролонгированный 30 — 120 мг/сут;
Дилтиазем пролонгированный 120—300 мг/сут
Дилтиазем менее эффективен, чем дигидропиридиновые производные. Побочные эффекты: тахикардия, отеки, головные боли, приливы, запоры, головокружение, ортостатическая гипотония.
Верапамил – назначают в дозе 120-360 мг в день.
Форидон – назначают в дозе 40-120 мг в день.
3. Блокаторы серотониновых рецепторов – кетансерин per os 80-120 мг/сут., флуоксетин – 20-40 мг/сут (побочные эффекты: бессоница, тошнота, диарея, тремор).
4. Другие сосудорасширяющие средства.
– Депо-падутин, продектин.
– Пролонгированные сосудорасширяющие средства.
– Альфа-адренергические блокаторы.
– Средства, воздействующие на метаболизм катехоламинов.
– Резертин, метилдофа, феноксибензамин, празозин.
– Препараты никотиновой кислоты.
– Калликреин и его производные, ангинин, андекалин, солкосерил.
5. Солкосерил можно использовать внутривенно, внутримышечно, per os и местно в виде мази или желе. Внутривенно назначают в виде обычных инъекций (1—2 ампулы) или капельно (3—5 ампул в 250 мл 5% раствора глюкозы или изотонического раствора натрия хлорида). Внутримышечно вводят не более 5 мл раствора для инъекций. Рег оs назначают по 1—2 таблетки 3 раза в сутки. Мазь и желе рекомендуется наносить на поврежденную поверхность 2—3 раза в сутки (20-30 дневные курсы 2-3 раза в год).
6. Симпатолитики
Эффект временный, часто исчезает через несколько недель:
Празозин внутрь 1—5мг 2-3 р/сут
Побочные эффекты — синкопе, ортостатическая гипотония, головокружение, сердцебиение.
7. Антагонисты рецепторов ангиотензина II
Эффект подтвержден в одном плацебо-контролируемом исследовании: Лозартан внутрь 25—100 мг/сут
Побочные эффекты — головокружение, головные боли, недомогание, диарея.
8. Вазидилататоры
Нитроглицерин местно 1/4 — 1/2 см 2% мази
Побочные эффекты — головные боли, тахикардия, синкопе, сыпь, импотенция, тошнота, гипертензия при отмене.
9. Гепарин – 5-10000 ед. в сутки.
10. Пентоксифиллин – повышает гибкость эритроцитов.
Внутрь: 400 мг 3 р в сутки.
Побочные эффекты: диспепсия, тошнота, рвота.
11. Дезагреганты.
Поскольку вещества, высвобождаемые тромбоцитами, повреждают сосудистую стенку, определенную роль в лечении ССД могут играть дезагреганты.
1) Трентал (600-1200 мг/сут), курантил (225 мг/сут+микродозы аспирина – 50 мг/сут).
2) Реополиглюкин, реомакродекс.
– Он снижает вязкость крови, уменьшает агрегацию тромбоцитов и эритроцитов.
– Препарат вводят капельно, по 400 мл через день 8-12 перфузий на курс.
– Показано проведение 2-3 курсов в год, а в период перерыва – пероральный приём антиагрегантов.
3) Аспирин в низких дозах угнетает синтез тромбоксана А2, вызывающего агрегацию тромбоцитов и обладающего мощным сосудосуживающим действием.
4) Дипиридамол в дозе 200—400 мг/сут (в несколько приемов) подавляет адгезию тромбоцитов к поврежденной стенке сосудов. Хотя использование этих препаратов при системной склеродермии представляется вполне обоснованным, двухлетнее испытание двойным слепым методом не подтвердило их эффективность.
12. Динатриевая соль ЭДТА.
13. Целесообразно курсовое применение гипербарической оксигенации.
14. Простагландины.
Появились сообщения об успешном лечении рефрактерных вазоспазмов и кожных язв внутривенным введением простагландинов. Используются при критической ишемии в условиях стационара.
Обнадеживающим, но недостаточно изученным представляется использование простагландинов (ПГ) и их синтетических аналогов для лечения выраженной сосудистой патологии.
1) Вазапростан.
Препаратом из группы ПГЕ1 является вазапростан (алпростадил, проставазин). Вазапростан обладает выраженным периферическим сосудорасширяющим действием, повышает кровоток в периферических сосудах, улучшает микроциркуляцию и реологические свойства крови, тормозит агрегацию тромбоцитов и оказывает дезагрегационное действие. Показан при критической ишемии конечностей, при язвенно-некротических изменениях и начальной гангрене конечностей. Для внутривенного, реже внутриартериального, использования содержимое 2 ампул (40 мкг препарата) разводят в 250 мл изотонического раствора натрия хлорида. Вводят капельно (в течение 2 ч) 1 раз в сутки, а в тяжелых случаях — 2 раза в сутки. При необходимости дозу увеличивают до 60 мкг (3 ампулы) и вводят в течение 3 ч. На курс можно использовать до 20 инъекций.
Рекомендуется медленное внутриартериальное или в/в введение препарата. Благодаря многоплановому фармакологическому действию вазапростана (вазодилятация, подавление активности и агрегации тромбоцитов и т.д.) можно ожидать и системного эффекта препарата.
При применении вазапростана возможны приливы, снижение артериального давления, потеря аппетита, диарея, сыпь, тупая боль в конечности, подвергающейся лечению, чувство жжения, покраснения в месте введения препарата.
2) Вазобрал.
Менее выраженным действием на периферические сосуды обладает вазобрал, который применяют по 1—2 таблетки или по 2—4 мл 2 раза в сутки во время еды.
3) Илопрост (синтетический аналог простациклина) 0,5-2,0 нг/кг/мин. Однако, в США этот препарат пока не разрешен к применению. Снижается частота и выраженность приступов Рейно.
15. Фотаферез.
16. Блокада шейно-грудного (звездчатого) ганглия.
Если ишемия пальцев вызывает сильную боль, может потребоваться блокада шейно-грудного (звездчатого) ганглия. Симпатэктомия обычно приводит лишь к временному улучшению. Как и другие методы лечения, она не предотвращает прогрессирующее поражение сосудов. Поскольку сужение артериол пальцев в значительной мере обусловлено повреждением сосудистой стенки, ни один из методов лечения синдрома Рейно не приводит к полному излечению. У некоторых больных развивается гангрена кончиков пальцев, и приходится прибегать к ампутации.
При поражении пищевода.
При рефлюкс-эзофагите рекомендуют есть часто и понемногу, исключение приема пищи после 18 часов, спать в кровати с высоким изголовьем, не ложиться в течение нескольких часов после еды, избегать употребления кофе, чая, шоколада и других продуктов, расслабляющих нижний пищеводный сфинктер, и принимать антацидные средства между приемами пищи.
1. Антирефлюксная терапия.
2. Мукозопротекторы.
Сукральфат (гель) – обволакивает и ингибирует активность пепсина на 30 %.
3. Блокаторы Н2 – рецепторов гистамина (ранитидин, циметидин и др.). Эти препараты являются средством выбора при сочетании сосудистого периферического синдрома с эзофагитом, язвенными (предъязвенными) изменениями ЖКТ.
4. Омепразол.
Это представитель новой группы препаратов, подавляющих желудочную секрецию. Действие препарата наступает быстро, зависит от величины принятой дозы и сохраняется в течение 24 и более после однократного приёма 20 мг омепразола. Его назначают в тяжёлых, рефрактерных случаях ССД, очень эффективен при эрозивном эзофагите.
5. Церукал и цизаприд.
Хороший эффект у ряда больных оказывает церукал (реглан) – 10 мг 4 раза в день и цизаприд (5-40 мг/2-3 раза в сутки за 15 мин до еды, стимулирующие моторику желудка и кишечника, почти не влияют на моторику пищевода. Однако оба препарата повышают тонус нижнего пищеводного сфинктера, благодаря чему они также могут быть эффективны при рефлюкс-эзофагите. Нифедипин и в меньшей степени дилтиазем, напротив, снижают тонус нижнего пищеводного сфинктера и поэтому могут приводить к желудочно-пищеводному рефлюксу.
6. Фотаферез.
Кроме того, больным с дисфагией советуют тщательно пережевывать и запивать пищу.
При поражении нижних отделов ЖКТ.
1. При синдроме нарушения всасывания и бактериального роста назначают антибиотики широкого спектра действия, может потребоваться парентеральное питание.
Поражение тонкого кишечника:
Амоксициллин внутрь;
Ванкомицин внутрь;
Метронидазол внутрь;
Ципрофлоксацин внутрь.
В ранней стадии заболевания показаны:
Внутрь:
Метоклопрамид по 10 мг 3—4 р/сут;
Цизаприд по 5—40 мг 2—3 р/сут за 15 мин до еды.
Подкожно:
Октреотид по 100—250 мг 3 р/сут
2. Препараты, усиливающие моторику кишечника.
При запорах используют препараты, усиливающие моторику кишечника, легкие слабительные.
При суставном синдроме.
1. Гормональная терапия. Желательно не более 15-20 мг/сут. Однако они не предупреждают прогрессирование фиброза.
2. НПВС: индометацин, бутадион, бруфен, вольтарен – также могут входить в комплексное лечение ССД, особенно при наличии противопоказаний или отсутствии показаний к применению кортикостероидов.
3 Хинолиновые препараты.
– Применяют при любом течении ССД длительно и, как правило, в сочетании с другими средствами.
– Хлорохин 0,25 г или плаквенил – 0,4 г в течение 2-3 лет с перерывом в летние месяцы и под контролем анализов крови и глазного дна.
4. Фотаферез.
При поражении мышц.
1. Гормональная терапия.
2. НПВС.
3. Хинолиновые производные
4. Фотаферез
При поражении сердца.
При поражении сердца требуется назначение тех же препаратов, что и при лечении стенокардии, нарушений ритма и недостаточности кровообращения. Диуретики и сердечные гликозиды. Диуретики следует назначать с осторожностью, чтобы избежать гиповолемии, которая может привести к снижению почечного кровотока, снижению сердечного выброса и развитию ПН и провокаций почечного криза.
ЛФК и массаж
С целью воздействия на общее состояние, кожно-сосудистые и иные проявления болезни, при отсутствии противопоказаний, целесообразно раннее включение в терапевтический комплекс массажа и ЛФК.
Физиотерапевтическое лечение.
- Ультразвук с гидрокортизоном.
- Электрофорез гиалуронидазы.
- Парафиновые аппликации.
- Бальнеотерапия (сероводородные, радоновые, углекислые ванны), грязи.
- Лазеротерапия.
- Гипербарическая оксигенация.
- Рефлексотерапия.
- Плазмаферез, карбогеносорбция.
Санаторно-курортное лечение
(в основном больным с хроническим течением).
При поражении опорно-двигательного аппарата — Евпатория, а при наличии поражения сосудов или внутренних органов — Пятигорск с родоновыми, сероводородными, углекислыми ваннами, грязелечением. И последнее — больной должен отказаться от курения, так как никотин является мощным сосудосуживающим агентом и может вызывать обострение ССД.
Профилактика
I. Первичная.
1. Выявление факторов риска.
2. Выявление лиц, угрожаемых в отношении заболевания ССД
II. Вторичная.
1. Ранняя диагностика (в стационарах).
2. После уточнения диагноза в стационаре, подбора оптимальных доз препаратов, стихания активности процесса больного переводят на амбулаторное лечение и длительно продолжают поддерживающую терапию в поликлинике, контролируют состояние больного, его социальную и физическую реабилитацию.
3. Важно правильно трудоустроить пациента.
1) При остром и подостром течении больные нетрудоспособны и должны переводиться на инвалидность.
2) При хроническом течении – ограниченно трудоспособны. Должны быть освобождены от тяжёлой физической работы, воздействия вибрации.
4. Должны быть ограничены контакты больных с химическими агентами, аллергизирующими факторами.
5. Больные должны избегать переохлаждения и инсоляции.
Прогноз
- Течение системной склеродермии очень разнообразно. Оцепить прогноз на ранних стадиях заболевания, когда различия между двумя его формами еще не выражены, сложно.
- При акросклеротической (лимитированной) форме, особенно при выявлении антител к центромерам, прогноз в целом благоприятный. Однако менее чем у 10% больных через 10—20 лет после начала заболевания (а иногда и позже) развивается легочная гипертензия. Иногда наблюдаются также синдром нарушенного всасывания и первичный билиарный цирроз печени.
- При диффузной форме системной склеродермии прогноз гораздо хуже, особенно у мужчин и лиц, заболевших в пожилом возрасте.
- У больных с быстро прогрессирующим обширным поражением кожи уже на ранних стадиях заболевания могут поражаться почки и другие внутренние органы.
- Основные причины смерти — поражение легких, почек и сердца. После внедрения новых методов лечения почечных склеродермических кризов, а также гемодиализа при почечной недостаточности десятилетняя выживаемость при системной склеродермии возросла до 65%. В целом же десятилетняя выживаемость при диффузной форме системной склеродермии составляет 55%, а при акросклеротической форме — 75%.
- Спустя годы после начала заболевания уплотнение кожи может уменьшиться, причем если поражение кожи сначала захватывает дистальные, затем проксимальные отделы конечностей и впоследствии распространяется на туловище и остальные участки тела, то исчезает оно в обратном порядке. Склеродактилия и сгибательные контрактуры при этом могут сохраняться. Толщина кожи со временем также может нормализоваться, хотя иногда кожа атрофируется.