Расширенный отчет
опубликовано 6 июля 2017
Predicting and managing primary and secondary non-response to rituximab using B-cell biomarkers in systemic lupus erythematosus (July 2017)
1. Md Yuzaiful Md Yusof
2. Daniel Shaw
3. Yasser M El-Sherbiny
4. Emma Dunn
5. Andy C Rawstron
6. Paul Emery
7. Edward M Vital
* e.m.j.vital@leeds.ac.ukedvital@gmail.com
*для связи
Аннотация
Цель Для оценки факторов, связанных с первичных и вторичной не ответчиков на ритуксимаба при системная красная волчанка (СКВ) и вычисление регулирования вторичных не- истощение не ответчиков non-depletion non-response (2NDNR).
методы 125 больных СКВ, получавших Ритуксимаб более 12 лет. Основной клинический ответ был определен как улучшение всех активных доменов British Isles Lupus Assessment Group (BILAG)-2004 по классу C/улучшение и не A / B обострения. Частичные ответчики были определены одним значением B по BILAG. B-клетки были измерены с помощью высокочувствительных проточной цитометрии. Пациенты с 2NDNR, определяется инфузионные реакции и дефектных истощение, лечились с ocrelizumab или ofatumumab.
Результаты 117 пациентов имели анализу данных. В цикле 1 (C1), 96/117 (82%) достиг BILAG ответ (основных = 50%, частично = 32%). В многомерный анализ молодом возрасте (или 0,97, 95% ДИ от 0,94 до 1,00) и B-клетки истощения в 6 недель (или 3.22, 95% ДИ 1.24 до 8,33) увеличить шансы большего ответа. Полное истощение было предсказано нормальным комплементом и низкими pre- ритуксимаба plasmablasts и не было связано с более серьезные инфекции пост ритуксимаба лечения. Семьдесят семь (с данными на 72) C1 ответчики наступили клинических рецидива. Из них 61/72 (85%) ответил в цикле 2 (C2). 11 не C2-ответчиков, девяти критериям 2NDNR (распространенность = 12%) и оказались позитивными на антитела анти ритуксимаба. Отсутствие сопутствующих иммунодепрессанта и выше pre ритуксимаба plasmablasts предсказывают 2NDNR. Пять были переведены в ocrelizumab/ofatumumab и все истощены и ответил.
Заключение Лечение с анти CD20 агентов можно руководствоваться по B-клетки мониторинг и должны стремиться к достижению полного истощения. 2NDNR связан с анти ритуксимаба антител, и переход на очеловеченные агентов восстанавливает истощения и ответ. В СКВ альтернативные анти CD20 антитела могут быть более последовательно эффективным.
Введение
Ритуксимаб, химерных анти CD20 моноклональных антител (monoclonal antibody (mAb)) остается важным вариантом для умеренной до тяжелой системная красная волчанка (СКВ). Высокая степень эффективности ритуксимаба в различных проявлениях волчанки сообщалось в исследованиях открытых исследованиях, мультицентровое реестров и систематический обзоров Несоответствие между рандомизированные испытания и реальных доказательств было обусловлено дизайном в том числе выбором конечных точки, использование активных компаратора, критерии включения и низкой статистической достоверности.
Тем не менее есть также механистический причины неудачи ритуксимаба в клинических испытаниях при СКВ. B-клетки, которые убивает Ритуксимаб оказываются при СКВ менее эффективны, чем ревматоидного артрита (РА) за счет интернализации путем взаимодействия с FcγRIIb, что приводит к снижение эффекторных активность и патогенных волчанки аутоантител, которые вырабатыватся долгоживущими клетками плазмы. С помощью высокочувствительных проточной цитометрии highly sensitive flow cytometry (HSFC), протокол, который был оптимизирован для обнаружения плазмоцитов, мы обнаружили, что глубина B-клетки истощения предсказал ответ при РА и СКВ. Аналогичные исследования, а также определение других клинические предикторы ответа ритуксимаба при СКВ необходимы для оптимизации его использования и помочь дизайн испытания альтернативных B-клетки истощающих стратегий.
B-клеточной терапии истощения с rituximab является преходящей(транзиторной). У некоторых пациентов с первоначальный ответ хороший опыт происходит рецидив после заселения B-клеток (хотя с интервалом в переменной). В нашем опубликованные обнаружения когорте мы показали Бимодальная модель рецидива. Ранее рецидив, требующих повторное применение ритуксимаба было предсказано плазматические клетки количество> 0,0008 × 10
9/ L через 6 месяцев (время первоначального клинического ответа). пациенты с низкими плазмоцитами через 6 месяцев имели устойчивый ответ без повторного введения. Проверка этого подхода в качестве биомаркера необходимо определить, может ли HSFC использоваться в клинической практике для обоснования показаний к повторному лечению.
Повторить лечение ритуксимабом является эффективным. однако, мы наблюдали случаи больных СКВ, которые ранее наступило истощение и ответил хорошо на Ритуксимаб, но впоследствии развилась тяжелой инфузионные реакции> 24 часа во время второй инфузии цикла, отсутствием истощения CD20 + (наивными и память) B-клетки и отсутствием клинических ответов во время повторных циклов. Мы назвали это явление вторичной не- истощение и не -ответа secondary non-depletion and non-response (2NDNR), который был результатом развившейся иммуногенности к Ритуксимаб и могут быть преодолены путем альтернативных анти CD20 mAbs, особенно гуманизированных. Таким образом цели исследования были для оценки факторов, предсказывая первичных и вторичных не- ответ ритуксимаба при СКВ, включая проверку B-клетки истощения и проведения оценки ведения 2NDNR с использованием альтернативных анти CD20 агентов.
Методы
Пациентов и дизайн
Проспективное обсервационное исследование было проведено с умеренной до тяжелой SLE всех пациентов, которые лечились с ритуксимаба в Лидсе между января 2004 года и июль 2016. Критериям включения в обзор включен взрослых (> 16 лет); revised 1997 American College of Rheumatology classification критерии для СКВ и интервал по крайней мере 6 месяцев пост- ритуксимаба использования.
Протокол лечения
Все пациенты получили первый цикл терапии, состоящий из 100 мг метилпреднизолона и 1000 мг ритуксимаба внутривенно на 1 и 14 дней. Дополнительные циклы подобной схемы были повторены на клинических рецидива (определено ниже).
Из тех, кто отвечал 2NDNR критериям, их лечение было перешли от ритуксимаба в гуманизированные анти CD20 mAbs с помощью либо 2 × 1000 мг ocrelizumab или 2 × 700 мг ofatumumab .
Клинические данные и результаты
Активность заболевания была оценена с помощью British Isles Lupus Assessment Group (BILAG-2004) на исходном уровне и раз в 3 месяца. Клинической ответ через 6 месяцев были определены следующие: (1) Основные клинические ответ = улучшение всех доменов, оценили A / B класс C/лучше и не A / B обострения между базовым и 6 месяцев; (2) частичное клинический ответ = максимальная 1 домена с стойкого класса B с улучшением всех других доменов и не A или B обострения и (3)-ответ = те не отвечают критериям для общей или частичное клинической реакции. Рецидив был определен как новый класс или повторения ≥1 класса B после либо общим/частичный клинический ответ через 6 месяцев. Глобальная оценка BILAG была рассчитана следующим образом: класс A = 12, B = 8 класс, класс C = 1 и классы D и E = 0.
Лаборатория оценки
Периферической крови B-клетки набор (наивными, памяти B-клетки и plasmablasts) были измерены с помощью HSFC как описано в начале, 6 месяцев и каждые 6 месяцев без изучения клинического статуса помимо момента начала ритуксимаба. Полное истощение B-клеток было определено как количество < 0,0001 × 10
9/L и репопуляция как ≥0.0001 × 10
9/ Л.
Титры антител анти dsDNA были измерены ELISA до июля 2012 года и иммуноанализа Bioplex 2200 (после июля 2012 года). Нефелометрия измерялись уровни комплемента (C3 и C4) и общая сыворотки иммуноглобулина титры.
Анти ритуксимаба антитела были протестированы на группе больных с 2NDNR с использованием Promonitor ИФА Anti-ритуксимаба® согласно инструкциям производителя и сравнить эти концентрации у тех с продолжение ответ ритуксимаба. Положительный тест (как это определено изготовителем) была концентрация> 140 AU/мл.
Безопасность
Серьезные инфекции были описаны независимо от предполагаемых ассоциации с СКВ и/или терапии. Это были инфекций, которые привели к госпитализации на > 24 часа или требовали внутривенное введение антибиотиков. Сведения о других оценки безопасности можно найти в Интернете дополнительные файлы.
Результаты
Характеристики пациентов
125 больных с СКВ, которые лечились с rituximab на наши подразделения были изучены 117 пациентов с анализу данных за 6 месяцев. Базовые характеристики описаны в
таблице 1. Сто двенадцать (96%) имел ркфрактерное и активной болезни как определено BILAG ≥1A Оценка и/или ≥2B баллов. Остальные пять были BILAG B в одном домене только но был рефрактерным других обычных методов лечения, а также поддерживающее лечение с мг ≥10 оральный преднизолона ежедневно. Общая наблюдение составило 492 пациено-лет.
Таблица 1
Исходные характеристики 117 больных СКВ, получавших Ритуксимаб
| Возраст первой инфузии RTX, медиана (ИКР) лет |
39 (26-52) |
| №. Женский пациент (%) |
109 (93) |
| Этничность и идентичность, N (%) |
| Кавказская |
80 (68) |
| Афро карибские |
11 (10) |
| Южной Азии |
20 (17) |
| Другие |
6 (5) |
| Продолжительность болезни СКВ до первого RTX, медиана (ИКР) лет |
6 (2 – 11) |
| ANA положительный диагноз, N (%) |
117 (100) |
| Антитело статус при первый RTX инфузии, N (%) Положительные |
108 (92) |
| анти dsDNA |
56 (48) |
| Анти Ro |
57 (49) |
| Анти La |
18 (15) |
| Анти Smith |
15 (13) |
| Анти-хроматину Anti-Chromatin |
19 (16) |
| Анти RNP |
23 (20) |
| Анти рибосомной P Anti-Ribosomal P |
6 (5) |
| Анти Cardiolipin/антиB2-гликопротеина |
14 (12) |
| Предшествующая терапия CYC, N (%) |
63 (54) |
| Суммарная доза CYC, среднее ± SD грамм |
6.6 ± 4,2 |
| Количество предыдущих иммунодепрессанта неэффективность (включая CYC, но исключая глюкокортикоидов), средний (диапазон) |
3 (0 – 9) |
| Сопутствующие противомалярийных препаратов, N (%) |
88 (75) |
| Сопутствующие иммунодепрессанта, N (%) |
| Азатиоприн |
19 (16) |
| Метотрексат |
16 (14) |
| Микофенолата мофетил |
39 (33) |
| Доза преднизолона при первой инфузии RTX, медиана (ИКР) мг |
10 (3-20) |
| СОЭ на первом RTX инфузии, медиана (IQR) мм/час |
29 (15 – 57) |
| BILAG показатель на базовом, N (%) |
| A Оценка ≥1 |
96 (82) |
| Оценка не A но ≥2 B баллы |
16 (14) |
| BILAG домены на базовом, N (%) |
Класс A |
Класс B |
| Общие |
9 (8) |
12 (10) |
| Кожно-слизистый |
23 (20) |
32 (27) |
| Неврологические |
17 (15) |
17 (15) |
| Опорно-двигательного аппарата |
30 (26) |
24 (20) |
| Кардиореспираторный |
6 (5) |
13 (11) |
| Желудочно-кишечного тракта |
6 (5) |
0 (0) |
| Офтальмология |
0 (0) |
0 (0) |
| Почечная |
34 (29) |
0 (0) |
| Гематология |
11 (9) |
12 (10) |
| Глобальный BILAG оценка, медиана (IQR) |
21 (14 – 27) |
| SLEDAI – 2K оценка, медиана (IQR) |
10 (6-14) |
| SLICC повреждения индекс, медиана (IQR) |
0 (0-1) |
- ANA, antinuclear antibody антиядерное антитело; BILAG, British Isles Lupus Assessment Group CYC, циклофосфамид; dsDNA, double-stranded DNA; ESR, erythrocyte sedimentation rate, СОЭ; RNP, ribonucleic protein рибонуклеиновой белка; RTX, rituximab Ритуксимаб; SLEDAI – 2K, Systemic Lupus Erythematosus Disease Activity Index 2000 индекс активности болезни системная красная волчанка 2000; SLICC, Systemic Lupus International Collaborating Clinics системная волчанка международных сотрудничающих клиники (SLICC).
Обсуждение
Клинические задачи для использования ритуксимаба в СКВ включают в себя определение подгруппы больных склонны реагировать на первоначальные и последующие циклы и стратегии оптимального повторного лечения. Анализ данных всех больных СКВ, которые лечились с ритуксимаба в этой крупнейшей сообщил когорты, а также долгосрочное наблюдение, это исследование предлагает понимание прагматического применения ритуксимаба и имеет последствия для будущего развития целевой терапии.
В этом исследования, только последовательное предсказатель любого (и крупных) клинический ответ на ритуксимаба является истощение B-клетки (измеренные с помощью HSFC) через 6 недель пост Ритуксимаб, который мы теперь проверяются независимым когорты. Это подчеркивает иммуномодулирующим действием ритуксимаба в исправлении аутоиммунных B-клеточной функции и нормализации аутоантител титры и дополнения уровнях без увеличения риска тяжелой инфекции. С точки зрения лечения стратификации наши данные поддерживают обоснование для B-клетки мониторинг во время терапии. Таким образом до Ритуксимаб, путем оценки пациентов для уровней низкого дополнением и выше плазмоциты, лечение модификации могут быть использованы для улучшения истощение, либо путем увеличения дозы или добавляя дополнительные вливания, как мы ранее показал в РА. Наступление в 6 недель пост Ритуксимаб, полного истощения является маркером хорошего ответа на терапию. Для тех, кто с неполной истощение необходим тщательный мониторинг. На 6 месяцев пост Ритуксимаб, заселение плазмоцитов от > 0,0008 × 10
9/L увеличивает риск клинических рецидивов в течение следующих 6 месяцев. Таким образом эти пациенты могут рассматриваться для раннего повторного курса с целью уменьшить повреждающее действие повышенного числа B-клеток и добиться повышения истощения в последующем цикле. Важно отметить, что для тех, кто с плазмацитов ≤0.0008 × 10
9/ L на 6 месяцев, мониторинг клинических рецидив представляется приемлемой стратегии.
Независимо от ответа около 12% впоследствии развился 2NDNR в C2. Это явление связано с образованием антитела к ритуксимабу. Однако измерения антитела анти ритуксимаба изолированно недостаточно для выявления больных как 2NDNR, как более половины пациентов, которые были протестированы положительный имели клинический ответ в именно этого цикла. Напротив, клинические проявления, то есть, тяжелой инфузионные реакции и не-ответчики и измерения B-клетки, более значимымы. Отсутствие оральных иммунодепрессантов и повышение pre ритуксимаба плазмоцитов предсказал 2NDNR. Назначение оральных иммунодепрессанта было решено по усмотрению врача, но наши данные указывают, что они могут иметь определенную роль в предотвращении иммуногенность. Точный механизм для ассоциации с количеством плазмацитов неизвестен, но плазмоциты являются маркерами для активации общей B-клеток. После первоначального истощения с Ритуксимаб увеличения уровни фактор B-клеток активация и способствуют формированию плазмоцитов (plasmablasts). Раннего увеличение plasmablasts увеличивает образование фолликулярные клетки Т-хелперов, таким образом создавая положительной обратной связью, которая закрепляет антитела- обусловленное воспаление и может объяснить, почему у некоторых пациентов стать рефрактерность ритуксимаба в СКВ.
После 2NDNR Ритуксимаб переход на humanised анти CD20 mAbs восстанавливает истощения и ответ в СКВ. Ocrelizumab и ofatumumab являются оба типа 1 анти CD20 mAbs. Первичной конечной точкой был встречен в ocrelizumab лечение групп РА и изучался при СКВ. Однако, развитие этих показаний был остановлен после увеличения в оппортунистические инфекции, некоторые из которых со смертельным исходом сообщалось. Все три пациента в нашем исследовании с большим клинических ответов и продолжительной ремиссии над 5-летний период пост- ocrelizumab. Ofatumumab имеет показания для устойчивых хронический лимфоцитарный лейкоз и продемонстрировала эффективность в РА. , которые оба пациента в нашем исследовании хорошо реагировали на ofatumumab включен один, кто достиг полного истощения в первый раз от разрушающих B-клеточной терапии. Кроме того несколько наблюдателей недавно сообщили о его эффективности в внепочечная и рефрактерном волчаном нефрите. Кроме того другие анти CD20 агентов с расширенной антитела зависимой клеточной цитотоксичности могут быть более эффективными при СКВ.
In vitro obinutuzumab продемонстрировал, что расширение истощения была достигнута при 2 типа mAb,, по сравнению с rituximab.
Это исследование имеет ряд ограничений. Во-первых, могло произойти межнаблюдательная изменчивость в BILAG оценках за длительность последующих и когорты, которое было весьма неоднородным в проявления волчанки. Однако BILAG оценки отражает намерение врача для лечения, и пациенты наблюдались в выделенный единого центра, таким образом позволяя для последовательно оценивать. Во-вторых, B-клетки и лабораторных данных были утеряны в некоторых случаях. Как они были сочтены недостающие наугад, несколько условных расчетов использовался для снижения потенциальных отклонений в оценивание параметров, а также повышения применимости результатов. Далее, сочетанной терапии с иммунодепрессанта были использованы в более чем 60% пациентов, таким образом эффективность не может быть присвоено только ритуксимаба. И наконец отсутствие контрольной группы ограничивает толкование эффективность и безопасность ритуксимаба.
В заключение лечение с анти CD20 агенты могут проводиться под мониторинг B-клеток, с целью достижения полного истощения. Приблизительно один из восьми больных СКВ потерять истощения на повторных циклов ритуксимаба независимо от предварительного ответа и вторичных не истощение связано с антител анти ритуксимаба anti-rituximab antibodies. Сопутствующие оральные иммунодепрессанты могут помочь предотвратить это. Если 2NDNR возникает, переход на humanised анти CD20 mAbs восстанавливает истощения и ответ. Таким образом альтернативные анти CD20 антитела могут быть более последовательно эффективным в лечении СКВ и несколько текущих исследований проводятся в решении этих вопросов.
Комментарий и ссылка для практики.
Современные методы оценки активности системной красной волчанки
Е.А. Асеева, С.К. Соловьев, Е.Л. Насонов
«BILAG, SLEDAI, SIS, ECLAM, WAM, SLAM… Thank you MAM», – так известный британский ревматолог David Isenberg озаглавил свою статью, опубликованную в журнале Lupus в 2007 г. [1]. Действительно, в настоя-щее время можно растеряться от разнообра-зия аббревиатур и акронимов, связанных с индексами активности системной красной волчанки (СКВ), которые играют важную роль в оценке состояния пациента, в своевре
менном назначении адекватной терапии, в прогнозировании исходов заболевания,
проведении клинических исследований. Все современные индексы активности СКВ основаны на количественной оценке различных комбинаций клинических и лабо-раторных признаков заболевания и были раз-работаны с целью стандартизации оценки со-стояния больного. В литературе описано бо-лее 60 различных индексов активности, но большинство из них не были валидирова-ны [1, 2]. Только пять индексов активности СКВ прошли валидацию и широко использу-ются в мировой медицинской лечебной и на-учной практике [3]:
1. SLE Disease Activity Index (SLEDAI) [4].
2. Systemic Lupus Activity Measure (SLAM) [5].
3. European Consensus Lupus Activity Measurement (ECLAM) [6].
4. Lupus Activity Index (LAI) [7].
5. Classic British Isles Lupus Assessment Group Index (Classic BILAG Index) [8].
Выделяют два типа индексов активно-сти СКВ. К первому относятся методы опре-деления общей активности заболевания. Для каждого из них итоговое значение пред-ставляет собой сумму баллов исходных пока-зателей (SLEDAI, SLAM и ECLAM и т. д.).
Ко второму типу относятся специфиче-ские индексы, оценивающие активность или выраженность обострения в каждом отдель-ном органе или системе (BILAG и SFI-R).
Поскольку индекс BILAG учитывает на-мерение врача назначить тот или иной вид те-рапии, он был признан в 2010 г. Управлением по контролю за пищевыми продуктами и ле-карственными препаратами (FDA) США предпочтительным для использования при проведении клинических исследований [9]. Для оценки активности СКВ FDA рекоменду-ет использовать и другие индексы (SLEDAI, SLAM и ECLAM), а также их модификации. В последнее десятилетие при проведении научных исследований большое внимание уде-ляется индексам SLEDAI, BILAG, а также их модификациям еще и в связи с тем, что они являются составляющими частями индексов обострения (SFI) и ответа на терапию (SRI). В связи с этим в данной статье мы уделим им более пристальное внимание.
Systemic Lupus Erythematosus
Disease Activity Index (SLEDAI)
Этот индекс оценки общей активности заболевания был разработан в 1985 г. на сове-щании в Торонто с привлечением 15 ведущих мировых экспертов по СКВ [1, 3]. На основа-нии заполнения анкет, включающих 37 кли-нических признаков СКВ, были выявлены 24 основных (16 клинических и 8 лаборатор-ных) показателей СКВ, которые и вошли в SLEDAI. Путем множественного регресси-онного анализа данных 574 пациентов значи-мость каждого из этих признаков была опре-делена в баллах от 1 до 8. Более серьезные проявления СКВ, такие как поражение нерв-ной системы, поражение почек, васкулит, имеют более высокую балльную оценку, чем другие признаки. Максимально возможное значение SLEDAI составляет 105 баллов [4, 10]. Для оценки активности по SLEDAI необ-ходимо отмечать признаки СКВ, которые присутствовали у пациента в течение 10 пред-шествующих осмотру дней, независимо от степени их тяжести, улучшения или ухудше-ния состояния. По индексу SLEDAI выделя-ют следующие степени активности СКВ: нет активности (SLEDAI 0 баллов), низкая актив-ность (SLEDAI 1–5 баллов), средняя степень активности (SLEDAI 6–10 баллов), высокая степень активности (SLEDAI 11–19 баллов) и очень высокая степень активности (SLEDAI >20 баллов). Увеличение SLEDAI между дву-мя визитами на 3–12 баллов интерпретирует-ся как умеренное обострение, более чем на 12 баллов – как тяжелое обострение СКВ [10, 11]
В настоящее время широко используют-ся три модификации индекса SLEDAI: SLEDAI 2000 (SLEDAI 2K), SELENA-SLEDAI и Mex-SLEDAI.
Mex-SLEDAI
Разработан J. Guzman и соавт. в 1992 г. [12] в первую очередь для использования в развивающихся странах, из-за затруднений определения уровня антител к ДНК и компо-нентов комплемента. Он включает 13 призна-ков вместо 24: поражение нервной системы, почек, кожи и слизистых оболочек, васкулит, 186 Науч-практич ревматол 2013; 51(2): 186–200 гемолиз, тромбоцитопению, миозит, артрит, серозит, лихо-радку, усталость, лейкопению и лимфопению. Значение Mex-SLEDAI может варьировать от 0 до 32 баллов. Счет <2 баллов показывает неактивное заболевание, от 2 до 5 – возможную активность, >5 баллов – явную активность за-болевания [12, 13]. Этот индекс и в настоящее время актив-но используется в латиноамериканских странах для опре-деления активности СКВ [11–13].
SLEDAI 2000 (SLEDAI 2K)
Модифицирован D. Gladman и соавт. в 2002 г. [14]. Внесены изменения в регистрацию следующих признаков: протеинурия >0,5 г/сут, кожные высыпания, алопеция, яз-вы слизистых оболочек. SLEDAI-2K, в отличие от SLEDAI, позволяет учитывать персистирующую актив-ность, в то время как SLEDAI учитывает только возникно-вение или рецидив этих признаков.
SELENA-SLEDAI
Модифицирован в 2005 г. J. Buyon и соавт. во время проведения исследования SELENA (Safety of Estrogens in Lupus Erythematosus National Assessment) [15]. SELENA-SLEDAI, так же как и SLEDAI 2K, учитывает персистиру-ющую активность, связанную с наличием высыпаний, язв слизистых оболочек и алопеции, и, кроме того, предусмат-ривает следующие изменения: в число признаков пораже-ния черепных нервов дополнительно включает «голово-кружение»; позволяет зафиксировать наличие плеврита или перикардита по одному из представленных в SLEDAI признаков, а не по комплексу перечисленных симптомов; признак «повышение протеинурии на 0,5 г/сут» учитывает лишь при наличии его возникновения в течении предше-ствующих осмотру пациента 10 дней.
SELENA Flare Index (SFI)
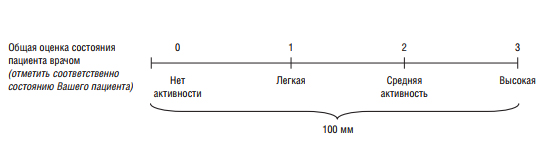
Исследование SELENA впервые определяет индекс обострения SELENA (SELENA Flare Index – SFI), который позволяет выделять умеренную и тяжелую степени обост-рения СКВ. SFI учитывает динамику активности заболева-ния по шкале SELENA-SLEDAI, изменение общей оценки состояния пациента врачом (physician’s global-assessment visual-analogue scale – PGA), модификацию схем терапии и ряд клинических параметров. Выраженность обострения выставляется при наличии хотя бы одного из перечислен-ных признаков.
SELENA предусматривает использование общей оценки состояния пациента врачом по 100-миллиметровой визуальной аналоговой шкале (ВАШ), на которой обозна-чены градации от 0 до 3, где 0 означает неактивное заболе-вание, а 3 – заболевание с высокой активностью (Прило-жение 1).
В последнее время термин «определение активности по шкале SELENA-SLEDAI» включает в себя оценку ак-тивности SELENA-SLEDAI, общую оценку состояния па-циента врачом по ВАШ (PGA) и индекс обострения SFI.
SFI-R (SFI-revised)
В 2009 г. по инициативе Lupus Foundation of America’s International Flare Definition and Validation индекс обостре-ния SELENA был пересмотрен с целью разграничения лег-кой и средней степени обострения СКВ. Также возникла необходимость в более точном определении тяжелой сте-пени обострения, поскольку исходный его вариант не удовлетворял требованиям клинических исследований. В 2009 г. на Конгрессе Американской коллегии ревматоло-гов (ACR) в Филадельфии М. Petri и соавт. представили пересмотренный индекс обострения SELENA, так называе-мый SFI-R (SFI-revised). SFI-R не связан ни индексами общей активности заболевания, включая SLEDAI, PGA, ни со специфическим индексом BILAG [16]. Это самосто-ятельный индекс, оценивающий изменение активности СКВ по 8 органам и системам: кожа и слизистые оболочки; костно-мышечная; сердечно-легочная система; система крови; конституциональные; почки; нервная система; же-лудочно-кишечный тракт. Для каждой системы органов, вовлеченной в процесс заболевания, оценивается степень обострения – обострение отсутствует, легкое, умеренное или тяжелое. В представленной в Приложении 2 таблице необходимо отметить «клиническое проявление», соответ-ствующее данному обострению в исследуемой системе по принципу «впервые появившийся признак», «ухудшение» или «рецидив». Также необходимо отметить «любое из те-рапевтических мероприятий», которое проведено в связи с данным клиническим проявлением. На основании соче-тания «клинического проявления» и «любого из терапев-тических мероприятий» выставляются степени обострения СКВ. Если «любое из терапевтических мероприятий» соот-ветствует более тяжелой степени обострения, чем «клини-ческое проявление», то степень обострения выставляется на основании «любого из терапевтических мероприятий».
Итоговое обострение, учитывающее несколько органов и си-стем, выставляется по присутствию наиболее выраженной степени обострения.
BILAG
В 1984 г. в Великобритании после ряда неформаль-ных обсуждений была создана группа BILAG (British Isles Lupus Assessment Group), в которую вошли ведущие специ-алисты-ревматологи страны: Paul Bacon (Университет Бир-мингема), John Coppock (Университет Эдинбурга), David Isenberg (Университетский колледж, Лондон), Peter Maddison (Национальный Королевский госпиталь ревма-тических заболеваний, Баз), Michael Snaith (Университет-ский колледж, Лондон), Deborah Symmons (Университет Бирмингема) и Asad Zoma (Университет Глазго).
Они считали, что для лучшего понимания течения и исходов СКВ необходимо оценивать активность заболе-вания (т. е. клинические проявления СКВ с обратимым по-тенциалом) и повреждения (необратимые изменения, вы-зываемые самим заболеванием или последствием тера-пии), а также иметь возможность получить информацию о собственной оценке пациентом своего заболевания. Та-кая концепция не укладывалась в понятие разработки ин-декса общей активности заболевания, поэтому целью ста-ла разработка индекса активности СКВ, который «дал бы точную, надежную и проверенную оценку в широком диа-пазоне органов или систем» [1].
В 1988 г. опубликована его первая версия [17], в кото-рой практически сразу был выявлен целый ряд недостат-ков. В 1993 г. Е. Hay и соавт. [18] опубликовали широко из-вестную версию индекса, так называемый Классический индекс BILAG. Он содержит 86 признаков СКВ и оценива-ет изменения по 8 органам и системам: общие; кожи и сли-зистых оболочек; нервной; костно-мышечной, сердечно-легочной систем, васкулита, почек и гематологические на-рушения. Регистрируется динамика симптомов СКВ за по-следний месяц в сравнении с предыдущим. Этот индекс уже может улавливать переход тяжелых признаков СКВ в более легкие и наоборот, за исключением лабораторных
Науч-практич ревматол 2013; 51(2): 186–200 187 показателей и нескольких симптомов, которые регистри-руются по принципу «Да» или «Нет». Активность заболева-ния делится на пять классов:
A – высоко активное заболевание, требующее назна-чения иммуносупрессивной терапии или пред-низолона в дозе >20 мг/сут;
B – среднеактивное заболевание, требующее назна-чения низких доз преднизолона (<20 мг/сут), или антималярийных препаратов, или нестероидных противовоспалительных препаратов (НПВП);
С – стабильно низкая активность заболевания;
D – нет активности заболевания в настоящее время, но система была ранее вовлечена в процесс;
E – нет активности заболевания в настоящее время, орган не вовлечен и ранее в процесс не вовлекался.
За 20 лет, прошедшие после появления классическо-го варианта индекса BILAG, существенно изменилось по-нимание целого ряда проявлений СКВ. В частности, было показано, что поражение глаз и желудочно-кишечного тракта при СКВ встречается гораздо чаще, чем считалось в прошлом, и отрицательно влияет на прогноз заболева-ния. Установлено, что миелопатия может быть обусловле-на не только воспалительными изменениями, но и нару-шениями микроциркуляции в результате тромбоза сосу-дов. Такие признаки, как асептический некроз, склеродак-тилия, телеангиэктазия и сухожильные контрактуры, в на-стоящее время рассматриваются как необратимые наруше-ния, которые не позволяют судить об активности заболева-ния [19–21]. Поэтому индекс был модифицирован. Его предварительная версия появилась в 2004 г. и получила на-звание «Индекс BILAG-2004» [22].
Индекс BILAG-2004 содержит 102 признака СКВ и оценивает изменения по 9 органам и системам: консти-туциональные; кожи и слизистых оболочек; нейропсихи-ческие; скелетно-мышечные; сердца и дыхательной систе-мы; желудочно-кишечные; офтальмологические; измене-ние почек и гематологические нарушения. К проверке но-вого индекса помимо английских специалистов были под-ключены 37 экспертов из группы SLICC (System Lupus International Collaborating Clinics).
В 2008–2009 гг. Yee Chee-Seng и соавт. провели мно-гоцентровую (8 центров) оценку индекса BILAG-2004 в ре-альной клинической практике на 444 пациентах. Результа-том этой работы стало создание последней версии индекса BILAG-2004 (модификация Yee Chee-Seng и соавт. 2009 г.), который в настоящее время широко используется в науч-ной и клинической практике ведущих мировых клиник [3, 23].
BILAG-2004 (модификация Yee Chee-Seng и соавт. 2009 г.) содержит 97 признаков СКВ и также оценивает из-менения по 9 органам и системам: конституциональные; кожи и слизистых оболочек; нейропсихические; скелетно-мышечные; сердца и дыхательной системы; желудочно-кишечные; офтальмологические; изменения почек и гема-тологические нарушения.
Использование индекса BILAG без общего числово-го счета достаточно затрудняло проведение статистическо-го анализа, особенно при сопоставлении результатов оцен-ки по индексу BILAG со SLEDAI и SLAM [3]. Поэтому с 90-х годов ХХ в. применялась следующая кодировка, ко-торая давала возможность провести сравнительный анализ значений индексов: А=9, В=3, С=1, D/E=0 баллов [24]. Эта кодировка не была валидирована, и поэтому в 2009 г. L. Cresswell и соавт. [25] провели исследование на 369 па-циентах с СКВ, которые были оценены 1510 раз по индек-су Классический BILAG. На основании этого наблюдения была присвоена следующая кодировка индексу Классиче-ский BILAG: А=12, В=5, С=1, D/E=0 баллов. В 2010 г. Yee Chee-Seng и соавт. [26], сравнив схему числового кодиро-вания индексов Классический BILAG и BILAG-2004, при-шли к выводу, что они различаются в градации В. Поэтому индексу BILAG-2004 была присвоена следующая кодиров-ка: А=12, В=8, С=1, D/E=0 баллов.
Индекс активности BILAG-2004 (модификация Yee Chee-Seng и соавт. 2009 г.; см. Приложение 3).
Состоит из перечня признаков СКВ, разделенных по 9 системам; терминологического словаря (Приложение 4) и компьютерной программы, позволяющей мгновенно об-рабатывать индекс.
Разработаны следующие правила заполнения индек-са BILAG-2004.
• Отмечаются только симптомы, связанные с актив-ностью СКВ, а не вызванные повреждением, ин-фекцией, тромбозом (в отсутствие воспалительно-го процесса) или другими состояниями.
• Оцениваются проявления СКВ, имеющие место в течение 4 нед до момента обследования по отно-шению к 4 предшествующим неделям.
• Термин «активность СКВ» относится к обратимым нарушениям, в то время как необратимые измене-ния рассматриваются как повреждение.
• Для определения повреждения следует опериро-вать индексом повреждения SLICC/ACR, который учитывает признаки, сохраняющиеся ≥6 мес.
• В некоторых ситуациях при возникновении трудно-стей в дифференцировке имеющихся проявлений СКВ от других причин, когда отсутствуют специфи-ческие признаки, решение принимает врач, осно-вываясь на своем опыте и балансе вероятностей.
• Офтальмологические проявления, как правило, должны оцениваться специалистом-офтальмологом и регистрироваться ретроспективно после по-лучения ответа от офтальмолога.
Руководство для подсчета баллов: каждый из 97 при-знаков, входящих в индекс, должен быть отмечен, как: 4 – «вновь возникший», 3 – «ухудшение», 2 – «без измене-ний», 1 – «улучшение», 0 – «отсутствует» или ND – «не проводилось».
«Вновь возникший» (4) отмечается в том случае, если:
– это новый симптом, возникший в течение послед-них 4 нед (по сравнению с предшествующими 4 нед), который не улучшается и включает в себя как совсем новые симптомы СКВ, так и рецидив старых проявлений;
– новый симптом, возникший в последние 4 нед, удовлетворяющий критериям улучшения (см. да-лее), классифицируется как улучшение, а не новое
проявление СКВ.
«Ухудшение» (3) отмечается в том случае, если прояв-ления ухудшились в последние 4 нед по сравнению с пред-шествующими 4 нед.
«Без изменений» (2) отмечается в том случае, если:
– проявления присутствовали в течение последних 4 нед и остались без значительного улучшения или ухудшения по сравнению с предшествующими 4 нед; 188 Науч-практич ревматол 2013; 51(2): 186–200
– проявления улучшились за последние 4 нед по сравнению с предшествующими 4 нед, но не отве-чают критериям улучшения.
«Улучшение» (1) отмечается в том случае, если:
– степень улучшения достаточно велика для рассмо-трения сокращения терапии и не оправдывает эс-калацию терапии (А);
– улучшение должно присутствовать в настоящее время и в течение по крайней мере двух из послед-них 4 нед или проявления полностью разрешились и отсутствуют в течение последней недели наблю-дения (Б).
«Отсутствует» (0) – отмечается в случае отсутствия признака.
«Не проводилось» (ND) относится к лабораторным ис-следованиям.
Если тест не проводился, важно указать это (в част-ности, лабораторные исследования), поскольку даже от-сутствие данных учитывается при подсчете результата.
Восемь признаков поражения почек (78–79, 81–87) и пять признаков гематологических нарушений (90–94) необходимо отметить, если они не связаны с активностью, а служат проявлением другого заболевания.
Изменение категории тяжести. Есть несколько пунк-тов в индексе, предусматривающих выделение легкой и тя-желой степени соответствующего признака. При этом:
1. Если признак, имевший легкую степень тяжести, в течение последних 4 нед ухудшился до тяжелой, то в пун-кте, соответствующем категории тяжелой степени, отмеча-ется: «вновь возникший» (4), а в пункте, соответствующем категории легкой степени, отмечается: «ухудшение» (3).
2. Если признак, имевший тяжелую степень, в тече-ние последних 4 нед улучшился до легкой, то в пункте, со-ответствующем категории тяжелой степени, отмечается: «нет» (0), если критерии для тяжелой степени тяжести от-сутствовали в течение последних 4 нед, или «улучшение» (1), если критерии тяжелой степени еще наблюдались в ка-кой-то момент в течение последних 4 нед, и признак, имевший легкую степень тяжести, отмечается как «улуч-шение» (1), если он улучшился в течение последних 4 нед; как «без изменений», если он остается стабильным на про-тяжении 4 нед наблюдения.
Активность заболевания делится на 5 классов – от А до Е (см. таблицу).
По представленной градации оценивается каждая из 9 систем и по сумме баллов определяется общая актив-ность заболевания.
Поскольку вычисление индекса BILAG является дос-таточно трудоемкой задачей, Nick Viner практически сразу создал его компьютерную версию. В дальнейшем, в 1996 г., результатом сотрудничества между группой BILAG и IT-компанией ADS-Limathon стало создание специально раз-работанной компьютерной программы для оценки паци-ентов с СКВ, так называемой British Lupus Integrated Prospective System (BLIPS). В настоящее время она пред-ставляет собой расширенную базу данных, содержащую калькуляторы для вычисления различных индексов актив-ности (SLAM, ECLAM, SLEDAI, BILAG) и повреждения СКВ (SLICC), а также для оценки качества жизни пациен-тов с СКВ по опросникам SF-36 и LupusQol. Она доступна как на CD-носителях, так и в онлайн режиме (i-BLIPS; Silver-BLIPS). Эту базу используют многие университеты Великобритании, США, Европы, занимающиеся изучением СКВ. Ее можно приобрести, обратившись к Гордону Га-мильтону (Gordon.Hamilton@limathon.com). Возможна также ручная обработка индекса BILAG [3, 10, 25, 26].
SRI
Большое разнообразие представленных выше индек-сов, а также их модификаций говорит прежде всего о том, что до настоящего времени еще не создан совершенный ме-тод оценки столь непредсказуемого и сложного в понима-нии заболевания, как СКВ. Существующие индексы оказа-лись недостаточно чувствительными для выявления эффекта генно-инженерных биологических препаратов (ГИБП). На первых этапах клинических исследований (II фаза) не было выявлено различия между группами, получающими плацебо и белимумаб, при использовании индекса SELENA-SLEDAI и SFI [29]. Но при индивидуальной оценке были выделены серологически активные пациенты, которые хорошо ответили на терапию белимумабом. Поэ-тому в 2009 г. поднимается вопрос о создании Systemic Lupus Erythematosus Responder Index (SRI), который дол-жен одновременно выявлять улучшение и ухудшение в раз-личных органах и системах. R. Furie и соавт. [30] разработа-ли такой индекс и валидировали его на 449 пациентах в рандомизированном двойном слепом плацебоконтролируемом исследовании трех доз белимумаба (1, 4, 10 мг/кг) и плацебо. Пациент считается ответившим на терапию, если у него в динамике соблюдаются следующие три принципа:
1. Уменьшился счет SELENA-SLEDAI на ≥4 балла от исходного уровня.
2. Отсутствует новое повреждение органа, соответст-вующее классу А по BILAG, или отсутствует появ-ление новых двух и более признаков повреждения органа класса В по BILAG по сравнению с исход-ным уровнем.
Классы активности заболевания по индексу BILAG-2004
Класс Определение
А Заболевание с высокой степенью активности, требующее назначения одного из следующих видов терапии:
1) высоких доз глюкокортикоидов (ГК) внутрь (эквивалентной >20 мг преднизолона в день)
2) пульс-терапии ГК внутривенно (эквивалентной ≥500 мг метилпреднизолона)
3) иммуномодуляторов, включая биологическую терапию, внутривенное введение иммуноглобулина и плазмаферез
4) высоких доз антикоагулянтов в сочетании с высокими дозами ГК и иммуномодуляторов
В Заболевание средней степени активности, требующее назначения одного из следующих видов терапии:
1) низких доз ГК внутрь (эквивалентных <20 мг преднизолона в день)
2) внутримышечного или внутрисуставного введения ГК в дозе, эквивалентной <500 мг метилпреднизолона в день
3) наружного применения ГК
4) наружного применения иммуномодуляторов
5) антималярийных препаратов, или талидомида,
или прастерона, или ацитретина
6) симптоматической терапии (НПВП для лечения артрита)
С Заболевание с легкой степенью активности
D Нет настоящей активности заболевания, но система была ранее вовлечена в процесс
E Система никогда не была повреждена
Науч-практич ревматол 2013; 51(2): 186–200 189
3. Отсутствует ухудшение по шкале общей оценки со-стояния пациента врачом (допустимо увеличение
не более чем на 0,3 пункта от исходного уровня). Индексы активности СКВ играют важную роль не только в оценке реального клинического статуса пациента, определении прогноза и выборе терапии, но и в оценке эф-фективности новых методов лечения этого заболевания. Впервые за последние 50 лет в фармакотерапию СКВ ак-тивно внедряется новый класс лекарственных препаратов:
Л И Т Е Р А Т У Р А
1. Isenberg D. BILAG, SLEDAI, SIS, ECLAM, WAM, SLAM… Thank you MAM. Lupus 2007;16:849–51.
2. Liang M.H., Socher S.A., Roberts W.N. et al. Measurement of systemic lupus erythematosus activity in clinical research. Arthr Rheum 1988;31:817–25.
3. Yee Chee-Seng. Development and validation of the BILAG-2004 Index for the assessment of disease activity in SLE. Rheumatology Research Group Division of Infection and Immunology, School of Medicine, The University of Birmingham. A thesis submitted to The University of Birmingham for the degree of doctor of philoso-phy. 2008; February.
4. Bombardier C., Gladman D.D., Urowitz M.B. et al. Derivation of the SLEDAI. A disease activity index for lupus patients. The Committee on Prognosis Studies in SLE. Arthr Rheum 1992;35:630–40.
5. Liang M.H., Socher S.A., Larson M.G. et al. Reliability and valid-ity of six systems for the clinical assessment of disease activity in systemic lupus erythematosus. Arthr Rheum 1989;32:1107–18.
6. Vitali C., Bencivelli W., Isenberg D.A. et al. Disease activity in sys-temic lupus erythematosus: report of the Consensus Study Group of the European Workshop for Rheumatology Research. II. Identification of the variables indicative of disease activity and their use in the development of an activity score. The European Consensus Study Group for Disease Activity in SLE. Clin Exp Rheumatol 1992;10:541–7.
7. Petri M., Hellmann D., Hochberg M. Validity and reliability of lupus activity measures in the routine clinic setting. J Rheumatol 1992;19:53–9.
8. Hay E.M., Bacon P.A., Gordon C. et al. The BILAG index: a reli-able and valid instrument for measuring clinical disease activity in systemic lupus erythematosus. Q J Med 1993;86:447–58.
9. Guidance for Industry, Systemic Lupus Erythematosus – Developing Medical Products for Treatment. U.S. Department of Health and Human Services. Food and Drug Administration. Center for Drug Evaluation and Research (CDER). Center for Biologics Evaluation and Research (CBER). Center for Devices and Radiological Health (CDRH). 2010; June.
10. Mosca M., Bombardieri S. Assessing remission in systemic lupus erythematosus. Clin Exp Rheumatol 2006;24:100–4.
11. Freire Е.А.М., Souto L.M., Ciconelli R.M. Assessment measures in systemic lupus erythematosus. Rev Bras Reumatol 2011;51:70–80.
12. Guzman J., Cardiel M.H., Arce-Salinas A. et al. Measurement of disease activity in systemic lupus erythematosus. Prospective vali-dation of 3 clinical indices. J Rheumatol 1992;19:1551–8.
13. Khanna S., Pal H., Pandey R.M., Handa R. The relationship between disease activity and quality of life in systemic lupus ery-thematosus. Rheumatology 2004;43:1536–40.
14. Gladman D.D., Ibanez D., Urowitz M.B. Systemic lupus erythe-matosus disease activity index 2000. J Rheumatol 2002;29:288–91.
15. Petri M., Kim M.Y., Kalunian K.C. et al. Combined oral contra-ceptives in women with systemic lupus erythematosus. N Engl J Med 2005;353:2550–8.
16. Petri М., Buyon J., Kalunian K. et al. Revision of the SELENA Flare Index. Arthr Rheum 2009;60, Abstract Suppl The 2009 ACR/ARHP Annual Scientific Meeting. Philadelphia, October 16–21, 2009. 190
ГИБП (ритуксимаб, окрелизумаб, белимумаб), антитела к интерферону (эпратузумаб, атасисепт, тоцилизумаб), ан-титела к Toll-like-рецепторам, антитела к СD40 и др. [31–34]. Применение ГИБП открывает принципиально но-вые подходы к лечению этого заболевания, вселяет надеж-ду на существенное улучшение прогноза и качества жизни. В связи с этим трудно переоценить значимость применения современных индексов активности в оценке эффективно-сти новых лекарственных средств в терапии СКВ.
17. Symmons D.P., Coppock J.S., Bacon P.A. et al. Development and assessment of a computerized index of clinical disease activity in systemic lupus erythematosus. Members of the British Isles Lupus Assessment Group (BILAG). Q J Med 1988;69:927–37.
18. Hay E.M., Bacon P.A., Gordon C. et al. The BILAG index: a reli-able and valid instrument for measuring clinical disease activity in systemic lupus erythematosus. Q J Med 1993;86:447–58.
19. Sivaraj R.R., Durrani O.M., Denniston A.K. et al. Ocular mani-festations of systemic lupus erythematosus. Rheumatology (Oxford) 2007;46:1757–62.
20. Lee C.K., Ahn M.S., Lee E.Y. et al. Acute abdominal pain in sys-temic lupus erythematosus: focus on lupus enteritis (gastrointesti-nal vasculitis). Ann Rheum Dis 2002;61:547–50.
21. Hallegua D.S., Wallace D.J. Gastrointestinal manifestations of systemic lupus erythematosus. Curr Opin Rheumatol 2000;12:379–85.
22. Isenberg D., Rahman A., Allen E. et al. BILAG-2004. Development and initial validation of an updated version of the British Isles Lupus Assessment Group’s disease activity index for patients with systemic lupus erythematosus. Rheumatology 2005;44:902–6.
23. Yee Chee-Seng, Farewell V., Isenberg D. The BILAG-2004 index is sensitive to change for assessment of SLE disease activity. Rheumatology 2009;48:691–5.
24. Stoll T., Stucki G., Malik J. et al. Association of the Systemic Lupus International Collaborating Clinics/American College of Rheumatology Damage Index with measures of disease activity and health status in patients with systemic lupus erythematosus. J Rheumatol 1997;24:309–13.
25. Cresswell L., Yee Chee-Seng, Farewell V. Numerical scoring for the Classic BILAG index. Rheumatology 2009;48:1548–52.
26. Yee Chee-Seng, Cresswell L., Farewell V. Numerical scoring for the BILAG-2004 index. Rheumatology 2010;49:1665–9.
27. Isenberg D.A., Gordon C. From BILAG to BLIPS-disease activity assessment in lupus past, present and future. Lupus 2000;9:651–4.
28. Merrill J.T., Neuwelt C.M., Wallace D.J., Shanahan J. Efficacy and safety of rituximab in moderately-to-severely active systemic lupus erythematosus: the randomized, double-blind, phase II/III systemic lupus erythematosus evaluation of rituximab trial. Arthr Rheum 2010;62:222–33.
Wallace D., Stohl W., Furie R. A phase II, randomized, double-blind, placebo17. controlled, dose-ranging study of belimumab in patients with active systemic lupus erythematosus. Arthr Rheum 2009;61:1168–78.
18. Furie R., Petri M., Wallace D. Novel Evidence-Based Systemic Lupus Erythematosus Responder Index. Arthr Rheum 2009;61:1143–51.
19. Dall’era M., Chakravarty E.F. Treatment of mild, moderate, and severe lupus erythematosus: focus on new therapies. Curr Rheumatol Rep 2011;4:308–16.
20. Tullus K. New developments in the treatment of systemic lupus erythematosus. Pediatr Nephrol 2012;27:727–32.
21. Gunnarsson I., van Vollenhoven R.F. Biologicals for the treatment of systemic lupus erythematosus? Ann Med 2012;44:225–32.
22. Fanouriakis A., Boumpas D.T., Bertsias G.K. Balancing efficacy and toxicity of novel therapies in systemic lupus erythematosus. Expert Rev Clin Pharmacol 2011;4:437–51. Науч-практич ревматол 2013; 51(2): 186–200
Приложение 1
Определение активности СКВ по шкале SELENA- SLEDAI
(Обвести балл, соответствующий проявлению, имевшему место на момент осмотра или в течение 10 предшествовавших осмотру дней)
| Балл |
Проявление |
Определение |
|
|
|
| 8 |
Эпилептический приступ |
Недавно возникший (последние 10 дней). Исключить метаболические, инфекционные и лекарственные причины |
| 8 |
Психоз |
Нарушение способности выполнять нормальные действия в нормальном режиме вследствие выраженного изменения воспри ятия действительности, включая галлюцинации, бессвязность, значительное снижение ассоциативных способностей, истоще ние мыслительной деятельности, выраженное алогичное мышление; странное, дезорганизованное или кататоническое поведе ние. Исключить подобные состояния, вызванные уремией или лекарственными препаратами |
| 8 |
Органические мозговые синдромы |
Нарушение умственной деятельности с нарушением ориентации, памяти или других интеллектуальных способностей с острым началом и нестойкими клиническими проявлениями, включая затуманенность сознания со сниженной способностью к концен трации и неспособностью сохранять внимание к окружающему, плюс минимум два из следующих признаков: нарушение вос приятия, бессвязная речь, бессонница или сонливость в дневное время, снижение или повышение психомоторной активности. Исключить метаболические, инфекционные и лекарственные воздействия. |
| 8 |
Зрительные нарушения |
Изменения в глазу или на сетчатке, включая клеточные тельца, кровоизлияния, серозный экссудат, или геморрагии в сосуди стой оболочке, или неврит зрительного нерва, склерит, эписклерит. Исключить случаи подобных изменений при гипертензии, инфекции и лекарственных воздействиях. |
| 8 |
Расстройства со стороны черепных нервов |
Впервые возникшая чувствительная или двигательная невропатия черепных нервов, включая головокружение, развившееся вследствие СКВ |
| 8 |
Головная боль |
Выраженная персистирующая головная боль (может быть мигренозной), не отвечающая на наркотические анальгетики |
| 8 |
Нарушение мозгового кровообращения |
Впервые возникшее. Исключить таковое вследствие атеросклероза или гипертензии |
| 8 |
Васкулит |
Язвы, гангрена, болезненные узелки на пальцах, околоногтевые инфаркты и геморрагии или данные биопсии либо ангиограм мы, подтверждающие васкулит – |
| 4 |
Артрит |
Более двух пораженных суставов с признаками воспаления (болезненность, отек или выпот) |
| 4 |
Миозит |
Проксимальная мышечная боль/слабость, ассоциированная с повышенным уровнем креатинфосфокиназы/альдолазы, или данные ЭМГ либо биопсии, подтверждающие миозит |
| 4 |
Цилиндрурия |
Зернистые или эритроцитарные цилиндры |
| 4 |
Гематурия |
>5 эритроцитов в поле зрения. Исключить мочекаменную болезнь, инфекционные и другие причины |
| 4 |
Протеинурия |
Острое начало или недавнее появление белка в моче в количестве >0,5 г/сут |
| 4 |
Пиурия |
>5 лейкоцитов в поле зрения. Исключить инфекционные причины |
| 2 |
Высыпания |
Новые или продолжающиеся высыпания воспалительного характера на коже |
| 2 |
Алопеция |
Впервые возникшее или продолжающееся повышенное очаговое или диффузное выпадение волос вследствие активности СКВ |
| 2 |
Язвы слизистых оболочек |
Впервые возникшее или продолжающееся изъязвление слизистых оболочек рта и носа вследствие активности СКВ |
| 2 |
Плеврит |
Боль в грудной клетке с шумом трения плевры, или выпотом, или утолщение плевры вследствие СКВ |
| 2 |
Перикардит |
Перикардиальная боль с одним из следующих признаков: шум трения перикарда, электрокардиографическое подтверждение перикардита |
| 2 |
Низкий уровень комплемента |
Снижение СН50, С3 или С4 ниже границы нормы тестирующей лаборатории |
Повышение уровня >25% связывания по методу Farr или превышение нормальных значений тестирующей лаборатории антител к ДНК
| 1 |
Лихорадка |
>38 °С. Исключить инфекционные причины |
| 1 |
Тромбоцитопения |
<100•109/л |
| 1 |
Лейкопения |
<3•109/л. Исключить лекарственные причины |
Общий балл (сумма баллов отмеченных проявлений)