Ann Rheum Dis doi:10.1136/annrheumdis-2016-209247
первая публикация август 2016
Аннотация
Отступление В 2012 году Европейская инициативная группа, названная
Single
Hub and
Access, стала пунктом для педиатрической Ревматологии в Европе
Single
Hub and
Access point for pediatric
Rheumatology in
Europe (SHARE) для оптимизации и распространения диагностики и схемы ведения в Европе для детей и подростков с ревматическими заболеваниями. Ювенильный дерматомиозит(JDM) (ЮДМ) является редким заболеванием в группе детских ревматических заболеваний
paediatric rheumatic diseases (PRDs и может привести к значительной заболеваемости. Научно обоснованные рекомендации скудны и ведение в основном основаны на опыте врачей. Следовательно, схемы лечения различаются по всей Европе.
Цель. Выработка рекомендаций по диагностике и лечению JDM.
Методы были разработаны рекомендации по научно-обоснованного консенсуса, используя Европейской лиги против ревматизма стандартных операционных процедур. Также был создан комитет, состоящий из 19 опытных педиатров-ревматологов и 2 специалисты в области детской физиологии упражнений и физкультурной терапии, в основном из Европы. Рекомендации, полученные от проверенных систематический обзор литературы, оценивались онлайн-опрос, и впоследствии обсуждался на двух заседаниях консенсус с использованием метода номинальных групп. Рекомендации были приняты, если была достигнута >80% соглашения.
Результаты в общей сложности, 7 основополагающих принципов, 33 рекомендации по диагностике и 19 рекомендации по терапии были приняты с >80% согласия между экспертами. Затронутые темы включают оценку кожи, мышц и крупных пораженных органов и предложены пути лечения.
Заключения Целью SHARE заключается в выявлении передовой практики для лечения пациентов, страдающих PRD. В рамках этой компетенции, рекомендаций по диагностике и лечению комплектации были сформулированы научно-обоснованного консенсуса для выработки стандарта медицинской помощи больным с ЮДМ по всей Европе.
Введение
Систематический поиск литературы
Электронные базы данных в pubmed/базах данных medline, embase и Кокрановском были дважды искали соответствующих товаров в июне 2013 года и впоследствии в феврале 2015 года. Все синонимы комплектации были проведены обыски в сетку термины/Emtree, название и Аннотация. Ссылка отслеживания проводилась во всех исследованиях (полная стратегии поиска в интернете дополнительный рисунок С1). Эксперты (ФБУ, LJMC, АВР-к) отдельные документы, относящиеся к комплектации исследования и/или лечения, чтобы быть взяты для оценки действия (критерии включения и исключения приведены в интернете дополнительный показатель С1). Все полнотекстовые документы введены в перечисленных в онлайн-дополнительный список С1.
Оценка достоверности
Группа экспертов (по два на каждый документ) независимо друг от друга оценивали методологическое качество работ, соответствующих критериям включения (см. в интернете дополнительный рисунок С1) и полученные данные с помощью стандартных оценочных анкет для диагностики и терапевтических исследований. Разногласия были урегулированы путем обсуждения или мнение третьего эксперта. Адаптированные таблицы классификации для диагностики, терапевтических, эпидемиологического исследований были использованы для определения уровня доказательств и силы каждой рекомендации.
Создание рекомендаций
В рамках стандартной операционной процедуры EULAR, эксперты описали основные результаты и выводы по каждой статье, наряду с законностью и уровнем доказательств. Эти описания были собраны три эксперта (ФБУ, LJMC и AVR-K) и использованы при разработке временных рекомендаций (N=65). Краткое изложение доказательств был представлен вместе с каждым предварительной рекомендации комитета экспертов (п=21) в онлайн-опросе (с 100% ответов). Рекомендации были пересмотрены в соответствии с ответами и обсуждены на двух последовательных очных встреч консенсуса в марте 2014 года (Генуя, количество участвующих экспертов: N=13) и 2015 (Барселона, количество участвующих экспертов: п=15), используя номинальной Групповой техники. Экспертов без права голоса (AR) продвигали процесс. Рекомендации были приняты, когда ≥80% экспертов согласились.
Результаты
Обзор литературы
Поиск литературы принесли 3429 уникальныхдокументы. После названия/Аннотация и последующего полнотекстового скрининг, 115 статей соответствовали критериям включения и были выбраны для качества скоринга: 45 статей по терапии, 70 для диагностики и 3 статьи в обеих группах (подробная в интернете дополнительный рисунок/список С1). Важную рукопись с описанием рандомизированные контролируемые испытания с участием лечение преднизолоном, метотрексатом (mtx) и циклоспорин был опубликован после систематического обзора и консенсусов, но перед отправкой этой статьи. По результатам этого рассматрения, уровень доказательств две рекомендации в разделе терапии был обновлен, но формулировка не изменилась.
Рекомендации
В следующем разделе описываются рекомендации с соответствующей вспомогательной литературы. Таблицы 1⇓-3 обобщить рекомендаций, уровни доказательств сила рекомендации и процент согласия экспертов для каждого. Следует отметить, что 39 из 59 приняты рекомендации основаны на мнении экспертов (уровень доказательности 4, в доказательности д). Рекомендации не достигает ≥80% от суммы договора перечисляются в режиме онлайн Дополнительная Таблица Т1 (п=6).
Таблица 1
Общие(всеобъемлющие) принципы ювенильного дерматомиозита (ЮДМ)
| L |
S |
Соглашение (%) |
| Все дети с подозрением на идиопатические воспалительные миопатии следует обращаться в специализированный центр |
4 |
D |
100 |
Пациенты высокого риска нуждаются в немедленном/срочное направление в специализированный центр. Пациенты с высоким риском определяются
- Тяжелая инвалидность, определяется невозможность слезть с кровати
- CMAS score <15, or MMT8 score <30
- Наличие аспирации или дисфагия (до невозможности глотать)
- Кишечный васкулит (как определено путем визуализации или наличие крови в каловых массах)
- Миокардит
- Паренхиматозные заболевания легких
- Болезнь центральной нервной системы (определяемая как снижение уровня сознания или судороги)
- Изъязвления кожи
- Потребность нахождения в реанимационные отделения
- Возраст <1 года
|
4 |
D |
100 |
| При JDM, жалобы пациента/ или родителей будут полезны при оценке активности заболевания и должна быть использована в диагностике и при мониторинге заболевания |
4 |
D |
100 |
| Проверенные инструменты должны быть использованы для оценки состояния здоровья, например, опросник оценки здоровья детства, пациент/родитель визуальная аналоговая шкала, опросник здоровья детства, Ювенильный Дерматомиозит многомерный Отчет об оценке |
4 |
D |
82 |
| Все дети с проявлениями активности заболевания (мышцы, кожа, главный орган) должны регулярно оцениваться по стандартной форме, используя такие инструменты, как оценка активности заболевания Disease Activity Score. |
4 |
D |
100 |
| Все дети с ЮДМ должны иметь оценку повреждений заболевания как минимум ежегодно с использованием стандартизированной оценки ущерба болезней, таких как Индекс повреждения Миозит Myositis Damage Index |
4 |
D |
100 |
| Все пациенты с ЮДМ должны иметь возможность быть зарегистрирован в научном реестре/репозиторий, например, реестр Euromyositis |
4 |
D |
100 |
- Соглашение указывает процент экспертов, которые согласились на рекомендации во время финального раунда голосования на заседании консенсусом.
- 1А, Мета-анализ хаотизированных контролируемых проб; 1Б, рандомизированное контролируемое исследование; 2А, контролируемое исследование без рандомизации; 2Б, квази-экспериментальное исследование; 3, описательное исследование; 4 экспертного заключения; в основе доказательства уровня 1; Б, на основе уровня 2 или экстраполированы с уровня 1; С, В зависимости от уровня 3 или экстраполированы с уровня 1 или 2; КМАС, детство Миозит шкалы оценивания; Д, В зависимости от уровня 4 или экстраполяция от уровня 3 или 4 экспертного заключения; Л уровень доказательств; ММТ ручное тестирование мышц; с сила рекомендаций;
Table 1
Overarching principles for juvenile dermatomyositis (JDM)
| L |
S |
Agreement (%) |
| All children with suspected idiopathic inflammatory myopathies should be referred to a specialised centre. |
4 |
D |
100 |
High-risk patients need immediate/urgent referral to a specialised centre. High risk patients are defined by
- Severe disability, defined by inability to get off bed
- CMAS score <15, or MMT8 score <30
- Presence of aspiration or dysphagia (to the point of inability to swallow)
- Gastrointestinal vasculitis (as determined by imaging or presence of bloody stools)
- Myocarditis
- Parenchymal lung disease
- Central nervous system disease (defined as decreased level of consciousness or seizures)
- Skin ulceration
- Requirement for intensive care unit management
- Age <1 year
|
4 |
D |
100 |
| For JDM, patient-/parent-reported outcome measures are helpful when assessing disease activity and should be used at diagnosis and during disease monitoring. |
4 |
D |
100 |
| Validated tools should be used to measure health status, for example, the Childhood Health Assessment Questionnaire, patient/parent visual analogue scale, Childhood Health Questionnaire, Juvenile Dermatomyositis Multi-dimensional Assessment Report. |
4 |
D |
82 |
| All children with JDM should have disease activity (muscle, skin, major organ) assessed regularly in a standardised way, using tools such as the Disease Activity Score. |
4 |
D |
100 |
| All children with JDM should have disease damage assessed at least yearly using a standardised disease damage measure, such as the Myositis Damage Index. |
4 |
D |
100 |
| All patients with JDM should have the opportunity to be registered within a research registry/repository, for example, the Euromyositis registry. |
4 |
D |
100 |
- Agreement indicates percentage of experts that agreed on the recommendation during the final voting round of the consensus meeting.
- 1A, meta-analysis of randomised controlled trial; 1B, randomised controlled study; 2A, controlled study without randomisation; 2B, quasi-experimental study; 3, descriptive study; 4 expert opinion; A, based on level 1 evidence; B, based on level 2 or extrapolated from level 1; C, based on level 3 or extrapolated from level 1 or 2; CMAS, Childhood Myositis Assessment Scale; D, based on level 4 or extrapolated from level 3 or 4 expert opinion; L, level of evidence; MMT, Manual Muscle Test; S, strength of recommendation;
Таблица 2
Рекомендации по диагностике
| L |
S |
Соглашение (%) |
| (a) общие рекомендации |
| При отсутствии кожных признаков и/или при отсутствии ожидаемого эффекта терапии, альтернативных диагнозов следует рассматривать в том числе метаболические или митохондриальной миопатии и дистрофии. |
4 |
D |
100 |
Каждому пациенту с диагнозом JDM должен быть выполнены следующий перечень исследований:
- Мышечные ферменты, включая креатинин фосфокиназа (КФК), ЛДГ, АСТ (SGOT), АЛТ (SGPT), adolase (если имеется)Full blood count and blood film
- Полный анализ крови м лейкоцитарная формула
- СОЭ(или вязкость плазмы) и СРБ
- Миозит-специфические и миозит-ассоциированных антител
- Функции почек и функции печени
- Скрининг инфекций (для дифференциального диагноза)
- Исследования по альтернативным системным причины миопатии, включая эндокринные нарушения (особенно щитовидной железы), электролитные нарушения, дефицит витамина D
- Другие тесты для метаболических/митохондриальные миопатии (особенно при отсутствии сыпи/атипичного начала)
- Мочевые тесты (с последующей оценке, если положительный протеинурия)
- Капилляроскопия ногтевого ложа
- Эхокардиография и ЭКГ
- Исследование функции легких (рентген грудной клетки и КТ по показаниям)
- МРТ мышц (+количественный ультразвук)
- ЭМГ (особенно при подозрении невропатии/нарушение нервно-мышечной передачи)
- Биопсия мышц (особенно при отсутствии сыпи/атипичная презентация) MRI brain if neurological involvement suspected
- УЗИ брюшной полости
|
4 |
D |
94 |
| (б) конкретные рекомендации |
| Оценка вовлечения мышц |
| И Мышечной силы и функции должны быть проверены на момент диагностики и в последующем формальной утвержденными тестами, такие как MMT8 and the CMAS. |
2a-3 |
B–C |
100 |
| МРТ может применяться для диагностики JDM. |
2B |
B |
100 |
| МРТ может использоваться для мониторинга активности заболевания |
2B |
B |
100 |
| При использовании МРТ должны выполняться определенные протоколы, которые повышают обнаружения воспаления мышц, такие как Т2-взвешенная /STIR режим . |
3 |
C |
100 |
| МРТ должны быть интерпретированы экспертом рентгенологом |
4 |
D |
100 |
| Биопсия мышцы следует выполнять во всех случаях, когда начало JDM это нетипично; в частности, при отсутствии сыпь/кожные признак |
4 |
D |
100 |
| Если мышечная биопсия проводится для диагностики JDM, стандартизированный счет JDM результата биопсии должны быть использованы для количественной оценки выраженности гистологических нарушений. |
2B |
B |
100 |
| Экспертное патогистологического заключение необходимо для определить особенности воспаления в JDM при мышечной биопсии |
4 |
D |
100 |
| При выполнении биопсии мышц, нет достаточных доказательств, чтобы рекомендовать биопсию иглой, в отличие от открытой биопсии у детей |
3 |
C |
100 |
| В тех случаях, когда МРТ или биопсия мышц не возможно, повышенный мышечный Эхо интенсивности при УЗИ мышц (когда выполняется опытным УЗИ) может быть признаком миозита. |
2B |
C |
82 |
| Функция глотания, должны быть официально оценены у каждого пациента. Оценка может включать в себя речь и оценке языковых терапия, видео рентгеноскопия исследований/ пассаж бария. |
3 |
C |
100 |
| ЭМГ или скорости нервной проводимости следует рассматривать чтобы отличить миопатии от нейропатии при диагностики JDM если имеется неопределенность |
4 |
D |
100 |
| ЭМГ не выявляет метаболические миопатии надежно и дальнейшее обследование не требуется, если этот диагноз подозревается. |
3 |
D |
100 |
| Оценка вовлечения кожи |
| Оценка капилляры ногтевого ложа должны быть использованы для помощи диагноза JDM. |
2 |
B |
100 |
| Во время диагностики или обострения заболевания, рекомендуется капилляроскопия ногтевого ложа стандартизированные оценки. В течение периода наблюдения, капилляроскопию следует проводить регулярно. |
3 |
C |
100 |
| Официальное CAT computerized axial tomography аксиальная компьютерная томография должны быть использованы для помощи диагноза JDM. |
4 |
D |
100 |
| Официальное CAT должна использоваться для мониторинга активности заболевания кожи с течением времени |
2B |
B |
100 |
| Инструменты для оценки состояния кожи включают DAS (skin), MITAX (skin) or CAT. |
4 |
D |
100 |
| Оценка поражением легких |
| У Всех пациенты с ЮДМ следует оценить поражением легких на момент постановки диагноза. |
3 |
C |
100 |
| Оценка должна включать исследование функции легких, в том числе CO диффузии. Если исследование функции легких указывают интерстициального заболевания легких, необходимы дальнейшие исследования (CXR/ HRCTCXR – chest X-ray мед. рентгеноскопия грудной клеткиHRCT: КТВР (Компьютерная томография высокого разрешения). |
4 |
D |
100 |
| Оценка поражение сердца. |
| Все пациенты с ЮДМ должны иметь эхокардиографии и ЭКГ в диагностике |
4 |
D |
94 |
| Пациенты, в частности, риск сердечной дисфункции должна была повторять сердечной оценки. Факторы риска: гипертония, высокая активность заболевания через 1 год после постановки диагноза, длительной высокой кортикостероидной нагрузки или хронических текущих заболеваний. |
2B |
B |
100 |
| Оценка кальциноза |
| Кальциноз следует искать у всех пациентов с JDM. |
4 |
D |
94 |
| Простые рентгенограммы могут быть использованы для оценки кальциноза. |
3 |
C |
100 |
| Аутоантитела и биомаркеры |
| Мы рекомендуем использовать мышечных ферментов (КФК, ЛДГ, АСТ) для диагностики и мониторинга заболевания в JDM, хотя следует признать, мышечных ферментов может быть нормальным, несмотря на активное заболевание. |
4 |
D |
100 |
| Измерение фактора фон Виллебранда не предоставить любую дополнительную информацию для диагностики JDM. |
3 |
C |
100 |
| Нет существенной диагностической преимуществ измерения антинуклеарных антител при JDM |
4 |
D |
100 |
| Измерение миозит-специфические антитела (such as anti-TIF 1-γ (p155), anti-NXP2/(p140/MJ), anti-MDA5 and anti-SRP) должны быть рассмотрены, если они доступны. |
2A-3 |
B–C |
100 |
| У пациентов с overlap синдромом , измерение миозит-ассоциированных антител, таких как anti-PmScl, anti-U1-RNP, anti-La (‘SSB’), anti-Ro (‘SSA’) and anti-Sm может быть полезным для уточнения диагноза. |
4 |
D |
100 |
| Дальнейшие научные исследования рекомендуют использование более чувствительных биомаркеров при JDM. |
4 |
D |
100 |
- • Соглашение указывает процент экспертов, которые согласились на рекомендации во время финального раунда голосования на заседании консенсусом.
- • 1А, Мета-анализ хаотизированных контролируемых проб; 1Б, рандомизированное контролируемое исследование; 2А, контролируемое исследование без рандомизации; 2Б, квази-экспериментальное исследование; 3, описательное исследование; 4 экспертного заключения; в основе доказательства уровня 1; Б на основе уровня 2 или экстраполированы с уровня 1; АЛТ-аланинаминотрансфераза; АСТ аспартатаминотрансфераза; в соответствии с уровнем 3 или экстраполированы с уровня 1 или 2; CAT, Cutaneous Assessment Tool; CMAS, Childhood Myositis Assessment Scale; детство Миозит шкалы оценивания; CO, carbon monoxide;; СРБ, с-реактивный белок;, рентген грудной клетки; Д, исходя из уровня 4 или экстраполяция от уровня 3 или 4 экспертного заключения; ЭМГ, электромиограмма; СОЭ, скорость оседания эритроцитов; КТВР высокого разрешения компьютерная томография; Л, уровень доказательств; ЛДГ, лактатдегидрогеназы; MITAX, myositis intention to treat activity index миозит намерение лечения активного населения; ММТ, Manual Muscle мануальное мышечное тестирование; RNP, anti-ribonuclear protein З, SGOT, Serum Glutamic-Oxaloacetic Transaminase сила рекомендации; эритроцитов указывала на наличие процесса, сыворотки Глутаминовой-Щавелевоуксусной Трансаминазы; лабораторные анализы включают:*, сыворотки Глутаминовой-Пировиноградной Трансаминазы; SRP, сигнал распознавания частиц; SSA, Ro antibodies; SSB , Sjögren’s syndrome type B antibodies; синдром Шегрена антитела типа Б STIR,, Short-TI инверсии восстановления.
Table 2
Recommendations regarding diagnosis
| L |
S |
Agreement (%) |
| (a) General recommendations |
| In the absence of cutaneous signs and/or failure to respond as expected to therapy, alternative diagnoses should be considered including metabolic or mitochondrial myopathies and dystrophies. |
4 |
D |
100 |
In every patient in whom a diagnosis of JDM is considered, the following list of investigations should be considered:
- Muscle enzymes—including creatinine phosphokinase (CPK), LDH, AST (SGOT), ALT (SGPT), adolase (if available)
- Full blood count and blood film
- ESR (or plasma viscosity) and CRP
- Myositis-specific and myositis-associated antibodies
- Renal function and liver function tests
- Infection screen (for differential diagnosis)
- Investigations for alternative systemic causes of myopathy including endocrine disorders (especially thyroid function), electrolyte disturbances, vitamin D deficiency
- Further tests for metabolic/mitochondrial myopathies (especially in the absence of rash/atypical presentation)
- Urine dipstick (with further evaluation if positive for protein)
- Nailfold capillaroscopy
- Echocardiogram and ECG
- Pulmonary function tests (chest X-ray and HRCT if concern)
- MRI of muscles (+quantitative ultrasound)
- EMG (particularly if suspicion of neuropathy/disorder of neuromuscular junction)
- Muscle biopsy (especially in the absence of rash/atypical presentation)
- MRI brain if neurological involvement suspected
- Abdominal ultrasound scan
|
4 |
D |
94 |
| (b) Specific recommendations |
| Assessment of muscle involvement |
| Both muscle strength and function should be tested at diagnosis and follow up by formal validated measures, such as the MMT8 and the CMAS. |
2a-3 |
B–C |
100 |
| MRI can be used to aid diagnosis of JDM. |
2B |
B |
100 |
| MRI can be used to help monitor disease activity. |
2B |
B |
100 |
| When used, MRI should be carried out by defined protocols that enhance detection of muscle inflammation, such as T2 weighted/STIR sequences. |
3 |
C |
100 |
| MRI should be interpreted by an expert radiologist. |
4 |
D |
100 |
| A muscle biopsy should be done in all cases where the presentation of JDM is atypical; in particular in the absence of rash/skin signs. |
4 |
D |
100 |
| If a muscle biopsy is performed for diagnosis of JDM, a standardised JDM biopsy score tool should be used to quantify severity of histological abnormalities. |
2B |
B |
100 |
| Expert histopathological opinion is required to define features of inflammation in JDM muscle biopsy. |
4 |
D |
100 |
| When doing a muscle biopsy, there is insufficient evidence to recommend a needle biopsy as opposed to an open biopsy in children. |
3 |
C |
100 |
| In cases where MRI or muscle biopsy is not possible, increased muscle echo intensity on muscle ultrasonography (when performed by an experienced sonographer) may be indicative of myositis. |
2B |
C |
82 |
| Swallow function should be formally assessed in every patient. The assessment may include a speech and language therapy assessment, video fluoroscopy/barium studies. |
3 |
C |
100 |
| EMG or nerve conduction velocity should be considered to differentiate myopathy from neuropathy when diagnosis of JDM is uncertain. |
4 |
D |
100 |
| EMG does not detect metabolic myopathies reliably and further workup is required if this diagnosis is suspected. |
3 |
D |
100 |
| Assessment of skin involvement |
| Assessment of nailfold capillaries should be used to aid diagnosis of JDM. |
2 |
B |
100 |
| At time of diagnosis or disease flare, standardised nailfold capillaroscopy assessment is recommended. During follow-up, assessment of nailfold capillaries should be performed regularly. |
3 |
C |
100 |
| A formal CAT should be used to aid diagnosis of JDM. |
4 |
D |
100 |
| A formal CAT should be used to monitor skin disease activity over time. |
2B |
B |
100 |
| Skin tools may include the DAS (skin), MITAX (skin) or CAT. |
4 |
D |
100 |
| Assessment of lung involvement |
| All patients with JDM should have an assessment of lung involvement at time of diagnosis. |
3 |
C |
100 |
| Assessment should include pulmonary function tests, including CO diffusion. If pulmonary function tests are indicative of interstitial lung disease, further investigations (CXR/ HRCT) are needed. |
4 |
D |
100 |
| Assessment of cardiac involvement. |
| All patients with JDM should have echocardiography and ECG at diagnosis. |
4 |
D |
94 |
| Patients at particular risk of cardiac dysfunction should have repeated cardiac evaluation. Risk factors include hypertension, high disease activity 1 year post diagnosis, long-term high corticosteroid burden or chronic ongoing active disease. |
2B |
B |
100 |
| Assessment of calcinosis |
| Calcinosis should be looked for in all patients with JDM. |
4 |
D |
94 |
| Plain radiographs may be used for the evaluation of calcinosis. |
3 |
C |
100 |
| Autoantibodies and biomarkers |
| We recommend use of muscle enzymes (CPK, LDH, AST) for diagnosis and disease monitoring in JDM, although it must be recognised muscle enzymes may be normal despite active disease. |
4 |
D |
100 |
| Measurement of von Willebrand factor does not provide any additional information for diagnosis of JDM. |
3 |
C |
100 |
| There is no significant diagnostic benefit gained from measurement of antinuclear antibody in JDM. |
4 |
D |
100 |
| Measurement of myositis-specific autoantibodies (such as anti-TIF 1-γ (p155), anti-NXP2/(p140/MJ), anti-MDA5 and anti-SRP) should be considered, when available. |
2A-3 |
B–C |
100 |
| In patients with overlap features, measurement of myositis-associated-antibodies such as anti-PmScl, anti-U1-RNP, anti-La (‘SSB’), anti-Ro (‘SSA’) and anti-Sm may be helpful to clarify the diagnosis. |
4 |
D |
100 |
| Further validation studies are recommended to define the use of more sensitive biomarkers in JDM. |
4 |
D |
100 |
- Agreement indicates percentage of experts that agreed on the recommendation during the final voting round of the consensus meeting.
- 1A, meta-analysis of randomised controlled trial; 1B, randomised controlled study; 2A, controlled study without randomisation; 2B, quasi-experimental study; 3, descriptive study; 4 expert opinion; A, based on level 1 evidence; B, based on level 2 or extrapolated from level 1; ALT, alanine aminotransferase; AST, aspartate aminotransferase; C, based on level 3 or extrapolated from level 1 or 2; CAT, Cutaneous Assessment Tool; CMAS, Childhood Myositis Assessment Scale; CO, carbon monoxide; CRP, C-reactive protein; CXR, chest X-ray; D, based on level 4 or extrapolated from level 3 or 4 expert opinion; EMG, electromyogram; ESR, erythrocyte sedimentation rate; HRCT, high-resolution computed tomography; L, level of evidence; LDH, lactate dehydrogenase; MITAX, myositis intention to treat activity index; MMT, Manual Muscle Test; RNP, anti-ribonuclear protein; S, strength of recommendation; SGOT, Serum Glutamic-Oxaloacetic Transaminase; SGPT, Serum Glutamic-Pyruvic Transaminase; SRP, signal recognition particle; SSA, Ro antibodies; SSB, Sjögren’s syndrome type B antibodies; STIR, Short-TI Inversion Recovery.
Таблица 3
Рекомендации по лечению
| L |
S |
Соглашение (%) |
| Защита от солнца, в том числе регулярное использование крема для загара на солнце открытых участков следует рекомендовать для пациентов с JDM. |
4 |
D |
100 |
| При лечении пациентов с JDM, это особенно важно иметь физиотерапевт и медсестра специалист для активного участия в составе мультидисциплинарной команды. |
4 |
D |
100 |
| Лечение JDM должна включать в себя безопасное и надлежащее физические упражнения, под наблюдением физиотерапевта. |
4 |
D |
100 |
| Мы рекомендуем индукции схема лечения новых(впервые установленным диагнозом) пациентов основываться на высокие дозы кортикостероидов (перорально или внутривенно) в сочетании с МТ. |
1B |
A |
100 |
| Высокие дозы кортикостероидов следует назначать системно устно или внутривенно при умеренной и тяжелом JDM. |
2A |
B |
100 |
| Высокие дозы кортикостероидов следует вводить внутривенно, если есть опасения по поводу абсорбции из ЖКТ |
3 |
C |
100 |
| Доза кортикостероидов должна быть уменьшена , если пациент показывает клиническое улучшение. |
4 |
D |
100 |
| Добавление Метотрексат или циклоспорин а, приводит к улучшению контроля заболевания, чем монотерапию преднизолоном; профиль безопасности способствуют комбинация метотрексата и преднизолона. |
1B |
A |
100 |
| МТ должен быть начат в дозе 15-20 мг/м2/неделю (максимум абсолютной дозе 40 мг /неделю) предпочтительно вводить подкожно в дебюте заболевания. |
4 |
D |
100 |
| Если с вновь установленным диагнозом пациент имеет неадекватный ответ на лечение, обострение лечение должно быть рассмотрено в течение первых 12 недель, после консультаций с эксперт центром. |
4 |
D |
100 |
| Внутривенное введение иммуноглобулина может быть полезным дополнением при рефрактерном течении болезни , особенно когда выражены поражения кожи. |
2B-4 |
C |
100 |
| ММФ может быть полезным для терапии мышечных и кожных проявлений заболевания (в том числе кальциноз). |
3 |
C |
100 |
| Сохранение поражения кожи свидетельствует о продолжающемся системное заболевание и, следовательно, должны рассматриваться показанием увеличения системной иммуносупрессии. Топический такролимус (0.1%)/топические стероиды могут помочь локализовать поражения кожи, особенно при симптоматическом покраснение или зуде. |
4 |
D |
100 |
| У пациентов с непереносимостью метотрексата, менять на другой БПВП, включая циклоспорин А или ММФ. |
3 |
C |
100 |
| Для пациентов с тяжелыми заболеваниями (например, участия органов/обширных язвенных болезнях кожи), добавление внутривенного введения циклофосфамида следует назначить. |
3 |
C |
100 |
| В истощение клеточной терапии (ритуксимаб) может рассматриваться в качестве вспомогательной терапии лиц с рефрактерной формой заболевания. Врачам следует знать, что ритуксимаб может занять до 26 недель до наступления клинического эффекта. |
1B |
D |
100 |
| Анти-ФНО терапии можно назначать при рефрактерном течении заболевания; инфликсимаб или адалимумаб имеет преимущество перед этанерцепт. |
3 |
D |
92 |
| В присутствии развивающихся или установленном кальцинозе, интенсификация иммуносупрессивной терапии следует рассматривать. |
3 |
C |
100 |
| Нет высокого уровня доказательств, когда прекращать терапию; однако, можно рассмотреть возможность отмены лечения если пациент отменены стероиды и в он находится в ремиссии на Метотрексат (или альтернативные БПВП) в течение минимум 1 год. |
4 |
D |
100 |
- Соглашение указывает процент экспертов, которые согласились на рекомендации во время финального раунда голосования на заседании консенсусом.
- 1А, Мета-анализ хаотизированных контролируемых проб; 1Б, рандомизированное контролируемое исследование; 2А, контролируемое исследование без рандомизации; 2Б, квази-экспериментальное исследование; 3, описательное исследование; 4 экспертного заключения; в основе доказательства уровня 1; Б, на основе уровня 2 или экстраполированы с уровня 1; С, В зависимости от уровня 3 или экстраполированы с уровня 1 или 2; д, в зависимости от уровня 4 или экстраполяция от уровня 3 или 4 экспертного заключения; DMARD, disease-modifying antirheumatic drug; ЮДМ, ювенильный дерматомиозит; L, level of evidence; Л, уровень доказательств; ММФ, микофенолата мофетил; Метотрексат, Метотрексат; ; S, strength of recommendation; сила рекомендаций; ФНО, фактор некроза опухоли.
Table 3
Recommendations regarding treatment
| L |
S |
Agreement (%) |
| Sun protection, including the routine use of sunblock on sun-exposed areas should be encouraged for patients with JDM. |
4 |
D |
100 |
| When treating patients with JDM, it is particularly important to have a physiotherapist and a specialist nurse actively involved as part of a multidisciplinary team. |
4 |
D |
100 |
| Treatment of JDM should include a safe and appropriate exercise programme, monitored by a physiotherapist. |
4 |
D |
100 |
| We recommend the induction regimen for treatment of new onset patients with JDM to be based on high dose of corticosteroids (oral or intravenous) combined with MTX. |
1B |
A |
100 |
| High-dose corticosteroids should be administered systemically either orally or intravenously in moderate–severe JDM. |
2A |
B |
100 |
| High-dose corticosteroids should be administered intravenously if there are concerns about absorption. |
3 |
C |
100 |
| Corticosteroid dose should be weaned as the patient shows clinical improvement. |
4 |
D |
100 |
| Addition of MTX or ciclosporin A leads to better disease control than prednisolone alone; safety profiles favour the combination of methotrexate and prednisolone. |
1B |
A |
100 |
| MTX should be started at a dose of 15–20 mg/m2/week (max absolute dose of 40 mg /week) preferably administered subcutaneously at disease onset. |
4 |
D |
100 |
| If a newly diagnosed patient has inadequate response to treatment, intensification of treatment should be considered within the first 12 weeks, after consultation with an expert centre. |
4 |
D |
100 |
| Intravenous immunoglobulin may be a useful adjunct for resistant disease, particularly when skin features are prominent. |
2B-4 |
C |
100 |
| MMF may be a useful therapy for muscle and skin disease (including calcinosis). |
3 |
C |
100 |
| Ongoing skin disease reflects ongoing systemic disease and therefore should be treated by increasing systemic immunosuppression. Topical tacrolimus (0.1%)/topical steroids may help localised skin disease, particularly for symptomatic redness or itching. |
4 |
D |
100 |
| In patients who are intolerant to methotrexate, change to another DMARD, including ciclosporin A or MMF. |
3 |
C |
100 |
| For patients with severe disease (such as major organ involvement/extensive ulcerative skin disease), addition of intravenous cyclophosphamide should be considered. |
3 |
C |
100 |
| B cell depletion therapy (rituximab) can be considered as an adjunctive therapy for those with refractory disease. Clinicians should be aware that rituximab can take up to 26 weeks to work. |
1B |
D |
100 |
| Anti-TNF therapies can be considered in refractory disease; infliximab or adalimumab are favoured over etanercept. |
3 |
D |
92 |
| In the presence of developing or established calcinosis, intensification of immunosuppressive therapy should be considered. |
3 |
C |
100 |
| There is no high-level evidence of when to stop therapy; however, consideration may be given to withdrawing treatment if a patient has been off steroids and in remission on methotrexate (or alternative DMARD) for a minimum of 1 year. |
4 |
D |
100 |
- Agreement indicates percentage of experts that agreed on the recommendation during the final voting round of the consensus meeting.
- 1A, meta-analysis of randomised controlled trial; 1B, randomised controlled study; 2A, controlled study without randomisation; 2B, quasi-experimental study; 3, descriptive study; 4 expert opinion; A, based on level 1 evidence; B, based on level 2 or extrapolated from level 1; C, based on level 3 or extrapolated from level 1 or 2; D, based on level 4 or extrapolated from level 3 or 4 expert opinion; DMARD, disease-modifying antirheumatic drug; JDM, juvenile dermatomyositis; L, level of evidence; MMF, mycophenolate mofetil; MTX, methotrexate; S, strength of recommendation; TNF, tumour necrosis factor.
Table 3
Recommendations regarding treatment
| L |
S |
Agreement (%) |
| Sun protection, including the routine use of sunblock on sun-exposed areas should be encouraged for patients with JDM. |
4 |
D |
100 |
| When treating patients with JDM, it is particularly important to have a physiotherapist and a specialist nurse actively involved as part of a multidisciplinary team. |
4 |
D |
100 |
| Treatment of JDM should include a safe and appropriate exercise programme, monitored by a physiotherapist. |
4 |
D |
100 |
| We recommend the induction regimen for treatment of new onset patients with JDM to be based on high dose of corticosteroids (oral or intravenous) combined with MTX. |
1B |
A |
100 |
| High-dose corticosteroids should be administered systemically either orally or intravenously in moderate–severe JDM. |
2A |
B |
100 |
| High-dose corticosteroids should be administered intravenously if there are concerns about absorption. |
3 |
C |
100 |
| Corticosteroid dose should be weaned as the patient shows clinical improvement. |
4 |
D |
100 |
| Addition of MTX or ciclosporin A leads to better disease control than prednisolone alone; safety profiles favour the combination of methotrexate and prednisolone. |
1B |
A |
100 |
| MTX should be started at a dose of 15–20 mg/m2/week (max absolute dose of 40 mg /week) preferably administered subcutaneously at disease onset. |
4 |
D |
100 |
| If a newly diagnosed patient has inadequate response to treatment, intensification of treatment should be considered within the first 12 weeks, after consultation with an expert centre. |
4 |
D |
100 |
| Intravenous immunoglobulin may be a useful adjunct for resistant disease, particularly when skin features are prominent. |
2B-4 |
C |
100 |
| MMF may be a useful therapy for muscle and skin disease (including calcinosis). |
3 |
C |
100 |
| Ongoing skin disease reflects ongoing systemic disease and therefore should be treated by increasing systemic immunosuppression. Topical tacrolimus (0.1%)/topical steroids may help localised skin disease, particularly for symptomatic redness or itching. |
4 |
D |
100 |
| In patients who are intolerant to methotrexate, change to another DMARD, including ciclosporin A or MMF. |
3 |
C |
100 |
| For patients with severe disease (such as major organ involvement/extensive ulcerative skin disease), addition of intravenous cyclophosphamide should be considered. |
3 |
C |
100 |
| B cell depletion therapy (rituximab) can be considered as an adjunctive therapy for those with refractory disease. Clinicians should be aware that rituximab can take up to 26 weeks to work. |
1B |
D |
100 |
| Anti-TNF therapies can be considered in refractory disease; infliximab or adalimumab are favoured over etanercept. |
3 |
D |
92 |
| In the presence of developing or established calcinosis, intensification of immunosuppressive therapy should be considered. |
3 |
C |
100 |
| There is no high-level evidence of when to stop therapy; however, consideration may be given to withdrawing treatment if a patient has been off steroids and in remission on methotrexate (or alternative DMARD) for a minimum of 1 year. |
4 |
D |
100 |
- Agreement indicates percentage of experts that agreed on the recommendation during the final voting round of the consensus meeting.
- 1A, meta-analysis of randomised controlled trial; 1B, randomised controlled study; 2A, controlled study without randomisation; 2B, quasi-experimental study; 3, descriptive study; 4 expert opinion; A, based on level 1 evidence; B, based on level 2 or extrapolated from level 1; C, based on level 3 or extrapolated from level 1 or 2; D, based on level 4 or extrapolated from level 3 or 4 expert opinion; DMARD, disease-modifying antirheumatic drug; JDM, juvenile dermatomyositis; L, level of evidence; MMF, mycophenolate mofetil; MTX, methotrexate; S, strength of recommendation; TNF, tumour necrosis factor.
Общие принципы
JDM это самой частая идиопатическая воспалительной миопатии детства, но частота очень низкая; 2-4 случая на миллион детей в год (Таблица 1). Стандартизации диагностики и схем лечения позволит совместными научными исследованиями повысить знания о этой редкой болезни. ЮДМ васкулопатия главным образом влияет на мышцы и кожу, но может поражать другие органы и вызвать конституционнальные симптомы. При раннем лечении, 30-50% пациентов имеют потенциал, чтобы достичь ремиссии в течение 2-3 лет от начала заболевания с небольшим числом осложнений и смертности <4%.Однако, полицикличность или персистирующая активность заболевание было описано в 41-60% случаев в последних когортных исследований (в зависимости от активности лечения) и осложнения в виде кальциноза, стойкая мышечная слабость, кожи или мышечной атрофии остаются проблематичными. Риск липодистрофии и кальциноз было связан с большей продолжительностью активной болезни и неадекватной кортикостероидной терапии. Качество жизни может ухудшиться по сравнению со здоровым контролем как физических, так и психологических разделах, что требует психологической поддержки. Ввиду редкости и тяжести состояния, было решено, что дети с ЮДМ должны лечиться в центрах, имеющих опыт и знания в этом области. Цели лечения включают контроль активности заболевания, предупреждение поражения органов-мишеней и улучшение качества жизни с участием в повседневной жизни. Оценка ответа на лечение (включая измерение активности заболевания и повреждения заболевания и мониторинга побочных эффектов иммуносупрессивных препаратов) является важным краеугольным камнем управления. Много стандартных оценок, разработанный в основном для исследования, доступны для этого, в том числе за счет активности болезни (DAS) и миозит шкалы оценки активности заболевания. Признается, что реестры обеспечивают полезные ресурсы для изучения редких заболеваний, таких как ЮДМ. Для того, чтобы лучше понять прогноз заболевания и повысить терапевтический эффект этого редкого заболевания, группа экспертов сочла необходимым рекомендовать всем пациентам ЮДМ должны иметь возможность участвовать в научно-исследовательской реестрахю
Рекомендации по диагностике
Диагностические критерии дерматомиозита, установленном Бохан и Питер в 1975 году, включают в себя пять пунктов: характерная сыпь на коже, слабость проксимальных мышц, повышение мышечных ферментов, миопатические изменения на электромиограмме (ЭМГ) и типичные результаты мышечной биопсии (табл. 2). В настоящее время в рамках проекта пересматривается Международные классификационные критерии Миозитов. Текущая практика свидетельствует о необходимости расширения диагностических критериев путем включения новых методик, таких как МРТ и УЗИ, и значимость кожных проявлений при JDM. Группа экспертов предложила неполный перечень исследований для рассмотрения в каждого пациента, у которых диагноз JDM подозревается. Были созданы более конкретные рекомендации.
Оценка заболевания мышц
Мышечная сила должна быть формально проверена с помощью проверенных мер мышечного тестирования, такие как Childhood Myositis Assessment Scale (CMAS) и ручной мышечный тест Manual Muscle Test (ММТ). Оба инструмента были проверены в качестве надежных и полезных тестов для оценки силы мышц при диагностике и последующего наблюдения. Они важны оценки результата в лечении и в клинических испытаниях и являются частью) критериев ремиссии детской Ревматологии Международная организация испытаний (ПРИНТО) Paediatric Rheumatology INternational Trials Organization (PRINTO) . Некоторые CMAS позиции зависят от возраста. Было показано, что здоровые дети до 9 лет не всегда достигали максимального счета 52 CMAS, следовательно, определение активной болезни/ремиссии должен включать в себя нижний порог у детей младшего возраста.
МРТ-это надежный инструмент для оценки воспаления в мышцах во время диагностики, а также может помочь дифференцировать активных и неактивных заболевания в течение периода наблюдения. Протоколы, которые повышают обнаружения воспаления мышц, такие как Т2-взвешенные (жира подавляется) методов визуализации, должны быть использованы. Специалист радиолог должен оценить результаты МРТ.
Обзоры и последних когортных исследований свидетельствуют о возрастающем использовании МРТ в настоящее время (26-89.9%) в качестве диагностического метода в противовес уменьшению мышечной биопсии (36-65%) и ЭМГ (7.6–55.5%). Группа экспертов рекомендуют ЭМГ или нервной проводимости скорость только тогда, когда диагноз остается неопределенным. Следует отметить, что ЭМГ не надежно обнаруживает метаболические миопатии.
Группа экспертов рекомендует биопсию, когда дебют является нетипичным или диагноз находится под сомнением. Рекомендуется использование стандартизированных инструментов ЮДМ результата биопсии для количественной оценки выраженности гистологических нарушений. Различные маркеры были предложены типизировать мышцы воспаления у пациентов с ЮДМ, как главный комплекс гистосовместимости (ГКГС) major histocompatibility complex (MHC) класса I, сосудистой клеточной молекулы адгезии vascular cell adhesion molecule (VCAM), межклеточные молекулы адгезии intercellular adhesion molecule (ICAM), CD59 и толл-подобных рецепторов toll-like receptor (TLR),но они нуждаются в дополнительной проверке. Экспертное заключение патогистологического необходимо для определить использование этих маркеров для диагностики ЮДМ, основанные на результатах биопсии мышц. Данные литературы свидетельствуют, что пункционная биопсия является безопасной и экономически эффективной альтернативой открытой биопсии у взрослых пациентов. однако, этого еще недостаточно оценена в детей, чтобы в быть рекомендованной.
УЗИ был найден в небольшие когорты пациентов (7-10 человек), чтобы быть полезным инструментом для миозита. Группа экспертов предполагает, что при невозможности МРТ или биопсия мышц УЗИ мышц может быть альтернативой для оценки активности миозита.
Данные литературы свидетельствуют, что глотательные дисфункции, в том числе и безмолвную аспирацию, недооценивается и не всегда предсказывает генерализованную мышечную слабость. Группа экспертов рекомендуют, что пациенты с трудности при глотании (например, тех, кто представляет с носовой речи или кашель во время глотания) должны иметь объективную оценку на основе локального обследования (произношение и языковых терапия, видео рентгеноскопия/бария пассаж).
Оценка заболеваний кожи
Группа экспертов рекомендует использовать инструмент оценки кожных (CAT), в том числе капилляроскопии ногтевого ложа обнаруживают околоногтевого капиллярных изменений, в рамках оценки проявлений ЮДМ кожи для диагностики и мониторирования. Это можно сделать в клинике с помощью увеличение с помощью отоскопа, офтальмоскопа или дерматоскопа, или проведением стандартной капилляроскопии. Очевидно, что плотность капилляров ногтевого ложа, является чувствительным мерилом кожной и мышечной активности заболевания. Значение остаточных изменений кожи при JDM все чаще признается, наличием стойких капиллярных аномалий и папул Gottron в течении 6 месяцев, что связано с более длительное время до ремиссии. Поэтому группа экспертов рекомендовала последующее ведение пациентов с ЮДМ должна включать использование CAT. Различные инструменты доступны, в том числе DAS (кожа), Myositis Intention to Treat Activity IndeX (MITAX, skin), САТ, Dermatomyositis Skin Severity Index or Cutaneous Dermatomyositis Disease Area and Severity Index; последние два реже используется у детей. В настоящее время нет достаточных доказательств того, что один инструмент лучше другого.
Оценка ЮДМ-ассоциированных заболеваний легких
Поражением легких (интерстициальные заболевания легких (ИЗЛ)) (interstitial lung disease (ILD)) присутствует только в ∼8% пациентов, и часто протекает бессимптомно, но оценка важна, поскольку ИЗЛ является одной из основных причин заболеваемости и смертности. Группа экспертов определила, что все дети должны иметь оценку поражением легких на момент постановки диагноза путем исследования функции легких, в том числе carbon monoxide (CO) диффузионной способности. Дальнейшее тестирование необходимо в тех с рестрективными проявлениями, желательно в сотрудничестве с детским пульмонолога. Выполнение тестов функции легких может быть затруднена у очень маленьких детей, а также может быть осложнено общей мышечная слабость. Компьютерная томография высокого разрешения является неинвазивным и чувствительным тестом для выявления ИЗЛ при JDM, но радиационный риск, связанный с повторным КТ должны быть учтен. Нет достаточных доказательств, чтобы сообщить о как часто оценки в течение периода наблюдения, но врачи должны быть осведомлены о долгосрочных рисках поражения легких, особенно в тех высокий миозит повреждение индекс myositis damage index (MDI)) и регулярная оценки функции легких может быть целесообразно у пациентов с положительным анти-РНК-синтетазы антител anti-RNA synthetase antibodies.
Оценка ЮДМ-ассоциированных сердечно-сосудистых заболеваний
Понимание сердечных проявлений в ЮДМ ограничено. Одно долгосрочное осложнение гипертония из-за стероидного лечения. Сообщается о наличии перикардита, эндокардита и сердечной аритмии. Последние доказательства с помощью эхокардиографии обнаруживают систолическая и диастолическая дисфункция, особенно у пациентов с высокими баллами долгосрочного повреждению органа (MDI, контроль) и высокой ранней кожной (но не мышечной) активности болезни DAS (для кожи, 1 год). В частности, большинство пациентов были бессимптомными. Авторы исследования предполагают, что васкулопатии в миокарде напоминает васкулопатии в коже. Долгосрочных клинических последствий аномальных эхокардиографические находки у бессимптомных пациентов с ЮДМ не ясны. Группа экспертов рекомендует оценка сердца по ЭКГ и эхокардиографии для всех пациентов. Повторные оценки сердечной деятельности следует рассматривать у пациентов с высоким риском вовлечения сердца; факторы риска: гипертония, высокая активность заболевания через 1 год после постановки диагноза, длительной высокой кортикостероидной нагрузки или хронические текущие заболеваний. Изменения эндокарда признаются даже тогда, когда пациенты находятся в клинической ремиссии и, таким образом, долгосрочные оценки сердечной деятельности следует проводить у пациентов с высоким риском. В настоящее время нет достаточных доказательств, чтобы сообщить о частоте и продолжительности мониторинга.
Оценка кальциноза
Кальциноз-это хорошо известное осложнение у пациентов с ЮДМ, часто происходит позже в ходе болезни, в среднем через 2,9 года после начала заболевания. Группа экспертов активно рекомендует искать кальциноз ручной пальпацией, с использованием обычных рентгенограммах, где это необходимо. Было установлено, что КТ никаких дополнительных преимуществ над рентгенограммы для выявления кальциноза.
Биомаркеры и аутоантитела
Мышечные ферменты не всегда повышен при диагностике ЮДМ и плохо реагирует на изменение активности заболевания. Консенсус продемонстрировал расхождения во мнениях относительно включения мышечных ферментов в качестве базового набора для оценки активности. The International Myositis Association and Clinical Studies Group (IMACS включила в основной набор мышечные ферменты, но PRINTO исключает мышечные ферменты в связи с их слабой статистикой., Несмотря на эти ограничения, мышечные ферменты легко определяются и обзоры практики предполагают, что ферменты используются в обычной помощи при диагностике и во время последующего нпблюдения. Группа экспертов рекомендует использовать всех перечисленных ферментов в диагностике (табл. 2) и последующем наблюдении, как один из них может быть повышен при наличие нормальной креатинин фосфокиназа (КФК). Из современной литературы, нет никаких доказательств, что фактор фон Виллебранда обеспечивает дополнительную информацию по сравнению с мышечных ферментов. Несколько маркеров иммунологической активации коррелирует с активностью заболевания или, возможно, с худшим исходом заболевания в JDM, но необходимы дальнейшие исследования для определения их чувствительности, таких как интерферон (ИФН)-I (IFN)-I chemokine signatures и неоптерина. Антинуклеарные антитела часто являются положительным у пациентов с комплектации (распространенность варьирует в зависимости от разных групп населения), но не диагностическое значение не было установлено. Больше доказательств имеет ассоциации между серотипом и клинического фенотипом. Мишень Миозит-специфических аутоантител либо ядерные или цитоплазматических компонентов, вовлеченных в транскрипцию гена, транслокация белков и противовирусные реакции. Данные литературы свидетельствуют, что наличие анти-ст. 155 (анти-TIF1y) миозит-ассоциированных антител (МАА) anti-p155 (anti-TIF1γ) myositis-associated antibodies (MAA) прогнозирует большее кожные поражения, анти-р140 (также известный как NXP-2 или МJ), anti-p140 (also known as NXP-2 or MJ) прогнозирует кальциноз, тяжелое течение заболеваниях и постоянные активность болезни, и анти-MDA5 anti-MDA5 связано с повышенным риском язвы кожи и ротовой, артриты, более легкое заболевание мышц и интерстициальные болезни легких. Ассоциация тяжелой болезнью легких было наиболее ярким у японских пациентов Anti-signal recognition particle (SRP)связан с некротизирующей аутоиммунной миопатии. Исследований, упомянутых выше, обеспечивают контроль сывороток, полученных от взрослых и ни один из этих аутоантител были проверены на сегодняшний день в крупных когортах пациентов. На момент публикации, есть недостаточные доказательства, чтобы рекомендовать измерения аутоантител для стратификации риска из-за недостаточной проверки и данных у пациентов разных этнических групп. Однако, при наличии, измерения миозит-специфические антитела или МАА могут быть полезны, но должны быть выполнены и проверены в лаборатории с опытом и знаниями.
Терапия
Ранняя и агрессивная терапия может предотвратить или стабилизировать повреждения органов и осложнений заболевания, таких как кальциноз, причем последний связан со значительной заболеваемостью из-за боли и риска инфицирования (табл. 3). ЮДМ лечения во многом основана на опыте лечения детского ревматолога. Управление является сложным и требует мультидисциплинарного подхода, включая физиотерапевтов, дипломированных медсестер и педиатров ревматологов, с другими специалистами, по мере необходимости, например, кардиолог/пульмонолог. Основой терапии высокими дозами кортикостероидов изначально в сочетании с болезнь-модифицирующие препараты, такие как Метотрексат или циклоспорин А ciclosporin A (CsA). Доказательность для лечения ограничена и часто ограничивается небольшими случай-контролируемых исследований, за исключением двух рандомизированных контролируемых испытаний. Childhood Arthritis and Rheumatology Research Alliance (CARRA) в 2010 достигли консенсуса по планам лечения тяжелой ЮДМ в течение первых двух месяцев после постановки диагноза, которые включают в себя комбинацию стероидов (метилпреднизолон внутривенно, затем пероральный прием преднизолона или высокие дозы перорального преднизолона в одиночку) и МТХ±внутривенного иммуноглобулина (ВИГ) intravenous immunoglobulin (IVIG).
Единственное рандомизированное контролируемое испытание для вновь диагностированных пациентов была выполнена PRINTO с 2006 по 2011 год, сравнивая три наиболее часто используемых протоколов (только преднизолон против комбинации преднизолона с mtx или CsA). Сочетание стероидов и МТХ показали лучшие результаты по эффективности и безопасности. В 2013 году, рандомизированное контролируемое исследование было опубликовано по использования ритуксимаба при рефрактерных миозитах, в том числе ЮДМ. Не было статистически значимой разницы между группами лечения, но 83% пациентов отметили улучшение в ходе исследования. Эти данные, с возможностью сокращения глюкокортикоидной терапии и хороший ответа на лечения, свидетельствуют, что ритуксимаб может быть полезный в рефрактерных случаях миозита.
Группа экспертов предложила рекомендации по лечению вновь выявленных больных и рефрактерной болезни. Лечение рефрактерных пациентов с или без кальциноза по-прежнему актуальна. Процедуры, используемые для рефрактерного заболевания, включают иммуноглобулин, циклофосфамид, CsA, азатиоприн, микофенолата мофетил (ММФ), гидроксихлорохин, такролимус, ритуксимаб, инфликсимаб и аутологичной трансплантации стволовых клеток. Параллельных или преимущественных исследований не проводилось.
Опубликованные данные свидетельствуют о том, что раннее агрессивное лечение может снизить частоту кальциноза. Установлено, кальциноз может реагировать на лечение бисфосфонаты (памидронат/алендронат), инфликсимаб, абатацепт, дилтиазем, пробенецид, иммуноглобулины для внутривенного введения, введения в очаг поражения стероиды или хирургическая резекция. Доказательств для индивидуальных процедур ограничивается отчетами(сообщениями), за исключением инфликсимаба, дилтиазем и памидронат (публикации о пяти, четырех и трех пациентов, соответственно); поэтому, никаких рекомендаций относительно конкретного лечения кальциноза не было сделано.
Терапевтические исследования ограничены малым числом пациентов с ЮДМ, а также ограниченные средства или биомаркеров для оценки результата. В настоящее время нет единой, простой и практичный инструмент для оценки улучшения или неактивной болезни, чтобы направлять индивидуальное лечение. PRINTO и IMACS разработали предварительного определения улучшения (definitions of improvement (DoI)) для использования в клинических исследованиях, к которым относятся многократные оценки базового набора мер core set measures (CSMs). Хотя CSMs использовать с DoI отличаться незначительно, PRINTO и IMACS ожидать как минимум 20% улучшение по трем из шести CSMs с ухудшением не более одного или двух других пунктов и мышечной силы которая не ухудшиться. Эти определения и рекомендации лучше всего подходят для клинических исследований, с соответствующей инфраструктурой, но занимают много времени в клинической практике. В 2012 году CARRA разработан единый консенсус план по снижению стероид, в том числе, включающий, когда и как отменять стероиды. Вместе с тем группа экспертов SHARE не согласны с конкретным стероид-снижающим режимом.
В 2012 году PRINTO опубликованных критериев, определяющих клинически неактивной болезни, а это требовало выполнение трех из четырех переменных из КФК ≤150 ед/Л, CMAS ≥48, MMT8 ≥78 и PGA счет общей активности заболевания ≤0.2. Эти критерии тяготеют к заболеванию мышц, и при испытании в норвежской когорте при определении КФК не было разницы между активной и неактивной болезнью. При проведении испытания в когорте Великобритании, без PGA, отмечается высокая заболеваемость кожи, что приводит к предположению, что PGA должно стать важнейшим критерием, поскольку это единственная мера, которая включает в себя поражение кожи. группа экспертов определила, что лечение должен быть усилено, если пациент имеет неадекватный ответ на лечение, в том числе изолированное заболевание кожи.
Нет высокого уровня доказательств о том, когда прекратить иммуносупрессивную терапию. Экспертная группа предложила к рассмотрению вопроса о снятии МТХ (или альтернативной болезнь-модифицирующих препаратов) после того, как пациент находится в стадии ремиссии и без стероидов в течение минимум 1 год.
Основываясь на рекомендациях консенсуса, схема была создана для лечения ЮДМ (рис. 1).
Рисунок 1А
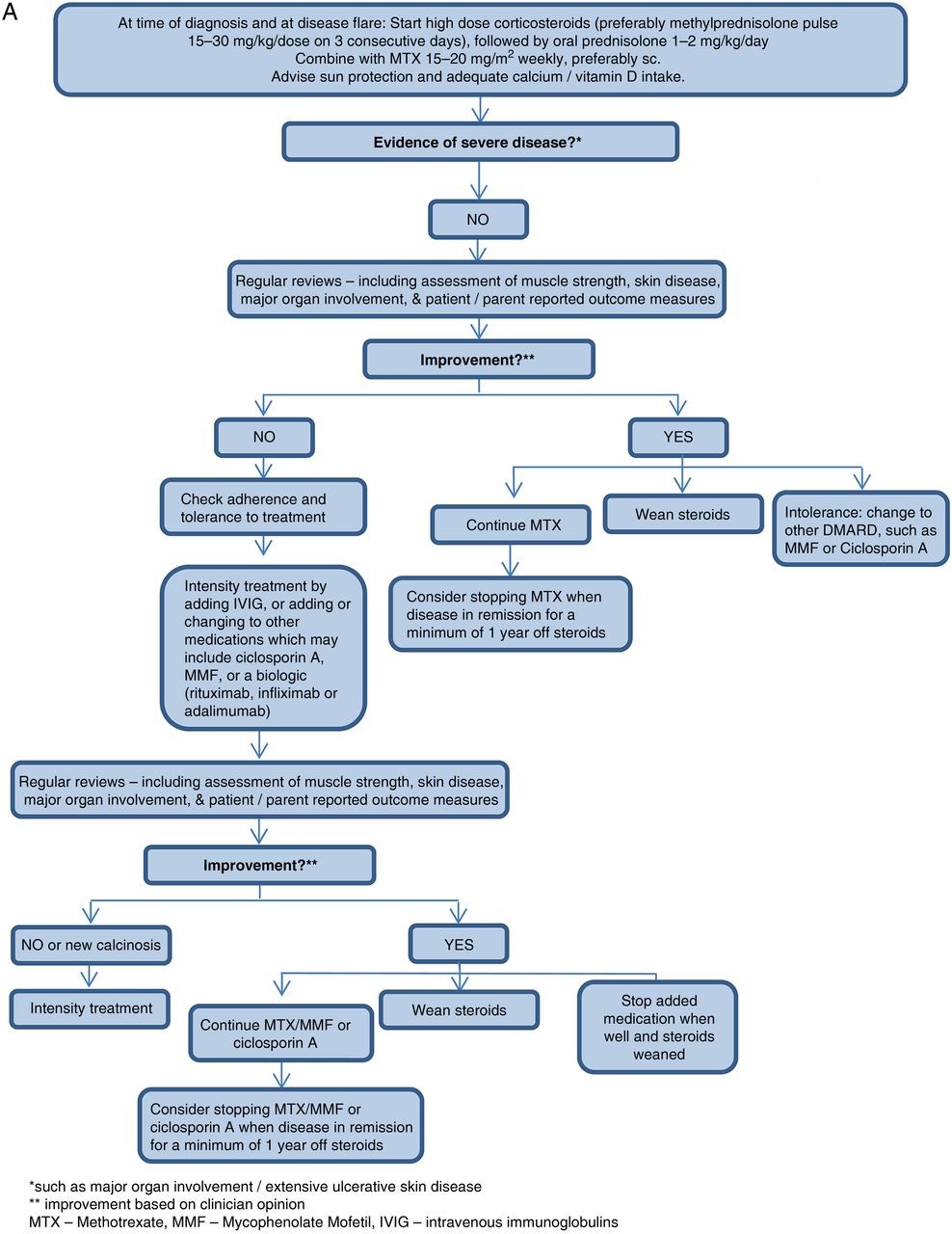
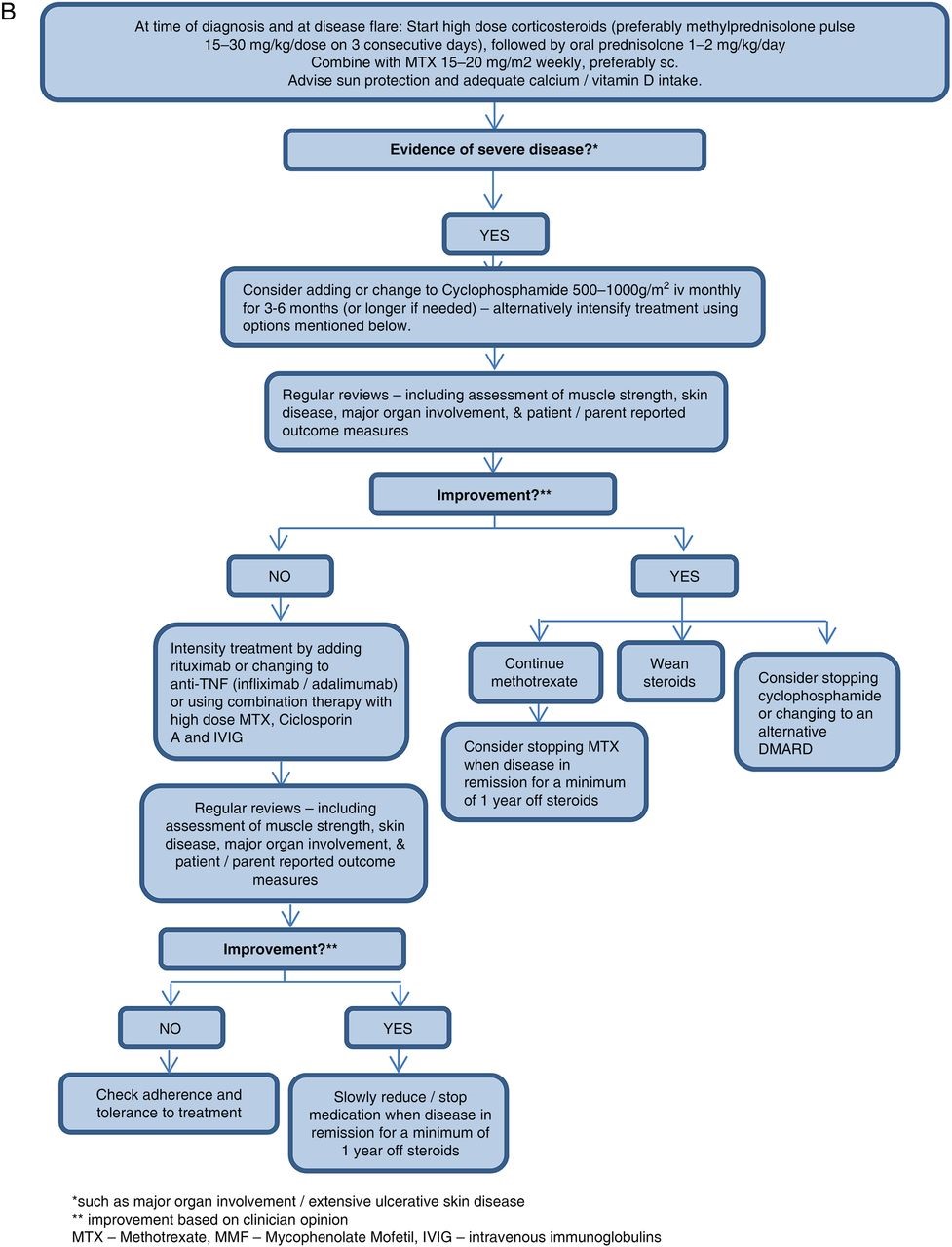
рис. 1Б Схема для лечения легкой/умеренной болезнью в впервые диагностированных и рефрактерных пациентов с ювенильным дерматомиозитом (ЮДМ).
 Обсуждение
Обсуждение
ЮДМ рабочей группы SHARE сформулированы в общей сложности 62 рекомендации по диагностике и ведению ЮДМ, основаны на систематическом обзоре литературы и процедура консенсуса. В общей сложности, 7 основополагающих принципов, 33 рекомендации по диагностике и 19 по терапии были приняты с >80% согласия между экспертами. Темы включают оценку состояния кожи, мышц и крупных вовлечения органов и лечение в дебюте заболевания и при рефрактерном течении заболевания.
Диагностические критерии в JDM пересматриваются, однако потребуется дальнейшая корректировка как новый инструменты по оценке результатов, особенно аутоантител и биомаркеров, которые разрабатываются.
Тщательный мониторинг состояния болезни пациентов и наличие опытной мультидисциплинарной команды имеет важное значение для хорошего клинического результата. Последние данные подчеркивают важность лечения заболеваний кожи агрессивно, как это связано с высокой болезненностью. Долгосрочные последующие исследования необходимы для уточнения осложнений. Учитывая редкость заболевания, международное сотрудничество имеет решающее значение для набора достаточной пациентов. Утверждена для оценки активности заболевания и повреждения необходимы для того, чтобы выполнить структурированный оценка результатов. Активности заболевания и оценки ущерба были разработаны, главным образом для клинических испытаний, что может быть сложным и трудоемким для использования в повседневной клинической практике.
В заключение эти SHARE основываются на мнениях экспертов сообщает наилучших имеющихся фактических данных и даются рекомендации по диагностике и лечению пациентов с комплектации, наряду с другими педиатрическими ревматические заболеваниями с целью улучшения исхода для пациентов с ЮДМ в Европе. Теперь будет важно расширить обсуждение и тестирование приемлемости для общества в целом.

 рис. 1Б Схема для лечения легкой/умеренной болезнью в впервые диагностированных и рефрактерных пациентов с ювенильным дерматомиозитом (ЮДМ).
рис. 1Б Схема для лечения легкой/умеренной болезнью в впервые диагностированных и рефрактерных пациентов с ювенильным дерматомиозитом (ЮДМ).
 Обсуждение
ЮДМ рабочей группы SHARE сформулированы в общей сложности 62 рекомендации по диагностике и ведению ЮДМ, основаны на систематическом обзоре литературы и процедура консенсуса. В общей сложности, 7 основополагающих принципов, 33 рекомендации по диагностике и 19 по терапии были приняты с >80% согласия между экспертами. Темы включают оценку состояния кожи, мышц и крупных вовлечения органов и лечение в дебюте заболевания и при рефрактерном течении заболевания.
Диагностические критерии в JDM пересматриваются, однако потребуется дальнейшая корректировка как новый инструменты по оценке результатов, особенно аутоантител и биомаркеров, которые разрабатываются.
Тщательный мониторинг состояния болезни пациентов и наличие опытной мультидисциплинарной команды имеет важное значение для хорошего клинического результата. Последние данные подчеркивают важность лечения заболеваний кожи агрессивно, как это связано с высокой болезненностью. Долгосрочные последующие исследования необходимы для уточнения осложнений. Учитывая редкость заболевания, международное сотрудничество имеет решающее значение для набора достаточной пациентов. Утверждена для оценки активности заболевания и повреждения необходимы для того, чтобы выполнить структурированный оценка результатов. Активности заболевания и оценки ущерба были разработаны, главным образом для клинических испытаний, что может быть сложным и трудоемким для использования в повседневной клинической практике.
В заключение эти SHARE основываются на мнениях экспертов сообщает наилучших имеющихся фактических данных и даются рекомендации по диагностике и лечению пациентов с комплектации, наряду с другими педиатрическими ревматические заболеваниями с целью улучшения исхода для пациентов с ЮДМ в Европе. Теперь будет важно расширить обсуждение и тестирование приемлемости для общества в целом.
Обсуждение
ЮДМ рабочей группы SHARE сформулированы в общей сложности 62 рекомендации по диагностике и ведению ЮДМ, основаны на систематическом обзоре литературы и процедура консенсуса. В общей сложности, 7 основополагающих принципов, 33 рекомендации по диагностике и 19 по терапии были приняты с >80% согласия между экспертами. Темы включают оценку состояния кожи, мышц и крупных вовлечения органов и лечение в дебюте заболевания и при рефрактерном течении заболевания.
Диагностические критерии в JDM пересматриваются, однако потребуется дальнейшая корректировка как новый инструменты по оценке результатов, особенно аутоантител и биомаркеров, которые разрабатываются.
Тщательный мониторинг состояния болезни пациентов и наличие опытной мультидисциплинарной команды имеет важное значение для хорошего клинического результата. Последние данные подчеркивают важность лечения заболеваний кожи агрессивно, как это связано с высокой болезненностью. Долгосрочные последующие исследования необходимы для уточнения осложнений. Учитывая редкость заболевания, международное сотрудничество имеет решающее значение для набора достаточной пациентов. Утверждена для оценки активности заболевания и повреждения необходимы для того, чтобы выполнить структурированный оценка результатов. Активности заболевания и оценки ущерба были разработаны, главным образом для клинических испытаний, что может быть сложным и трудоемким для использования в повседневной клинической практике.
В заключение эти SHARE основываются на мнениях экспертов сообщает наилучших имеющихся фактических данных и даются рекомендации по диагностике и лечению пациентов с комплектации, наряду с другими педиатрическими ревматические заболеваниями с целью улучшения исхода для пациентов с ЮДМ в Европе. Теперь будет важно расширить обсуждение и тестирование приемлемости для общества в целом.

 рис. 1Б Схема для лечения легкой/умеренной болезнью в впервые диагностированных и рефрактерных пациентов с ювенильным дерматомиозитом (ЮДМ).
рис. 1Б Схема для лечения легкой/умеренной болезнью в впервые диагностированных и рефрактерных пациентов с ювенильным дерматомиозитом (ЮДМ).
 Обсуждение
ЮДМ рабочей группы SHARE сформулированы в общей сложности 62 рекомендации по диагностике и ведению ЮДМ, основаны на систематическом обзоре литературы и процедура консенсуса. В общей сложности, 7 основополагающих принципов, 33 рекомендации по диагностике и 19 по терапии были приняты с >80% согласия между экспертами. Темы включают оценку состояния кожи, мышц и крупных вовлечения органов и лечение в дебюте заболевания и при рефрактерном течении заболевания.
Диагностические критерии в JDM пересматриваются, однако потребуется дальнейшая корректировка как новый инструменты по оценке результатов, особенно аутоантител и биомаркеров, которые разрабатываются.
Тщательный мониторинг состояния болезни пациентов и наличие опытной мультидисциплинарной команды имеет важное значение для хорошего клинического результата. Последние данные подчеркивают важность лечения заболеваний кожи агрессивно, как это связано с высокой болезненностью. Долгосрочные последующие исследования необходимы для уточнения осложнений. Учитывая редкость заболевания, международное сотрудничество имеет решающее значение для набора достаточной пациентов. Утверждена для оценки активности заболевания и повреждения необходимы для того, чтобы выполнить структурированный оценка результатов. Активности заболевания и оценки ущерба были разработаны, главным образом для клинических испытаний, что может быть сложным и трудоемким для использования в повседневной клинической практике.
В заключение эти SHARE основываются на мнениях экспертов сообщает наилучших имеющихся фактических данных и даются рекомендации по диагностике и лечению пациентов с комплектации, наряду с другими педиатрическими ревматические заболеваниями с целью улучшения исхода для пациентов с ЮДМ в Европе. Теперь будет важно расширить обсуждение и тестирование приемлемости для общества в целом.
Обсуждение
ЮДМ рабочей группы SHARE сформулированы в общей сложности 62 рекомендации по диагностике и ведению ЮДМ, основаны на систематическом обзоре литературы и процедура консенсуса. В общей сложности, 7 основополагающих принципов, 33 рекомендации по диагностике и 19 по терапии были приняты с >80% согласия между экспертами. Темы включают оценку состояния кожи, мышц и крупных вовлечения органов и лечение в дебюте заболевания и при рефрактерном течении заболевания.
Диагностические критерии в JDM пересматриваются, однако потребуется дальнейшая корректировка как новый инструменты по оценке результатов, особенно аутоантител и биомаркеров, которые разрабатываются.
Тщательный мониторинг состояния болезни пациентов и наличие опытной мультидисциплинарной команды имеет важное значение для хорошего клинического результата. Последние данные подчеркивают важность лечения заболеваний кожи агрессивно, как это связано с высокой болезненностью. Долгосрочные последующие исследования необходимы для уточнения осложнений. Учитывая редкость заболевания, международное сотрудничество имеет решающее значение для набора достаточной пациентов. Утверждена для оценки активности заболевания и повреждения необходимы для того, чтобы выполнить структурированный оценка результатов. Активности заболевания и оценки ущерба были разработаны, главным образом для клинических испытаний, что может быть сложным и трудоемким для использования в повседневной клинической практике.
В заключение эти SHARE основываются на мнениях экспертов сообщает наилучших имеющихся фактических данных и даются рекомендации по диагностике и лечению пациентов с комплектации, наряду с другими педиатрическими ревматические заболеваниями с целью улучшения исхода для пациентов с ЮДМ в Европе. Теперь будет важно расширить обсуждение и тестирование приемлемости для общества в целом.



