Патофизиология, передача, диагностика и лечение коронавирусной болезни 2019 (COVID-19)

Обзор 10 июля 2020 года
Pathophysiology, Transmission, Diagnosis, and Treatment of Coronavirus Disease 2019 (COVID-19)
Аннотация
Важность коронавирусной болезни 2019 (COVID-19) пандемии, в связи с новым тяжелым острым респираторным синдромом коронавируса 2 (SARS-CoV-2), вызвало во всем мире внезапное и существенное увеличение госпитализаций пневмонии с мультиорганной болезнью. В этом обзоре рассматриваются текущие данные о патофизиологии, передаче, диагностике и управлении COVID-19.
Наблюдения SARS-CoV-2 распространяются в основном через дыхательные капли при тесном контакте лицом к лицу. Инфекция может распространяться бессимптомными, пресимптоматическими и симптоматическими носителями. Среднее время от контакта с симптомом начала составляет 5 дней, и 97,5% людей, у которых развивают симптомы случается это в течение 11,5 дней. Наиболее распространенными симптомами являются лихорадка, сухой кашель, и одышка. Радиографические и лабораторные аномалии, такие как лимфопения и повышенная лактат дегидрогеназа, являются общими, но неспецифическими. Диагноз производится путем обнаружения SARS-CoV-2 с помощью тестирования цепной реакции на обратную транскрипцию полимеразы, хотя ложноотрицательные результаты теста могут возникать у 20% до 67% пациентов; однако это зависит от качества и сроков тестирования. Проявления КОВИД-19 включают бессимптомные носители и fulminant фулминантную болезнь, характеризующуюся сепсисом и острой дыхательной недостаточностью. Приблизительно 5% пациентов с КОВИД-19, и 20% из госпитализированных, испытывают тяжелые симптомы, требующие интенсивной терапии. Более 75% пациентов, госпитализированных с КОВИД-19, нуждаются в дополнительном кислороде. Лечение лиц с КОВИД-19 включает в себя лучшие практики для поддерживающего управления острой гипоксической дыхательной недостаточностью. Новые данные показывают, что дексаметазонная терапия снижает 28-дневную смертность у пациентов, нуждающихся в дополнительном кислороде, по сравнению с обычным уходом (21,6% против 24,6%; age-adjusted rate ratio, 0,83 (95% ДИ, 0,74-0,92) и то, что remdesivir ремдесивир улучшает время восстановления (выписка из больницы или отсутствие дополнительной потребности в кислороде) с 15 до 11 дней. В рандомизированном исследовании 103 пациентов с COVID-19 плазма реконвалисцентов не сократила время восстановления. Продолжающиеся испытания – тестирование противовирусной терапии, иммуномодуляторов и антикоагулянтов. Коэффициент летальности для COVID-19 заметно варьируется в зависимости от возраста: от 0,3 смертей на 1000 случаев среди пациентов в возрасте от 5 до 17 лет до 304,9 смертей на 1000 случаев среди пациентов в возрасте 85 лет и старше в США. Среди пациентов, госпитализированных в реанимацию, летальность составляет до 40%. В настоящее время разрабатывается по меньшей мере 120 вакцин SARS-CoV-2. До тех пор, пока не будет получена эффективная вакцина, основными методами сокращения распространения являются маски для лица, социальное дистанцирование и отслеживание контактов. Моноклональные антитела и hyperimmune гипериммунный глобулин могут обеспечить дополнительные профилактические стратегии.
Выводы и Актуальность. По состоянию на 1 июля 2020 года более 10 миллионов человек во всем мире были инфицированы SARS-CoV-2. Многие аспекты передачи, инфекции и лечения остаются неясными. Достижения в области профилактики и эффективного управления КОВИД-19 потребуют проведения фундаментальных и клинических исследований, а также мероприятий в области общественного здравоохранения и клинических мероприятий.
Введение
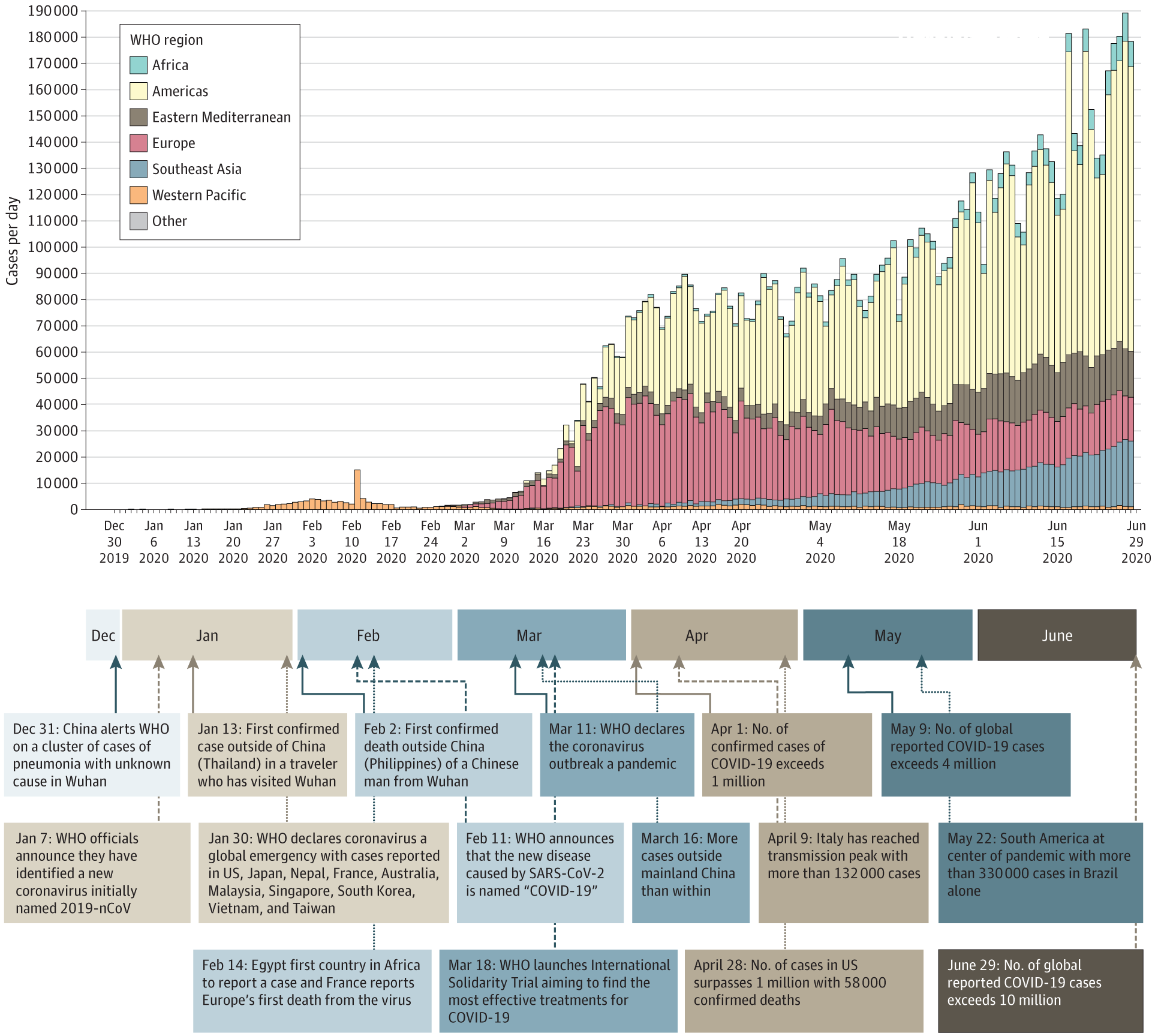
Пандемия коронавирусной болезни 2019 года (COVID-19) привела к резкому увеличению числа госпитализаций при пневмонии с многооргановой болезнью. COVID-19 вызван новым тяжелым острым коронавирусом острого респираторного синдрома 2 (SARS-CoV-2). ИНФЕКЦИЯ SARS-CoV-2 может быть бессимптомной или вызывать широкий спектр симптомов, таких как легкие симптомы инфекции верхних дыхательных путей и опасный для жизни сепсис. COVID-19 впервые появился в декабре 2019 года, когда группа пациентов с пневмонией неизвестной причины была признана в Ухане, Китай. По состоянию на 1 июля 2020 года SARS-CoV-2 затронул более 200 стран, в результате чего было выявлено более 10 миллионов выявленных случаев заболевания с 508 000 подтвержденных случаев смерти (рисунок 1).
В настоящем обзоре кратко излагаются имеющиеся данные о патофизиологии, передаче, диагностике и ведения COVID-19.
Методы
Мы искали PubMed, LitCovid и MedRxiv, используя поисковые термины коронавирус, коронавирус тяжелого острого респираторного синдрома 2, 2019-nCoV, SARS-CoV-2, SARS-CoV, MERS-CoV и COVID-19 для исследований, опубликованных с 1 января 2002 года по 15 июня 2020 года, и вручную искали ссылки на отдельные статьи. Текущие или завершенные клинические испытания были выявлены с использованием термина коронавирусной инфекции для поиска заболеваний на ClinicalTrials.gov, Китайского реестра клинических испытаний и Международной платформы регистра клинических испытаний. Мы выбрали статьи, относящиеся к общей читательской аудитории медицины, приоритеты рандомизированных клинических испытаний, систематические обзоры, и клинической практике руководящих принципов.
Наблюдения
Патофизиология
Коронавирусы являются крупными, окутанными, одноцепочечные РНК вирусы, найденные в людях и других млекопитающих, таких как собаки, кошки, курица, крупный рогатый скот, свиньи и птицы. Коронавирусы вызывают респираторные, желудочно-кишечные и неврологические заболевания. Наиболее распространенными коронавирусами в клинической практике являются 229E, OC43, NL63 и HKU1, которые обычно вызывают симптомы простуды у иммунокомпетентных лиц с препаратами. SARS-CoV-2 является третьим коронавирусом, который вызвал тяжелое заболевание у людей, которое распространяется я по всему миру в течение последних 2 декад. Первый коронавирус, который вызвал тяжелое заболевание был тяжелый острый респираторный синдром (SARS), который, как считалось, происходит из Фошане, Китай, и привел к пандемии SARS-CoV 2002-2003. Вторым был коронавирус, вызванный ближневосточным респираторным синдромом (БВРС), который возник с Аравийского полуострова в 2012 году.
SARS-CoV-2 имеет диаметр от 60 нм до 140 нм и отличительные шипы, начиная от 9 нм до 12 нм, давая вирионы появление солнечной короны (рисунок 2).
Через генетическую рекомбинацию и вариации, коронавирусы могут адаптироваться и заразить новых хозяев. Летучие мыши считаются естественным резервуаром для SARS-CoV-2, но было высказано предположение, что люди заразились SARS-CoV-2 через промежуточного хозяина, например, ящерицы.
Защита хозяина от SARS-CoV-2
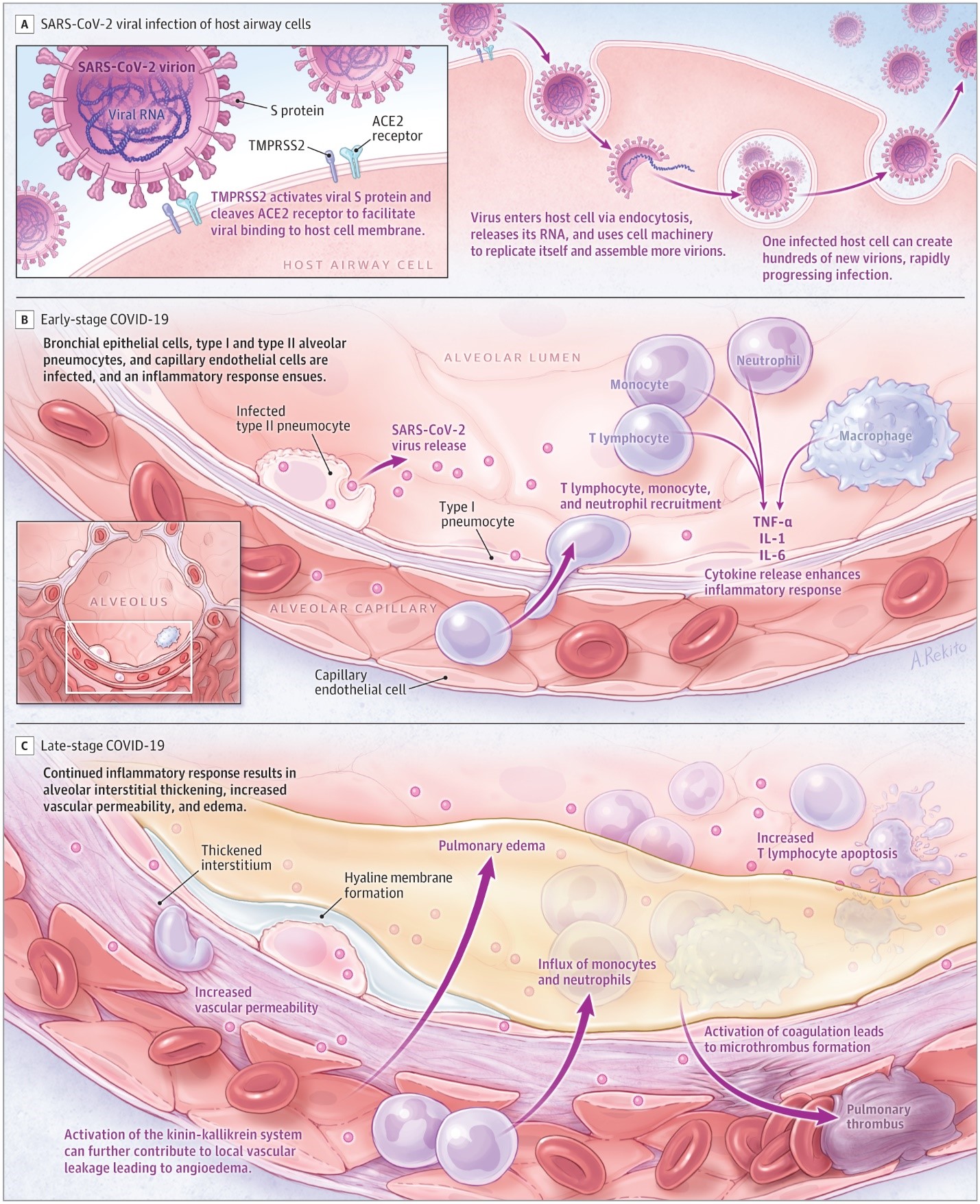
В начале инфекции SARS-CoV-2 поражает клетки, такие как носовые и бронхиальные эпителиальные клетки и пневмоциты, через вирусный структурный шип (S) белок, который связывается с ангиотензин-преобразовывая фермент 2 (ACE2) рецептор (рисунок 2). Тип 2 трансмембрана серин протеазы (TMPRSS2), присутствующие в клетке-хозяине, способствует вирусного поглощения путем расщепления ACE2 и активации БЕЛКА SARS-CoV-2 S, который опосредует вход коронавируса в клетки-хозяина. ACE2 и TMPRSS2 экспрессируются в клетках-мишенях-хозяев, особенно в клетках-мишенях альвеолярного эпителиального типа II. Подобно другим респираторным вирусным заболеваниям, таким как грипп, глубокая лимфопения может возникнуть у людей с КОВИД-19, когда SARS-CoV-2 заражает и убивает Т лимфоциты. Кроме того, вирусная воспалительный ответ, состоящая как из врожденного, так и адаптивного иммунного ответа (состоящий из гуморального и клеточного иммунитета), ухудшает лимфопоэзис и увеличивает апоптоз лимфоцитов. Хотя блокада рецепторов ACE2 от ингибитора АПФ и ангиотензин рецептор блокатор лекарства были гипотезы для повышения восприимчивости к инфекции ТОРС-КоВ-2, большие наблюдательные когорты не нашли связи между этими лекарствами и риском инфицирования или больничной смертности из-за COVID-19. Например, в исследовании 4480 пациентов с COVID-19 из Дании, предыдущее лечение ингибиторами АПФ или блокаторами рецепторов ангиотензина не было связано со смертностью.
На более поздних стадиях инфекции, когда репликация вируса ускоряется, целостность эпителиального эндотелиального барьера скомпрометирована. Помимо эпителиальных клеток, SARS-CoV-2 заражает легочные капиллярные эндотелиальные клетки, ускоряя воспалительный ответ и вызывая приток моноцитов и нейтрофилов. Вскрытия показали, диффузное утолщение альвеолярной стенки с моноядерными клетками и макрофагами, проникающих в воздушное пространство в дополнение к эндотелииту. Интерстициальные моноядерные воспалительные инфильтраты и отеки развиваются и появляются как матовые непрозрачности на компьютерной томографической визуализации. Легочный отек заполнения альвеолярных пространств с образованием гиалиновой мембраны следует, сочетается с ранней фазы острого респираторного дистресс-синдрома (ARDS). Брадикинин-зависимая ангиоэдема легких может способствовать болезни. Суммарно, эндотелиальный барьер нарушение, дисфункциональные альвеоларно-капиллярной передачи кислорода, и нарушение кислорода диффузии являются характерными особенностями COVID-19.
В тяжелой COVID-19 происходит фулминантная активация свертывания и потребления факторов свертывания крови. Отчет от Ухана, Китай, указал, что 71% из 183 лиц, которые умерли от COVID-19 отвечает критериям для диффузной внутрисосудистой коагуляции. Воспаленные ткани легких и легочные эндотелиальные клетки могут привести к образованию микротромбов и способствовать высокой частоте тромботических осложнений, таких как глубокий венозный тромбоз, легочная эмболия и тромботические артериальные осложнения (например, ишемия конечностей, ишемический инсульт, инфаркт миокарда) у тяжелобольных пациентов. Развитие вирусного сепсиса, определяемого как жизнеугрожающая дисфункция органов, вызванная дисрегулируемой реакцией хозяина на инфекцию, может способствовать дальнейшей мультиорганной недостаточности.
Передача инфекции SARS-CoV-2
Эпидемиологические данные свидетельствуют о том, что капли, выделяемые вовремя face-to-face во время разговора, кашля или чихания, являются наиболее распространенным способом передачи инфекции (Box 1). Длительное воздействие инфицированного человека (находясь в пределах 6 футов в течение по крайней мере 15 минут) и краткое воздействие на лиц, которые симптоматически (например, кашель) связаны с более высоким риском передачи, в то время как краткое воздействие бессимптомных контактов менее вероятно, приведет к передаче. Контактное распространение поверхности (прикосновение к поверхности с вирусом на нем) является еще одним возможным способом передачи. Передача может также происходить через аэрозоли (меньшие капли, которые остаются взвешенными в воздухе), но неясно, если это является значительным источником инфекции у людей за пределами лабораторных испытаний. Существование аэрозолей в физиологических состояниях (например, кашель) или обнаружение нуклеиновой кислоты в воздухе не означает, что мелкие частицы, передаваемые до воздуха, являются инфекционными. Материнская COVID-19 в настоящее время считается связанным с низким риском вертикальной передачи. В большинстве описанных случаев материнская инфекция SARS-CoV-2 произошла в третьем триместре беременности, без материнской смертности и благоприятного клинического курса у новорожденных.

Блок 1.
Передача, симптомы и осложнения коронавирусной болезни 2019 (COVID-19)
Передача тяжелого острого респираторного синдрома коронавируса 2 (SARS-CoV-2) происходит главным образом через дыхательные капли от очного контакта и, в меньшей степени, через загрязненные поверхности. Распространение аэрозолей может иметь место, но роль аэрозольного распространения у человека остается неясной. По оценкам, от 48% до 62% передачи может происходить через пресимптоматических носителей.
Общие симптомы у госпитализированных пациентов включают лихорадку (70%-90%), сухой кашель (60%-86%), одышку (53%-80%), усталость (38%), миалгии (15%-44%), тошноту/рвоту или диарею (15%-39%), головную боль, слабость (25%), и ринорея (7%). Аносмия или агевзия может быть единственным симптомом представления примерно в 3% лиц с COVID-19.
Общие лабораторные аномалии среди госпитализированных пациентов включают лимфопения (83%), повышенные воспалительные маркеры (например, скорость осаждения эритроцитов, C-реактивный белок, ферритин, фактор некроза опухоли- я, IL-1, IL-6), а также аномальные параметры коагуляции (например, длительное время протромбина, тромбоцитопения, повышенный Д-димер (46% пациентов), низкий фибриноген).
Общие радиографические выводы лиц с COVID-19 включают двусторонние, нижней доли преобладают инфильтраты радиографической визуализации грудной клетки и двусторонних, периферийных, нижней доли матового стекла непрозрачности и / или консолидации при томографии органов грудной клетки.
Общие осложнения у госпитализированных пациентов с КОВИД-19 включают пневмонию (75%); острый респираторный дистресс-синдром (15%); острую повреждение печени, характеризующуюся повышением аспартатной трансаминазе, аланина трансаминаза и билирубина (19%); повреждение сердца, включая повышение тропонина (7%-17%), острая сердечная недостаточность, дисритмии и миокардит; протромботическая коагулопатия, приводящая к венозным и артериальным тромбоэмболическим явлениям (10%-25%); острая повреждение почек(9%); неврологические проявления, в том числе в том числе нарушенное сознание (8%) и острое цереброваскулярное заболевание (3%); и шок (6%).
Редкие осложнения среди тяжелобольных пациентов с COVID-19 включают цитокинового шторма и синдром активации макрофага (т. е. вторичный гемофагоцитарный лимфогистиоцитоз).
Клиническое значение передачи SARS-CoV-2 с неодушевленных поверхностей трудно интерпретировать, не зная минимальную дозу вирусных частиц, которые могут инициировать инфекцию. Вирусная нагрузка, как представляется, сохраняется на более высоких уровнях на непроницаемых поверхностях, такие как нержавеющая сталь и пластик, чем проницаемые поверхности, такие как картон. Вирус был идентифицирован на непроницаемых поверхностях на срок до 3 до 4 дней после инокуляции. Широкое вирусное загрязнение больничных палат было задокументировано. Однако считается, что количество вируса, обнаруженного на поверхностях, быстро распадается в пределах 48 до 72 часов. Хотя обнаружение вируса на поверхностях может привести к потенциальной передаче возбудителя через (объекты, такие как дверная дверь, столовые приборы, или одежда, которые могут быть загрязнены SARS-CoV-2) и необходимость надлежащей гигиены окружающей среды, капельное распространения при лицом к лицу контакт остается основным способом передачи.
Вирусная нагрузка в верхних дыхательных путях, как представляется, достигает пика во время появления симптомов и вирусного выделения начинается примерно за 2 до 3 дней до появления симптомов. Бессимптомные и пресимптоматические носители могут передавать SARS-CoV-2. В Сингапуре пресимпомтическая передача была описана в кластерах пациентов с близким контактом (например, через церковный или пение класса) примерно за 1 до 3 дней до того, как исходного пациента развились симптомы. Пресимптоматическая передача считается основным фактором распространение SARS-CoV-2. Моделирование исследований из Китая и Сингапура оценили процент инфекций, передаваемых от пресимптоматического человека, как 48% до 62%. Глоточное выделение высоко в течение первой недели инфекции в то время, в котором симптомы по-прежнему мягкий, что может объяснить эффективную передачу SARS-CoV-2, потому что инфицированные люди могут быть инфекционными, прежде чем они понимают, что они заболели. Хотя исследования описали долю, начиная от 4% до 32%, неясно, представляют ли эти доклады действительно бессимптомную инфекцию лиц, которые никогда не развиваются симптомы, передача лицами с очень мягкими симптомами, или передачи лиц, которые бессимптомно во время передачи, но впоследствии развивать симптомы. Систематический обзор по этой теме предложил, что истинная бессимптомная инфекция, вероятно, редкость.
Хотя вирусная нуклеиновая кислота может быть обнаружена в мазках горла в течение 6 недель после начала болезни, несколько исследований показывают, что вирусные культуры, как правило, отрицательные для SARS-CoV-2 через 8 дней после появления симптомов. Это подтверждается эпидемиологическими исследованиями, которые показали, что передача не произошло при контактах, воздействие которых на индикаторный случай началось более чем через 5 дней после появления симптомов в индикаторном случае. Это позволяет предположить, что люди могут быть освобождены от изоляции, основанной на клиническом улучшении. Центры по контролю и профилактике заболеваний рекомендуют изолировать, по крайней мере, 10 дней после появления симптомов и 3 дня после улучшения симптомов. Однако остается неопределенность относительно того, требуется ли последовательное тестирование для конкретных подгрупп, таких как пациенты с ослабленным иммунитетом или тяжелобольные пациенты, для которых разрешение симптомов может быть отложено, или пожилые люди, проживающие в учреждениях краткосрочного или долгосрочного ухода.
Клиническая Презентация
Средний (межквартильный диапазон) инкубационный период (время от воздействия симптомов начала) для COVID-19 составляет примерно 5 (2-7) дней. Приблизительно 97,5% лиц, которые развивают симптомы будет проявляться в течение 11,5 дней после инфицирования. Средний (межквартильный диапазон) интервал от появления симптомов до госпитализации составляет 7 (3-9) дней. Средний возраст госпитализированных пациентов колеблется между 47 и 73 годами, с большинством когорт, имеющих мужской перевес примерно 60%. Среди пациентов, госпитализированных с COVID-19, от 74% до 86% в возрасте не менее 50 лет.
COVID-19 имеет различные клинические проявления (Box 1 и Box 2). В исследовании 44 672 пациентов с COVID-19 в Китае, 81% пациентов имели легкие проявления, 14% имели тяжелые проявления, и 5% имели критические проявления (определяемые дыхательной недостаточностью, септическим шоком и/или множественной дисфункцией органов). Исследование 20 133 человек, госпитализированных с COVID-19 в Великобритании, сообщило, что 17,1% были госпитализированы в отделения интенсивной или блоки интенсивной терапии (intensive care units (ICUs)).

Блок 2.
Обычно задаваемые вопросы о коронавирусной болезни 2019 (COVID-19)
Как чаще всего передается тяжелый коронавирус острого респираторного синдрома 2 (SARS-CoV-2)?
SARS-CoV-2 чаще всего распространяется через дыхательные капли (например, от кашля, чихания, криках) вовремя face-to-face контакта или при поверхностном загрязнении.
Каковы наиболее распространенные симптомы COVID-19?
3 наиболее распространенных симптомы лихорадка, кашель, и одышка. Дополнительные симптомы включают слабость, усталость, тошнота, рвота, диарея, изменения вкуса и запаха.
Как ставится диагноз?
Диагноз COVID-19, как правило, производится с помощью полимеразной цепной реакции тестирования носоглотки мазок. Однако, учитывая возможность ложноотрицательных результатов теста, клинические, лабораторные и визуальные результаты также могут быть использованы для постановки предполагаемого диагноза для лиц, для которых существует высокий индекс клинических подозрений на инфекцию.
Каковы современные фактические методы лечения для лиц с COVID-19?
Поддерживающая помощь, включая дополнительный кислород, является основным методом лечения для большинства пациентов. Недавние исследования показывают, что дексаметазон снижает смертность (анализ подгрупп показывает, что польза ограничена пациентами, которые нуждаются в дополнительном кислороде и у которых есть симптомы >7 дней) и ремдесивир улучшает время для восстановления (анализ подгрупп показывает, что польза ограничена у пациентов, не получающими механическую вентиляцию легких).
Какой процент людей являются бессимптомными носителями, и насколько они важны в передаче болезни?
Истинная бессимптомная инфекция считается редкостью. Среднее время от контакта с симптомами начала составляет 5 дней, и до 62% передачи может произойти до появления симптомов.
Эффективны ли маски в предотвращении распространения?
Да. Маски для лица снижают распространение вирусной респираторной инфекции. Респираторы N95 и хирургические маски обеспечивают существенную защиту (по сравнению с маской), а хирургические маски обеспечивают большую защиту, чем тканевые маски. Однако физическое дистанцирование также связано со значительным сокращением вирусной передачи, при этом большие расстояния обеспечивают большую защиту. Важное значение имеют также такие дополнительные меры, как дезинфекция рук и окружающей среды.
Хотя только около 25% инфицированных пациентов имеют коморбидность , от 60% до 90% госпитализированных инфицированных пациентов имеют сопутствующие заболевания. Наиболее распространенными сопутствующими заболеваниями у госпитализированных пациентов являются гипертония (присутствует у 48%-57% пациентов), диабет (17%-34%), сердечно-сосудистые заболевания (21%-28%), хронические легочные заболевания (4%-10%), хронические заболевания почек (3%-13%), злокачественность (6%-8%) и хронические заболевания печени (<5%).
Наиболее распространенными симптомами у госпитализированных пациентов являются лихорадка (до 90% пациентов), сухой кашель (60%-86%), одышка (53%-80%), усталость (38%), тошнота/рвота или диарея (15%-39%), и миалгия (15%-44%). Пациенты также могут присутствовать с неклассическими симптомами, например, изолированные желудочно-кишечные симптомы. Аносмия и/или вкусовые дисфункции зарегистрированы у 64% до 80% пациентов. Аносмия или агенезия может быть единственным симптомом представления примерно у 3% пациентов.
Осложнения COVID-19 включают нарушение функции сердца, мозга, легких, печени, почек и системы свертывания. COVID-19 может привести к миокардиту, кардиомиопатии, желудочковой аритмии, и гемодинамическая нестабильность. Острые цереброваскулярные заболевания и энцефалит наблюдаются при тяжелых заболеваниях (до 8% пациентов). Венозные и артериальные тромбоэмболические явления происходят в 1 от 25% до 25% у госпитализированных пациентов с КОВИД-19. В отделении интенсивной терапии венозные и артериальные тромбоэмболические явления могут возникать в до 31% до 59% пациентов с CO VID-19.
Приблизительно от 17% до 35% госпитализированных пациентов с КОВИД-19 проходят лечение в отделении интенсивной терапии, чаще всего из-за гипоксемической дыхательной недостаточности. Среди пациентов в отделении интенсивной терапии с КОВИД-19, от 29% до 91% требуют инвазивной механической вентиляции. В дополнение к дыхательной недостаточности у госпитализированных пациентов могут развиться острая поражение почек (9%), дисфункция печени (19%), кровотечения и дисфункция коагуляции (10%-25%), а также септический шок (6%).
Приблизительно от 2% до 5% людей с лабораторно подтвержденным COVID-19 моложе 18 лет, при этом средний возраст составляет 11 лет. Дети с КОВИД-19 имеют более легкие симптомы, которые преимущественно ограничены верхними дыхательными путями, и редко требуют госпитализации. Непонятно, почему дети менее восприимчивы к COVID-19. Потенциальные объяснения включают в себя, что дети имеют менее надежные иммунные реакции (т.е. без цитокинов буря), частичный иммунитет от других вирусных воздействий, и более низкие показатели воздействия ТОРС-КоВ-2. Несмотря на то, что большинство педиатрических случаев являются мягкими, небольшой процент (<7%) у детей, поступивших в больницу для COVID-19, развивается тяжелое заболевание, требующее механической вентиляции легких. Редкий мультисистемный воспалительный синдром, похожий на болезнь Кавасаки, недавно был описан у детей в Европе и Северной Америке с инфекцией SARS-CoV-2. Этот многосистемный воспалительный синдром у детей является редкостью (2 из 100 000 человек в возрасте <21 года).
Анализы и диагностика
Диагноз COVID-19, как правило, производится с помощью полимеразы цепной реакции тестирования с помощью носовой тампон (Box 2). Однако, из-за ложноотрицательных результатов теста ставки SARS-CoV-2 ПЦР тестирования носовых тампонов, клинические, лабораторные и изображения выводы также могут быть использованы для принятия предполагаемого диагноза.
Диагностическое тестирование: Полимеразная цепная реакция и серология
Обратная транскрипция полимеразной цепной реакции на основе SARS-CoV-2 РНК обнаружения из респираторных образцов (например, носоглотки) является стандартом для диагностики. Тем не менее, чувствительность тестирования варьируется в зависимости от времени тестирования относительно воздействия. Одно моделирование исследования оценкам чувствительность на 33% на 4 дня после воздействия, 62% в день появления симптомов, и 80% на 3 дня после появления симптомов. Факторы, способствующие ложноотрицательные результаты теста включают адекватность метода сбора образцов, время от воздействия, и образец источника. Образцы нижних дыхательных путей, такие как бронхоалволярная жидкость для лаважа, более чувствительны, чем образцы верхних дыхательных путей. Среди 1070 образцов, собранных у 205 пациентов с COVID-19 в Китае, бронхоальолярный лаваж жидкости образцы имели самые высокие положительные показатели SARS-CoV-2 ПЦР результаты тестирования (93%), а затем мокроты (72%), носовые мазки (63%), и фарингиальные тампоны (32%). SARS-CoV-2 также могут быть обнаружены в фекалиях, но не в моче. Слюна может быть альтернативным источником образца, который требует меньше личного защитного оборудования и меньше тампонов, но требует дальнейшей проверки.
Несколько серологических тестов могут также помочь в диагностике и измерении ответов на новые вакцины. Однако наличие антител не может подтверждать иммунитет, потому что не все антитела, вырабатываемые в ответ на инфекцию, нейтрализуются. Возможно ли и как часто возникают повторные инфекций SARS-CoV-2, остается неизвестным. Неизвестно, изменяет ли наличие антител восприимчивость к последующей инфекции или как долго длится защита антител. IgM антитела обнаруживаются в течение 5 дней после заражения, с более высокими уровнями IgM в течение нескольких недель от 2 до 3 болезни, в то время как ответ IgG впервые видели примерно через 14 дней после появления симптомов. Высокие титры антител появляются при более тяжелом заболевании. Доступные серологические анализы включают на пунктах оказания медицинской помощи количественные анализы и высокой пропускной способности ферментные иммуноанализы. Однако производительность теста, точность и достоверность являются переменными.
Лабораторные Данные
Систематический обзор 19 исследований 2874 пациентов, которые были в основном из Китая (средний возраст, 52 лет), из которых 88% были госпитализированы, сообщил типичный диапазон лабораторных аномалий при COVID-19, в том числе повышенный С-реактивный белок сыворотки (увеличенный в 60% пациентов), лактат дегидрогеназы (увеличенный примерно в 50%-60%), аланин аминотрансфераза (повышенный примерно в 25%), а также апартат аминотрансферазы (приблизительно 33%. Приблизительно 75% пациентов имели низкий альбумин. Наиболее распространенной гематологической аномалией является лимфопения (абсолютное количество лимфоцитов 1.0 и 109/L), который присутствует у 83% госпитализированных пациентов с COVID-19. В сочетании с коагулопатией, незначительное удлинение протромбиного времени (удлинено у >5% пациентов), мягкий тромбоцитопения (присутствует примерно в 30% пациентов) и повышенные значения D-dimer (в настоящее время 43%- 60% пациентов) являются общими. Однако, большинство из этих лабораторных характеристик являются неспецифическими и распространены при пневмонии. Более тяжелые лабораторные аномалии были связаны с более тяжелой инфекцией. D-димер и, в меньшей степени, лимфопенения, кажется, имеют самые большие прогностические ассоциации.
Визуализация
Характерные аномалии томографической томографии грудной клетки для COVID-19 являются диффузными, периферийными непрозрачностями матового стекла (рисунок 3).70 Непрозрачность матового стекла имеет плохо определенные поля, воздушные бронхограммы, гладкие или нерегулярные интралобулярные или септальные утолщения, и утолщение прилегающей плевры. В начале болезни томография грудной клетки визуализации выявляет находки примерно в 15% лиц, и рентгенография грудной клетки примерно в 40% людей может быть нормальным. Быстрая динамика аномалий может произойти в первые 2 недели после появления симптомов, после чего они постепенно спадают.
Находки, выявляемой томографией, неспецифические и перекрываются с другими инфекциями, поэтому диагностическая ценность компьютерной томографической томографии для COVID-19 ограничена. Некоторые пациенты, поступившие в больницу с полимеразной цепной реакции тестирования-подтвержденных SARS-CoV-2 инфекции имеют нормальные компьютерные томографические изображения , в то время как у других пациентов патологические изменения при компьютерной томографические грудной клетки изображений соответствующие COVID-19 появляются днями раньше до обнаружения SARS-CoV-2 РНК.
Лечение
Поддерживающая терапия и дыхательная поддержка
В настоящее время многие страны и профессиональные общества должны следовать передовым практикам по поддержке управления острой гипоксической дыхательной недостаточностью и ОРДС. Основанными на доказанных данных, были разработаны многими странами и профессиональными обществами,72-74, включая руководящие принципы, которые регулярно обновляются Национальными институтами здравоохранения.
Более 75% пациентов, госпитализированных с КОВИД-19, нуждаются в дополнительной кислородной терапии. Для пациентов, которые не реагируют на обычную кислородную терапию, подогретый кислорода высоким потоком через носовую канулю может быть введен. Для пациентов, нуждающихся в инвазивной механической вентиляции легких, защитная вентиляция легких с низкими приливными объемами (4-8 м/кг, предполагаемому весу тела) и плато давления менее 30 мг Hg рекомендуется. Кроме того, прон -позиционирования, более высокий положительное давления в конце выдоха, и краткосрочные нейромышечная блокада с цисакурином или другими мышечными релаксантами может облегчить оксигинацию. Хотя некоторые пациенты с КОВИД-19- связанных дыхательной недостаточности имеют высокие резервы легких, они по-прежнему могут извлечь выгоду из защитной вентиляции легких. Когорты пациентов с ОРДС показали аналогичную неоднородность в возможностях легких, и даже пациенты с большими возможностями показали выгоду от более низких стратегий вентиляционного объема.
Показания интубации в КОВИД-19- связанных дыхательной недостаточности является спорным, потому что многие пациенты имеют нормальную работу дыхания, но тяжелую гипоксемии. “Ранняя” интубации дает время для более контролируемого процесса интубации, что важно, учитывая логистические проблемы перемещения пациентов в изолятор с аппаратами ИВЛ и надевать средства индивидуальной защиты перед интубацией. Тем не менее, гипоксемия при отсутствии дыхательной недостаточности хорошо переносится, и пациенты могут справляться без механической вентиляции легких. Раннее выполнение интубации могут привести к лечению некоторых пациентов механической вентиляцией легких без необходимости и подвергая их дополнительным осложнениям. В настоящее время имеется недостаточно доказательств для вынесения рекомендаций в отношении более ранней интубации.
В обсервационных исследованиях примерно 8% госпитализированных пациентов с КОВИД-19 имеют бактериальную или грибковую ко-инфекцию, но до 72% лечатся антибиотиками широкого спектра действия. В ожидании дальнейших данных, может быть разумно продолжать антибактериальные препараты у пациентов с COVID-19 и резервировать их для тех, у кого имеются радиологические находки и / или воспалительные маркеры связанные с ко-инфекцией или которые являются иммунокомпроментированными и / или у критически больных.
Таргетирование вируса и ответ организма
В настоящее время проводится оценка или разработаны следующие классы лекарственных средств для ведения КОВИД-19: противовирусные препараты (например, ремдесивир, фавипиравир), антитела (например, плазма выздоравливающая, гипериммунные иммуноглобулины), противовоспалительные средства (дексаметазон, статины), целевые иммуномодуляторные терапии (например, тоцилизумаб, сарилумаб, анакинра, руксолитиниб), антикоагулянты (например, гепарин). Вполне вероятно, что различные методы лечения могут иметь различные эффективности на разных стадиях болезни и в различных проявлениях заболевания. Вирусные ингибирование, как ожидается, будет наиболее эффективным на ранних стадиях инфекции, в то время как у госпитализированных пациентов иммуномодуляционные средства могут быть полезны для предотвращения прогрессирования заболевания, а антикоагулянты могут быть полезны для предотвращения тромбоэмболических осложнений.
Более 200 испытаний хлорохина/гидроксихлорохина, соединений, которые подавляют вирусный вход и эндоцитоз ТОРС-КоВ-2 в пробирке и могут иметь полезные иммуномодуляционные эффекты in vivo, были начаты, но ранние данные клинических испытаний у госпитализированных пациентов с КОВИД-19 не продемонстрировали явную пользу. Клинические испытания 150 пациентов в Китае, поступивших в больницу для легкой и умеренной КОВИД-19, не нашли влияния на отрицательное трансформацию SARS-CoV-2 на 28 дней (основной показатель исхода) по сравнению только со стандартом медицинской помощи. Два ретроспективных исследования не обнаружили влияния гидроксихлорохина на риск интубации или смертности среди пациентов, госпитализированных для COVID-19. Одно из этих ретроспективных многоцентровых когортных исследований по сравнению с больничной смертностью между больными гидроксихлорохином плюс азитромицин (735 пациентов) , гидроксихлорохин только (271 пациентов), азитромицин только (211 пациентов), и ни один препарат (221 пациентов), но не сообщил никаких различий по группам. Неблагоприятные эффекты являются общими, наиболее примечательно удлинение QT с повышенным риском сердечных осложнений в и без того уязвимой популяции. Эти выводы не поддерживают использование off-label (гидрокси)хлорохин либо с или без коадминистиции азитромицина. Рандомизированные клинические испытания продолжаются и должны обеспечить больше доказательств.
Большинство противовирусных препаратов, проходящих клиническое тестирование у пациентов с КОВИД-19, перепрофилированные противовирусные препараты, первоначально разработанными против гриппа, ВИЧ, Эбола или SARS/MERS. Использование ингибитора протеазы лопинавир-ритонавир, который нарушает репликацию вируса в пробирке, не показали пользы по сравнению со стандартной помощью в рандомизированном, контролируемом, открытом исследовании 199 госпитализированных взрослых пациентов с тяжелой COVID-19. Среди ингибитора РНК-зависимой РНК, которые останавливают репликацию SARS-CoV-2, оцениваемые, включая рибавирин, фавипиравир и ремдесивир, последний, кажется, самый многообещающий. Первые предварительные результаты двойного слепого, рандомизированного, плацебо-контролируемого испытания 1063 взрослых госпитализированы с COVID-19 и доказательства участия нижних дыхательных путей, которые были случайным образом назначены для получения внутривенного ремдесивира или плацебо на срок до 10 дней показали, что пациенты рандомизированных получать remdesivir было меньше времени для восстановления, чем пациенты в группе плацебо (11 против 15 дней). Отдельные рандомизированные, открытый исследования среди 397 госпитализированных пациентов с COVID-19, которые не требуют механической вентиляции сообщили, что 5 дней лечения с ремдесивиром не отличается от 10 дней с точки зрения клинического состояния на 14день. Влияние ремдесивира на выживание остается неизвестным.
Лечение плазмой, полученной у пациентов, выздоровевших от вирусных инфекций, впервые было зарегистрировано во время пандемии гриппа 1918 года. Первый доклад 5 критически больных пациентов с COVID-19 лечение выздоравливающей плазмы, содержащей нейтрализующие антитела показали улучшение клинического статуса среди всех участников, определяемой как сочетание изменений температуры тела, Sequential Organ Failure Assessment score, (*Последовательная оценка органной недостаточности (SOFA score), ранее известная как оценка органной недостаточности, связанной с сепсисом, используется для отслеживания состояния человека во время пребывания в отделении интенсивной терапии (ОИТ), чтобы определить степень функции органов человека или частоту недостаточности .Оценка основана на шести различных шкалах, по одному для дыхательной, сердечно-сосудистой, печеночной, коагуляционной, почечной и неврологической систем. Шкала SOFA. Онлайн калькулятор https://medsoftpro.ru/kalkulyatory/sofa-scores.html,
Оценка результатов в баллах:
12 — множественные органные дисфункции
13-17 — переход дисфункции в недостаточность
24 — высокая вероятность летального исхода), частичное давление кислорода / фракция вдыхаемого кислорода, вирусная нагрузка, сыворотка антитела титр, обычный биохимический индекс крови, ARDS, и вентиляции и статус экстракорпоральной мембраны оксигенации поддержки до и после выздоравливающей плазмы переливания. Однако, последующий мультицентровое, открытое, рандомизированные клинические испытания 103 пациентов в Китае с тяжелой COVID-19 не нашли статистической разницы во времени к клиническому улучшению в течение 28 дней среди пациентов рандомизированных получать выздоравливающей плазмы против стандартное лечение только (51,9% против 43,1%).91 Однако, испытание было остановлено рано из-за замедления регистрации , которые ограничивали возможности для обнаружения клинически важной разницы. Изучаемые альтернативные подходы включают использование выздоравливающих плазменных гипериммуновых глобулинов и моноклональных антител, нацеленных на SARS-CoV-2.
Альтернативные терапевтические стратегии состоят из модуляции воспалительной реакции у пациентов с COVID-19. Моноклональные антитела, направленные против ключевых воспалительных посредников, таких как интерферон гамма, интерлейкин 1, интерлейкин 6, и дополнение фактор 5a, все целевые подавляющее воспалительные реакции после инфекции SARS-CoV-2 с целью предотвращения повреждения органов. Из них интерлейкин 6 ингибиторы tocilizumab и сарилумаб лучше изучены, с более чем десятка рандомизированных клинических испытаний в стадии реализации. Ингибиторы тирозин, такие ингибиторы, как imatinib, изучаются на их потенциал для предотвращения проницаемости легочных сосудов у людей с COVID-19.
Исследования кортикостероидов для вирусной пневмонии и ОРДС дали смешанные результаты. Однако, рандомизированная оценка COVID-19 Терапия (RECOVERY) исследование, который рандомизированных 2104 пациентов с COVID-19 получать 6 мг ежедневно дексаметазона на срок до 10 дней и 4321 для получения обычного ухода, обнаружили, что дексаметазон снизил 28-дневный все-причины смертности (21,6% против 24,6%; соотношение с поправкой на возраст, 0,83 95% CI , 0.74-0.92]; P < .001). Наибольший результат был у пациентов с симптомами более 7 дней и пациентов, которым требовалась механическая вентиляция легких. В отличие от этого не было никакой пользы (и возможность вреда) среди пациентов с более короткой продолжительностью симптомов и без дополнительных потребностей в кислороде. Ретроспективное когортное исследование 201 пациента в Ухане, Китай, с подтвержденной пневмонией COVID-19 и ОРДС сообщило, что лечение метилпреднизолоном было связано со снижением риска смерти (коэффициент опасности, 0,38 (95% ДИ, 0,20-0,72).
Тромбоэмболическая профилактика с подкожной низкой молекулярной массой гепарина рекомендуется для всех госпитализированных пациентов с COVID-19. Исследования продолжаются, чтобы оценить, имеют ли некоторые пациенты (т. е. с повышенным D-димер) выгоду от терапевтической антикоагуляляции.
Различия
Непропорционально большой процент госпитализаций и смертей COVID-19 приходится на население с низким уровнем дохода и меньшинств. В докладе Центров по контролю и профилактике заболеваний 580 госпитализированных пациентов, по которым имеются данные о расе, 33% были черными и 45% были белыми, в то время как 18% жителей в окружающем сообществе были черными и 59% были белыми. Непропорционально распространенность COVID-19 среди чернокожих пациентов была отдельно зарегистрирована в ретроспективном когортном исследовании 3626 пациентов с COVID-19 из Луизианы, в котором 77% пациентов, госпитализированных с COVID-19 и 71% пациентов, которые умерли от COVID-19 были черные, но черные лица составили только 31% населения области. Это непропорциональное бремя может быть отражением неравенства в жилье, транспорт, занятость и здоровье. Меньшинства с большей вероятностью живут в густонаселенных общинах или жилищах, зависят от общественного транспорта или работают на работах, для которых удаленные работы невозможны (например, водитель автобуса, работник общественного питания). Чернокожие также имеют более высокую распространенность хронических заболеваний, чем белые.
Прогноз
Общая больничная смертность от COVID-19 составляет примерно от 15% до 20%, но до 40% среди пациентов, нуждающихся в госпитализации. Однако показатели смертности варьируются в зависимости от когорт, что отражает различия в полноте тестирования и идентификации случаев заболевания, переменных пороговых значениях госпитализации и различиях в исходах. Больничная смертность колеблется от менее 5% среди пациентов в возрасте до 40 лет до 35% для пациентов в возрасте от 70 до 79 лет и более 60% для пациентов в возрасте от 80 до 89 лет. Расчетные общие показатели смертности по возрастной группе на 1000 подтвержденных случаев заболевания приведены в таблице. Поскольку не все люди, которые умирают во время пандемии, проходят тестирование на КОВИД-19, фактическое число случаев смерти от КОВИД-19 превышает зарегистрированные цифры.
Хотя долгосрочные исходы ОТ COVID-19 в настоящее время неизвестны, пациенты с тяжелыми заболеваниями, вероятно, пострадают от существенных осложнений. Выживание от сепсиса связано с повышенным риском смертности в течение по крайней мере 2 лет, новой физической неполноценности, новых когнитивных нарушений и повышенной уязвимости к рецидивирующей инфекции и дальнейшему ухудшению здоровья. Подобные осложнения, вероятно, будут замечены у выживших после тяжелой COVID-19.
Профилактика и разработка вакцин
COVID-19 является потенциально предотвратимым заболеванием. Взаимосвязь между интенсивностью действий в области общественного здравоохранения и контролем за передачей инфекции ясна из эпидемиологии инфекции во всем мире. Однако, поскольку большинство стран приняли многочисленные меры по борьбе с инфекцией, трудно определить относительную пользу каждого. Этот вопрос становится все более важным, поскольку дальнейшие мероприятия будут необходимы до тех пор, пока не станут доступны эффективные вакцины или методы лечения. В целом, эти мероприятия могут быть разделены на те, которые состоят из личных действий (например, физическое дистанцирование, личная гигиена, и использование защитного оборудования), случае и контакт идентификации (например, тест-след-трек-изоляция, reactive школы или изоляция на рабочем месте), нормативные действия (например, правительственные ограничения на размеры собраний или деловой потенциал; пребывание на дому; проактивные школы, рабочие места, и закрытие общественного транспорта или его ограничения; , а также международные пограничные меры (например, закрытие границ или принудительное карантин). Ключевым приоритетом является определение сочетания мер, которые сводят к минимуму социальные и экономические потрясения при адекватном контроле за инфекцией. Оптимальные меры могут варьироваться в зависимости от ограниченности ресурсов, географии (например, островных государств и международных пограничных мер), численности населения и политических факторов (например, грамотность в области здравоохранения, доверие к правительству, культурное и языковое разнообразие).
Доказательства, лежащие в основе этих мероприятий в области общественного здравоохранения, не изменились со 1918 года, когда пандемия гриппа 1918 года и эмпирические данные подтверждают, что мероприятия общественного здравоохранения, включая карантин на дому после инфицирования, ограничение массовых мероприятий, ограничений на поездки и социальное дистанцирование, связаны со снижением уровня передачи. Риск вспышки следует за этим, когда эти мероприятия отменяются.
В настоящее время вакцина для человека не доступна для SARS-CoV-2, однако в настоящее время разрабатывается около 120 кандидатов. Подходы включают в себя использование нуклеиновых кислот (ДНК или РНК), инактивированных или живых ослабленных вирусов, вирусных векторов, а также рекомбинантных белков или вирусных частиц. Трудности для разработки эффективной вакцины состоят из технических барьеров (например, являются ли S или рецептор-связывающие белки домена провоцируют больше защитных антител, до контакта с аденовирусным серотипом 5(который уменьшает иммуногенность в вирусной векторной вакцине) , осуществимость крупномасштабного производства и регулирования (например, обеспечение безопасности и эффективности), а также правовых барьеров (например, соглашения о передаче технологии и лицензировании). Белок SARS-CoV-2 S, по-видимому, является перспективным иммуногеном для защиты, но достаточно ли для того, чтобы ориентироваться на полноценный белок или только рецептор-связывающую область, чтобы предотвратить передачу инфекции. Другие соображения включают потенциальную продолжительность иммунитета и, таким образом, количество доз вакцин, необходимых для обеспечения иммунитета. В настоящее время тестируется более десятка вакцин SARS-CoV-2.
Другие подходы к профилактике, вероятно, появятся в ближайшие месяцы, в том числе моноклональные антитела, гипериммунный глобулин, и титр у выздоровших. Если эти подходы окажутся эффективными, они могут быть использованы для лиц с высоким риском, включая работников здравоохранения, других основных работников и пожилых людей (особенно в домах престарелых или учреждениях долгосрочного ухода).
Ограничения
Этот обзор имеет ряд ограничений. Во-первых, информация о SARS CoV-2 ограничена. Во-вторых, представленная здесь информация основана на имеющихся данных, но может быть изменена по мере поступления дополнительной информации. В-третьих, было опубликовано несколько рандомизированных исследований для руководства COVID-19.
Выводы
По состоянию на 1 июля 2020 года более 10 миллионов человек во всем мире были инфицированы SARS-CoV-2. Многие аспекты передачи, инфекции и лечения остаются неясными. Достижения в области профилактики и эффективного управления КОВИД-19 потребуют проведения фундаментальных и клинических исследований, а также мероприятий в области общественного здравоохранения и клинических мероприятий.
Информация о статье
Принято к публикации: 30 июня 2020 года.
Для связи: W. Joost Wiersinga, MD, PhD, Division of Infectious Diseases, Department of Medicine, Amsterdam UMC, location AMC, Meibergdreef 9, 1105 AZ Amsterdam, the Netherlands (w.j.wiersinga@amsterdamumc.nl).
Опубликовано: 10 июля 2020 года. doi:10.1001/jama.2020.12839 JAMA
https://jamanetwork.com/journals/jama/fullarticle/2768391
Комментарии к рисункам
Текущее понимание тяжелого острого респираторного синдрома коронавируса 2 (SARS-CoV-2) – индуцированный иммунный ответ хозяина. SARS-CoV-2 мигирует клетки через вирусный структурный шип (S) белок, который связывается с ангиотензин-преобразующим ферментом 2 (ACE2). Протеазы серина типа 2 трансмембрана серина протеи (TMPRSS2) в клетке-хозяине также способствует вирусному поглощению путем расщепления ACE2 и активации белка SARS-CoV-2 S. На ранней стадии количество вирусных копий могут быть высокими в нижние дыхательные пути. Воспалительные сигнальные молекулы высвобождаются инфицированными клетками и альвеолярными макрофагами в дополнение к набранным Т-лимфоцитам, моноцитам и нейтрофилом. На поздней стадии отек легких может заполнить альвеолярные пространства образованием гиалиновых мембран, совместимых с ранним фазовым острым респираторным дистресс-синдромом.
A, Поперечное тонкосековое компьютерное томографическое сканирование 76-летнего мужчины, через 5 дней после появления симптомов, показывая субплеральную непрозрачность матовых стекол и консолидацию с субплеуральной плеврой.
B, Поперечное тонко секционное компьютерное томографическое сканирование 76-летнего мужчины, через 21 день после появления симптомов, показывающее двустороннюю и периферийную преобладающую консолидацию, матовое стекло ретикуляцию и бронходилятацию.
C, Патологические проявления легочной ткани у пациента с тяжелой пневмонией, вызванной тяжелым острым коронавирусом острого респираторного синдрома 2 (SARS-CoV-2), показывающие интерстициальные моноядерные воспалительные инфильтрации, в которых доминируют лимфоциты (увеличение, No10).
D, Патологические проявления легочной ткани у пациента с тяжелой пневмонией, вызванной SARS-CoV-2 с диффузным альвеолярным повреждением с отеком и фибрином осаждения, что указывает на острый респираторный дистресс-синдром с ранним фиброзом (увеличение, No10).
Авторы
Joost Wiersinga, MD, PhD1,2; Andrew Rhodes, MD, PhD3; Allen C. Cheng, MD, PhD4,5; Sharon J. Peacock, PhD6,7; Hallie C. Prescott, MD, MSc8,9
Медицинские учреждения
1Division of Infectious Diseases, Department of Medicine, Amsterdam UMC, location AMC, University of Amsterdam, Amsterdam, the Netherlands
2Center for Experimental and Molecular Medicine (CEMM), Amsterdam UMC, location AMC, University of Amsterdam, Amsterdam, the Netherlands
3Department of Intensive Care Medicine, St George’s University Hospitals Foundation Trust, London, United Kingdom
4Infection Prevention and Healthcare Epidemiology Unit, Alfred Health, Melbourne, Australia
5School of Public Health and Preventive Medicine, Monash University, Monash University, Melbourne, Australia
6National Infection Service, Public Health England, London, United Kingdom
7Department of Medicine, University of Cambridge, Addenbrooke’s Hospital, Cambridge, United Kingdom
8Division of Pulmonary and Critical Care Medicine, University of Michigan, Ann Arbor
9VA Center for Clinical Management Research, Ann Arbor, Michigan


