Сологуб Елена Николаевна, кандидат биологических наук.
Глава 3. Общая вирусология
Вирусы – (лат.virus – яд) не имеют клеточного строения. Вирусы – внутриклеточные паразиты, вне клетки не проявляют свойств живого. Они не потребляют пищи, не вырабатывают энергии, не растут, у них нет обмена веществ. От неживой материи вирусы отличаются способностью воспроизводить себе подобные формы, и обладают наследственностью и изменчивостью.
Вирусы существуют в двух качественно разных формах: внеклеточной
– вирион и внутриклеточной –
вирус.
3.1.Морфология, химический состав вирусов
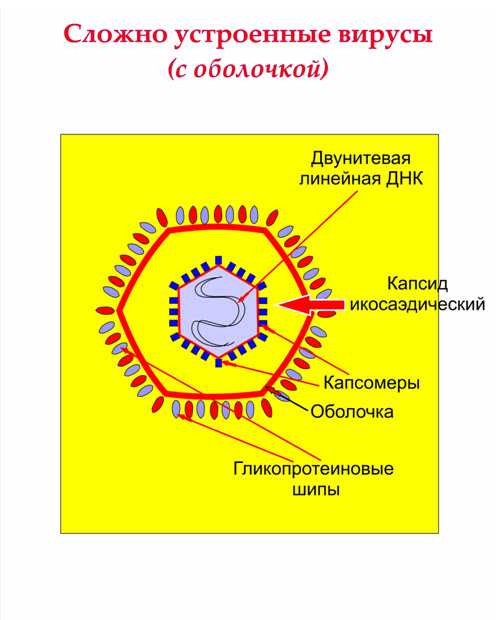
Просто организованные вирусы представляют собой нуклеопротеиды (нуклеокапсиды) и состоят из нуклеиновой кислоты (
ДНК или РНК) и белков, формирующих оболочку вируса –
капсид.Пикорнавирусы и парвовирусы относят к просто устроенным.
Сложные вирусы содержат дополнительные оболочки (белковые или липопротеидные) и имеют сложный химический состав.
Рис4. Просто устроенные вирусы (без оболочки)
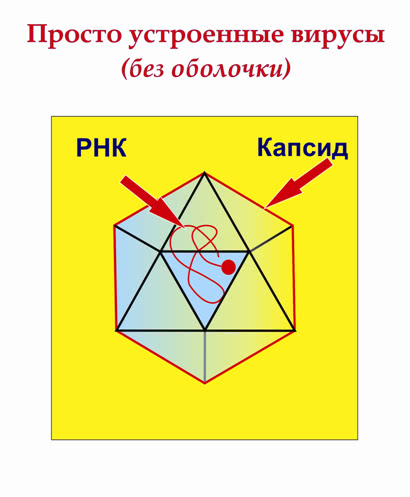 Рис. 5. Сложно устроенные вирусы (с оболочкой)
Рис. 5. Сложно устроенные вирусы (с оболочкой)
Морфологической субъединицей
капсида является
капсомер. Белковые субъединицы вируса могут содержать одну или несколько молекул. Существует два типа строения капсидов вирионов: 1.Капсомеры ассоциированы с геномом и образуют спиралевидную (винтовую) структуру, такой тип симметрии называют
спиральным. Его имеют вирус табачной мозаики, парамиксовирусы, ортомиксовирусы; 2.Капсомеры образуют полое изометрическое тело, в центре которого находится геном; такой тип укладки
называют кубический. Тело таких вирусов симметрическое в трех взаимно перпендикулярных направлениях; вирус полиомиелита представляет икосаэдр и состоит из 60 капсомеров. Отсутствие постоянной симметрии характерно для вирусов больших размеров, например бактериофагов.
Нуклеиновые кислоты. Клетки всех живых организмов содержат два вида нуклеиновой кислоты – ДНК и РНК. ДНК представляет собой двунитчатую молекулу, а РНК – однонитчатую. РНК представлена тремя классами молекул: иРНК, рРНК, тРНК. В отличие от клеток, вирусы содержат только один вид нуклеиновой кислоты – либо РНК, либо ДНК.И та и другая выполняют функцию генома. Вирусные НК характеризуются поразительным разнообразием форм. Вирусный геном может быть представлен как однонитчатыми, так и двунитчатыми молекулами РНК и ДНК. ДНК может быть линейной и кольцевой, а РНК – непрерывной, фрагментированной, кольцевой.
Рис6. Типы молекул вирусных ДНК и РНК
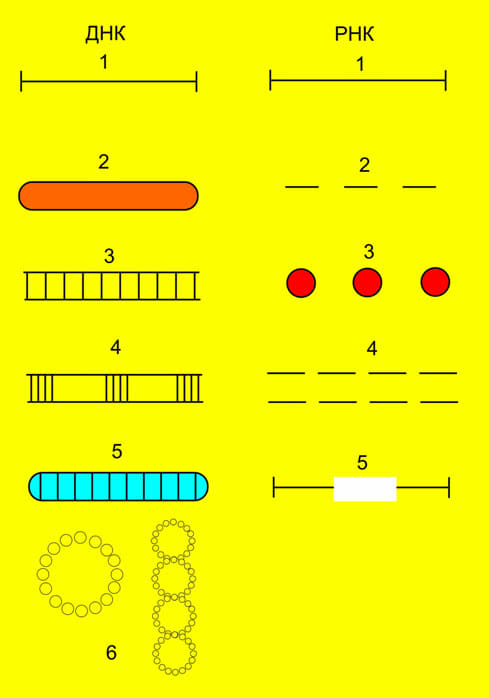
ДНК: 1-парвовирусы, 2-фаг Х174, 3- аденовирусы, 4- фаг Т5, 6- паповирусы, 7- вирус гепатита В; РНК: 1- пикорнавирусы, тогавирусы, парамиксовирусы, рабдовирусы, 2- ортомиксовирусы, 3- буньявирусы, 4- реовирусы, 5- ретровирусы.
Белки. В зараженной клетке вирусный геном кодирует синтез
структурных и неструктурных белков. Структурные белки нужны вирусным частицам потомства, неструктурные обслуживают процесс внутриклеточной репродукции вируса. Структурные белки бывают капсидные и суперкапсидные.
Белки просто и сложно устроенных вирусов Таблица 8.
| Белки просто устроенных вирусов |
| Структурные
|
Неструктурные
- предшественники структурных
- полимеразы
- ферменты, модифицирующие белки
- функции не идентифицированы
|
| Белки сложно устроенных вирусов |
| структурные |
неструктурные |
В составе капсида
- капсидные
- геномные
- полимеразы
|
В составе суперкапсида
- прикрепительные
- белки слияния
- ферменты, модифицирующие белки
- предшественники структурных
- полимеразы
- регуляторы синтеза РНК, ДНК
- функции не идентифицированы
|
|
|
|
|
Липиды обнаружены у сложно организованных вирусов, входят в состав суперкапсидов.
Углеводы. Гликопротеиды вирусов включают углеводный компонент, который определяется, подобно липидам, клеткой-хозяином.
Ферменты вирусов подразделяют на вирионные и вирусиндуцированные. Вирионные – это ферменты транскрипции и репликации (ДНК и РНК-полимеразы). Обнаружены у многих вирусов: обратная транскриптаза ретровирусов, эндонуклеаза и экзонуклуаза, нейраминидаза, АТФ-аза и др. Структура вирусиндуцированных ферментов закодирована в вирусном геноме, это относится к РНК-полимеразе пикорна-, орто-, парамиксовирусам, ДНК-полимеразе герпес и поксвирусов.
3.2.Устойчивость вирусов к окружающей среде
Устойчивость вирусов к воздействию факторов внешней среды неодинакова. Менее устойчивы вирусы с липопротеидными оболочками, наиболее устойчивы – изометрические вирусы. Так, ортомиксовирусы и парамиксовирусы инактивируются на поверхностях в течение нескольких часов, тогда как вирус полиомиелита, аденовирусы и реовирусы сохраняют инфицирующую активность в течение нескольких дней.Однако, есть исключения: вирус гепатита В сохраняет свою активность в сыворотке даже при кратковременном кипячении, вирус оспы устойчив к высыханию и сохраняется в экстрактах в течение многих месяцев. Вирусы, имеющие липопротениновую оболочку, чувствительны к эфиру, хлороформу, детергентам; просто устроенные вирусы устойчивы к их действию.
3.3. Классификация вирусов
Современная классификация вирусов является универсальной для вирусов простейших, беспозвоночных, позвоночных, растений. В основу класификации положены следующие основные критерии:
- Тип нуклеиновой кислоты (ДНК или РНК)
- Наличие липопротеидной оболочки
- Вирусный геном
- Размер, морфология вириона, тип симметрии, число капсомеров
- Генетические взаимодействия
- Восприимчивые хозяева
- Патогенность
- Географическое распространение
- Способ передачи
- Антигенная характеристика.
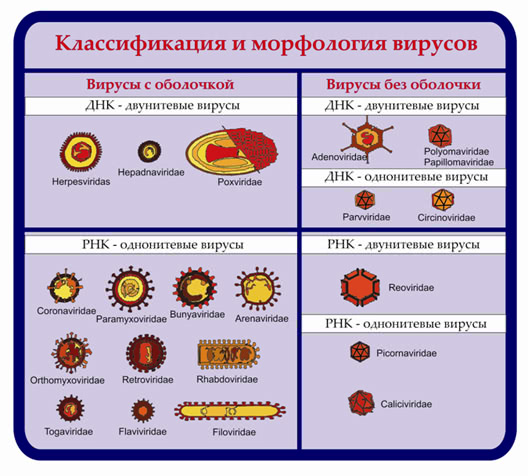
На основании перечисленныех признаков вирусы делятся на семейства, подсемейства, роды, типы. Современная классификация вирусов человека и дивотных охватывает более 4/5 всех известных вирусов, которые распределены в 19 семейств, из них 7 – ДНК-содержащие вирусы. Для наименования вирусов существуют следующие правила: название семейств оканчивается на «viridae», подсемейства на «virinae», рода – «virus».
Рис.7. Классификация и морфология вирусов
 3.4. Морфогенез вирусов
3.4. Морфогенез вирусов
Репродукция вирусов включает две следующие друг за другом фазы. Первая фаза заключается в адсорбции и проникновении вируса в клетку, модификации вируса до способности вызвать инфекцию. Три стадии первой фазы:
- Адсорбция вируса на клетках
- Проникновение в клетки
- Раздевание вируса в клетке.
Эти стадии направлены на то, чтобы вирус был доставлен в соответствующие клеточные структуры, и его внутренний компонент был освобожден от защитных оболочек. Как только эта цель достигнута, начинается вторая фаза репродукции, в течение которой происходит экспрессия вирусного генома. Эта фаза включает в себя стадии:
- Транскрипции
- Трансляции информационной РНК
- Репликации генома
- Сборки вирусных частиц.
Выход вирусных частиц из клетки происходит путем «взрыва» или почкования. Взрыв связан с деструкцией клетки, а при почковании клетка может длительное время сохранять жизнеспособность и продуцировать вирусное потомство, пока не произойдет полное ее истощение.
Таким образом., проникнув в клетку, вирус изменяет в ней обмен веществ, направляет всю ее деятельность на производство вирусной НК и вирусных белков. Внутри клетки-хозяина происходит самостоятельная сборка вирусных частиц из синтезированных молекул НК и белков. В конечном итоге клетка гибнет, и вирусы выходят из клетки-хозяина.
3.5.Генетика вирусов
Вирусы являются излюбленным объектом молекулярной генетики благодаря простому строению и малой молекулярной массе геномов. Число генов у вирусов варьирует. Геном вирусов животных гаплоиден, за исключением ретровирусов – у них он диплоиден, представлен двумя идентичными молекулами ДНК. Геном вирусов имеет мозаичную структуру, представлен чередованием информативных и неинформативных последовательностей.
Некоторые вирусные иРНК могут направлять синтез двух белков.
У многих вирусов масса синтезирующихся белков превышает теоретически рассчитанную. Этот феномен объясняется наличием у вирусов специальных механизмов получения генетической информации при максимальной экономии генетического материала. Способами увеличения генетической информации являются:
- двукратное считывание одной и той же иРНК, но с другого иницирующего кодона
- сдвиг рамки трансляции
- сплайсинг
- транскрипция с перекрывающихся частей ДНК и др.
Основные процессы, контролирующие наследственность и изменчивость вирусов:
1. Модификации. Модификациями называют фенотипические (ненаследуемые) изменения у вирусов, обусловленные клеткой-хозяином. Они лежат в основе адаптации вируса к новому хозяину.
2. Мутации. В основе изменчивости вирусов лежат мутации – изменения состава и последовательности нуклеотидов вирусного генома, приводят к появлению новых свойств. Мутации происходят у всех вирусов, могут быть летальными, условно-летальными, не изменять жизнеспособности вирусов. Прямые мутации меняют фенотип, а обратные (реверсии) восстанавливают фенотип вируса. Мутации вирусов носят случайный характер
3.6. Взаимодействие между вирусами
При смешанных вирусных инфекциях (заражение несколькими вирусами) имеют место различные формы взаимодействия вирусов. При взаимодействии вирусных генов возможна:
1.
Множественная реактивация. Заключается в том, что вирионы с поражением разных генов кооперируются, между ними происходит генетическая рекомбинация, в результате репродуцируется исходный неповрежденный вирус, который способен вызвать инфекцию.
2. Рекомбинация – обмен генетическим материалом между родительскими формами вирусов, при этом появляется вирусное потомство со свойствами родителей.
3.
Пересортировка генов. Это вариант рекомбинации, происходит между вирусами с сегментированным геномом.
4.
Перекрестная реактивация – кросс реактивация, происходит при скрещивании вируса с поврежденным геномом и интактным. При смешанной инфекции такими вирусами возможна рекомбинация участков генома с появлением вирусного штамма, обладающего признаками обоих родителей.
5
.Гетерозиготность – при совместном культивировании двух штаммов вируса может происходить формирование вирионов, содержащих полностью или частично геном второго вируса.
6.
Комплементация – дополнение, партнеры стимулируют репродукцию друг друга.
7.
Фенотипическое смешивание происходит при совместном культивировании двух вирусов, при этом геном одного вируса бывает заключен в капсид другого вируса полностью или частично.
3.7. Методы культивирования вирусов
Для культивирования вирусов используют культуры клеток, куриные эмбрионы и чувствительных лабораторных животных. Эти же методы применимы и для культивирования риккетсий, хламидий – внутриклеточных бактерий, которые не растут на искусственных питательных средах. Культуры клеток представляют собой соматические или эмбриональные клетки животных или человека, культивируемых в лабораторных условиях. Клеточные культуры отличаются по источнику получения, способности к размножению in vitro и кариотипу. Их подразделяют на первичные, полуперевиваемые и перевиваемые. Первичные (неперевиваемые) культуры не способны размножаться in vitro, используются однократно. Полуперевиваемые культуры клеток представляют собой диплоидные клетки человека способные выдержать 50 пассажей. Перевиваемые культуры злокачественных или нормальных клеток длительно размножаются in vitro, сохраняются длительно. О репродукции вирусов в культуре клеток судят по их цитопатическому действию (ЦПД), учет проводят микроскопически.
3.8.Бактериофаги (вирусы бактерий)
Бактериофаги – инфекционные агенты, лизирующие бактерии.
Структура. Форма бактериофагов сперматозоидная. Состоят из головки, в ней находится нуклеиновая кислота, и отростка.
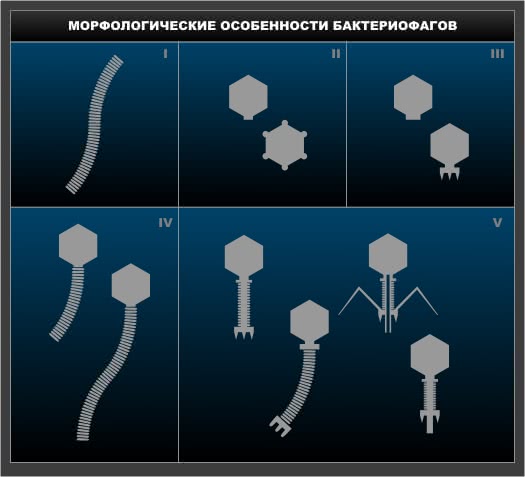
Морфологическая классификация бактериофагов:
1 тип – нитевидные ДНК-содержащие фаги, лизируют бактерии, имеющие F-плазмиды;
2 тип – фаги с аналогом отростка, мелкие РНК-содержащие фаги;
3 тип – фаги с коротким отростком (Т3,Т7);
4 тип – фаги с несокращающимся чехлом отростка и двунитевой ДНК (Т1,Т5 и др.);
5 тип – ДНК-содержащие фаги с сокращающимся чехлом отростка, заканчивающимся базальной пластинкой (Т2, Т4, Т6).
Т-фаги (типовые) наиболее изучены. Самая сложная структура у Т2.Он состоит из головки гексагональной формы и отростка, который образован полым стержнем. Снаружи стержень покрыт сокращающимся чехлом. На дистальном конце имеется базальная пластинка, в углах которой располагаются зубцы. От зубцов отходят нити. Нити и базальная пластинка осуществляют адсорбцию фага на бактериальной клетке.
Химический состав. Нуклеиновые кислоты, белок. Большинство фагов содержат ДНК. Могут содержать необычные азотистые основания, лизоцим.
Антигены. Бактериофаги могут содержать типоспецифические и группоспецифические антигены, при парентеральном введении на которые образуются антитела.
Резистентность. Фаги достаточно устойчивы к факторам внешней среды. Инактивируются при температуре +65-70 оС, хорошо переносят замораживание, длительно сохраняются при низких температурах и высушивании. Чувствительны к 1% раствору формалина.
3.8.1.Взаимодействие с бактериальной клеткой
Стадии взаимодействия:
- А. Адсорбция. Произойдет при условии соответствия рецепторов клетки и рецепторов бактериофага. На бактериях без клеточной стенки (протопласты) фаги не адсорбируются.
- Б. Проникновение осуществляется инъекцией нуклеиновой кислоты фага через канал отростка.
В. Репликация фаговой НК и синтез фагоспецифических ферментов транскрипции и репликации идентичен вирусам.
Г.Выход зрелых фагов из клетки происходит путем «взрыва» при последующем лизисе бактерий, возможно также проникновением через ЦПМ бактерий без повреждения стенки.
Рис.8.Морфологические особенности бактериофагов
 Лизогения. Вирулентные фаги вызывают гибель (лизис) бактериальной клетки. Умеренные фаги при взаимодействии с клеткой хозяина встраивают свою НК в бактериалъный геном. Профаг – неинфекционная форма, состояние ассоциации фаговой НК с геномом хозяина.
Бактериальная клетка, содержащая профаг, называется лизогенной, а явление – лизогенией. При облучении УФ лучами лизогенных бактерий продукция фага увеличивается, феномен этот называется индукцией профага и применяется для определения дозы радиации на космических кораблях.
Лизогенная конверсия заключается в приобретении лизогенными бактериями определенных признаков (способности продуцировать токсины, изменять антигенные свойства и т.п.). Дефектные умеренные фаги не способны к образованию зрелых фаговых частиц, что используется в генной инженерии.
Практическое применение бактериофагов. Бактериофаги используют для типирования бактерий и индикации (выявлении) в окружающей среде, для лечения и профилактики инфекционных заболеваний (редко). Метод фаготипирования бактерий с целью определения фаготипа широко применяется в микробиологической практике, что позволяет установить источник инфекции и пути ее передачи.
Рис.9.Развитие умеренного фага
Лизогения. Вирулентные фаги вызывают гибель (лизис) бактериальной клетки. Умеренные фаги при взаимодействии с клеткой хозяина встраивают свою НК в бактериалъный геном. Профаг – неинфекционная форма, состояние ассоциации фаговой НК с геномом хозяина.
Бактериальная клетка, содержащая профаг, называется лизогенной, а явление – лизогенией. При облучении УФ лучами лизогенных бактерий продукция фага увеличивается, феномен этот называется индукцией профага и применяется для определения дозы радиации на космических кораблях.
Лизогенная конверсия заключается в приобретении лизогенными бактериями определенных признаков (способности продуцировать токсины, изменять антигенные свойства и т.п.). Дефектные умеренные фаги не способны к образованию зрелых фаговых частиц, что используется в генной инженерии.
Практическое применение бактериофагов. Бактериофаги используют для типирования бактерий и индикации (выявлении) в окружающей среде, для лечения и профилактики инфекционных заболеваний (редко). Метод фаготипирования бактерий с целью определения фаготипа широко применяется в микробиологической практике, что позволяет установить источник инфекции и пути ее передачи.
Рис.9.Развитие умеренного фага
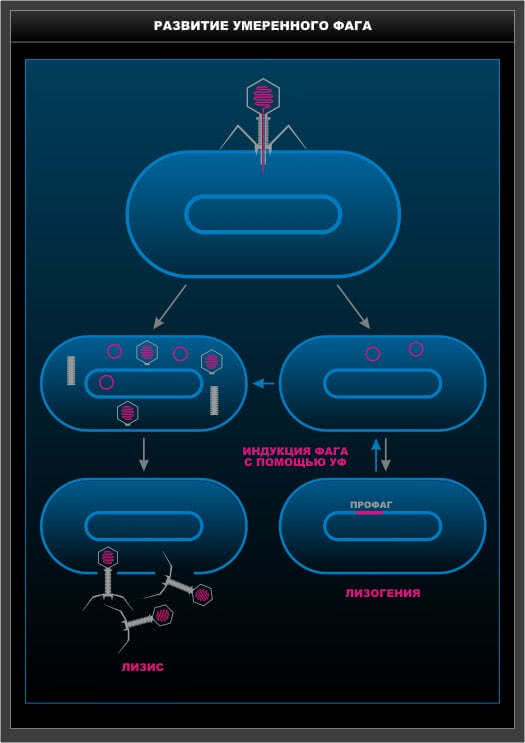 Рис.10. Взаимодействие бактериофага с оболочкой бактерий
Рис.10. Взаимодействие бактериофага с оболочкой бактерий
 3.9. Прионы
Прионы – белковая инфекционная единица. Состоят из белковых молекул определенной структуры. Отличаются устойчивостью к высоким температурам, ионизирующей радиации, излучению и другим экстремальным воздействиям. Они чувствительны к фенолу и детергентам при нагревании. Могут персистировать в организме человека длительное время, не вызывая иммунного ответа. Накопление прионов в клетке приводит к гибели последней. Прионный белок существует в двух формах – нормальной и патологической. В первом случае это естественный компонент клеток здорового организма, участвует в передаче нервного импульса, в поддержании циркадных ритмов, в механизмах старения мозга и нервной системы. Патологическая форма вызывает медленные инфекции человека.
3.10. Патогенез вирусных инфекций
3.10.1. Взаимодействие вируса с клеткой.
В основе взаимодействия вирусов с организмом всегда лежит инфекционный процесс на уровне клетки, который реализуется путем взаимодействия вирусного и клеточного геномов. Это позволяет классифицировать инфекции на клеточном и на организменных уровнях.
Схема 2. Классификация вирусных инфекций
3.9. Прионы
Прионы – белковая инфекционная единица. Состоят из белковых молекул определенной структуры. Отличаются устойчивостью к высоким температурам, ионизирующей радиации, излучению и другим экстремальным воздействиям. Они чувствительны к фенолу и детергентам при нагревании. Могут персистировать в организме человека длительное время, не вызывая иммунного ответа. Накопление прионов в клетке приводит к гибели последней. Прионный белок существует в двух формах – нормальной и патологической. В первом случае это естественный компонент клеток здорового организма, участвует в передаче нервного импульса, в поддержании циркадных ритмов, в механизмах старения мозга и нервной системы. Патологическая форма вызывает медленные инфекции человека.
3.10. Патогенез вирусных инфекций
3.10.1. Взаимодействие вируса с клеткой.
В основе взаимодействия вирусов с организмом всегда лежит инфекционный процесс на уровне клетки, который реализуется путем взаимодействия вирусного и клеточного геномов. Это позволяет классифицировать инфекции на клеточном и на организменных уровнях.
Схема 2. Классификация вирусных инфекций
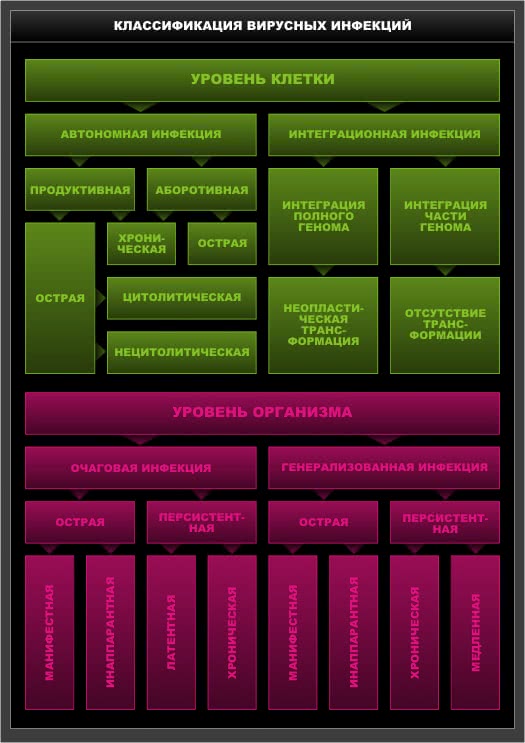 3.10.2.Классификация вирусных инфекций на клеточном уровне.
При автономной вирусной инфекции геном вируса реплицируется независимо, но взаимодействие между геномами вируса и клетки сохраняется. Автономная вирусная инфекция характерна для большинства животных.
При интегрированной инфекции вирусный геном включается в состав клеточного генома, реплицируется вместе с ним как составная часть клеточного генома. Интегрировать могут как полный геном, так и часть его: при гепатите В происходит интеграция полного генома, при аденовирусных и герпетических инфекциях обычно интегрирует часть генома, при инфекциях онковирусами может быть двояко. Интеграция может привести к неопластической трансформации клетки – способности неограниченно делиться.
Общепринят следующий механизм интеграции. Вирусная ДНК должна быть кольцевой формы и двунитчатой. Эта молекула прикрепляется к клеточной ДНК, места прикрепления разрезаются и вновь сшиваются.
Инфекция может быть продуктивной и абортивной. Продуктивная инфекция завершается образованием инфекционного потомства. Абортивная инфекция не завершается образованием инфекционных вирусных частиц или они образуются в меньшем количестве. Может возникнуть путем:
3.10.2.Классификация вирусных инфекций на клеточном уровне.
При автономной вирусной инфекции геном вируса реплицируется независимо, но взаимодействие между геномами вируса и клетки сохраняется. Автономная вирусная инфекция характерна для большинства животных.
При интегрированной инфекции вирусный геном включается в состав клеточного генома, реплицируется вместе с ним как составная часть клеточного генома. Интегрировать могут как полный геном, так и часть его: при гепатите В происходит интеграция полного генома, при аденовирусных и герпетических инфекциях обычно интегрирует часть генома, при инфекциях онковирусами может быть двояко. Интеграция может привести к неопластической трансформации клетки – способности неограниченно делиться.
Общепринят следующий механизм интеграции. Вирусная ДНК должна быть кольцевой формы и двунитчатой. Эта молекула прикрепляется к клеточной ДНК, места прикрепления разрезаются и вновь сшиваются.
Инфекция может быть продуктивной и абортивной. Продуктивная инфекция завершается образованием инфекционного потомства. Абортивная инфекция не завершается образованием инфекционных вирусных частиц или они образуются в меньшем количестве. Может возникнуть путем:
- заражения чувствительных клеток дефектным вирусом
- заражения чувствительных клеток в неразрешаюших условиях
- заражения нечувствительных клеток стандартным вирусом.
Дефектным называют вирус, который не способен давать инфекционное потомство.
Продуктивные и абортивные инфекции могут протекать остро и хронически. Острой называют такую форму инфекции, при которой после образования вирусного потомства клетка либо погибает, либо выздоравливает и не содержит вирусных компонентов. Хроническая инфекция характеризуется тем, что клетки продолжают продуцировать вирусные частицы или вирусные компоненты длительное время и передают это свойство дочерней популяции. Чаще хроническую форму приобретает абортивная инфекция.
В зависимости от судьбы зараженной клетки инфекция может быть:
– цитолитическая – завершается гибелью клетки
– нецитолитическая – не приводит к гибели клетки, клетка некоторое время функционирует, продуцирует вирусные частицы.
Смешанная инфекция – клетки заражаются несколькими разными вирусами. Происходит одновременно два и более инфекционных процесса в клетке, которые оказывают различное влияние друг на друга. Варианты взаимодействия вирусов:
А) один из вирусов подавляет репродукцию другого или подавляется репродукция обоих вирусов. Это называется интерференцией вирусов.
- Б) один вирус усиливает репродукцию второго в результате комплементации или экзольтации.
- В) не влияя на репродукцию, нарушают морфогенез обоих вирусов.
Персистирующая инфекция – в клетке сохраняются стабильные обменные и синтетические процессы, и поддерживается репродукция возбудителя. При латентной инфекции дочерние популяции возбудителя образуются спорадически. Иннапарантные инфекции сопровождаются бессимптомной циркуляцией незначительного количества возбудителя в отдельных органах при большей вероятности клинических проявлений.
-
3.10.3. Цитопатология заражения вирусом клетки
Патологические изменения зараженных вирусами клеток обусловлены специфическими и неспецифическими процессами. К неспецифическим относят изменения проницаемости мембран, маргинация хроматина, хромосомные аберрации, пикноз ядер, вакуолизация цитоплазмы. Специфическими изменениями являются вирусные включения, образования симпластов.
Включения являются специфическим морфологическим признаком вирусной инфекции, имеют диагностическое значение. Выявляются вирусные включения в ядре или цитоплазме. Чаще всего это место размножения вируса или скопления вирусных частиц. Характерные ядерные включения образуют вирусы герпеса, полиомиелита, аденовирусы. Цитоплазматические включения формируются в клетках, зараженных вирусом оспы, гриппа, бешенства.
Рис. 11. Типы вирусных включений
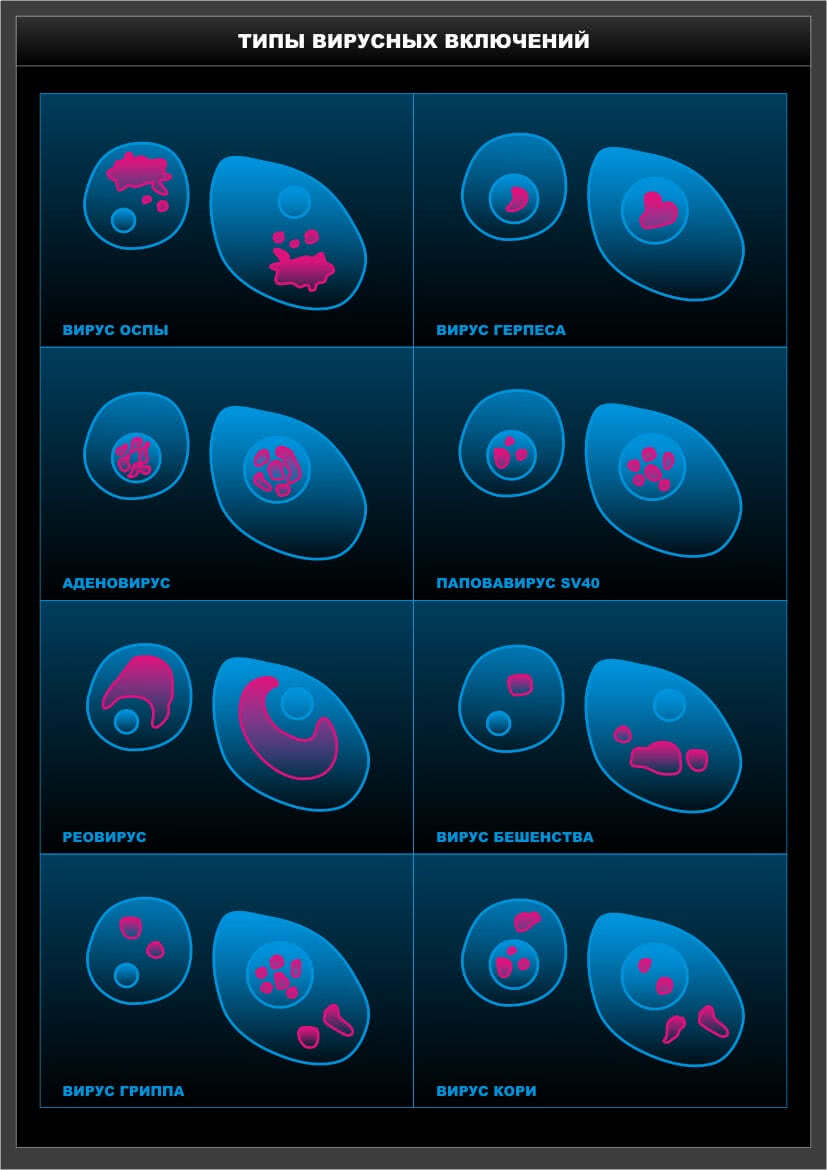 Некоторые вирусы вызывают характерный цитопатический эффект, проявляющийся в слиянии клеток и образовании многоядерных клеток – симпластов (синцитий). Такими свойствами обладают парамиксовирусы, некоторые ретровирусы, вирусы герпеса.
3.10.4. Классификация вирусных инфекций на организменном уровне
В основу классификации положены:
Некоторые вирусы вызывают характерный цитопатический эффект, проявляющийся в слиянии клеток и образовании многоядерных клеток – симпластов (синцитий). Такими свойствами обладают парамиксовирусы, некоторые ретровирусы, вирусы герпеса.
3.10.4. Классификация вирусных инфекций на организменном уровне
В основу классификации положены:
- генерализация вируса
- продолжительность инфекции
- проявление клинических симптомов
- выделение в окружающую среду.
Очаговая инфекция – действие вируса проявляется у входных ворот инфекции с его локальной репродукцией.
Генерализованная инфекция – после ограниченного периода репродукции вируса в первичных очагах происходит генерализация процесса, вирус достигает чувствительных тканей, формируя вторичные очаги инфекции.
Примером очаговых инфекций являются респираторные и кишечные вирусные инфекции, генерализованных – оспа, корь, полиомиелит.
Острая инфекция длится относительно непродолжительный период времени с выделением вируса в окружающую среду. Окончание инфекции сопровождается элиминацией вирусов благодаря иммунным механизмам. Инфекция протекает в клинической и инаппарантной форме. Острая инфекция может завершаться выздоровлением или гибелью организма. Она соответствует продуктивной инфекции на уровне клетки.
Таблица 9. Сравнительная характеристика очаговых и генерализованных вирусных инфекций
| Свойства инфекции |
Очаговые инфекции |
Генерализованные инфекции |
|
| Место патологического процесса |
Входные ворота |
Системы тканей и органов |
|
| Инкубационный период |
Относительно короткий |
Относительно длинный
|
|
| Наличие вирусемии |
Редко |
Обычно |
|
| Продолжительность иммунитета |
Кратковременный или неизученный |
Обычно длительный
|
|
| Иммунные механизмы |
Секреторные антитела(Ig A),
Локальный клеточный иммунитет |
Гуморальные антитела(IgG, IgM) системный клеточный иммунитет |
|
3.10.5.Особенности патогенеза вирусных инфекций
Под патогенезом следует понимать совокупность процессов, вызывающих заболевание и определяющих его развитие и исход.Определяется следующими факторами:
- тропизмом вируса
- скоростью репродукции вируса и количеством инфекционных частиц в потомстве
- реакцией клетки на инфекцию
- реакцией организма на вызванные инфекцией изменения клеток и тканей.
Пути проникновения вирусов в организм:
- Горизонтальная передача возбудителя осуществляется от человека к человеку. Наиболее распространены механизмы:
- а) воздушно-капельный. Таким путем в организм попадают две группы вирусов – респираторные, которые репродуцируются в эпителии слизистых оболочек дыхательных путей, вызывают местную инфекцию (редко – генерализованную) и выводятся из организма; и вирусы, для которых дыхательные пути являются входными воротами инфекции, они обусловливают генерализацию процесса (вирус натуральной оспы, вирусы ветряной оспы, кори, свинки).
- б) фекально-оральный (пищевой) механизм значим для энтеровирусов семейств Picornaviridae, Reoviridae, Caliciviridae.
- в) трансмиссивный. Вирус проникает в организм при укусе кровососущего насекомого (арбовирусы, некоторые рабдовирусы).
- г) через кожу. Некоторые вирусы проникают в организм через поврежденную или неповрежденную кожу (вирус бешенства, коровьей оспы, папилломы).
- д) парентеральный (инъекционная передача). Путь проникновения ВИЧ,ЦМВ, вируса гепатита В – заражение происходит при всякого рода парентеральных манипуляциях – хирургических вмешательствах, переливании крови, стоматологических операциях, применении инфицированных трансплантатов роговицы, маникюре, педикюре и т.п.
- е) половой. Таким путем проникают вирусы герпеса, бородавок человека (паповавирусы).
- 2. Вертикальная передача возбудителя (от матери плоду). Трансплацентарно передаются ВИЧ,ЦМВ, вирусы герпеса, краснухи, гепатита В, возбудители хронических аденовирусных инфекций, редко – гриппа. Перинально заражается плод при прохождении через инфицированные родовые пути. Заражение ВИЧ возможно при лактации.
-
3.11. Лабораторная диагностика вирусных инфекций
- Лабораторная диагностика вирусных инфекций складывается из трех направлений:
- Обнаружение возбудителя или его компонентов непосредственно в клиническом материале (быстрая диагностика).
- Выделение вируса из клинического материала и его идентификация.
- Серодиагностика вирусных инфекций.
Методы лабораторной диагностики вирусных инфекций основаны на использовании биологических свойств вирусов. Выбор метода определяется характером заболевания и предполагаемым возбудителем, и решается в каждом отдельном случае в зависимости от периода болезни и условий протекания.
- Глава 4. Генетика микроорганизмов
- Уникальные свойства микроорганизмов – гаплоидность, высокая скорость размножения, половая дифференциация (доноры и реципиенты), наличие обособленных фрагментов ДНК позволяют ученым изучать общие генетические закономерности, а современные методы генной инженерии положены в основу биотехнологии производства вакцин, интерферона, гормонов и других биологически активных веществ.
4.1.Организация генетического материала бактерий
Вся генетическая информация закодирована в ДНК. Исключение составляют РНК-содержащие вирусы – у них генетическая информация заложена в РНК.
Нуклеоид бактерий представлен кольцевой ДНК, часто замкнутой. Дополнительно генетический материал заложен у бактерий во внехромосомных генетических элементах – плазмидах, находящихся в автономном состоянии в цитоплазме клетки. Приняты условные обозначения генов бактерий, например:his+– гистидиновый ген, leu++ – лейциновый ген, strR– ген резистентности к стрептомицину.
Ген – участок молекулы ДНК, детерминирующий порядок аминокислот в определенном полипептиде или нуклеотидов в РНК (В.Иогансон,1909).Ген – единица наследственности, определяющая развитие какого-либо признака организма. Ген дискретен, стабилен, лабилен, специфичен. Ген способен отвечать за несколько признаков (плейотропен).
Генотип – совокупность генов организма. Экспрессия генов – проявление их, степень выраженности, зависит от условий окружающей среды.
Фенотип- совокупность всех признаков и свойств организма, развивающихся под действием генотипа и факторов среды.
4.2. Внехромосомные факторы наследственности
Плазмиды, транспозоны, Is–последовательности относят к внехромосомным факторам наследственности. Представляют собой молекулы ДНК, отличающиеся молекулярной массой, объемом закодированной в них информации, способностью к репликации и т.п. Внехромосомные факторы наследственнности не являются жизненно необходимыми бактериальной клетке, они способны дополнять бактерии новыми свойствами, например резистентностью к антибиотикам. Плазмиды автономны, или могут быть интегрированы с хромосомой бактерии, а транспозоны и Is –последовательности всегда связаны с хромосомой.
4.2.1.Плазмиды
Функции плазмид – регуляторная и кодирующая. Регуляторная функция обеспечивает компенсацию нарушений метаболизма ДНК клетки хозяина. Кодирующая функция заключается во внесении в клетку новой информации (R- плазмиды,F- плазмиды, Col–плазмиды). Нахождение плазмид в автономном или интегрированном состоянии часто определяют факторы внешней среды. В настоящее время описано более 20 плазмид. F- плазмиды, или половой фактор, представляют замкнутую нить ДНК с молекулярной массой 60х106, контролируют синтез половых ворсинок (sex или F-pili). F- плазмиды активно участвуют в конъюгации (половом процессе бактерий), передаются при этом в клетку бактерии-реципиента.Tran-оперон F- плазмид детерминирует перенос генетического материала, легко удаляется из клеток в результате химической обработки при автономном способе существования в клетке.
R– плазмиды определяют устойчивость бактерий к лекарственным препаратам. В их состав входит r-ген, который соответственно содержит более мелкие элементы: Is– последовательности, транспозоны, tra – опероны. R-ген контролирует синтез соответствующего фермента, значительное число r -генов являются транспозонами, способными перемещаться в другие репликоны. Один r-ген содержит несколько транспозонов, контролирующих устойчивость к нескольким антибиотикам. Это объясняет множественную лекарственную устойчивость бактерий.Tra-оперон обеспечивает конъюгативность плазмид, входит в состав R-плазмид грамотрицательных бактерий. Грамположительные бактерии содержат неконъюгативные плазмиды, которые передаются трансдукцией.
Плазмиды патогенности контролируют вирулентность и токсинообразование бактерий.
Бактериоциногенные плазмиды (col-плазмиды) контролируют синтез бактериоциногенов – антибактериальных веществ, вызывающих гибель бактерий того же или близких видов. Бактериоцины обнаружены у кишечной палочки (колицины), бактерий чумы (пестицины), холерных вибрионов (вибриоцины), стафилококков (стафилоцины) и др.
Колицины энтеробактерий – вещества белковой природы. Изучено 25 типов колицинов, различающихся по физико-химическим свойствам, антигенной характеристике, способности адсорбироваться на определенных участках поверхности бактериальных клеток. Продукция колицинов происходит спонтанно в одной из тысячи клеток. Возможна стимуляция продукции колицинов УФ – лучами, что приводит в конечном итоге к гибели клеток, продуцирующих колицины. Т.о. col-плазмиды являются потенциально летальными для клеток – продуцентов. Механизм действия колицинов состоит в нарушении функции рибосом, ЦПМ и др. структур клетки.
Бактериоциногения имеет экологическое значение как один из факторов, формирующих микробный биоценоз микрофлоры организма человека, а так же для типирования бактерий с целью эпиданализа.
Плазмиды биодеградации. Несут информацию об утилизации органических соединений, используемые бактериями в качестве источников углевода и энергии. Могут таким образом обеспечивать селективные преимущества пребывания патогенных бактерий в объектах окружающей среды и в организме человека. Так, плазмиду гидролизации мочевины содержат урологические штаммы кишечных палочек.
4.2.2. Транспозоны
Транспозоны представляют собой нуклеотидные последовательности (2000-20500 пар), несущие генетическую информацию для транспозиции. При встраивании в бактериальную ДНК они вызывают в ней дупликации, а при перемещении – делеции и инверсии. Транспозоны могут находиться автономно в виде кольцевой ДНК, не способной к репликации. Реплицируются они только в составе бактериальной хромосомы. Важное свойство транспозонов – способность к перемещению с одного репликона (хромосомная ДНК) на другой (плазмида) и наоборот. Функции транспозонов – регуляторная и кодирующая.
Концевые структуры транспозонов являются маркерами, отличающими их от других фрагментов ДНК. Интеграция транспозонов в хромосому клеток человека или животных обеспечивает им схожесть с провирусами, находящимися в составе хромосом клеток-хозяина.
4.2.3. Is –последовательности
Is –последовательности – это фрагменты ДНК длиной 1000 пар нуклеотидов и более, представляющие собой транспозируемые элементы. В свободном состоянии не обнаруживаются. В Is –последовательностях содержится информация, которая необходима только для их транспозиции, т.е. перемещения в различные участки ДНК.
Функции Is –последовательностей:
– координация взаимодействия транспозонов плазмид, умеренных фагов, хромосомы бактериальной клетки, обеспечивая их рекомбинацию;
– инактивация генов, в которых произошла интеграция Is –последовательности («выключение гена»);
– встраиваться в определенном положении в бактериальную хромосому и выполнять роль промотора, включая или выключая транскрипцию соответствующих генов (регуляторная функция);
– индукция мутация типа делеций или инверсий при перемещении и дупликации в 5-9 парах нуклеотидов при встраивании в бактериальную хромосому.
4.3. Умеренные фаги
Умеренные и дефектные фаги по своим свойствам напоминают плазмиды бактерий, являются факторами изменчивости. Встраиваясь в хромосому, вызывают лизогенизацию бактерий, обеспечивая их новыми признаками.
4.4. Модификации
Модификациями называют фенотипические изменения какого-либо признака организма. Они не наследуются, предсказуемы, не стойки, не затрагивают генотип, адаптивны, носят массовый и обратимый характер.
Являются ответом на изменяющиеся условия окружающей среды, что позволяет микробной популяции быстро адаптироваться к окружающей среде и сохранять жизнеспособность. Модификация затрагивает морфологические, биохимические, иммунологические и другие признаки с последующим возвращением к первоначальному фенотипу после устранения действия внешнего фактора (химического или физического).
Под непосредственным действием антибиотиков (химическое воздействие) бактерии способны переходить в L-формы, могут сохраняться и размножаться внутри клеток хозяина, после чего вновь реверсировать в исходную форму.
4.5. Мутации
Мутация – это наследуемое изменение в первичной структуре ДНК.
Классификация мутаций:
А.По происхождению – спонтанные и индуцированные. Спонтанные мутации составляют естественный фон, происходят in vitro и in vivo (в естественных биотопах организма человека) под воздействием различных факторов. Одной из причин изменения естественного фона могут быть инсертационные мутации, появляющиеся при встраивании Is –последовательностей, транспозонов и плазмид в хромосому микробной клетки. И если интеграция происходит вблизи промотора, то нарушаются функции регуляторного гена, а если вблизи структурного гена – нарушается синтез закодированного в нем продукта.
Индуцированные мутации возникают под действием искусственно созданного мутагена.
Б.По количеству мутировавших генов различают генные и хромосомные мутации. Генные происходят только в одном гене, хромосомные мутации затрагивают участки хромосом.
Точковые мутации – изменения происходят путем деления или вставки азотистых пар оснований в ДНК, затрагивается при этом один кодон. Конечный результат – новая последовательность нуклеотидов кодирует совершенно другую аминокислоту, как следствие – новый белок.
Мутации со сдвигом считывания затрагивают один ген, происходит вставка или выпадение одной пары азотистых оснований.
Прямые и обратные мутации приводят к восстановлению дикого фенотипа. Так, прямая мутация ведет к появлению мутантного фенотипа, а обратная – к возврату дикого фенотипа, при условии,если изменение состоит в простой замене пары азотистых оснований.
Исправляет мутационные изменения внутригенная супрессия. Внегеннаяс упрессия вторичных мутаций локализуется в генах супрессорах и нарушает работу т-РНК.
Хромосомные мутации возникают при делеции (выпадении), инверсии (повороте), дупликации участков хромосом. Одним из механизмов возникновения хромосомных мутаций является перемещение Is –последовательностей и транспозонов одного участка ДНК в другой, или из хромосомы в плазмиду и наоборот.
В. По фенотипическим последствиям мутации бывают нейтральные, условно-летальные и летальные. Нейтральные мутации не проявляются фенотипически, условно-летальные изменяют, но не утрачивают функции фермента. Летальные мутации приводят к полной утрате способности синтеза ферментов. Основной механизм таких мутаций – делеции.
Фенотипическое проявление мутаций – это утрата пилей, жгутиков, капсулы, клеточной стенки, способности ферментировать углеводы, а так же синтезировать аминокислоты, витамины и другие соединения, появление лекарственной устойчивости.
Ауксотрофные мутаниты нуждаются в определенных факторах роста и сохраняют жизнеспособность при наличии готового вещества в среде обитания.
4.6. R– S– диссоциации
Своеобразной формой изменчивости являются R- S- диссоциации бактерий, которые приводят к образованию двух видов бактериальных клеток, отличающихся по характеру образуемых колоний на твердой питательной среде. R- колонии характеризуются неровными краями, шероховатой поверхностью. Для S- колоний типична круглая форма, гладкая поверхность. Диссоциация (расщепление) обычно протекает в направлении от S- к R-форме, иногда через промежуточные стадии слизистых колоний. Обратный переход форм наблюдается реже. Большинство вирулентных бактерий растет в виде S-форм колоний на плотной питательной среде. Исключение составляют микобактерии туберкулеза, иерсинии чумы, сибиреязвенные бактерии и некоторые другие, растущие в R-форме.
В процессе диссоциации меняется не только морфология колоний, но и биохимические, антигенные, патогенные и др. свойства бактерий.
Биологическое значение R- S- диссоциации состоит в приобретении бактериями селективных преимуществ существования в организме человека или во внешней среде.
Во многих случаях R- S- диссоциация может затруднить бактериологическую диагностику инфекционных заболеваний – дизентерии Зонне, эшерихиоза, вызванного E. Coli О124 и др.
4.7. Мутагены
Мутагены – это химические и физические факторы, вызывающие предмутационные повреждения в отдельном фрагменте ДНК, которые переходят в мутации при нарушении процессов репарации. Одни мутагены способны изменять первичную структуру ДНК, другие – вызывать выпадение или вставку азотистых оснований. Третьи обладают множественным эффектом (супермутагены). Из физических факторов УФ- облучение используют в качестве индуктора мутаций. Мутагены не обладают специфическим действием, т.е. могут вызывать изменения в любом гене. Некоторые химиотерапевтические препараты (например, производные нитрофуранового ряда) также обладают мутагенным действием.
4.8. Репарации
Чтобы восстанавливать поврежденный генетический материал существуют специальные системы – репарационные.
Репарация– процесс исправления повреждений в молекулах ДНК, восстановления клеточного генома, в котором участвуют репарационные ферменты. Они устанавливают места повреждения, вырезают их, синтезируют поврежденные фрагменты и обеспечивают встраивание новых в молекулу ДНК.
Репарационная система, действующая в присутствии видимого света, называется системой фотореактивации.
Система темновой репарации работает в отсутствии видимого света.
Схема дорепликативной репарации выглядит следующим образом:
1) фермент эндонуклеаза обнаруживает и надрезает поврежденный фрагмент ДНК,
2) ДНК-полимераза 1 удаляет вырезанный фрагмент,
3) ДНК-полимераза 1 или III синтезирует нуклеотиды на матрице второй нити ДНК,
4) «сшивание» лигазой восстановленного фрагмента ДНК с основной нитью.
Пострепликативную репарацию путем рекомбинаций применяют мутантам, утратившим способность к темновой репарации.
SOS- репарация – индуцибельный процесс, который происходит при множественных изменениях в ДНК и при участии около 20 новых белков. При низких и средних системах активации происходят ошибки, при высокой степени активации гибнет клетка, но спасаются маркеры бактериальной популяции в целом.
Репарационные системы – свойства клеток млекопитающих и человека. Они восстанавливают поврежденный клеточный геном, вызванный радиацией. Дефекты этих систем – причина ряда заболеваний, например наследственного заболевания человека с летальным исходом Xeroderma pigmentosum. У таких больных отсутствует система репарации, восстанавливающая повреждение ДНК УФ – лучами.
4.9.Генетические рекомбинации
Генетические рекомбинации прокариот имеют свои особенности. Рекомбинации происходят в результате внутригеномных перестроек или при внесении в клетки-реципиенты части ДНК-донора. Последнее приводит к появлению неполной зиготы – мерозиготы.
Рекомбинации подразделяют на законные и незаконные. Законная рекомбинация происходит между близкородственными видами микроорганизмов и требует наличия комплементарных участков ДНК в рекомбинируемых молекулах. Незаконная рекомбинация происходит при участии Is- элементов , которые имеют мелкие концы для быстрого встраивания в бактериальную хромосому.
Практическое значение имеют запрограммированные внутригеномные рекомбинации, при которых происходят изменения локализации имеющихся генов. Они изменяют антигенную структуру микробов и эффективно противостоят факторам иммунитета (боррелии, трипаносомы, малярийный плазмодий).
В генетических рекомбинациях участвует ряд ферментов, rec- генов и происходят они путем трансформации, трансдукции и конъюгации.
4.9.1 Трансформация
Трансформация – непосредственная передача генетического материала (фрагмента ДНК) донора реципиентной клетке. В 1928 году Ф.Гриффитс, в 1944 году О. Эвери, К. Мак-Мод, К. Мак-Карти изучали феномен трансформации и доказали роль ДНК как носителя генетической информации.
Клетки, воспринимающие донорскую ДНК – компетентные. Это состояние непродолжительно, оно совпадает с концом логарифмической фазы роста бактериальной культуры.
Трансформирующей активностью обладают двунитчатые фрагменты ДНК с молекулярной массой не менее 0,5-1х106.
Фазы процесса трансформации бактерий:
- адсорбция ДНК-донора на клетке-реципиенте,
- проникновение ДНК внутрь клетки-реципиента,
- соединение ДНК с гомологичным участком хромосомы реципиента с последующей рекомбинацией.
После проникновения внутрь клетки трансформирующая ДНК деспирализуется, происходит включение любой из двух нитей ДНК донора в геном реципиента.
Степень гомологичности ДНК донора и реципиента обуславливает эффективность процесса трансформации – чем выше гомологичность, тем эффективнее спаривание и большее количество трансформантов.
4.9.2. Трансдукция
Трансдукцией называют передачу генетического материала от одной бактерии к другой с помощью фагов. Процесс открыт в 1951 году Н.Циндером и Дж. Ледербергом.
Различают три вида трансдукции: неспецифическая (общая), специфическая, абортивная.
А. Неспецифическая трансдукция. В момент сборки фаговых частиц в головку фага вместе с фаговой ДНК может проникнуть любой фрагмент ДНК бактерии-донора при репродукции. При этом фаг может утратить часть своего генома и стать дефектным. При таком виде трансдукции в клетку-реципиент могут быть внесены любые гены донора. Принесенный фагом фрагмент ДНК бактерии-донора рекомбинирует в гомологичную область ДНК клетки-реципиента. При неспецифической трансдукции трансдуцирующие фаги являются только переносчиками генетического материала от одних бактерий к другим, а сама фаговая ДНК не участвует в образовании трансдуктантов.
Б.Специфическая трансдукция. Характеризуется способностью фага переносить определенные гены от бактерии-донора к бактерии-реципиенту,при этом образование трансдуцирующего фага происходит путем выщепления профага из бактериальной хромосомы вместе с генами, расположенными рядом с профагом, на хромосоме клетки-донора.
При взаимодействии трансдуцирующих фагов с клетками реципиентного штамма происходит включение гена бактерии-донора вместе с ДНК дефектного фага в хромосому бактерии-реципиента. Бактерии, лизогенированные дефектным фагом, невосприимчивы к последующему заражению гомологичным вирулентным фагом.
В. Абортивная трансдукция. При таком виде трансдукции принесенный фагом фрагмент ДНК бактерии-донора не включается в хромосому бактерии-реципиента, а располагается в цитоплазме. При делении клетки трансдуцированный фрагмент ДНК-донора передается одной дочерней клетке, т.е. наследуется однолинейно и в конечном итоге утрачивается в потомстве.
4.9.3. Конъюгация
Конъюгация – перенос генетического материала из клетки-донора в клетку реципиента при их скрещивании. Этот процесс обнаружили в 1946 году Д.Леденберг и Э. Тейтум.
Бактерии, несущие F-плазмиду (F+ – половой фактор) – всегда доноры. Реципиентами являются бактериальные клетки, не имеющие F-плазмид (F–). При скрещивании F+ и F– – клеток высока частота передачи полового фактора, при этом почти все реципиенты становятся F+– клетками.
F-плазмида способна интегрировать в определенные участки бактериальной хромосомы и становиться ее частью. В некоторых случаях, освобождаясь из хромосомы, F-плазмида захватывает сцепленные с ней бактериальные гены.
Этапы конъюгации:
- прикрепление клетки – донора к реципиентной клетке с помощью половых ворсинок,
- образование конъюгативного мостика между клетками,
- передача F-фактора из клеток – донора в клетки-реципиента , возможна передача и других автономных плазмид.
- В процессе конъюгации эндонуклеаза включает F-плазмиду в цепь ДНК и разрывает ее. Проксимальный конец ДНК через конъюгативный мостик проникает в клетку-реципиент и сразу же достраивается до двунитевой структуры. Оставшаяся в клетке- доноре нить ДНК становится матрицей для синтеза второй цепи. Т.о., при конъюгации передается только одна нить ДНК-донора. Существуют штаммы бактерий доноров – Hfr, которые при соединении с клеткой передают только гены бактериальной хромосомы, а не F-фактор.
-
-
- 4.10. Генетика популяций
- В организме человека микробы находятся в определенных биотопах
- ( полость рта, просвет кишки, кожа и т.п.) в виде популяций. Генофонд популяции обеспечивает ее стабильность и выживаемость. По действием внешних факторов в процессе жизнедеятельности в микробной популяции появляются отдельные особи с новыми признаками, которые являются гетерогенными по отношению к большинству клеток. Чем выше гетерогенность популяции, тем больше шансов на ее выживание. Накопление гетерогенных особей в популяции изменяет ее генофонд. Изменчивость генофонда бывает фенотипической (модификационной) и генотипической (мутационной, рекомбинантной).
- Модификационную изменчивость обеспечивают механизмы репрессии и индукции структурных генов без их перестройки. Выживают клетки, лучше других адаптирующиеся к изменениям окружающей среды. Прекращение действия факторов внешней среды приводит к первоначальному фенотипу.
- Мутационно- рекомбинационный механизм связан с появлением в популяции генотипов, постоянно возникающих в результате мутаций и рекомбинаций, внесения внешней информации с транспозируемыми элементами.
- Увеличение гетерогенности микробных популяций в организме человека происходит за счет воздействия мутагенных факторов, образующихся в результате метаболических реакций (нитрозамины и др.), некоторых химиотерапевтических средств (производные нитрофурана и др.), а также молекул ДНК и РНК, освобождающихся после гибели микроорганизмов и клеток разнообразных тканей и органов.
- В организме человека в качестве селективных факторов выступают химиотерапевтические средства, специфические антитела и др. Вместе с тем, эти факторы могут служить индукторами соответствующих сигналов, воспринимающимися рецепторами бактерий и передающимися регуляторным генам, что приводит к появлению новых генотипов и фенотипов.
-
-
-
-
 Рис. 5. Сложно устроенные вирусы (с оболочкой)
Рис. 5. Сложно устроенные вирусы (с оболочкой)
 Морфологической субъединицей капсида является капсомер. Белковые субъединицы вируса могут содержать одну или несколько молекул. Существует два типа строения капсидов вирионов: 1.Капсомеры ассоциированы с геномом и образуют спиралевидную (винтовую) структуру, такой тип симметрии называют спиральным. Его имеют вирус табачной мозаики, парамиксовирусы, ортомиксовирусы; 2.Капсомеры образуют полое изометрическое тело, в центре которого находится геном; такой тип укладки называют кубический. Тело таких вирусов симметрическое в трех взаимно перпендикулярных направлениях; вирус полиомиелита представляет икосаэдр и состоит из 60 капсомеров. Отсутствие постоянной симметрии характерно для вирусов больших размеров, например бактериофагов.
Нуклеиновые кислоты. Клетки всех живых организмов содержат два вида нуклеиновой кислоты – ДНК и РНК. ДНК представляет собой двунитчатую молекулу, а РНК – однонитчатую. РНК представлена тремя классами молекул: иРНК, рРНК, тРНК. В отличие от клеток, вирусы содержат только один вид нуклеиновой кислоты – либо РНК, либо ДНК.И та и другая выполняют функцию генома. Вирусные НК характеризуются поразительным разнообразием форм. Вирусный геном может быть представлен как однонитчатыми, так и двунитчатыми молекулами РНК и ДНК. ДНК может быть линейной и кольцевой, а РНК – непрерывной, фрагментированной, кольцевой.
Рис6. Типы молекул вирусных ДНК и РНК
Морфологической субъединицей капсида является капсомер. Белковые субъединицы вируса могут содержать одну или несколько молекул. Существует два типа строения капсидов вирионов: 1.Капсомеры ассоциированы с геномом и образуют спиралевидную (винтовую) структуру, такой тип симметрии называют спиральным. Его имеют вирус табачной мозаики, парамиксовирусы, ортомиксовирусы; 2.Капсомеры образуют полое изометрическое тело, в центре которого находится геном; такой тип укладки называют кубический. Тело таких вирусов симметрическое в трех взаимно перпендикулярных направлениях; вирус полиомиелита представляет икосаэдр и состоит из 60 капсомеров. Отсутствие постоянной симметрии характерно для вирусов больших размеров, например бактериофагов.
Нуклеиновые кислоты. Клетки всех живых организмов содержат два вида нуклеиновой кислоты – ДНК и РНК. ДНК представляет собой двунитчатую молекулу, а РНК – однонитчатую. РНК представлена тремя классами молекул: иРНК, рРНК, тРНК. В отличие от клеток, вирусы содержат только один вид нуклеиновой кислоты – либо РНК, либо ДНК.И та и другая выполняют функцию генома. Вирусные НК характеризуются поразительным разнообразием форм. Вирусный геном может быть представлен как однонитчатыми, так и двунитчатыми молекулами РНК и ДНК. ДНК может быть линейной и кольцевой, а РНК – непрерывной, фрагментированной, кольцевой.
Рис6. Типы молекул вирусных ДНК и РНК
 ДНК: 1-парвовирусы, 2-фаг Х174, 3- аденовирусы, 4- фаг Т5, 6- паповирусы, 7- вирус гепатита В; РНК: 1- пикорнавирусы, тогавирусы, парамиксовирусы, рабдовирусы, 2- ортомиксовирусы, 3- буньявирусы, 4- реовирусы, 5- ретровирусы.
Белки. В зараженной клетке вирусный геном кодирует синтез структурных и неструктурных белков. Структурные белки нужны вирусным частицам потомства, неструктурные обслуживают процесс внутриклеточной репродукции вируса. Структурные белки бывают капсидные и суперкапсидные.
Белки просто и сложно устроенных вирусов Таблица 8.
ДНК: 1-парвовирусы, 2-фаг Х174, 3- аденовирусы, 4- фаг Т5, 6- паповирусы, 7- вирус гепатита В; РНК: 1- пикорнавирусы, тогавирусы, парамиксовирусы, рабдовирусы, 2- ортомиксовирусы, 3- буньявирусы, 4- реовирусы, 5- ретровирусы.
Белки. В зараженной клетке вирусный геном кодирует синтез структурных и неструктурных белков. Структурные белки нужны вирусным частицам потомства, неструктурные обслуживают процесс внутриклеточной репродукции вируса. Структурные белки бывают капсидные и суперкапсидные.
Белки просто и сложно устроенных вирусов Таблица 8.
 3.4. Морфогенез вирусов
Репродукция вирусов включает две следующие друг за другом фазы. Первая фаза заключается в адсорбции и проникновении вируса в клетку, модификации вируса до способности вызвать инфекцию. Три стадии первой фазы:
3.4. Морфогенез вирусов
Репродукция вирусов включает две следующие друг за другом фазы. Первая фаза заключается в адсорбции и проникновении вируса в клетку, модификации вируса до способности вызвать инфекцию. Три стадии первой фазы:
 Лизогения. Вирулентные фаги вызывают гибель (лизис) бактериальной клетки. Умеренные фаги при взаимодействии с клеткой хозяина встраивают свою НК в бактериалъный геном. Профаг – неинфекционная форма, состояние ассоциации фаговой НК с геномом хозяина.
Бактериальная клетка, содержащая профаг, называется лизогенной, а явление – лизогенией. При облучении УФ лучами лизогенных бактерий продукция фага увеличивается, феномен этот называется индукцией профага и применяется для определения дозы радиации на космических кораблях.
Лизогенная конверсия заключается в приобретении лизогенными бактериями определенных признаков (способности продуцировать токсины, изменять антигенные свойства и т.п.). Дефектные умеренные фаги не способны к образованию зрелых фаговых частиц, что используется в генной инженерии.
Практическое применение бактериофагов. Бактериофаги используют для типирования бактерий и индикации (выявлении) в окружающей среде, для лечения и профилактики инфекционных заболеваний (редко). Метод фаготипирования бактерий с целью определения фаготипа широко применяется в микробиологической практике, что позволяет установить источник инфекции и пути ее передачи.
Рис.9.Развитие умеренного фага
Лизогения. Вирулентные фаги вызывают гибель (лизис) бактериальной клетки. Умеренные фаги при взаимодействии с клеткой хозяина встраивают свою НК в бактериалъный геном. Профаг – неинфекционная форма, состояние ассоциации фаговой НК с геномом хозяина.
Бактериальная клетка, содержащая профаг, называется лизогенной, а явление – лизогенией. При облучении УФ лучами лизогенных бактерий продукция фага увеличивается, феномен этот называется индукцией профага и применяется для определения дозы радиации на космических кораблях.
Лизогенная конверсия заключается в приобретении лизогенными бактериями определенных признаков (способности продуцировать токсины, изменять антигенные свойства и т.п.). Дефектные умеренные фаги не способны к образованию зрелых фаговых частиц, что используется в генной инженерии.
Практическое применение бактериофагов. Бактериофаги используют для типирования бактерий и индикации (выявлении) в окружающей среде, для лечения и профилактики инфекционных заболеваний (редко). Метод фаготипирования бактерий с целью определения фаготипа широко применяется в микробиологической практике, что позволяет установить источник инфекции и пути ее передачи.
Рис.9.Развитие умеренного фага
 Рис.10. Взаимодействие бактериофага с оболочкой бактерий
Рис.10. Взаимодействие бактериофага с оболочкой бактерий
 3.9. Прионы
Прионы – белковая инфекционная единица. Состоят из белковых молекул определенной структуры. Отличаются устойчивостью к высоким температурам, ионизирующей радиации, излучению и другим экстремальным воздействиям. Они чувствительны к фенолу и детергентам при нагревании. Могут персистировать в организме человека длительное время, не вызывая иммунного ответа. Накопление прионов в клетке приводит к гибели последней. Прионный белок существует в двух формах – нормальной и патологической. В первом случае это естественный компонент клеток здорового организма, участвует в передаче нервного импульса, в поддержании циркадных ритмов, в механизмах старения мозга и нервной системы. Патологическая форма вызывает медленные инфекции человека.
3.10. Патогенез вирусных инфекций
3.10.1. Взаимодействие вируса с клеткой.
В основе взаимодействия вирусов с организмом всегда лежит инфекционный процесс на уровне клетки, который реализуется путем взаимодействия вирусного и клеточного геномов. Это позволяет классифицировать инфекции на клеточном и на организменных уровнях.
Схема 2. Классификация вирусных инфекций
3.9. Прионы
Прионы – белковая инфекционная единица. Состоят из белковых молекул определенной структуры. Отличаются устойчивостью к высоким температурам, ионизирующей радиации, излучению и другим экстремальным воздействиям. Они чувствительны к фенолу и детергентам при нагревании. Могут персистировать в организме человека длительное время, не вызывая иммунного ответа. Накопление прионов в клетке приводит к гибели последней. Прионный белок существует в двух формах – нормальной и патологической. В первом случае это естественный компонент клеток здорового организма, участвует в передаче нервного импульса, в поддержании циркадных ритмов, в механизмах старения мозга и нервной системы. Патологическая форма вызывает медленные инфекции человека.
3.10. Патогенез вирусных инфекций
3.10.1. Взаимодействие вируса с клеткой.
В основе взаимодействия вирусов с организмом всегда лежит инфекционный процесс на уровне клетки, который реализуется путем взаимодействия вирусного и клеточного геномов. Это позволяет классифицировать инфекции на клеточном и на организменных уровнях.
Схема 2. Классификация вирусных инфекций
 3.10.2.Классификация вирусных инфекций на клеточном уровне.
При автономной вирусной инфекции геном вируса реплицируется независимо, но взаимодействие между геномами вируса и клетки сохраняется. Автономная вирусная инфекция характерна для большинства животных.
При интегрированной инфекции вирусный геном включается в состав клеточного генома, реплицируется вместе с ним как составная часть клеточного генома. Интегрировать могут как полный геном, так и часть его: при гепатите В происходит интеграция полного генома, при аденовирусных и герпетических инфекциях обычно интегрирует часть генома, при инфекциях онковирусами может быть двояко. Интеграция может привести к неопластической трансформации клетки – способности неограниченно делиться.
Общепринят следующий механизм интеграции. Вирусная ДНК должна быть кольцевой формы и двунитчатой. Эта молекула прикрепляется к клеточной ДНК, места прикрепления разрезаются и вновь сшиваются.
Инфекция может быть продуктивной и абортивной. Продуктивная инфекция завершается образованием инфекционного потомства. Абортивная инфекция не завершается образованием инфекционных вирусных частиц или они образуются в меньшем количестве. Может возникнуть путем:
3.10.2.Классификация вирусных инфекций на клеточном уровне.
При автономной вирусной инфекции геном вируса реплицируется независимо, но взаимодействие между геномами вируса и клетки сохраняется. Автономная вирусная инфекция характерна для большинства животных.
При интегрированной инфекции вирусный геном включается в состав клеточного генома, реплицируется вместе с ним как составная часть клеточного генома. Интегрировать могут как полный геном, так и часть его: при гепатите В происходит интеграция полного генома, при аденовирусных и герпетических инфекциях обычно интегрирует часть генома, при инфекциях онковирусами может быть двояко. Интеграция может привести к неопластической трансформации клетки – способности неограниченно делиться.
Общепринят следующий механизм интеграции. Вирусная ДНК должна быть кольцевой формы и двунитчатой. Эта молекула прикрепляется к клеточной ДНК, места прикрепления разрезаются и вновь сшиваются.
Инфекция может быть продуктивной и абортивной. Продуктивная инфекция завершается образованием инфекционного потомства. Абортивная инфекция не завершается образованием инфекционных вирусных частиц или они образуются в меньшем количестве. Может возникнуть путем:
 Некоторые вирусы вызывают характерный цитопатический эффект, проявляющийся в слиянии клеток и образовании многоядерных клеток – симпластов (синцитий). Такими свойствами обладают парамиксовирусы, некоторые ретровирусы, вирусы герпеса.
3.10.4. Классификация вирусных инфекций на организменном уровне
В основу классификации положены:
Некоторые вирусы вызывают характерный цитопатический эффект, проявляющийся в слиянии клеток и образовании многоядерных клеток – симпластов (синцитий). Такими свойствами обладают парамиксовирусы, некоторые ретровирусы, вирусы герпеса.
3.10.4. Классификация вирусных инфекций на организменном уровне
В основу классификации положены:
 Рис. 5. Сложно устроенные вирусы (с оболочкой)
Рис. 5. Сложно устроенные вирусы (с оболочкой)
 Морфологической субъединицей капсида является капсомер. Белковые субъединицы вируса могут содержать одну или несколько молекул. Существует два типа строения капсидов вирионов: 1.Капсомеры ассоциированы с геномом и образуют спиралевидную (винтовую) структуру, такой тип симметрии называют спиральным. Его имеют вирус табачной мозаики, парамиксовирусы, ортомиксовирусы; 2.Капсомеры образуют полое изометрическое тело, в центре которого находится геном; такой тип укладки называют кубический. Тело таких вирусов симметрическое в трех взаимно перпендикулярных направлениях; вирус полиомиелита представляет икосаэдр и состоит из 60 капсомеров. Отсутствие постоянной симметрии характерно для вирусов больших размеров, например бактериофагов.
Нуклеиновые кислоты. Клетки всех живых организмов содержат два вида нуклеиновой кислоты – ДНК и РНК. ДНК представляет собой двунитчатую молекулу, а РНК – однонитчатую. РНК представлена тремя классами молекул: иРНК, рРНК, тРНК. В отличие от клеток, вирусы содержат только один вид нуклеиновой кислоты – либо РНК, либо ДНК.И та и другая выполняют функцию генома. Вирусные НК характеризуются поразительным разнообразием форм. Вирусный геном может быть представлен как однонитчатыми, так и двунитчатыми молекулами РНК и ДНК. ДНК может быть линейной и кольцевой, а РНК – непрерывной, фрагментированной, кольцевой.
Рис6. Типы молекул вирусных ДНК и РНК
Морфологической субъединицей капсида является капсомер. Белковые субъединицы вируса могут содержать одну или несколько молекул. Существует два типа строения капсидов вирионов: 1.Капсомеры ассоциированы с геномом и образуют спиралевидную (винтовую) структуру, такой тип симметрии называют спиральным. Его имеют вирус табачной мозаики, парамиксовирусы, ортомиксовирусы; 2.Капсомеры образуют полое изометрическое тело, в центре которого находится геном; такой тип укладки называют кубический. Тело таких вирусов симметрическое в трех взаимно перпендикулярных направлениях; вирус полиомиелита представляет икосаэдр и состоит из 60 капсомеров. Отсутствие постоянной симметрии характерно для вирусов больших размеров, например бактериофагов.
Нуклеиновые кислоты. Клетки всех живых организмов содержат два вида нуклеиновой кислоты – ДНК и РНК. ДНК представляет собой двунитчатую молекулу, а РНК – однонитчатую. РНК представлена тремя классами молекул: иРНК, рРНК, тРНК. В отличие от клеток, вирусы содержат только один вид нуклеиновой кислоты – либо РНК, либо ДНК.И та и другая выполняют функцию генома. Вирусные НК характеризуются поразительным разнообразием форм. Вирусный геном может быть представлен как однонитчатыми, так и двунитчатыми молекулами РНК и ДНК. ДНК может быть линейной и кольцевой, а РНК – непрерывной, фрагментированной, кольцевой.
Рис6. Типы молекул вирусных ДНК и РНК
 ДНК: 1-парвовирусы, 2-фаг Х174, 3- аденовирусы, 4- фаг Т5, 6- паповирусы, 7- вирус гепатита В; РНК: 1- пикорнавирусы, тогавирусы, парамиксовирусы, рабдовирусы, 2- ортомиксовирусы, 3- буньявирусы, 4- реовирусы, 5- ретровирусы.
Белки. В зараженной клетке вирусный геном кодирует синтез структурных и неструктурных белков. Структурные белки нужны вирусным частицам потомства, неструктурные обслуживают процесс внутриклеточной репродукции вируса. Структурные белки бывают капсидные и суперкапсидные.
Белки просто и сложно устроенных вирусов Таблица 8.
ДНК: 1-парвовирусы, 2-фаг Х174, 3- аденовирусы, 4- фаг Т5, 6- паповирусы, 7- вирус гепатита В; РНК: 1- пикорнавирусы, тогавирусы, парамиксовирусы, рабдовирусы, 2- ортомиксовирусы, 3- буньявирусы, 4- реовирусы, 5- ретровирусы.
Белки. В зараженной клетке вирусный геном кодирует синтез структурных и неструктурных белков. Структурные белки нужны вирусным частицам потомства, неструктурные обслуживают процесс внутриклеточной репродукции вируса. Структурные белки бывают капсидные и суперкапсидные.
Белки просто и сложно устроенных вирусов Таблица 8.
 3.4. Морфогенез вирусов
Репродукция вирусов включает две следующие друг за другом фазы. Первая фаза заключается в адсорбции и проникновении вируса в клетку, модификации вируса до способности вызвать инфекцию. Три стадии первой фазы:
3.4. Морфогенез вирусов
Репродукция вирусов включает две следующие друг за другом фазы. Первая фаза заключается в адсорбции и проникновении вируса в клетку, модификации вируса до способности вызвать инфекцию. Три стадии первой фазы:
 Лизогения. Вирулентные фаги вызывают гибель (лизис) бактериальной клетки. Умеренные фаги при взаимодействии с клеткой хозяина встраивают свою НК в бактериалъный геном. Профаг – неинфекционная форма, состояние ассоциации фаговой НК с геномом хозяина.
Бактериальная клетка, содержащая профаг, называется лизогенной, а явление – лизогенией. При облучении УФ лучами лизогенных бактерий продукция фага увеличивается, феномен этот называется индукцией профага и применяется для определения дозы радиации на космических кораблях.
Лизогенная конверсия заключается в приобретении лизогенными бактериями определенных признаков (способности продуцировать токсины, изменять антигенные свойства и т.п.). Дефектные умеренные фаги не способны к образованию зрелых фаговых частиц, что используется в генной инженерии.
Практическое применение бактериофагов. Бактериофаги используют для типирования бактерий и индикации (выявлении) в окружающей среде, для лечения и профилактики инфекционных заболеваний (редко). Метод фаготипирования бактерий с целью определения фаготипа широко применяется в микробиологической практике, что позволяет установить источник инфекции и пути ее передачи.
Рис.9.Развитие умеренного фага
Лизогения. Вирулентные фаги вызывают гибель (лизис) бактериальной клетки. Умеренные фаги при взаимодействии с клеткой хозяина встраивают свою НК в бактериалъный геном. Профаг – неинфекционная форма, состояние ассоциации фаговой НК с геномом хозяина.
Бактериальная клетка, содержащая профаг, называется лизогенной, а явление – лизогенией. При облучении УФ лучами лизогенных бактерий продукция фага увеличивается, феномен этот называется индукцией профага и применяется для определения дозы радиации на космических кораблях.
Лизогенная конверсия заключается в приобретении лизогенными бактериями определенных признаков (способности продуцировать токсины, изменять антигенные свойства и т.п.). Дефектные умеренные фаги не способны к образованию зрелых фаговых частиц, что используется в генной инженерии.
Практическое применение бактериофагов. Бактериофаги используют для типирования бактерий и индикации (выявлении) в окружающей среде, для лечения и профилактики инфекционных заболеваний (редко). Метод фаготипирования бактерий с целью определения фаготипа широко применяется в микробиологической практике, что позволяет установить источник инфекции и пути ее передачи.
Рис.9.Развитие умеренного фага
 Рис.10. Взаимодействие бактериофага с оболочкой бактерий
Рис.10. Взаимодействие бактериофага с оболочкой бактерий
 3.9. Прионы
Прионы – белковая инфекционная единица. Состоят из белковых молекул определенной структуры. Отличаются устойчивостью к высоким температурам, ионизирующей радиации, излучению и другим экстремальным воздействиям. Они чувствительны к фенолу и детергентам при нагревании. Могут персистировать в организме человека длительное время, не вызывая иммунного ответа. Накопление прионов в клетке приводит к гибели последней. Прионный белок существует в двух формах – нормальной и патологической. В первом случае это естественный компонент клеток здорового организма, участвует в передаче нервного импульса, в поддержании циркадных ритмов, в механизмах старения мозга и нервной системы. Патологическая форма вызывает медленные инфекции человека.
3.10. Патогенез вирусных инфекций
3.10.1. Взаимодействие вируса с клеткой.
В основе взаимодействия вирусов с организмом всегда лежит инфекционный процесс на уровне клетки, который реализуется путем взаимодействия вирусного и клеточного геномов. Это позволяет классифицировать инфекции на клеточном и на организменных уровнях.
Схема 2. Классификация вирусных инфекций
3.9. Прионы
Прионы – белковая инфекционная единица. Состоят из белковых молекул определенной структуры. Отличаются устойчивостью к высоким температурам, ионизирующей радиации, излучению и другим экстремальным воздействиям. Они чувствительны к фенолу и детергентам при нагревании. Могут персистировать в организме человека длительное время, не вызывая иммунного ответа. Накопление прионов в клетке приводит к гибели последней. Прионный белок существует в двух формах – нормальной и патологической. В первом случае это естественный компонент клеток здорового организма, участвует в передаче нервного импульса, в поддержании циркадных ритмов, в механизмах старения мозга и нервной системы. Патологическая форма вызывает медленные инфекции человека.
3.10. Патогенез вирусных инфекций
3.10.1. Взаимодействие вируса с клеткой.
В основе взаимодействия вирусов с организмом всегда лежит инфекционный процесс на уровне клетки, который реализуется путем взаимодействия вирусного и клеточного геномов. Это позволяет классифицировать инфекции на клеточном и на организменных уровнях.
Схема 2. Классификация вирусных инфекций
 3.10.2.Классификация вирусных инфекций на клеточном уровне.
При автономной вирусной инфекции геном вируса реплицируется независимо, но взаимодействие между геномами вируса и клетки сохраняется. Автономная вирусная инфекция характерна для большинства животных.
При интегрированной инфекции вирусный геном включается в состав клеточного генома, реплицируется вместе с ним как составная часть клеточного генома. Интегрировать могут как полный геном, так и часть его: при гепатите В происходит интеграция полного генома, при аденовирусных и герпетических инфекциях обычно интегрирует часть генома, при инфекциях онковирусами может быть двояко. Интеграция может привести к неопластической трансформации клетки – способности неограниченно делиться.
Общепринят следующий механизм интеграции. Вирусная ДНК должна быть кольцевой формы и двунитчатой. Эта молекула прикрепляется к клеточной ДНК, места прикрепления разрезаются и вновь сшиваются.
Инфекция может быть продуктивной и абортивной. Продуктивная инфекция завершается образованием инфекционного потомства. Абортивная инфекция не завершается образованием инфекционных вирусных частиц или они образуются в меньшем количестве. Может возникнуть путем:
3.10.2.Классификация вирусных инфекций на клеточном уровне.
При автономной вирусной инфекции геном вируса реплицируется независимо, но взаимодействие между геномами вируса и клетки сохраняется. Автономная вирусная инфекция характерна для большинства животных.
При интегрированной инфекции вирусный геном включается в состав клеточного генома, реплицируется вместе с ним как составная часть клеточного генома. Интегрировать могут как полный геном, так и часть его: при гепатите В происходит интеграция полного генома, при аденовирусных и герпетических инфекциях обычно интегрирует часть генома, при инфекциях онковирусами может быть двояко. Интеграция может привести к неопластической трансформации клетки – способности неограниченно делиться.
Общепринят следующий механизм интеграции. Вирусная ДНК должна быть кольцевой формы и двунитчатой. Эта молекула прикрепляется к клеточной ДНК, места прикрепления разрезаются и вновь сшиваются.
Инфекция может быть продуктивной и абортивной. Продуктивная инфекция завершается образованием инфекционного потомства. Абортивная инфекция не завершается образованием инфекционных вирусных частиц или они образуются в меньшем количестве. Может возникнуть путем:
 Некоторые вирусы вызывают характерный цитопатический эффект, проявляющийся в слиянии клеток и образовании многоядерных клеток – симпластов (синцитий). Такими свойствами обладают парамиксовирусы, некоторые ретровирусы, вирусы герпеса.
3.10.4. Классификация вирусных инфекций на организменном уровне
В основу классификации положены:
Некоторые вирусы вызывают характерный цитопатический эффект, проявляющийся в слиянии клеток и образовании многоядерных клеток – симпластов (синцитий). Такими свойствами обладают парамиксовирусы, некоторые ретровирусы, вирусы герпеса.
3.10.4. Классификация вирусных инфекций на организменном уровне
В основу классификации положены:


