Просмотров: 5 189
ГАСТРОПАТИИ, ИНДУЦИРОВАННЫЕ НЕСТЕРОИДНЫМИ ПРОТИВОВОСПАЛИТЕЛЬНЫМИ ПРЕПАРАТАМИ: КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ, ЛЕЧЕНИЕ, ПРОФИЛАКТИКА
Ирина Александровна Зборовская – д.м.н., профессор, заведующая кафедрой госпитальной терапии с курсом клинической ревматологии факультета усовершенствования врачей Волгоградского государственного медицинского университета, заместитель директора по научной работе Государственного учреждения ” Научно-исследовательский институт клинической и экспериментальной ревматологии” РАМН, руководитель регионального Центра по проблемам остеопороза, член президиума Ассоциации ревматологов России, член редакционных советов журналов “Научно – практическая ревматология” и “Современная ревматология”
 Патогенез НПВП – гастропатии
1. Как известно, НПВП ингибируют активность фермента циклооксигеназы (ЦОГ), имеющего два изомера ЦОГ-1 и ЦОГ-2. Угнетение активности ЦОГ-2 собственно и определяет противовоспалительное действие, угнетение активности ЦОГ-1 приводит к снижению синтеза простагладинов и простациклина в слизистой оболочке желудка. Функция простагладинов по отношению к гастродуоденальной слизистой оболочке является протективной. В эксперименте показано, что экзогенно введенные простагладины способствуют устойчивости слизистой оболочки к таким повреждающим агентам, как этанол, желчные кислоты, растворы кислот и солей, а также НПВП. Спектр основных физиологических эффектов простагландинов включает:
Патогенез НПВП – гастропатии
1. Как известно, НПВП ингибируют активность фермента циклооксигеназы (ЦОГ), имеющего два изомера ЦОГ-1 и ЦОГ-2. Угнетение активности ЦОГ-2 собственно и определяет противовоспалительное действие, угнетение активности ЦОГ-1 приводит к снижению синтеза простагладинов и простациклина в слизистой оболочке желудка. Функция простагладинов по отношению к гастродуоденальной слизистой оболочке является протективной. В эксперименте показано, что экзогенно введенные простагладины способствуют устойчивости слизистой оболочки к таким повреждающим агентам, как этанол, желчные кислоты, растворы кислот и солей, а также НПВП. Спектр основных физиологических эффектов простагландинов включает:
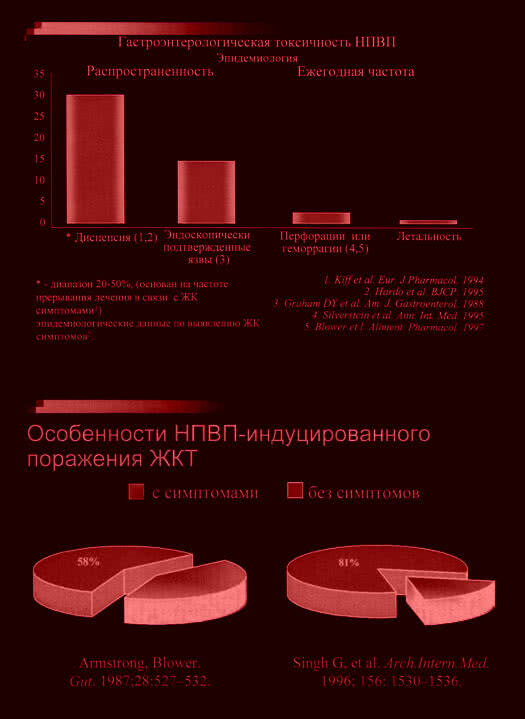
 II. Между язвами, вызванными приемом НПВП, и спонтанно возникшими существует определенная разница. Во-первых, язвы, вызванные приемом НПВП, чаще всего бывают бессимптомными (у 60% больных, особенно пожилых), и диагноз во многих случаях устанавливают при фиброгастродуоденоскопии. Во-вторых, слизистая оболочка желудка приспосабливается к длительному воздействию кислот (НПВП), в связи с чем после 2-8 недель приема медикамента острота поражения несколько уменьшается. Ряд экспериментов показал, что наиболее опасными могут считаться первые недели приема НПВП. Эндоскопическое обследование, проведенное у пациентов, применявших непрерывную терапию НПВП на протяжении 6 месяцев, показало, что только у 32% пациентов слизистая желудка остается в норме. У оставшихся 68% выявляются патологические изменения слизистой. Гистологически слизистая вокруг язвы, вызванной НПВП, обычно нормальная или только слегка воспалена в отличие от хронического гастрита при типичных хронических язвах желудка.
II. Между язвами, вызванными приемом НПВП, и спонтанно возникшими существует определенная разница. Во-первых, язвы, вызванные приемом НПВП, чаще всего бывают бессимптомными (у 60% больных, особенно пожилых), и диагноз во многих случаях устанавливают при фиброгастродуоденоскопии. Во-вторых, слизистая оболочка желудка приспосабливается к длительному воздействию кислот (НПВП), в связи с чем после 2-8 недель приема медикамента острота поражения несколько уменьшается. Ряд экспериментов показал, что наиболее опасными могут считаться первые недели приема НПВП. Эндоскопическое обследование, проведенное у пациентов, применявших непрерывную терапию НПВП на протяжении 6 месяцев, показало, что только у 32% пациентов слизистая желудка остается в норме. У оставшихся 68% выявляются патологические изменения слизистой. Гистологически слизистая вокруг язвы, вызванной НПВП, обычно нормальная или только слегка воспалена в отличие от хронического гастрита при типичных хронических язвах желудка.
 Факторы риска
Факторы риска
 II. Предполагается, что у разных противовоспалительных препаратов разный «повреждающий» потенциал.
1. Кроме того, частота возникновения гастро- и дуоденопатий, желудочных и дуоденальных кровотечений зависит от используемого препарата, продолжительности приема и некоторых других факторов.
Сравнительный риск возникновения эрозивно-язвенных поражений при приеме различных НПВП: данные метаанализа.
(Garsia Rodrigues L.A., 1998).
II. Предполагается, что у разных противовоспалительных препаратов разный «повреждающий» потенциал.
1. Кроме того, частота возникновения гастро- и дуоденопатий, желудочных и дуоденальных кровотечений зависит от используемого препарата, продолжительности приема и некоторых других факторов.
Сравнительный риск возникновения эрозивно-язвенных поражений при приеме различных НПВП: данные метаанализа.
(Garsia Rodrigues L.A., 1998).
Как вы видите, наименьшим риском развития гастро- и дуоденопатий, осложненных кровотечением, обладают ибупрофен (бруфен и другие синонимы) и диклофенак (вольтарен и другие синонимы), а наибольшим – азопропазон, кеторолак, пироксикам, тометил, бутадион (фенилбутазон), аспирин, дифлунизал. Напроксен и сулиндак занимают промежуточное положение.
2. Индекс гастроинтестинальной токсичности НПВП (он определяется соотношением доз, вызывающих в 50% случаев противовоспалительный и ульцерогенный эффекты) представлен в следующей таблице.
Индекс гастроинтестинальной токсичности различных НПВП, рассчитанный на основе банка ARAMIS.
Однако по данным А.Е. Каратаевой, В.А. Насоновой (2000), при использовании НПВП в дозах ниже и выше средних терапевтических частота развития язв и эрозий статистически достоверно не различалась. Кроме того, в этом российском исследовании было показано, что совместный прием НПВП и кортикостероидов не только не повышал, но даже снижал риск развития эрозивно-язвенных поражений.
3. Влияет ли длительность приема НПВП на частоту развития эрозивно-язвенного поражения желудка?
В большинстве исследований продолжительность приема НПВП считается фактором риска, однако подчеркивается, как я уже говорила, что риск максимален в первый месяц их назначения. F. Silverstain и соавт. (1995) не обнаружили снижения величины относительного риска развития существенного гастроэнтерологического осложнения при продолжении приема НПВП.
4. Значение инфекции H. pylori в качестве фактора риска для развития эрозивно-язвенных поражений желудка и 12-перстной кишки при приеме НПВП неоднозначно и требует более подробного рассмотрения. Данные литературы по вопросу о влиянии колонизации гастродуоденальной слизистой оболочки H. pylori на частоту ульцерации больных, принимающих НПВП, различны. В большинстве зарубежных клинических исследований было показано, что наличие инфекции ассоциировано с существенным увеличением числа дуоденальных язв и с незначительным увеличением язв, локализующихся в желудке. При исследовании было обнаружено, что наличие микроорганизма было связано с незначительным увеличением у инфицированных частоты язв в желудке и существенным увеличением частоты язв в 12 – перстной кишке.
Для нашей страны эти результаты имеют скорее косвенное значение. Дело в том, что в нашей стране частота инфицирования H. pylori взрослой популяции очень высока (превышает 80%), поэтому выделить группу H.pylori – негативных, принимавших НПВП, будет, вероятно, затруднительно.
Диагностика
I. Диагностика гастро- и дуоденопатий, ассоциированных с НПВП, основывается в первую очередь на результатах эндоскопического исследования верхних отделов пищеварительного тракта. Его необходимо проводить всем больным, имеющим высокий риск развития осложнений от приема данных препаратов, т.е. с наличием клинических симптомов гастропатии, особенно эпигастральных болей, изжоги, тошноты, рвоты, анорексии и анемии.
II. К диагностическим эндоскопическим признакам относятся: наличие гиперемии, отека, кровоизлияний, эрозий, изъязвлений и отсутствие характерного для ЯБ периульцерозного воспалительного вала. Эти изменения чаще локализуются в антральном отделе, реже – в теле желудка и в 12 – перстной кишке. [
III. После отмены НПВП клинические симптомы и изменения в гастродуоденальной СО обычно купируются, если они не ассоциированы с HP – инфекцией. В заключении этого вопроса, еще раз хочется подчеркнуть основное положение: синдром НПВП – гастродуоденопатии лишь отчасти связан с локальным повреждающим влиянием НПВП на слизистую, а в основном обусловлен системным действием препарата. Поэтому гастротоксичность может иметь место при парентеральном или ректальном введении НПВП.
- I. Основные причины зрозивно-язвенного поражения желудочно кишечного тракта
- При обширных ожогах (язвы Курлинга);
- При поражении ЦНС (язвы Кушинга);
- При стрессе;
- В результате приема лекарств (ацетилсалициловая кислота, индометацин и др.), алкоголя и других токсических веществ;
- У больных пожилого возраста («старческие язвы»);
- При заболеваниях внутренних органов (легкие, сердце, печень, почки);
- При заболеваниях эндокринных желез и т.д.
 Патогенез НПВП – гастропатии
1. Как известно, НПВП ингибируют активность фермента циклооксигеназы (ЦОГ), имеющего два изомера ЦОГ-1 и ЦОГ-2. Угнетение активности ЦОГ-2 собственно и определяет противовоспалительное действие, угнетение активности ЦОГ-1 приводит к снижению синтеза простагладинов и простациклина в слизистой оболочке желудка. Функция простагладинов по отношению к гастродуоденальной слизистой оболочке является протективной. В эксперименте показано, что экзогенно введенные простагладины способствуют устойчивости слизистой оболочки к таким повреждающим агентам, как этанол, желчные кислоты, растворы кислот и солей, а также НПВП. Спектр основных физиологических эффектов простагландинов включает:
Патогенез НПВП – гастропатии
1. Как известно, НПВП ингибируют активность фермента циклооксигеназы (ЦОГ), имеющего два изомера ЦОГ-1 и ЦОГ-2. Угнетение активности ЦОГ-2 собственно и определяет противовоспалительное действие, угнетение активности ЦОГ-1 приводит к снижению синтеза простагладинов и простациклина в слизистой оболочке желудка. Функция простагладинов по отношению к гастродуоденальной слизистой оболочке является протективной. В эксперименте показано, что экзогенно введенные простагладины способствуют устойчивости слизистой оболочки к таким повреждающим агентам, как этанол, желчные кислоты, растворы кислот и солей, а также НПВП. Спектр основных физиологических эффектов простагландинов включает:
- стимуляцию секреции защитных гидрокарбонатов и слизи;
- усиление местного кровотока слизистой оболочки;
- активизацию пролиферации клеток в процессах нормальной регенерации.
Клиника и морфология
I. 1. Клинически НПВП – гастропатии проявляются тошнотой, иногда рвотой, чувством тяжести и болью в эпигастрии, вздутием живота, анорексией и другими диспептическими расстройствами. 2. В основном различают три вида поражений СОЖ и СОДПК, являющихся как бы последовательными стадиями одного патологического процесса: кровоизлияния в СО, варьирующие от мелких петехий до обширных участков, эрозии, язвы. Нередко у одного больного обнаруживаются все эти элементы одновременно. Острые язвы и эрозии чаще локализуются в области дна и тела желудка, гораздо реже в пилорическом отделе желудка и 12 – перстной кишке. Но все-таки, к наиболее тяжелым проявлениям гастропатии относят эрозивно-язвенные поражения СОЖ и СО 12-перстной кишки, причем частота образования язв желудке составляет в среднем 20%, в 12-перстной кишке – 10%. На фоне продолжающегося приема НПВП гастродуоденальные изъязвления в 40% случаев осложняются кровотечением. II. Между язвами, вызванными приемом НПВП, и спонтанно возникшими существует определенная разница. Во-первых, язвы, вызванные приемом НПВП, чаще всего бывают бессимптомными (у 60% больных, особенно пожилых), и диагноз во многих случаях устанавливают при фиброгастродуоденоскопии. Во-вторых, слизистая оболочка желудка приспосабливается к длительному воздействию кислот (НПВП), в связи с чем после 2-8 недель приема медикамента острота поражения несколько уменьшается. Ряд экспериментов показал, что наиболее опасными могут считаться первые недели приема НПВП. Эндоскопическое обследование, проведенное у пациентов, применявших непрерывную терапию НПВП на протяжении 6 месяцев, показало, что только у 32% пациентов слизистая желудка остается в норме. У оставшихся 68% выявляются патологические изменения слизистой. Гистологически слизистая вокруг язвы, вызванной НПВП, обычно нормальная или только слегка воспалена в отличие от хронического гастрита при типичных хронических язвах желудка.
II. Между язвами, вызванными приемом НПВП, и спонтанно возникшими существует определенная разница. Во-первых, язвы, вызванные приемом НПВП, чаще всего бывают бессимптомными (у 60% больных, особенно пожилых), и диагноз во многих случаях устанавливают при фиброгастродуоденоскопии. Во-вторых, слизистая оболочка желудка приспосабливается к длительному воздействию кислот (НПВП), в связи с чем после 2-8 недель приема медикамента острота поражения несколько уменьшается. Ряд экспериментов показал, что наиболее опасными могут считаться первые недели приема НПВП. Эндоскопическое обследование, проведенное у пациентов, применявших непрерывную терапию НПВП на протяжении 6 месяцев, показало, что только у 32% пациентов слизистая желудка остается в норме. У оставшихся 68% выявляются патологические изменения слизистой. Гистологически слизистая вокруг язвы, вызванной НПВП, обычно нормальная или только слегка воспалена в отличие от хронического гастрита при типичных хронических язвах желудка.
 Факторы риска
Факторы риска
- Более высокому риску развития осложнений от приема НПВП подвержены:
- больные старшего возраста (старше 65 лет);
- больные, имеющие язвенную болезнь в анамнезе;
- больные с сопутствующими заболеваниями, особенно сердечно-сосудистой системы;
- курящие и употребляющие алкоголь.
 II. Предполагается, что у разных противовоспалительных препаратов разный «повреждающий» потенциал.
1. Кроме того, частота возникновения гастро- и дуоденопатий, желудочных и дуоденальных кровотечений зависит от используемого препарата, продолжительности приема и некоторых других факторов.
Сравнительный риск возникновения эрозивно-язвенных поражений при приеме различных НПВП: данные метаанализа.
(Garsia Rodrigues L.A., 1998).
II. Предполагается, что у разных противовоспалительных препаратов разный «повреждающий» потенциал.
1. Кроме того, частота возникновения гастро- и дуоденопатий, желудочных и дуоденальных кровотечений зависит от используемого препарата, продолжительности приема и некоторых других факторов.
Сравнительный риск возникновения эрозивно-язвенных поражений при приеме различных НПВП: данные метаанализа.
(Garsia Rodrigues L.A., 1998).
ПРЕПАРАТ |
Число работ, взятых для метаанализа | Относительный риск (М + m) |
| Ибупрофен | 11 | 1,0 + 0 |
| Диклофенак | 8 | 2,3 + 0,5 |
| Дифлунизал | 2 | 3,5 + 0,5 |
| Фенопрофен | 2 | 3,5 + 1,2 |
| Аспирин | 6 | 4,8 + 0,5 |
| Сулидак | 5 | 6,0 + 0 |
| Напроксен | 10 | 7,0 + 0 |
| Индометацин | 11 | 8,0 + 0 |
| Пироксикам | 10 | 9,0 + 0 |
| Кетопрофен | 7 | 10,3 + 0,5 |
| Толметин | 2 | 11,0 + 0,9 |
| Азапропазон | 2 | 11,7 + 0,5 |
| Препарат |
Число больных |
Индекс токсичности |
|
| Салсалат | 187 | 0,81 + 0,51 | |
| Ибупрофен | 577 | 1,13 + 0,29 | |
| Аспирин | 1521 | 1,18 + 0,18 | |
| Сулидак | 562 | 1,68 + 0,29 | |
| Диклофенак | 415 | 1,81 + 0,35 | |
| Напроксен | 1062 | 1,91 + 0,21 | |
| Толметин | 243 | 2,02 + 0,44 | |
| Пироксикам | 814 | 2,03 + 0,24 | |
| Фенопрофен | 158 | 2,35 + 0,55 | |
| Индометацин | 418 | 2,39 + 0,34 | |
| Кетопрофен | 259 | 2,65 + 0,43 | |
| Меклофеномат | 165 | 3,91 + 0,54 | |


