Просмотров: 28 567
ОБЩИЕ ПРИНЦИПЫ ТЕРАПИИ СИСТЕМНЫХ ВАСКУЛИТОВ
Ирина Александровна Зборовская – директор Федерального бюджетного государственного учреждения “Научно-исследовательский институт клинической и экспериментальной ревматологии” РАМН, профессор кафедры госпитальной терапии с курсом клинической ревматологии факультета усовершенствования врачей Волгоградского государственного медицинского университета, д.м.н.
Можно выделить несколько основных этапов в лечении системных васкулитов.
 Цель первого этапа – максимально быстро, до развития необратимых ишемических, некротических изменений в органах и тканях, добиться подавления иммунного воспаления, что предполагает:
Цель первого этапа – максимально быстро, до развития необратимых ишемических, некротических изменений в органах и тканях, добиться подавления иммунного воспаления, что предполагает:
 В настоящее время ГК широко используются для лечения васкулитов. Они назначаются практически при всех их формах.
1) Монотерапия ГК.
Монотерапия ГК является основным методом лечения некоторых васкулитов ГКА (гиганто-клеточного артериита), реже – артериита Такаясу и некоторых некротизирующих васкулитов с локальным поражением сосудов и отсутствием признаков прогрессирования заболевания. Тяжелые абдоминальные формы геморрагического васкулита служат показанием для назначения преднизолона. Полагают, что при этом заболевании лечение ГК позволяет предотвратить последующие поражения почек. Однако другие авторы не разделяют этого мнения. ГК используются как системно, так и местно, в виде мазей и кремов для лечения язв полости рта и половых органов. Обычно доза преднизолона при системных васкулитах колеблется 1-2 мг/кг (в несколько приемов). Более высокие дозировки препарата применяются при ГКА, синдроме Черджа – Стросса, классическом УП, чем при болезни Бехчета, артериите Такаясу, геморрагическом васкулите и гранулематозе Вегенера. При положительном эффекте переходят на однократный прием утром.
Длительность подавляющей терапии ГК составляет 3-4 недели, затем проводится постепенное (2-3 месяца) снижение их дозы до поддерживающей (0,15 – 0,2 мг/кг/сутки), которая назначается от одного года до трех – пяти лет.
Возможен другой вариант терапии ГК-ми.
2) Альтернирующая терапия
Альтернирующая терапия ГК – метод лечения, заключающийся в назначении ГК короткого действия без выраженной минерало-кортикоидной активности (преднизон, преднизолон, метилпреднизолон) однократно, утром каждые 48 часов. Целью альтернирующей терапии является уменьшение побочных реакций ГК при сохранении их терапевтической эффективности.
Полагают, что этот метод лечения показан больным, которые длительно (более нескольких недель) принимают ГК. Его не следует применять при кратковременном использовании этих препаратов, а также в начальной стадии лечения или в период обострения заболевания.
Однако при системных васкулитах такая тактика лечения, как правило, неэффективна. Полагают, что при этих заболеваниях альтернирующий прием ГК предпочтителен только для поддерживающей терапии.
3) Пульс-терапия
По данным многих исследований, на фоне пульс терапии быстрое улучшение наблюдается у 75% больных с активным волчаночным нефритом, поражением ЦНС, пневмонитом, полисерозитом, васкулитом, тромбоцитопенией (см. приложение к лекциям).
Табл. Показания к проведению пульс – терапии глюкокортикоидами при системных васкулитах
В настоящее время ГК широко используются для лечения васкулитов. Они назначаются практически при всех их формах.
1) Монотерапия ГК.
Монотерапия ГК является основным методом лечения некоторых васкулитов ГКА (гиганто-клеточного артериита), реже – артериита Такаясу и некоторых некротизирующих васкулитов с локальным поражением сосудов и отсутствием признаков прогрессирования заболевания. Тяжелые абдоминальные формы геморрагического васкулита служат показанием для назначения преднизолона. Полагают, что при этом заболевании лечение ГК позволяет предотвратить последующие поражения почек. Однако другие авторы не разделяют этого мнения. ГК используются как системно, так и местно, в виде мазей и кремов для лечения язв полости рта и половых органов. Обычно доза преднизолона при системных васкулитах колеблется 1-2 мг/кг (в несколько приемов). Более высокие дозировки препарата применяются при ГКА, синдроме Черджа – Стросса, классическом УП, чем при болезни Бехчета, артериите Такаясу, геморрагическом васкулите и гранулематозе Вегенера. При положительном эффекте переходят на однократный прием утром.
Длительность подавляющей терапии ГК составляет 3-4 недели, затем проводится постепенное (2-3 месяца) снижение их дозы до поддерживающей (0,15 – 0,2 мг/кг/сутки), которая назначается от одного года до трех – пяти лет.
Возможен другой вариант терапии ГК-ми.
2) Альтернирующая терапия
Альтернирующая терапия ГК – метод лечения, заключающийся в назначении ГК короткого действия без выраженной минерало-кортикоидной активности (преднизон, преднизолон, метилпреднизолон) однократно, утром каждые 48 часов. Целью альтернирующей терапии является уменьшение побочных реакций ГК при сохранении их терапевтической эффективности.
Полагают, что этот метод лечения показан больным, которые длительно (более нескольких недель) принимают ГК. Его не следует применять при кратковременном использовании этих препаратов, а также в начальной стадии лечения или в период обострения заболевания.
Однако при системных васкулитах такая тактика лечения, как правило, неэффективна. Полагают, что при этих заболеваниях альтернирующий прием ГК предпочтителен только для поддерживающей терапии.
3) Пульс-терапия
По данным многих исследований, на фоне пульс терапии быстрое улучшение наблюдается у 75% больных с активным волчаночным нефритом, поражением ЦНС, пневмонитом, полисерозитом, васкулитом, тромбоцитопенией (см. приложение к лекциям).
Табл. Показания к проведению пульс – терапии глюкокортикоидами при системных васкулитах
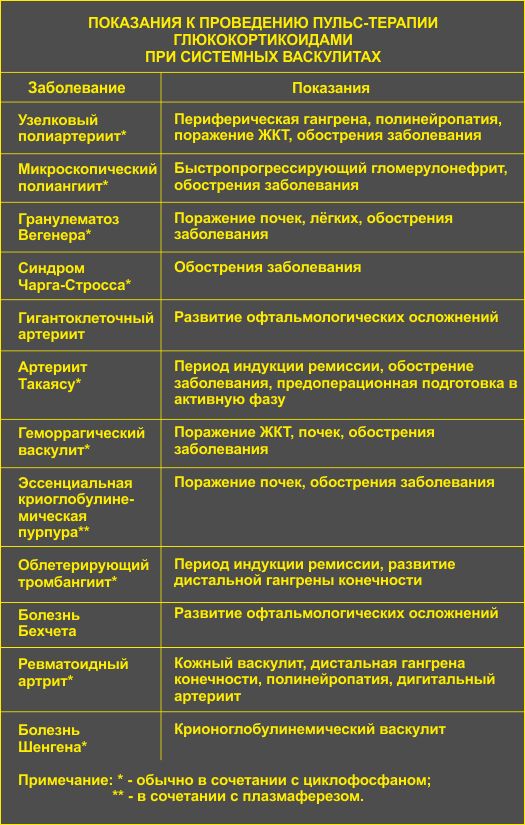 В настоящее время при системных васкулитах подавление активности заболевания предусматривает более раннее назначение пульс – терапии. Полагают, что одним из преимуществ пульс – терапии при этих заболеваниях является возможность более быстрого перевода больного на поддерживающую дозу ГК. Предварительные результаты свидетельствуют также о том, что повторные процедуры (1-3 дня в месяц) пульс-терапии являются альтернативой назначения цитостатиков.
Табл. Схема назначения высоких доз циклофосфана и метилпреднизолона в виде пульс – терапии для лечения системных васкулитов
В настоящее время при системных васкулитах подавление активности заболевания предусматривает более раннее назначение пульс – терапии. Полагают, что одним из преимуществ пульс – терапии при этих заболеваниях является возможность более быстрого перевода больного на поддерживающую дозу ГК. Предварительные результаты свидетельствуют также о том, что повторные процедуры (1-3 дня в месяц) пульс-терапии являются альтернативой назначения цитостатиков.
Табл. Схема назначения высоких доз циклофосфана и метилпреднизолона в виде пульс – терапии для лечения системных васкулитов
 При гранулематозе Вегенера, МПА (микроскопический полиангиит), УП, СКВ, ревматоидном васкулите пульс – терапию проводят ежемесячно в течение 9-24 мес. подряд (т.е проводят повторные курсы).
По данным Института ревматологии, при артериите Такаясу предпочтительнее повторные курсы пульс-терапии 1 раз в месяц в сроки от 7 до 12 мес.
Наиболее часто для проведения пульс-терапии используют метилпреднизолон в виде раствора гемисукцината натрия.
В последнее время с этой целью стали использовать дексаметазон (в частности – препарат дексавен 2 мг/кг в сутки), который в 7 раз активнее, чем преднизолон. Препарат оказывает выраженное противовоспалительное действие, не задерживает ионов Na+ в организме и слабо влияет на выделение ионов К+. Период его полувыведения составляет 36-54 часа, в то время как для метилпреднизолона он колеблется от 12 до 36 часов.
Имеются сообщения о высокой эффективности пульс – терапии дексаметазоном у больных резистентной тромбоцитопенической пурпурой.
Хороший клинико-лабораторный эффект был достигнут при назначении в качестве пульс-терапии для лечения СКВ и РА препарата дексавена – натриевой соли фосфата дексаметазона в дозировке 2 мг/кг/сут. Было доказано, что препарат дексавен, применяемый в качестве пульс-терапии, обладает выраженным противовоспалительным действием. Он также является эффективным корректором процессов гемостаза. Последнее достигается, по-видимому, за счет подавления иммунопатологических процессов, инициирующих свертывание крови.
Однако, результаты клинических исследований свидетельствуют о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым быстропрогрессирующим поражением сосудов мелкого калибра.
Необходимо подчеркнуть, что у больных системными некротизирующими васкулитами, а также при тяжелых формах геморрагического васкулита и синдрома Черджа-Стросса, у которых наблюдается тяжелое быстропрогрессирующее поражение сосудов и почек, даже несмотря на хороший начальный клинический ответ на глюкокортикостероиды, введение высоких доз ГК обязательно должно сочетаться с активной цитостатической терапией, в первую очередь циклофосфамидом, так как только такая комбинированная терапия позволяет реально улучшить прогноз заболевания.
2. Цитотоксические препараты.
Для лечения системных васкулитов используются цитотоксические препараты трех основных классов: алкилирующие агенты (циклофосфамид), пуриновые аналоги (азатиоприн) антагонисты фолиевой кислоты (метотрексат). Последние в низких дозах не обладают явной цитотоксической активностью.
1) Циклофосфамид применяется для лечения васкулитов уже более 25 лет. ЦФ воздействует на различные звенья патогенеза васкулитов (см. приложение).
Табл. Основные механизмы действия циклофосфана при васкулитах
При гранулематозе Вегенера, МПА (микроскопический полиангиит), УП, СКВ, ревматоидном васкулите пульс – терапию проводят ежемесячно в течение 9-24 мес. подряд (т.е проводят повторные курсы).
По данным Института ревматологии, при артериите Такаясу предпочтительнее повторные курсы пульс-терапии 1 раз в месяц в сроки от 7 до 12 мес.
Наиболее часто для проведения пульс-терапии используют метилпреднизолон в виде раствора гемисукцината натрия.
В последнее время с этой целью стали использовать дексаметазон (в частности – препарат дексавен 2 мг/кг в сутки), который в 7 раз активнее, чем преднизолон. Препарат оказывает выраженное противовоспалительное действие, не задерживает ионов Na+ в организме и слабо влияет на выделение ионов К+. Период его полувыведения составляет 36-54 часа, в то время как для метилпреднизолона он колеблется от 12 до 36 часов.
Имеются сообщения о высокой эффективности пульс – терапии дексаметазоном у больных резистентной тромбоцитопенической пурпурой.
Хороший клинико-лабораторный эффект был достигнут при назначении в качестве пульс-терапии для лечения СКВ и РА препарата дексавена – натриевой соли фосфата дексаметазона в дозировке 2 мг/кг/сут. Было доказано, что препарат дексавен, применяемый в качестве пульс-терапии, обладает выраженным противовоспалительным действием. Он также является эффективным корректором процессов гемостаза. Последнее достигается, по-видимому, за счет подавления иммунопатологических процессов, инициирующих свертывание крови.
Однако, результаты клинических исследований свидетельствуют о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым быстропрогрессирующим поражением сосудов мелкого калибра.
Необходимо подчеркнуть, что у больных системными некротизирующими васкулитами, а также при тяжелых формах геморрагического васкулита и синдрома Черджа-Стросса, у которых наблюдается тяжелое быстропрогрессирующее поражение сосудов и почек, даже несмотря на хороший начальный клинический ответ на глюкокортикостероиды, введение высоких доз ГК обязательно должно сочетаться с активной цитостатической терапией, в первую очередь циклофосфамидом, так как только такая комбинированная терапия позволяет реально улучшить прогноз заболевания.
2. Цитотоксические препараты.
Для лечения системных васкулитов используются цитотоксические препараты трех основных классов: алкилирующие агенты (циклофосфамид), пуриновые аналоги (азатиоприн) антагонисты фолиевой кислоты (метотрексат). Последние в низких дозах не обладают явной цитотоксической активностью.
1) Циклофосфамид применяется для лечения васкулитов уже более 25 лет. ЦФ воздействует на различные звенья патогенеза васкулитов (см. приложение).
Табл. Основные механизмы действия циклофосфана при васкулитах
 а) ЦФ применяется для лечения некротизирующих васкулитов, прежде всего за счет влияния на клетки-медиаторы сосудистого повреждения.
Однако, наряду с иммуносупрессивной активностью, описано и иммуностимулирующее действие ЦФ, связанное, как полагают, с разной чувствительностью Т- и В-лимфоцитов к воздействию этого препарата. Его эффекты на систему иммунитета в определенной степени зависят от особенностей терапии. Установлено, что длительный постоянный прием низких доз ЦФ в большей степени вызывает депрессию клеточного иммунитета, а интермиттирующее введение высоких его доз в первую очередь подавляют его гуморальное звено.
ЦФ эффективное средство лечения некротизирующих васкулитов: гранулематоза Вегенера, УП и синдрома Черджа-Стросса.
б) Интермиттирующая пульс-терапия ЦФ рассматривается как наиболее эффективный метод лечения системного ревматоидного васкулита.
Препарат также назначают при артериите Такаясу, ГКА, облитерирующем тромбангиите (ОТА), болезни Бехчета, как правило, в виде пульс-терпаии в сочетании с ГК. При геморрагическом васкулите показанием для терапии ЦФ служит развитие быстропрогрессирующего гломерулонефрита.
в) Существуют две принципиальные схемы назначения ЦФ
– Пероральный прием в дозе 1-2 мг/кг/сут в течение 10-14 дней с последующим титрованием в зависимости от уровня лейкоцитов в периферической крови.
При очень быстром прогрессировании васкулита циклофосфамид назначают в дозе 4 мг/кг/сут в течение 3 дней, затем 2 мк/кг/сут в течение 7 дней. Общая длительность лечения циклофосфамидом составляет не менее 12 месяцев после достижения полной ремиссии. Затем дозу препарата постепенно снижают в течение 2-3 месяцев по 25-50 мг.
Особое значение имеет титрование дозы циклофосфамида, на фоне лечения которым концентрация лейкоцитов не должна быть ниже 3000- 3500 мм3, а нейтрофилов – 1000-1500/мм3. В начале лечения целесообразно мониторировать концентрацию лейкоцитов через день, а после стабилизации количества лейкоцитов — не реже 1 раза в 2 недели.
У пациентов с почечной недостаточностью (сывороточный креатинин более 2 мг%) доза циклофосфамида, должна быть снижена на 25-50°/
– Болюсное интермиттирующее внутривенное введение высоких доз (500-1000 мг/м2 в сутки или 10-15 мг/кг в сутки) в течение первых 4-6 мес. ежемесячно, а затем 1 раз в 3 мес.
Обычно лечение ЦФ сочетают с назначением умеренных или высоких доз ГК, включая пульс-терапию.
Превалирует мнение, что обе схемы лечения примерно равнозначны, но на фоне интермиттирующего внутривенного введения частота токсических реакций меньше, чем при постоянном приеме per os.
В то же время, имеются данные о том, что у больных гранулематозом Вегенера пульс-терапия и пероральный прием ЦФ в равной степени эффективны только в отношении ближайших результатов, но долгосрочную ремиссию заболевания удается достигнуть только при длительном ежедневном приеме препарата. Таким образом, пульс-терапия и длительный прием низких доз ЦФ имеют разный терапевтический профиль.
в) По мнению Т. Cupps в некоторых случаях применение низких доз ЦФ имеет преимущества перед интермитирующим введением высоких. Например, в фазу индукции риск супрессии костного мозга выше у больных, леченных пульс – терапией, чем у пациентов, получающих низкие дозы ЦФ. Полагают, что, поскольку истинное изменение количества лейкоцитов в периферической крови после пульс-терапии становится очевидным через 10-20 дней от начала лечения, постольку дозу ЦФ изменяют только в этот период. Напротив, при ежедневном приеме препарата его дозировку можно подбирать на основе мониторинга уровня лейкоцитов в периферической крови и функции почек. Таким образом, опасность появления токсических реакций в ранние сроки лечения высокими дозами ЦФ особенно велика у больных с нарушениями функции многих органов, быстрым прогрессированием почечной недостаточности; ишемией кишечника, а также у пациентов, получающих высокие ГК. Однако по данным R.A. Lugmani и соавт, супрессия костного мозга и инфекционные осложнения чаще встречаются при постоянном приеме ЦФ, чем при пульс-терапии.
– Частое осложнение, возникающее на фоне лечения ЦФ – геморрагический цистит. Он развивается почти у 30% больных. Его частота несколько меньше на фоне парентерального введения ЦФ, чем при приеме per os. Для профилактики геморрагического цистита рекомендуется прием препарата месна, который является детоксирующим агентом. Месна вводится внутривенно в дозе, составляющей 20% от дозы ЦФ, до приема последнего и через 4-8 часов после него.
Развитие тяжелого цистита является абсолютным показанием к отмене ЦФ. У больных с умеренным циститом возможно продолжение лечения меньшими дозами препарата под тщательным клиническим и инструментальным (цистоскопия) контролем.
– Другой побочный эффект ЦФ – нейтропения. Она является наиболее частым осложнением, ограничивающим возможность продолжения терапии. В начале лечения общий анализ крови следует поводить раз в 7-14 дней, а при стабилизации процесса и дозы препарата каждые 2-3 месяца. Препарат, отменяют, если количество лейкоцитов менее 3,5*109/л.
– Описаны больные с персистирующей гипогаммаглобулинемией. Этот побочный эффект ЦФ очень опасен, особенно в сочетании с нейтропенией, так как на его фоне значительно возрастает риск развития инфекционных осложнений. Необходимо иметь в виду, что у больных, получающих ЦФ, наблюдается увеличение чувствительности к инфекциям даже при нормальной концентрации нейтрофилов и иммуноглобулинов. При появлении инфекционных осложнений показано прекращение приема цитостатика.
– У больных, длительно принимающих ЦФ, повышен риск появления злокачественных новообразований. В литературе описано около 100 пациентов с СКВ, у которых развилась неходжкинская лимфома, и 13 случаев лимфогранулематоза. Обнаружено, что у больных СКВ уже в течение первых четырех лет от начала лечения этим препаратом умеренно нарастает частота рака влагалища и шейки матки.
– К частым токсическим осложнениям ЦФ относят тошноту, которая нередко делает невозможным проведение пульс – терапии этим препаратом. Для ее профилактики рекомендуется внутривенное введение метоклопрамида в дозе 1-3 мг/кг (максимальная доза 10 мг/кг) в 100 мл 0,9% раствора хлористого натрия за 15 минут до начала инфузии ЦФ в сочетании с седативными средствами (диазепам 5-10 мг).
– Алопеция чаще встречается на фоне приема высоких доз ЦФ, прерывание лечения ведет к нормализации роста волос.
– Олигоспермия или азооспермия у мужчин и олигоменорея или аменорея у женщин – почти обязательные побочные эффекты лечения ЦФ. Риск их развития повышается при длительном приеме препарата, назначении его высоких доз. Полагают, что проведение пульс – терапии ЦФ во время менструации позволяет снизить риск стерилизации.
2) Азатиоприн
а) В организме человека он метаболизируется в эритроцитах и печени с образованием биологически активных молекул и выводится через почки. В отличие от алкилирующих агентов, азатиоприн обладает цитостатической активностью.
Азатиоприн вызывает периферическую Т – и В – лимфопению. В высоких дозах он уменьшает уровень CD4+ Т – лимфоцитов, а при длительном приеме снижает синтез антител. Однако, поскольку Т-супрессоры особенно чувствительны к его действию, на фоне приема низких доз препарата может наблюдаться увеличение образования антител.
б) В настоящее время при васкулитах азатиоприн рассматривается как препарат второго ряда. Обычно он назначается после достижения ремиссии от приема ЦФ.
Оптимальная доза препарата составляет 1-3 мг/кг/сутки. В первые два месяца лечения азатиоприном необходимо каждые две недели проводить исследование общего анализа крови с обязательным определением количества тромбоцитов. В дальнейшем лабораторный контроль проводят один раз в 6-8 недель. Дозу препарата снижают на 50-75% у больных, получающих аллопуринол или имеющих почечную недостаточность. Поддерживающая доза азаиоприна обычно составляет 50 мг/день.
Комбинированная терапия азатиоприном и преднизолоном предотвращает прогрессирование сосудистого процесса у больных РА с васкулитом и при болезни Бехчета.
в) Наиболее часто на фоне лечения азатиоприном отмечается тошнота и рвота, выраженность которых снижается при приеме препарата с пищей и дробными дозами. Поражение печени встречается не более чем у 1% больных и, вероятно, связано с аллергической реакцией на него. Тем не менее, рекомендуется концентрацию билирубина и печеночных ферментов контролировать не реже, чем 1 раз в 3 месяца.
Лейкопения, обычно встречающаяся в начале лечения также, как полагают, связана с повышенной чувствительностью к этому лекарству. Однако в большинстве случаев появление цитопении отражает подавление костно-мозгового кроветворения. Общая частота цитопении может достигать 30%. При ее развитии азатиоприн отменяют до восстановления нормальных показателей крови, а затем продолжают его прием в меньших дозировках. Среди инфекционных осложнений часто встречается герпетическая инфекция, развитие которой не всегда коррелирует с выраженностью нейтропении. При лечении азатиоприном возможно развитие злокачественных новообразований. Полагают, что имеется генетически детерминированная предрасположенность к развитию токсических реакций на азатиоприн. Препарат противопоказан при беременности.
3) Метотрексат
Табл. Основные механизмы действия метотрексата при васкулитах.
а) ЦФ применяется для лечения некротизирующих васкулитов, прежде всего за счет влияния на клетки-медиаторы сосудистого повреждения.
Однако, наряду с иммуносупрессивной активностью, описано и иммуностимулирующее действие ЦФ, связанное, как полагают, с разной чувствительностью Т- и В-лимфоцитов к воздействию этого препарата. Его эффекты на систему иммунитета в определенной степени зависят от особенностей терапии. Установлено, что длительный постоянный прием низких доз ЦФ в большей степени вызывает депрессию клеточного иммунитета, а интермиттирующее введение высоких его доз в первую очередь подавляют его гуморальное звено.
ЦФ эффективное средство лечения некротизирующих васкулитов: гранулематоза Вегенера, УП и синдрома Черджа-Стросса.
б) Интермиттирующая пульс-терапия ЦФ рассматривается как наиболее эффективный метод лечения системного ревматоидного васкулита.
Препарат также назначают при артериите Такаясу, ГКА, облитерирующем тромбангиите (ОТА), болезни Бехчета, как правило, в виде пульс-терпаии в сочетании с ГК. При геморрагическом васкулите показанием для терапии ЦФ служит развитие быстропрогрессирующего гломерулонефрита.
в) Существуют две принципиальные схемы назначения ЦФ
– Пероральный прием в дозе 1-2 мг/кг/сут в течение 10-14 дней с последующим титрованием в зависимости от уровня лейкоцитов в периферической крови.
При очень быстром прогрессировании васкулита циклофосфамид назначают в дозе 4 мг/кг/сут в течение 3 дней, затем 2 мк/кг/сут в течение 7 дней. Общая длительность лечения циклофосфамидом составляет не менее 12 месяцев после достижения полной ремиссии. Затем дозу препарата постепенно снижают в течение 2-3 месяцев по 25-50 мг.
Особое значение имеет титрование дозы циклофосфамида, на фоне лечения которым концентрация лейкоцитов не должна быть ниже 3000- 3500 мм3, а нейтрофилов – 1000-1500/мм3. В начале лечения целесообразно мониторировать концентрацию лейкоцитов через день, а после стабилизации количества лейкоцитов — не реже 1 раза в 2 недели.
У пациентов с почечной недостаточностью (сывороточный креатинин более 2 мг%) доза циклофосфамида, должна быть снижена на 25-50°/
– Болюсное интермиттирующее внутривенное введение высоких доз (500-1000 мг/м2 в сутки или 10-15 мг/кг в сутки) в течение первых 4-6 мес. ежемесячно, а затем 1 раз в 3 мес.
Обычно лечение ЦФ сочетают с назначением умеренных или высоких доз ГК, включая пульс-терапию.
Превалирует мнение, что обе схемы лечения примерно равнозначны, но на фоне интермиттирующего внутривенного введения частота токсических реакций меньше, чем при постоянном приеме per os.
В то же время, имеются данные о том, что у больных гранулематозом Вегенера пульс-терапия и пероральный прием ЦФ в равной степени эффективны только в отношении ближайших результатов, но долгосрочную ремиссию заболевания удается достигнуть только при длительном ежедневном приеме препарата. Таким образом, пульс-терапия и длительный прием низких доз ЦФ имеют разный терапевтический профиль.
в) По мнению Т. Cupps в некоторых случаях применение низких доз ЦФ имеет преимущества перед интермитирующим введением высоких. Например, в фазу индукции риск супрессии костного мозга выше у больных, леченных пульс – терапией, чем у пациентов, получающих низкие дозы ЦФ. Полагают, что, поскольку истинное изменение количества лейкоцитов в периферической крови после пульс-терапии становится очевидным через 10-20 дней от начала лечения, постольку дозу ЦФ изменяют только в этот период. Напротив, при ежедневном приеме препарата его дозировку можно подбирать на основе мониторинга уровня лейкоцитов в периферической крови и функции почек. Таким образом, опасность появления токсических реакций в ранние сроки лечения высокими дозами ЦФ особенно велика у больных с нарушениями функции многих органов, быстрым прогрессированием почечной недостаточности; ишемией кишечника, а также у пациентов, получающих высокие ГК. Однако по данным R.A. Lugmani и соавт, супрессия костного мозга и инфекционные осложнения чаще встречаются при постоянном приеме ЦФ, чем при пульс-терапии.
– Частое осложнение, возникающее на фоне лечения ЦФ – геморрагический цистит. Он развивается почти у 30% больных. Его частота несколько меньше на фоне парентерального введения ЦФ, чем при приеме per os. Для профилактики геморрагического цистита рекомендуется прием препарата месна, который является детоксирующим агентом. Месна вводится внутривенно в дозе, составляющей 20% от дозы ЦФ, до приема последнего и через 4-8 часов после него.
Развитие тяжелого цистита является абсолютным показанием к отмене ЦФ. У больных с умеренным циститом возможно продолжение лечения меньшими дозами препарата под тщательным клиническим и инструментальным (цистоскопия) контролем.
– Другой побочный эффект ЦФ – нейтропения. Она является наиболее частым осложнением, ограничивающим возможность продолжения терапии. В начале лечения общий анализ крови следует поводить раз в 7-14 дней, а при стабилизации процесса и дозы препарата каждые 2-3 месяца. Препарат, отменяют, если количество лейкоцитов менее 3,5*109/л.
– Описаны больные с персистирующей гипогаммаглобулинемией. Этот побочный эффект ЦФ очень опасен, особенно в сочетании с нейтропенией, так как на его фоне значительно возрастает риск развития инфекционных осложнений. Необходимо иметь в виду, что у больных, получающих ЦФ, наблюдается увеличение чувствительности к инфекциям даже при нормальной концентрации нейтрофилов и иммуноглобулинов. При появлении инфекционных осложнений показано прекращение приема цитостатика.
– У больных, длительно принимающих ЦФ, повышен риск появления злокачественных новообразований. В литературе описано около 100 пациентов с СКВ, у которых развилась неходжкинская лимфома, и 13 случаев лимфогранулематоза. Обнаружено, что у больных СКВ уже в течение первых четырех лет от начала лечения этим препаратом умеренно нарастает частота рака влагалища и шейки матки.
– К частым токсическим осложнениям ЦФ относят тошноту, которая нередко делает невозможным проведение пульс – терапии этим препаратом. Для ее профилактики рекомендуется внутривенное введение метоклопрамида в дозе 1-3 мг/кг (максимальная доза 10 мг/кг) в 100 мл 0,9% раствора хлористого натрия за 15 минут до начала инфузии ЦФ в сочетании с седативными средствами (диазепам 5-10 мг).
– Алопеция чаще встречается на фоне приема высоких доз ЦФ, прерывание лечения ведет к нормализации роста волос.
– Олигоспермия или азооспермия у мужчин и олигоменорея или аменорея у женщин – почти обязательные побочные эффекты лечения ЦФ. Риск их развития повышается при длительном приеме препарата, назначении его высоких доз. Полагают, что проведение пульс – терапии ЦФ во время менструации позволяет снизить риск стерилизации.
2) Азатиоприн
а) В организме человека он метаболизируется в эритроцитах и печени с образованием биологически активных молекул и выводится через почки. В отличие от алкилирующих агентов, азатиоприн обладает цитостатической активностью.
Азатиоприн вызывает периферическую Т – и В – лимфопению. В высоких дозах он уменьшает уровень CD4+ Т – лимфоцитов, а при длительном приеме снижает синтез антител. Однако, поскольку Т-супрессоры особенно чувствительны к его действию, на фоне приема низких доз препарата может наблюдаться увеличение образования антител.
б) В настоящее время при васкулитах азатиоприн рассматривается как препарат второго ряда. Обычно он назначается после достижения ремиссии от приема ЦФ.
Оптимальная доза препарата составляет 1-3 мг/кг/сутки. В первые два месяца лечения азатиоприном необходимо каждые две недели проводить исследование общего анализа крови с обязательным определением количества тромбоцитов. В дальнейшем лабораторный контроль проводят один раз в 6-8 недель. Дозу препарата снижают на 50-75% у больных, получающих аллопуринол или имеющих почечную недостаточность. Поддерживающая доза азаиоприна обычно составляет 50 мг/день.
Комбинированная терапия азатиоприном и преднизолоном предотвращает прогрессирование сосудистого процесса у больных РА с васкулитом и при болезни Бехчета.
в) Наиболее часто на фоне лечения азатиоприном отмечается тошнота и рвота, выраженность которых снижается при приеме препарата с пищей и дробными дозами. Поражение печени встречается не более чем у 1% больных и, вероятно, связано с аллергической реакцией на него. Тем не менее, рекомендуется концентрацию билирубина и печеночных ферментов контролировать не реже, чем 1 раз в 3 месяца.
Лейкопения, обычно встречающаяся в начале лечения также, как полагают, связана с повышенной чувствительностью к этому лекарству. Однако в большинстве случаев появление цитопении отражает подавление костно-мозгового кроветворения. Общая частота цитопении может достигать 30%. При ее развитии азатиоприн отменяют до восстановления нормальных показателей крови, а затем продолжают его прием в меньших дозировках. Среди инфекционных осложнений часто встречается герпетическая инфекция, развитие которой не всегда коррелирует с выраженностью нейтропении. При лечении азатиоприном возможно развитие злокачественных новообразований. Полагают, что имеется генетически детерминированная предрасположенность к развитию токсических реакций на азатиоприн. Препарат противопоказан при беременности.
3) Метотрексат
Табл. Основные механизмы действия метотрексата при васкулитах.
 а) Метотрексат (MТ) относится к группе антиметаболитов, по структуре он близок фолиевой кислоте.
После приема МТ максимальная его концентрация в крови достигается через 2-4 часа. Прием препарата во время еды не влияет на уровень его абсорбции и биодоступности. Элиминация МТ происходит преимущественно в почках за счет клубочковой фильтрации и канальцевой секреции. Время полужизни препарата колеблется от 2 до 6 часов. Недостаточность функции почек приводит к замедлению экскреции МТ и увеличению его токсичности.
Несмотря на достаточно быстрое выведение из крови, полиглютаминовые метаболиты МТ обнаруживаются внутри клеток в течении 7 дней после его однократного приема. Основные механизмы действия этого препарата будут представлены ниже (см. приложение).
а) МТ назначают 3 раза в неделю (per оs или парентерально). Более частый прием препарата, как правило, приводит к увеличению числа острых или хронических токсических реакций. Рекомендуется принимать лекарство в утренние и вечерние часы, с двенадцатичасовым перерывом. Начальная доза МТ в большинстве случаев составляет 7,5 мг/неделю, а в пожилом возрасте 5 мг/неделю. Эффект от назначения препарата оценивается через 4-8 недель. В случае его отсутствия и при нормальной переносимости вещества дозу МТ постепенно увеличивают на 2,5 мг в неделю, максимально до 25 мг. Обычно при системных васкулитах доза этого препарата составляет 12,5-17,5 мг в неделю.
– При повышении дозы МТ оценка токсичности проводиться через 6 дней после приема препарата, а при достижении общего количества принятого препарата в 1500 мг показана биопсия печени. Парентеральное введение МТ используется при отсутствии эффекта от приема per os или при развитии токсических реакций со стороны желудочно-кишечного тракта. Необходимо иметь в виду, что в ряде случаев отсутствие эффекта при энтеральном введении МТ связано не столько с неэффективностью самого препарата, сколько с низкой абсорбцией его в желудочно-кишечном тракте, не позволяющей достичь оптимальной концентрации вещества в крови.
– В настоящее время изучается эффективность низких доз метотрексата (0,15 – 0,3 мг/кг/нед) в сочетании с высокими дозами преднизолона (1мг/кг/сут) у пациентов с кожной формой узелкового полиартериита и гранулематозом Вегенера без угрожающих жизни осложнений.
в) Побочные эффекты от применения МТ обычно включают тошноту и рвоту, которые появляются через 1-8 дней после начала приема препарата и длятся 1-3 дня. Для уменьшения выраженности этих явлений дозу МТ снижают, или вводят его парентерально. Рекомендуется также назначение симптоматических средств, например метоклопрамида. Относительным противопоказанием к применению МТ являются язвы желудка и двенадцатиперстной кишки. В 6% случаев причиной отмены препарата служит стоматит.
– Тяжелые гематологические нарушения развиваются нечасто. Риск гематологических осложнений повышается при почечной недостаточности, дефиците фолиевой кислоты и при сочетанном использовании МТ с салицилатами и препаратами, обладающими антифолатной активностью, особенно триметопримом/сульфаметоксазолом. Изредка встречается алопеция или кожный васкулит.
– Очень редким осложнением лечения МТ является пневмонит (1-8%), обусловленный аллергической реакцией на этот препарат. Он описан исключительно у больных РА.
– Транзиторное увеличение, уровня трансаминаз, нарастающее при повышении дозы МТ, нередкий побочный эффект этого препарата. Двух-, трехкратное увеличение их концентрации не является основанием для его отмены, но более существенное их нарастание свидетельствует о необходимости снижения дозы препарата или прекращения лечения им.
– Лечение низкими дозами МТ может сопровождаться увеличением чувствительности к инфекционным осложнениям. Развитие инфекции является основанием для отмены МТ.
3. Внутривенный иммуноглобулин
1) В последнее время для лечения васкулитов применяют иммуноглобулин, вводимый внутривенно. Этот препарат используется в клинической практике для терапии аутоиммунных заболеваний в течение уже более 15 лет. Полагают, что терапевтическая эффективность применения ВВИГ при аутоиммунных заболеваниях и васкулитах опосредуется через следующие механизмы (см. приложение).
Схема применения ВВИГ в настоящее время не стандартизирована. Обычно его доза варьирует от 0,4 до 2 г/кг/сутки. Препарат вводится внутривенно в течение 3-5 дней. При необходимости его инфузии повторяют 1 раз каждые 4 недели.
2) Терапия ВВИГ является относительно безопасным методом лечения, однако у отдельных больных развиваются побочные реакции. Наиболее часто они обусловлены высокой скоростью инфузии препарата. К ним относятся головные боли, лихорадка, ознобы, затруднения дыхания, боли в животе и спине, умеренная гипотензия. Для уменьшения выраженности этих реакций показано профилактическое назначение антигистаминных препаратов или небольших доз ГК. Истинные анафилактические реакции при введении ВВИГ встречаются довольно редко. Описано развитие симптомов, напоминающих асептический менингит и гемолитическую анемию, связанную с присутствием агглютининов в препарате ВВИГ. Кроме того, потенциальную опасность представляет трансмиссия инфекционных агентов. Но это наблюдается крайне редко.
3) При системных васкулитах ВВИГ является препаратом выбора для лечения болезни Кавасаки. В многочисленных исследованиях показано, что его применение приводит к достоверному снижению частоты развития аневризм коронарных артерий и быстрому исчезновению других признаков системного воспаления. Полагают, что его однократное введение в дозе 2 г/кг/сут не уступает по эффективности стандартному курсу лечения, который проводится в течение четырех дней в дозе 0,4 г/кг/сут.
ВВИГ также применяется в терапии гранулематоза Вегенера и МПА (микроскопического полиангиита).
По мнению K. Pirner и соавт ВВИГ, учитывая механизм действия, можно использовать в тех случаях, когда не показаны цитостатические препараты: при инфекционных осложнениях, беременности, до и после хирургического вмешательства.
ВВИГ эффективен при СКВ у больных с тяжелым поражением ЦНС, выраженной тромбоцитопенией, распространенным поражением кожи и слизистых, торпидных к ударным дозам стероидов.
4) Однако, последние данные, касающиеся эффективности внутривенного иммуноглобулина при других формах системных васкулитов, противоречивы. В единственном проспективном двойном слепом плацебо-контролируемом исследовании однократное введение внутривенного иммуноглобулина больным гранулематозом Вегенера и микроскопическим полиартериитом с сохраняющейся клинической активностью, несмотря на двухмесячное лечение глюкокортикоидами и цитотоксиками, привело к достоверному улучшению клинических и лабораторных показателей. Однако положительная динамика сохранялась только в течение 3-х месяцев, после чего различия между основной и контрольной группами нивелировалась. Таким образом, эффективность внутривенного иммуноглобулина (в первую очередь, повторных курсов) при системных васкулитах требует дальнейшего подтверждения.
Табл. Механизмы действия внутривенного иммуноглобулина (ВВИГ)
а) Метотрексат (MТ) относится к группе антиметаболитов, по структуре он близок фолиевой кислоте.
После приема МТ максимальная его концентрация в крови достигается через 2-4 часа. Прием препарата во время еды не влияет на уровень его абсорбции и биодоступности. Элиминация МТ происходит преимущественно в почках за счет клубочковой фильтрации и канальцевой секреции. Время полужизни препарата колеблется от 2 до 6 часов. Недостаточность функции почек приводит к замедлению экскреции МТ и увеличению его токсичности.
Несмотря на достаточно быстрое выведение из крови, полиглютаминовые метаболиты МТ обнаруживаются внутри клеток в течении 7 дней после его однократного приема. Основные механизмы действия этого препарата будут представлены ниже (см. приложение).
а) МТ назначают 3 раза в неделю (per оs или парентерально). Более частый прием препарата, как правило, приводит к увеличению числа острых или хронических токсических реакций. Рекомендуется принимать лекарство в утренние и вечерние часы, с двенадцатичасовым перерывом. Начальная доза МТ в большинстве случаев составляет 7,5 мг/неделю, а в пожилом возрасте 5 мг/неделю. Эффект от назначения препарата оценивается через 4-8 недель. В случае его отсутствия и при нормальной переносимости вещества дозу МТ постепенно увеличивают на 2,5 мг в неделю, максимально до 25 мг. Обычно при системных васкулитах доза этого препарата составляет 12,5-17,5 мг в неделю.
– При повышении дозы МТ оценка токсичности проводиться через 6 дней после приема препарата, а при достижении общего количества принятого препарата в 1500 мг показана биопсия печени. Парентеральное введение МТ используется при отсутствии эффекта от приема per os или при развитии токсических реакций со стороны желудочно-кишечного тракта. Необходимо иметь в виду, что в ряде случаев отсутствие эффекта при энтеральном введении МТ связано не столько с неэффективностью самого препарата, сколько с низкой абсорбцией его в желудочно-кишечном тракте, не позволяющей достичь оптимальной концентрации вещества в крови.
– В настоящее время изучается эффективность низких доз метотрексата (0,15 – 0,3 мг/кг/нед) в сочетании с высокими дозами преднизолона (1мг/кг/сут) у пациентов с кожной формой узелкового полиартериита и гранулематозом Вегенера без угрожающих жизни осложнений.
в) Побочные эффекты от применения МТ обычно включают тошноту и рвоту, которые появляются через 1-8 дней после начала приема препарата и длятся 1-3 дня. Для уменьшения выраженности этих явлений дозу МТ снижают, или вводят его парентерально. Рекомендуется также назначение симптоматических средств, например метоклопрамида. Относительным противопоказанием к применению МТ являются язвы желудка и двенадцатиперстной кишки. В 6% случаев причиной отмены препарата служит стоматит.
– Тяжелые гематологические нарушения развиваются нечасто. Риск гематологических осложнений повышается при почечной недостаточности, дефиците фолиевой кислоты и при сочетанном использовании МТ с салицилатами и препаратами, обладающими антифолатной активностью, особенно триметопримом/сульфаметоксазолом. Изредка встречается алопеция или кожный васкулит.
– Очень редким осложнением лечения МТ является пневмонит (1-8%), обусловленный аллергической реакцией на этот препарат. Он описан исключительно у больных РА.
– Транзиторное увеличение, уровня трансаминаз, нарастающее при повышении дозы МТ, нередкий побочный эффект этого препарата. Двух-, трехкратное увеличение их концентрации не является основанием для его отмены, но более существенное их нарастание свидетельствует о необходимости снижения дозы препарата или прекращения лечения им.
– Лечение низкими дозами МТ может сопровождаться увеличением чувствительности к инфекционным осложнениям. Развитие инфекции является основанием для отмены МТ.
3. Внутривенный иммуноглобулин
1) В последнее время для лечения васкулитов применяют иммуноглобулин, вводимый внутривенно. Этот препарат используется в клинической практике для терапии аутоиммунных заболеваний в течение уже более 15 лет. Полагают, что терапевтическая эффективность применения ВВИГ при аутоиммунных заболеваниях и васкулитах опосредуется через следующие механизмы (см. приложение).
Схема применения ВВИГ в настоящее время не стандартизирована. Обычно его доза варьирует от 0,4 до 2 г/кг/сутки. Препарат вводится внутривенно в течение 3-5 дней. При необходимости его инфузии повторяют 1 раз каждые 4 недели.
2) Терапия ВВИГ является относительно безопасным методом лечения, однако у отдельных больных развиваются побочные реакции. Наиболее часто они обусловлены высокой скоростью инфузии препарата. К ним относятся головные боли, лихорадка, ознобы, затруднения дыхания, боли в животе и спине, умеренная гипотензия. Для уменьшения выраженности этих реакций показано профилактическое назначение антигистаминных препаратов или небольших доз ГК. Истинные анафилактические реакции при введении ВВИГ встречаются довольно редко. Описано развитие симптомов, напоминающих асептический менингит и гемолитическую анемию, связанную с присутствием агглютининов в препарате ВВИГ. Кроме того, потенциальную опасность представляет трансмиссия инфекционных агентов. Но это наблюдается крайне редко.
3) При системных васкулитах ВВИГ является препаратом выбора для лечения болезни Кавасаки. В многочисленных исследованиях показано, что его применение приводит к достоверному снижению частоты развития аневризм коронарных артерий и быстрому исчезновению других признаков системного воспаления. Полагают, что его однократное введение в дозе 2 г/кг/сут не уступает по эффективности стандартному курсу лечения, который проводится в течение четырех дней в дозе 0,4 г/кг/сут.
ВВИГ также применяется в терапии гранулематоза Вегенера и МПА (микроскопического полиангиита).
По мнению K. Pirner и соавт ВВИГ, учитывая механизм действия, можно использовать в тех случаях, когда не показаны цитостатические препараты: при инфекционных осложнениях, беременности, до и после хирургического вмешательства.
ВВИГ эффективен при СКВ у больных с тяжелым поражением ЦНС, выраженной тромбоцитопенией, распространенным поражением кожи и слизистых, торпидных к ударным дозам стероидов.
4) Однако, последние данные, касающиеся эффективности внутривенного иммуноглобулина при других формах системных васкулитов, противоречивы. В единственном проспективном двойном слепом плацебо-контролируемом исследовании однократное введение внутривенного иммуноглобулина больным гранулематозом Вегенера и микроскопическим полиартериитом с сохраняющейся клинической активностью, несмотря на двухмесячное лечение глюкокортикоидами и цитотоксиками, привело к достоверному улучшению клинических и лабораторных показателей. Однако положительная динамика сохранялась только в течение 3-х месяцев, после чего различия между основной и контрольной группами нивелировалась. Таким образом, эффективность внутривенного иммуноглобулина (в первую очередь, повторных курсов) при системных васкулитах требует дальнейшего подтверждения.
Табл. Механизмы действия внутривенного иммуноглобулина (ВВИГ)
 4. Плазмаферез
1) Его механизмы действия связаны с улучшением функциональной активности ретикулоэндотелиальной системы, удалением аутоантител, ЦИК и воспалительных медиаторов из кровяного русла (см. приложение).
2) Полагают, что проведение при СКВ наиболее оправдано у больных с криоглобулинемией, повышением вязкости крови, тромботической тромбоцитопейической пурпурой, тяжелым васкулитом, с резистентными к ГК и цитостатикам формами пролиферативного нефрита, а также аутоиммунной гемолитической анемией, АФС и геморрагическим волчаночным пневмонитом.
При системных васкулитах плазмаферез в сочетании с ГК применяют для лечения УП, ассоциированного с вирусом гепатита В; эссенциального криоглобулинемического васкулита, гранулематоза Вегенера.
По мнению многих авторов показанием к применению плазмафереза при системных васкулитах является острое, прогрессирующее течение заболеваний, проявляющееся быстропрогрессирующим нефритом и тяжелым васкулитом.
Сообщается об эффективности повторных процедур малообъемного плазмафереза при артериите Такаясу (750-1000 мл/сут).
3) Общая частота осложнений при проведении плазмафереза колеблется от 4,5 до 25%.
Табл. Рекомендации по применению плазмафереза
4. Плазмаферез
1) Его механизмы действия связаны с улучшением функциональной активности ретикулоэндотелиальной системы, удалением аутоантител, ЦИК и воспалительных медиаторов из кровяного русла (см. приложение).
2) Полагают, что проведение при СКВ наиболее оправдано у больных с криоглобулинемией, повышением вязкости крови, тромботической тромбоцитопейической пурпурой, тяжелым васкулитом, с резистентными к ГК и цитостатикам формами пролиферативного нефрита, а также аутоиммунной гемолитической анемией, АФС и геморрагическим волчаночным пневмонитом.
При системных васкулитах плазмаферез в сочетании с ГК применяют для лечения УП, ассоциированного с вирусом гепатита В; эссенциального криоглобулинемического васкулита, гранулематоза Вегенера.
По мнению многих авторов показанием к применению плазмафереза при системных васкулитах является острое, прогрессирующее течение заболеваний, проявляющееся быстропрогрессирующим нефритом и тяжелым васкулитом.
Сообщается об эффективности повторных процедур малообъемного плазмафереза при артериите Такаясу (750-1000 мл/сут).
3) Общая частота осложнений при проведении плазмафереза колеблется от 4,5 до 25%.
Табл. Рекомендации по применению плазмафереза
 Наиболее часто вртречается кардиогенный шок, анафилактические и цитратные реакции. Инфекционные осложнения встречаются крайне редко. Возможно развитие синдрома «рикошета» (удаление аутоантител стимулирует их синтез), который особенно часто наблюдается у больных с активным воспалительным процессом.
Итак, подводя итог вышесказанному, хочу подчеркнуть еще раз.
5. Комбинированная терапия системных васкулитов
Результаты клинических исследований свидетельствует о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым, быстропрогрессирующим поражением сосудов мелкого калибра. В этих случаях проводится комбинированная терапия ГК и ЦФ, включая пульс -терапию ими.
В настоящее время имеется тенденция к более раннему назначению этих групп препаратов (см. приложение).
Назначение ГК в сочетании с азатиоприном и МТ также позволяет добиться большего клинического эффекта, чем изолированное применение этих препаратов. Большинство исследователей предпочитают в начале использовать ЦФ, а азатиоприн применяют как препарат второго ряда при достижении ремиссии. У некоторых больных гранулематозом Вегенера назначение ГК и МТ рассматривается как альтернатива классической терапии, но эти препараты обычно применяют у пациентов без тяжелого поражения легких и почек или при непереносимости циклофосфамида.
Гиганто-клеточный артериит хорошо контролируется ГК. При этом заболевании ЦФ обычно назначают дополнительно, в виде пульс – терапии при офтальмонологических нарушениях. При ГКА не доказано преимущество комбинированной терапии ГК и МТ над изолированным применением преднизолона. У большинства больных артериитом Такаясу наблюдается положительная динамика при монотерапии ГК. Однако часть из них стероидорезистентна: В этих случаях к преднизолону добавляют метотрексат или проводят пульс – терапию ГК и ЦФ. Применение пульс – терапии ГК и ЦФ или per os также показано при быстро прогрессирующем облитерирующем тромбангиите до развития полной облитерации магистральных артерий нижних или верхних конечностей.
В ряде случаев введение преднизолона и ЦФ комбинируют с процедурами плазмафереза. Такая тактика предпочтительнее для ведения больных при фульминантном течении васкулита, сопровождающемся нарушением функции жизненно важных органов, и при артериите Такаясу.
При УП, ассоциированном с вирусом гепатита В, как у взрослых так и у детей показано назначение противовирусных препаратов и преднизолона в средних дозах в сочетании с повторными процедурами плазмафереза.
6. Пульс – синхронизация
В настоящее время разработана схема, получившая название «пульс – синхронизация», которая, как полагают, способствует увеличению эффективности цитотоксической терапии. Суть этого метода заключается в отмене на четыре недели поддерживающей терапии ГК и цитотоксическими препаратами, что вызывает стимуляцию пролиферации лимфоидных клеток и развитие синдрома «рикошета». Последний купируется тремя циклами интенсивного плазмафереза и высокими дозами ЦФ. Предполагается, что такое лечение позволяет добиться более эффективной элиминации патологических клонов клеток, синтезирующих аутоантитела.
С.К. Соловьев и В. А. Насонова сформулировали принципы применения синхронной интенсивной терапии с последовательным назначением экстракорпоральных процедур плазмафереза или гемосорбции и ударных доз метилпреднизолона и ЦФ для лечения СКВ. Аналогичная схема используется и педиатрами при острых и молниеносных формах УП. Однако для других форм васкулитов «пульс – синхронизация» еще не разработана. Что касается ВВИГ в комбинации с ГК, то он с успехом применяется при гранулематозе Вегенера и некоторых других васкулитах.
Большинство авторов в комбинированную терапию васкулитов рекомендуют включать и другие препараты, влияющие на реологические свойства крови (гепарин, фраксипарин), дезагреганты (пентоксифиллин, тиклид, аспирин), препараты простагландина Е, (вазапростан) и простациклина (илопрост), а также периферические вазодилататоры. Важной составляющей терапии васкулитов является профилактика развития инфекции и поражения ЖКТ. Кроме того, учитывая увеличение продолжительности жизни больных васкулитами и возможности развития у них раннего атеросклероза, СС осложнений, необходимо в целях профилактики назначать препараты, обладающие противовоспалительным, антитромботическим и гиподемическим действием (плаквенил, делагин, аспирин, пентоксифиллин).
Итак, другие препараты и методы лечения.
7. Пентоксифилин
Пентоксифилин (трентал) – ингиботор ксантиновой фосфодиэстеразы, который улучшает доставку кислорода к тканям при перифирических сосудистых заболеваниях человека.
Этот препарат широко применяется для лечения системных васкулитов, особенно при вазоспастическом и ишемическом синдромах, поражениях кожи и почек. В настоящее время получены клинические и экспериментальные факты, свидетельствующие о его противовоспалительном иммуномодулирующем эффекте, снижение нефротоксичности и потенцирование эффекта ЦСА, а также усиление противовоспалительного действия метотрексата. Является важным дополнением к терапии ГК и ЦФ. Некоторые рассматривают его как базисный препарат для лечения геморрагического васкулита.
Лечение пентоксифиллином обычно начинают с внутривенных капельных инфузий по 200-300 мг/сутки в 200 мл физиологического раствора. Курс лечения состоит из 10 – 15 инъекций. Непосредственно после окончания инфузионной терапии переходят на пероральный прием препарата по 600-800 мг/сутки в течение 30-40 дней с последующим снижением дозы до 200-300 мг/сутки и ее приемом в течение длительного времени (6-12 мес).
Нередко внутривенное введение пентоксифиллина сочетают с реополиглюкином, который снижает вязкость крови, уменьшает агрегацию тромбоцитов и эритроцитов, а также обладает антитромботическим эффектом.
Е.Н. Семенкова и О.Г. Кривошееев при геморрагическом васкулите считают наиболее эффективным использование пентоксифиллина в дозе 1000-1200 мг/сутки в сочетании с дапсоном (100-200 мг/сутки).
8. Циклоспорин А
1) Наряду с имуносупрессивной активностью, ЦСА в фармакологических концентрациях проявляет определенные противовоспалительные эффекгы, ингибируя высвобождение гистамина, триптазы и синтез лейкотриенов базофилами и тучными клетками.
2) В начале лечения ЦСА назначают в дозе 2-3 мг/кг/сутки в 1 или 2 приема в течение 4-8 недель. При неэффективности препарата его дозу постепенно увеличивают на 0,5 – 1,0 мг/кг/сутки до максимальной 5 мг/кг/сутки. При стабилизации процесса в течение 3 месяцев рекомендуется очень медленное ее снижение (по 0,5 мг/кг за 1 месяц) до минимально эффективной. При отсутствии эффекта в течение 6 месяцев на фоне приема оптимально переносимой дозы препарата продолжение лечения нецелесообразно.
3) В процессе лечения особое внимание следует уделить динамике уровня креатинина в сыворотке, увеличение которого более чем на 30% от исходного диктует необходимость немедленного уменьшения дозы ЦСА. Препарат не следует назначать больным с нарушенной функцией почек, тяжелой артериальной гипертензией, инфекционными заболеваниями и злокачественными новообразованиями.
В то же время, на фоне лечения ЦСА наблюдается развитее некоторых специфических осложнений, наиболее тяжелым из которых является поражение почек.
ЦСА вызывает так называемую функциональную нефротоксичность, приводящую к увеличению концентрации креатинина и мочевины. Она связана с вазоконстрикцией афферентных артериол клубочков, ведущей к снижению почечного кровотока и четко коррелирует с дозой препарата, но обычно не сопровождается явными морфологическими нарушениями.
У 5-15 % больных ЦСА вызывает зависимое от дозы повышение диастолического артериального давления в среднем на 2-3 мм рт. ст. при дозе 2,5 мг/кг/сутки и на 5 мм рт. ст. при дозе 5 мг/кг/сугки.
Препаратами выбора при лечении артериальной гипертензии вызванной ЦСА, являются антагонисты Са: нифедипин или исрадипин, которые в отличие от дилтиазема и верапамила существенно не влияют на фармакокинетику ЦСА.
К другим побочным реакциям относятся гипертрихоз, гиперплазия слизистой полости рта, парастезии, тремор, желудочно-кишечные расстройства, умеренная гипербилирубинемия, анемия. Обычно они развиваются через несколько дней после начала лечения ЦСА и затем исчезают, несмотря на его продолжение. При синдроме Бехчета у больных с активным увеитом ЦСА в дозе 2,5 мг/кг/сутки более эффективен, чем пульс-терапия. Имеются сообщения об успешном применении ЦСА (5 мг/кг/сутки) в сочетании с ГК у больных, резистентных к ЦФ. Создается впечатление, что ЦСА в ряде случаев может быть альтернативой ЦФ, который, хотя и обладает высокой клинической эффективностью при гранулематозе Вегенера, нередко вызывает инфекционные осложнения.
Кроме того, имеется наблюдение успешного лечения некротизирующею ревматоидного васкулита этим препаратом в дозе 4 мг/кг/сутки на фоне применения преднизолона в комбинации с вазапростаном в течение 16 недель.
В ряде работ отмечается положительный эффект от назначения ЦСА при рецидивирующем полихондрите, синдроме Вебера-Крисгена и гангренозной пиодермии.
9. Аминохинолиновые препараты
По данным токсилогических исследований, хлорохин примерно в 2-3 раза токсичнее плаквенила.
Эти препараты редко используются для лечения васкулитов. Они не относятся к препаратам первого ряда. Однако многочисленные противовоспалительные эффекты делагила и гидроксихлорохина (плаквенила) позволяют рекомендовать их к включению в комбинированную терапию васкулитов.
В недавних исследованиях было показано, что плаквенил обладает определенной антивирусной активностью.
Аминохинолиновые препараты подавляют агрегацию и адгезию тромбоцитов, снижают вязкость крови и уменьшают размер тромба.
Антималярийные препараты обладают гиполипидемическим действием. Эти данные свидетельствуют о том, что препараты следует включать в комбинированную терапию больных васкулитами с повышенным риском развития сердечно-сосудистых осложнений и, вероятно, длительно получающих ГК. Обычно, суточная доза плаквенила 400 мг (6,5 мг/кг), а хлорохина – 250 мг (4,0 мг/кг). Препараты хорошо переносятся. Частым осложнением является кожная сыпь. Наиболее грозным побочным эффектом этих препаратов является поражение глаз (ретинопатия). К ним относятся: центральная скотома, сужение периферических полей зрения, позднее общее ухудшение зрения. Однако плаквенил реже вызывает ретинопатию, чем хлорохин.
10. Энзимные препараты
В последнее время для лечения сосудистых заболеваний используют препараты, которые являются комбинацией ферментов растительного и животного происхождения. К ним относятся вобэнзим, флогензим, мульсал. Имеются данные о том, что они снижают вязкость крови, ускоряют фибринолиз, повышают деформируемость эритроцитов, подавляют агрегацию их и тромбоцитов, ингибируют выработку ИЛ-1 и ФНО-a. Обнаружен их иммуномодулирующей эффект на субпопуляции Т-лимфоцитов, проявляющийся в нормализации существующего дисбаланса этих клеток в организме человека. Однако при системных васкулитах эти препараты следует назначать в комбинации с ГК и ЦФ.
11. Противовирусные препараты.
Как уже отмечалось, при некоторых формах васкулитов важное значение в патогенезе имеет инфекция вирусами гепатита В и С. При наличии маркеров репликации этих вирусов показано назначение препаратов интерферона (реальдерон, ИФ-a) в сочетании с ГК и плазмаферезом. В отдельных клинических наблюдениях описаны положительные результаты лечения ИФ-a язвенного поражения слизистой полости рта при болезни Бехчета и глазных проявлениях заболевания.
12. Аспирин
Аспирин (ацетилсалициловая кислота) является одним из основных фармакологических средств, применяющихся для терапии различных состояний с повышенной агрегацией тромбоцитов. После однократного его приема значительный дезагрегирующий эффект на тромбоциты длится в течение 4-7 дней. Он обусловлен блокадой аспирином циклооксигеназного пути метаболизма арахидоновой кислоты и более выражен в тромбоцитах, чем в эндотелии сосудов. Применение аспирина при васкулитах связано со следующими его механизмами:
Наиболее часто вртречается кардиогенный шок, анафилактические и цитратные реакции. Инфекционные осложнения встречаются крайне редко. Возможно развитие синдрома «рикошета» (удаление аутоантител стимулирует их синтез), который особенно часто наблюдается у больных с активным воспалительным процессом.
Итак, подводя итог вышесказанному, хочу подчеркнуть еще раз.
5. Комбинированная терапия системных васкулитов
Результаты клинических исследований свидетельствует о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым, быстропрогрессирующим поражением сосудов мелкого калибра. В этих случаях проводится комбинированная терапия ГК и ЦФ, включая пульс -терапию ими.
В настоящее время имеется тенденция к более раннему назначению этих групп препаратов (см. приложение).
Назначение ГК в сочетании с азатиоприном и МТ также позволяет добиться большего клинического эффекта, чем изолированное применение этих препаратов. Большинство исследователей предпочитают в начале использовать ЦФ, а азатиоприн применяют как препарат второго ряда при достижении ремиссии. У некоторых больных гранулематозом Вегенера назначение ГК и МТ рассматривается как альтернатива классической терапии, но эти препараты обычно применяют у пациентов без тяжелого поражения легких и почек или при непереносимости циклофосфамида.
Гиганто-клеточный артериит хорошо контролируется ГК. При этом заболевании ЦФ обычно назначают дополнительно, в виде пульс – терапии при офтальмонологических нарушениях. При ГКА не доказано преимущество комбинированной терапии ГК и МТ над изолированным применением преднизолона. У большинства больных артериитом Такаясу наблюдается положительная динамика при монотерапии ГК. Однако часть из них стероидорезистентна: В этих случаях к преднизолону добавляют метотрексат или проводят пульс – терапию ГК и ЦФ. Применение пульс – терапии ГК и ЦФ или per os также показано при быстро прогрессирующем облитерирующем тромбангиите до развития полной облитерации магистральных артерий нижних или верхних конечностей.
В ряде случаев введение преднизолона и ЦФ комбинируют с процедурами плазмафереза. Такая тактика предпочтительнее для ведения больных при фульминантном течении васкулита, сопровождающемся нарушением функции жизненно важных органов, и при артериите Такаясу.
При УП, ассоциированном с вирусом гепатита В, как у взрослых так и у детей показано назначение противовирусных препаратов и преднизолона в средних дозах в сочетании с повторными процедурами плазмафереза.
6. Пульс – синхронизация
В настоящее время разработана схема, получившая название «пульс – синхронизация», которая, как полагают, способствует увеличению эффективности цитотоксической терапии. Суть этого метода заключается в отмене на четыре недели поддерживающей терапии ГК и цитотоксическими препаратами, что вызывает стимуляцию пролиферации лимфоидных клеток и развитие синдрома «рикошета». Последний купируется тремя циклами интенсивного плазмафереза и высокими дозами ЦФ. Предполагается, что такое лечение позволяет добиться более эффективной элиминации патологических клонов клеток, синтезирующих аутоантитела.
С.К. Соловьев и В. А. Насонова сформулировали принципы применения синхронной интенсивной терапии с последовательным назначением экстракорпоральных процедур плазмафереза или гемосорбции и ударных доз метилпреднизолона и ЦФ для лечения СКВ. Аналогичная схема используется и педиатрами при острых и молниеносных формах УП. Однако для других форм васкулитов «пульс – синхронизация» еще не разработана. Что касается ВВИГ в комбинации с ГК, то он с успехом применяется при гранулематозе Вегенера и некоторых других васкулитах.
Большинство авторов в комбинированную терапию васкулитов рекомендуют включать и другие препараты, влияющие на реологические свойства крови (гепарин, фраксипарин), дезагреганты (пентоксифиллин, тиклид, аспирин), препараты простагландина Е, (вазапростан) и простациклина (илопрост), а также периферические вазодилататоры. Важной составляющей терапии васкулитов является профилактика развития инфекции и поражения ЖКТ. Кроме того, учитывая увеличение продолжительности жизни больных васкулитами и возможности развития у них раннего атеросклероза, СС осложнений, необходимо в целях профилактики назначать препараты, обладающие противовоспалительным, антитромботическим и гиподемическим действием (плаквенил, делагин, аспирин, пентоксифиллин).
Итак, другие препараты и методы лечения.
7. Пентоксифилин
Пентоксифилин (трентал) – ингиботор ксантиновой фосфодиэстеразы, который улучшает доставку кислорода к тканям при перифирических сосудистых заболеваниях человека.
Этот препарат широко применяется для лечения системных васкулитов, особенно при вазоспастическом и ишемическом синдромах, поражениях кожи и почек. В настоящее время получены клинические и экспериментальные факты, свидетельствующие о его противовоспалительном иммуномодулирующем эффекте, снижение нефротоксичности и потенцирование эффекта ЦСА, а также усиление противовоспалительного действия метотрексата. Является важным дополнением к терапии ГК и ЦФ. Некоторые рассматривают его как базисный препарат для лечения геморрагического васкулита.
Лечение пентоксифиллином обычно начинают с внутривенных капельных инфузий по 200-300 мг/сутки в 200 мл физиологического раствора. Курс лечения состоит из 10 – 15 инъекций. Непосредственно после окончания инфузионной терапии переходят на пероральный прием препарата по 600-800 мг/сутки в течение 30-40 дней с последующим снижением дозы до 200-300 мг/сутки и ее приемом в течение длительного времени (6-12 мес).
Нередко внутривенное введение пентоксифиллина сочетают с реополиглюкином, который снижает вязкость крови, уменьшает агрегацию тромбоцитов и эритроцитов, а также обладает антитромботическим эффектом.
Е.Н. Семенкова и О.Г. Кривошееев при геморрагическом васкулите считают наиболее эффективным использование пентоксифиллина в дозе 1000-1200 мг/сутки в сочетании с дапсоном (100-200 мг/сутки).
8. Циклоспорин А
1) Наряду с имуносупрессивной активностью, ЦСА в фармакологических концентрациях проявляет определенные противовоспалительные эффекгы, ингибируя высвобождение гистамина, триптазы и синтез лейкотриенов базофилами и тучными клетками.
2) В начале лечения ЦСА назначают в дозе 2-3 мг/кг/сутки в 1 или 2 приема в течение 4-8 недель. При неэффективности препарата его дозу постепенно увеличивают на 0,5 – 1,0 мг/кг/сутки до максимальной 5 мг/кг/сутки. При стабилизации процесса в течение 3 месяцев рекомендуется очень медленное ее снижение (по 0,5 мг/кг за 1 месяц) до минимально эффективной. При отсутствии эффекта в течение 6 месяцев на фоне приема оптимально переносимой дозы препарата продолжение лечения нецелесообразно.
3) В процессе лечения особое внимание следует уделить динамике уровня креатинина в сыворотке, увеличение которого более чем на 30% от исходного диктует необходимость немедленного уменьшения дозы ЦСА. Препарат не следует назначать больным с нарушенной функцией почек, тяжелой артериальной гипертензией, инфекционными заболеваниями и злокачественными новообразованиями.
В то же время, на фоне лечения ЦСА наблюдается развитее некоторых специфических осложнений, наиболее тяжелым из которых является поражение почек.
ЦСА вызывает так называемую функциональную нефротоксичность, приводящую к увеличению концентрации креатинина и мочевины. Она связана с вазоконстрикцией афферентных артериол клубочков, ведущей к снижению почечного кровотока и четко коррелирует с дозой препарата, но обычно не сопровождается явными морфологическими нарушениями.
У 5-15 % больных ЦСА вызывает зависимое от дозы повышение диастолического артериального давления в среднем на 2-3 мм рт. ст. при дозе 2,5 мг/кг/сутки и на 5 мм рт. ст. при дозе 5 мг/кг/сугки.
Препаратами выбора при лечении артериальной гипертензии вызванной ЦСА, являются антагонисты Са: нифедипин или исрадипин, которые в отличие от дилтиазема и верапамила существенно не влияют на фармакокинетику ЦСА.
К другим побочным реакциям относятся гипертрихоз, гиперплазия слизистой полости рта, парастезии, тремор, желудочно-кишечные расстройства, умеренная гипербилирубинемия, анемия. Обычно они развиваются через несколько дней после начала лечения ЦСА и затем исчезают, несмотря на его продолжение. При синдроме Бехчета у больных с активным увеитом ЦСА в дозе 2,5 мг/кг/сутки более эффективен, чем пульс-терапия. Имеются сообщения об успешном применении ЦСА (5 мг/кг/сутки) в сочетании с ГК у больных, резистентных к ЦФ. Создается впечатление, что ЦСА в ряде случаев может быть альтернативой ЦФ, который, хотя и обладает высокой клинической эффективностью при гранулематозе Вегенера, нередко вызывает инфекционные осложнения.
Кроме того, имеется наблюдение успешного лечения некротизирующею ревматоидного васкулита этим препаратом в дозе 4 мг/кг/сутки на фоне применения преднизолона в комбинации с вазапростаном в течение 16 недель.
В ряде работ отмечается положительный эффект от назначения ЦСА при рецидивирующем полихондрите, синдроме Вебера-Крисгена и гангренозной пиодермии.
9. Аминохинолиновые препараты
По данным токсилогических исследований, хлорохин примерно в 2-3 раза токсичнее плаквенила.
Эти препараты редко используются для лечения васкулитов. Они не относятся к препаратам первого ряда. Однако многочисленные противовоспалительные эффекты делагила и гидроксихлорохина (плаквенила) позволяют рекомендовать их к включению в комбинированную терапию васкулитов.
В недавних исследованиях было показано, что плаквенил обладает определенной антивирусной активностью.
Аминохинолиновые препараты подавляют агрегацию и адгезию тромбоцитов, снижают вязкость крови и уменьшают размер тромба.
Антималярийные препараты обладают гиполипидемическим действием. Эти данные свидетельствуют о том, что препараты следует включать в комбинированную терапию больных васкулитами с повышенным риском развития сердечно-сосудистых осложнений и, вероятно, длительно получающих ГК. Обычно, суточная доза плаквенила 400 мг (6,5 мг/кг), а хлорохина – 250 мг (4,0 мг/кг). Препараты хорошо переносятся. Частым осложнением является кожная сыпь. Наиболее грозным побочным эффектом этих препаратов является поражение глаз (ретинопатия). К ним относятся: центральная скотома, сужение периферических полей зрения, позднее общее ухудшение зрения. Однако плаквенил реже вызывает ретинопатию, чем хлорохин.
10. Энзимные препараты
В последнее время для лечения сосудистых заболеваний используют препараты, которые являются комбинацией ферментов растительного и животного происхождения. К ним относятся вобэнзим, флогензим, мульсал. Имеются данные о том, что они снижают вязкость крови, ускоряют фибринолиз, повышают деформируемость эритроцитов, подавляют агрегацию их и тромбоцитов, ингибируют выработку ИЛ-1 и ФНО-a. Обнаружен их иммуномодулирующей эффект на субпопуляции Т-лимфоцитов, проявляющийся в нормализации существующего дисбаланса этих клеток в организме человека. Однако при системных васкулитах эти препараты следует назначать в комбинации с ГК и ЦФ.
11. Противовирусные препараты.
Как уже отмечалось, при некоторых формах васкулитов важное значение в патогенезе имеет инфекция вирусами гепатита В и С. При наличии маркеров репликации этих вирусов показано назначение препаратов интерферона (реальдерон, ИФ-a) в сочетании с ГК и плазмаферезом. В отдельных клинических наблюдениях описаны положительные результаты лечения ИФ-a язвенного поражения слизистой полости рта при болезни Бехчета и глазных проявлениях заболевания.
12. Аспирин
Аспирин (ацетилсалициловая кислота) является одним из основных фармакологических средств, применяющихся для терапии различных состояний с повышенной агрегацией тромбоцитов. После однократного его приема значительный дезагрегирующий эффект на тромбоциты длится в течение 4-7 дней. Он обусловлен блокадой аспирином циклооксигеназного пути метаболизма арахидоновой кислоты и более выражен в тромбоцитах, чем в эндотелии сосудов. Применение аспирина при васкулитах связано со следующими его механизмами:
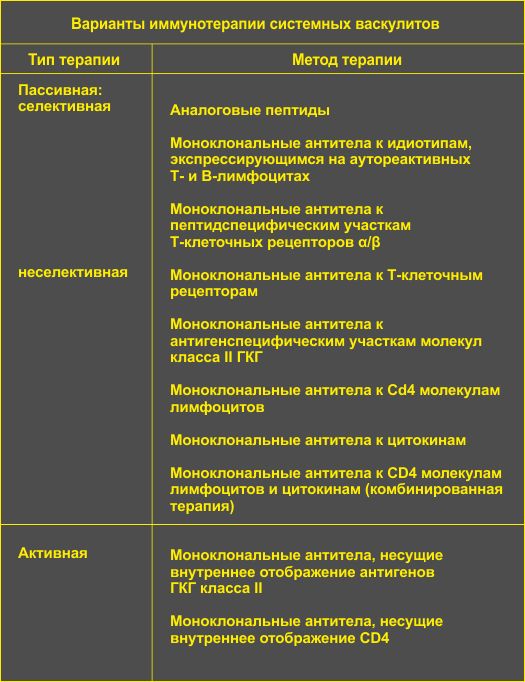 а) При РА после введения моноклональных анти-СD4+ антител в некоторых случаях наблюдается положительная динамика со стороны внесуставных (язвы голени) проявлений заболевания.
Использование антител позволяет достигнуть длительной ремиссии у больных с тяжелым ревматоидным васкулитом, при гранулематозе Вегенера.
б) При системных васкулитах (гранулематоз Вегенера, артериит Такаясу, узелковый периартериит, гигантоклеточный артериит), по-видимому, наибольшее значение будет иметь введение антител к ФНО-a и молекулам адгезии – инфликсимаб (Ремикейд).
2) В последнее время в клинической практике широко применяются иммунокорректоры животного происхождения, а именно препараты тимуса и их синтетические аналоги.
В нашей стране при васкулитах апробирован препарат тимуса – тактивин который оказался гетерогенным по функциональным свойствам. Тактивин восстанавливает число Т-лимфоцитов у больных со сниженным их содержанием, повышает киллерную активность. В зависимости от дозы влияет на функции естественных киллерных клеток, в низких дозах стимулирует продукцию ИФ–a, Однако его применение в качестве монотерапии при васкулитах неэффективно. Наиболее обосновано назначение этого препарата в сочетании с ГК и ЦФ.
3) В целом новые направления иммунотерапии системных васкулитов связаны с применением биотехнологических препаратов, позволяющих селективно влиять на функциональную активность иммунокомпетентных клеток, синтез цитокинов, экспрессию молекул адгезии и др.
23. Диета
Важное значение в лечении геморрагического васкулита имеет гипоантигенная диета. При эссенциальной криоглобулинемической пурпуре иногда эффективна диета с низким содержанием белка.
24. Местное лечение
1) В ряде случаев при язвенных поражениях кожи важное значение имеет местное лечение, которое должно быть этапным. Возможно наложение примочек или мазей с протеолитическими ферментами. Для примочек используют 0,5 % раствор новокаина с добавлением химопсина (100 мг на 100 мл). Эффективна мазь «Ируксол», которую наносят на очаги поражения 1-2 раза в день на салфетке. Для достижения дезинфицирующего эффекта перед каждой сменой повязки язвенную поверхность промывают перекисью водорода или раствором перманганата калия.
2) После полного очищения язвенных поверхностей от гнойно-некротического струпа используют эпителизирующие и дезинфицирующие средства при сильных болях – с добавлением анестетиков (5% анестезиновая или 5% дерматол-анестезиновая мази, левомеколь, левосин, мазь Вишневского, 10% метилурациловая мазь, пена «Пантенол», коллагеновые губки и т.п.)
3) Для местного лечения целесообразно использовать и препарат аргосульфан (Jelfa), который представляет собой крем с 2% серебряной солью сульфатиазола. Он оказывает выраженное местное антимикробное и болеутоляющее действие. Он эффективен для лечения трофических язв голеней различного генеза.
Препарат аргосульфан хорошо переносится больными. Его необходимо включать для местного лечения язвенных дефектов кожи, развивающихся на фоне различной сосудистой патологии, в том числе системных васкулитов.
25. Другие аспекты васкулитов
Другие аспекты ведения больных с васкулитами связаны с привлечением для их лечения специалистов различного профиля. Развитие осложнений при этих заболеваниях, как правило, требует согласованных действий терапевтов, нефрологов, отоларингологов, невропатологов, хирургов, окулистов и др. В этих ситуациях особенно важен единый подход к лечению васкулитов.
а) При РА после введения моноклональных анти-СD4+ антител в некоторых случаях наблюдается положительная динамика со стороны внесуставных (язвы голени) проявлений заболевания.
Использование антител позволяет достигнуть длительной ремиссии у больных с тяжелым ревматоидным васкулитом, при гранулематозе Вегенера.
б) При системных васкулитах (гранулематоз Вегенера, артериит Такаясу, узелковый периартериит, гигантоклеточный артериит), по-видимому, наибольшее значение будет иметь введение антител к ФНО-a и молекулам адгезии – инфликсимаб (Ремикейд).
2) В последнее время в клинической практике широко применяются иммунокорректоры животного происхождения, а именно препараты тимуса и их синтетические аналоги.
В нашей стране при васкулитах апробирован препарат тимуса – тактивин который оказался гетерогенным по функциональным свойствам. Тактивин восстанавливает число Т-лимфоцитов у больных со сниженным их содержанием, повышает киллерную активность. В зависимости от дозы влияет на функции естественных киллерных клеток, в низких дозах стимулирует продукцию ИФ–a, Однако его применение в качестве монотерапии при васкулитах неэффективно. Наиболее обосновано назначение этого препарата в сочетании с ГК и ЦФ.
3) В целом новые направления иммунотерапии системных васкулитов связаны с применением биотехнологических препаратов, позволяющих селективно влиять на функциональную активность иммунокомпетентных клеток, синтез цитокинов, экспрессию молекул адгезии и др.
23. Диета
Важное значение в лечении геморрагического васкулита имеет гипоантигенная диета. При эссенциальной криоглобулинемической пурпуре иногда эффективна диета с низким содержанием белка.
24. Местное лечение
1) В ряде случаев при язвенных поражениях кожи важное значение имеет местное лечение, которое должно быть этапным. Возможно наложение примочек или мазей с протеолитическими ферментами. Для примочек используют 0,5 % раствор новокаина с добавлением химопсина (100 мг на 100 мл). Эффективна мазь «Ируксол», которую наносят на очаги поражения 1-2 раза в день на салфетке. Для достижения дезинфицирующего эффекта перед каждой сменой повязки язвенную поверхность промывают перекисью водорода или раствором перманганата калия.
2) После полного очищения язвенных поверхностей от гнойно-некротического струпа используют эпителизирующие и дезинфицирующие средства при сильных болях – с добавлением анестетиков (5% анестезиновая или 5% дерматол-анестезиновая мази, левомеколь, левосин, мазь Вишневского, 10% метилурациловая мазь, пена «Пантенол», коллагеновые губки и т.п.)
3) Для местного лечения целесообразно использовать и препарат аргосульфан (Jelfa), который представляет собой крем с 2% серебряной солью сульфатиазола. Он оказывает выраженное местное антимикробное и болеутоляющее действие. Он эффективен для лечения трофических язв голеней различного генеза.
Препарат аргосульфан хорошо переносится больными. Его необходимо включать для местного лечения язвенных дефектов кожи, развивающихся на фоне различной сосудистой патологии, в том числе системных васкулитов.
25. Другие аспекты васкулитов
Другие аспекты ведения больных с васкулитами связаны с привлечением для их лечения специалистов различного профиля. Развитие осложнений при этих заболеваниях, как правило, требует согласованных действий терапевтов, нефрологов, отоларингологов, невропатологов, хирургов, окулистов и др. В этих ситуациях особенно важен единый подход к лечению васкулитов.
- Быстрое подавление иммунного ответа в дебюте заболевания – индукция ремиссии.
- Длительная, не менее 0,5-2 лет, поддерживающая терапия иммуносупрессантами в дозах, достаточных для достижения клинической и лабораторной ремиссии заболевания. Быстрое купирование иммунного ответа при обострениях заболевания.
- Достижение стойкой, полной ремиссии васкулита, определение степени повреждения органов или систем организма с целью их коррекции, проведение реабилитационных мероприятий.
 Цель первого этапа – максимально быстро, до развития необратимых ишемических, некротических изменений в органах и тканях, добиться подавления иммунного воспаления, что предполагает:
Цель первого этапа – максимально быстро, до развития необратимых ишемических, некротических изменений в органах и тканях, добиться подавления иммунного воспаления, что предполагает:
- использование адекватно высоких доз ГК в виде монотерапии или в сочетании с иммуносупрессантами преимущественно цитотоксического действия (ЦФ), вплоть до назначения пульс-терапии этими препаратами;
- или введение внутривенного иммуноглобулина;
- или применение экстракорпоральных методов лечения (плазмаферез).
 В настоящее время ГК широко используются для лечения васкулитов. Они назначаются практически при всех их формах.
1) Монотерапия ГК.
Монотерапия ГК является основным методом лечения некоторых васкулитов ГКА (гиганто-клеточного артериита), реже – артериита Такаясу и некоторых некротизирующих васкулитов с локальным поражением сосудов и отсутствием признаков прогрессирования заболевания. Тяжелые абдоминальные формы геморрагического васкулита служат показанием для назначения преднизолона. Полагают, что при этом заболевании лечение ГК позволяет предотвратить последующие поражения почек. Однако другие авторы не разделяют этого мнения. ГК используются как системно, так и местно, в виде мазей и кремов для лечения язв полости рта и половых органов. Обычно доза преднизолона при системных васкулитах колеблется 1-2 мг/кг (в несколько приемов). Более высокие дозировки препарата применяются при ГКА, синдроме Черджа – Стросса, классическом УП, чем при болезни Бехчета, артериите Такаясу, геморрагическом васкулите и гранулематозе Вегенера. При положительном эффекте переходят на однократный прием утром.
Длительность подавляющей терапии ГК составляет 3-4 недели, затем проводится постепенное (2-3 месяца) снижение их дозы до поддерживающей (0,15 – 0,2 мг/кг/сутки), которая назначается от одного года до трех – пяти лет.
Возможен другой вариант терапии ГК-ми.
2) Альтернирующая терапия
Альтернирующая терапия ГК – метод лечения, заключающийся в назначении ГК короткого действия без выраженной минерало-кортикоидной активности (преднизон, преднизолон, метилпреднизолон) однократно, утром каждые 48 часов. Целью альтернирующей терапии является уменьшение побочных реакций ГК при сохранении их терапевтической эффективности.
Полагают, что этот метод лечения показан больным, которые длительно (более нескольких недель) принимают ГК. Его не следует применять при кратковременном использовании этих препаратов, а также в начальной стадии лечения или в период обострения заболевания.
Однако при системных васкулитах такая тактика лечения, как правило, неэффективна. Полагают, что при этих заболеваниях альтернирующий прием ГК предпочтителен только для поддерживающей терапии.
3) Пульс-терапия
По данным многих исследований, на фоне пульс терапии быстрое улучшение наблюдается у 75% больных с активным волчаночным нефритом, поражением ЦНС, пневмонитом, полисерозитом, васкулитом, тромбоцитопенией (см. приложение к лекциям).
Табл. Показания к проведению пульс – терапии глюкокортикоидами при системных васкулитах
В настоящее время ГК широко используются для лечения васкулитов. Они назначаются практически при всех их формах.
1) Монотерапия ГК.
Монотерапия ГК является основным методом лечения некоторых васкулитов ГКА (гиганто-клеточного артериита), реже – артериита Такаясу и некоторых некротизирующих васкулитов с локальным поражением сосудов и отсутствием признаков прогрессирования заболевания. Тяжелые абдоминальные формы геморрагического васкулита служат показанием для назначения преднизолона. Полагают, что при этом заболевании лечение ГК позволяет предотвратить последующие поражения почек. Однако другие авторы не разделяют этого мнения. ГК используются как системно, так и местно, в виде мазей и кремов для лечения язв полости рта и половых органов. Обычно доза преднизолона при системных васкулитах колеблется 1-2 мг/кг (в несколько приемов). Более высокие дозировки препарата применяются при ГКА, синдроме Черджа – Стросса, классическом УП, чем при болезни Бехчета, артериите Такаясу, геморрагическом васкулите и гранулематозе Вегенера. При положительном эффекте переходят на однократный прием утром.
Длительность подавляющей терапии ГК составляет 3-4 недели, затем проводится постепенное (2-3 месяца) снижение их дозы до поддерживающей (0,15 – 0,2 мг/кг/сутки), которая назначается от одного года до трех – пяти лет.
Возможен другой вариант терапии ГК-ми.
2) Альтернирующая терапия
Альтернирующая терапия ГК – метод лечения, заключающийся в назначении ГК короткого действия без выраженной минерало-кортикоидной активности (преднизон, преднизолон, метилпреднизолон) однократно, утром каждые 48 часов. Целью альтернирующей терапии является уменьшение побочных реакций ГК при сохранении их терапевтической эффективности.
Полагают, что этот метод лечения показан больным, которые длительно (более нескольких недель) принимают ГК. Его не следует применять при кратковременном использовании этих препаратов, а также в начальной стадии лечения или в период обострения заболевания.
Однако при системных васкулитах такая тактика лечения, как правило, неэффективна. Полагают, что при этих заболеваниях альтернирующий прием ГК предпочтителен только для поддерживающей терапии.
3) Пульс-терапия
По данным многих исследований, на фоне пульс терапии быстрое улучшение наблюдается у 75% больных с активным волчаночным нефритом, поражением ЦНС, пневмонитом, полисерозитом, васкулитом, тромбоцитопенией (см. приложение к лекциям).
Табл. Показания к проведению пульс – терапии глюкокортикоидами при системных васкулитах
 В настоящее время при системных васкулитах подавление активности заболевания предусматривает более раннее назначение пульс – терапии. Полагают, что одним из преимуществ пульс – терапии при этих заболеваниях является возможность более быстрого перевода больного на поддерживающую дозу ГК. Предварительные результаты свидетельствуют также о том, что повторные процедуры (1-3 дня в месяц) пульс-терапии являются альтернативой назначения цитостатиков.
Табл. Схема назначения высоких доз циклофосфана и метилпреднизолона в виде пульс – терапии для лечения системных васкулитов
В настоящее время при системных васкулитах подавление активности заболевания предусматривает более раннее назначение пульс – терапии. Полагают, что одним из преимуществ пульс – терапии при этих заболеваниях является возможность более быстрого перевода больного на поддерживающую дозу ГК. Предварительные результаты свидетельствуют также о том, что повторные процедуры (1-3 дня в месяц) пульс-терапии являются альтернативой назначения цитостатиков.
Табл. Схема назначения высоких доз циклофосфана и метилпреднизолона в виде пульс – терапии для лечения системных васкулитов
 При гранулематозе Вегенера, МПА (микроскопический полиангиит), УП, СКВ, ревматоидном васкулите пульс – терапию проводят ежемесячно в течение 9-24 мес. подряд (т.е проводят повторные курсы).
По данным Института ревматологии, при артериите Такаясу предпочтительнее повторные курсы пульс-терапии 1 раз в месяц в сроки от 7 до 12 мес.
Наиболее часто для проведения пульс-терапии используют метилпреднизолон в виде раствора гемисукцината натрия.
В последнее время с этой целью стали использовать дексаметазон (в частности – препарат дексавен 2 мг/кг в сутки), который в 7 раз активнее, чем преднизолон. Препарат оказывает выраженное противовоспалительное действие, не задерживает ионов Na+ в организме и слабо влияет на выделение ионов К+. Период его полувыведения составляет 36-54 часа, в то время как для метилпреднизолона он колеблется от 12 до 36 часов.
Имеются сообщения о высокой эффективности пульс – терапии дексаметазоном у больных резистентной тромбоцитопенической пурпурой.
Хороший клинико-лабораторный эффект был достигнут при назначении в качестве пульс-терапии для лечения СКВ и РА препарата дексавена – натриевой соли фосфата дексаметазона в дозировке 2 мг/кг/сут. Было доказано, что препарат дексавен, применяемый в качестве пульс-терапии, обладает выраженным противовоспалительным действием. Он также является эффективным корректором процессов гемостаза. Последнее достигается, по-видимому, за счет подавления иммунопатологических процессов, инициирующих свертывание крови.
Однако, результаты клинических исследований свидетельствуют о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым быстропрогрессирующим поражением сосудов мелкого калибра.
Необходимо подчеркнуть, что у больных системными некротизирующими васкулитами, а также при тяжелых формах геморрагического васкулита и синдрома Черджа-Стросса, у которых наблюдается тяжелое быстропрогрессирующее поражение сосудов и почек, даже несмотря на хороший начальный клинический ответ на глюкокортикостероиды, введение высоких доз ГК обязательно должно сочетаться с активной цитостатической терапией, в первую очередь циклофосфамидом, так как только такая комбинированная терапия позволяет реально улучшить прогноз заболевания.
2. Цитотоксические препараты.
Для лечения системных васкулитов используются цитотоксические препараты трех основных классов: алкилирующие агенты (циклофосфамид), пуриновые аналоги (азатиоприн) антагонисты фолиевой кислоты (метотрексат). Последние в низких дозах не обладают явной цитотоксической активностью.
1) Циклофосфамид применяется для лечения васкулитов уже более 25 лет. ЦФ воздействует на различные звенья патогенеза васкулитов (см. приложение).
Табл. Основные механизмы действия циклофосфана при васкулитах
При гранулематозе Вегенера, МПА (микроскопический полиангиит), УП, СКВ, ревматоидном васкулите пульс – терапию проводят ежемесячно в течение 9-24 мес. подряд (т.е проводят повторные курсы).
По данным Института ревматологии, при артериите Такаясу предпочтительнее повторные курсы пульс-терапии 1 раз в месяц в сроки от 7 до 12 мес.
Наиболее часто для проведения пульс-терапии используют метилпреднизолон в виде раствора гемисукцината натрия.
В последнее время с этой целью стали использовать дексаметазон (в частности – препарат дексавен 2 мг/кг в сутки), который в 7 раз активнее, чем преднизолон. Препарат оказывает выраженное противовоспалительное действие, не задерживает ионов Na+ в организме и слабо влияет на выделение ионов К+. Период его полувыведения составляет 36-54 часа, в то время как для метилпреднизолона он колеблется от 12 до 36 часов.
Имеются сообщения о высокой эффективности пульс – терапии дексаметазоном у больных резистентной тромбоцитопенической пурпурой.
Хороший клинико-лабораторный эффект был достигнут при назначении в качестве пульс-терапии для лечения СКВ и РА препарата дексавена – натриевой соли фосфата дексаметазона в дозировке 2 мг/кг/сут. Было доказано, что препарат дексавен, применяемый в качестве пульс-терапии, обладает выраженным противовоспалительным действием. Он также является эффективным корректором процессов гемостаза. Последнее достигается, по-видимому, за счет подавления иммунопатологических процессов, инициирующих свертывание крови.
Однако, результаты клинических исследований свидетельствуют о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым быстропрогрессирующим поражением сосудов мелкого калибра.
Необходимо подчеркнуть, что у больных системными некротизирующими васкулитами, а также при тяжелых формах геморрагического васкулита и синдрома Черджа-Стросса, у которых наблюдается тяжелое быстропрогрессирующее поражение сосудов и почек, даже несмотря на хороший начальный клинический ответ на глюкокортикостероиды, введение высоких доз ГК обязательно должно сочетаться с активной цитостатической терапией, в первую очередь циклофосфамидом, так как только такая комбинированная терапия позволяет реально улучшить прогноз заболевания.
2. Цитотоксические препараты.
Для лечения системных васкулитов используются цитотоксические препараты трех основных классов: алкилирующие агенты (циклофосфамид), пуриновые аналоги (азатиоприн) антагонисты фолиевой кислоты (метотрексат). Последние в низких дозах не обладают явной цитотоксической активностью.
1) Циклофосфамид применяется для лечения васкулитов уже более 25 лет. ЦФ воздействует на различные звенья патогенеза васкулитов (см. приложение).
Табл. Основные механизмы действия циклофосфана при васкулитах
 а) ЦФ применяется для лечения некротизирующих васкулитов, прежде всего за счет влияния на клетки-медиаторы сосудистого повреждения.
Однако, наряду с иммуносупрессивной активностью, описано и иммуностимулирующее действие ЦФ, связанное, как полагают, с разной чувствительностью Т- и В-лимфоцитов к воздействию этого препарата. Его эффекты на систему иммунитета в определенной степени зависят от особенностей терапии. Установлено, что длительный постоянный прием низких доз ЦФ в большей степени вызывает депрессию клеточного иммунитета, а интермиттирующее введение высоких его доз в первую очередь подавляют его гуморальное звено.
ЦФ эффективное средство лечения некротизирующих васкулитов: гранулематоза Вегенера, УП и синдрома Черджа-Стросса.
б) Интермиттирующая пульс-терапия ЦФ рассматривается как наиболее эффективный метод лечения системного ревматоидного васкулита.
Препарат также назначают при артериите Такаясу, ГКА, облитерирующем тромбангиите (ОТА), болезни Бехчета, как правило, в виде пульс-терпаии в сочетании с ГК. При геморрагическом васкулите показанием для терапии ЦФ служит развитие быстропрогрессирующего гломерулонефрита.
в) Существуют две принципиальные схемы назначения ЦФ
– Пероральный прием в дозе 1-2 мг/кг/сут в течение 10-14 дней с последующим титрованием в зависимости от уровня лейкоцитов в периферической крови.
При очень быстром прогрессировании васкулита циклофосфамид назначают в дозе 4 мг/кг/сут в течение 3 дней, затем 2 мк/кг/сут в течение 7 дней. Общая длительность лечения циклофосфамидом составляет не менее 12 месяцев после достижения полной ремиссии. Затем дозу препарата постепенно снижают в течение 2-3 месяцев по 25-50 мг.
Особое значение имеет титрование дозы циклофосфамида, на фоне лечения которым концентрация лейкоцитов не должна быть ниже 3000- 3500 мм3, а нейтрофилов – 1000-1500/мм3. В начале лечения целесообразно мониторировать концентрацию лейкоцитов через день, а после стабилизации количества лейкоцитов — не реже 1 раза в 2 недели.
У пациентов с почечной недостаточностью (сывороточный креатинин более 2 мг%) доза циклофосфамида, должна быть снижена на 25-50°/
– Болюсное интермиттирующее внутривенное введение высоких доз (500-1000 мг/м2 в сутки или 10-15 мг/кг в сутки) в течение первых 4-6 мес. ежемесячно, а затем 1 раз в 3 мес.
Обычно лечение ЦФ сочетают с назначением умеренных или высоких доз ГК, включая пульс-терапию.
Превалирует мнение, что обе схемы лечения примерно равнозначны, но на фоне интермиттирующего внутривенного введения частота токсических реакций меньше, чем при постоянном приеме per os.
В то же время, имеются данные о том, что у больных гранулематозом Вегенера пульс-терапия и пероральный прием ЦФ в равной степени эффективны только в отношении ближайших результатов, но долгосрочную ремиссию заболевания удается достигнуть только при длительном ежедневном приеме препарата. Таким образом, пульс-терапия и длительный прием низких доз ЦФ имеют разный терапевтический профиль.
в) По мнению Т. Cupps в некоторых случаях применение низких доз ЦФ имеет преимущества перед интермитирующим введением высоких. Например, в фазу индукции риск супрессии костного мозга выше у больных, леченных пульс – терапией, чем у пациентов, получающих низкие дозы ЦФ. Полагают, что, поскольку истинное изменение количества лейкоцитов в периферической крови после пульс-терапии становится очевидным через 10-20 дней от начала лечения, постольку дозу ЦФ изменяют только в этот период. Напротив, при ежедневном приеме препарата его дозировку можно подбирать на основе мониторинга уровня лейкоцитов в периферической крови и функции почек. Таким образом, опасность появления токсических реакций в ранние сроки лечения высокими дозами ЦФ особенно велика у больных с нарушениями функции многих органов, быстрым прогрессированием почечной недостаточности; ишемией кишечника, а также у пациентов, получающих высокие ГК. Однако по данным R.A. Lugmani и соавт, супрессия костного мозга и инфекционные осложнения чаще встречаются при постоянном приеме ЦФ, чем при пульс-терапии.
– Частое осложнение, возникающее на фоне лечения ЦФ – геморрагический цистит. Он развивается почти у 30% больных. Его частота несколько меньше на фоне парентерального введения ЦФ, чем при приеме per os. Для профилактики геморрагического цистита рекомендуется прием препарата месна, который является детоксирующим агентом. Месна вводится внутривенно в дозе, составляющей 20% от дозы ЦФ, до приема последнего и через 4-8 часов после него.
Развитие тяжелого цистита является абсолютным показанием к отмене ЦФ. У больных с умеренным циститом возможно продолжение лечения меньшими дозами препарата под тщательным клиническим и инструментальным (цистоскопия) контролем.
– Другой побочный эффект ЦФ – нейтропения. Она является наиболее частым осложнением, ограничивающим возможность продолжения терапии. В начале лечения общий анализ крови следует поводить раз в 7-14 дней, а при стабилизации процесса и дозы препарата каждые 2-3 месяца. Препарат, отменяют, если количество лейкоцитов менее 3,5*109/л.
– Описаны больные с персистирующей гипогаммаглобулинемией. Этот побочный эффект ЦФ очень опасен, особенно в сочетании с нейтропенией, так как на его фоне значительно возрастает риск развития инфекционных осложнений. Необходимо иметь в виду, что у больных, получающих ЦФ, наблюдается увеличение чувствительности к инфекциям даже при нормальной концентрации нейтрофилов и иммуноглобулинов. При появлении инфекционных осложнений показано прекращение приема цитостатика.
– У больных, длительно принимающих ЦФ, повышен риск появления злокачественных новообразований. В литературе описано около 100 пациентов с СКВ, у которых развилась неходжкинская лимфома, и 13 случаев лимфогранулематоза. Обнаружено, что у больных СКВ уже в течение первых четырех лет от начала лечения этим препаратом умеренно нарастает частота рака влагалища и шейки матки.
– К частым токсическим осложнениям ЦФ относят тошноту, которая нередко делает невозможным проведение пульс – терапии этим препаратом. Для ее профилактики рекомендуется внутривенное введение метоклопрамида в дозе 1-3 мг/кг (максимальная доза 10 мг/кг) в 100 мл 0,9% раствора хлористого натрия за 15 минут до начала инфузии ЦФ в сочетании с седативными средствами (диазепам 5-10 мг).
– Алопеция чаще встречается на фоне приема высоких доз ЦФ, прерывание лечения ведет к нормализации роста волос.
– Олигоспермия или азооспермия у мужчин и олигоменорея или аменорея у женщин – почти обязательные побочные эффекты лечения ЦФ. Риск их развития повышается при длительном приеме препарата, назначении его высоких доз. Полагают, что проведение пульс – терапии ЦФ во время менструации позволяет снизить риск стерилизации.
2) Азатиоприн
а) В организме человека он метаболизируется в эритроцитах и печени с образованием биологически активных молекул и выводится через почки. В отличие от алкилирующих агентов, азатиоприн обладает цитостатической активностью.
Азатиоприн вызывает периферическую Т – и В – лимфопению. В высоких дозах он уменьшает уровень CD4+ Т – лимфоцитов, а при длительном приеме снижает синтез антител. Однако, поскольку Т-супрессоры особенно чувствительны к его действию, на фоне приема низких доз препарата может наблюдаться увеличение образования антител.
б) В настоящее время при васкулитах азатиоприн рассматривается как препарат второго ряда. Обычно он назначается после достижения ремиссии от приема ЦФ.
Оптимальная доза препарата составляет 1-3 мг/кг/сутки. В первые два месяца лечения азатиоприном необходимо каждые две недели проводить исследование общего анализа крови с обязательным определением количества тромбоцитов. В дальнейшем лабораторный контроль проводят один раз в 6-8 недель. Дозу препарата снижают на 50-75% у больных, получающих аллопуринол или имеющих почечную недостаточность. Поддерживающая доза азаиоприна обычно составляет 50 мг/день.
Комбинированная терапия азатиоприном и преднизолоном предотвращает прогрессирование сосудистого процесса у больных РА с васкулитом и при болезни Бехчета.
в) Наиболее часто на фоне лечения азатиоприном отмечается тошнота и рвота, выраженность которых снижается при приеме препарата с пищей и дробными дозами. Поражение печени встречается не более чем у 1% больных и, вероятно, связано с аллергической реакцией на него. Тем не менее, рекомендуется концентрацию билирубина и печеночных ферментов контролировать не реже, чем 1 раз в 3 месяца.
Лейкопения, обычно встречающаяся в начале лечения также, как полагают, связана с повышенной чувствительностью к этому лекарству. Однако в большинстве случаев появление цитопении отражает подавление костно-мозгового кроветворения. Общая частота цитопении может достигать 30%. При ее развитии азатиоприн отменяют до восстановления нормальных показателей крови, а затем продолжают его прием в меньших дозировках. Среди инфекционных осложнений часто встречается герпетическая инфекция, развитие которой не всегда коррелирует с выраженностью нейтропении. При лечении азатиоприном возможно развитие злокачественных новообразований. Полагают, что имеется генетически детерминированная предрасположенность к развитию токсических реакций на азатиоприн. Препарат противопоказан при беременности.
3) Метотрексат
Табл. Основные механизмы действия метотрексата при васкулитах.
а) ЦФ применяется для лечения некротизирующих васкулитов, прежде всего за счет влияния на клетки-медиаторы сосудистого повреждения.
Однако, наряду с иммуносупрессивной активностью, описано и иммуностимулирующее действие ЦФ, связанное, как полагают, с разной чувствительностью Т- и В-лимфоцитов к воздействию этого препарата. Его эффекты на систему иммунитета в определенной степени зависят от особенностей терапии. Установлено, что длительный постоянный прием низких доз ЦФ в большей степени вызывает депрессию клеточного иммунитета, а интермиттирующее введение высоких его доз в первую очередь подавляют его гуморальное звено.
ЦФ эффективное средство лечения некротизирующих васкулитов: гранулематоза Вегенера, УП и синдрома Черджа-Стросса.
б) Интермиттирующая пульс-терапия ЦФ рассматривается как наиболее эффективный метод лечения системного ревматоидного васкулита.
Препарат также назначают при артериите Такаясу, ГКА, облитерирующем тромбангиите (ОТА), болезни Бехчета, как правило, в виде пульс-терпаии в сочетании с ГК. При геморрагическом васкулите показанием для терапии ЦФ служит развитие быстропрогрессирующего гломерулонефрита.
в) Существуют две принципиальные схемы назначения ЦФ
– Пероральный прием в дозе 1-2 мг/кг/сут в течение 10-14 дней с последующим титрованием в зависимости от уровня лейкоцитов в периферической крови.
При очень быстром прогрессировании васкулита циклофосфамид назначают в дозе 4 мг/кг/сут в течение 3 дней, затем 2 мк/кг/сут в течение 7 дней. Общая длительность лечения циклофосфамидом составляет не менее 12 месяцев после достижения полной ремиссии. Затем дозу препарата постепенно снижают в течение 2-3 месяцев по 25-50 мг.
Особое значение имеет титрование дозы циклофосфамида, на фоне лечения которым концентрация лейкоцитов не должна быть ниже 3000- 3500 мм3, а нейтрофилов – 1000-1500/мм3. В начале лечения целесообразно мониторировать концентрацию лейкоцитов через день, а после стабилизации количества лейкоцитов — не реже 1 раза в 2 недели.
У пациентов с почечной недостаточностью (сывороточный креатинин более 2 мг%) доза циклофосфамида, должна быть снижена на 25-50°/
– Болюсное интермиттирующее внутривенное введение высоких доз (500-1000 мг/м2 в сутки или 10-15 мг/кг в сутки) в течение первых 4-6 мес. ежемесячно, а затем 1 раз в 3 мес.
Обычно лечение ЦФ сочетают с назначением умеренных или высоких доз ГК, включая пульс-терапию.
Превалирует мнение, что обе схемы лечения примерно равнозначны, но на фоне интермиттирующего внутривенного введения частота токсических реакций меньше, чем при постоянном приеме per os.
В то же время, имеются данные о том, что у больных гранулематозом Вегенера пульс-терапия и пероральный прием ЦФ в равной степени эффективны только в отношении ближайших результатов, но долгосрочную ремиссию заболевания удается достигнуть только при длительном ежедневном приеме препарата. Таким образом, пульс-терапия и длительный прием низких доз ЦФ имеют разный терапевтический профиль.
в) По мнению Т. Cupps в некоторых случаях применение низких доз ЦФ имеет преимущества перед интермитирующим введением высоких. Например, в фазу индукции риск супрессии костного мозга выше у больных, леченных пульс – терапией, чем у пациентов, получающих низкие дозы ЦФ. Полагают, что, поскольку истинное изменение количества лейкоцитов в периферической крови после пульс-терапии становится очевидным через 10-20 дней от начала лечения, постольку дозу ЦФ изменяют только в этот период. Напротив, при ежедневном приеме препарата его дозировку можно подбирать на основе мониторинга уровня лейкоцитов в периферической крови и функции почек. Таким образом, опасность появления токсических реакций в ранние сроки лечения высокими дозами ЦФ особенно велика у больных с нарушениями функции многих органов, быстрым прогрессированием почечной недостаточности; ишемией кишечника, а также у пациентов, получающих высокие ГК. Однако по данным R.A. Lugmani и соавт, супрессия костного мозга и инфекционные осложнения чаще встречаются при постоянном приеме ЦФ, чем при пульс-терапии.
– Частое осложнение, возникающее на фоне лечения ЦФ – геморрагический цистит. Он развивается почти у 30% больных. Его частота несколько меньше на фоне парентерального введения ЦФ, чем при приеме per os. Для профилактики геморрагического цистита рекомендуется прием препарата месна, который является детоксирующим агентом. Месна вводится внутривенно в дозе, составляющей 20% от дозы ЦФ, до приема последнего и через 4-8 часов после него.
Развитие тяжелого цистита является абсолютным показанием к отмене ЦФ. У больных с умеренным циститом возможно продолжение лечения меньшими дозами препарата под тщательным клиническим и инструментальным (цистоскопия) контролем.
– Другой побочный эффект ЦФ – нейтропения. Она является наиболее частым осложнением, ограничивающим возможность продолжения терапии. В начале лечения общий анализ крови следует поводить раз в 7-14 дней, а при стабилизации процесса и дозы препарата каждые 2-3 месяца. Препарат, отменяют, если количество лейкоцитов менее 3,5*109/л.
– Описаны больные с персистирующей гипогаммаглобулинемией. Этот побочный эффект ЦФ очень опасен, особенно в сочетании с нейтропенией, так как на его фоне значительно возрастает риск развития инфекционных осложнений. Необходимо иметь в виду, что у больных, получающих ЦФ, наблюдается увеличение чувствительности к инфекциям даже при нормальной концентрации нейтрофилов и иммуноглобулинов. При появлении инфекционных осложнений показано прекращение приема цитостатика.
– У больных, длительно принимающих ЦФ, повышен риск появления злокачественных новообразований. В литературе описано около 100 пациентов с СКВ, у которых развилась неходжкинская лимфома, и 13 случаев лимфогранулематоза. Обнаружено, что у больных СКВ уже в течение первых четырех лет от начала лечения этим препаратом умеренно нарастает частота рака влагалища и шейки матки.
– К частым токсическим осложнениям ЦФ относят тошноту, которая нередко делает невозможным проведение пульс – терапии этим препаратом. Для ее профилактики рекомендуется внутривенное введение метоклопрамида в дозе 1-3 мг/кг (максимальная доза 10 мг/кг) в 100 мл 0,9% раствора хлористого натрия за 15 минут до начала инфузии ЦФ в сочетании с седативными средствами (диазепам 5-10 мг).
– Алопеция чаще встречается на фоне приема высоких доз ЦФ, прерывание лечения ведет к нормализации роста волос.
– Олигоспермия или азооспермия у мужчин и олигоменорея или аменорея у женщин – почти обязательные побочные эффекты лечения ЦФ. Риск их развития повышается при длительном приеме препарата, назначении его высоких доз. Полагают, что проведение пульс – терапии ЦФ во время менструации позволяет снизить риск стерилизации.
2) Азатиоприн
а) В организме человека он метаболизируется в эритроцитах и печени с образованием биологически активных молекул и выводится через почки. В отличие от алкилирующих агентов, азатиоприн обладает цитостатической активностью.
Азатиоприн вызывает периферическую Т – и В – лимфопению. В высоких дозах он уменьшает уровень CD4+ Т – лимфоцитов, а при длительном приеме снижает синтез антител. Однако, поскольку Т-супрессоры особенно чувствительны к его действию, на фоне приема низких доз препарата может наблюдаться увеличение образования антител.
б) В настоящее время при васкулитах азатиоприн рассматривается как препарат второго ряда. Обычно он назначается после достижения ремиссии от приема ЦФ.
Оптимальная доза препарата составляет 1-3 мг/кг/сутки. В первые два месяца лечения азатиоприном необходимо каждые две недели проводить исследование общего анализа крови с обязательным определением количества тромбоцитов. В дальнейшем лабораторный контроль проводят один раз в 6-8 недель. Дозу препарата снижают на 50-75% у больных, получающих аллопуринол или имеющих почечную недостаточность. Поддерживающая доза азаиоприна обычно составляет 50 мг/день.
Комбинированная терапия азатиоприном и преднизолоном предотвращает прогрессирование сосудистого процесса у больных РА с васкулитом и при болезни Бехчета.
в) Наиболее часто на фоне лечения азатиоприном отмечается тошнота и рвота, выраженность которых снижается при приеме препарата с пищей и дробными дозами. Поражение печени встречается не более чем у 1% больных и, вероятно, связано с аллергической реакцией на него. Тем не менее, рекомендуется концентрацию билирубина и печеночных ферментов контролировать не реже, чем 1 раз в 3 месяца.
Лейкопения, обычно встречающаяся в начале лечения также, как полагают, связана с повышенной чувствительностью к этому лекарству. Однако в большинстве случаев появление цитопении отражает подавление костно-мозгового кроветворения. Общая частота цитопении может достигать 30%. При ее развитии азатиоприн отменяют до восстановления нормальных показателей крови, а затем продолжают его прием в меньших дозировках. Среди инфекционных осложнений часто встречается герпетическая инфекция, развитие которой не всегда коррелирует с выраженностью нейтропении. При лечении азатиоприном возможно развитие злокачественных новообразований. Полагают, что имеется генетически детерминированная предрасположенность к развитию токсических реакций на азатиоприн. Препарат противопоказан при беременности.
3) Метотрексат
Табл. Основные механизмы действия метотрексата при васкулитах.
 а) Метотрексат (MТ) относится к группе антиметаболитов, по структуре он близок фолиевой кислоте.
После приема МТ максимальная его концентрация в крови достигается через 2-4 часа. Прием препарата во время еды не влияет на уровень его абсорбции и биодоступности. Элиминация МТ происходит преимущественно в почках за счет клубочковой фильтрации и канальцевой секреции. Время полужизни препарата колеблется от 2 до 6 часов. Недостаточность функции почек приводит к замедлению экскреции МТ и увеличению его токсичности.
Несмотря на достаточно быстрое выведение из крови, полиглютаминовые метаболиты МТ обнаруживаются внутри клеток в течении 7 дней после его однократного приема. Основные механизмы действия этого препарата будут представлены ниже (см. приложение).
а) МТ назначают 3 раза в неделю (per оs или парентерально). Более частый прием препарата, как правило, приводит к увеличению числа острых или хронических токсических реакций. Рекомендуется принимать лекарство в утренние и вечерние часы, с двенадцатичасовым перерывом. Начальная доза МТ в большинстве случаев составляет 7,5 мг/неделю, а в пожилом возрасте 5 мг/неделю. Эффект от назначения препарата оценивается через 4-8 недель. В случае его отсутствия и при нормальной переносимости вещества дозу МТ постепенно увеличивают на 2,5 мг в неделю, максимально до 25 мг. Обычно при системных васкулитах доза этого препарата составляет 12,5-17,5 мг в неделю.
– При повышении дозы МТ оценка токсичности проводиться через 6 дней после приема препарата, а при достижении общего количества принятого препарата в 1500 мг показана биопсия печени. Парентеральное введение МТ используется при отсутствии эффекта от приема per os или при развитии токсических реакций со стороны желудочно-кишечного тракта. Необходимо иметь в виду, что в ряде случаев отсутствие эффекта при энтеральном введении МТ связано не столько с неэффективностью самого препарата, сколько с низкой абсорбцией его в желудочно-кишечном тракте, не позволяющей достичь оптимальной концентрации вещества в крови.
– В настоящее время изучается эффективность низких доз метотрексата (0,15 – 0,3 мг/кг/нед) в сочетании с высокими дозами преднизолона (1мг/кг/сут) у пациентов с кожной формой узелкового полиартериита и гранулематозом Вегенера без угрожающих жизни осложнений.
в) Побочные эффекты от применения МТ обычно включают тошноту и рвоту, которые появляются через 1-8 дней после начала приема препарата и длятся 1-3 дня. Для уменьшения выраженности этих явлений дозу МТ снижают, или вводят его парентерально. Рекомендуется также назначение симптоматических средств, например метоклопрамида. Относительным противопоказанием к применению МТ являются язвы желудка и двенадцатиперстной кишки. В 6% случаев причиной отмены препарата служит стоматит.
– Тяжелые гематологические нарушения развиваются нечасто. Риск гематологических осложнений повышается при почечной недостаточности, дефиците фолиевой кислоты и при сочетанном использовании МТ с салицилатами и препаратами, обладающими антифолатной активностью, особенно триметопримом/сульфаметоксазолом. Изредка встречается алопеция или кожный васкулит.
– Очень редким осложнением лечения МТ является пневмонит (1-8%), обусловленный аллергической реакцией на этот препарат. Он описан исключительно у больных РА.
– Транзиторное увеличение, уровня трансаминаз, нарастающее при повышении дозы МТ, нередкий побочный эффект этого препарата. Двух-, трехкратное увеличение их концентрации не является основанием для его отмены, но более существенное их нарастание свидетельствует о необходимости снижения дозы препарата или прекращения лечения им.
– Лечение низкими дозами МТ может сопровождаться увеличением чувствительности к инфекционным осложнениям. Развитие инфекции является основанием для отмены МТ.
3. Внутривенный иммуноглобулин
1) В последнее время для лечения васкулитов применяют иммуноглобулин, вводимый внутривенно. Этот препарат используется в клинической практике для терапии аутоиммунных заболеваний в течение уже более 15 лет. Полагают, что терапевтическая эффективность применения ВВИГ при аутоиммунных заболеваниях и васкулитах опосредуется через следующие механизмы (см. приложение).
Схема применения ВВИГ в настоящее время не стандартизирована. Обычно его доза варьирует от 0,4 до 2 г/кг/сутки. Препарат вводится внутривенно в течение 3-5 дней. При необходимости его инфузии повторяют 1 раз каждые 4 недели.
2) Терапия ВВИГ является относительно безопасным методом лечения, однако у отдельных больных развиваются побочные реакции. Наиболее часто они обусловлены высокой скоростью инфузии препарата. К ним относятся головные боли, лихорадка, ознобы, затруднения дыхания, боли в животе и спине, умеренная гипотензия. Для уменьшения выраженности этих реакций показано профилактическое назначение антигистаминных препаратов или небольших доз ГК. Истинные анафилактические реакции при введении ВВИГ встречаются довольно редко. Описано развитие симптомов, напоминающих асептический менингит и гемолитическую анемию, связанную с присутствием агглютининов в препарате ВВИГ. Кроме того, потенциальную опасность представляет трансмиссия инфекционных агентов. Но это наблюдается крайне редко.
3) При системных васкулитах ВВИГ является препаратом выбора для лечения болезни Кавасаки. В многочисленных исследованиях показано, что его применение приводит к достоверному снижению частоты развития аневризм коронарных артерий и быстрому исчезновению других признаков системного воспаления. Полагают, что его однократное введение в дозе 2 г/кг/сут не уступает по эффективности стандартному курсу лечения, который проводится в течение четырех дней в дозе 0,4 г/кг/сут.
ВВИГ также применяется в терапии гранулематоза Вегенера и МПА (микроскопического полиангиита).
По мнению K. Pirner и соавт ВВИГ, учитывая механизм действия, можно использовать в тех случаях, когда не показаны цитостатические препараты: при инфекционных осложнениях, беременности, до и после хирургического вмешательства.
ВВИГ эффективен при СКВ у больных с тяжелым поражением ЦНС, выраженной тромбоцитопенией, распространенным поражением кожи и слизистых, торпидных к ударным дозам стероидов.
4) Однако, последние данные, касающиеся эффективности внутривенного иммуноглобулина при других формах системных васкулитов, противоречивы. В единственном проспективном двойном слепом плацебо-контролируемом исследовании однократное введение внутривенного иммуноглобулина больным гранулематозом Вегенера и микроскопическим полиартериитом с сохраняющейся клинической активностью, несмотря на двухмесячное лечение глюкокортикоидами и цитотоксиками, привело к достоверному улучшению клинических и лабораторных показателей. Однако положительная динамика сохранялась только в течение 3-х месяцев, после чего различия между основной и контрольной группами нивелировалась. Таким образом, эффективность внутривенного иммуноглобулина (в первую очередь, повторных курсов) при системных васкулитах требует дальнейшего подтверждения.
Табл. Механизмы действия внутривенного иммуноглобулина (ВВИГ)
а) Метотрексат (MТ) относится к группе антиметаболитов, по структуре он близок фолиевой кислоте.
После приема МТ максимальная его концентрация в крови достигается через 2-4 часа. Прием препарата во время еды не влияет на уровень его абсорбции и биодоступности. Элиминация МТ происходит преимущественно в почках за счет клубочковой фильтрации и канальцевой секреции. Время полужизни препарата колеблется от 2 до 6 часов. Недостаточность функции почек приводит к замедлению экскреции МТ и увеличению его токсичности.
Несмотря на достаточно быстрое выведение из крови, полиглютаминовые метаболиты МТ обнаруживаются внутри клеток в течении 7 дней после его однократного приема. Основные механизмы действия этого препарата будут представлены ниже (см. приложение).
а) МТ назначают 3 раза в неделю (per оs или парентерально). Более частый прием препарата, как правило, приводит к увеличению числа острых или хронических токсических реакций. Рекомендуется принимать лекарство в утренние и вечерние часы, с двенадцатичасовым перерывом. Начальная доза МТ в большинстве случаев составляет 7,5 мг/неделю, а в пожилом возрасте 5 мг/неделю. Эффект от назначения препарата оценивается через 4-8 недель. В случае его отсутствия и при нормальной переносимости вещества дозу МТ постепенно увеличивают на 2,5 мг в неделю, максимально до 25 мг. Обычно при системных васкулитах доза этого препарата составляет 12,5-17,5 мг в неделю.
– При повышении дозы МТ оценка токсичности проводиться через 6 дней после приема препарата, а при достижении общего количества принятого препарата в 1500 мг показана биопсия печени. Парентеральное введение МТ используется при отсутствии эффекта от приема per os или при развитии токсических реакций со стороны желудочно-кишечного тракта. Необходимо иметь в виду, что в ряде случаев отсутствие эффекта при энтеральном введении МТ связано не столько с неэффективностью самого препарата, сколько с низкой абсорбцией его в желудочно-кишечном тракте, не позволяющей достичь оптимальной концентрации вещества в крови.
– В настоящее время изучается эффективность низких доз метотрексата (0,15 – 0,3 мг/кг/нед) в сочетании с высокими дозами преднизолона (1мг/кг/сут) у пациентов с кожной формой узелкового полиартериита и гранулематозом Вегенера без угрожающих жизни осложнений.
в) Побочные эффекты от применения МТ обычно включают тошноту и рвоту, которые появляются через 1-8 дней после начала приема препарата и длятся 1-3 дня. Для уменьшения выраженности этих явлений дозу МТ снижают, или вводят его парентерально. Рекомендуется также назначение симптоматических средств, например метоклопрамида. Относительным противопоказанием к применению МТ являются язвы желудка и двенадцатиперстной кишки. В 6% случаев причиной отмены препарата служит стоматит.
– Тяжелые гематологические нарушения развиваются нечасто. Риск гематологических осложнений повышается при почечной недостаточности, дефиците фолиевой кислоты и при сочетанном использовании МТ с салицилатами и препаратами, обладающими антифолатной активностью, особенно триметопримом/сульфаметоксазолом. Изредка встречается алопеция или кожный васкулит.
– Очень редким осложнением лечения МТ является пневмонит (1-8%), обусловленный аллергической реакцией на этот препарат. Он описан исключительно у больных РА.
– Транзиторное увеличение, уровня трансаминаз, нарастающее при повышении дозы МТ, нередкий побочный эффект этого препарата. Двух-, трехкратное увеличение их концентрации не является основанием для его отмены, но более существенное их нарастание свидетельствует о необходимости снижения дозы препарата или прекращения лечения им.
– Лечение низкими дозами МТ может сопровождаться увеличением чувствительности к инфекционным осложнениям. Развитие инфекции является основанием для отмены МТ.
3. Внутривенный иммуноглобулин
1) В последнее время для лечения васкулитов применяют иммуноглобулин, вводимый внутривенно. Этот препарат используется в клинической практике для терапии аутоиммунных заболеваний в течение уже более 15 лет. Полагают, что терапевтическая эффективность применения ВВИГ при аутоиммунных заболеваниях и васкулитах опосредуется через следующие механизмы (см. приложение).
Схема применения ВВИГ в настоящее время не стандартизирована. Обычно его доза варьирует от 0,4 до 2 г/кг/сутки. Препарат вводится внутривенно в течение 3-5 дней. При необходимости его инфузии повторяют 1 раз каждые 4 недели.
2) Терапия ВВИГ является относительно безопасным методом лечения, однако у отдельных больных развиваются побочные реакции. Наиболее часто они обусловлены высокой скоростью инфузии препарата. К ним относятся головные боли, лихорадка, ознобы, затруднения дыхания, боли в животе и спине, умеренная гипотензия. Для уменьшения выраженности этих реакций показано профилактическое назначение антигистаминных препаратов или небольших доз ГК. Истинные анафилактические реакции при введении ВВИГ встречаются довольно редко. Описано развитие симптомов, напоминающих асептический менингит и гемолитическую анемию, связанную с присутствием агглютининов в препарате ВВИГ. Кроме того, потенциальную опасность представляет трансмиссия инфекционных агентов. Но это наблюдается крайне редко.
3) При системных васкулитах ВВИГ является препаратом выбора для лечения болезни Кавасаки. В многочисленных исследованиях показано, что его применение приводит к достоверному снижению частоты развития аневризм коронарных артерий и быстрому исчезновению других признаков системного воспаления. Полагают, что его однократное введение в дозе 2 г/кг/сут не уступает по эффективности стандартному курсу лечения, который проводится в течение четырех дней в дозе 0,4 г/кг/сут.
ВВИГ также применяется в терапии гранулематоза Вегенера и МПА (микроскопического полиангиита).
По мнению K. Pirner и соавт ВВИГ, учитывая механизм действия, можно использовать в тех случаях, когда не показаны цитостатические препараты: при инфекционных осложнениях, беременности, до и после хирургического вмешательства.
ВВИГ эффективен при СКВ у больных с тяжелым поражением ЦНС, выраженной тромбоцитопенией, распространенным поражением кожи и слизистых, торпидных к ударным дозам стероидов.
4) Однако, последние данные, касающиеся эффективности внутривенного иммуноглобулина при других формах системных васкулитов, противоречивы. В единственном проспективном двойном слепом плацебо-контролируемом исследовании однократное введение внутривенного иммуноглобулина больным гранулематозом Вегенера и микроскопическим полиартериитом с сохраняющейся клинической активностью, несмотря на двухмесячное лечение глюкокортикоидами и цитотоксиками, привело к достоверному улучшению клинических и лабораторных показателей. Однако положительная динамика сохранялась только в течение 3-х месяцев, после чего различия между основной и контрольной группами нивелировалась. Таким образом, эффективность внутривенного иммуноглобулина (в первую очередь, повторных курсов) при системных васкулитах требует дальнейшего подтверждения.
Табл. Механизмы действия внутривенного иммуноглобулина (ВВИГ)
 4. Плазмаферез
1) Его механизмы действия связаны с улучшением функциональной активности ретикулоэндотелиальной системы, удалением аутоантител, ЦИК и воспалительных медиаторов из кровяного русла (см. приложение).
2) Полагают, что проведение при СКВ наиболее оправдано у больных с криоглобулинемией, повышением вязкости крови, тромботической тромбоцитопейической пурпурой, тяжелым васкулитом, с резистентными к ГК и цитостатикам формами пролиферативного нефрита, а также аутоиммунной гемолитической анемией, АФС и геморрагическим волчаночным пневмонитом.
При системных васкулитах плазмаферез в сочетании с ГК применяют для лечения УП, ассоциированного с вирусом гепатита В; эссенциального криоглобулинемического васкулита, гранулематоза Вегенера.
По мнению многих авторов показанием к применению плазмафереза при системных васкулитах является острое, прогрессирующее течение заболеваний, проявляющееся быстропрогрессирующим нефритом и тяжелым васкулитом.
Сообщается об эффективности повторных процедур малообъемного плазмафереза при артериите Такаясу (750-1000 мл/сут).
3) Общая частота осложнений при проведении плазмафереза колеблется от 4,5 до 25%.
Табл. Рекомендации по применению плазмафереза
4. Плазмаферез
1) Его механизмы действия связаны с улучшением функциональной активности ретикулоэндотелиальной системы, удалением аутоантител, ЦИК и воспалительных медиаторов из кровяного русла (см. приложение).
2) Полагают, что проведение при СКВ наиболее оправдано у больных с криоглобулинемией, повышением вязкости крови, тромботической тромбоцитопейической пурпурой, тяжелым васкулитом, с резистентными к ГК и цитостатикам формами пролиферативного нефрита, а также аутоиммунной гемолитической анемией, АФС и геморрагическим волчаночным пневмонитом.
При системных васкулитах плазмаферез в сочетании с ГК применяют для лечения УП, ассоциированного с вирусом гепатита В; эссенциального криоглобулинемического васкулита, гранулематоза Вегенера.
По мнению многих авторов показанием к применению плазмафереза при системных васкулитах является острое, прогрессирующее течение заболеваний, проявляющееся быстропрогрессирующим нефритом и тяжелым васкулитом.
Сообщается об эффективности повторных процедур малообъемного плазмафереза при артериите Такаясу (750-1000 мл/сут).
3) Общая частота осложнений при проведении плазмафереза колеблется от 4,5 до 25%.
Табл. Рекомендации по применению плазмафереза
 Наиболее часто вртречается кардиогенный шок, анафилактические и цитратные реакции. Инфекционные осложнения встречаются крайне редко. Возможно развитие синдрома «рикошета» (удаление аутоантител стимулирует их синтез), который особенно часто наблюдается у больных с активным воспалительным процессом.
Итак, подводя итог вышесказанному, хочу подчеркнуть еще раз.
5. Комбинированная терапия системных васкулитов
Результаты клинических исследований свидетельствует о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым, быстропрогрессирующим поражением сосудов мелкого калибра. В этих случаях проводится комбинированная терапия ГК и ЦФ, включая пульс -терапию ими.
В настоящее время имеется тенденция к более раннему назначению этих групп препаратов (см. приложение).
Назначение ГК в сочетании с азатиоприном и МТ также позволяет добиться большего клинического эффекта, чем изолированное применение этих препаратов. Большинство исследователей предпочитают в начале использовать ЦФ, а азатиоприн применяют как препарат второго ряда при достижении ремиссии. У некоторых больных гранулематозом Вегенера назначение ГК и МТ рассматривается как альтернатива классической терапии, но эти препараты обычно применяют у пациентов без тяжелого поражения легких и почек или при непереносимости циклофосфамида.
Гиганто-клеточный артериит хорошо контролируется ГК. При этом заболевании ЦФ обычно назначают дополнительно, в виде пульс – терапии при офтальмонологических нарушениях. При ГКА не доказано преимущество комбинированной терапии ГК и МТ над изолированным применением преднизолона. У большинства больных артериитом Такаясу наблюдается положительная динамика при монотерапии ГК. Однако часть из них стероидорезистентна: В этих случаях к преднизолону добавляют метотрексат или проводят пульс – терапию ГК и ЦФ. Применение пульс – терапии ГК и ЦФ или per os также показано при быстро прогрессирующем облитерирующем тромбангиите до развития полной облитерации магистральных артерий нижних или верхних конечностей.
В ряде случаев введение преднизолона и ЦФ комбинируют с процедурами плазмафереза. Такая тактика предпочтительнее для ведения больных при фульминантном течении васкулита, сопровождающемся нарушением функции жизненно важных органов, и при артериите Такаясу.
При УП, ассоциированном с вирусом гепатита В, как у взрослых так и у детей показано назначение противовирусных препаратов и преднизолона в средних дозах в сочетании с повторными процедурами плазмафереза.
6. Пульс – синхронизация
В настоящее время разработана схема, получившая название «пульс – синхронизация», которая, как полагают, способствует увеличению эффективности цитотоксической терапии. Суть этого метода заключается в отмене на четыре недели поддерживающей терапии ГК и цитотоксическими препаратами, что вызывает стимуляцию пролиферации лимфоидных клеток и развитие синдрома «рикошета». Последний купируется тремя циклами интенсивного плазмафереза и высокими дозами ЦФ. Предполагается, что такое лечение позволяет добиться более эффективной элиминации патологических клонов клеток, синтезирующих аутоантитела.
С.К. Соловьев и В. А. Насонова сформулировали принципы применения синхронной интенсивной терапии с последовательным назначением экстракорпоральных процедур плазмафереза или гемосорбции и ударных доз метилпреднизолона и ЦФ для лечения СКВ. Аналогичная схема используется и педиатрами при острых и молниеносных формах УП. Однако для других форм васкулитов «пульс – синхронизация» еще не разработана. Что касается ВВИГ в комбинации с ГК, то он с успехом применяется при гранулематозе Вегенера и некоторых других васкулитах.
Большинство авторов в комбинированную терапию васкулитов рекомендуют включать и другие препараты, влияющие на реологические свойства крови (гепарин, фраксипарин), дезагреганты (пентоксифиллин, тиклид, аспирин), препараты простагландина Е, (вазапростан) и простациклина (илопрост), а также периферические вазодилататоры. Важной составляющей терапии васкулитов является профилактика развития инфекции и поражения ЖКТ. Кроме того, учитывая увеличение продолжительности жизни больных васкулитами и возможности развития у них раннего атеросклероза, СС осложнений, необходимо в целях профилактики назначать препараты, обладающие противовоспалительным, антитромботическим и гиподемическим действием (плаквенил, делагин, аспирин, пентоксифиллин).
Итак, другие препараты и методы лечения.
7. Пентоксифилин
Пентоксифилин (трентал) – ингиботор ксантиновой фосфодиэстеразы, который улучшает доставку кислорода к тканям при перифирических сосудистых заболеваниях человека.
Этот препарат широко применяется для лечения системных васкулитов, особенно при вазоспастическом и ишемическом синдромах, поражениях кожи и почек. В настоящее время получены клинические и экспериментальные факты, свидетельствующие о его противовоспалительном иммуномодулирующем эффекте, снижение нефротоксичности и потенцирование эффекта ЦСА, а также усиление противовоспалительного действия метотрексата. Является важным дополнением к терапии ГК и ЦФ. Некоторые рассматривают его как базисный препарат для лечения геморрагического васкулита.
Лечение пентоксифиллином обычно начинают с внутривенных капельных инфузий по 200-300 мг/сутки в 200 мл физиологического раствора. Курс лечения состоит из 10 – 15 инъекций. Непосредственно после окончания инфузионной терапии переходят на пероральный прием препарата по 600-800 мг/сутки в течение 30-40 дней с последующим снижением дозы до 200-300 мг/сутки и ее приемом в течение длительного времени (6-12 мес).
Нередко внутривенное введение пентоксифиллина сочетают с реополиглюкином, который снижает вязкость крови, уменьшает агрегацию тромбоцитов и эритроцитов, а также обладает антитромботическим эффектом.
Е.Н. Семенкова и О.Г. Кривошееев при геморрагическом васкулите считают наиболее эффективным использование пентоксифиллина в дозе 1000-1200 мг/сутки в сочетании с дапсоном (100-200 мг/сутки).
8. Циклоспорин А
1) Наряду с имуносупрессивной активностью, ЦСА в фармакологических концентрациях проявляет определенные противовоспалительные эффекгы, ингибируя высвобождение гистамина, триптазы и синтез лейкотриенов базофилами и тучными клетками.
2) В начале лечения ЦСА назначают в дозе 2-3 мг/кг/сутки в 1 или 2 приема в течение 4-8 недель. При неэффективности препарата его дозу постепенно увеличивают на 0,5 – 1,0 мг/кг/сутки до максимальной 5 мг/кг/сутки. При стабилизации процесса в течение 3 месяцев рекомендуется очень медленное ее снижение (по 0,5 мг/кг за 1 месяц) до минимально эффективной. При отсутствии эффекта в течение 6 месяцев на фоне приема оптимально переносимой дозы препарата продолжение лечения нецелесообразно.
3) В процессе лечения особое внимание следует уделить динамике уровня креатинина в сыворотке, увеличение которого более чем на 30% от исходного диктует необходимость немедленного уменьшения дозы ЦСА. Препарат не следует назначать больным с нарушенной функцией почек, тяжелой артериальной гипертензией, инфекционными заболеваниями и злокачественными новообразованиями.
В то же время, на фоне лечения ЦСА наблюдается развитее некоторых специфических осложнений, наиболее тяжелым из которых является поражение почек.
ЦСА вызывает так называемую функциональную нефротоксичность, приводящую к увеличению концентрации креатинина и мочевины. Она связана с вазоконстрикцией афферентных артериол клубочков, ведущей к снижению почечного кровотока и четко коррелирует с дозой препарата, но обычно не сопровождается явными морфологическими нарушениями.
У 5-15 % больных ЦСА вызывает зависимое от дозы повышение диастолического артериального давления в среднем на 2-3 мм рт. ст. при дозе 2,5 мг/кг/сутки и на 5 мм рт. ст. при дозе 5 мг/кг/сугки.
Препаратами выбора при лечении артериальной гипертензии вызванной ЦСА, являются антагонисты Са: нифедипин или исрадипин, которые в отличие от дилтиазема и верапамила существенно не влияют на фармакокинетику ЦСА.
К другим побочным реакциям относятся гипертрихоз, гиперплазия слизистой полости рта, парастезии, тремор, желудочно-кишечные расстройства, умеренная гипербилирубинемия, анемия. Обычно они развиваются через несколько дней после начала лечения ЦСА и затем исчезают, несмотря на его продолжение. При синдроме Бехчета у больных с активным увеитом ЦСА в дозе 2,5 мг/кг/сутки более эффективен, чем пульс-терапия. Имеются сообщения об успешном применении ЦСА (5 мг/кг/сутки) в сочетании с ГК у больных, резистентных к ЦФ. Создается впечатление, что ЦСА в ряде случаев может быть альтернативой ЦФ, который, хотя и обладает высокой клинической эффективностью при гранулематозе Вегенера, нередко вызывает инфекционные осложнения.
Кроме того, имеется наблюдение успешного лечения некротизирующею ревматоидного васкулита этим препаратом в дозе 4 мг/кг/сутки на фоне применения преднизолона в комбинации с вазапростаном в течение 16 недель.
В ряде работ отмечается положительный эффект от назначения ЦСА при рецидивирующем полихондрите, синдроме Вебера-Крисгена и гангренозной пиодермии.
9. Аминохинолиновые препараты
По данным токсилогических исследований, хлорохин примерно в 2-3 раза токсичнее плаквенила.
Эти препараты редко используются для лечения васкулитов. Они не относятся к препаратам первого ряда. Однако многочисленные противовоспалительные эффекты делагила и гидроксихлорохина (плаквенила) позволяют рекомендовать их к включению в комбинированную терапию васкулитов.
В недавних исследованиях было показано, что плаквенил обладает определенной антивирусной активностью.
Аминохинолиновые препараты подавляют агрегацию и адгезию тромбоцитов, снижают вязкость крови и уменьшают размер тромба.
Антималярийные препараты обладают гиполипидемическим действием. Эти данные свидетельствуют о том, что препараты следует включать в комбинированную терапию больных васкулитами с повышенным риском развития сердечно-сосудистых осложнений и, вероятно, длительно получающих ГК. Обычно, суточная доза плаквенила 400 мг (6,5 мг/кг), а хлорохина – 250 мг (4,0 мг/кг). Препараты хорошо переносятся. Частым осложнением является кожная сыпь. Наиболее грозным побочным эффектом этих препаратов является поражение глаз (ретинопатия). К ним относятся: центральная скотома, сужение периферических полей зрения, позднее общее ухудшение зрения. Однако плаквенил реже вызывает ретинопатию, чем хлорохин.
10. Энзимные препараты
В последнее время для лечения сосудистых заболеваний используют препараты, которые являются комбинацией ферментов растительного и животного происхождения. К ним относятся вобэнзим, флогензим, мульсал. Имеются данные о том, что они снижают вязкость крови, ускоряют фибринолиз, повышают деформируемость эритроцитов, подавляют агрегацию их и тромбоцитов, ингибируют выработку ИЛ-1 и ФНО-a. Обнаружен их иммуномодулирующей эффект на субпопуляции Т-лимфоцитов, проявляющийся в нормализации существующего дисбаланса этих клеток в организме человека. Однако при системных васкулитах эти препараты следует назначать в комбинации с ГК и ЦФ.
11. Противовирусные препараты.
Как уже отмечалось, при некоторых формах васкулитов важное значение в патогенезе имеет инфекция вирусами гепатита В и С. При наличии маркеров репликации этих вирусов показано назначение препаратов интерферона (реальдерон, ИФ-a) в сочетании с ГК и плазмаферезом. В отдельных клинических наблюдениях описаны положительные результаты лечения ИФ-a язвенного поражения слизистой полости рта при болезни Бехчета и глазных проявлениях заболевания.
12. Аспирин
Аспирин (ацетилсалициловая кислота) является одним из основных фармакологических средств, применяющихся для терапии различных состояний с повышенной агрегацией тромбоцитов. После однократного его приема значительный дезагрегирующий эффект на тромбоциты длится в течение 4-7 дней. Он обусловлен блокадой аспирином циклооксигеназного пути метаболизма арахидоновой кислоты и более выражен в тромбоцитах, чем в эндотелии сосудов. Применение аспирина при васкулитах связано со следующими его механизмами:
Наиболее часто вртречается кардиогенный шок, анафилактические и цитратные реакции. Инфекционные осложнения встречаются крайне редко. Возможно развитие синдрома «рикошета» (удаление аутоантител стимулирует их синтез), который особенно часто наблюдается у больных с активным воспалительным процессом.
Итак, подводя итог вышесказанному, хочу подчеркнуть еще раз.
5. Комбинированная терапия системных васкулитов
Результаты клинических исследований свидетельствует о низкой эффективности монотерапии ГК, особенно при системных некротизирующих васкулитах, характеризующихся тяжелым, быстропрогрессирующим поражением сосудов мелкого калибра. В этих случаях проводится комбинированная терапия ГК и ЦФ, включая пульс -терапию ими.
В настоящее время имеется тенденция к более раннему назначению этих групп препаратов (см. приложение).
Назначение ГК в сочетании с азатиоприном и МТ также позволяет добиться большего клинического эффекта, чем изолированное применение этих препаратов. Большинство исследователей предпочитают в начале использовать ЦФ, а азатиоприн применяют как препарат второго ряда при достижении ремиссии. У некоторых больных гранулематозом Вегенера назначение ГК и МТ рассматривается как альтернатива классической терапии, но эти препараты обычно применяют у пациентов без тяжелого поражения легких и почек или при непереносимости циклофосфамида.
Гиганто-клеточный артериит хорошо контролируется ГК. При этом заболевании ЦФ обычно назначают дополнительно, в виде пульс – терапии при офтальмонологических нарушениях. При ГКА не доказано преимущество комбинированной терапии ГК и МТ над изолированным применением преднизолона. У большинства больных артериитом Такаясу наблюдается положительная динамика при монотерапии ГК. Однако часть из них стероидорезистентна: В этих случаях к преднизолону добавляют метотрексат или проводят пульс – терапию ГК и ЦФ. Применение пульс – терапии ГК и ЦФ или per os также показано при быстро прогрессирующем облитерирующем тромбангиите до развития полной облитерации магистральных артерий нижних или верхних конечностей.
В ряде случаев введение преднизолона и ЦФ комбинируют с процедурами плазмафереза. Такая тактика предпочтительнее для ведения больных при фульминантном течении васкулита, сопровождающемся нарушением функции жизненно важных органов, и при артериите Такаясу.
При УП, ассоциированном с вирусом гепатита В, как у взрослых так и у детей показано назначение противовирусных препаратов и преднизолона в средних дозах в сочетании с повторными процедурами плазмафереза.
6. Пульс – синхронизация
В настоящее время разработана схема, получившая название «пульс – синхронизация», которая, как полагают, способствует увеличению эффективности цитотоксической терапии. Суть этого метода заключается в отмене на четыре недели поддерживающей терапии ГК и цитотоксическими препаратами, что вызывает стимуляцию пролиферации лимфоидных клеток и развитие синдрома «рикошета». Последний купируется тремя циклами интенсивного плазмафереза и высокими дозами ЦФ. Предполагается, что такое лечение позволяет добиться более эффективной элиминации патологических клонов клеток, синтезирующих аутоантитела.
С.К. Соловьев и В. А. Насонова сформулировали принципы применения синхронной интенсивной терапии с последовательным назначением экстракорпоральных процедур плазмафереза или гемосорбции и ударных доз метилпреднизолона и ЦФ для лечения СКВ. Аналогичная схема используется и педиатрами при острых и молниеносных формах УП. Однако для других форм васкулитов «пульс – синхронизация» еще не разработана. Что касается ВВИГ в комбинации с ГК, то он с успехом применяется при гранулематозе Вегенера и некоторых других васкулитах.
Большинство авторов в комбинированную терапию васкулитов рекомендуют включать и другие препараты, влияющие на реологические свойства крови (гепарин, фраксипарин), дезагреганты (пентоксифиллин, тиклид, аспирин), препараты простагландина Е, (вазапростан) и простациклина (илопрост), а также периферические вазодилататоры. Важной составляющей терапии васкулитов является профилактика развития инфекции и поражения ЖКТ. Кроме того, учитывая увеличение продолжительности жизни больных васкулитами и возможности развития у них раннего атеросклероза, СС осложнений, необходимо в целях профилактики назначать препараты, обладающие противовоспалительным, антитромботическим и гиподемическим действием (плаквенил, делагин, аспирин, пентоксифиллин).
Итак, другие препараты и методы лечения.
7. Пентоксифилин
Пентоксифилин (трентал) – ингиботор ксантиновой фосфодиэстеразы, который улучшает доставку кислорода к тканям при перифирических сосудистых заболеваниях человека.
Этот препарат широко применяется для лечения системных васкулитов, особенно при вазоспастическом и ишемическом синдромах, поражениях кожи и почек. В настоящее время получены клинические и экспериментальные факты, свидетельствующие о его противовоспалительном иммуномодулирующем эффекте, снижение нефротоксичности и потенцирование эффекта ЦСА, а также усиление противовоспалительного действия метотрексата. Является важным дополнением к терапии ГК и ЦФ. Некоторые рассматривают его как базисный препарат для лечения геморрагического васкулита.
Лечение пентоксифиллином обычно начинают с внутривенных капельных инфузий по 200-300 мг/сутки в 200 мл физиологического раствора. Курс лечения состоит из 10 – 15 инъекций. Непосредственно после окончания инфузионной терапии переходят на пероральный прием препарата по 600-800 мг/сутки в течение 30-40 дней с последующим снижением дозы до 200-300 мг/сутки и ее приемом в течение длительного времени (6-12 мес).
Нередко внутривенное введение пентоксифиллина сочетают с реополиглюкином, который снижает вязкость крови, уменьшает агрегацию тромбоцитов и эритроцитов, а также обладает антитромботическим эффектом.
Е.Н. Семенкова и О.Г. Кривошееев при геморрагическом васкулите считают наиболее эффективным использование пентоксифиллина в дозе 1000-1200 мг/сутки в сочетании с дапсоном (100-200 мг/сутки).
8. Циклоспорин А
1) Наряду с имуносупрессивной активностью, ЦСА в фармакологических концентрациях проявляет определенные противовоспалительные эффекгы, ингибируя высвобождение гистамина, триптазы и синтез лейкотриенов базофилами и тучными клетками.
2) В начале лечения ЦСА назначают в дозе 2-3 мг/кг/сутки в 1 или 2 приема в течение 4-8 недель. При неэффективности препарата его дозу постепенно увеличивают на 0,5 – 1,0 мг/кг/сутки до максимальной 5 мг/кг/сутки. При стабилизации процесса в течение 3 месяцев рекомендуется очень медленное ее снижение (по 0,5 мг/кг за 1 месяц) до минимально эффективной. При отсутствии эффекта в течение 6 месяцев на фоне приема оптимально переносимой дозы препарата продолжение лечения нецелесообразно.
3) В процессе лечения особое внимание следует уделить динамике уровня креатинина в сыворотке, увеличение которого более чем на 30% от исходного диктует необходимость немедленного уменьшения дозы ЦСА. Препарат не следует назначать больным с нарушенной функцией почек, тяжелой артериальной гипертензией, инфекционными заболеваниями и злокачественными новообразованиями.
В то же время, на фоне лечения ЦСА наблюдается развитее некоторых специфических осложнений, наиболее тяжелым из которых является поражение почек.
ЦСА вызывает так называемую функциональную нефротоксичность, приводящую к увеличению концентрации креатинина и мочевины. Она связана с вазоконстрикцией афферентных артериол клубочков, ведущей к снижению почечного кровотока и четко коррелирует с дозой препарата, но обычно не сопровождается явными морфологическими нарушениями.
У 5-15 % больных ЦСА вызывает зависимое от дозы повышение диастолического артериального давления в среднем на 2-3 мм рт. ст. при дозе 2,5 мг/кг/сутки и на 5 мм рт. ст. при дозе 5 мг/кг/сугки.
Препаратами выбора при лечении артериальной гипертензии вызванной ЦСА, являются антагонисты Са: нифедипин или исрадипин, которые в отличие от дилтиазема и верапамила существенно не влияют на фармакокинетику ЦСА.
К другим побочным реакциям относятся гипертрихоз, гиперплазия слизистой полости рта, парастезии, тремор, желудочно-кишечные расстройства, умеренная гипербилирубинемия, анемия. Обычно они развиваются через несколько дней после начала лечения ЦСА и затем исчезают, несмотря на его продолжение. При синдроме Бехчета у больных с активным увеитом ЦСА в дозе 2,5 мг/кг/сутки более эффективен, чем пульс-терапия. Имеются сообщения об успешном применении ЦСА (5 мг/кг/сутки) в сочетании с ГК у больных, резистентных к ЦФ. Создается впечатление, что ЦСА в ряде случаев может быть альтернативой ЦФ, который, хотя и обладает высокой клинической эффективностью при гранулематозе Вегенера, нередко вызывает инфекционные осложнения.
Кроме того, имеется наблюдение успешного лечения некротизирующею ревматоидного васкулита этим препаратом в дозе 4 мг/кг/сутки на фоне применения преднизолона в комбинации с вазапростаном в течение 16 недель.
В ряде работ отмечается положительный эффект от назначения ЦСА при рецидивирующем полихондрите, синдроме Вебера-Крисгена и гангренозной пиодермии.
9. Аминохинолиновые препараты
По данным токсилогических исследований, хлорохин примерно в 2-3 раза токсичнее плаквенила.
Эти препараты редко используются для лечения васкулитов. Они не относятся к препаратам первого ряда. Однако многочисленные противовоспалительные эффекты делагила и гидроксихлорохина (плаквенила) позволяют рекомендовать их к включению в комбинированную терапию васкулитов.
В недавних исследованиях было показано, что плаквенил обладает определенной антивирусной активностью.
Аминохинолиновые препараты подавляют агрегацию и адгезию тромбоцитов, снижают вязкость крови и уменьшают размер тромба.
Антималярийные препараты обладают гиполипидемическим действием. Эти данные свидетельствуют о том, что препараты следует включать в комбинированную терапию больных васкулитами с повышенным риском развития сердечно-сосудистых осложнений и, вероятно, длительно получающих ГК. Обычно, суточная доза плаквенила 400 мг (6,5 мг/кг), а хлорохина – 250 мг (4,0 мг/кг). Препараты хорошо переносятся. Частым осложнением является кожная сыпь. Наиболее грозным побочным эффектом этих препаратов является поражение глаз (ретинопатия). К ним относятся: центральная скотома, сужение периферических полей зрения, позднее общее ухудшение зрения. Однако плаквенил реже вызывает ретинопатию, чем хлорохин.
10. Энзимные препараты
В последнее время для лечения сосудистых заболеваний используют препараты, которые являются комбинацией ферментов растительного и животного происхождения. К ним относятся вобэнзим, флогензим, мульсал. Имеются данные о том, что они снижают вязкость крови, ускоряют фибринолиз, повышают деформируемость эритроцитов, подавляют агрегацию их и тромбоцитов, ингибируют выработку ИЛ-1 и ФНО-a. Обнаружен их иммуномодулирующей эффект на субпопуляции Т-лимфоцитов, проявляющийся в нормализации существующего дисбаланса этих клеток в организме человека. Однако при системных васкулитах эти препараты следует назначать в комбинации с ГК и ЦФ.
11. Противовирусные препараты.
Как уже отмечалось, при некоторых формах васкулитов важное значение в патогенезе имеет инфекция вирусами гепатита В и С. При наличии маркеров репликации этих вирусов показано назначение препаратов интерферона (реальдерон, ИФ-a) в сочетании с ГК и плазмаферезом. В отдельных клинических наблюдениях описаны положительные результаты лечения ИФ-a язвенного поражения слизистой полости рта при болезни Бехчета и глазных проявлениях заболевания.
12. Аспирин
Аспирин (ацетилсалициловая кислота) является одним из основных фармакологических средств, применяющихся для терапии различных состояний с повышенной агрегацией тромбоцитов. После однократного его приема значительный дезагрегирующий эффект на тромбоциты длится в течение 4-7 дней. Он обусловлен блокадой аспирином циклооксигеназного пути метаболизма арахидоновой кислоты и более выражен в тромбоцитах, чем в эндотелии сосудов. Применение аспирина при васкулитах связано со следующими его механизмами:
- дезагрегирующим действием на тромбоциты в результате подавления низкими (меньше 100 мг/сутки) дозами этого препарата тромбоцитарной циклооксигеназы-1;
- противовоспалительным действием в результате ингибиции ИЛ-1- зависимой экспрессии циклооксигеназы-2 в культуре эндотелиальных клеток;
- иммуномодулирующим действием (?) через стимуляцию синтеза ИЛ-3.
- усиление кровотока путем прямого расширения кровеносных сосудов;
- активация фибринолиза через стимуляцию синтеза тканевого активатора плазминогена;
- блокада активации тромбоцитов, вызываемой АДФ, тромбином или коллагеном, посредством уменьшения в них количества ионов свободного кальция;
- подавление агрегации тромбоцитов и их адгезии к субэндотелию, уменьшение выброса из них b-тромбоглобулина, серотонина и АДФ, торможение синтеза тромбоксана;
- подавление активации нейтрофилов, высвобождения ими супероксидных ионов, лейкотриена В4; торможение агрегации нейтрофилов, уменьшение их адгезии к эндотелию;
- повышение способности эритроцитов к изменению своей формы, уменьшение агрегации эритроцитов;
- восстановление нормального метаболизма в ишемизированных тканях путем улучшения утилизации кислорода и глюкозы (переход от анаэробного к аэробному клеточному дыханию);
- подавление митотической активности и пролиферации клеток гладкой мускулатуры.
 а) При РА после введения моноклональных анти-СD4+ антител в некоторых случаях наблюдается положительная динамика со стороны внесуставных (язвы голени) проявлений заболевания.
Использование антител позволяет достигнуть длительной ремиссии у больных с тяжелым ревматоидным васкулитом, при гранулематозе Вегенера.
б) При системных васкулитах (гранулематоз Вегенера, артериит Такаясу, узелковый периартериит, гигантоклеточный артериит), по-видимому, наибольшее значение будет иметь введение антител к ФНО-a и молекулам адгезии – инфликсимаб (Ремикейд).
2) В последнее время в клинической практике широко применяются иммунокорректоры животного происхождения, а именно препараты тимуса и их синтетические аналоги.
В нашей стране при васкулитах апробирован препарат тимуса – тактивин который оказался гетерогенным по функциональным свойствам. Тактивин восстанавливает число Т-лимфоцитов у больных со сниженным их содержанием, повышает киллерную активность. В зависимости от дозы влияет на функции естественных киллерных клеток, в низких дозах стимулирует продукцию ИФ–a, Однако его применение в качестве монотерапии при васкулитах неэффективно. Наиболее обосновано назначение этого препарата в сочетании с ГК и ЦФ.
3) В целом новые направления иммунотерапии системных васкулитов связаны с применением биотехнологических препаратов, позволяющих селективно влиять на функциональную активность иммунокомпетентных клеток, синтез цитокинов, экспрессию молекул адгезии и др.
23. Диета
Важное значение в лечении геморрагического васкулита имеет гипоантигенная диета. При эссенциальной криоглобулинемической пурпуре иногда эффективна диета с низким содержанием белка.
24. Местное лечение
1) В ряде случаев при язвенных поражениях кожи важное значение имеет местное лечение, которое должно быть этапным. Возможно наложение примочек или мазей с протеолитическими ферментами. Для примочек используют 0,5 % раствор новокаина с добавлением химопсина (100 мг на 100 мл). Эффективна мазь «Ируксол», которую наносят на очаги поражения 1-2 раза в день на салфетке. Для достижения дезинфицирующего эффекта перед каждой сменой повязки язвенную поверхность промывают перекисью водорода или раствором перманганата калия.
2) После полного очищения язвенных поверхностей от гнойно-некротического струпа используют эпителизирующие и дезинфицирующие средства при сильных болях – с добавлением анестетиков (5% анестезиновая или 5% дерматол-анестезиновая мази, левомеколь, левосин, мазь Вишневского, 10% метилурациловая мазь, пена «Пантенол», коллагеновые губки и т.п.)
3) Для местного лечения целесообразно использовать и препарат аргосульфан (Jelfa), который представляет собой крем с 2% серебряной солью сульфатиазола. Он оказывает выраженное местное антимикробное и болеутоляющее действие. Он эффективен для лечения трофических язв голеней различного генеза.
Препарат аргосульфан хорошо переносится больными. Его необходимо включать для местного лечения язвенных дефектов кожи, развивающихся на фоне различной сосудистой патологии, в том числе системных васкулитов.
25. Другие аспекты васкулитов
Другие аспекты ведения больных с васкулитами связаны с привлечением для их лечения специалистов различного профиля. Развитие осложнений при этих заболеваниях, как правило, требует согласованных действий терапевтов, нефрологов, отоларингологов, невропатологов, хирургов, окулистов и др. В этих ситуациях особенно важен единый подход к лечению васкулитов.
а) При РА после введения моноклональных анти-СD4+ антител в некоторых случаях наблюдается положительная динамика со стороны внесуставных (язвы голени) проявлений заболевания.
Использование антител позволяет достигнуть длительной ремиссии у больных с тяжелым ревматоидным васкулитом, при гранулематозе Вегенера.
б) При системных васкулитах (гранулематоз Вегенера, артериит Такаясу, узелковый периартериит, гигантоклеточный артериит), по-видимому, наибольшее значение будет иметь введение антител к ФНО-a и молекулам адгезии – инфликсимаб (Ремикейд).
2) В последнее время в клинической практике широко применяются иммунокорректоры животного происхождения, а именно препараты тимуса и их синтетические аналоги.
В нашей стране при васкулитах апробирован препарат тимуса – тактивин который оказался гетерогенным по функциональным свойствам. Тактивин восстанавливает число Т-лимфоцитов у больных со сниженным их содержанием, повышает киллерную активность. В зависимости от дозы влияет на функции естественных киллерных клеток, в низких дозах стимулирует продукцию ИФ–a, Однако его применение в качестве монотерапии при васкулитах неэффективно. Наиболее обосновано назначение этого препарата в сочетании с ГК и ЦФ.
3) В целом новые направления иммунотерапии системных васкулитов связаны с применением биотехнологических препаратов, позволяющих селективно влиять на функциональную активность иммунокомпетентных клеток, синтез цитокинов, экспрессию молекул адгезии и др.
23. Диета
Важное значение в лечении геморрагического васкулита имеет гипоантигенная диета. При эссенциальной криоглобулинемической пурпуре иногда эффективна диета с низким содержанием белка.
24. Местное лечение
1) В ряде случаев при язвенных поражениях кожи важное значение имеет местное лечение, которое должно быть этапным. Возможно наложение примочек или мазей с протеолитическими ферментами. Для примочек используют 0,5 % раствор новокаина с добавлением химопсина (100 мг на 100 мл). Эффективна мазь «Ируксол», которую наносят на очаги поражения 1-2 раза в день на салфетке. Для достижения дезинфицирующего эффекта перед каждой сменой повязки язвенную поверхность промывают перекисью водорода или раствором перманганата калия.
2) После полного очищения язвенных поверхностей от гнойно-некротического струпа используют эпителизирующие и дезинфицирующие средства при сильных болях – с добавлением анестетиков (5% анестезиновая или 5% дерматол-анестезиновая мази, левомеколь, левосин, мазь Вишневского, 10% метилурациловая мазь, пена «Пантенол», коллагеновые губки и т.п.)
3) Для местного лечения целесообразно использовать и препарат аргосульфан (Jelfa), который представляет собой крем с 2% серебряной солью сульфатиазола. Он оказывает выраженное местное антимикробное и болеутоляющее действие. Он эффективен для лечения трофических язв голеней различного генеза.
Препарат аргосульфан хорошо переносится больными. Его необходимо включать для местного лечения язвенных дефектов кожи, развивающихся на фоне различной сосудистой патологии, в том числе системных васкулитов.
25. Другие аспекты васкулитов
Другие аспекты ведения больных с васкулитами связаны с привлечением для их лечения специалистов различного профиля. Развитие осложнений при этих заболеваниях, как правило, требует согласованных действий терапевтов, нефрологов, отоларингологов, невропатологов, хирургов, окулистов и др. В этих ситуациях особенно важен единый подход к лечению васкулитов. 

