Ирина Александровна Зборовская – директор Федерального бюджетного государственного учреждения «Научно-исследовательский институт клинической и экспериментальной ревматологии» РАМН, профессор кафедры госпитальной терапии с курсом клинической ревматологии факультета усовершенствования врачей Волгоградского государственного медицинского университета, д.м.н.
Лечение гастропатий, индуцированных нестероидными противовоспалительными препаратами (НПВП), является не только актуальной проблемой, но и сложной задачей, так как, большинству больных не удается отменить прием НПВП в связи с высоким риском обострения основного заболевания, по поводу которого пациент их систематически принимает.
В тактике ведения таких больных, у которых диагностируются гастродуоденальные осложнения или имеются факторы риска НПВП – гастропатии, можно выделить два взаимосвязанных подхода:
- Оптимизация применения НПВП
- Противоязвенная терапия, которая должна проводиться дифференцированно, в зависимости от того, направлена ли она на профилактику или на лечение НПВП – гастропатий.
I. Оптимизация применения НПВП включает следующие основные положения
1. При появлении любых гастроэнтерологоческих побочных эффектов необходимо решить вопрос о целесообразности дальнейшего приема НПВП.
Отмена препарата хотя и не приводит к «излечиванию», но повышает эффективность противоязвенной терапии и снижает риск рецидивирования эрозивно-язвенного процесса в ЖКТ.
2. При невозможности полностью отказаться от приема НПВП следует максимально уменьшить дозу и лечение проводить под эндоскопическим контролем.
3. Эффективным способом снижения риска НПВП – гастропатии является использование НПВП с наименьшими побочными эффектами (ибупрофен, диклофенак), а также использование препаратов, обладающих более высокой селективностью в отношении ЦОГ-2 (мовалис, нимесулид = найз, целебрекс). Итак, это основные положения оптимизации лечения.
Необходимо отметить, что переход на парентеральное, ректальное введение НПВП, а также использование препаратов с кишечным покрытием не снижает риска эрозивно-язвенных поражений и не оказывает существенного влияния на скорость рубцевания на фоне противоязвенной терапии, что еще раз подтверждает положение:
гастропатии, индуцированные НПВП следует считать не местным, а системным побочным эффектом НПВП, связанным прежде всего с подавлением синтеза простагладинов и уже затем с прямым повреждающим эффектом на слизистую оболочку ЖКТ (желудочно-кишечного тракта).
II. Противоязвенная терапия в лечении НПВП – гастропатий.
1. В лечении НПВП – гастропатий, исходя из всего выше сказанного, патогенетически обосновано применение 3-х групп лекарственных препаратов
1 гр.- Синтетические аналоги простагладина Е
1: мизопростол, сайтотек, цитотек.
2 гр. – Блокаторы Н
2 – рецепторов гистамина: ранитидин, фамотидин (II поколение), квамател (III поколение).
3 гр. – Ингибиторы протоновой помпы: омепразол (Омез), ланзопразол (ланзап) рабепразол (париет).
2-я и 3-я группы препаратов представляют собой класс антисекреторных средств.
Обоснованием для назначения антисекреторных препаратов, блокирующих выработку соляной кислоты является:
во-первых: снижение обратной диффузии ионов водорода и их повреждающего действия на слизистую оболочку;
во-вторых: падение активности пепсина или его инактивация при повышении интрагастрального рН до 4,0 и выше, что приводит к снижению агрессивных свойств желудочного сока;
в-третьих: при высоком внутрижелудочном уровне рН резко падает диффузия ионов водорода в слизистую оболочку.
Длительная супрессия кислотной продукции желудка с поддержанием интрагастрального уровня рН выше 4,0 и особенно на уровне 6,0 является одной из главных задач лечения гастропатии, ассоциированной с приемом НПВП, которую с успехом решают именно антисекреторные препараты.
Установлено, что подавление кислотной продукции приводит к рубцеванию язв и эпителизации эрозий желудка даже у больных, продолжающих прием НПВП.
В лечении гастропатии обоснованно и применение синтетических аналогов простагладина Е
1 (мизопростола), который можно считать средством заместительной терапии.
Эффект мизопростола связан с его способностью стимулировать продукцию бикарбонатов и слизи, поддерживать нормальный местный кровоток и целостность слизистой оболочки как защитного барьера. Мизопростол усиливает пролиферацию эпителия слизистой оболочки в ответ на повреждение.
2. Для оценки и подтверждения этого положения необходимо вспомнить, как работает париетальная, клетка, синтезирующая соляную кислоту.
Очень кратко!
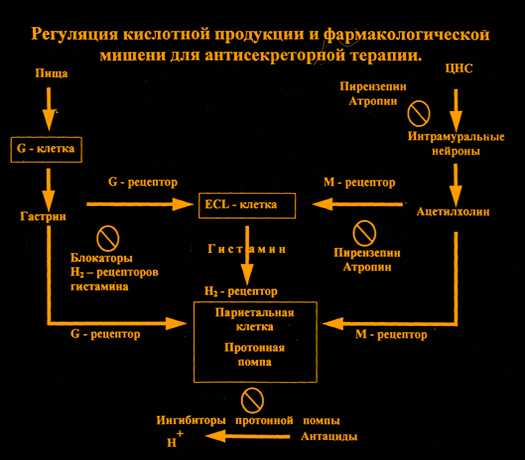
На рисунке схематично представлен механизм работы париетальной клетки, непосредственно отвечающий за кислотную продукцию.
На базолатеральной мембране париетальной клетки располагается ряд рецепторов (М-холинорецепторы, Н
2-рецепторы гистамина, гастриновые рецепторы), которые регулируют секреторную активность клетки.
Стимуляция этих рецепторов ведет (через ряд промежуточных реакций) к стимуляции протонной помпы (ПП) ,т.е. активности Н
+К
+ АТФ-азы, которая участвует в заключительной стадии синтеза HCl и за счет энергии АТФ переносит ионы водорода в просвет железы из клетки обменивая их на ионы К из внеклеточного пространства. Ионы Н
+ в просвете железы соединяются с ионами Cl и образуется HCl.
3 Наиболее эффективными препаратами при лечении гастродуоденальных язв и эрозий являются ингибиторы протонной помпы (ИПП).
Схема: Регуляция кислотной продукции и фармакологические мишени для антисекреторной терапии.
1) ИПП угнетая активность (именно) фермента Н
+К
+ АТФ-азу (водородно-калиевую АТФ-азу), блокируют тем самым заключительную стадию синтеза соляной кислоты.
В результате происходит значительное снижение уровня базальной и стимулированной секреции, независимо от стимулирующего фактора.
Это выгодно отличает ИПП от других антисекреторных препаратов, в том числе блокаторов Н
2 – рецепторов, которые блокируют лишь один из множества механизмов секреции HCl (соляной кислоты).
Высокая эффективность ИПП превосходящая эффективность блокаторов Н
2 – рецепторов гистамина и мизопростола подтверждена многочисленными исследованиями, отвечающими требованиям доказательной медицины.
2) В последние 5 лет проведен целый ряд широкомасштабных клинических исследований по изучению сравнительной эффективности основных групп препаратов, используемых в лечении НПВП – гастропатий.
Особый интерес представляют международные исследования OMNION и ASTRONAVT.
В исследовании OMNION проводилось (таблица 1) сравнение эффективности Омеза и мизопростола в лечении язв и эрозий, вызванных НПВП по данным 93-х центров Европейских стран, а также США, Канады, Австралии и Новой Зеландии.
Таблица 1.
Заживление (в %) эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП, через 8 недель лечения.
| Препарат |
ЯБЖ |
ЯБДПК |
Эрозии |
| Омепразол 20 мг |
87 |
93 |
77 |
| Омепразол 40 мг |
80 |
89 |
79 |
| Мизопростол |
73 |
77 |
87 |
В исследование включали больных, постоянно принимающих НПВП (в основном с РА и ОА), эффект лечения оценивался через 8 недель.
Результаты исследований показали, что Омез в дозе 20 и 40 мг достаточно более эффективен, чем мизопростол для рубцевания язвы в желудке и, особенно в рубцевании дуоденальных язв (см. таблицу 1).
Интересно отметить, что заживление гастродуоденальных эрозий более активно происходит при применении мизопростола, % заживления равен 87, против 77-79 на фоне лечения Омезом.
В другом международном исследовании ASTRONAVT (по данным 73 научных центров из 14 стран) проводилось сравнение эффективности Омеза и ранитидина в лечении язв и эрозий, вызванных НПВП.
Таблица 2
Заживление (%) эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП, через 8 недель лечения.
| Препарат |
ЯБЖ |
ЯБДПК |
Эрозии |
| Омепразол 20 мг |
84 |
92 |
89 |
| Омепразол 40 мг |
87 |
88 |
86 |
| Ранитидин |
64 |
81 |
77 |
В данном исследовании Омез также оказался более эффективным в заживлении язв желудка и 12-перстной кишки, по сравнению с ранитидином (см. таблицу 2).
Необходимо также отметить, что при назначении блокаторов Н
2 -рецепторов гистамина III поколения кваматела (фамотидина) % заживления язв по сравнению с ранитидином (II поколение) значительно выше и составляет при ЯБЖ – 84, а при ЯБДПК – 86, что несколько ниже, чем при приеме Омеза.
Таким образом, результаты международных исследований по оценке эффективности лечения гастропатий, индуцированных НПВП, дают основания рекомендовать (при наличии язв желудка и 12-перстной кишки) ИПП: Омез по 20 мг 2 р. или ланзап 30 мг 2 р/день, а в терапии эрозий, наряду с Омезом и ланзапом, ранитидин по 150 мг 2 р. или квамател по 20 мг 2 р. или мизопростол по 200 мкг 4 р/день. Лечение должно проводиться в среднем 4 недели, далее целесообразно суточную дозу препарата уменьшить в 2 раза и продолжить его прием с профилактической целью в течении всего срока приема НПВП.
Побочные эффекты проводимой терапии наблюдаются значительно чаще у больных, принимавших мизопростол (боли в животе, метеоризм, диарея).
4. При обнаружении у больных с гастропатиями Helicobacter pylori в слизистой оболочке антрального отдела желудка целесообразно в соответствии с Маастрихским соглашением от 2000 г. провести эрадикационную терапию, добавив антибиотики.
Проведение данной терапии, считают большинство исследователей, является особенно целесообразным у тех больных, у которых в анамнезе имелись указания на наличие язвенной болезни, поскольку уничтожение Helicobacter pylori в таких случаях снижает риск её обострения на фоне приема НПВП.
С целью эрадикации Helicobacter pylori применяют одну из стандартных схем:
Первая схема (3 препарата).
1) ИПП: Омез 20 мг 2 р. или ланзап 30 мг 2 р./д.
2) Кларитромицин по 500 мг 2 р./д.
3) Амоксициллин по 1000 мг 2 р./д.
Курс лечения 7 дней, в случае неэффективности назначается
Вторая схема (4 препарата):
1) Омез20 мг 2 р. или ланзап 30 мг х 2 р./д.
2) Де-нол по 120 мг 4 р./д.
3) Метронидазол 500 мг 3 р./д.
4) Тетрациклин 500 мг 4 р./д.
Длительность терапии 7 дней.
В отдельных случаях, с учетом материальных возможностей стационара и пациента, с несколько меньшим успехом можно заменить в указанных схемах Омез ранитидином по 150 мг 2 р./д. или квамателом по 20 мг 2р/д.
В последние годы в схемах эрадикации Н. pylori рекомендовано применение ИПП нового поколения – рабепрозола (париета) по 20 мг х 2 р./д.

Париет в качестве базового компонента антихеликобактерных схем выгодно отличается от других ИПП способностью обеспечивать быстрое и мощное антисекреторное действие.
Париет конвертируется в свою активную форму быстрее, чем Омепразол и лансопразол (т.е. другие ИПП), что и объясняет более быстрое начало его ингибирующего действия на секрецию HCl (с 1-ого дня) по сравнению с омепразолом и лансопразолом.
Внутрижелудочный рН при лечении париетом достоверно выше, чем при лечении другими ИПП, что оказывается достаточным и оптимальным для развития синергизма ИПП и антибактериальных препаратов в эрадикации Н. pylori.
5. Итак, по современным представлениям алгоритм лечения НПВП – гастропатии включает следующие положения:
1) Решить вопрос о возможности отмены НПВП.
2) Если такая возможность имеется, то должны одновременно назначатся ИПП в стандартных дозах или блокаторы Н
2-рецепторов гистамина в стандартных или удвоенных дозах или мизопростол в дозе 800 мг/сутки.
3) Если отменить НПВП невозможно, назначают ИПП.
4) Лечение продолжается 4-8 недель и сочетается с проведением эрадикации Н.рilori. по показаниям.
6. Профилактика НПВП – гастропатий.
Профилактическое назначение противоязвенных лекарственных препаратов показано больным, у которых повышен риск развития эрозивно-язвенных поражений желудка и 12-перстной кишки.
 Выделяют 10 основных факторов риска.
Выделяют 10 основных факторов риска.
А. Возраст
Б. Предшествующие и сопутствующие заболевания
В. Вид и дозы препарата
Г. Продолжительность лечения НПВП
Д. Связь приема НПВП с приемом пищи
Е. Курение
Ж. Прием алкоголя
З. Одновременный прием других препаратов
И. Пол
К.
Наличие Нelicobacter pylori
Так как влияние их неоднозначно, необходимо остановиться на каждом факторе.
А. Возраст.
Частота развития НПВП – гастропатии у пожилых пациентов в 4 раза выше, чем у лиц молодого возраста, что может быть связано:
а) с большей выраженностью основного заболевания и
б) наличием сопутствующей патологии
Б. Предшествующие и сопутствующие заболевания
а) Наличие в анамнезе ЯБ (в сочетании с пожилым возрастом) повышает вероятность развития эрозивно-язвенных поражений желудка и 12-перстной кишки в 12-14 раз.
б) Риск развития НПВП – гастропатии возрастает и при наличии других заболеваний, таких, как: ПЭРБ, ССД, ЦП с портальной гипертензией, заболевания ССС.
В. Вид и доза препарата
а) Наиболее высок риск развития гастропатии при приеме пироксикама, индометацина, кетопрофена.
б) Увеличение дозы «стандартных» НПВП больше рекомендуемой приводит к нарастанию токсичности, но не эффективности. Так применение НПВП в дозах, превышающих стандарты в 1,5 раза. увеличивает риск развития НПВП – гастропатии в 2,8 раз.
в) Увеличение дозы НПВП, преимущественно ингибирующих ЦОГ – 2 (мовалис, найз) ведет к потере их селективности.
г) При одномоментном приеме нескольких НПВП риск развития гастропатии удваивается.
Г. Продолжительность лечения
а) Наибольшая вероятность возникновения эрозий и язв желудка и 12-перстной кишки отличается в первый месяц применения НП.
б) Отмечено развитие желудочных и дуоденальных кровотечений у 50% больных, применяющих НПВП не более 7 дней.
в) Риск развития поражения ЖКТ несколько снижается при длительном применении (после 4-го месяца) и остается стабильным на протяжении нескольких лет лечения, что связывает с процессом адаптации за счет увеличения скорости выработки слизи и появления молодых эпителиальных клеток.
Д. Связь применения НПВП с приемом пищи
Общеизвестно, что риск развития гастропатии возрастает в случае приема НПВП перед едой, что, естественно, служит основанием рекомендовать прием препаратов только после еды.
Е. Курение
Вероятность возникновения НПВП – гастропатии повышается у курящих лиц, риск поражения ЖКТ увеличивается если в анамнезе есть указания на перенесенные обострения ЯБ.
Ж. Прием алкоголя
Ульцерогенное действие НПВП на слизистую оболочку желудка и 12-перстной кишки потенциируется приемом алкоголя, отмечается большая частота перфорации язв при сочетании таких факторов, как прием НПВП, злоупотребление алкоголем, курение.
З. Одновременный прием других препаратов
а) При одновременном приеме НПВП и антикоагулянтов возрастает риск желудочно-кишечных кровотечений, особенно у пожилых лиц, при недостаточном питании, гипопротенемии.
б) При сочетанном приеме НПВП и ГКС риск развития эрозивно-язвенных поражений ЖКТ возрастаете 10 раз.
в) К другим средствам, повышающим риск развития НПВП – гастропатии относятся: хлорид калия, ингибиторы АПФ, диуретики.
И. Пол
Чаще эрозивно-язвенные гастродуоденальные поражения встречаются у женщин, особенно в пожилом возрасте, что объясняется повышенной чувствительностью женщин к действию НПВП и более частым, и не всегда оправданным приемам НПВП по поводу болевого синдрома различного генеза.
t
К. Helicobacter pylori
Роль Н. pylori в развитии НПВП – гастропатии неоднозначна. Одни исследователи отвечают утвердительно, другие отрицательно.
2) Итак: Алгоритм профилактики НПВП – гастропатии включает:
А. Своевременное выявление больных с высоким риском развития эрозивно-язвенных поражений ЖКТ.
Б. Назначение наименее ульцерогенных НПВП или селективных ингибиторов ЦОГ – 2 (мовалис, найз).
В. Профилактическое назначение противоязвенных препаратов. ИПП: Омез назначается в стандартных дозах – 20 мг/сут., ланзап – 30 мг/сут., париет – 10 мг/сут. или блокаторы Н
2– рецепторов гистамина в стандартных, а лучше в удвоенных дозах или аналоги простагландинов (мизпростол в дозе 400-800 мкг/сут.)
Г. Проведение эрадикационной терапии Helicobacter pylori. в течении 7 дней по показаниям (Омепразол 20 мг 2 р., Амоксициллин 1000 мг х 2 р. Кларитромицин 500 мг х 2 р./день).
3) Итак, как вы видели из схемы алгоритма, наиболее эффективными препаратами в профилактике НПВП – гастропатий являются (как и при лечении) ИПП Омез или л
анзап, что подтверждается международными исследованиями.
 Таблица 3
Таблица 3
Профилактика эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП через 6 мес. лечения.
| Препарат |
Удалось поддержать ремиссию на фоне приема НПВП (% больных) |
| Омепразол 20 мг |
61 |
| Мизопростол 400 мг |
48 |
| Плацебо |
27 |
Как видно из таблицы 3, по данным исследования OMNION удалось поддержать ремиссию на фоне приема НПВП в течении 6 мес. при назначении Омеза у 61% больных, а при назначении мизопростола у 48% больных.
Однако, как вы помните, если учитывать только возникновение эрозий, мизопростол был более эффективным по сравнению с Омезом и плацебо, но эффективнее, если принимать вместе.
Омез оказался более эффективным, чем ранитидин в предупреждении НПВП – гастропатий и по данным исследования ASTRONAVT.
Таблица 5
Профилактика эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП, через 6 мес. лечения.
| Препарат |
Удалось поддержать ремиссию на фоне приема НПВП (% больных) |
| Омепразол 20 мг |
72 |
| Ранитидин 300 мг |
59 |
Ремиссия отмечалась у 72% больных на фоне приема Омеза и у 59% на фоне приема ранитидина, и, если вы помните, у 69% на фоне приема кваматела.
4) Следует подчеркнуть, что монотерапия невсасывающимися антацидами (маалокс, фосфолюгель)
и сукральфатгель, хотя и может быть использована для временного уменьшения симптомов диспепсии, неэффективна как в отношении лечения, так и профилактики НПВП-гастропатий.
Таким образом, адекватная оценка факторов риска, грамотное назначение НПВП, а также использование средств профилактики (мовалис) и лечения поражений ЖКТ, особенно ИПП (Омез и ланзап), позволяет существенно повысить безопасность лечения больных с ревматологическими заболеваниями и более успешно решать проблему НПВП – гастропатий.
 1) ИПП угнетая активность (именно) фермента Н+К+ АТФ-азу (водородно-калиевую АТФ-азу), блокируют тем самым заключительную стадию синтеза соляной кислоты.
В результате происходит значительное снижение уровня базальной и стимулированной секреции, независимо от стимулирующего фактора.
Это выгодно отличает ИПП от других антисекреторных препаратов, в том числе блокаторов Н2 – рецепторов, которые блокируют лишь один из множества механизмов секреции HCl (соляной кислоты).
Высокая эффективность ИПП превосходящая эффективность блокаторов Н2 – рецепторов гистамина и мизопростола подтверждена многочисленными исследованиями, отвечающими требованиям доказательной медицины.
2) В последние 5 лет проведен целый ряд широкомасштабных клинических исследований по изучению сравнительной эффективности основных групп препаратов, используемых в лечении НПВП – гастропатий.
Особый интерес представляют международные исследования OMNION и ASTRONAVT.
В исследовании OMNION проводилось (таблица 1) сравнение эффективности Омеза и мизопростола в лечении язв и эрозий, вызванных НПВП по данным 93-х центров Европейских стран, а также США, Канады, Австралии и Новой Зеландии.
Таблица 1.
Заживление (в %) эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП, через 8 недель лечения.
1) ИПП угнетая активность (именно) фермента Н+К+ АТФ-азу (водородно-калиевую АТФ-азу), блокируют тем самым заключительную стадию синтеза соляной кислоты.
В результате происходит значительное снижение уровня базальной и стимулированной секреции, независимо от стимулирующего фактора.
Это выгодно отличает ИПП от других антисекреторных препаратов, в том числе блокаторов Н2 – рецепторов, которые блокируют лишь один из множества механизмов секреции HCl (соляной кислоты).
Высокая эффективность ИПП превосходящая эффективность блокаторов Н2 – рецепторов гистамина и мизопростола подтверждена многочисленными исследованиями, отвечающими требованиям доказательной медицины.
2) В последние 5 лет проведен целый ряд широкомасштабных клинических исследований по изучению сравнительной эффективности основных групп препаратов, используемых в лечении НПВП – гастропатий.
Особый интерес представляют международные исследования OMNION и ASTRONAVT.
В исследовании OMNION проводилось (таблица 1) сравнение эффективности Омеза и мизопростола в лечении язв и эрозий, вызванных НПВП по данным 93-х центров Европейских стран, а также США, Канады, Австралии и Новой Зеландии.
Таблица 1.
Заживление (в %) эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП, через 8 недель лечения.
 Париет в качестве базового компонента антихеликобактерных схем выгодно отличается от других ИПП способностью обеспечивать быстрое и мощное антисекреторное действие.
Париет конвертируется в свою активную форму быстрее, чем Омепразол и лансопразол (т.е. другие ИПП), что и объясняет более быстрое начало его ингибирующего действия на секрецию HCl (с 1-ого дня) по сравнению с омепразолом и лансопразолом.
Внутрижелудочный рН при лечении париетом достоверно выше, чем при лечении другими ИПП, что оказывается достаточным и оптимальным для развития синергизма ИПП и антибактериальных препаратов в эрадикации Н. pylori.
5. Итак, по современным представлениям алгоритм лечения НПВП – гастропатии включает следующие положения:
1) Решить вопрос о возможности отмены НПВП.
2) Если такая возможность имеется, то должны одновременно назначатся ИПП в стандартных дозах или блокаторы Н2-рецепторов гистамина в стандартных или удвоенных дозах или мизопростол в дозе 800 мг/сутки.
3) Если отменить НПВП невозможно, назначают ИПП.
4) Лечение продолжается 4-8 недель и сочетается с проведением эрадикации Н.рilori. по показаниям.
6. Профилактика НПВП – гастропатий.
Профилактическое назначение противоязвенных лекарственных препаратов показано больным, у которых повышен риск развития эрозивно-язвенных поражений желудка и 12-перстной кишки.
Париет в качестве базового компонента антихеликобактерных схем выгодно отличается от других ИПП способностью обеспечивать быстрое и мощное антисекреторное действие.
Париет конвертируется в свою активную форму быстрее, чем Омепразол и лансопразол (т.е. другие ИПП), что и объясняет более быстрое начало его ингибирующего действия на секрецию HCl (с 1-ого дня) по сравнению с омепразолом и лансопразолом.
Внутрижелудочный рН при лечении париетом достоверно выше, чем при лечении другими ИПП, что оказывается достаточным и оптимальным для развития синергизма ИПП и антибактериальных препаратов в эрадикации Н. pylori.
5. Итак, по современным представлениям алгоритм лечения НПВП – гастропатии включает следующие положения:
1) Решить вопрос о возможности отмены НПВП.
2) Если такая возможность имеется, то должны одновременно назначатся ИПП в стандартных дозах или блокаторы Н2-рецепторов гистамина в стандартных или удвоенных дозах или мизопростол в дозе 800 мг/сутки.
3) Если отменить НПВП невозможно, назначают ИПП.
4) Лечение продолжается 4-8 недель и сочетается с проведением эрадикации Н.рilori. по показаниям.
6. Профилактика НПВП – гастропатий.
Профилактическое назначение противоязвенных лекарственных препаратов показано больным, у которых повышен риск развития эрозивно-язвенных поражений желудка и 12-перстной кишки.
 Выделяют 10 основных факторов риска.
А. Возраст
Б. Предшествующие и сопутствующие заболевания
В. Вид и дозы препарата
Г. Продолжительность лечения НПВП
Д. Связь приема НПВП с приемом пищи
Е. Курение
Ж. Прием алкоголя
З. Одновременный прием других препаратов
И. Пол
К. Наличие Нelicobacter pylori
Так как влияние их неоднозначно, необходимо остановиться на каждом факторе.
А. Возраст.
Частота развития НПВП – гастропатии у пожилых пациентов в 4 раза выше, чем у лиц молодого возраста, что может быть связано:
а) с большей выраженностью основного заболевания и
б) наличием сопутствующей патологии
Б. Предшествующие и сопутствующие заболевания
а) Наличие в анамнезе ЯБ (в сочетании с пожилым возрастом) повышает вероятность развития эрозивно-язвенных поражений желудка и 12-перстной кишки в 12-14 раз.
б) Риск развития НПВП – гастропатии возрастает и при наличии других заболеваний, таких, как: ПЭРБ, ССД, ЦП с портальной гипертензией, заболевания ССС.
В. Вид и доза препарата
а) Наиболее высок риск развития гастропатии при приеме пироксикама, индометацина, кетопрофена.
б) Увеличение дозы «стандартных» НПВП больше рекомендуемой приводит к нарастанию токсичности, но не эффективности. Так применение НПВП в дозах, превышающих стандарты в 1,5 раза. увеличивает риск развития НПВП – гастропатии в 2,8 раз.
в) Увеличение дозы НПВП, преимущественно ингибирующих ЦОГ – 2 (мовалис, найз) ведет к потере их селективности.
г) При одномоментном приеме нескольких НПВП риск развития гастропатии удваивается.
Г. Продолжительность лечения
а) Наибольшая вероятность возникновения эрозий и язв желудка и 12-перстной кишки отличается в первый месяц применения НП.
б) Отмечено развитие желудочных и дуоденальных кровотечений у 50% больных, применяющих НПВП не более 7 дней.
в) Риск развития поражения ЖКТ несколько снижается при длительном применении (после 4-го месяца) и остается стабильным на протяжении нескольких лет лечения, что связывает с процессом адаптации за счет увеличения скорости выработки слизи и появления молодых эпителиальных клеток.
Д. Связь применения НПВП с приемом пищи
Общеизвестно, что риск развития гастропатии возрастает в случае приема НПВП перед едой, что, естественно, служит основанием рекомендовать прием препаратов только после еды.
Е. Курение
Вероятность возникновения НПВП – гастропатии повышается у курящих лиц, риск поражения ЖКТ увеличивается если в анамнезе есть указания на перенесенные обострения ЯБ.
Ж. Прием алкоголя
Ульцерогенное действие НПВП на слизистую оболочку желудка и 12-перстной кишки потенциируется приемом алкоголя, отмечается большая частота перфорации язв при сочетании таких факторов, как прием НПВП, злоупотребление алкоголем, курение.
З. Одновременный прием других препаратов
а) При одновременном приеме НПВП и антикоагулянтов возрастает риск желудочно-кишечных кровотечений, особенно у пожилых лиц, при недостаточном питании, гипопротенемии.
б) При сочетанном приеме НПВП и ГКС риск развития эрозивно-язвенных поражений ЖКТ возрастаете 10 раз.
в) К другим средствам, повышающим риск развития НПВП – гастропатии относятся: хлорид калия, ингибиторы АПФ, диуретики.
И. Пол
Чаще эрозивно-язвенные гастродуоденальные поражения встречаются у женщин, особенно в пожилом возрасте, что объясняется повышенной чувствительностью женщин к действию НПВП и более частым, и не всегда оправданным приемам НПВП по поводу болевого синдрома различного генеза. t
К. Helicobacter pylori
Роль Н. pylori в развитии НПВП – гастропатии неоднозначна. Одни исследователи отвечают утвердительно, другие отрицательно.
2) Итак: Алгоритм профилактики НПВП – гастропатии включает:
А. Своевременное выявление больных с высоким риском развития эрозивно-язвенных поражений ЖКТ.
Б. Назначение наименее ульцерогенных НПВП или селективных ингибиторов ЦОГ – 2 (мовалис, найз).
В. Профилактическое назначение противоязвенных препаратов. ИПП: Омез назначается в стандартных дозах – 20 мг/сут., ланзап – 30 мг/сут., париет – 10 мг/сут. или блокаторы Н2– рецепторов гистамина в стандартных, а лучше в удвоенных дозах или аналоги простагландинов (мизпростол в дозе 400-800 мкг/сут.)
Г. Проведение эрадикационной терапии Helicobacter pylori. в течении 7 дней по показаниям (Омепразол 20 мг 2 р., Амоксициллин 1000 мг х 2 р. Кларитромицин 500 мг х 2 р./день).
3) Итак, как вы видели из схемы алгоритма, наиболее эффективными препаратами в профилактике НПВП – гастропатий являются (как и при лечении) ИПП Омез или ланзап, что подтверждается международными исследованиями.
Выделяют 10 основных факторов риска.
А. Возраст
Б. Предшествующие и сопутствующие заболевания
В. Вид и дозы препарата
Г. Продолжительность лечения НПВП
Д. Связь приема НПВП с приемом пищи
Е. Курение
Ж. Прием алкоголя
З. Одновременный прием других препаратов
И. Пол
К. Наличие Нelicobacter pylori
Так как влияние их неоднозначно, необходимо остановиться на каждом факторе.
А. Возраст.
Частота развития НПВП – гастропатии у пожилых пациентов в 4 раза выше, чем у лиц молодого возраста, что может быть связано:
а) с большей выраженностью основного заболевания и
б) наличием сопутствующей патологии
Б. Предшествующие и сопутствующие заболевания
а) Наличие в анамнезе ЯБ (в сочетании с пожилым возрастом) повышает вероятность развития эрозивно-язвенных поражений желудка и 12-перстной кишки в 12-14 раз.
б) Риск развития НПВП – гастропатии возрастает и при наличии других заболеваний, таких, как: ПЭРБ, ССД, ЦП с портальной гипертензией, заболевания ССС.
В. Вид и доза препарата
а) Наиболее высок риск развития гастропатии при приеме пироксикама, индометацина, кетопрофена.
б) Увеличение дозы «стандартных» НПВП больше рекомендуемой приводит к нарастанию токсичности, но не эффективности. Так применение НПВП в дозах, превышающих стандарты в 1,5 раза. увеличивает риск развития НПВП – гастропатии в 2,8 раз.
в) Увеличение дозы НПВП, преимущественно ингибирующих ЦОГ – 2 (мовалис, найз) ведет к потере их селективности.
г) При одномоментном приеме нескольких НПВП риск развития гастропатии удваивается.
Г. Продолжительность лечения
а) Наибольшая вероятность возникновения эрозий и язв желудка и 12-перстной кишки отличается в первый месяц применения НП.
б) Отмечено развитие желудочных и дуоденальных кровотечений у 50% больных, применяющих НПВП не более 7 дней.
в) Риск развития поражения ЖКТ несколько снижается при длительном применении (после 4-го месяца) и остается стабильным на протяжении нескольких лет лечения, что связывает с процессом адаптации за счет увеличения скорости выработки слизи и появления молодых эпителиальных клеток.
Д. Связь применения НПВП с приемом пищи
Общеизвестно, что риск развития гастропатии возрастает в случае приема НПВП перед едой, что, естественно, служит основанием рекомендовать прием препаратов только после еды.
Е. Курение
Вероятность возникновения НПВП – гастропатии повышается у курящих лиц, риск поражения ЖКТ увеличивается если в анамнезе есть указания на перенесенные обострения ЯБ.
Ж. Прием алкоголя
Ульцерогенное действие НПВП на слизистую оболочку желудка и 12-перстной кишки потенциируется приемом алкоголя, отмечается большая частота перфорации язв при сочетании таких факторов, как прием НПВП, злоупотребление алкоголем, курение.
З. Одновременный прием других препаратов
а) При одновременном приеме НПВП и антикоагулянтов возрастает риск желудочно-кишечных кровотечений, особенно у пожилых лиц, при недостаточном питании, гипопротенемии.
б) При сочетанном приеме НПВП и ГКС риск развития эрозивно-язвенных поражений ЖКТ возрастаете 10 раз.
в) К другим средствам, повышающим риск развития НПВП – гастропатии относятся: хлорид калия, ингибиторы АПФ, диуретики.
И. Пол
Чаще эрозивно-язвенные гастродуоденальные поражения встречаются у женщин, особенно в пожилом возрасте, что объясняется повышенной чувствительностью женщин к действию НПВП и более частым, и не всегда оправданным приемам НПВП по поводу болевого синдрома различного генеза. t
К. Helicobacter pylori
Роль Н. pylori в развитии НПВП – гастропатии неоднозначна. Одни исследователи отвечают утвердительно, другие отрицательно.
2) Итак: Алгоритм профилактики НПВП – гастропатии включает:
А. Своевременное выявление больных с высоким риском развития эрозивно-язвенных поражений ЖКТ.
Б. Назначение наименее ульцерогенных НПВП или селективных ингибиторов ЦОГ – 2 (мовалис, найз).
В. Профилактическое назначение противоязвенных препаратов. ИПП: Омез назначается в стандартных дозах – 20 мг/сут., ланзап – 30 мг/сут., париет – 10 мг/сут. или блокаторы Н2– рецепторов гистамина в стандартных, а лучше в удвоенных дозах или аналоги простагландинов (мизпростол в дозе 400-800 мкг/сут.)
Г. Проведение эрадикационной терапии Helicobacter pylori. в течении 7 дней по показаниям (Омепразол 20 мг 2 р., Амоксициллин 1000 мг х 2 р. Кларитромицин 500 мг х 2 р./день).
3) Итак, как вы видели из схемы алгоритма, наиболее эффективными препаратами в профилактике НПВП – гастропатий являются (как и при лечении) ИПП Омез или ланзап, что подтверждается международными исследованиями.
 Таблица 3
Профилактика эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП через 6 мес. лечения.
Таблица 3
Профилактика эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП через 6 мес. лечения.
 1) ИПП угнетая активность (именно) фермента Н+К+ АТФ-азу (водородно-калиевую АТФ-азу), блокируют тем самым заключительную стадию синтеза соляной кислоты.
В результате происходит значительное снижение уровня базальной и стимулированной секреции, независимо от стимулирующего фактора.
Это выгодно отличает ИПП от других антисекреторных препаратов, в том числе блокаторов Н2 – рецепторов, которые блокируют лишь один из множества механизмов секреции HCl (соляной кислоты).
Высокая эффективность ИПП превосходящая эффективность блокаторов Н2 – рецепторов гистамина и мизопростола подтверждена многочисленными исследованиями, отвечающими требованиям доказательной медицины.
2) В последние 5 лет проведен целый ряд широкомасштабных клинических исследований по изучению сравнительной эффективности основных групп препаратов, используемых в лечении НПВП – гастропатий.
Особый интерес представляют международные исследования OMNION и ASTRONAVT.
В исследовании OMNION проводилось (таблица 1) сравнение эффективности Омеза и мизопростола в лечении язв и эрозий, вызванных НПВП по данным 93-х центров Европейских стран, а также США, Канады, Австралии и Новой Зеландии.
Таблица 1.
Заживление (в %) эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП, через 8 недель лечения.
1) ИПП угнетая активность (именно) фермента Н+К+ АТФ-азу (водородно-калиевую АТФ-азу), блокируют тем самым заключительную стадию синтеза соляной кислоты.
В результате происходит значительное снижение уровня базальной и стимулированной секреции, независимо от стимулирующего фактора.
Это выгодно отличает ИПП от других антисекреторных препаратов, в том числе блокаторов Н2 – рецепторов, которые блокируют лишь один из множества механизмов секреции HCl (соляной кислоты).
Высокая эффективность ИПП превосходящая эффективность блокаторов Н2 – рецепторов гистамина и мизопростола подтверждена многочисленными исследованиями, отвечающими требованиям доказательной медицины.
2) В последние 5 лет проведен целый ряд широкомасштабных клинических исследований по изучению сравнительной эффективности основных групп препаратов, используемых в лечении НПВП – гастропатий.
Особый интерес представляют международные исследования OMNION и ASTRONAVT.
В исследовании OMNION проводилось (таблица 1) сравнение эффективности Омеза и мизопростола в лечении язв и эрозий, вызванных НПВП по данным 93-х центров Европейских стран, а также США, Канады, Австралии и Новой Зеландии.
Таблица 1.
Заживление (в %) эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП, через 8 недель лечения.
 Париет в качестве базового компонента антихеликобактерных схем выгодно отличается от других ИПП способностью обеспечивать быстрое и мощное антисекреторное действие.
Париет конвертируется в свою активную форму быстрее, чем Омепразол и лансопразол (т.е. другие ИПП), что и объясняет более быстрое начало его ингибирующего действия на секрецию HCl (с 1-ого дня) по сравнению с омепразолом и лансопразолом.
Внутрижелудочный рН при лечении париетом достоверно выше, чем при лечении другими ИПП, что оказывается достаточным и оптимальным для развития синергизма ИПП и антибактериальных препаратов в эрадикации Н. pylori.
5. Итак, по современным представлениям алгоритм лечения НПВП – гастропатии включает следующие положения:
1) Решить вопрос о возможности отмены НПВП.
2) Если такая возможность имеется, то должны одновременно назначатся ИПП в стандартных дозах или блокаторы Н2-рецепторов гистамина в стандартных или удвоенных дозах или мизопростол в дозе 800 мг/сутки.
3) Если отменить НПВП невозможно, назначают ИПП.
4) Лечение продолжается 4-8 недель и сочетается с проведением эрадикации Н.рilori. по показаниям.
6. Профилактика НПВП – гастропатий.
Профилактическое назначение противоязвенных лекарственных препаратов показано больным, у которых повышен риск развития эрозивно-язвенных поражений желудка и 12-перстной кишки.
Париет в качестве базового компонента антихеликобактерных схем выгодно отличается от других ИПП способностью обеспечивать быстрое и мощное антисекреторное действие.
Париет конвертируется в свою активную форму быстрее, чем Омепразол и лансопразол (т.е. другие ИПП), что и объясняет более быстрое начало его ингибирующего действия на секрецию HCl (с 1-ого дня) по сравнению с омепразолом и лансопразолом.
Внутрижелудочный рН при лечении париетом достоверно выше, чем при лечении другими ИПП, что оказывается достаточным и оптимальным для развития синергизма ИПП и антибактериальных препаратов в эрадикации Н. pylori.
5. Итак, по современным представлениям алгоритм лечения НПВП – гастропатии включает следующие положения:
1) Решить вопрос о возможности отмены НПВП.
2) Если такая возможность имеется, то должны одновременно назначатся ИПП в стандартных дозах или блокаторы Н2-рецепторов гистамина в стандартных или удвоенных дозах или мизопростол в дозе 800 мг/сутки.
3) Если отменить НПВП невозможно, назначают ИПП.
4) Лечение продолжается 4-8 недель и сочетается с проведением эрадикации Н.рilori. по показаниям.
6. Профилактика НПВП – гастропатий.
Профилактическое назначение противоязвенных лекарственных препаратов показано больным, у которых повышен риск развития эрозивно-язвенных поражений желудка и 12-перстной кишки.
 Выделяют 10 основных факторов риска.
А. Возраст
Б. Предшествующие и сопутствующие заболевания
В. Вид и дозы препарата
Г. Продолжительность лечения НПВП
Д. Связь приема НПВП с приемом пищи
Е. Курение
Ж. Прием алкоголя
З. Одновременный прием других препаратов
И. Пол
К. Наличие Нelicobacter pylori
Так как влияние их неоднозначно, необходимо остановиться на каждом факторе.
А. Возраст.
Частота развития НПВП – гастропатии у пожилых пациентов в 4 раза выше, чем у лиц молодого возраста, что может быть связано:
а) с большей выраженностью основного заболевания и
б) наличием сопутствующей патологии
Б. Предшествующие и сопутствующие заболевания
а) Наличие в анамнезе ЯБ (в сочетании с пожилым возрастом) повышает вероятность развития эрозивно-язвенных поражений желудка и 12-перстной кишки в 12-14 раз.
б) Риск развития НПВП – гастропатии возрастает и при наличии других заболеваний, таких, как: ПЭРБ, ССД, ЦП с портальной гипертензией, заболевания ССС.
В. Вид и доза препарата
а) Наиболее высок риск развития гастропатии при приеме пироксикама, индометацина, кетопрофена.
б) Увеличение дозы «стандартных» НПВП больше рекомендуемой приводит к нарастанию токсичности, но не эффективности. Так применение НПВП в дозах, превышающих стандарты в 1,5 раза. увеличивает риск развития НПВП – гастропатии в 2,8 раз.
в) Увеличение дозы НПВП, преимущественно ингибирующих ЦОГ – 2 (мовалис, найз) ведет к потере их селективности.
г) При одномоментном приеме нескольких НПВП риск развития гастропатии удваивается.
Г. Продолжительность лечения
а) Наибольшая вероятность возникновения эрозий и язв желудка и 12-перстной кишки отличается в первый месяц применения НП.
б) Отмечено развитие желудочных и дуоденальных кровотечений у 50% больных, применяющих НПВП не более 7 дней.
в) Риск развития поражения ЖКТ несколько снижается при длительном применении (после 4-го месяца) и остается стабильным на протяжении нескольких лет лечения, что связывает с процессом адаптации за счет увеличения скорости выработки слизи и появления молодых эпителиальных клеток.
Д. Связь применения НПВП с приемом пищи
Общеизвестно, что риск развития гастропатии возрастает в случае приема НПВП перед едой, что, естественно, служит основанием рекомендовать прием препаратов только после еды.
Е. Курение
Вероятность возникновения НПВП – гастропатии повышается у курящих лиц, риск поражения ЖКТ увеличивается если в анамнезе есть указания на перенесенные обострения ЯБ.
Ж. Прием алкоголя
Ульцерогенное действие НПВП на слизистую оболочку желудка и 12-перстной кишки потенциируется приемом алкоголя, отмечается большая частота перфорации язв при сочетании таких факторов, как прием НПВП, злоупотребление алкоголем, курение.
З. Одновременный прием других препаратов
а) При одновременном приеме НПВП и антикоагулянтов возрастает риск желудочно-кишечных кровотечений, особенно у пожилых лиц, при недостаточном питании, гипопротенемии.
б) При сочетанном приеме НПВП и ГКС риск развития эрозивно-язвенных поражений ЖКТ возрастаете 10 раз.
в) К другим средствам, повышающим риск развития НПВП – гастропатии относятся: хлорид калия, ингибиторы АПФ, диуретики.
И. Пол
Чаще эрозивно-язвенные гастродуоденальные поражения встречаются у женщин, особенно в пожилом возрасте, что объясняется повышенной чувствительностью женщин к действию НПВП и более частым, и не всегда оправданным приемам НПВП по поводу болевого синдрома различного генеза. t
К. Helicobacter pylori
Роль Н. pylori в развитии НПВП – гастропатии неоднозначна. Одни исследователи отвечают утвердительно, другие отрицательно.
2) Итак: Алгоритм профилактики НПВП – гастропатии включает:
А. Своевременное выявление больных с высоким риском развития эрозивно-язвенных поражений ЖКТ.
Б. Назначение наименее ульцерогенных НПВП или селективных ингибиторов ЦОГ – 2 (мовалис, найз).
В. Профилактическое назначение противоязвенных препаратов. ИПП: Омез назначается в стандартных дозах – 20 мг/сут., ланзап – 30 мг/сут., париет – 10 мг/сут. или блокаторы Н2– рецепторов гистамина в стандартных, а лучше в удвоенных дозах или аналоги простагландинов (мизпростол в дозе 400-800 мкг/сут.)
Г. Проведение эрадикационной терапии Helicobacter pylori. в течении 7 дней по показаниям (Омепразол 20 мг 2 р., Амоксициллин 1000 мг х 2 р. Кларитромицин 500 мг х 2 р./день).
3) Итак, как вы видели из схемы алгоритма, наиболее эффективными препаратами в профилактике НПВП – гастропатий являются (как и при лечении) ИПП Омез или ланзап, что подтверждается международными исследованиями.
Выделяют 10 основных факторов риска.
А. Возраст
Б. Предшествующие и сопутствующие заболевания
В. Вид и дозы препарата
Г. Продолжительность лечения НПВП
Д. Связь приема НПВП с приемом пищи
Е. Курение
Ж. Прием алкоголя
З. Одновременный прием других препаратов
И. Пол
К. Наличие Нelicobacter pylori
Так как влияние их неоднозначно, необходимо остановиться на каждом факторе.
А. Возраст.
Частота развития НПВП – гастропатии у пожилых пациентов в 4 раза выше, чем у лиц молодого возраста, что может быть связано:
а) с большей выраженностью основного заболевания и
б) наличием сопутствующей патологии
Б. Предшествующие и сопутствующие заболевания
а) Наличие в анамнезе ЯБ (в сочетании с пожилым возрастом) повышает вероятность развития эрозивно-язвенных поражений желудка и 12-перстной кишки в 12-14 раз.
б) Риск развития НПВП – гастропатии возрастает и при наличии других заболеваний, таких, как: ПЭРБ, ССД, ЦП с портальной гипертензией, заболевания ССС.
В. Вид и доза препарата
а) Наиболее высок риск развития гастропатии при приеме пироксикама, индометацина, кетопрофена.
б) Увеличение дозы «стандартных» НПВП больше рекомендуемой приводит к нарастанию токсичности, но не эффективности. Так применение НПВП в дозах, превышающих стандарты в 1,5 раза. увеличивает риск развития НПВП – гастропатии в 2,8 раз.
в) Увеличение дозы НПВП, преимущественно ингибирующих ЦОГ – 2 (мовалис, найз) ведет к потере их селективности.
г) При одномоментном приеме нескольких НПВП риск развития гастропатии удваивается.
Г. Продолжительность лечения
а) Наибольшая вероятность возникновения эрозий и язв желудка и 12-перстной кишки отличается в первый месяц применения НП.
б) Отмечено развитие желудочных и дуоденальных кровотечений у 50% больных, применяющих НПВП не более 7 дней.
в) Риск развития поражения ЖКТ несколько снижается при длительном применении (после 4-го месяца) и остается стабильным на протяжении нескольких лет лечения, что связывает с процессом адаптации за счет увеличения скорости выработки слизи и появления молодых эпителиальных клеток.
Д. Связь применения НПВП с приемом пищи
Общеизвестно, что риск развития гастропатии возрастает в случае приема НПВП перед едой, что, естественно, служит основанием рекомендовать прием препаратов только после еды.
Е. Курение
Вероятность возникновения НПВП – гастропатии повышается у курящих лиц, риск поражения ЖКТ увеличивается если в анамнезе есть указания на перенесенные обострения ЯБ.
Ж. Прием алкоголя
Ульцерогенное действие НПВП на слизистую оболочку желудка и 12-перстной кишки потенциируется приемом алкоголя, отмечается большая частота перфорации язв при сочетании таких факторов, как прием НПВП, злоупотребление алкоголем, курение.
З. Одновременный прием других препаратов
а) При одновременном приеме НПВП и антикоагулянтов возрастает риск желудочно-кишечных кровотечений, особенно у пожилых лиц, при недостаточном питании, гипопротенемии.
б) При сочетанном приеме НПВП и ГКС риск развития эрозивно-язвенных поражений ЖКТ возрастаете 10 раз.
в) К другим средствам, повышающим риск развития НПВП – гастропатии относятся: хлорид калия, ингибиторы АПФ, диуретики.
И. Пол
Чаще эрозивно-язвенные гастродуоденальные поражения встречаются у женщин, особенно в пожилом возрасте, что объясняется повышенной чувствительностью женщин к действию НПВП и более частым, и не всегда оправданным приемам НПВП по поводу болевого синдрома различного генеза. t
К. Helicobacter pylori
Роль Н. pylori в развитии НПВП – гастропатии неоднозначна. Одни исследователи отвечают утвердительно, другие отрицательно.
2) Итак: Алгоритм профилактики НПВП – гастропатии включает:
А. Своевременное выявление больных с высоким риском развития эрозивно-язвенных поражений ЖКТ.
Б. Назначение наименее ульцерогенных НПВП или селективных ингибиторов ЦОГ – 2 (мовалис, найз).
В. Профилактическое назначение противоязвенных препаратов. ИПП: Омез назначается в стандартных дозах – 20 мг/сут., ланзап – 30 мг/сут., париет – 10 мг/сут. или блокаторы Н2– рецепторов гистамина в стандартных, а лучше в удвоенных дозах или аналоги простагландинов (мизпростол в дозе 400-800 мкг/сут.)
Г. Проведение эрадикационной терапии Helicobacter pylori. в течении 7 дней по показаниям (Омепразол 20 мг 2 р., Амоксициллин 1000 мг х 2 р. Кларитромицин 500 мг х 2 р./день).
3) Итак, как вы видели из схемы алгоритма, наиболее эффективными препаратами в профилактике НПВП – гастропатий являются (как и при лечении) ИПП Омез или ланзап, что подтверждается международными исследованиями.
 Таблица 3
Профилактика эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП через 6 мес. лечения.
Таблица 3
Профилактика эрозивно-язвенных поражений желудка и 12-перстной кишки, вызванных НПВП через 6 мес. лечения.


