Просмотров: 2 427
Дополнительные материалы исследования CRIB по отсутствию плацентарной передачи цертолизумаб пегола во время беременности: результаты проспективного, пострегистрационного, фармакокинетического исследования
CRIB Appendix
Lack of placental transfer of certolizumab pegol during pregnancy: results from CRIB, a prospective, postmarketing, pharmacokinetic study
Xavier Mariette, Frauke Förger, Bincy Abraham, Ann D Flynn, Anna Moltó, René-Marc Flipo, Astrid van Tubergen, Laura Shaughnessy, Jeff Simpson, Marie Teil, Eric Helmer, Maggie Wang, Eliza F Chakravarty
Supplementary Appendix
Обоснование исключения одного младенца из набора анализа протокола
У одного младенца при рождении наблюдалась неожиданно высокая концентрация CZP плазмы (0,485 мкг/мл) по сравнению с результатами проб, собранных у других 14 младенцев. Напротив, в 4 и 8 недели образец результатов в этой детской были ниже пробирной LLOQ (<0.032 мкг/мл). Зная, что период полувыведения иммуноглобулина IgG у детей больше чем у взрослых, и в свете доказательств того, что CZP могут выводиться в более медленном темпе в младенцев1, чем у взрослых пациентов2, этот результат требовало дальнейшего расследования.
По данным клинических повествования, мать ребенка пережила очень тяжелые роды, и младенец родоразрешался по экстренным кесаревым сечением. Записки медсестры указывают на то, что образец крови ребенка были ненормального цвета и получен с трудом. Кроме того, не удалось собрать образец пуповинной крови из-за спадания пуповины.
С помощью модели детского населения PK для прогнозирования CZP плазменной концентрации на 4 недели от рождения (неопубликованные данные из CZP исследования у пациентов с ювенильным идиопатическим артритом [NCT01550003]), а CZP концентрации при рождении 0.485 мг/мл приведет, в среднем, 4 неделя CZP концентрации 0.182 мкг/мл (0.1st–99.9th процентили: 0.059–0.351 мкг/мл; Supplementary Figure S1A). Другой, более консервативный подход был применен, в котором объем крови младенца был рассчитан с использованием их известной массы тела (0,109 х вес тела). Этот расчетный объем крови был установлен как объем распределения (V/F), который представляет наименьший возможный V/F и более короткий период полураспада элиминации (T1/2) для CZP. При таком подходе концентрация CZP при рождении 0.485 мг/мл приведет, в среднем, 4 неделя концентрация CZP к 0.186 мг/мл (0.1st–99.9th процентили: 0.062–0.354 мг/мл; Supplementary Figure S1B). В соответствии с этими двумя подходами, существует очень низкая вероятность (<0.1%) младенца с концентрацией CZP из 0.485 мкг/мл при рождении для отображения уровней ниже LLOQ (<0.032 мкг/мл) на 4 неделе (т. е. недопустимо увеличенный разброс CZP [СL/F] в новорожденного).
Основываясь на вышеизложенных доказательствах, мы полагали, что неожиданно высокий уровень плазмы CZP при рождении может быть вызван ошибкой отбора проб крови. Таким образом, этот образец считался отклонением протокола, и младенец был исключен из итогового набора анализа протокола.
Обоснование неитерпритируемых PEG концентрации в плазме крови младенцев
Общая концентрация PEG в образцах материнской и пуповинной крови в целом в соответствии с соответствующих измерений CZP. Напротив, концентрации PEG в детской образцы не соответствуют уровню CZP: 13/14, пока детей не имели количественных CZP плазменные уровни при рождении, и не имели количественной оценке CZP на неделях 4 и 8, большинство образцов младенцев в этих трех временных точках имели количественных PEG уровнями без устойчивой связи по датам. Это привело нас к исследованию того, была ли процедура сбора крови загрязнена образцами экзогенной PEG.
Becton Dickinson трубки были использованы для сбора крови от матерей и пуповины. Sarstedt monovette шприцы использовались для сбора крови из младенцев во всех временных точках. Для оценки риска загрязнения образцов экзогенной PEG в ходе процедуры сбора было собрано 10 образцов крови человека, не подвергшихся воздействию CZP, с использованием обоих типов труб. Затем уровни PEG измерялись тем же методом, что и в исследовании CRIB (ядерная магнитно-резонансная спектроскопия; LLOQ: 2,5 мкг/мл). Результаты исследования показали, что образцы, собранные с помощью трубок Becton Dickinson, находились ниже уровня LLOQ, в то время как 7/10 образцов, собранных с помощью шприцев Sarstedt, имели поддающиеся количественной оценке уровни PEG.
Таким образом, мы пришли к выводу, что существует значительный риск загрязнения в результате процедуры, используемые для сбора образцов крови с Sarstedt monovette, шприцы. Следовательно, результаты ПЭГ младенца не могут быть интерпретированы. Эти данные не влияют на достоверность данных детского CZP
Дополнительный рисунок S1. Предсказанные профили плазмы CZP концентрации с течением времени для младенца с CZP уровне при рождении 0.485 мг/мл
А) подход к моделированию на основе детского населения PK моделиа
 B) Моделирование подхода на основе модели PK педиатрической популяции, в которой объем крови младенца был рассчитан с использованием их известной массы телаb
B) Моделирование подхода на основе модели PK педиатрической популяции, в которой объем крови младенца был рассчитан с использованием их известной массы телаb
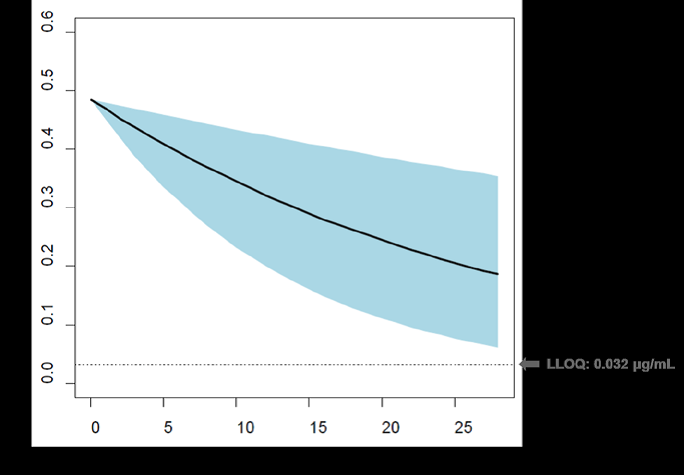 Затененная область на каждом графике представляет собой 0.1st–99.9th процентиль. модель в педиатрии PK базируется на опубликованных данных, исследование CZP у пациентов с ювенильным идиопатическим артритом (NCT01550003); bмладенцев объем кровь была рассчитана, используя их известные массы тела (0.109 x вес тела). Этот расчетный объем крови был установлен как объем распределения (V/F), который представляет наименьший возможный V/F и более короткий период полураспада элиминации (T1/2) для CZP. CZP certolizumab pegol;: цертолизумаб pegol; PK: pharmacokinetic фармакокинетический ; LLOQ: lower limit of quantification нижний предел определения
Дополнительная таблица S1. Индивидуальных концентраций в плазме CZP у матерей, пуповинах, и у младенцев при рождении, на 4 недели , и 8 недел
Затененная область на каждом графике представляет собой 0.1st–99.9th процентиль. модель в педиатрии PK базируется на опубликованных данных, исследование CZP у пациентов с ювенильным идиопатическим артритом (NCT01550003); bмладенцев объем кровь была рассчитана, используя их известные массы тела (0.109 x вес тела). Этот расчетный объем крови был установлен как объем распределения (V/F), который представляет наименьший возможный V/F и более короткий период полураспада элиминации (T1/2) для CZP. CZP certolizumab pegol;: цертолизумаб pegol; PK: pharmacokinetic фармакокинетический ; LLOQ: lower limit of quantification нижний предел определения
Дополнительная таблица S1. Индивидуальных концентраций в плазме CZP у матерей, пуповинах, и у младенцев при рождении, на 4 недели , и 8 недел
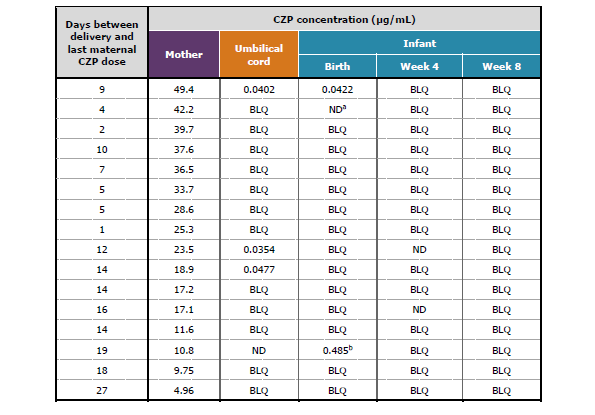
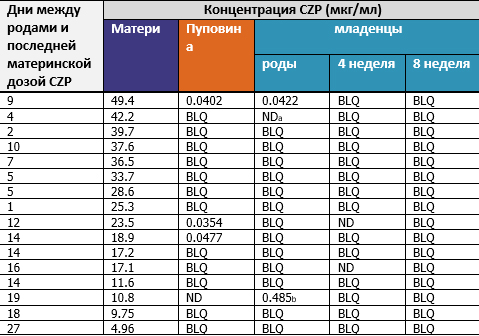 aмладенцы исключены из протокола анализа из-за отсутствия данных ND) при рождении; bмладенцы исключены из протокола анализа из-за недостоверного фармакокинетические (PK) данные при рождении (т. е. данные не согласуются с детской CZP PK модель, на основе ожидаемого диапазона клиренс, объем распределения и последующей ликвидации период полураспада; в разделе “обоснование исключения одного младенца из-за протокола анализа”). CZP PK: цертолизумаб pegol; BLQ: below the LLOQ ниже LLOQ (<0.032 мг/мл); LLOQ: lower limit of quantification; нижний предел количественного определения; ND: not done: не выполнено.
CRIB Appendix
References
aмладенцы исключены из протокола анализа из-за отсутствия данных ND) при рождении; bмладенцы исключены из протокола анализа из-за недостоверного фармакокинетические (PK) данные при рождении (т. е. данные не согласуются с детской CZP PK модель, на основе ожидаемого диапазона клиренс, объем распределения и последующей ликвидации период полураспада; в разделе “обоснование исключения одного младенца из-за протокола анализа”). CZP PK: цертолизумаб pegol; BLQ: below the LLOQ ниже LLOQ (<0.032 мг/мл); LLOQ: lower limit of quantification; нижний предел количественного определения; ND: not done: не выполнено.
CRIB Appendix
References

 B) Моделирование подхода на основе модели PK педиатрической популяции, в которой объем крови младенца был рассчитан с использованием их известной массы телаb
B) Моделирование подхода на основе модели PK педиатрической популяции, в которой объем крови младенца был рассчитан с использованием их известной массы телаb
 Затененная область на каждом графике представляет собой 0.1st–99.9th процентиль. модель в педиатрии PK базируется на опубликованных данных, исследование CZP у пациентов с ювенильным идиопатическим артритом (NCT01550003); bмладенцев объем кровь была рассчитана, используя их известные массы тела (0.109 x вес тела). Этот расчетный объем крови был установлен как объем распределения (V/F), который представляет наименьший возможный V/F и более короткий период полураспада элиминации (T1/2) для CZP. CZP certolizumab pegol;: цертолизумаб pegol; PK: pharmacokinetic фармакокинетический ; LLOQ: lower limit of quantification нижний предел определения
Дополнительная таблица S1. Индивидуальных концентраций в плазме CZP у матерей, пуповинах, и у младенцев при рождении, на 4 недели , и 8 недел
Затененная область на каждом графике представляет собой 0.1st–99.9th процентиль. модель в педиатрии PK базируется на опубликованных данных, исследование CZP у пациентов с ювенильным идиопатическим артритом (NCT01550003); bмладенцев объем кровь была рассчитана, используя их известные массы тела (0.109 x вес тела). Этот расчетный объем крови был установлен как объем распределения (V/F), который представляет наименьший возможный V/F и более короткий период полураспада элиминации (T1/2) для CZP. CZP certolizumab pegol;: цертолизумаб pegol; PK: pharmacokinetic фармакокинетический ; LLOQ: lower limit of quantification нижний предел определения
Дополнительная таблица S1. Индивидуальных концентраций в плазме CZP у матерей, пуповинах, и у младенцев при рождении, на 4 недели , и 8 недел

 aмладенцы исключены из протокола анализа из-за отсутствия данных ND) при рождении; bмладенцы исключены из протокола анализа из-за недостоверного фармакокинетические (PK) данные при рождении (т. е. данные не согласуются с детской CZP PK модель, на основе ожидаемого диапазона клиренс, объем распределения и последующей ликвидации период полураспада; в разделе “обоснование исключения одного младенца из-за протокола анализа”). CZP PK: цертолизумаб pegol; BLQ: below the LLOQ ниже LLOQ (<0.032 мг/мл); LLOQ: lower limit of quantification; нижний предел количественного определения; ND: not done: не выполнено.
CRIB Appendix
References
aмладенцы исключены из протокола анализа из-за отсутствия данных ND) при рождении; bмладенцы исключены из протокола анализа из-за недостоверного фармакокинетические (PK) данные при рождении (т. е. данные не согласуются с детской CZP PK модель, на основе ожидаемого диапазона клиренс, объем распределения и последующей ликвидации период полураспада; в разделе “обоснование исключения одного младенца из-за протокола анализа”). CZP PK: цертолизумаб pegol; BLQ: below the LLOQ ниже LLOQ (<0.032 мг/мл); LLOQ: lower limit of quantification; нижний предел количественного определения; ND: not done: не выполнено.
CRIB Appendix
References
- Sarvas H, Seppälä I, Kurikka S, Siegberg R, Mäkelä O. Half-life of the maternal IgG1 allotype in infants. J Clin Immunol 1993;13(2):145-51.
- FDA. Cimzia® (certolizumab pegol) Prescribing Information, 2016 (Accessed April 15, 2017, at http://www.accessdata.fda.gov/drugsatfda_docs/label/2016/125160s241lbl.pdf).



