Просмотров: 10 006
АКТУАЛЬНЫЕ ПРОБЛЕМЫ СОВРЕМЕННОЙ РЕВМАТОЛОГИИ. Сборник научных трудов. Выпуск 30-й

 Алехина И.Ю., Александров А.В., Курбанова Р.Д., Бенедицкая Е.В., Александрова Н.В., Фофанова Н.А.
Алехина И.Ю., Александров А.В., Курбанова Р.Д., Бенедицкая Е.В., Александрова Н.В., Фофанова Н.А.
ЛАБОРАТОРНАЯ ДИАГНОСТИКА СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКИ: ПЕРСПЕКТИВЫ ИСПОЛЬЗОВАНИЯ ИММУНОЛОГИЧЕСКИХ МЕТОДОВ ДЛЯ ОПРЕДЕЛЕНИЯ АУТОАНТИТЕЛ К ФЕРМЕНТАМ
ФГБУ «Научно-исследовательский институт клинической и экспериментальной ревматологии» РАМН, Волгоград Прогрессирующее поражение органов и систем у больных системной красной волчанкой (СКВ) в значительной степени определяет жизненный и социальный прогноз, параметрами оценки которого являются уровень выживаемости, степень повреждения органов, длительное сохранение высокой активности заболевания, возможность развития ремиссии, а также показатели качества жизни. На этом фоне не теряет свою актуальность проблема своевременной диагностики начальных проявлений активации и прогрессирования патологического процесса у больных СКВ. Целью работы явилась разработка дополнительных критериев лабораторной диагностики СКВ с использованием иммобилизированных антигенных наносистем (АНС) на основе ферментов антиоксидантной системы (АОС) и пуринового метаболизма (ПМ) – церулоплазмина (ЦП), ксантиноксидазы (КО), пуриннуклеозидфосфорилазы (ПНФ) и гуаниндезаминазы (ГДА). Методы исследования. Исследовалась сыворотка крови 30 практически здоровых лиц – доноров станции переливания крови (контрольная группа), а также 46 больных СКВ (основная группа) с различной активностью патологического процесса (минимальная – 16 человек, умеренная – 27 человек, высокая – 3 человека). Показатели активности SLEDAI (8,9±5,7 баллов) и ECLAM (5,3±2,7 баллов) демонстрировали небольшое число больных СКВ, имеющих неактивную фазу заболевания. Объектом исследований служила сыворотка крови. Антитела к ЦП (анти-ЦП), КО (анти-КО), ПНФ (антиПНФ) и ГДА (анти-ГДА) выявляли твердофазным иммуноферментным анализом с использованием АНС, для получения которых применяли метод эмульсионной полимеризации в потоке газообразного азота с включением магнитного материала и соответствующей антигенной матрицы. Результаты. При исследовании сыворотки крови здоровых лиц на со-держание антител к ферментам АОС и ПМ с помощью иммуноферментного метода на основе АНС были получены следующие результаты: уровень анти-ЦП (M±m) составил 0,022±0,014 Ед, анти-КО – 0,032±0,013 Ед, анти-ПНФ – 0,067±0,019 Ед и анти-ГДА – 0,06±0,022 Ед. Динамика показателей ферментативной активности и уровней антител к изучаемым энзимам у больных СКВ в зависимости от активности патологиче-ского процесса характеризовалась снижением активности ЦП (p=0,024), ГДА (p=0,033) и сопровождалась ростом уровня антител к данным ферментам 4 (p<0,002). Следует отметить, что в группе больных СКВ с наличием антител к ЦП активность ЦП была существенно ниже, чем у больных без данных ан-тител (p<0,001). В группе больных СКВ с наличием антител к КО отмечено увеличение активности фермента в сыворотке крови (p=0,041). Была отме-чена положительная корреляция уровня анти-ГДА со значениями индекса SLEDAI (r=0,36) и отрицательная корреляция с биохимической активностью ГДА в сыворотке крови (r= -0,34). Наиболее высокие уровни анти-ГДА отме-чались у больных СКВ с поражением печени (р=0,024) и у больных с выра-женным цитопеническим синдромом (р=0,039). Уровень анти-ПНФ коррели-ровал с увеличением индекса SLEDAI (p=0,012), а также со снижением фер-ментативной активности сывороточной ПНФ (p=0,007). Интересные результаты были получены в ходе динамического наблюде-ния за больными. При выписке из стационара отмечалось некоторое сниже-ние активности ЦП в группе больных без антител к ЦП. Однако в группе больных с наличием антител к ферменту активность ЦП не только не снижа-лась, а повышалась (p=0,037). Уровень антител к ЦП на фоне лечения имел тенденцию к снижению (р>0,05). Стандартная терапия оказывала слабое воздействие на нормализацию иммунобиохимических сдвигов в группе больных с высоким уровнем анти-КО, а также в группе больных с высоким уровнем анти-ПНФ. Иммунные механизмы оказывают существенное влияние на выраженность реакций свободнорадикального окисления при СКВ, причем активные формы кислорода могут оказывать патогенное воздействие на биомолекулы и структуры клетки непосредственно, либо инициируя процессы перекисного окисления липидов, приводя к повреждению белков, липидов, нуклеиновых кис-лот и придавая им свойства аутоантигенов. Образование аутоантител к таким структурам является ключевым звеном патогенеза системных ревматических заболеваний и происходит задолго до развития выраженных клинических проявлений. Выводы. Показатели содержания антител к ферментам антиоксидантной защиты организма и пуринового метаболизма могут использоваться в диа-гностике клинических проявлений СКВ, а также в качестве дополнительного критерия оценки эффективности проводимой терапии. Ахунова Г.Р., Ахунова Р.Р.СОСТОЯНИЕ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У БОЛЬНЫХ С БОЛЕЗНЬЮ БЕХТЕРЕВА ГБОУ ВПО
«Казанский ГМУ» Минздравсоцразвития России Цель. Оценить структурно-функциональное состояние щитовидной железы (ЩЖ) у больных с болезнью Бехтерева (ББ). Материалы и методы. В исследование были включены 26 пациентов с достоверным диагнозом ББ, из них 21 (80,8%) мужчина и 5 (19,2%) женщин 5 (возраст – 36,1 [32,0; 41,0] лет, длительность ББ – 1 [0,3;3,5] год). Клиническое обследование пациентов проводилось с использованием рекомендованного ASAS набора клинических тестов. Исследовали уровни острофазовых показателей (скорость оседания эритроцитов (СОЭ) по Вестергрену и С-реактивный белок (СРБ)). Всем пациентам было выполнено ультразвуковое исследование ЩЖ, определение уровня тиреотропного гормона (ТТГ), свободных фракций тироксина (св.Т4) и трийодтиронина (св.Т3), антител к тиреопероксидазе (АТ к ТПО) и тиреоглобулину (АТ к ТГ). Контрольную группу составили 15 здоровых лиц, сопоставимых по полу и возрасту с обследуемыми больными АС. Исходно высокая клиническая активность АС (BASDAI≥4) отмечена у 25 (96,2%), умеренная активность – у 1 (3,8%) пациента. У 23 (88,5%) пациентов присутствовали признаки активного спондилита (ночная боль в позвоночнике≥4). Превалировала периферическая форма АС – 16 (61,5%) пациентов. У 21 (80,8%) пациента отмечались значительные функциональные нарушения (BASFI≥4). II рентгенологическая стадия сакроилеита наблюдалась у 8 (30,8%), III стадия – у 11 (42,3%), IV стадия – у 7 (26,9%) больных. Статистическая обработка полученных результатов осуществлялась с использованием пакета статистических программ Statistica 6,0. Результаты и обсуждение. При оценке структурно-функционального состояния ЩЖ у 15,2% (4) пациентов с ББ была выявлена патология ЩЖ. Среди вариантов тиреоидной патологии у 3,8% (1) пациентов диагностирован аутоиммунный тиреоидит (АИТ), у 3,8% (1) – субклинический гипотиреоз, у 3,8% (1) – узловой зоб, у 3,8% (1) пациентов – кистозный зоб. У 23,1% (6) пациентов с ББ был выявлен высокий уровень АТ к ЩЖ. С функциональной точки зрения у больных ББ с тиреоидной патологией сниженная функция ЩЖ отмечалась в 50%, которая была представлена субклиническим гипотиреозом. Все пациенты, имевшие различные формы зоба, были эутиреоидны. В таблице 1 представлены уровни гормонов ЩЖ и АТ к ЩЖ у больных ББ (n=26). Уровень св.Т4 и АТ к ТПО были достоверно выше у пациентов с ББ по сравнению с контролем (р<0,05). Значения св.Т3, ТТГ и АТ к ТГ были сопоставимы с контролем, но несколько выше последнего (табл. 1). Таблица 1. Уровень гормонов ЩЖ и АТ к ЩЖ у больных ББ (n=26). Несмотря на то, что средние значения гормонов (ТТГ, св.Т3) и АТ к ТГ до-стоверно не отличались от средних значений контрольной группы, при инди-видуальном рассмотрении этих показателей у пациентов с ББ наблюдались индивидуальные максимальные колебания содержания ТТГ до 5,4 мМЕ/мл, св.Т3 до 6,4 пг/мл, АТ к ТГ до 728,7 мМЕд/л. Максимальное значение св.Т4 было 24,9 пмоль/л, АТ к ТПО – 94,2 Ед/мл. Был проведен анализ вышеука-занных лабораторных показателей состояния ЩЖ у больных ББ в зависимо-сти от наличия тиреоидной патологии. Как видно из таблицы 2, у пациентов с ББ, имеющих патологию ЩЖ, уровень св.Т4 был выше по сравнению с кон-трольной группой. Ожидаемо содержание св.Т3, ТТГ и АТ к ТПО и АТ к ТГ были выше у пациентов с тиреоидным поражением, хотя и недостоверно.
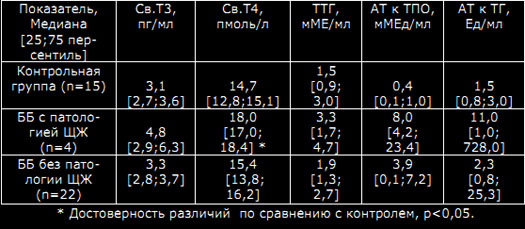
Таблица 2. Уровень гормонов ЩЖ и АТ к ЩЖ у больных ББ с патологией ЩЖ и без нее (n=26)
Несмотря на то, что средние значения гормонов (ТТГ, св.Т3) и АТ к ТГ до-стоверно не отличались от средних значений контрольной группы, при инди-видуальном рассмотрении этих показателей у пациентов с ББ наблюдались индивидуальные максимальные колебания содержания ТТГ до 5,4 мМЕ/мл, св.Т3 до 6,4 пг/мл, АТ к ТГ до 728,7 мМЕд/л. Максимальное значение св.Т4 было 24,9 пмоль/л, АТ к ТПО – 94,2 Ед/мл. Был проведен анализ вышеука-занных лабораторных показателей состояния ЩЖ у больных ББ в зависимо-сти от наличия тиреоидной патологии. Как видно из таблицы 2, у пациентов с ББ, имеющих патологию ЩЖ, уровень св.Т4 был выше по сравнению с кон-трольной группой. Ожидаемо содержание св.Т3, ТТГ и АТ к ТПО и АТ к ТГ были выше у пациентов с тиреоидным поражением, хотя и недостоверно.
Таблица 2. Уровень гормонов ЩЖ и АТ к ЩЖ у больных ББ с патологией ЩЖ и без нее (n=26)
 Для выявления возможной взаимосвязи характера течения основного заболевания с патологией ЩЖ были проанализированы основные характеристики ББ в группах больных ББ с поражением ЩЖ (n=4) и без него (n=22). Больные ББ с поражением ЩЖ имели достоверно более высокую клиническую активность заболевания по индексу BASDAI (7,8 [5,9; 9,8] и 5,3 [4,7; 6,0] соответственно, р < 0,05), большие функциональные нарушения по индексу BASFI (7,6 [6,5; 8,4] и 5,5 [4,3; 6,6] соответственно, р < 0,05), меньшую подвижность позвоночника (индекс BASMI) (6,1 [5,9; 6,3] и 3,2 [2,6; 4,1] соответственно, р < 0,05), чем больные без поражения ЩЖ (р<0,05). Таким образом, суставной синдром был значимо хуже по множеству пара-метров у пациентов ББ с тиреоидной патологией, что не исключает возможность наличия общих механизмов суставного и тиреоидного поражения при ББ. Ультразвуковые размеры ЩЖ, структура ЩЖ у пациентов с ББ статисти-чески не отличались от размеров ЩЖ контрольной группы. Следует отметить, что при проведении этого исследования были обнаружены в части случаев качественные изменения паренхимы железы с изменением эхогенности и наличием очаговости. Раздельный анализ ультразвуковых размеров ЩЖ у больных ББ с поражением ЩЖ и без поражения были сопоставимы друг с другом и контрольной группой, хотя имелась некоторая тенденция к увеличению некоторых линейных и объемных показателей. Закономерное увеличение размеров ЩЖ отмечалось у больных с тиреоидной патологией. Качественные изменения паренхимы органа отмечались и у пациентов АС, не имевших каких-либо клинико-лабораторных признаков поражения ЩЖ. Так, у этих пациентов имелись неоднородность структуры (n=1) и повышение эхогенности (n=6), хотя кровоток в железе был обычным. Был проведен корреляционный анализ для выявления связей клинических параметров течения ББ с показателями состояния ЩЖ. Имелась достоверная взаимосвязь уровня св.Т3 и длительности утренней скованности (r=0,40, p<0,05); уровня СРБ (r=0,44, p<0,05), индекса ASDAS (по СРБ) (r=0,40, p<0,05). Достоверные корреляционные связи имелись между уров-нем ТТГ и активностью заболевания по индексу BASDAI (r=0,61, p<0,01), индексом функционального состояния больных BASFI (r=0,51, p<0,01); об-щей оценкой самочувствия пациента, оцененной пациентом (r=0,74, p<0,01), общей оценкой самочувствия пациента, оцененной врачом (r=0,71, p<0,01); интенсивностью боли в спине в течение дня (r=0,50, p<0,05), интенсивностью ночной боли в позвоночнике (r=0,50, p<0,05), интенсивностью боли в суставах (r=0,40, p<0,05); уровнем СОЭ (по методу Вестергрена) (r=0,43, p<0,05); индексом ASDAS (по СРБ) (r=0,58, p<0,01), индексом ASDAS (по СОЭ) (r=0,51, p<0,01). Была выявлена достоверная взаимосвязь уровня АТ к ТПО и активности заболевания по индексу BASDAI (r=0,51, p<0,05), интенсивности боли в суставах (r=0,53, p<0,05), интенсивности боли в энтезисах (r=0,50, p<0,05); интенсивности испытываемой боли в левом тазобедренном суставе (r=0,45, p<0,05), количества болезненных суставов (r=0,48, p<0,05), количества припухших суставов (r=0,43, p<0,05), количества воспаленных энтезисов (r=0,47, p<0,05); уровня СОЭ (по методу Вестергрена) (r=0,68, p<0,01), уровня СРБ (r=0,50, p<0,05); индекса ASDAS (по СРБ) (r=0,57, p<0,01), ин-декса ASDAS (по СОЭ) (r=0,65, p<0,01). Достоверные корреляционные связи были обнаружены между уровнем АТ к ТГ и активностью заболевания по индексу BASDAI (r=0,65, p<0,01), общей оценкой самочувствия пациента, оцененной пациентом (r=0,47, p<0,05), общей оценкой самочувствия пациента, оцененной врачом (r=0,56, p<0,01); интенсивностью боли в спине в течение дня (r=0,44, p<0,05), интенсивностью боли в суставах (r=0,51, p<0,01), интенсивностью боли в энтезисах (r=0,41, p<0,05); количеством воспаленных энтезисов (r=0,42, p<0,05), индексом ASDAS (по СРБ) (r=0,54, p<0,01), индексом ASDAS (по СОЭ) (r=0,47, p<0,05).
Выводы. Поражение ЩЖ отмечалось у 15,2% больных ББ в виде АИТ (3,8%), узлового и кистозного зоба (7,6%), субклинического гипотиреоза (3,8%) без структурных изменений органа. У половины больных с тиреоидной патологией отмечался субклинический гипотиреоз (50%). В 23,1% слу-чаев имелся повышенный уровень антител к ЩЖ. Больные ББ с поражением ЩЖ имели достоверно более высокую клиническую активность заболевания по индексу BASDAI, большие функциональные нарушения по индексу BASFI, меньшую подвижность позвоночника по ряду показателей, чем больные без поражения ЩЖ. Таким образом, у больных ББ необходимо динамическое наблюдение за структурно-функциональным состоянием ЩЖ для раннего выявления аутоиммунного поражения органа.
Ахунова Р.Р., Ахунова Г.Р.
Для выявления возможной взаимосвязи характера течения основного заболевания с патологией ЩЖ были проанализированы основные характеристики ББ в группах больных ББ с поражением ЩЖ (n=4) и без него (n=22). Больные ББ с поражением ЩЖ имели достоверно более высокую клиническую активность заболевания по индексу BASDAI (7,8 [5,9; 9,8] и 5,3 [4,7; 6,0] соответственно, р < 0,05), большие функциональные нарушения по индексу BASFI (7,6 [6,5; 8,4] и 5,5 [4,3; 6,6] соответственно, р < 0,05), меньшую подвижность позвоночника (индекс BASMI) (6,1 [5,9; 6,3] и 3,2 [2,6; 4,1] соответственно, р < 0,05), чем больные без поражения ЩЖ (р<0,05). Таким образом, суставной синдром был значимо хуже по множеству пара-метров у пациентов ББ с тиреоидной патологией, что не исключает возможность наличия общих механизмов суставного и тиреоидного поражения при ББ. Ультразвуковые размеры ЩЖ, структура ЩЖ у пациентов с ББ статисти-чески не отличались от размеров ЩЖ контрольной группы. Следует отметить, что при проведении этого исследования были обнаружены в части случаев качественные изменения паренхимы железы с изменением эхогенности и наличием очаговости. Раздельный анализ ультразвуковых размеров ЩЖ у больных ББ с поражением ЩЖ и без поражения были сопоставимы друг с другом и контрольной группой, хотя имелась некоторая тенденция к увеличению некоторых линейных и объемных показателей. Закономерное увеличение размеров ЩЖ отмечалось у больных с тиреоидной патологией. Качественные изменения паренхимы органа отмечались и у пациентов АС, не имевших каких-либо клинико-лабораторных признаков поражения ЩЖ. Так, у этих пациентов имелись неоднородность структуры (n=1) и повышение эхогенности (n=6), хотя кровоток в железе был обычным. Был проведен корреляционный анализ для выявления связей клинических параметров течения ББ с показателями состояния ЩЖ. Имелась достоверная взаимосвязь уровня св.Т3 и длительности утренней скованности (r=0,40, p<0,05); уровня СРБ (r=0,44, p<0,05), индекса ASDAS (по СРБ) (r=0,40, p<0,05). Достоверные корреляционные связи имелись между уров-нем ТТГ и активностью заболевания по индексу BASDAI (r=0,61, p<0,01), индексом функционального состояния больных BASFI (r=0,51, p<0,01); об-щей оценкой самочувствия пациента, оцененной пациентом (r=0,74, p<0,01), общей оценкой самочувствия пациента, оцененной врачом (r=0,71, p<0,01); интенсивностью боли в спине в течение дня (r=0,50, p<0,05), интенсивностью ночной боли в позвоночнике (r=0,50, p<0,05), интенсивностью боли в суставах (r=0,40, p<0,05); уровнем СОЭ (по методу Вестергрена) (r=0,43, p<0,05); индексом ASDAS (по СРБ) (r=0,58, p<0,01), индексом ASDAS (по СОЭ) (r=0,51, p<0,01). Была выявлена достоверная взаимосвязь уровня АТ к ТПО и активности заболевания по индексу BASDAI (r=0,51, p<0,05), интенсивности боли в суставах (r=0,53, p<0,05), интенсивности боли в энтезисах (r=0,50, p<0,05); интенсивности испытываемой боли в левом тазобедренном суставе (r=0,45, p<0,05), количества болезненных суставов (r=0,48, p<0,05), количества припухших суставов (r=0,43, p<0,05), количества воспаленных энтезисов (r=0,47, p<0,05); уровня СОЭ (по методу Вестергрена) (r=0,68, p<0,01), уровня СРБ (r=0,50, p<0,05); индекса ASDAS (по СРБ) (r=0,57, p<0,01), ин-декса ASDAS (по СОЭ) (r=0,65, p<0,01). Достоверные корреляционные связи были обнаружены между уровнем АТ к ТГ и активностью заболевания по индексу BASDAI (r=0,65, p<0,01), общей оценкой самочувствия пациента, оцененной пациентом (r=0,47, p<0,05), общей оценкой самочувствия пациента, оцененной врачом (r=0,56, p<0,01); интенсивностью боли в спине в течение дня (r=0,44, p<0,05), интенсивностью боли в суставах (r=0,51, p<0,01), интенсивностью боли в энтезисах (r=0,41, p<0,05); количеством воспаленных энтезисов (r=0,42, p<0,05), индексом ASDAS (по СРБ) (r=0,54, p<0,01), индексом ASDAS (по СОЭ) (r=0,47, p<0,05).
Выводы. Поражение ЩЖ отмечалось у 15,2% больных ББ в виде АИТ (3,8%), узлового и кистозного зоба (7,6%), субклинического гипотиреоза (3,8%) без структурных изменений органа. У половины больных с тиреоидной патологией отмечался субклинический гипотиреоз (50%). В 23,1% слу-чаев имелся повышенный уровень антител к ЩЖ. Больные ББ с поражением ЩЖ имели достоверно более высокую клиническую активность заболевания по индексу BASDAI, большие функциональные нарушения по индексу BASFI, меньшую подвижность позвоночника по ряду показателей, чем больные без поражения ЩЖ. Таким образом, у больных ББ необходимо динамическое наблюдение за структурно-функциональным состоянием ЩЖ для раннего выявления аутоиммунного поражения органа.
Ахунова Р.Р., Ахунова Г.Р.
СТРУКТУРА ПСИХИЧЕСКИХ РАССТРОЙСТВ НЕПСИХОТИЧЕСКОГО УРОВНЯ У ПАЦИЕНТОВ С РЕВМАТОИДНЫМ АРТРИТОМ ГБОУ ВПО
«Казанский ГМУ» Минздравсоцразвития России, г. Казань, Россия Цель. Изучить структуру психических расстройств непсихотического уровня у пациентов с ревматоидным артритом (РА) во взаимосвязи с разными клиническими характеристиками заболевания. Материалы и методы. 192 пациентам с РА (167(87,0%) женщинам и 25(13,0%) мужчинам в возрасте 51[44;59] лет) проведены клиническое, ла-бораторное и рентгенологическое обследования. Пациентами заполнены клинический опросник для оценки и выявления невротических состояний (Яхин К.К., Менделевич Д.М., 1978), опросник Health Assessment Questionnaire (HAQ). Статистическая обработка полученных результатов осуществлялась с использованием пакета программ Exel, Statististica 6,0, SPSS. Результаты и обсуждение. У 123 (64,1%) пациентов с РА были диагностированы психические расстройства непсихотического уровня. Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов с длительностью РА до 2 лет позволил выявить 4 фактора. 1 фактор – фактор гипостении (снижение работоспособности, медлительность, повышенная утомляемость, поверхностный, неспокойный сон). 2 фактор – фактор тревожной гиперестезии (неприятные ощущения (покалывание, онемение), сильная утомляемость после нагрузок, защитные действия, рассеянность, головокружения, чувство пульсации крови в сосудах, плохая переносимость ожидания, легкая потливость при волнениях). 3 фактор – фактор эмоциональной лабильности (усталость, разбитость после сна, головные боли, обидчивость, раздражительность и вспыльчивость, навязчивые сомнения в правильности поступков и решений, эмоциональное недержание). 4 фактор – фактор тревоги (тревога и беспокойство, нарушение за-сыпания, усталость и разбитость после сна, поверхностный и неспокойный сон, головокружения, раздражительность, вспыльчивость). Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов с длительностью РА 2 и более лет позволил также вы-явить 4 фактора: фактор астенической депрессии (медлительность, вялость, повышенная утомляемость, снижение работоспособности, усталость и разбитость после сна, поверхностный и неспокойный сон, подавленное и угнетенное настроение), фактор тревоги (тревога и беспокойство, защитные действия, рассеянность и невнимательность, обидчивость, затруднения перед принятием решений, поверхностный и неспокойный сон, эмоциональное не-держание, навязчивые сомнения в правильности поступков, решений), фак-тор вегетативных расстройств (метеотропность, тревога и беспокойство, не-приятные ощущения и боли в области сердца, головные боли, неприятные ощущения, головокружения, чувство пульсации крови в сосудах), фактор адинамической депрессии (повышенная утомляемость, стремление к одиночеству, подавленное и угнетенное настроение). Итак, если у больных с длительностью заболевания до 2 лет ведущим синдромом является астенический синдром, синдром тревожной гиперестезии, эмоциональной лабильности и тревожное расстройство, то у больных с длительностью заболевания более 2 лет ведущими становятся депрессивные расстройства в сочетании с тревогой и вегетативными нарушениями. Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов с серонегативным РА также позволил выявить 4 факто-ра: фактор астении с гиперестезией (медлительность, вялость, нарушение засыпания, снижение работоспособности, повышенную утомляемость, усталость после сна, покалывание в теле, неприятные ощущения, поверхностный и неспокойный сон, неприятные ощущения и боли в области сердца, рассеянность, невнимательность), фактор тревожной гиперестезии (метеотроп-ность, защитные действия, эмоциональное недержание, рассеянность, не-внимательность), фактор вегетативных расстройств в рамках маскированной депрессии (неприятные ощущения в теле, метеотропность, неприятные ощу-щения и боли в области сердца, стремление к одиночеству), фактор астени-ческой гиперестезии (сильную утомляемость после нагрузок, плохую пере-носимость ожидания, чувство пульсации крови в сосудах при волнениях, раздражительность, вспыльчивость). Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов с серопозитивным РА позволил также выявить 4 факто-ра: фактор тревожной депрессии (нарушение засыпания, поверхностный и неспокойный сон, чувство вины, долгие колебания перед принятием реше-ний, обидчивость, навязчивые сомнения в правильности поступков, решений и эмоциональное недержание), фактор астенической депрессии (медлительность, вялость, повышенную утомляемость, снижение работоспособности, метеотропность, сильная утомляемость после нагрузок, усталость и разбитость после сна, подавленное и угнетенное настроение), фактор тревожной гиперестезии (тревога и беспокойство головные боли, покалывание, онеме-ние в пальцах рук и ног или в теле, головокружения, чувство пульсации крови в сосудах), астеновегетативный фактор (утомляемость после нагрузок, рассеянность и невнимательность, защитные действия, головокружения, легкая потливость). Таким образом, при серонегативном варианте РА психические расстрой-ства ограничиваются астеническими и тревожными радикалами, при серопозитивным варианте РА ведущими являются расстройства депрессивного и тревожного спектров. Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов, испытывающих минимальную интенсивность боли поз-волил выявить 4 фактора: фактор астении с преобладанием гипостении (нарушение засыпания, медлительность, вялость, повышенная утомляемость, снижение работоспособности, приступы учащенного сердцебиения, сильная утомляемость после нагрузок), фактор тревожной гиперестезии (медлительность, вялость, чувство пульсации крови в сосудах, тревога и беспокойство, головные боли, метеотропность), фактор астенической гиперестезии (медли-тельность, вялость, усталость, разбитость после сна, тревога и беспокойство, поверхностный и неспокойный сон, неприятные ощущения и боли в области сердца, парестезии и сенестопатии или зябкость рук), фактор эмоциональной лабильности (нарушение засыпания, легкую потливость при волнениях, навязчивые сомнения, эмоциональное недержание). Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов, испытывающих умеренную и выраженную интенсивность боли позволил также выявить 4 фактора: фактор астенической (адинамической) депрессии (медлительность, вялость, повышенная утомляемость, снижение работоспособности, сильная утомляемость после нагрузок, усталость и разбитость после сна, поверхностный и неспокойный сон, подав-ленное и угнетенное настроение), фактор тревоги (защитные действия, рассеянность и невнимательность, обидчивость, поверхностный и неспокойный сон, затруднения в принятии решений, эмоциональное недержание, навязчивые сомнения в правильности поступков), фактор соматизации тревоги (метеотропность, тревога и беспокойство, покалывание, онемение в пальцах рук и ног или в теле, головные боли, неприятные ощущения и боли в области сердца, головокружения), тревожно – депрессивный фактор (тревога и беспокойство, поверхностный и неспокойный сон, стремление к одиночеству). Таким образом, у пациентов с отсутствием и минимальной интенсивностью боли психические расстройства ограничиваются астеническим радикалом, у пациентов с умеренной и выраженной болью ведущими являются расстройства депрессивного и тревожного спектров. Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов с отсутствием и минимальными нарушениями функционального статуса (по HAQ), позволил выявить 4 фактора: фактор депрессии (сниженный аппетит, подавленное и угнетенное настроение, навязчивые сомнения, неустойчивость настроения, чувство собственной вины, навязчивые воспоминания, заниженная самооценка), фактор гипостении (усталость и разбитость после сна, сниженный аппетит, снижение работоспособности, медлительность, вялость, рассеянность и невнимательность, неприятные ощущения и боли в области сердца), фактор конверсионных расстройств (комок в горле при волнении, боли или неприятные ощущения в области сердца при расстройствах, чувство пульсации крови в сосудах при волнениях, головокружение), фактор тревожно – депрессивных расстройств (подав-ленное и угнетенное настроение, плохая переносимость ожидания, комок в 11 горле при волнении, беспокойство и неусидчивость, навязчивые движения при волнениях, беспричинное беспокойство). Факторный анализ симптомов психических расстройств непсихотического уровня у пациентов с умеренными и сильными нарушениями функционального статуса (по HAQ), позволил выявить также 4 фактора: фактор тревож-ной депрессии (нарушение засыпания, тревога и беспокойство, поверхностный и неспокойный сон, рассеянность и невнимательность, защитные действия, подавленность и угнетенность, обидчивость, чувство вины, эмоциональное недержание), фактор астении (повышенная утомляемость, снижение работоспособности, медлительность, вялость, сильная утомляемость по-сле нагрузок, усталость и разбитость после сна, поверхностный и неспокойный сон), фактор вегетативных расстройств (метеотропность, парестезии и сенестопатии, боли или неприятные ощущения в области сердца, головные боли), фактор депрессивного мировоззрения (стремление к одиночеству и чувство собственной вины). Таким образом, при отсутствии и минимальных нарушениях функцио-нального статуса выявленные психические расстройства колеблются от ре-акции личности на болезнь (конверсионных расстройств) до субдепрессив-ных и тревожно – депрессивных расстройств. При ухудшении социального функционирования больных ведущими расстройствами становятся тревожно – депрессивные, астенические и вегетативные расстройства. Выводы. Результаты факторного анализа позволили выявить структуру ведущих психопатологических синдромов у пациентов с разными клиниче-скими характеристиками РА и показали усложнение и утяжеление структуры психических расстройств непсихотического уровня по мере увеличения дли-тельности РА, интенсивности боли, нарушения функционального статуса (по HAQ) и при серопозитивном варианте РА. Понимание взаимосвязи клинических характеристик РА и психических расстройств непсихотического уровня важно для адекватного построения лечебной и реабилитационной работы у пациентов с РА. Баранов Е.В., Маслакова Л.А., Гонтарь И.П., Трубенко Ю.А.ПАТОГЕНЕТИЧЕСКАЯ РОЛЬ ИММУННЫХ МЕХАНИЗМОВ ПОРАЖЕНИЯ ЦЕНТРАЛЬНОЙ И ПЕРИФЕРИЧЕСКОЙ НЕРВНОЙ СИСТЕМЫ ФГБУ
«НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ Как известно, все главные интегративные и адаптивные системы организма – нервная, эндокринная, иммунная – находятся в теснейшем функциональном и трофическом взаимодействии. Иммуноциты обладают рецептора-ми к различным нейромедиаторам, а иммунная система испытывает регулирующие нервные влияния. Наряду с этим, элементы иммунной системы продуцируют вещества, которые используются нервной системой как трофогены или источники трофогенов. Поэтому заболевания нервной системы нередко обусловлены иммунными расстройствами, которые в некоторых случаях могут быть первичными. Иммунная система — уникальная саморегулирующаяся организация, со-стоящая из различных популяций и субпопуляций лимфоидных клеток, постоянно взаимодействующих между собой. Однако их жизнедеятельность, активация, пролиферация и дифференцировка во многом зависят от других систем организма, в первую очередь, от нервной. Между иммунной и нерв-ной системами сложилось и постоянно осуществляется взаимодействие, с помощью которого они взаимно контролируют свои функции. Интеграция их со всеми другими функциями и обеспечивает существование организма как единого целого. Особое внимание исследователей привлекает участие медиаторов иммунитета в нейроиммунном взаимодействии. Считается, что помимо выполнения своих специфических функций внутри иммунной системы, медиаторы иммунитета могут осуществлять и межсистемные связи. Об этом говорит наличие рецепторов к иммуноцитокинам в нервной системе. Наибольшее количество исследований посвящено участию ИЛ-1, который не только является ключевым элементом иммунорегуляции на уровне иммунокомпетентных клеток, но и играет существенную роль в регуляции функции ЦНС. Цитокин ИЛ-2 также оказывает множество различных эффектов на иммунную и нервную систему, опосредуемых путем аффинного связывания с соответствую-щими рецепторами клеточной поверхности. Тропность множества клеток к ИЛ-2 обеспечивает ему центральное место в формировании как клеточного, так и гуморального иммунного ответа. Активирующее влияние ИЛ-2 на лим-фоциты и макрофаги проявляется в усилении антителозависимой цитоток-сичности этих клеток с параллельной стимуляцией секреции ФНО-альфа. ИЛ-2 индуцирует пролиферацию и дифференцировку олигодендроцитов, влияет на реактивность нейронов гипоталамуса, повышает уровень АКТГ и кортизола в крови. Клетками-мишенями для действия ИЛ-2 служат Т-лимфоциты, В-лимфоциты, NK-клетки и макрофаги. Помимо стимуляции пролиферации, ИЛ-2 вызывает функциональную активацию этих клеточных типов и секрецию ими других цитокинов. Изучение влияния ИЛ-2 на NK-клетки показало, что он способен стимулировать их пролиферацию с сохранением функциональной активности, увеличивать продукцию NK-клетками ИНФ- гамма и дозоза-висимо усиливать NK-опосредованный цитолизис. Существуют данные о продукции клетками центральной нервной системы (микроглией и астроцитами) таких цитокинов, как ИЛ-1, ИЛ-6 и ФНО-альфа. Продукция ФНО – альфа непосредственно в ткани мозга специфична для типичного нейроиммунологического заболевания – рассеянного склероза (PC). Повышение продукции ФНО-альфа в культуре изолированных ЛПС-стимулированных моноцитов/макрофагов наиболее отчетливо выявляется у больных с активным течением заболевания. Установлена возможность уча-стия в продукции интерферонов клеток мозга, в частности нейроглии или эпендимы, а также лимфоидных элементов сосудистых сплетений. В процессе формирования иммунного ответа включаются нервные окончания в соответствующих лимфоидных органах. Инициирующие сигналы мо-гут передаваться от иммунной системы в нервную гуморальным путем, в том числе, когда продуцируемые иммунокомпетентными клетками цитокины непосредственно проникают в нервную ткань и изменяют функциональное состояние определенных структур и описано проникновение через неповрежденный ГЭБ самих иммунокомпетентных клеток с последующей модуляцией функционального состояния нервных структур. Влияние иммунной и нервной систем друг на друга реализуется через рецепторные структуры клеток, взаимодействие которых создает связи «рецептор-рецептор» и таким образом организует молекулярный механизм сов-местной работы обеих систем. Функционирование клеток и сигнальная ин-формация обеспечиваются медиаторами и нейротрансмиттерами в обеих си-стемах, между нервной и иммунной системой происходит взаимообмен информацией с помощью цитокинов, стероидов и нейропептидов. Выводы: Таким образом, доказана общность и взаимосвязь нервной и иммунной систем, сходство между их структурами и функциями и развитие нового направления современной иммунологии – нейроиммунологии. Широкий диапазон неврологических симптомов при аутоиммунных системных заболеваниях позволяет рассматривать их как модельные системы для изучения патогенетической роли иммунных механизмов поражения центральной и периферической нервной системы. Бедина С.А., Евдокимова Е.В., Мякишев М.В., Левкина М.В., Некрасова С.П.АКТИВНОСТЬ ЭНЗИМОВ В СЫВОРОТКЕ КРОВИ БОЛЬНЫХ РЕАКТИВНЫМ АРТРИТОМ, ДИСКОИДНОЙ И СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКОЙ ФГБУ
«НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ Цель: выявить особенности активности гуаниндезаминазы (ГДА), гуано-зиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфос-форилазы (ГФ) в сыворотке крови больных реактивным артритом (РеА), дис-коидной красной волчанкой (ДКВ) и системной красной волчанкой (СКВ) для повышения качества дифференциации этих заболеваний. Материал и методы. Под наблюдением находились 54 больных РеА, 26 – СКВ и 24 больных ДКВ. Среди больных РеА 35 (66,7%) мужчин и 18 женщин. Средний возраст больных – 31,9±1.0 год. Больные СКВ были представ-лены 5 (19,2%) мужчинами и 21 женщиной. Средний возраст больных – 39,4±2,2 года. Определение активности ГДА, ГЗДА, ПНФ и ГФ проводилось по оригинальным методикам. Контрольную группу составили 30 практически здоровых людей. Результаты. По сравнению со здоровыми у больных РеА в сыворотке крови выше активность ГДА, ПНФ, ниже ГЗДА и ГФ (все р<0,001); у больных СКВ выше активность ГДА, ГЗДА, ПНФ и ниже ГФ (все р<0,001), у больных ДКВ выше активность ГДА, ПНФ и ниже ГФ (все р<0,05). Сравнительные ис-следования показали, что у больных РеА по сравнению с больными СКВ ни-же активность ГДА (р<0,001), ГЗДА (р<0,001), ПНФ (р<0,001) и выше ак-тивность ГФ (р<0,01); по сравнению с больными ДКВ выше активность ПНФ (р<0,01), ниже ГЗДА (р<0,001) и ГФ (р<0,001) и нет различий по активности ГДА (р>0,05). У больных СКВ по сравнению с больными ДКВ выше актив-ность ГДА, ГЗДА, ПНФ и ниже ГФ (все р<0,001). Заключение. Выявленные энзимные различия в комплексе с клиниче-скими данными могут способствовать дифференциации РеА, СКВ и ДКВ. Бычков И.Н., Савицкая Г.Н., Ханов А.Г.ВИТАМИНЫ И МИНЕРАЛЫ В ПИТАНИИ БОЛЬНЫХ ОСТЕОАРТРОЗОМ
ГБОУ ВПО РостГМУ Минздрава России, ГБУ РО «Госпиталь для ветеранов войн», ГБУ РО «Областная клиническая больница №2, Ростов-на-Дону, Россия В настоящее время рациональное питание является методом профилак-тики и одной из составляющих лечения больных ревматологического профи-ля. Несбалансированное питание с избыточным количеством калорий спо-собствует ожирению, на фоне которого проявляются проблемы связанные с поражением тазобедренных и коленных суставов. Также недостаточное по-требление некоторых нутриентов, таких как магний, витамин Д, аскорбино-вая кислота, способствует прогрессии деформации суставов. Материалы и методы: Были исследованы больные ОА в количестве 25 человек (критерии ОА по классификации согласно Althman R.D., 1995). Группа сравнения – 10 добровольцев без патологии суставов. Все участники исследования были женщинами. Для исследования состояния питания была использована компьютерная программа «Анализ состояния питания челове-ка» версия 1.2.4 ГУ НИИ питания РАМН 2003-2006гг. Результаты исследования: Необходимо отметить, что показатели мас-сы тела и соответственно, ИМТ были выше в группе больных ОА, что под-тверждает ведущую роль избыточной массы тела и ожирения в генезе ОА. В группе больных ОА питание было достаточно несбалансированным по основ-ным нутриентам. Соотношение белков и жиров было 1/1,6 вместо 1/1 при рациональном питании, в контрольной группе данное соотношение было 1/1,1. Большее место в рационе питания больных ОА в сравнении с контро-лем занимали углеводы, при этом пищевые волокна составляли только чет-вертую часть от минимально необходимого потребления. Данное соотноше-ние наблюдалось в обеих группах. Больные ОА больше потребляли насы-щенных жиров. При этом оказались практически одинаковые показатели потребления полиненасыщенных жирных кислот. Соотношение Ω-3 ПНЖК/ Ω-6 ПНЖК в два раза превышает рекомендуемые нормы. Увеличенное по-требление Ω-6 ПНЖК ведет к усилению воспалительного компонента в пато-генезе ОА. Количество потребляемого кальция в обоих группах примерно в два раза ниже рекомендуемых величин, что способствует усилению остеопоротиче-ских процессов в организме. При этом потребление магния в группе больных ОА в 2 раза ниже нормы. Дефицит аскорбиновой кислоты присутствует в рационах обеих групп, но в группе ОА он несколько более выражен.
Выводы: У больных ОА отмечается нерациональное питание с низким потреблением белка, пищевых волокон,Ω-3 ПНЖК, кальция, магния, аскор-биновой кислоты, что ведет к нарушениям в процессах репарации хрящевой и костной тканей. Также у этих больных имеет место избыточное потребле-ние жиров, из-за чего отмечаются более высокие цифры ИМТ, ведущей к постоянно увеличенной механической нагрузки на суставы.
Войналович-Ханова Ю.А.
Количество потребляемого кальция в обоих группах примерно в два раза ниже рекомендуемых величин, что способствует усилению остеопоротиче-ских процессов в организме. При этом потребление магния в группе больных ОА в 2 раза ниже нормы. Дефицит аскорбиновой кислоты присутствует в рационах обеих групп, но в группе ОА он несколько более выражен.
Выводы: У больных ОА отмечается нерациональное питание с низким потреблением белка, пищевых волокон,Ω-3 ПНЖК, кальция, магния, аскор-биновой кислоты, что ведет к нарушениям в процессах репарации хрящевой и костной тканей. Также у этих больных имеет место избыточное потребле-ние жиров, из-за чего отмечаются более высокие цифры ИМТ, ведущей к постоянно увеличенной механической нагрузки на суставы.
Войналович-Ханова Ю.А.
СИНДРОМ РЕМОДЕЛИРОВАНИЯ МИОКАРДА-7 (КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ)
ГБУ РО «Областная клиническая больница № 2», г. Ростов-на-Дону, Россия. Современный больной характеризуется наличием транссиндромальной, транснозологической и хронологической полиморбидности (коморбидности), что требует максимальной индивидуализации лечения с одновременным лабораторным и инструментальным контролем состояния здоровья и результатов лечения. Формальное исполнение стандарта лечения не позволяет учитывать всю неповторимость клинического случая. Лечащему врачу необходим универсальный показатель, характеризующий состояния миокарда и эффективность проводимой терапии. Таким может быть контроль за ремоделированием миокарда, особенно в динамике, на протяжении ряда лет. Под нашим наблюдением 9-й год находится мужчина, 64 лет, продолжающий выполнять работу служащего в полном объеме с удовлетворительным качеством повседневной жизни. В 2003 году в течение 4-х месяцев он пере-нес два трансмуральных инфаркта миокарда. До этого в течение 10 лет страдал ГБ, лечился нерегулярно. Течение заболевания осложнилось формированием аневризмы сердца, преходящими нарушениями ритма (желудочковая экстрасистолия), застойной сердечной недостаточностью ХСН IIA ФК III, стабильной стенокардией II-III ФК с периодическими ухудшениями. В начале наблюдения исходная масса сердца 263 г. Острый период ремоделирования миокарда, после перенесенных инфарктов, за 3 месяца привел к увеличению массы сердца до 342 г(+30%). Стабилизация процессов ремоделирования наступила через год после ИМ. Диастолическая дисфункция ЛЖ исчез-ла, но сохранялась незначительная дилатация ЛЖ, толщина стенок не изменилась. ФВ увеличилась до 41%. Через полтора года наблюдения и лечения масса миокарда продолжала снижаться и составила 237 г. (-11% от исходной и 40% от максимальной). В результате проводимого «Д» наблюдения и лечения на протяжении ряда лет масса миокарда оставалась стабильной, и год назад составляла 150г (-40% от предыдущей и -57% от максимальной). В мае 2011 больной перенес третий ИМ, по поводу которого проводился системный тромболизис, КАГ и операция: Прямая реваскуляризация миокарда в условиях ИК (АКШ аутовеной с ВТК ОВ ЛКА, ЗМЖ МКШ-ПМЖВ). Описание клинической ситуации и результаты динамического наблюдения в течение года описаны в статье по адресу: http://visualrheumatology.ru/sindrom-remodelirovaniya-miokarda.html. В клинической картине заболевания присоединились явления легочной гипертен-зии и застоя в большом круге кровообращения. В результате проводимого лечения легочная гипертензия исчезла, уменьшились явления сердечной недостаточности. Подробное описание ле-чебных и диагностических мероприятий в течение года представлены в статье по адресу: http://visualrheumatology.ru/www-remodelirovanie-html.html. В 2012 году состояние пациента оставалось стабильным. Динамический УЗИ контроль показал постинфарктное ремоделирование ЛЖ. Акинезию передней стенки ЛЖ с переходом на ММП и верхушку. Участок дискинезии на верхушке ЛЖ. Фракция выброса за год наблюдения снизилась с 37% до 33%. ДДЛЖ I типа сменилась ДДЛЖ II типа . Толщина задней стенки ЛЖ и межжелудочковой перегородки 11мм( гипертрофия +1 и +2мм соответ-ственно). Давление в полости ПЖ в норме, легочной гипертензии нет. Имеет-ся небольшая относительная недостаточность трехстворчатого клапана. По-дробное описание клинического наблюдения за 2012 год данные представ-лены по адресу http://visualrheumatology.ru/sindrom-remodelirovaniya-miokarda-7.html Обсуждение. Выполнение стандартов и протоколов лечения и обследования в рамках национальных кардиологических рекомендаций с персонифицируемой терапией конкретного больного позволяет реально продлить жизнь и сохранить ее качество для пациента. Регулярный, плановый УЗИ -контроль за ремоделированием миокарда дает возможность выбрать оптимальную терапию до появления выраженных клинических проявлений или осложнений основного заболевания. Воропай Л.А., Елкина Т.Н., Воропай Н.Г.ПРИМЕНЕНИЕ СИСТЕМНОЙ ЭНЗИМОТЕРАПИИ В ЛЕЧЕНИИ РЕАКТИВНЫХ АРТРИТОВ У ДЕТЕЙ
Новосибирский государственный медицинский университет, Городской неврологический центр Сибнейромед, г. Новосибирск, Россия Целью лечения реактивных артритов является быстрое купирование су-ставного синдрома, с полным восстановлением функции пораженных суста-вов, отсутствием рецидивов и трансформации в хронический процесс. В про-токоле лечения реактивных артритов используются антибиотики, нестеро-идные противовоспалительные препараты, но не всегда цель бывает достиг-нута. В связи с этим наше внимание было обращено на системную энзимоте-рапию (вобэнзим), которая стала широко использоваться в педиатрии. Воб-энзим ограничивает очаг воспаления, устраняет продукты повреждения при воспалении, поддерживает процессы регенерации тканей, препятствует хронизации процесса. Системная энзимотрепия – это самостоятельное направление медикамен-тозного лечения, использующее комплексное воздействие на организм энзи-мов. Энзимы – это специфические белки, способные ускорить химические процессы в живых организмах, их можно назвать биокатализаторами. В ре-зультате многочисленных исследований немецких ученых получены специ-ально подобранные смеси гидролитических ферментов (гидролаз). Гидрола-зы, хоть и являются белками, лишены антигенных свойств, благодаря анти-протеиназам, находящимся в организме человека. Блокирующее действие антипротеиназ снижает активность ферментов, лечебный эффект снижается на 20%, поэтому необходимо назначать высокие дозы препарата. Взаимо-действие вобэнзима с иммунной системой человека проявляется расщепле-нием и элиминацией циркулирующих иммунных комплексов. Вобэнзим обла-дает иммуномоделирующим действием, т.к. контролирует как недостаточ-ность, так и чрезмерность иммунного ответа с возможным переходом к ауто-агрессии. Системные энзимы (вобэнзим) не подавляют, а ограничивают очаг воспаления, устраняют продукты повреждения, поддерживает процессы ре-генерации тканей, препятствуют хронизации воспалительного процесса, ускоряют выведение провоспалительных цитокинов. Влияние вобензима на систему гемостаза при воспалении проявляется снижением агрегации тром-боцитов и эритроцитов, снижением тробогенного потенциала эндотелия, ак-тивацией фибринолиза. Вобэнзим, при сочетанном применении с антибиоти-ками, снижает их токсичность и побочные действия, в том числе и дисбакте-риоз. Материалы и методы: обследовано 50 детей с реактивными артритами в возрасте от 8 до 12 лет, 20 девочек, 30 мальчиков. Основной причиной реактивных артритов (54%) была патология ЖКТ и почек. У 15 детей забо-леванию предшествовала вирусная инфекция, у двух детей артрит возник после прививки. У 60% детей выявлена хроническая носоглоточная инфек-ция, у 6 детей причиной артритов доказана А-стрептококковая инфекция. 70% детей имели в анамнезе аллергию, чаще поливалентную. У 40% детей заболевание протекало по типу моноартита, у 60% был олигоартрит. Чаще поражались коленные и голеностопные суставы. На рентгенограммах пора-женных суставов отмечалось утолщение мягких тканей, на УЗИ – у всех об-следованных выявлены синовиты и небольшое количество жидкости в пора-женных суставах. Дети были разделены на 2 группы: I группа получала бруфен в возрастной дозировке и местное лечение: лазеротерапия, гели с противовоспалительными препаратами. Во II группе детей кроме перечис-ленных препаратов был добавлен вобэнзим (3-5 таблеток 3 раза в день). Динамика клинико-лабораторных показателей оценивалась комплексно: уровень боли по шкале ВАШ, по числу припухших суставов, по индексу Ричи, функциональному тесту Ли, уровню СОЭ, СРБ, АСЛО. Эффективность лечения оценивалась через 2 недели. Результаты: в I группе все показатели уменьшались, но нормы не до-стигали, сохранялись синовиты и жидкость в суставах на УЗИ. Во II группе все показатели нормализовались (оценка по шкале ВАШ – 0, индекс Ричи 0, число припухших суставов 0, функция суставов восстановлена полностью, СОЭ 10 мм/час, СРБ – 2. На УЗИ суставов – только остаточные явления си-новитов, жидкости нет. В I группе у 8 детей появились боли в эпигастрии, у 3 – детей аллергиче-ская сыпь, у 5 детей выявлен дисбактериоз. У 10 детей ЛОР-врач выявил обострение хронического тонзиллита. Во II группе за время лечения не вы-явлено ни одного побочного действия лекарственных препаратов. Хороший эффект во II группе мы связываем с применением вобэнзима, обладающим хорошим противовоспалительным эффектом при хорошей переносимостью препарата. Выводы: таким образом, применение вобэнзима, наряду с традицион-ным лечением, позволит детским ревматологам более эффективно решить проблему лечения реактивных артритов. Вобэнзим можно считать патогене-тическим препаратом при лечении реактивных артритов. Вобэнзим обладает значительно меньшим количеством побочных действий, чем НПВП, не уступая им по противовоспалительному эффекту. Гайдукова И.З., Ребров А.П., Полянская О.Г., Спицина М.Ю.НАРУШЕНИЯ ФУНКЦИИ ПЕЧЕНИ И ПОЧЕК ПРИ ДЛИТЕЛЬНОМ ПРИМЕНЕНИИ НИМЕСУЛИДА В РЕАЛЬНОЙ КЛИНИЧЕСКОЙ ПРАКТИКЕ
ГБОУ ВПО Саратовский ГМУ им. В.И.Разумовского Минздрава России Согласно современным рекомендациям нестероидные противовоспали-тельные препараты (НПВП) являются препаратами первой линии при лече-нии аксиального спондилоартрита (акс-СпА). Пациентам с персистирующей активностью и сохранением симптомов заболевания показано их длительное применение. Существенно ограничивают выполнение данной рекомендации нежелательные явления, ассоциирующиеся с приемом НПВП, из которых наиболее значимыми являются ульцерогенный эффект, кардио-, гепато- и нефротоксические эффекты. Цель исследования – изучение встречаемости нарушений функции пе-чени и/или почек у пациентов с аксиальным спондилоартритом (акс-СпА), принимающих нимесулид не менее 1 года, и их ассоциации с особенностями применения препарата в реальной клинической практике. Материалы и методы. Обследовали 96 пациентов c акс-СпА, соответ-ствующим критериям ASAS для акс-СпА (2009). Средний возраст пациентов составил 42,3 ± 10,5 года, длительность заболевания – 14,1 ± 8,0 лет, муж-чины составили 55,2% (n=53). Исследовали ОАК, ОАМ, С-РБ; общий белок, альбумины, мочевину, креатинин, глюкозу, билирубин, аспартат- и аланина-минотрансферазу (АСТ, АЛТ), ГГТП, щелочную фосфатазу сыворотки крови; суточную протеинурию. Наличие гипостенурии констатировали при сниже-нии удельного веса утренней мочи менее 1018 у.е. на фоне сухоядения. Скорость клубочковой фильтрации (СКФ) рассчитывали по формуле MDRD. Наличие ХБП констатировали на основании рекомендаций K/DOQI, 2002. Активность СпА определяли путем расчета индекса BASDAI. Пациентам предоставляли вопросник, уточняющий длительность, кратность приема и применяемые пациентом дозировки нимесулида. Статистическую обработку осуществляли с использованием программ Microsoft Office Exсel 2007 (Microsoft Corp., США) и Statistica 8.0 (StatSoft Inc., США). Результаты. Более года принимали нимесулид 70 (72,92%) пациентов: 8 больных – курсами по 10 дней несколько раз в год, 12 пациентов – несколь-ко раз в неделю, 26 больных – постоянно, 24 пациента – в режиме «по тре-бованию». Суточная доза препарата, принимаемого пациентами в реальной клинической ситуации, существенно различалась: 24 пациента обычно при-нимали 200 мг препарата в сутки, 34 больных – 400 мг в сутки, 12 пациен-тов – более 500 мг в сутки. При сильных болях 18 (25,7%) пациентов при-нимали от 500 до 800 мг препарата в сутки, 2 (2,85%) пациента – более 800 мг препарата. Из опрошенных пациентов 22 (31,43%) отметили, что превы-шали дозу 400 мг/сутки несколько раз в год, 3 (4,2%) больных– несколько раз в месяц, 2 (2,85%) пациента нарушали режим дозирования постоянно. Повышение печеночных ферментов до 2-х норм установили у 4 пациентов, у 1 больного – до 4-х норм. Признаки ХБП установили у 52 (78,78%) пациен-тов (n=66). Изолированное снижение СКФ < 90 мл/мин/1,73м2 выявили у 24 (36,36%) пациентов, протеинурию – у 23 (34,84%), гипостенурию – у 40 (60,6%) больных. Установлена взаимосвязь между длительностью приема нимесулида и СКФ (R Спирмена = – 0,34, p=0,02). СКФ у пациентов, применявших нимесулид курсами несколько раз в год в рекомендованной дозировке, составила 93,2 ± мл/мин/1,73м2 (n = 8); у пациентов, принимавших нимесулид несколько раз в неделю или постоянно – 84,1 ± мл/мин/1,73 м2 (n = 21); у пациентов, принимавших препарат несколько раз в неделю или постоянно в дозировке, превышавшей 400 мг/сутки, СКФ составила 68,2 ± мл/мин/1,73 м2 (n =14). Различия между значениями СКФ пациентов, принимавших 200-400 мг препарата и более 400 мг нимесулида в сутки, достоверны (p<0,05). Курсовый прием препарата несколько раз в год ассоциируется с формированием ХБП в 25% случаев (частота встречаемости ХБП в популяции составляет 39%), постоянный длительный прием нимесулида в дозе 400 мг в сутки ассоциируется с формированием I ст. ХБП не более чем у 40% пациентов (различия с частотой встречаемости ХБП в общей популяции установлено не было). Прием препарата в дозировках, превышающих рекомендованные дозы, приводит к формированию ХБП в 100% случаев и более значимо-му снижению СКФ, при этом снижение СКФ установлено у 92,85% пациентов. Выводы. У пациентов с акс-СпА постоянный длительный прием нимесулида в максимально рекомендованных дозах ассоциируется с обратимыми нарушениями функции печени в 7% случаев и формированием I ст. ХБП у 40% пациентов. Каждый четвертый пациент со СпА периодически превышает рекомендованные дозировки нимесулида, что ассоциируется с большей частотой встречаемости ХБП и более выраженным снижением СКФ, чем у лиц, соблюдающих рекомендованный режим дозирования препарата. Галаева О.Ю., Мартемьянов В.Ф., Зборовская И.А., Бедина С.А., Стажаров М.Ю., Мозговая Е.Э.АКТИВНОСТЬ ЭНЗИМОВ НУКЛЕИНОВОГО МЕТАБОЛИЗМА В ЛИЗАТАХ ЛИМФОЦИТОВ БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ НА РАННЕЙ СТАДИИ ЗАБОЛЕВАНИЯ
ФГБУ «НИИ КиЭР» РАМН, Волгоград Под наблюдением находились 77 больных ревматоидным артритом (РА), из которых 20 (26%) мужчин. Средний возраст больных (М±m) – 42,3±1,0 лет. В соответствии с диагностическими критериями АРА и рабочей класси-фикации РА I степень активности процесса установлена у 15 (19,5%) боль-ных, II – у 50 (64,9%), III степень – у 12 (15,6%) больных. I стадия пораже-ния суставов – у 7 (9,1%), II – У 40 (51,9%), III – У 24 (31,2%) и IV стадия – у 6 (7,8%) больных. В плазме, лизатах лимфоцитов и эритроцитов по ори-гинальным методикам определялась активность аденозиндезаминазы (АДА), АМФ-дезаминазы (АМФДА) и адениндезаминазы (АД). Результаты. По сравнению со здоровыми у больных РА в плазме ниже активность АД (р<0,001), в эритроцитах выше активность АМФДА и АД (все р<0,001), в лимфоцитах ниже активность АДА и АД (все р<0,001) и выше АМФДА (р<0,001). Чем выше активность процесса, тем в плазме ниже актив-ность АДА, АМФДА и выше АД, в лимфоцитах ниже АДА, АД и выше АМФДА, в эритроцитах ниже активность АДА, выше АД и АМФДА. Определенное влия-ние на энзимную активность оказывает стадия поражения суставов: чем больше стадия, тем в плазме ниже активность АДА, АМФДА и АД, в эритроцитах ниже АДА, выше АМФДА и АД, в лимфоцитах выше активность АМФДА и ниже АД. Чтобы определиться, что же больше влияет на активность энзимов – степень активности процесса или стадия поражения суставов, и не может ли стадия помешать уточнению степени активности процесса по энзимным показателям, мы провели следующие сравнительные исследования. У больных РА с I степенью и II стадией, по сравнению с больными РА с II степенью и I стадией, в плазме выше активность АДА (р<0,05), ниже АМФДА (р<0,001) и АД (р<0,01), в лимфоцитах выше активность АДА (р<0,01),АД (р<0,05), ниже АМФДА (все р<0,001), в эритроцитах выше активность АДА (р<0,05), ниже АМФДА (р<0,001) и АД (р<0,05). У больных РА с II степенью и III стадией, по сравнению с больными РА с III степенью и II стадией, в плазме выше активность АДА, АМФДА и ниже АД, в лимфоцитах выше активность АДА, АД и ниже АМФДА, в эритроцитах выше активность АДА, ниже АМФДА и АД (все р<0,001). Заключение. Результаты проведенных исследований показали, что, не-смотря на определенное влияние стадии поражения суставов на активность энзимов, влияние активности процесса на энзимные показатели более выраженное, что позволяет уточнить степень активности ревматоидного процесса при любой стадии поражения суставов. Галаева О.Ю., Мозговая Е.Э., Зборовский А.Б., Кузнецов В.И., Мартемьянов В.Ф.ЭНЗИМНАЯ АКТИВНОСТЬ В ЛИЗАТАХ ЛИМФОЦИТОВ БОЛЬНЫХ РАННИМ РЕВМАТОИДНЫМ АРТРИТОМ
ФГБУ «НИИ КиЭР» РАМН, МУЗ «КБ СМП №15», г.Волгоград Цель исследования: изучить особенности активности аденозиндезами-назы (АДА), АМФ-дезаминазы (АМФДА), адениндезаминазы (АД) и 5′-нуклеотидазы (5′-НТ) в лизатах эритроцитов больных ранним ревматоидным артритом (РРА). Материал и методы. Под наблюдением находились 55 больных РРА, из которых 40 (72,7%) женщин. Средний возраст больных (М±σ) 48,1±3,2 лет, длительность болезни – от 2 до 11 месяцев (5,4±0,4) Диагностика РРА проводилась на основании диагностических и классификационных критериев ACR и EULAR, 2010. Серопозитивная форма определялась у 35 (63,6%) больных, с системными поражениями – у 6 (10,9%), полиартрит – 78,2%, I стадия поражения суставов – 65,5%, II стадия – 34,5%, ФК-1 – 16,4%, ФК-2 – 41,8%, ФК-3 – 41,8%. I степень активности процесса установлена у 12 (21,8%) больных, II степень – у 25 (45,5%), III степень – у 18 (32,7%) бал-лов. Активность АДА, АМФДА, АД и 5′-НТ в лизатах лимфоцитов определялась по оригинальным методикам. Результаты. По сравнению со здоровыми у больных РРА (всей группы) выше активность АДА, 5′-НТ, АМФДА и ниже активность АД (все р<0,001), у больных с I степенью выше активность АДА, 5′-НТ, ниже АД (все р<0,001), у больных с II степенью выше активность АДА, АМФДА, 5′-НТ и ниже АД (все р<0,001), у больных с III степенью выше активность АМФДА (р<0,001), АД (р=0,048), 5′-НТ (р<0,001). Сравнительные исследования показали, что у больных с I степенью по сравнению с II степенью ниже активность АДА (р=0,004), АМФДА (р<0,001), 5′-НТ (р=0,002) и выше АД (р<0,001); по сравнению с III степенью выше активность АДА, ниже АМФДА, АД и 5′-НТ (все р<0,001). У больных с II степенью по сравнению с III степенью выше активность АДА, ниже АМФДА, АД (все р<0,001) и 5′-НТ (р=0,041). Заключение. Проведенные исследования показали, что уже на ранней стадии РА имеются существенные нарушения пуринового метаболизма в лимфоцитах крови, что может инициировать и поддерживать иммунные нарушения, составляя один из патогенетических механизмов РА, а выявленные энзимные различия между степенями активности патологического процесса могут способствовать уточнению клинического диагноза и назначению адекватной терапии. Гонтарь И.П., Маслакова Л.А., Красильников А.Н., Емельянов Н.И.КЛИНИКО-ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ ИССЛЕДОВАНИЯ АКТИВНОСТИ, КОЛИЧЕСТВА И АНТИТЕЛ К ЦЕРУЛОПЛАЗМИНУ В СЫВОРОТКЕ БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ
ФГБУ НИИ КиЭР РАМН; кафедра госпитальной терапии ВолГМУ Антителообразование к церулоплазмину (ЦП) при ревматоидном артрите (РА) представляет собой малоизученную проблему. Выбор этого медьсодержащего альфа 2 – гликопротеида плазмы крови, обладающего мультиферментными свойствами в качестве объекта исследования не случаен. Данные о содержании и активности ЦП в крови больных РА весьма противоречивы, что связано с различными подходами к отбору больных и разными методиками определения. Цель: усовершенствование иммунологической диагностики РА путем определения АТ к ЦП, а также количества его и ферментативной активности. Материалы и методы исследования. Исследовалась сыворотка 30 практически здоровых лиц (доноров Областной станции переливания крови), 108 больных РА. Исследование проводилось в соответствии с принципами Хельсинкской декларации Международной медицинской ассоциации (1996г.). Соблюдение требований биоэтики подтверждено результатами экспертизы Регионального этического комитета. Обследованные нами больные являлись пациентами ревматологических отделений ГУЗ ГКБ № 25 г. Волгограда и ГУЗ ГБ № 1 г. Волжского. АТ к ЦП определяли иммуноферментным методом с использованием им-мобилизированных гранулированных антигенных препаратов (ИГАП). Полученные значения выражали в единицах оптической плотности (е.о.п.) и считали положительными при превышении величин экстинции, найденных для здоровых лиц, более чем на 2д. Определение количества ЦП проводили иммуноферментным методом по И.С. Кузьминой и сотр. (1991) с использованием коммерческого иммуноферментного диагностикума производства НИИ вакцин и сывороток им. И.И. Мечникова РАМН (г. Москва) ФС 42-42ОВС –93 серия №12. Обработка данных проводилась с использованием программного пакета STATISTICA FOR WINDOWS. Результаты исследования. По данным ИФА средний уровень антител к ЦП в донорских сыворотках составил 0,020±0,006 е.о.п. Уровень нормальных показателей специфических антител, определяемый как М±2σ, включает значения экстинкции в интервале от 0 – 0,086. Среднее значение оксидазной активности и количества ЦП у здоровых лиц составило 716±26,3 и 921±32 нг/мл соответственно. В процессе исследований выявлено достоверное повышение содержания антител к ЦП, активности и количества ЦП у больных РА, при этом во всех случаях исследуемые показатели коррелировали со степенью активности заболевания (р<0,05), при I степени активности – АТ к ЦП 0,098±0,011, активность – 954±48,1, количество ЦП – 1292±73,4; при II ст. активности – АТ к ЦП 0,138±0,007, активность ЦП – 1163±39,6, количество ЦП – 1763±69,3; при III – АТ к ЦП –0,182±0,015, активность ЦП – 1368±89,5, количество ЦП – 1794±102,8. По окончании курса стационарного лечения по сравнению с исходными данными происходило достоверное снижение активности и количества ЦП (при I степени активности РА р<0,001 и при II степени – р<0,01 для обоих показателей, при III степени -р<0,05). Снижение антител к ЦП отличается замедленной динамикой, особенно у больных с выраженной активностью патологического процесса, что отражает серьезные нарушения в иммунной системе, полностью не купирующиеся за 30-40 дневный курс стационарного лечения. Выводы: Определение антител к ЦП, а также его количественное содержание и оксидазной активности, могут служить не только показателем активности, клинико-анатомической формы, характера течения, клинического варианта РА, но и дополнительным критерием эффективности проводимой терапии. Гонтарь И.П., Трофименко А.С., Емельянов Н.И., Трубенко Ю.А., Симакова Е.С.ЭФФЕКТИВНОСТЬ РАСЩЕПЛЕНИЯ ФРАКЦИЙ ЦИРКУЛИРУЮЩЕЙ ДНК ПРИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКЕ. ДОКЛИНИЧЕСКОЕ ИЗУЧЕНИЕ КОМБИНИРОВАННОГО СОРБЕНТА
ФГБУ НИИ КиЭР РАМН; кафедра госпитальной терапии ВолгГМУ В настоящее время принято считать, что внеклеточная ДНК персистирует у больных системной красной волчанке (СКВ) в виде двух основных форм: «свободной», находящейся в комплексе с транспортными молекулами (SAP, C1q-компонент комплемента и СРБ), а также связанной с антителами в со-ставе циркулирующих иммунных комплексов (ЦИК). Доказана существенная роль ДНК-содержащих иммунных комплексов (ИК) в прогрессировании по-ражения почек при СКВ. Кроме того, выдвинута гипотеза о ведущей роли персистенции обеих форм внеклеточной ДНК в индукции и поддержании синтеза антител к ДНК при СКВ (Berden J.H.M., 2003; Mortensen E.S. et al., 2008). Удобным инструментом для разрушения ДНК является дезоксирибону-клеаза I типа (ДНКаза I), иммобилизированная на магнитоуправляемых по-лиакриламидных гранулах (МПГ). Однако в ходе ферментативного расщеп-ления образуются также свободные антитела к ДНК, обладающие значитель-ным патогенным потенциалом. Данный побочный эффект может быть умень-шен путем совместного применения композиции иммобилизированной ДНКа-зы I и иммобилизированного C1q-компонента комплемента, фиксирующего промежуточные продукты распада ИК. Цель: изучение эффективности снижения содержания ДНК и ДНК-содержащих ЦИК путем пропускания крови через смесь МПГ с иммобилизи-рованной ДНКазой I и МПГ с иммобилизированным C1q (далее эта компози-ция обозначается как «комбинированный сорбент»). Материалы и методы: МПГ с иммобилизированной ДНКазой I и МПГ с иммобилизированным C1q получали раздельно, используя метод И.П. Гонта-ря с соавт. (1992). В колонку объемом 40 мл вносили МПГ: при исследовании комбинированного сорбента – смесь МПГ с иммобилизированной ДНКазой I и МПГ с иммобилизированным C1q в соотношении 3 : 1 (объем : объем), при исследовании прототипа – МПГ с иммобилизированной ДНКазой I. Через комбинированный сорбент и прототип перфузировали со скоростью 10 мл/ч образцы нативной гепaринизированной крови 23 больных СКВ объемом 20 мл. Содержание ЦИК в сыворотке крови определяли методом преципитации в ПЭГ-6000 по методу Лемперта (1988), концентрацию сывороточных антител к двуспиральной ДНК (анти-дсДНК) – методом ИФА с использованием ком-мерческих наборов (Orgentec Diagnostika, Германия), концентрацию ДНК – флюориметрическим методом с использованием флюорофора «PicoGreen» (Invitrogen-Molecular Probes, Юджин, США) по методу, описанному V.L. Singer et al. (1997). Значения всех исследуемых показателей для каждого образца измеряли до и после перфузии, выражая их как среднее арифметическое и 95% доверительный интервал (М (95%ДИ)); различия тестировали с помощью непарного t-критерия Стъюдента. Результаты и обсуждение: Исходные значения ЦИК, ДНК и анти-дсДНК составили 7,6 (6,7-8,5) Ед, 141,0 (129,9-152,1) нг/мл и 46,4 (36,9-55,9) МЕ/мл, соответственно. После перфузии через комбинированный сорбент уровни ЦИК, ДНК и анти-дсДНК составляли 2,3 (1,1-3,5) Ед, 72,2 (63,6-80,8) нг/мл 50,3 (39,7-60,9) МЕ/мл и 53,7 (44,2-63,2) МЕ/мл, соответственно. Различия между исходным и конечным значениями для ЦИК и ДНК были статистически значимыми (р < 0,001); для анти-дсДНК р = 0,211. Средние темпы прироста ЦИК, ДНК и анти-дсДНК составили -69,7 (-82,2 – -57,2)%, -50,2 (-63,8 – -36,6)% и 8,4 (-2,0 – 18,8)%, соответственно. Выводы: Из вышеприведенных результатов следует, что перфузия через смесь МГ с ДНКазой I и МГ с C1q вызывает существенное снижение изменения как концентрации ЦИК, так и концентрации циркулирующей «свобод-ной» ДНК; выраженность изменений этих двух показателей была сопоставимой. Кроме того, концентрация антител к двуспиральной ДНК при использовании комбинированного сорбента повышается на 8,4%; данная динамика не является статистически значимой. Следовательно, перфузия через комбинированный сорбент может быть эффективным инструментом элиминации обеих форм циркулирующей ДНК при СКВ и, в перспективе, полезным иммуномодулирующим средством в комбинированной терапии данного заболевания. Гордеева И.Е., Матохина Н.В.ПЕРИАРТРОПАТИИ В ПРАКТИКЕ НЕВРОЛОГА: ОПТИМИЗАЦИЯ ТЕРАПИИ
Кафедра неврологии, нейрохирургии с курсом медицинской генетики ВолгГМУ Боли в области суставов, связанные с патологией периартикулярных мягких тканей, довольно частая нейроортопедическая проблема и нередкая причина нетрудоспособности в зрелом возрасте; так, например, распростра-ненность плечелопаточного периартрита составляет до 4-7% в популяции, увеличиваясь с возрастом до 15-20% у 60-70 летних (Астапенко М.Г., 1975; Walch G., 1999; Makela М., 1999; Солоха О.А., 2004). До настоящего времени эта патология является предметом обсуждения врачами смежных специальностей: неврологами, ортопедами, ревматологами, но большинство пациентов с такой патологией ведутся неврологами, т.к. патологии самих суставов у большинства не обнаруживается (Солоха О.А., 2004). Основными патогенетическими вариантами периартропатий являются – первичный дегенеративный процесс в сухожилиях мышц в сочетании с их хронической микротрав-матизацией, ишемией и реактивным воспалением, адгезивный капсулит и миотонический (миофасциальный) синдром с формированием активных и пассивных триггерных пунктов в пораженных мышцах (Тревелл Дж.Г., Симмонс Д.Г. , 1989; Bonica J.I. , 1990; Попелянский Я.Ю. , 2003). Учитывая многообразие патогенетических факторов и вариантов формирования боле-вого синдрома, двигательной дисфункции, а также недостаточную эффективность традиционных методов лечения (НПВС, ФТЛ, массаж и ЛФК) ( Вейн А.М., Авруцкий М.Я., 1997; Teefey S.A., 2000; Беленький А. Г., 2004), акту-альной является проблема поиска оптимальной и наиболее эффективной методики лечения. Мы обследовали группу больных – 65 человек (37 женщин и 28 мужчин в возрасте от 34 до 73 лет) с периартропатиями различной локализации. Всем пациентам назначался стандартный набор исследований (ОАК, ОАМ, рентгенография заинтересованного сустава, неврологический осмотр с выявлением периартикулярных триггерных пунктов, анкетирование больных с помощью специально разработанной анкеты, а также определение интенсивности бо-левого синдрома по ВАШ). Из них у 27 человек (41,5%) была выявлена периартропатия плече-лопаточной локализации, у 24 (36,9%) человек – илеосакральной локализации, у 10 больных (15,3%) – тазобедренной локализа-ции, у 4 пациентов (6,1%) – локтевой локализации. Больные в произвольном порядке были поделены на две подгруппы. Первой подгруппе (32 пациента) была назначена стандартная схема лечения (НПВС, миорелаксанты, ФТЛ, ЛФК). Второй группе больных (33 пациента) были назначены микроинвазив-ные методы лечения (лидокаиновые и лидокаин-дексаметазоновые блокады с помощью инсулиновых шприцов) и постизометрическая релаксация мышц (Иваничев Г.А.), выполняемая как врачом, так и обученнм пациентом не-сколько раз в течение дня. Средняя продолжительность курсового лечения была 14,1+3,2 дней. В первой группе интенсивность болевого синдрома по ВАШ до лечения составила 57,8+4,3%, после лечения – 43,2+2,9% (р<0,05). Во второй группе – интенсивность болевого синдрома по ВАШ до лечения составила 60,3+3,9%, после лечения – 23,2+3,9% (р<0,001). Ку-пирование болевого синдрома более чем на 50% в первой группе отмечалось на 6,5+2,3 сутки, а во второй группе – на 3,2+1,1 сутки. Увеличение объема движений в заинтересованном суставе до нормы происходило в первой группе – на 10,5+ 2,9 сутки, а во второй группе – на 5,7+2,5 сутки. Таким образом, применение микроинвазивных методов лечения и постизометрической релаксации мышц показало высокую эффективность в лечении больных с периартропатиями по сравнению с традиционными методиками. Греков И.Ю., Ханов А.Г.ЗНАЧЕНИЕ ВИЗУАЛЬНЫХ ОБРАЗОВ В РЕВМАТОЛОГИЧЕСКОЙ ПРАКТИКЕ
ФГАОУ ВПО «Южный федеральный университет», ГБУ РО «Областная клини-ческая больница №2» г. Ростов-на-Дону, Россия Ревматология – один из «счастливых» разделов медицины имеющих возможность диагностировать заболевания на ранних стадиях и проводить не симптоматическое, а патогенетическое лечение РЗ. Так, по мнению ряда авторов, диагноз РА может быть установлен даже впервые часы заболевания, а артрит необходимо лечить как неотложное состояние. Ранний период заболевания рассматривается как «окно возможностей», когда терапия может дать максимальный эффект в снижении активности и значительного улучшения отдаленного прогноза. При этом, в лечении РЗ основное внимание отводится терапии «treat to target». Теоретические предпосылки для успехов ревматологической помощи имеются, но реальная практика ревматолога как «узкого» специалиста показывает, что РЗ диагностируются далеко не на ранних стадиях, а консультация ревматолога больше подходит к стадии «end-stage». Некоторые практические врачи затрудняются в диагностике подострых или ранних стадиях хронических состояний без лаборатории, рентгенограмм, а невропатологи в топической диагностике без КТ и МРТ. Показатели заболеваемости БКМС по Ростовской области (РО) отличаются от средних значений по РФ. Разброс значений показателя зарегистрированных заболеваний ревматической группы, подлежащих статистическому учету, составляет 3-5 раз в целом. Различия в показателях болезненности и заболеваемости по отдельным нозологиям РЗ в РО между сельскими территориями и городами составляют 2-3 раза. Складывается ситуация, что в 40% сельских территорий в течении года не устанавливался диагноз Болезни Бехтерева. Обеспеченность врачебными кадрами РО, в целом, меньше чем по РФ. 42 врача-ревматолога не могут решить проблем 4,2 млн населения РО. Причем, 85% ревматологов работают в областном центре. Более подробная информация по обеспеченности врачами специалистами, их распределения по тер-ритории области, заболеваемости взрослого населения БКМС, отдельными нозологиями и их территориальном распределении по адресу http://visualrheumatology.ru/zdorove-vzroslogo-naseleniya-rostovskoy-oblasti-2-4.html Решение проблемы ранней диагностики РЗ возможно только путем повышения информированности врачей массовых терапевтических специальностей по вопросам ревматологии, тесном сотрудничестве с неврологами, хирургами поликлиник и травматологами-ортопедами. Для этого достаточно постоянно информировать их об основных, часто встречающихся РЗ, таких как РА, АС, подагра, ОА и других. Возможно, даже ограничиться основными признаками артрита или спондилита. Особенно это актуально для фельдшеров и акушерок сельских ФАП и ФП. В решении данной задачи важное место занимают визуальные образы в виде фотографий, рисунков, схем и диаграмм и картин известных художников с типичными проявлениями болезней, что позволит врачу уже на амбулаторном приеме, при первой встрече, «схватить», «увидеть» внешние признаки и симптомы РЗ. В качестве примера приводим возможности графики плаката отражения основных проблем «Слова о полку Игореве» по адресу http://visualrheumatology.ru/znachenie-vizualnyih-obrazov.html Грехов Р.А., Харченко С.А., Бондаренко Е.А.ПРИМЕНЕНИЕ МЕТОДА СТРУКТУРНО-РЕЗОНАНСНОЙ ЭЛЕКТРОМАГНИТНОЙ ТЕРАПИИ ПРИ РЕВМАТОИДНОМ АРТРИТЕ
ФГБУ «НИИ КиЭР» РАМН, Волгоград В лечении ревматоидного артрита (РА) за последние годы достигнут значительный прогресс. С помощью современных базисных противоревматических препаратов и особенно «биологических» агентов удается достигнуть существенного снижения активности заболевания и в целом улучшить прогноз болезни у многих пациентов. Тем не менее, фармакотерапия этого заболевания остается одной из наиболее сложных проблем медицины, а возможность полного излечения пациентов представляется сомнительной. В связи с чем, поиск новых методов в комплексной терапии РА остается до-вольно актуальным вопросом. Это требует системного подхода к планированию и проведению лечения, которое должно включать как традиционную лекарственную терапию, так и применение методов, рассчитанных на нормализацию естественных процессов регуляции гомеостаза. Весьма перспективным в этом плане представляется использование структурно-резонансной электромагнитной (СРЭМ) терапии – лечебной методики, в основе которой лежит воздействие на организм переменным электромагнитным полем, параметры которого соответствуют частотам спонтанной биопотенциальной активности органов и тканей здорового организма. Методы СРЭМТ все чаще привлекают внимание исследователей и врачей-ревматологов разных стран и получают все большее развитие. Цель настоящей работы – изучение сравнительной эффективности СРЭМТ и общепринятых методов лечения больных ревматоидным артритом (РА). В исследование были включены 70 больных с диагнозом РА, из них у 58 – суставная форма заболевания, у 12 – суставно-висцеральная. Женщин было 52 (74,3%), мужчин – 18 (25,7%). Средний возраст– 42,5 года. Средняя продолжительность заболевания -7 лет. Больные были разделены на две группы, сопоставимые по клиническим характеристикам заболевания. В основной группе пациенты получали ежедневные сеансы СРЭМТ на аппарате «РЕМА-ТЕРП» на фоне медикаментозной терапии. Курс – 10-15 сеансов. Контрольная группа, состоявшая из 30 человек, получала аналогичное медикаментозное лечение. Анализ эффективности терапии у больных РА проводился путем изучения динамики обязательных клинико-лабораторных показателей эффективности лечения и их сопоставления у больных основной и контрольной групп до и после лечения. Результаты лечения были достоверно лучшими в основной группе больных РА (χ2 = 7,57; p < 0,01), где наблюдалась достоверная положи-тельная динамика: уменьшение воспалительного индекса, суставного счета, времени утренней скованности, снижение СОЭ, С-реактивного протеина, серомукоида. Следовательно, в группе больных, получавших структурно-резонансную терапию, наблюдался не только анальгетический, но и более выраженный противовоспалительный эффект (χ2 = 4,44; р = 0,05). Можно предположить, что под действием электромагнитных низкочастотных токов в подлежащих тканях происходит активация системы регуляции локального кровотока, повышение резорбционной способности тканей, что приводит к ослаблению мышечного тонуса, усилению выделительной функции кожи и уменьшению отека в очаге воспаления. Кроме того, вследствие электроосмоса снижается компрессия болевых проводников. Таким образом, структурно-резонансная электромагнитная терапия является эффективной и безопасной лечебной методикой, воздействующей на различные звенья патогенеза РА. Григорьянц С.Р., Бедина С.А., Мозговая Е.Э., Мартемьянов В.Ф, Романов А.И., Евдокимова Е.В.АКТИВНОСТЬ ЭНЗИМОВ ПУРИНОВОГО МЕТАБОЛИЗМА В ПЛАЗМЕ КРОВИ БОЛЬНЫХ ЭНТЕРОГЕННЫМ РЕАКТИВНЫМ АРТРИТОМ И ПОДАГРИЧЕСКИМ АРТРИТОМ
ФГБУ «НИИ КиЭР» РАМН, г. Волгоград; ФГБУ «Центр реабилитации» УДП РФ, Московская область Цель исследования. Выявить особенности активности гуаниндезамина-зы (ГДА), гуанозиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфосфорилазы (ГФ) в плазме крови больных энтерогенным реак-тивным артритом (энтер.РеА) и подагрическим артритом (Под.А) с целью дифференциации заболеваний. Материалы и методы. Под наблюдением находились 24 больных эн-тер.РеА, из которых 10 (41,7%) женщин и 14 (58,3%) мужчин. Средний воз-раст больных 38,1±1,1 лет (триггерная инфекция – Yersinia enterocolitica). Группу больных Под.А составили 39 мужчин и 3 женщины (7,1%). Средний возраст больных 53,1±2,2 года. Интермиттирующая форма отмечалась у 15 больных, хроническая – у 27 больных. В плазме крови больных и 30 здоро-вых лиц по оригинальным методикам определялась активность ГДА, ГЗДА, ПНФ и ГФ. Результаты исследования. По сравнению со здоровыми, у больных эн-тер.РеА в плазме крови выше активность ГДА, ПНФ (все р<0,001), ниже ак-тивность ГЗДА (р<0,01) и ГФ (р<0,001); у больных с интермиттирующей формой под.А значимых энзимных различий не определялось (р<0,05); у больных с хронической формой под.А выше активность ГДА, ПНФ, ГФ и ниже ГЗДА (все р<0,001); у больных подагрой (всей группы) выше активность ГДА, ПНФ, ГФ и ниже ГЗДА (все р<0,001). Сравнительный анализ показал, что у больных энтер.РеА, по сравнению с больными с интермиттирующей формой под.А выше активность ПНФ (р<0,001), остальные энзимные различия малозначимы (р>0,05); по сравне-нию с больными с хронической формой под.А выше активность ГЗДА (р<0,001), ниже ГДА, ГФ (все р<0,001) и незначительно ниже ПНФ (р>0,05); по сравнению с больными Под.А (всей группы) выше активность ГЗДА (р<0,001), ниже ГДА, ГФ (все р<0,001) и незначительно выше активность ПНФ (р>0,05). Заключение. Определение активности ГДА, ГЗДА, ПНФ и ГФ в плазме крови больных энтерогенным РеА и подагрическим артритом в комплексе с клинико-инструментальными данными способствует дифференциации этих заболеваний. Давыдова А.Ф., Малхасян И.Г., Елисеева Л.Н., Кисьян Ж.А., Рассовская Т.А.СТЕРОИДСБЕРЕГАЮЩАЯ ЭФФЕКТИВНОСТЬ ГЕННО-ИНЖЕНЕРНОЙ БАЗИСНОЙ ТЕРАПИИ РЕВМАТОИДНОГО АРТРИТА
ГБОУ ВПО КубГМУ Минздрава России, Краснодар, Россия2 Краевая клиниче-ская больница №1 им С.В.Очаповского, Краснодар, Россия Применение глюкокортикостероидов (ГКС) остается наиболее частой причиной развития инфекционных и метаболических нарушений, стероидной спондилопатии и миопатического синдрома, язвенного поражения желудоч-но-кишечного тракта у больных с ревматоидным артритом (РА). Поэтому со-временные рекомендации по лечению РА рассматривают вопросы адекватности базисной терапии, исключающей необходимость коррекции активного процесса с использованием ГКС. Цель. На основании комплекса клинико-лабораторных и инструменталь-ных следований мы проанализировали использование различных схем тера-пии РА в аспекте снижения значимости применения ГКС. Под нашим наблюдением находилось 185 больные РА в возрасте от 22 до 78 лет (средний возраст 51,48±10,2 лет) с достоверным диагнозом РА. Сред-няя продолжительность заболевания составила 9,7±4,8 года (от 3 месяцев до 35 лет). Наряду с общеклиническим обследованием оценивали традици-онные показатели активности по DAS28, интенсивность боли по ВАШ, уро-вень здоровья по анкете НАQ, проявления депрессии и тревоги, нутритивный статус по шкале MNA, риск развития остеопороза и переломов по FRAX. Результаты исследования. Все обследованные пациенты в зависимости от применяемой базисной терапии разделены на 5 групп. В группе принимающих нестероидные противовоспалительные средства (НПВС) и ГКС без базисной терапии (отказ от лечения цитостатиками, длительность верифика-ции диагноза и др) отмечено наиболее частое нарушение нутритивного статуса с положительной корреляцией суммарной дозы ГКС и содержанием жировой ткани (r = 0,59, р = 0,001). Показатель суммарной дозы НПВС также положительно коррелировал с содержанием жировой ткани (r=0,42, p=0,03), что свидетельствует о негативном влиянии долговременной терапии симптоматическими средствами на риск формирования ожирения при РА. Показа-тель суммарной дозы НПВС негативно коррелировал с содержанием мышечной ткани, что может свидетельствовать о роли этой группы средств в развитии гипотрофии при РА. Нами также установлено негативное влияние системного воспаления, оцененного по индексу DAS28 и сывороточной концентрации СРБ, на содержание мышечной ткани. В группе пациентов принимавших базисную терапию метотрексатом от-мечены выраженные метаболические изменения и снижение значений гемоглобина, общего белка, альбумина, СКФ при лечении более 5 лет. Пациенты, получающие в качестве базисной терапии лефлюномид отмечено наилучшие значения показателей метаболического и нутритивного статуса, наименьшее количество побочных явлений. Обследованные больные, имеющие наиболее высокую активность процесса, не купируемую приемом стандартных базисных препаратов даже при комбинированном лечении, согласно современным рекомендациям переводились на базисную терапию инфликсимабом (ИМ). В этой группе больных при рассмотрении лабораторных показателей в зависимости от длительности терапии ИМ, уже через 2 года его применения достоверно нормализовались значения трансаминаз (АЛТ, АСТ), гемоглобина и альбумина. Традиционные показатели активности РА – СОЭ, СРБ и РФ так же достоверно снижались, а показатели общего холестерина, общего белка и СКФ достоверно не изменялись. В группе получающих ритуксимаб (РМ) достоверные изменения с нормализацией значений биохимических показателей и параметров нутритивного статуса определялись уже в первые 2 года терапии. У пациентов последних двух групп определена наименьшая суммарная доза ГКС. Пациенты, получающие комбинированную терапию базисными препаратами в сочетании с ГКС имели наименее выраженные метаболические и нутритивные нарушения в случаях применения схем лечения с кратковременными назначениями ГКС внутривенно по 120-300 мг, 3-5 дней подряд в периоды обострения (1 раз в 4-6 месяцев). Наибольшая суммарная доза ГКС зарегистрирована у пациентов, принимающих постоянно низкие дозы ГКС перорально. В этой группе определен самый высокий уровень тревожности и депрессии, наиболее выраженные признаки нарушения нутритивного статуса, наиболее высокие риски развития остеопороза и перелома шейки бедра. Таким образом, в реальной клинической практике у пациентов, получающих с целью коррекции выраженной активности процесса при РА длительно перорально ГКС определены наиболее выраженные нарушения метаболических и нутритивных показателей. В то же время адекватная коррекция активности процесса с применением генноинженерных препаратов значительно уменьшает потребность в применении ГКС и снижает риски метаболических повреждений. Дятчина Л.И., Ханов А.Г.СЛУЧАЙ РАЗВИТИЯ АНКИЛОЗИРУЮЩЕГО СПОНДИЛОАРТРИТА НА ФОНЕ ХРОНИЧЕСКОЙ АКТИВНОЙ ВЭБ-ИНФЕКЦИИ С ГЕМОФАГОЦИТАРНЫМ СИНДРОМОМ (КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ)
ГБОУ ВПО «Ростовский государственный медицинский университет» МЗ РФ, ГБУ РО «Областная клиническая больница №2» г. Ростов-на-Дону, Россия Под нашим наблюдением 3 года находится больная З., 29 лет, которая впервые госпитализирована в ревматологическое отделение по поводу арт-ралгий. Во время обследования обнаружена лейкопения. Состояние расце-нено как лекарственное поражение крови и подробно описано в статье по адресу http://visualrheumatology.ru/sluchaygematologicheskih-oslozhneniy.html . Лейкопения предположительно была связана с длительным в течение 1 года приемом Гриппферона (интерферона альфа-2 b) с целью профилактики ОРВИ. Поводом повторной госпитализации в феврале 2013 года послужили жалобы на слабость, повышенную утомляемость, длительный субфебрили-тет, артралгии, дорсалгии в пояснично-кресцовом отделе, головные боли, учащенное сердцебиение, нарушения сна, эмоциональную лабильность. Из анамнеза известно, что 2 года назад больная обследовалась в ревматологическом отделении с вышеуказанными жалобами и выписана с диагнозом: Реактивная артропатия, а/ф, I ст. активности, ФК I, лейкопения лекарственного генеза. Осенью 2012 г после тяжелой ангины, сопровождавшейся сильной лихорадкой, интоксикацией, возникла лимфоаденопатия, вновь появились артралгии и боли внизу спины. При поступлении: Т-37,80,больная астенической конституции, кожные покровы бледные, отмечалось увеличение лимфоузлов (подчелюстные, шей-ные, подмышечные) до 1-2 см, которые были плотноэластической консистенции, умеренно болезненные, не спаяны с окружающими тканями, гиперемия зева, явления фарингита, миндалины увеличены, рыхлые, умеренно гиперемированы. Сетчатое ливедо, арахнодактилия пальцев рук, нарушение конфигурации лучезапясных суставов, hallux valgus стоп. Положительные симптомы сакроилеита. Тоны сердца ритмичные, короткий систолический шум над верхушкой, ЧСС — 92 в минуту, АД — 80/50 мм рт. ст. По данным УЗИ органов брюшной полости, незначительное увеличение размеров печени и – в несколько большей степени – селезенки. При рентгенологическом ис-следовании илеосакральных сочленений выявлены рентгенологические при-знаки двухстороннего сакроилеита. При рентгенологическом исследовании кистей и стоп признаки реактивного артрита. Из лабораторных анализов обращали на себя внимание изменения лейкоцитарной формулы в виде лимфоцитоза – 45,эозинофилии -5, моноцитоза с большим количеством атипичных мононуклеаров, ускорение СОЭ. количество лейкоцитов -4,99х109.В биохимических анализах крови отмечалось умеренное повышение трансаминаз, КФК. LE – клетки найдены. Типирование антигенов HLA: установлен фенотип HLA-A 24, В 44, 27. Антиген В 27 обнаружен. ЭКГ: ритм синусовый, снижение вольтажа в стандартных отведениях, диффузные изменения миокарда. По данным УЗИ сердца – пролапс митрального клапана 1 степени без нарушения гемодинамики. Выявлены существен-ные нарушения иммунного статуса — повышено содержание иммуноглобулина М (IgМ) и снижено иммуноглобулинов А и G (IgА и IgG), наблюдалось преобладание продукции низкоавидных, то есть функционально неполно-ценных антител, дисфункция Т-звена иммунитета, повышение уровня сывороточного ИФН, снижение способности к продукции ИФН в ответ на многие стимулы. В крови были повышены титры IgG-антител к ранним и поздним вирусным антигенам (VCA, EA, EBV). При вирусологическом исследовании (в динамике) методом полимеразной цепной реакции (ПЦР) в лейкоцитах периферической крови была обнаружена ДНК ВЭБ. Больной были выставлены следующие диагнозы: Анкилозирующий спондилоартрит (болезнь Бехтерева), с явлениями двустороннего сакроилеита, активная фаза, 1 степень активности, 2 рентгенологическая ста-дия, ФК 1 с внесуставными проявлениями (гематологические нарушения). Соп. Хроническая активная ВЭБ-инфекция, умеренная гепатоспленомегалия, соматогенно обусловленная персистирующая депрессия; вирус, ассоциированный гемофагоцитарный синдром. Иммунодефицитное состояние; хронический фарингит. Учитывая наличие в анамнезе реакции на введение Гриппферона, препараты интерферона-альфа не вводились, от ГКС больная категорически отказалась. Было проведено лечение; детоксикационное, метаболическая терапия, назначена «базисная» терапия (сульфасалазин), НПВП, иммунокорригирующая терапия. После проведенного лечения у больной нормализовалась температура, уменьшились артралгии, дорсалгии, слабость, потливость, улучшились пока-затели иммунного статуса. При повторном исследовании через 1 месяц в слюне и лимфоцитах ВЭБ не определялся, хотя сохранялся умеренный лим-фо- и моноцитоз, а также иммунная дисфункция. Таким образом, развитие АС было спровоцировано острой ВЭБ-инфекцией, которая приняла хроническое течение и осложнилась развитием гемофагоцитарного синдрома. Полный текст обсуждения клинического слу-чая с комментариями по адресу: http://visualrheumatology.ru/sluchay-razvitiya-ankiloziruyushhego-spondiloartrita-na-fone-hronicheskoy-aktivnoy-veb-infektsii-s-gemofagotsitarnyim-sindromom-klinicheskoe-nablyudenie.html Евдокимова Е.В., Григорьянц С.Р., Зборовский А.Б., Мозговая Е.Э., Мартемьянов В.Ф.АКТИВНОСТЬ ЭНЗИМОВ ПУРИНОВЫХ МЕТАБОЛИТОВ В ПЛАЗМЕ КРОВИ БОЛЬНЫХ УРОГЕННЫМ РЕАКТИВНЫМ АРТРИТОМ И ПОДАГРОЙ
ФГБУ «НИИ КиЭР» РАМН, г. Волгоград Цель исследования. Выявить особенности активности гуаниндезаминазы (ГДА), гуанозиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфосфорилазы (ГФ) в плазме крови больных урогенным реактивным артритом (ур.РеА) и подагрой для улучшения дифференциации этих заболеваний. Материалы и методы. Под наблюдением в условиях стационара нахо-дились 30 больных ур.РеА (триггерная инфекция – Сhlamidya Trachomatis) и 42 больных подагрой с наличием артрита. В группу больных ур.РеА вошли 22 мужчины и 8 женщин. Средний возраст больных 27,0±0,96 лет. Группу больных подагрой составили 39 мужчин и 3 женщины. Средний возраст больных 53,1±2,2 года. У 15 больных отмечалась интермиттирующая форма подагры, у 27 больных – хроническая. В плазме крови больных и 30 здоро-вых лиц по оригинальным методикам определялась активность ГДА, ГЗДА, ПНФ и ГФ. Результаты исследования. По сравнению со здоровыми, у больных ур.РеА в плазме крови выше активность ГДА, ПНФ (все р<0,001), ниже ГЗДА (р<0,01); у больных с интермиттирующей формой подагры статистически значимых энзимных различий не определялось (р<0,05); у больных с хрони-ческой формой подагры выше активность ГДА, ПНФ, ГФ и ниже ГЗДА (все р<0,001); у больных подагрой (всей группы) выше активность ГДА, ПНФ, ГФ и ниже ГЗДА (все р<0,001). Сравнительный анализ показал, что у больных ур.РеА, по сравнению с больными с интермиттирующей формой подагры в плазме выше активность ПНФ (р<0,001), незначительно выше ГЗДА, ГФ и ниже ГДА (все р>0,05); по сравнению с больными с хронической формой подагры – ниже активность ГДА, ГФ (все р<0,001), выше ГЗДА (р<0,001), незначительно ниже ПНФ (р>0,05); по сравнению со всей группой больных подагрой – ниже активность ГДА, ГФ, выше ГЗДА (все р<0,001) и нет разли-чий по активности ПНФ (р>0,05). Заключение. Определение активности ГДА, ГЗДА, ПНФ и ГФ в плазме крови больных урогенным РеА и подагрическим артритом в комплексе с кли-ническими данными способствует дифференциации этих заболеваний. Евдокимова Е.В., Пересыпкин М.В., Пересыпкин В.В., Бедина С.А., Стажаров М.Ю.ЭНЗИМНЫЕ РАЗЛИЧИЯ В ЭРИТРОЦИТАХ И ПЛАЗМЕ БОЛЬНЫХ УРОГЕННОЙ И ЭНТЕРОГЕННОЙ ФОРМАМИ РЕАКТИВНОГО АРТРИТА
ФГБУ «НИИ КиЭР» РАМН, ГУЗ ВОКЦ восстановительной медицины и реабили-тации №2, г.Волгоград Цель: выявить особенности активности гуаниндезаминазы (ГДА), гуано-зиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфос-форилазы (ГФ) в эритроцитах и плазме больных урогенным и энтерогенным реактивным артритом (РеА). Материал и методы. Под наблюдением в условиях стационара находи-лись 54 больных РеА. Из которых у 24 определялся энтерогенный РеА (триггерная инфекция – энтеробактерии – Yersinia enterocolitica) и у 30 больных – урогенный РеА (триггерная инфекция – Chlamydia trachomatis). В группу сурогенным РеА (ур.РеА) вошли 8 (26,7%) женщин и 22 (73,3%) мужчины. Средний возраст больных – 27,0±0,96 лет, длительность болезни – 9,3±1,3 месяца. Энторенный РеА (энтер.РеА) составили 14 (58,3%) мужчин и 10 (41,7%) женщин. Возраст больных – 38,1±1,1 лет, длительность болезни – 9,3±1,2 месяца. В лизатах эритроцитов и плазме крови определялись по оригинальным методикам активности ГДА, ГЗДА, ПНФ и ГФ. Определение триггерных инфекций из различных источников проводилось с использова-нием иммуноферментного анализа и реакций непрямой гемагглютинации. Результаты. По сравнению со здоровыми у больных с ур.РеА в плазме выше активность ГДА, ПНФ (все р<0,001), ниже ГЗДА (р<0,01), в эритроци-тах выше активность ГДА (р<0,05) и ниже ГЗДА (р<0,001); у больных энтер.РеА в плазме выше активность ГДА, ПНФ (все р<0,001), ниже ГЗДА (р<0,01) и ГФ (р<0,001), в эритроцитах выше активность ГДА (р<0,01), ПНФ (р<0,05), ниже ГЗДА (р<0,001) и ГФ (р<0,01). Сравнительный анализ пока-зал, что у больных ур.РеА по сравнению с больными энтер. РеА в плазме статистически значимых энзимных различий не выявлено (р>0,05), но в эритроцитах выше активность ГФ (р<0,05), ниже ГДА (р<0,05%) и ПНФ (р<0,01). Заключение. Отсутствие энзимных различий в плазме крови больных ур.РеА и энтер.РеА, вероятно, связано с общностью патогенетических меха-низмов обеих форм РеА, но наличие энзимных различий в лизатах эритроци-тов свидетельствует о том, что все-таки в отдельных звеньях патогенеза имеются и некоторые отличия, что может быть обусловлено этиологическими факторами в развитии ур.РеА и энтер.РеА. Елисеева Л.Н., Резникова Л.Б., Тихомирова Н.Ю., Мастерицин Н.К., Просёлков Ю.Е.ПЕРВИЧНЫЙ СКРИНИНГ СЫВОРОТОЧНОЙ КОНЦЕНТРАЦИИ ВИТАМИНА Д В ПОПУЛЯЦИИ КРАСНОДАРСКОГО КРАЯ
ГБОУ ВПО КубГМУ Минздрава России, Краснодар, Россия; Медицинский центр Гармония, Краснодар, Россия; Краевая клиническая больница №1 им С.В.Очаповского, Краснодар, Россия В последние годы в ревматологической литературе широко обсуждается вопрос о значении и влиянии витамина Д на состояние здоровья населения всех стран, особенности течения ревматологических заболеваний. Наряду с традиционной значимостью витамина Д, как фактора риска развития рахита, остеопороза, мышечной активности, появляются новые данные о значимости витамина Д в нормальном функционировании многих органов и систем и ин-дуцировании некоторых заболеваний. Среди витамин Д зависимых болезней отмечаются артериальная гипертензия, инфаркт, сахарный диабет 1 и 2 типов, ожирение, аутоиммунные заболевания, злокачественные опухоли, нарушение репродуктивной функции у женщин, психиатрические заболевания (деменция, депрессии) и другие. Отмечается положительная корреляция между низким уровнем витамина D и смертностью от сердечно-сосудистых заболеваний. Наряду с паратиреоидным гормоном, витамин Д является важнейшим регулятором обмена кальция и фосфатов в организме, обеспечивающим нормальный рост и минерализацию костей и дентина зубов. Считается, что недостаточность витамина D – очень распространенное состояние во всех возрастных группах. По современным оценкам, эта проблема затрагивает более половины населения Земли. Своевременное выявление недостаточности или передозировки витамина D позволяет вовремя скорректировать его уровень и избежать развития серьезных осложнений. Результатом этого является, в частности, тот факт, что число назначений данного анализа в европейских странах в последние годы резко возрастает. Учитывая значимость дефицита витамина Д в популяции, целью нашего исследования стало изучение частоты и выраженности дефицита витамина Д среди пациентов, обратившихся в медицинский центр по различным поводам в период декабрь 2012 – апрель 2013г. Материалы и методы. Сывороточная концентрация витамина Д (25(OH)D) определена у 38 пациентов, обратившихся в медицинский центр Гармония г. Краснодара по поводу различных заболеваний. Все пациенты не имели заболеваний щитовидной и паращитовидных желез. Средний возраст обследованных составил 58,5±6,9 лет (от 38 до 77 лет). Основная причина обращений – заключалась в дегенеративных заболеваниях опоронодвигательного аппарата. Гиповитаминоз D определяли как уровень 25(OH)D в сыворотке <30 нг/мл. Результаты обследования. При анализе сывороточной концентрации 25(OH)D установлены значительные колебания 9,0-47,0 мкг/л, при этом средняя концентрация составила 22,63 мкг/л (норма 25-80). Среди всех об-следованных концентрация 25(OH)D выше 30 мкг/л (пороговое значение, рекомендуемое для достижения максимальной кишечной абсорбции кальция и предупреждения вторичного гиперпаратиреоза) установлено только у 7 человек (18,42%), при этом среднее значение составило 35,33 мкг/л, а средний возраст этой группы – 55,83±3,8 лет. Пациенты, значения витамина Д у которых было ниже 30мкг/л, но выше 20мкг/л составили 44,74% (17 человек). Средний возраст этой группы был практически таким же (56,63±4,6 лет), но уровень витамина Д был достоверно ниже в 1,5 раз (23,95 мкг/л). У 36,84% пациентов (14 человек), 15,5 мкг/л, но это в основном были пациенты более старшего возраста (61,64±2,7 лет). В обследованной популяции было только 7 пациентов в возрасте моложе 50 лет (43,6±3,8 лет) значения вит Д 29,43 мкг/л. Интересно, что среди обследованных было двое мужчин 75 и 64 лет и значения вит Д у них были 18 и 16 мкг/л соответственно. Данные международного эпидемиологического исследования свидетельствуют о высокой распространенности гиповитаминоза D среди женщин с постменопаузальным остеопорозом в мире, даже в регионах с достаточным количеством солнечного света. Выводы. Проведенное нами исследование содержания витамина Д (по 25(OH)D) среди пациентов, обратившихся в медицинский центр по различным причинам и не имеющих нарушений функции щитовидной, паращитовидной желез, не принимавших глюкокортикостероиды, отмечено низкое содержание витамина Д у 81,6% обследованных. Краснодарский край относится к региону с повышенной инсоляцией, достаточно высоким уровнем жизни, несмотря на это, низкий уровень витамина Д в крови может быть причиной прогрессирования некоторых заболеваний (включая онкологические и гипертоническиую болезнь). Учитывая полученные нами данные, следует повысить значимость дополнительных лабораторных исследований, включающих определение концентрации витамина Д. Жукова Е.В., Меньшикова Т.Б., Кайсинова А.С.РАДОНОВЫЕ ВАННЫ РАЗЛИЧНОЙ КОНЦЕНТРАЦИИ В ЛЕЧЕНИИ ОСТЕОАРТРОЗА У ЖЕНЩИН С МЕТАБОЛИЧЕСКИМИ НАРУШЕНИЯМИ
ФГБУ ПГНИИК ФМБА России, г.Пятигорск, Россия. Актуальность проблемы. Остеоартроз – прогрессирующее заболевание суставов, в основе которого лежат дегенерация суставного хряща, развитие остеофитов, изменение субхондральной кости на фоне скрыто или явно протекающего синовита. Преимущественно остеоартрозом страдают женщины 4:1 и 7:1 при локализации процесса в тазобедренном суставе. Ведущими факторами риска развития и прогрессирования остеоартроза являются возраст зависимые состояния – дисгормональные нарушения, дислипидемия, избыточная масса тела, генетическая предрасположенность. О роли гормональных сдвигов в патогенезе остеоартроза свидетельству-ет его высокая распространенность среди женщин и пик манифестации в климактерическом периоде. Эстрогены оказывают значительное хондропротективное влияние на хрящевую ткань (синтез хондроцитов и компонентов хрящевого матрикса), контролируют содержание общего холестерина и холестерина низкой плотности в сыворотке крови, стабилизируют концентрацию холестерина высокой плотности. Нарушение липидного обмена способствует поражению интимы сосудов и снижению кровоснабжения сустава за счет нарушения микроциркуляции. Нарушения гормонального и липидного обменов играют важную роль в увеличении массы тела, избыточной нагрузке на суставную поверхность и прогрессированию процесса. В связи с чем, лечение больных остеоартрозом предполагает не только медикаментозную терапию, а комплекс мероприятий с включением природных физических факторов. Цель. Научное обоснование дифференцированного применения радоновых ванн различной концентрации для профилактики и лечения остеоартроза у женщин в период менопаузы. Материалы и методы. Наблюдались 90 женщин с наиболее частой локализацией остеоартроза (коленные и тазобедренные суставы), I-III -рентгенологической стадией, функциональной недостаточностью 1-2 степе-ни. Больным назначались радоновые ванны высокой (180 нКи/л), средней (40 нКи/л) и низкой (20 нКи/л) концентрации по стандартной методике. Результаты и обсуждение. В наших исследованиях у женщин в менопаузе при применении радоновых ванн низкой и средней концентрации отмечалось повышение уровня эстрадиола в рамках возрастных нормативных показателей, стабилизировались процессы естественного угасания функции яичников. Радоновые ванны высокой концентрации снижали уровень эстрадиола в рамках нормативных показателей, что может быть использовано при лечении остеоартроза при сопутствующей гинекологической патологии. В изучаемой группе выявлено повышение уровня холестерина сыворотки крови в 50% наблюдений. Отмечена также зависимость уровня гиперхолестеринемии от состояния репродуктивной фазы, так при менопаузе повышение холестерина и его атерогенных фракций выявлено у 90% женщин, в то время как в репродуктивном периоде лишь у 28%. После курсового лечения ваннами низкой и средней концентрации нами получена положительная достоверная динамика показателей липидного обмена по параметрам – общий холестерин, триглицериды, холестерин низкой плотности, холестерин высокой плотности. Радоновые ванны высокой концентрации, по данным показа-телям достоверной динамики не показали. Можно полагать, что радон высокой концентрации угнетает процессы метаболизма холестерина и всех его фракций, в том числе фракций принимающих участие в стероидогенезе. Избыточная масса тела была отмечена у половины пациентов и обусловлена как нарушением гормонального и липидного обмена, так и снижением уровня двигательных нагрузок из-за болевого синдрома в крупных суставах. Динамика массы тела была положительной и достоверной после курса радо-новых ванн низкой концентрации. Так снижение массы тела отмечалось на 7% от исходной на фоне радоновых ванн 20 нКи/л и сохранялась стабильной после курса ванн высокой концентрации (180 нКи/л). Выводы. Остеоартроз у женщин сопровождается существенными эндокринно-обменными нарушениями, а именно дисбалансом половых гормонов, атерогенными сдвигами липидного спектра и ожирением. Наши исследования показали возможность воздействия на некоторые факторы развития и прогрессирования заболевания путем коррекции уровня половых гормонов, липидного обмена, массы тела. Радоновые ванны низкой концентрации обладают стимулирующим действием: улучшают липидный обмен, уменьшают массу тела, повышают уровень эстрадиола в рамках нормативных показателей для данной возрастной категории. Радоновые ванны высокой концентрации, обладая супрессивным действием, подавляют выработку эстрадиола в том числе при его патологических уровнях. Эффект радоновых ванн сред-ней концентрации при преимущественных аналгетических и трофических проявлениях не показал значительных колебаний гормонального и липидного обмена в изучаемой группе пациенток. Данное исследование позволяет рассматривать дифференцированную методику альфа терапии при различ-ном уровне поглощенной дозы излучения с позиций не только болезнь модифицирующего действия, но и профилактического направления. Журавлева М.О.ОЦЕНКА ОТДАЛЕННЫХ ИСХОДОВ РЕАКТИВНОГО АРТРИТА
ГБОУ ВПО «Оренбургская государственная медицинская академия» Мин-здрава России, г.Оренбург, Россия. Реактивный артрит это иммуновоспалительное заболевание суставов, обусловленное очагом инфекции в кишечнике или урогенитальном тракте, имеющее характерную клиническую картину с поражением периферических суставов, позвоночного столба и нередко принимающее хроническое течение, среди ревматических заболеваний занимает одно из ведущих мест по распространенности. Дебют заболевания приходится, как правило, на воз-раст 20—40 лет. Реактивный артрит (РеА) на сегодняшний день приобретает все большие масштабы вследствие неуклонного роста числа страдающих им людей. Заболевание представляет серьезную социально-экономическую проблему в связи с широкой распространенностью, тяжелым течением, длительной нетрудоспособностью, применением дорогостоящей терапии. Поэтому оценка отдаленных исходов данного заболевания представляет несомненный интерес. Цель исследования – оценить отдаленные исходы РеА. Материал и Методы – проанкетировано 50 человек, получавших лечение во второй взрослой поликлинике ММУЗ ГКБ имени Н.И. Пирогова г. Оренбурга с диагнозом РеА 10 – 12 лет назад. Было 19 мужчин и 31 женщина, средний возраст которых составил 48,34 ± 3,47 лет. Опрос проводили через 10 – 12 лет после амбулаторного комплексного лечения, включающего кор-рекцию иммунного статуса, антибактериальную терапию, НПВС. Полученные результаты: За истекший период времени 40 человек (80%) не обращались к ревматологу. Состояние своего здоровья в настоящий момент по визуально аналоговой шкале (ВАШ) проанкетированные оценивали на 3,14±0,58 см. Полное выздоровление отмечали 14% (7 человек), существенное улучшение – 56% (28 человек), без перемены состояния – 30% (15 человек), что отражено на рисунке №1. Не наблюдали улучшения состояния суставов те, у кого за последнее десятилетие развился остеоартроз или аутоиммунные ревматические заболевания.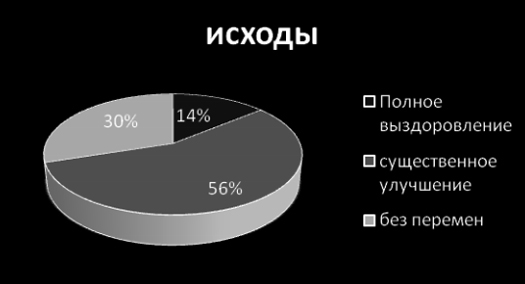 Рисунок 1. Отдаленные исходы РеА.
Обострения отсутствовали в последние годы у 20% опрошенных. У 72% не было припухлости в области суставов (36 человек) за последнее десятилетие, у 22% она периодически возникала. В 6% случаев припухлость суставов нижней конечности появилась вновь в последний год. Вероятно, повторно развился РеА, вследствие нового заражения. Гиперемии и гипертермии в области суставов не отмечали 88%. Утренней скованности не было у 43 человек (86%). У 6 опрошенных (12%) имелась утренняя скованность продолжительностью до полудня, у 1 (2%) – в течение всего дня. Она наблюдалась у больных ревматоидным артритом и анкилозирующим спондилоартритом. 94% (47 человек) отмечали болезненность в опорно-двигательном аппарате. Боли в пятках были у 32% анкетированных, вследствие наличия пяточных шпор. В суставах боли имелись у 55% (26 человек), которые почти у всех были связаны с физической нагрузкой (24 человека). Болезненность в позвоночнике была у 9%, сочетание болей в суставах и позвоночнике – у 36%. Преобладали коленные (32 случая) и голеностопные (13 случаев) суставы, затем следовали дистальные (8 случаев) и проксимальные (8 случаев) межфаланговые, тазобедренные (5 случаев), локтевые (5 случаев), остальные поражались в единичных случаях. Отмечался незначительный болевой симптом (3,47±0,78 по ВАШ), который, по-видимому, связан с развитием остеоартроза и аутоиммунных заболеваний. У 6 человек был диагностирован ревматоидный артрит (12%), у 1 – анкилозирующий спондилоартрит (2%), у 11 – остеоартроз (22%), у 16 – остеохондроз (34%), что отражено на рисунке №2.
Рисунок 1. Отдаленные исходы РеА.
Обострения отсутствовали в последние годы у 20% опрошенных. У 72% не было припухлости в области суставов (36 человек) за последнее десятилетие, у 22% она периодически возникала. В 6% случаев припухлость суставов нижней конечности появилась вновь в последний год. Вероятно, повторно развился РеА, вследствие нового заражения. Гиперемии и гипертермии в области суставов не отмечали 88%. Утренней скованности не было у 43 человек (86%). У 6 опрошенных (12%) имелась утренняя скованность продолжительностью до полудня, у 1 (2%) – в течение всего дня. Она наблюдалась у больных ревматоидным артритом и анкилозирующим спондилоартритом. 94% (47 человек) отмечали болезненность в опорно-двигательном аппарате. Боли в пятках были у 32% анкетированных, вследствие наличия пяточных шпор. В суставах боли имелись у 55% (26 человек), которые почти у всех были связаны с физической нагрузкой (24 человека). Болезненность в позвоночнике была у 9%, сочетание болей в суставах и позвоночнике – у 36%. Преобладали коленные (32 случая) и голеностопные (13 случаев) суставы, затем следовали дистальные (8 случаев) и проксимальные (8 случаев) межфаланговые, тазобедренные (5 случаев), локтевые (5 случаев), остальные поражались в единичных случаях. Отмечался незначительный болевой симптом (3,47±0,78 по ВАШ), который, по-видимому, связан с развитием остеоартроза и аутоиммунных заболеваний. У 6 человек был диагностирован ревматоидный артрит (12%), у 1 – анкилозирующий спондилоартрит (2%), у 11 – остеоартроз (22%), у 16 – остеохондроз (34%), что отражено на рисунке №2.
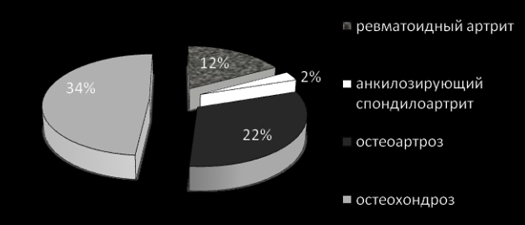 Рисунок 2. Ревматические заболевания у больных, перенесших РеА.
Болезненность в мышцах и сухожилиях наблюдали 30% опрошенных. Деформации суставов, в основном за счет узелков Гебердена и Бушара, были у 11 человек. Сопутствующие заболевания отмечали 28 анкетированных (56%). Поражения сердечно-сосудистой системы имелись у 21 пациента (42%), болезни мочеполовой системы – у 16 (32%), из них пиелонефрит – у 10, цистит – у 5, простатит – у 1. В течение 10 лет лечение и диспансерное наблюдение получали всего 32% (16 человек), в основном по поводу сопутствующей патологии. Полностью трудоспособными себя считали 44%, снижение трудоспособности отмечали 56%. Инвалидности по ревматическим заболеваниям ни у кого не было.
Вывод: Таким образом, в течение 10 лет после амбулаторного лечения РеА сохраняется хороший терапевтический эффект. Полностью здоровыми считают себя 14%, более половины отмечают значительное улучшение состояния в течение длительного времени и отсутствие болей. Однако у 7 человек появились аутоиммунные ревматические заболевания.
Зборовская И.А., Евдокимова Е.В., Бедина С.А., Мартемьянов В.Ф., Стажаров М.Ю.
Рисунок 2. Ревматические заболевания у больных, перенесших РеА.
Болезненность в мышцах и сухожилиях наблюдали 30% опрошенных. Деформации суставов, в основном за счет узелков Гебердена и Бушара, были у 11 человек. Сопутствующие заболевания отмечали 28 анкетированных (56%). Поражения сердечно-сосудистой системы имелись у 21 пациента (42%), болезни мочеполовой системы – у 16 (32%), из них пиелонефрит – у 10, цистит – у 5, простатит – у 1. В течение 10 лет лечение и диспансерное наблюдение получали всего 32% (16 человек), в основном по поводу сопутствующей патологии. Полностью трудоспособными себя считали 44%, снижение трудоспособности отмечали 56%. Инвалидности по ревматическим заболеваниям ни у кого не было.
Вывод: Таким образом, в течение 10 лет после амбулаторного лечения РеА сохраняется хороший терапевтический эффект. Полностью здоровыми считают себя 14%, более половины отмечают значительное улучшение состояния в течение длительного времени и отсутствие болей. Однако у 7 человек появились аутоиммунные ревматические заболевания.
Зборовская И.А., Евдокимова Е.В., Бедина С.А., Мартемьянов В.Ф., Стажаров М.Ю.
К ИССЛЕДОВАНИЮ АКТИВНОСТИ ЭНЗИМОВ ГУАНИЛОВЫХ ПРОИЗВОДНЫХ У БОЛЬНЫХ РЕАКТИВНЫМ АРТРИТОМ С РАЗЛИЧНЫМ ХАРАКТЕРОМ ТЕЧЕНИЯ ЗАБОЛЕВАНИЯ
ФГБУ «НИИ КиЭР» РАМН, г. Волгоград Цель исследования. Выявить особенности активности гуаниндезамина-зы (ГДА), гуанозиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфосфорилазы (ГФ) в плазме, лизатах лимфоцитов и эритроцитов крови больных реактивным артритом (РеА) в зависимости от характера тече-ния болезни. Материалы и методы. Под наблюдением находились 54 больных РеА, из которых 36 мужчин и 18 женщин. Средний возраст больных 31,9±1,0 год, длительность болезни – 9,39±0,85 месяцев. Острое течение определялось у 20 больных, затяжное – у 19 и хроническое – у 15 больных. У всех больных РеА и 30 здоровых людей в плазме крови, лизатах лимфоцитов и эритроци-тов по оригинальным методикам определялась активность ГДА, ГЗДА, ПНФ и ГФ. Результаты исследования. По сравнению со здоровыми, у больных с острым течением в плазме выше активность ГДА, ПНФ, ниже ГЗДА и ГФ (все р<0,001), в лимфоцитах выше активность ГДА (р<0,001), ПНФ (р<0,05); ниже ГЗДА (р<0,001) и ГФ (р<0,05), в эритроцитах выше активность ГДА и ниже ГЗДА (все р<0,001); у больных с хроническим течением в плазме выше активность ПНФ (р<0,05), в лимфоцитах выше активность ГДА (р<0,01), ПНФ (р<0,001), выше ГЗДА и ГФ (р<0,001), в эритроцитах выше активность ГДА и ниже ГЗДА (р<0,05). Сравнительные исследования показали, что у больных с острым течением, по сравнению с затяжным течением, в плазме выше активность ГДА, ПНФ (все р<0,001), ниже ГЗДА (р<0,01), в лимфоцитах выше активность ПНФ (р<0,05) и ниже ГФ (р<0,05), в эритроцитах выше активность ПНФ (р<0,01). Заключение. Определение активности ГДА, ГЗДА, ПНФ и ГФ в лизатах лимфоцитов, эритроцитов и плазме крови РеА способствует уточнению вари-анта течения и, соответственно, назначению адекватной терапии. Зборовский А.Б., Емельянова О.И., Гонтарь И.П., Красильников А.Н.КЛИНИКО-ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ ИССЛЕДОВАНИЯ АКТИВНОСТИ, КОЛИЧЕСТВА И АНТИТЕЛ К ЦЕРУЛОПЛАЗМИНУ В СЫВОРОТКЕ БОЛЬНЫХ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКИ
ФГБУ НИИ КиЭР РАМН; кафедра госпитальной терапии ВолгГМУ Теоретическим обоснованием участия свободных радикалов в патогенезе системной красной волчанки (СКВ) является способность повреждать белки, липиды, ДНК, придавая им свойства аутоантигенов и провоцируя выработку аутоантител. Церулоплазмин (ЦП) является одним из основных внеклеточных ферментов – антитоксидантов, диагностическое значение которого при СКВ до настоящего времени четко не определено. Данные о содержании и активности ЦП в крови больных СКВ весьма противоречивы, что связано с различными подходами к отбору больных и разными методиками определения. Учитывая гиперпродукцию активных форм кислорода (АФК) при СКВ можно ожидать компенсаторное увеличение синтеза антиоксидантов, в том числе и ЦП, что должно приводить к ингибированию свободных радикалов. Однако при СКВ отмечено накопление вторичных токсичных продуктов свободно-радикальных реакций, таким образом, имеется дисбаланс между продукцией и утилизацией АФК. Причины подобного дисбаланса до сих пор не ясны. Одной из причин функциональной недостаточности энзимов, в том числе ферментов-антиоксидантов, считают образование антител (АТ) к ним. Цель: усовершенствование иммунологической диагностики СКВ путем определения АТ к ЦП, а также количества его и ферментативной активности. Материалы и методы исследования. Исследовалась сыворотка 30 практически здоровых лиц (доноров Областной станции переливания крови), 68 – больных СКВ. Исследование проводилось в соответствии с принципами Хельсинкской декларации Международной медицинской ассоциации (1996г.). Соблюдение требований биоэтики подтверждено результатами экспертизы Регионального этического комитета. Обследованные нами больные являлись пациентами ревматологических отделений ГУЗ ГКБ № 25 г. Волго-града и ГУЗ ГБ № 1 г. Волжского. АТ к ЦП определяли иммуноферментным методом с использованием ИГАП. Полученные значения выражали в единицах оптической плотности (е.о.п.) и считали положительными при превышении величин экстинции, найденных для здоровых лиц, более чем на 2д. Определение количества ЦП проводили иммуноферментным методом по И.С. Кузьминой и сотр. (1991) с использованием коммерческого иммуноферментного диагностикума произ-водства НИИ вакцин и сывороток им. И.И. Мечникова РАМН (г. Москва) ФС 42-42ОВС –93 серия №12. Обработка данных проводилась с использованием программного пакета STATISTICA FOR WINDOWS. Результаты исследования. По данным ИФА средний уровень антител к ЦП в донорских сыворотках составил 0,020±0,006 е.о.п. Уровень нормальных показателей специфических антител, определяемый как М±2, включает значения экстинкции в интервале от 0 – 0,086. Среднее значение оксидазной активности и количества ЦП у здоровых лиц составило 716±26,3 и 921±32 нг/мл соответственно. Корреляционный анализ активности и количества ЦП с поражением органов и систем при СКВ позволил выявить достоверные связи между поражением легких, нервной системы, сосудов, наличи-ем инфекционных осложнений и количеством и удельной оксидазной активностью ЦП. Стационарное лечение привело к статистически значимому снижению оксидазной активности (p<0,0005) и количества ЦП (p<0,0005), изменения удельной оксидазной активности ЦП были незначимыми (p=0,160). Доля лиц, имевших антитела к ЦП, через 2 недели терапии уменьшилась недостоверно, однако уменьшение было значимым (p=0,031) к концу стационарного лечения. Также статистически значимо снизился уровень антител к ЦП Анализ влияния различных видов терапии на уровень антител к ЦП и по-казатели активности и количества ЦП был затруднен тем, что выбор режима лечения основывался на клинических показателях и, в первую очередь, на активности процесса, а, как уже было показано, исследуемые показатели имеют достаточно тесную корреляцию с активностью СКВ. Были выявлены различия в динамике уровня антител к ЦП в зависимости от вида терапии – в подгруппе, получавших наряду с кортикостероидами и иммуносупрессивными препаратами процедуры плазмафереза, снижение аутоантител было бо-лее выраженным по сравнению с больными, получавшей кортикостероиды (включая пульс-терапию глюкокортикоидами) и цитостатики, без последующих процедур плазмафереза. Снижение количества и оксидазной активности ЦП не зависело от вида проводимой терапии. Выводы: при СКВ отмечается повышение как ферментативной активности, так и количества ЦП, что может быть использовано как дополнительный критерий диагностики этих заболеваний и отражает напряженность системы антиоксидантной защиты при хронических иммунологических заболеваниях. В сыворотках крови значительной части больных СКВ методом ИФА с применением ИГАП выявляются АТ к ЦП. Уровень АТ к ЦП при СКВ коррелирует со степенью активности заболевания, что позволяет использовать его опреде-ление в качестве дополнительного критерия активности патологического процесса. Иванова К.В., Майко О.Ю.ОЦЕНКА ЭФФЕКТИВНОСТИ КОМБИНИРОВАННОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ЛОЗАПА И УРИСАНА ИЛИ АЛЛОПУРИНОЛА У БОЛЬНЫХ ПОДАГРОЙ
ГАУЗ ГКБ им. Пирогова взрослая поликлиника №3; ГБОУ ВПО «Оренбургская государственная медицинская академия» Минздрава России. Введение. Подагра системное тофусное заболевание, характеризующееся отложением кристаллов моноурата натрия в различных тканях и развивающимся в связи с этим воспалением у лиц с гиперурикемией (ГУЕ), обусловленное внешнесредовыми и / или генетическими факторами, протекающее с рецидивирующими приступами острого артрита, кристалл-индуцированными синовитами и образованием подагрических тофусов. Заболеваемость подагрой растет с каждым десятилетием, однако арсенал лекарственных средств, используемых для лечения больных невелик. Приверженность к лечению у больных подагрой крайне низка, из-за мнимого благополучия болезни, длительного светлого промежутка, необходимости соблюдения строгих диетических рекомендаций и нежелания длительного приема « химических» препаратов. Основным методом терапии хронической тофусной подагры и профилактики острых подагрических атак является применение антигиперурикемических препаратов (ингибиторы ксантинокси-дазы – аллопуринол и урикозурические средства). Повышенный уровень мочевой кислоты ассоциирован с сердечно-сосудистой заболеваемостью и может рассматриваться в качестве фактора риска артериальной гипертонии (АГ), что требует комбинации антигипертензивных и гипоурикемических средств у пациентов с подагрой при нали-чии у них АГ. Установлено,что наиболее выраженным влиянием на уровень артериального давления (АД) и мочевой кислоты (МК) обладает лозартан, который относится к группе блокаторов ангиотензиновых рецепторов, а именно блокады АТ1-рецепторов. В последние годы появилась возможность использовать растительный комплекс урисан, интерес к которому связан с его свойствами: ощелачивание мочи, увеличение почечной фильтрации, диуреза, выведение МК почка-ми, а также описан противоспалительный эффект. В связи с этим проблема повышения эффективности лечения подагры остается актуальной, поскольку до конца не ясно, когда начинать лечение при бестофусной подагре, и какой препарат лучше избрать при отсутствии гиперэкскреции уратов. Цель нашего исследования: Оценить в сравнительном аспекте эффек-тивность комбинированной терапии лозапа с урисаном или аллопуринолом у больных подагрой при наличии АГ. Материалы и методы. В исследование были включены 30 больных с достоверным диагнозом подагры, согласно критериям S.L.Wallace (1977), при наличии АГ (I-III степени). Возраст пациентов был от 41 до 79 лет (средний возраст 58,5 ±6,32 лет), из них 24 мужчин (80%) и 6 женщины (20%). У 3 больных (10%) имелись тофусы. Средняя продолжительность заболевания – 4,2±1,27 года. Число пораженных суставов на момент осмотра составило 3 (от 1 до 6). Преобладало рецидивирующее течение заболевания (78%), хроническое течение отмечалось у (22%) больных. Продолжительность АГ у больных составила 10,68±5,25 года, преобладала АГ II степени-43%, III стенени-35% и I степени-20%. При антропометрическом обследовании у 13 больных отмечалась избыточная масса тела (44%), ожирение I степени у 9 (30%), II степени у 5 (16%), III степени у 3 (10%). Всем пациентам проводилось общеклиническое обследование с оценкой антропометрических показателей. Выполнялось биохимическое исследование крови с определением липидного профиля общего холестерина (ХС), ХС ЛПВП, ХС ЛПНП, триглицеридов (ТГ), индекса атерогенности (ИА), мочевины, креатинина, мочевой кислоты (МК) крови и мочи. Критерии исключения из исследования: тяжелая тофусная подагра, вторичные артериальные гипертензии, сердечно-сосудистые события в анамнезе, аритмии, сахарный диабет, тяжелые сопутствующие заболевания желу-дочно-кишечного тракта, печени, почек, тяжелая сердечная недостаточность, онкологический анамнез. Всем пациентам была назначено комбинированное лечение с использованием препаратов лозап (ЗЕНТИВА, Чешская Республика) 50 мг в сутки и урисан (« ГРИНВУД» Индонезия) 550 мг по 2 капсулы 2 раза в день в течении 1 месяца. У 80% больных в связи с недостаточным снижением АД, доза лозапа была увеличена до 100 мг в сутки через 2 недели. Эффективность лечения оценивалась по уровню МК крови и мочи, показателям липидного профиля, а также степени снижения АД. Через 1 месяц от начала лечения у 7 человек (23%) не отмечалось снижение уровня МК. Этим пациентам был назначен аллопуринол в дозе от 100 до 300 мг (средн. 150 мг) в сутки в те-чении 6 месяцев, а остальные 77% продолжили прием только лозапа. Статическая обработка данных проводилась с помощью программы Statistica 6.0 (Statsoft, США) Использовались непараметрические методы описательной статистики, анализ по Вилкоксону, Манна-Уитни. Результаты представлены в виде средней арифметической (М) и стандартного отклоне-ния(SD). За статистически значимые принимались отличия при р<0,05. Результаты и обсуждение. До начала лечения у всех больных отмеча-лось повышение уровня МК крови, который колебался от 408 до 621 ммоль/л (средн. 528,42±61,22 ммоль/л). У 85% пациентов наблюдалась гиперхолестеринемия , средн. ХС- 6,28±0,93ммоль/л, ХС ЛПВП -1,28±0,47 ммоль/л, ХС ЛПНП- 3,75±1,06 ммоль/л, ИА- 3,69±1,68, уровень креатинина средн. 118,68±13,86 ммоль/л. Гуперурикозурия отмечалась у 25% больных колебалась от 2,51-6,98 мкмоль/л (средн.- 4,38±3,18 мкмоль/л). Через 1 месяц от начала комбинированной терапии отмечалась достовер-ная положительна динамика всех биохимических показателей крови, уровень МК составил средн. 409,47 ±62,31 ммоль/л, показатели липидного про-филя нормализовались. Так, уровень общего ХС составил 5, 25±1,08 ммоль/л, (р<0,01), ЛПНП – 3,21 ±0,68 ммоль/л (р<0,05), ТГ -1,32±0,36 ммоль/л, ИА- 3,24±0,89. Повышение ЛПВП не носило достоверный характер. Выделение МК с мочой на фоне терапии не изменилось по сравнению с ис-ходными значениями, что позволяет предположить преимущественно антигиперурикемический эффект препаратов по сравнению с урикозурическим. У 12 пациентов (40%) с изначально повышенным уровнем креатинина (120- 176 ммоль/л), отмечалось снижение этого показателя в среднем на 10%. У 8 человек (27%) показатели МК не достигли нормы, при этом показатели липидного профиля достоверно улучшились. В связи с этим им был назначен аллопуринол в течение 6 месяцев. Через 6 месяцев на фоне тера-пии отмечалась достоверная положительная динамика гиперурикемии. Уровень МК в крови нормализовался (средн. 326,14± 21,17 ммоль/л), уровень МК в моче (средн. 3,82±3,02 мкмоль/л). Все показатели липидного профиля сохранялись в пределах нормы. У пациентов принимающих только лозап, через 6 месяцев уровень МК средн.- 426,37±64,31 ммоль/л, уровень МК в моче, липидный профиль не имели доставерных изменений. Выводы: 1. Комбинированная терапия в течении 1 месяца с использованием лоза-па и урисана, была эффективна у большинства больных 77% с хронической бестофусной подагрой, только у ¼ больных потребовалось дополнительное назначение аллопуринола, что привело к нормализации урикоземии и урикозурии. 2. У пациентов принимающих только лозап через 6 месяцев наблюдалась отрицательная динамика показателей уровня МК в крови. Исаева Б.Г., Сапарбаева М.М., Исаева С.М.О ЗАБОЛЕВАЕМОСТИ И ТАКТИКЕ ВЕДЕНИЯ БОЛЬНЫХ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКОЙ В КАЗАХСТАНЕ
Казахский Национальный медицинский университет имени С.Д.Асфендиярова, Алматы, Казахстан Согласно Постановления Правительства Республики Казахстан №2018 (2009) системные поражения соединительной ткани (СПСТ), в том числе системная красная волчанка (СКВ) относятся к социально значимым заболе-ваниям и пациентам, страдающими данными заболеваниями, помощь ока-зывается в рамках Гарантированного объема бесплатной медицинской по-мощи. Одной из главных задач в тактике ведения больных данной катего-рии является разработка, внедрение международных стандартов, комплекс-ных программ диагностики и лечения. Цель исследования: изучение распространенности, динамики прироста заболеваемости, а также тактики ведения и лечения больных системной красной волчанкой в Казахстане. Материал и методы: проводился анализ официальных статистических материалов Министерства здравоохранения Республики Казахстан за пе-риод с 2006 по 2011 годы. Результаты. Анализ официальных статистических материалов подтвер-дил высокую социальную значимость СКВ в стране. В 2011 году было за-регистрировано 2568 больных СКВ, из них 2113 женщин, а в 2006 году – 1762 и 1377 соответственно. Отмечалась высокая динамика прироста заболеваемости СКВ за изучаемый период – 45,7%, особенно у женщин –53,4%. Число больных с впервые установленным диагнозом СКВ в 2011 году составило 361 человек, женщин – 289, в 2006 году – 237 и 173, что соответствовало динамике прироста в 52,3% и 61,8%. Преобладаю-щее большинство больных СКВ (82%) составили женщины , что соответ-ствует основным статистическим показателям по заболеваемости. Изучение показателей заболеваемости СКВ по возрастным группам выявило высокую динамику прироста за изучаемый период у девочек (15-17 лет) – 38,6% и у женщин репродуктивного возраста (53,4%). Распространенность СПСТ в 2011 году составила 42,8, в то время как СКВ- 15,6 случая на 100 тыс. населения. Уровень распространенности СКВ в Казахстане ниже, чем в дру-гих странах с превалирующим азиатским населением или в сравнении с ази-атскими группами населения, что, вероятно, связано с более низкой выяв-ляемостью заболевания. К примеру, согласно данным Jonson AE, Gordon C (1995) в Великобритании распространенность СКВ среди всех рас соста-вила 27,7, с превалирующим азиатским населением – 46,7, а в Японии, по данным Osio-Salido E. (2010), этот показатель равнялся 19,2 на 100 тыс. населения. Анализ показателей диспансеризации за 2011 год выявил низкий про-цент (66,5%) охвата больных диспансерным наблюдением. Изучение пока-зателей обеспеченности населения республики ревматологами выявило позитивные сдвиги. Сравнительный анализ показателей за 2010 и 2011 год показал прирост как штатных (35), так и занятых (28,25) ставок, что соответствовало 141,25 и 115,75 . Причем, увеличение ставок отмечается и в поликлиническом звене – из 199,25 штатных ставок было занято 160,5 (2012). Единая Национальная система здравоохранения (ЕНСЗ) внедряется по-этапно с 1 января 2010 года и является одним из направлений и путей до-стижений поставленных целей Государственной программы «Саламатты Ка-захстан» на 2011-2015 годы. Цели ЕНСЗ: формирование эффективной системы здравоохранения, ос-нованной на приоритетном развитии первичной медико-санитарной помощи; совершенствование системы управления и менеджмента в отрасли здраво-охранения; совершенствование механизмов финансирования здравоохране-ния; обеспечение высокого качества и доступности медицинской помощи. Основные принципы ЕНСЗ: свободный выбор медицинской организации и лечащего врача; прозрачность процесса оказания медицинских услуг; фор-мирование конкурентной среды оказания медицинских услуг; работа меди-цинских организаций, направленных на достижение конечных результатов и оплату медицинских услуг по фактическим затратам. ЕНСЗ ориентирована на конечный результат и оплату за фактические расходы за лечение каждо-го конкретного заболевания, оплату на основе контроля качества, прозрач-ность оплаты медицинских услуг с учетом протокола клинико-затратных групп и внедрением медико-экономических тарифов. Внедрен свободный выбор пациентом врача и медицинской организации (портал госпитализа-ции). Обследование и лечение больных СКВ согласно Протокола диагностики и лечения, в основе которого рекомендации Европейской лиги ревматологов (2007). Стандартная терапия включает, по показаниям, глюкокортикоиды (преднизолон, метилпреднизолон, пульс терапия метилпреднизолоном), ци-тотоксические препараты (циклофосфамид, азатиоприн, метотрексат, мико-фенолата мофетил, циклоспорин), гидроксихлорохин, нестероидные проти-вовоспалительные препараты, экстракорпоральные методы лечения (плаз-маферез), внутривенный иммуноглобулин, биологические препараты (ри-туксимаб, белимумаб). Заключение. СКВ остается значимым заболеванием в республике с преобладанием лиц женского пола (82%). Уровень распространенности СКВ в Казахстане ниже, чем в других странах с превалирующим азиатским населением. Низкий показатель охвата диспансери-зацией больных СКВ свидетельствует о необходимости усиления работы по качеству медицин-ского обслуживания в стране. Каллистов Д.Ю., Романов А.И., Колганова Э.В.МАРКЕРЫ СИСТЕМНОГО ВОСПАЛЕНИЯ У ПАЦИЕНТОВ С НАРУШЕНИЯМИ ДЫХАНИЯ ВО ВРЕМЯ СНА
ФГБУ «Центр реабилитации» УДП РФ, Московская область Нарушения дыхания во время сна широко распространены в общей попу-ляции населения (от 2%-4% до 20%) и оказывают существенное негатив-ное влияние на состояние здоровья, продолжительность и качество жизни людей. К основным последствиям обструктивного апноэ сна относят си-стемную и легочную артериальную гипертензию, нарушения сердечного ритма и проводимости, ускоренный атерогенез, нарушения липидного и углеводного обмена. Ведущую роль в патогенезе последствий СОАС имеют циклические эпизоды гипоксии-реоксигенации, изменения внутрито-ракального давления и фрагментация сна вследствие повторяющихся реак-ций активации ЦНС. Механизмы трансформации патофизиологический фак-торов СОАС в сосудистую патологию, и, в частности, роль системного воспаления в генезе кардиоваскулярных последствий СОАС, обратимость изменений требует уточнения. Цель: провести изучение маркеров системного воспаления и показате-лей цитокинового звена иммунитета и у пациентов с гипертонической бо-лезнью с синдромом обструктивного апноэ сна различной степени тяжести и оценить влияние терапии положительным давлением в дыхательных путях на указанные параметры. Методы: проведено обследование 35 пациентов с гипертонической бо-лезнью 2 стадии и синдромом обструктивного апноэ сна средней и тяжелой степени (21 мужчина и 14 женщин, ср. возраст 52,5±6,5 года, индекс массы тела – 28,7±3,1 кг/м2,, индекс апноэ-гипопноэ – 37,1+-14,2 события в час, минимальный уровень Sa02 = 71,1+_10,2%). Контрольную группу состави-ли 37 сопоставимых по основным характеристикам пациентов с ГБ 2 ст. без нарушений дыхания во время сна (23 мужчины и 14 женщин, ср. возраст 54,1±7,3 года, индекс массы тела – 27,9±4,5 кг/м2,, индекс апноэ-гипопноэ – 4,1+-3,2 события в час, минимальный уровень Sa02 = 89,1+_3,2%). В качестве инструментального метода диагностики расстройств сна проводи-лось полисомнографическое исследование с использованием системы Comet PSG (США). Количественное определение С-реактивного белка, фак-тора некроза опухоли, интерлейкинов (ИЛ 1β, ИЛ6). проводилось методом иммуноферментного анализа (Immulite 1000, США) в начале программы реа-билитации для пациентов обеих групп и через 2 недель после начала про-ведения терапии положительным давлением (СРАР-терапии) для пациентов основной группы (Breas iSleep 20+). Подбор СРАР-терапии осуществлялся в соответствии с критериями Американской академии медицины сна. Результаты. У обследованных основной подгруппы были выявлены по-вышенные, по сравнению с больными контрольной группы, уровни С-реактивного белка (14,2±3,1 мг/л и 5,8±2,1 мг/л), ФНО (15,0±4,9 пг/мл и 6,0±3,9 пг/мл) интерлейкина 1β (8,9±4,0 пг/мл и 3,8±2,9 пг/мл). Резуль-таты статистического анализа показали наличие положительной корреляци-онной связи между максимальной величиной десатурации и уровнем С-реактивного белка (r=0,41) и уровнем ФНО (r=0,45). Результаты повтор-ного исследования лабораторных показателей после курса СРАР-терапии показали снижение уровней ФНО (15,0±4,9 пг/мл); уровень снижения ФНО коррелировал с динамикой избыточной дневной сонливости по Эпфордской шкале. Обсуждение. Выявленные у пациентов с СОАС повышенные значе-ния цитокинов, СРБ и ФНО, свидетельствующие о наличии признаков хронического системного воспаления у лиц с нарушениями дыхания во время сна, могут играть существенную роль в формировании ведущих кар-диоваскулярных и метаболических последствий апноэ сна. Снижение уровня ФНО на фоне терапии положительным давлением в дыхательных путях мо-жет указывать на частичную обратимость выявленных изменений. Выводы. Включение методик диагностики и коррекции расстройств сна в программы лечения и реабилитации пациентов кардиологического профи-ля является патогенетически обоснованным и способно улучшить непосред-ственные и отсроченные результаты терапии. Кузнецов В.И., Морозова Т.А., Папичев В.А., Мозговая Е.Э., Бедина С.А.АКТИВНОСТЬ АМИНООКСИДАЗ В СЫВОРОТКЕ КРОВИ БОЛЬНЫХ ОСТЕОАРТРОЗОМ
ФГБУ «НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ, МУЗ «ГБ СМП №15», ГУЗ “Волгоградский областной клинический хоспис», г.Волгоград Цель исследования. Выявление особенностей активности бензиламино-оксидазы (БАО), лизиламинооксидазы (ЛАО) и диаминоксидазы (ДАО) в сы-воротке крови больных остеоартрозом (ОА) в зависимости от клинических особенностей. Материалы и методы. Под наблюдением в условиях стационара нахо-дились 49 больных, из которых 32 (65,3%) женщины. Преобладали больные в возрасте после 40 лет (83,7%). Явления синовита выявлены у 22 (44,9%) больных. I стадия поражения суставов по Штейнброкеру определялась у 12 (24,5%), II стадия – у 35 (71,4%) и III стадия – у 2 (4,1%) больных. В сыво-ротке крови по оригинальным методикам определялась активность бензила-минооксидазы (БАО), лизиламинооксидазы (ЛАО) и диаминоксидазы (ДАО). Контрольную группу составили 30 практически здоровых людей. Результаты. У больных ОА (всей группы), по сравнению со здоровыми, выше активность ДАО, БАО (р<0,001) и несколько выше активность ЛАО (р>0,05). Через 10-12 дней лечения снизилась активность ЛАО (р<0,01), ДАО (р<0,001) и проявилась тенденция к снижению активности БАО (р>0,05). По окончании лечения активность ДАО и БАО не имели отличий от здоровых, но активность ЛАО была ниже чем у здоровых (р<0,001). По сравнению со здоровыми, у больных ОА с синовитом выше активность БАО, ДАО и ниже ЛАО (все р<0,001), у больных без синовита выше активность всех ферментов (р<0,001). У больных с синовитом, по сравнению с больны-ми без синовита, ниже активность БАО (р<0,05), ЛАО (р<0,001) и незначи-тельно ниже ДАО (р>0,05). Энзимных различий между стадиями поражения суставов не выявлено (р>0,05). Заключение. Определение активности ЛАО, БАО и ДАО сыворотке крови больных ОА способствует объективизации оценки эффективности проводи-мой терапии, и необходимо учитывать влияние клинических особенностей ОА на активность аминооксидаз сыворотки крови. Кузнецов В.И., Рогаткина Т.Ф., Григорьянц С.Р., Морозова Т.А., Мозговая Е.Э., Стажаров М.Ю.АКТИВНОСТЬ ЭНЗИМОВ АДЕНИЛОВОЙ ВЕТВИ ПУРИНОВОГО МЕТАБОЛИЗМА В КЛЕТКАХ КРОВИ БОЛЬНЫХ ОСТЕОАРТРОЗОМ В ПЕРВЫЕ 5 ЛЕТ БОЛЕЗНИ
ФГБУ «НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ, МУЗ «КБ СМП №15», г.Волгоград Цель: выявить изменения активности аденозиндезаминазы (АДА), АМФ-дезаминазы (АМФДА), адениндезаминазы (АД) и 5′-нуклеотидазы (5′-НТ) в лизатах лимфоцитов и эритроцитов больных остеоартрозом (ОА) на протяже-нии первых 5 лет болезни. Материал и методы. Под наблюдением находились 78 больных ОА. Все больные в зависимости от длительности болезни были разделены на 3 группы. 1-ую группу составили 37 больных (женщины – 23 (62,2%)) с длитель-ностью болезни от 3 до 11 месяцев. Средний возраст (M±σ) – 47,3±3,7 лет. I стадия поражения суставов – у 36 (97,3%), II стадия – у 1 (2,7%) больного. 2-ую группу составили 20 больных (18 женщин – 90%) с длительностью болезни 12-23 месяца. Средний возраст – 44,4±3,9 лет. I стадия – у 9 (45%), II стадия – у 11 (55%) больных. В 3-ю группу вошли 21 больной (14 женщин – 66,7%) с длительностью болезни от 2 до 5 лет. Средний возраст – 54,5±0,5 лет, I стадия – у 15 (71,4%), II стадия – у 6 (28,6%) больных. Определение активности АДА, АМФДА, АД и 5′-НТ в лизатах лимфоцитов и эритроцитов проводилось по оригинальным методикам. Результаты. По сравнению со здоровыми у больных 1-ой группы в лиза-тах лимфоцитов выше активность АДА (р=0,046), АД (р<0,001), 5′-НТ (р=0,004), в эритроцитах выше активность АДА (р<0,001), АМФДА (р=0,006), АД (р<0,001); у больных 2-й группы в лимфоцитах выше актив-ность АД (р=0,004), в эритроцитах незначительно выше активность всех энзимов (р>0,05); у больных 3-й группы в лимфоцитах ниже активность АДА (р=0,038), выше АД (р<0,001), в эритроцитах выше активность АДА (р<0,001), 5′-НТ (р<0,001). У больных 1-й группы по сравнению с 2-й груп-пой, в лимфоцитах выше активность АДА (р<0,001), АМФДА (р=0,006) и 5′-НТ (р=0,003), в эритроцитах выше активность всех ферментов: АДА (р=0,034), АМФДА (р=0,005), 5′-НТ (р=0,041), АД (р=0,005); по сравнению с 3-й группой в лимфоцитах выше активность АДА (р<0,001), 5′-НТ (р=0,004), в эритроцитах выше активность АМФДА (р<0,001), 5′-НТ (р=0,004). У больных 2-й группы по сравнению с 3-й группой в лимфоцитах выше активность АДА (р<0,001), в эритроцитах ниже активность АДА (р<0,001). Заключение. Проведенные исследования показали, что с увеличением длительности заболевания активность большинства ферментов, повышенная на первом году болезни, через 2-5 лет снижается или имеет тенденцию к снижению. Леушина Е.А., Симонова О.В., Немцов Б.Ф., Сухих Е.Н.ВЛИЯНИЕ БАЗИСНОЙ ТЕРАПИИ НА КАЧЕСТВО ЖИЗНИ И РЕНТГЕНОЛОГИЧЕСКОЕ ПРОГРЕССИРОВАНИЕ ГОНАРТРОЗА
ГБОУ ВПО Кировская ГМА Минздравсоцразвития РФ, Россия, г.Киров Цель: Оценить влияние терапии диацереином, хондроитин сульфатом (ХС) и глюкозамин сульфатом (ГС) на качество жизни и темпы рентгенологи-ческого прогрессирования гонартроза гонартроза в 18-месячном контроли-руемом, рандомизируемом исследовании. Материал и методы: Исследование проведено у 160 больных достовер-ным диагнозом ГА. 40 больных (I группа) получали диацереин 50 мг 2 р/сутки (2 курса по 4 месяца), 40 больных (II группа) – ГС 1500 мг/сутки (2 курса по 3 месяца), 40 больных (III группа) – ХС 500 мг 2 р/сутки (2 курса по 6 месяцев), 40 (IV) – ацеклофенак 100-200 мг/сутки. Группы были сопо-ставимы по основным клиническим и демографическим показателям (р>0,05). Средний возраст пациентов I-й группы составил 57,2±5,4 лет, II-й – 60,8±6,8 года, III-й – 60,1±5,2, IV- 58,2±6,6. Длительность заболевания до 5 лет составило 35% -I группы, 37% – II группы, 32,5% – III группы, 50%- IV группы. Стаж болезни от 6 до 10 лет составляли 40%; 37,5%; 45% и 40% соответственно. Более 10 лет -25%; 25%; 22,5% и 10% соответ-ственно. Все пациенты имели II (50%) или III (50%) рентгенологическую стадию гонартроза. Для оценки рентгенологического прогрессирования ис-следовали степень сужения рентгенологической суставной щели (РСЩ) и наличие остеофитов (ОФ). Качество жизни изучали по шкале SF-36 до лече-ния и через 6 месяцев терапии. Для оценки влияния заболевания на КЖ больных проводили сравнительную оценку показателей КЖ больных ОА и показателей популяционных норм, которые были получены Межнациональ-ным центром исследования КЖ в Санкт-Петербурге с вычислением 8 основ-ных показателей: ФФ – физическое функционирование, РФФ – ролевое фи-зическое функционирование, РЭФ – ролевое эмоциональное функционирова-ние, Ж – жизнеспособность, ПЗ-психическое здоровье, СФ – социальное функционирование, Б – боль, ОЗ – общее здоровье. Результаты: При анализе рентгенологического прогрессирования к 18 месяцу терапии статистически значимое сужение РСЩ (p<0,001) и отрица-тельная динамика ОФ (p<0,01) отмечены только в IV группе пациентов, имеющих III стадию. У пациентов с II стадией статистически значимого сужения РСЩ не выявлено во всех группах, хотя в IV группе, по сравнению с I, II и III, наблюдалась более отчетливая отрицательная динамика. Утяже-ление рентгенологической стадии отмечено у 10% пациентов I группы, у 10,7% – III и у 25% -IV. Все показатели КЖ были достоверно значимо хуже у больных гонартрозом в сравнении со здоровыми лицами (p<0,05). В наибольшей степени изменялись показатели физического здоровья: ФФ, РФФ, Б. Все параметры были значительно ниже у больных с III стадией го-нартроза. Показатель Б был снижен на 51,4% в группах со II стадией и на 53,3% в группах с III стадией гонартроза. Показатель ФФ был ниже на 54,1% и на 61,6% соответственно. Самое значительное снижение наблюда-лось показателя РФФ: на 69,1% у больных со II стадией и на 74,9% у боль-ных с III стадией. Среди показателей КЖ, характеризующих психологиче-ское здоровье (Ж, СФ, РЭФ, ПЗ), в большей степени было снижено РЭФ – на 52,6% у пациентов со II стадией и y 61,2% у пациентов с III стадией. На более высоком уровне сохранялось СФ, тем не менее, его уровень был на 29% хуже, чем в популяции. Была выявлена отрицательная корреляция между ФФ и рентгенологической стадией ( r=-0,31; р<0,01), стажем заболе-вания (r=-0,193; р<0,05); между РФФ и рентгенологической стадией (r=-0,17; р<0,05), а также между Б и рентгенологической стадией (r=-0,202; р<0,05). Отрицательная корреляция наблюдалась между Ж и стажем болез-ни (r=- 0,205; р<0,05); между ПЗ и стажем заболевания ( r=-0,196; р<0,05). Терапия базисными препаратами улучшала некоторые параметры КЖ боль-ных. Статистически значимая (р<0,05) положительная динамика у больных отмечена в 1-й, 2-й и 3-й группах по шкале ролевое эмоциональное функци-онирование (РЭФ) как при II, так и при III стадиях гонартроза. В I-й и 2-й группах при II и III стадиях наблюдалось также улучшение ролевого физи-ческого функционирования (РФФ) (р<0,05). Друге шкалы КЖ в 1-й и 3-й группах достоверно не изменялись , но имели тенденции к их повышению. Во 2-й группе при IIстадии гонартроза отмечено статистически значимое улучшение всех шкал КЖ (р<0,05). При III стадии гонартроза во 2-й группе статистически значимая (р<0,05) положительная динамика наблюдалась по шкалам ФФ, РФФ, Б. Ж и РЭФ. Достоверного изменения показателей в 4-й группе на фоне лечения не наблюдалось, причем при III стадии гонартроза показатели практически не отличались от исходных. Обсуждение: Сравнительный анализ влияния базисной терапии в нашем исследовании выявил преимущество глюкозамин сульфата, по сравнению с диацереином и хондроитин сульфатом, по влиянию на показатели КЖ у больных гонартрозом II–III стадии. При IIстадии гонартроза показатели име-ли более высокие значения в сравнении с III стадией гонартроза при тера-пии ГС. Замедление темпов рентгенологического прогрессирования также отмечено у пациентов, принимавших ГС. Заключение: Терапия диацереином, ГС, ХС, по сравнению с ацеклофе-наком, сдерживает темпы рентгенологического прогрессирования особенно у пациентов II рентгенологической стадией. ГС, по сравнению с диацереином и ХС, оказывает более стабилизирующее влияние на рентгенологическое прогрессирование. В исследовании отмечено, что терапия препаратами мед-ленного действия улучшает качество жизни пациентов гонартрозом. Леушина Е.А., Симонова О.В., Немцов Б.Ф., Сухих Е.Н.ВЛИЯНИЕ БАЗИСНОЙ ТЕРАПИИ НА АРТРОСОНОГРАФИЧЕСКИЕ ПОКАЗАТЕЛИ ПРИ ГОНАРТРОЗЕ
ГБОУ ВПО «Кировская ГМА» Минздравсоцразвития РФ, Россия, г.Киров Цель. Оценить влияние терапии диацереином, хондроитин сульфатом (ХС) и глюкозамин сульфатом (ГС) на артросонографические показатели при гонартрозе в 18-месячном контролируемом, рандомизируемом исследовании. Материал и методы. Исследование проведено у 160 больных достовер-ным диагнозом гонартроза. 40 больных (I группа) получали диацереин 50 мг 2 р/сутки (2 курса по 4 месяца), 40 больных (II группа) – ГС 1500 мг/сутки (2 курса по 3 месяца), 40 больных (III группа) – ХС 500 мг 2 р/сутки (2 курса по 6 месяцев), 40 (IV) – ацеклофенак 100-200 мг/сутки. Группы были сопо-ставимы по основным клиническим и демографическим показателям (р>0,05). Средний возраст пациентов I-й группы составил 57,2±5,4 лет, II-й – 60,8±6,8 года, III-й – 60,1±5,2, IV- 58,2±6,6. Все пациенты имели II (50%) или III (50%) рентгенологическую стадию гонартроза. Длительность заболевания до 5 лет составило 35% -I группы, 37% – II группы, 32,5% – III группы, 50%- IV группы. Длительность заболевания 6-10 лет составляли 40%, 37,5%, 45% и 40% соответственно. Более 10 лет -25%, 25%,22,5% и 10% соответственно. Частота синовита составила 77,5% – I группы, 75%- II группы, 35% -III группы и 70% – IV группы. Эффективность лечения оцени-валась по индексам WOMAC, Лекена, боли по ВАШ при ходьбе и в покое, суточной потребности в нестероидных противовоспалительных препаратах НПВП. Для оценки динамики синовита проводили измерение артросоногра-фических показателей коленных суставов исходно и через 18 месяцев наблюдения. Оценивали состояние суставного хряща, синовиальную оболоч-ку, остеофиты и наличие выпота в суставе. Исследование проводили на УЗВ аппарате SONOLINE G-20 датчиком 6,5-10 МГЦ в стандартных для обследо-вания коленного сустава позициях. Результаты. К 18 мес. достоверное уменьшение боли при ходьбе ( р<0,05) отмечено во всех группах у пациентов с гонартрозом II и III стади-ей. Боль в покое достоверно уменьшалась ( р<0,05) во 2-4-х группах при гонартрозе IIIстадии и 2-й и 4-й группе при гонартрозе II стадией. В 1-х группах достоверное уменьшение боли ( р<0,05) отмечено только к 15 мес. Индекс Лекена достоверно уменьшался во всех группах при гонартрозе II стадии и во 2-й и 4-й групп ах при гонартрозе III стадии. Уменьшение ско-ванности достоверно отмечено ( р<0,05) в 1-й, 2-й и 4–й группах при го-нартрозе II и III стадиях. Достоверное уменьшение ( р<0,05) суммарного индекса WOMAC наблюдалась в 1-й, 2-й и 4-й группах при гонартрозе IIста-дии и и только в 4-й группе при гонартрозе III стадии. Улучшение функции ( р<0,05) суставов отмечено в 2-4-й группах при II стадии гонартроза. Стати-стически значимое ( р<0,05) улучшение функции в 1-х группах замечено к 15 мес.. При анализе показателей положительная их динамика отмечалась с 12 недель и сохранялась до 18 мес. только во 2-й группе. К 18 мес прием НПВП отменили пациенты с гонартрозом II стадии 25% -1-й группы, 37,5%-2-й группы и 18,7% 3-й группы. Число пациентов с гонартрозом III стадией, отменивших НПВП, составило 7% только во 2-й группе. При анализе соно-графических показателей к 18 месяцу терапии отмечено уменьшение толщи-ны синовиальной оболочки в 1-3 группах при II и III стадиях гонартроза, но статистически значимое уменьшение (р< 0,05) толщины синовиальной обо-лочки отмечено в 1-й группе на 10% при гонартрозе II стадии гонартроза и во 2-й группе при III стадии гонартроза. В 4-й группе толщина синовиальной оболочки не изменялась от исходной. Статистически значимое (р< 0,05) уменьшение толщины суставного хряща отмечено в 4-й группе на -0,34 мм и -0. 31 мм при II и IIIстадиях гонартроза соответственно. В остальных груп-пах достоверных изменений толщины суставного хряща не отмечено. При анализе размеров остеофитов статистически значимых изменений не полу-чено, но отмечено увеличение размеров остеофитов в 4-й группе на +0,2 мм. и на + 0,15мм в 3-й группе при гонартрозе III стадии. Уменьшение синовита у пациентов с гонартрозом II стадии составило 64% в 1-й группе; 70% -2-й группе; 44% в 3-й группе и 40% в 4-й группе. Уменьшение синовита у больных, имеющих III стадию гонартроза составило 50%; 50% ; 25% и 43% соответственно. Обсуждение: В данном исследовании отмечено, что препараты медлен-ного действия являются эффективными. Они уменьшают боль, скованность, улучшают функцию суставов. При II стадии гонартроза эффективность пре-паратов несколько выше , чем при гонартрозе III стадии. Отмечено, что при применении ГС и диацереина все показатели имели тенденцию к более ран-ней и стабильно положительной динамике.. При гонартрозе диацереин, ГС и ХС уменьшают толщину синовиальной оболочки, синовит, стабилизируют толщину суставного хряща. Терапия только НПВП приводит к снижению толщины суставного хряща, увеличению размеров остеофитов. Заключение. Терапия диацереином, ГС, по сравнению с ХС и ацеклофе-наком, сдерживает темпы прогрессирования. И оказывает более заметную положительную динамику сонографических показателей. Маланин Д.А., Рогова Л.Н., Демкин С.А., Демещенко М.В.ОПЫТ ПРИМЕНЕНИЯ АУТОЛОГИЧНОЙ ОБОГАЩЕННОЙ ТРОМБОЦИТАМИ ПЛАЗМЫ КРОВИ ПРИ ЛЕЧЕНИИ ПАЦИЕНТОВ С ГОНАРТРОЗОМ III СТАДИИ
ГБОУ ВПО Волгоградский государственный медицинский университет мини-стерства здравоохранения Российской Федерации, Волгоград, Россия. Введение. Аутологичная обогащенная тромбоцитами плазма (ОТП) – взвесь тромбоцитов, содержащаяся в концентрации в единице объема плаз-мы крови человека в 6-8 раз. Тромбоциты содержат как специфичные для остеогенеза факторы роста, так и неспецифичные факторы, инициирующие процесс регенерации любой соединительной ткани. В последние годы по-явились клинические исследования по использованию ОТП при лечении па-циентов с гонартрозом, однако однозначного мнения на этот счет еще не существует, а многие вопросы остаются дискутабельными. Целью нашего исследования являлось клиническое обоснование приме-нения обогащенной тромбоцитами плазмы в комплексном лечении пациентов с гонартрозом. В задачи входила оценка влияния внутрисуставного введения ОТП на выраженность болевого синдрома и функцию коленного сустава. Материалы и методы. В исследовании приняли участие 16 пациентов (10 женщин и 6 мужчин) с гонартрозом III стадии по классификации Косинской Н.С. (1975), установленным на основании клинико-рентгенологических данных. Выраженность болевого синдрома и функцию коленного сустава оценивали по 10-балльной визуально-аналоговой шкале боли (ВАШ) и по индексу Лекена в сроки от 7 дней до 12 месяцев после проведенного лече-ния. Обогащение тромбоцитами плазмы крови выполняли в несколько этапов. На первом этапе 50 мл венозной крови пациента в стерильном мерном кон-тейнере смешивали с 5 мл цитрата натрия, центрифугировали (центрифуга «Rotofix» 32A, Венгрия) в течение 15 минут при 2400 об/мин. Затем забира-ли 20 мл надосадочной плазмы, которую смешивали с 2 мл хлорида кальция. Второй этап заключался в центрифугировании надосадочной плазмы в тече-ние 20 минут при 3400 об/мин. и заборе 5 мл богатой факторами роста взве-си, которую вводили под местной анестезией в полость коленного сустава. Каждому пациенту выполняли 3 инъекции с периодичностью введения 1 раз в 3 недели. Результаты. Хороший результат лечения наблюдали у 8 пациентов, что сопровождалось уменьшением выраженности болевого синдрома по ВАШ с 7-8 баллов (сильная боль) до 3-4 баллов (незначительная боль) и снижением степени тяжести гонартроза по шкале Лекена с резко выраженной до сред-ней. У 7 пациентов был получен удовлетворительный результат, выражав-шийся в уменьшении болевого синдрома с 9-10 баллов (резко выраженная боль) до 5-6 баллов (умеренная боль) и изменении степени тяжести гонарт-роза с резко выраженной до выраженной. Отсутствие обезболивающего дей-ствия ОТП после первой инъекции наблюдали у 1 пациентки, которая отка-залась принимать участие в дальнейшем исследовании. Средняя продолжи-тельность достигнутого положительного эффекта составляла от 14 дней до 3 месяцев. Выводы. Внутрисуставное введение аутологичной обогащенной тромбо-цитами плазмы при лечении пациентов с гонартрозом позволяет уменьшить выраженность болевого синдрома и улучшить функцию коленного сустава, даже при выраженной стадии заболевания. Мартемьянов В.Ф., Бедина С.А., Стажаров М.Ю., Евдокимова Е.В., Зборовский А.Б.ЭНЗИМНЫЕ РАЗЛИЧИЯ В КРОВИ БОЛЬНЫХ УРОГЕННЫМ РЕАКТИВНЫМ АРТРИТОМ И АНКИЛОЗИРУЮЩИМ СПОНДИЛИТОМ
ФГБУ «НИИ КиЭР» РАМН, г. Волгоград Цель исследования. Выявить особенности активности энзимов пурино-вого метаболизма (ПМ) в плазме крови и лизатах лимфоцитов, способствую-щие дифференциации урогенного реактивного артрита (ур.РеА) и анкилози-рующего спондилита (АС). Материалы и методы. Под наблюдением находились 30 больных ур.РеА и 22 больных АС. Средний возраст (M±m) больных ур.РеА – 27,0±1,0 лет, больных АС – 36,8±1,7 лет. Контрольная группа – 30 здоровых лиц. В плазме и лизатах лимфоцитов крови по оригинальным методикам определя-лись активности гуаниндезаминазы (ГДА), гуанозиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфосфорилазы (ГФ). Результаты исследования. В плазме здоровых лиц активность (нмоль/мин/мл) ГДА составила 1,16±0,02; ГЗДА – 2,08±0,05; ПНФ – 0,85±0,02; ГФ – 1,09±0,02; в лимфоцитах активность ГДА – 11,7±0,18; ГЗДА – 7,49±0,13; ПНФ – 34,5±0,7; ГФ – 11,5±0,3 нмоль/мин/мл. По сравнению со здоровыми, у больных ур.РеА в плазме выше активность ГДА, ПНФ (все р<0,001), ниже ГЗДА (р<0,01), в лизатах лимфоцитов ниже активность ГДА (р<0,05), ПНФ (р<0,01), выше ГЗДА и ГФ (р<0,001), у больных АС в плазме выше активность ГДА, ПНФ, ГФ и ниже ГЗДА (р<0,001), в выше активность ГЗДА и ГФ (р<0,001). У больных ур.РеА, по сравнению с больными АС, в плазме ниже активность ГДА, ПНФ, ГФ (все р<0,001) и выше ГЗДА (р<0,01), в лимфоцитах ниже активность ГДА (р<0,05), ПНФ (р<0,01) и ГФ (р<0,001). Для более четкой дифференциации ур.РеА и АС целесообразно ориентиро-ваться на максимальные и минимальные величины активности энзимов, по-лученные нами у больных. Так, если у больного в плазме активность (в нмоль/мин/мл) ГДА ниже 1,32; ПНФ<0,88; ГФ<1,12, в лимфоцитах актив-ность ГЗДА<6,8; ГФ<12,6, то очень вероятен диагноз РеА. Если же в плазме активность ГДА>1,48; ПНФ>1,16 и ГФ>1,28 нмоль, в лимфоцитах ГДА>13,8; ГЗДА>12,5; ПНФ<25,6 или >40,3 и ГФ>16,5 нмоль, то много данных за диа-гноз АС. Заключение. Если возникает проблема дифференциации ур.РеА и АС, то в комплексе с клинико-инструментальными и лабораторными данными опре-деление активности ГДА, ГЗДА, ПНФ и ГФ в плазме и лимфоцитах может ока-зать существенную помощь. Мартемьянов В.Ф., Зборовская И.А.К ВОПРОСУ О ГИПЕРФЕРМЕНТЕМИИ ПРИ РЕВМАТИЧЕСКИХ ЗАБОЛЕВАНИЯХ
ФГБУ «НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ В клинической практике определение активности ферментов в сыворотке (плазме) крови в диагностических целях имеет широкое распространение. Чаще всего при воспалительных, реже дистрофических процессах имеет ме-сто повышение активности ферментов – гиперферментемия. Одной из основ-ных причин гиперферментемии признается повышенная проницаемость мем-бран клеток тканей, вовлеченных в патологический процесс. При нормаль-ных размерах мембранных пор (0,3-0,4 нм) ферменты могут проходить через них, так как молекулярная масса большинства ферментов довольно высока (свыше 90000 дальтон). Одной из причин появления ферментов в экстрацеллюлярной жидкости является естественная гибель клеток и выход их содержимого, в том числе и ферментов, в плазму. Учитывая, что в нормально функционирующем орга-низме естественная гибель клеток держится на постоянном уровне, то и уро-вень энзимной активности плазмы в этих случаях, как правило, постоянен, что и принимается в клинической практике за условную норму активности того или иного фермента. Границей раздела между периферической кровью и внутриклеточными энзимами является клеточная мембрана. Концентрационные градиенты фер-ментов между клеткой и плазмой достаточно высоки, и содержание энзимов внутри клетки в десятки-сотни раз превышает их плазменную концентрацию. Клеточные мембраны имеют две противоречивые функции: с одной стороны поддерживают необходимый концентрационный градиент между клеткой и плазмой, а с другой стороны обеспечивают быстрый и селективный обмен метаболитов и ионов в зависимости от меняющихся условий функционирова-ния клетки. Сложности поддержания необходимого градиента концентраций различных метаболитов, в том числе и ферментов, и в то же время обеспе-чения селективного обмена между клеткой и экстрацеллюлярным простран-ством при наличии ограниченно проницаемой мембраны обусловили в про-цессе эволюции многоступенчатый механизм регуляции на основе активного и пассивного транспорта. Активный транспорт требует участия АТФ, АТФ-аз, фосфолипидов и в случае их дефицита скорость транспорта резко падает. Пассивный транспорт обеспечивается структурными особенностями внешней мембраны, имеющей микроворсинки, которые способны изменять свою форму и величину в зависимости от меняющихся условий, вследствие чего мембранная поверхность клетки увеличивается в 10-15 раз с раскрыти-ем дополнительных малых и больших пор (больше 10 нм), через которые и осуществляется селективная диффузия. Любой патологический процесс, в том числе и воспалительный, сопровождается или даже начинается с изме-нения отдельных звеньев метаболизма, в которых некоторые ферменты при-нимают непосредственное участие, модифицируя свою активность. Причем, эти изменения невозможны без повышения скорости транспорта между клет-кой и экстрацеллюлярным пространством. Следствием этого является повы-шение клеточной проницаемости для некоторых метаболитов и ферментов. Кроме того, поддержание нормальных параметров мембранных пор может осуществляться лишь при наличии в клетке определенного запаса макроэр-гических соединений (АТФ, КРФ и др.). При патологических состояниях энергообеспечение клеток, как правило, нарушается чаще всего в сторону уменьшения энергетического потенциала за счет снижения окислительного фосфорилирования, гликолиза и других метаболических каскадов, являющихся поставщиками макроэргических со-единений. Следствием этого является повышенный выход внутриклеточных энзимов в плазму за счет увеличения мембранной проницаемости. В экспе-рименте было показано, что как только в клетках падают запасы глюкозы, являющейся источником АТФ, наблюдается значительный выход ферментов из клетки, но добавление в перфузионную среду АТФ, КРФ прекращает вы-ход энзимов в экстрацеллюлярную среду (Вилкинсон Д., 1981). Потеря внут-риклеточных энзимов из любого типа клеток связана обратной зависимостью с содержанием в них АТФ. Повышение активности ферментов в плазме всегда является признаком наличия патологических процессов в организме. Причем, если повреждение клеток незначительное, то при повышении проницаемости наружных мем-бран в экстрацеллюлярное пространство в первую очередь выходят цито-зольные ферменты, так как они имеют меньшую молекулярную массу, чем митохондриальные. Появление же в плазме митохондриальных форм энзи-мов свидетельствует о более выраженной клеточной патологии. Выход ядер-ных ферментов из клетки в плазму сигнализирует уже о существенном по-вреждении клеток, вплоть до ее некроза. Если известно содержание тех или иных ферментов в тканях (органах) здоровых людей, то уровень гиперфер-ментемии при патологии во многом зависит от массы органа и площади (объ-ема) поражения. Поэтому при заболеваниях печени, сердца, почек, мышеч-ной ткани в плазме определяются высокие величины активности энзимов. Большинство ревматических заболеваний характеризуется выраженными воспалительными процессами и наличием повышенной мембранной прони-цаемостью клеток, которая инициируется и поддерживается интенсификаци-ей свободнорадикального окисления и ослаблением антиоксидантной систе-мы, нарушением энергетического заряда клеток, расстройством электролит-ного обмена (повышение внутриклеточного содержания кальция и натрия), резкой активацией кальций-зависимых фосфолипаз А, обуславливающих деградацию фосфолипидного слоя мембран, нарушением содержания цикли-ческих нуклеотидов за счет повышения уровня ц-ГМФ, способствующего ла-билизации лизосомальных мембран (Коровкин Б.Ф. и др., 1987; Friedel et al., 1979; Gebhard M. et al., 1977; Nesta J. et al., 1987). Мартемьянов В.Ф., Мякишев М.В., Пересыпкин М.В., Пересыпкин В.В., Левкина М.В.АКТИВНОСТЬ ЭНЗИМОВ ГУАНИЛОВОЙ ВЕТВИ ПУРИНОВОГО МЕТАБОЛИЗМА В СЫВОРОТКЕ КРОВИ БОЛЬНЫХ СИСТЕМНОЙ СКЛЕРОДЕРМИЕЙ И РЕАКТИВНЫМ АРТРИТОМ
ФГБУ «НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ, ГУЗ ВОКЦ восстановительной медицины и реабилитации №2, г.Волгоград Наличие суставного синдрома у больных системной склеродермией и ре-активным артритом обуславливает трудности в их дифференциации. Цель: выявить особенности активности гуаниндезаминазы (ГДА), гуано-зиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфос-форилазы (ГФ) в сыворотке крови больных системной склеродермией (ССД) и реактивным артритом (РеА) для повышения качества их дифференциации. Материал и методы. Под наблюдением находились 52 больных ССД (женщины – 44, мужчины – 8, возраст больных – 34,8±1,3 лет, длительность болезни – 6,4±0,5 лет) и 54 больных РеА (женщины – 18, мужчины – 36, возраст больных – 31,9±1,0 лет, длительность болезни – 9,4±0,9 месяцев). У больных ССД I степень активности процесса определялась у 17, II степень – у 30 и III степень – у 5 больных. У больных РеА I степень установлена у 21, II степень – у 22 и III степень – у 11 больных. Активность ГДА, ГЗДА, ПНФ и ГФ в сыворотке крови определялась по оригинальным методикам. Результаты. По сравнению со здоровыми, у больных ССД (всей группы) в сыворотке выше активность ГДА (р<0,001), ГЗДА (р<0,05), ГФ (р<0,05) и ПНФ (р<0,001), у больных ССД с I степенью выше активность ГДА, ГЗДА и ПНФ (все р<0,01), у больных с II степенью выше активность ГДА (р<0,001), ГФ (р<0,05) и ПНФ (р<0,001), у больных с III степенью выше активность ГДА, ПНФ (р<0,001) и ГФ (р<0,01). У больных РеА (всей группы) выше ак-тивность ГДА, ПНФ, ниже ГЗДА и ГФ (все р<0,001); у больных с I степенью выше активность ПНФ (р<0,01); у больных с II степенью выше активность ГДА, ПНФ (р<0,001), ниже ГЗДА и ГФ (р<0,01), у больных с III степенью выше активность ГДА, ПНФ, ниже ГЗДА (все р<0,001) и ГФ (р<0,01). Сравнительные исследования показали, что у больных ССД (всей группы) по сравнению с больными РеА (всей группы) выше ГДА, ГЗДА, ПНФ (все р<0,001) и ГФ (р<0,01). У больных ССД с I степенью по сравнению с боль-ными РеА с I степенью выше активность ГДА, ГЗДА (все р<0,001). У больных ССД с II степенью по сравнению с больными РеА с II степенью выше актив-ность всех ферментов: ГДА, ГЗДА, ПНФ (все р<0,001) и ГФ (р<0,01). У боль-ных ССД с III степенью по сравнению с больными РеА с III степенью выше активность всех ферментов (р<0,001). Заключение. Определение активности ГДА, ГЗДА, ПНФ и ГФ в сыворотке крови больных ССД и РеА в комплексе с клиническими данными способствует их дифференциации. Мартемьянов В.Ф., Рогаткина Т.Ф., Некрасова С.П., Кузнецов В.И., Стажаров М.Ю.ЭНЗИМЫ МЕТАБОЛИЗМА БИОГЕННЫХ АМИНОВ В КРОВИ БОЛЬНЫХ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКОЙ
ФГБУ «НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ, МУЗ «КБ СМП №15», г.Волгоград Цель: повышение качества диагностики активности патологического процесса у больных системной красной волчанкой (СКВ). Материал и методы. Под наблюдением в условиях стационара находи-лись 27 больных СКВ, из которых 25 (92,6%) женщин. Возраст больных был в пределах от 20 до 60 лет с преобладанием возраста до 40 лет (62,9%). I степень активности патологического процесса определялась у 12 (44,4%), II степень – также у 12 (44,4%) и III степень – у 3 (11,2%) больных. В сыво-ротке крови по оригинальным методикам определялись активности диами-ноксидазы (ДАО), бензиламинооксидазы (БАО) и лизиламинооксидазы (ЛАО). Контрольную группу составили 30 практически здоровых людей. Результаты. Активность аминоксидаз в сыворотке крови здоровых лю-дей (нмоль/мг/час) составила: для БАО – 5,2±0,3; ЛАО – 6,0±0,3 и ДАО – 4,8±0,2 нмоль/мг/час. По сравнению со здоровыми у больных СКВ с I степе-нью активности процесса при поступлении на лечение ниже активность БАО и ЛАО (р<0,001), ДАО (р<0,05), у больных СКВ с II степенью – ниже актив-ность БАО (р<0,001), ЛАО (р<0,001) и ДАО (р<0,05), у больных СКВ с III степенью – ниже активность всех ферментов (р<0,001). Сравнительный ана-лиз показал, что у больных СКВ с I степенью по сравнению с больными СКВ с II степенью, выше активность ЛАО (р<0,01) и незначительно выше актив-ность БАО и ДАО (р>0,05) по сравнению с больными СКВ с III степенью вы-ше активность ЛАО (р<0,01), ДАО (р<0.05) и незначительно выше БАО (р>0,05). При II степени по сравнению с III степенью выше активность ДАО (р<0,01) и незначительно выше активность БАО и ЛАО (р>0,05). Заключение. Определение активности ЛАО и ДАО в комплексе с клини-ческими данными может способствовать уточнению степени активности пато-генетического процесса при СКВ. Машкунова О.В.СРАВНИТЕЛЬНАЯ ОЦЕНКА КОМПЛЕКСНОЙ ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИ УЗЛОВАТОЙ ЭРИТЕМЫ В РЕВМАТОЛОГИЧЕСКОЙ ПРАКТИКЕ
Казахский Национальный Медицинский Университет им. С.Д. Асфендиярова, г. Алматы, Республика Казахстан В клиническом аспекте узловатая эритема – неспецифический иммуно-воспалительный синдром, встречающийся при широком спектре соматиче-ских, инфекционных, паранеопластических, лекарственных заболеваний, в патогенетическом – иммунокомплексный васкулит из группы аллергических ангиитов, протекающий по типу реакций гиперчувствительности замедленно-го типа. Узловатая эритема может быть первичной и вторичной, как один из симптомов аутоиммунных заболеваний. Актуальной проблемой в лечении пациентов с узловатой эритемой является её рецидивирование, которое должно насторожить врача в отношении её вторичности или неадекватности терапии. Цель исследования: выбор оптимальной схемы лечения первичной уз-ловатой эритемы у ревматологических пациентов для максимального сниже-ния и предупреждения её рецидивирования. Материал и методы. Обследовано 84 пациента с узловатой эритемой, из них 94% женщин и 6% мужчин. Средняя длительность заболевания состави-ла 8 лет. Проводился тщательный сбор анамнеза для выяснения этиологии узловатой эритемы для исключения туберкулеза, саркоидоза, онкологиче-ского процесса, заболеваний соединительной ткани и выявление факторов риска в виде сопутствующей сосудистой патологии. Все пациенты были раз-делены на три группы, в зависимости от назначаемого лечения. Пациентам первой группы назначалась противовоспалительная терапия нестероидными противовоспалительными препаратами – диклофенак в суточной дозе 150 мг. не менее 30 дней, второй группы – пероральными кортикостероидами в дозе 20–30 мг. в течение 10–15 дней в зависимости от активности, с после-дующим постепенным снижением до полной отмены, третья группа получала пульс-терапию метилпреднизолоном в курсовой дозе от 325 мг. до 1000 мг. в течение 3-х последовательных дней с переходом на поддерживающие дозы перорально 20–30 мг. с последующим снижением до полной отмены. В ком-плексную схему лечения всем больным включались антибактериальные пре-параты при доказанной связи со стрептококковой инфекцией, вазоактивные препараты – пентоксифиллин 5,0 мл. на 100 мл. физиологического раствора № 5 в/в капельно, антиагреганты – дипиридамол в суточной дозе 75 мг., местно – аппликации димексида, ихтиоловой мази. В динамике фиксирова-лись следующие показатели: быстрота наступления инволюции высыпаний, динамика снижения скорости оседания эритроцитов, С–реактивного белка, циркулирующих иммунных комплексов на 10-й, 30-й дни заболевания. Для выявления рецидивов наблюдение за пациентами в динамике проводилось в течение 2 лет. Применялись обще-принятые клинические и лабораторные исследования. Уровень циркулирую-щих иммунных комплексов определяли методом осаждения 3,5% полиэти-ленгликоля. Степени активности узловатой эритемы устанавливали по клас-сификации кожных ангиитов по Иванову О.Л. (1984г.) Результаты и обсуждение. Первичная узловатая эритема, чаще стреп-тококковой этиологии наблюдалась у 71% пациентов; вторичная, причиной которой были туберкулез, бруцеллез, иерсиниоз, саркоидоз, системные за-болевания соединительной ткани, в том числе и системные васкулиты – у 29% больных. Пациенты с вторичной узловатой эритемой направлялись к соответствующим специалистам. Во всех трех группах пациентов с первич-ной узловатой эритемой среднее количество рецидивов в течение болезни составило от 2 до 4. Наиболее частые и ранние рецидивы наблюдались в течение 1–3 лет от дебюта болезни. У 48% пациентов были обнаружены фо-новые сопутствующие сосудистые заболевания нижних конечностей, такие как варикозное расширение вен нижних конечностей, тромбофлебиты, лим-фангииты; ожирение, лекарственная аллергия, которые провоцировали и усугубляли течение узловатой эритемы. Активность I степени наблюдалась у 35% больных, II степень – у 41% больных, III степень – у 24% больных. Скорость оседания эритроцитов на начало заболевания во всех группах составила 47±2,3 мм/ч; количество С–реактивного белка – 34±3,1 мг/л; значения циркулирующих иммунных комплексов – 6,5±1,4 ед.опт.пл. На фоне проводимой терапии у пациентов I группы значимая инволюция уз-лов наступала на 5 сутки заболевания, во II группе – на 3-4 сутки; в III – на 2-3 сутки; скорость оседания эритроцитов на 10 сутки составила соот-ветственно – 31±2,2 мм/ч., 27±1,7 мм/ч., 23±1,2 мм/ч.; уровень С–реактивного белка соответственно– 26±3,2 мг/л., 18±1,8 мг/л., 13±1,2 мг/л.; значения циркулирующих иммунных комплексов – 6,4±1,3 ед.опт.пл., 6,2±1,4 ед.опт.пл., 6,1±1,6 ед.опт.пл. На 30-е сутки заболева-ния – средняя скорость оседания эритроцитов составила – 26±2,1 мм/ч., 14±1,3 мм/ч., 12±1,5 мм/ч; уровень С–реактивного белка – 16±2,3 мг/л, 8±1,2 мг/л., 4±1,4 мг/л.; значения циркулирующих иммунных ком-плексов – 6,2±1,6 ед.опт.пл., 6,1±1,4 ед.опт.пл., 5,2±1,6 ед.опт.пл. Процент рецидивирования через 2 года составил в первой группе – 22 %, во второй – 7%, в третьей – 3%. Рецидивирование наступало, как прави-ло, после очередной стрептококковой инфекции или вакцинации. Узловатая эритема в наибольшем числе случаев выступала как первич-ный аллергический иммунокомплексный васкулит, реже – как неспецифиче-ский кожный синдром инфекционных, соматических, аутоиммунных заболе-ваний. Наибольшее значение в возникновении первичной узловатой эритемы имела стрептококковая инфекция. Сопутствующие сосудистые заболевания провоцировали возникновение узловатой эритемы вследствие усугубления микроциркуляторных сосудистых нарушений. Узловатая эритема наблюда-лась при таких системных заболеваниях, как системная красная волчанка, неспецифический аортоартериит, болезнь Бехчета, что требовало лечения основного заболевания. Изменения в лабораторном статусе характеризуются повышением острофазовых показателей и циркулирующих иммунных ком-плексов. У всех пациентов с узловатой эритемой независимо от активности наблюдался повышенный уровень циркулирующих иммунных комплексов, что может приводить к рецидивированию узловатой эритемы. Схема лече-ния узловатой эритемы с включением на ранних стадиях заболевания пульс-терапии метилпреднизолоном значительно уменьшает процент рецидивиро-вания. В патогенезе рецидивирования узловатой эритемы играют роль им-мунные механизмы в виде повышенных циркулирующих иммунных комплек-сов, которые остаются повышенными у пациентов длительное время, не-смотря на проводимую противовоспалительную кортикостероидную терапию. Выводы. Перед началом лечения необходимо выявить этиологический фактор возникновения узловатой эритемы на предмет первичности или вто-ричности. Наиболее эффективной схемой лечения первичной узловатой эритемы является кортикостероидная терапия в виде последовательного назначения пульс-терапии метилпреднизолоном в адекватных дозах с после-дующим переходом на пероральные кортикостероиды до полной отмены, что значительно ускоряет сроки выздоровления и уменьшает процент рециди-вов. Мозговая Е.Э., Евдокимова Е.В., Мартемьянов В.Ф, Кузнецов В.И., Бедина С.А.КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ ИССЛЕДОВАНИЙ АКТИВНОСТИ ЭНЗИМОВ ГУАНИЛОВОЙ ВЕТВИ ПУРИНОВОГО МЕТАБОЛИЗМА В КРОВИ БОЛЬНЫХ РЕВМАТОИДНЫМ И РЕАКТИВНЫМ АРТРИТАМИ
ФГБУ «НИИ КиЭР» РАМН, МУЗ КБ СМП №15, г.Волгоград Цель исследования. Выявить особенности активности гуаниндезамина-зы (ГДА), гуанозиндезаминазы (ГЗДА), пуриннуклеозидфосфорилазы (ПНФ) и гуанозинфосфорилазы (ГФ) в лизатах лимфоцитов и плазме крови больных ревматоидным артритом (РА) и реактивным артритом (РеА) с целью повы-шения качества дифференциации этих заболеваний. Материалы и методы. Под наблюдением в условиях стационара наблюдались 80 больных РА и 54 больных РеА. Группа больных РА была представлена 57 (71,3%) женщинами и 23 мужчинами. Средний возраст больных 42,5±0,9 лет. В группу больных РеА вошли 36 мужчин и 18 женщин. Средний возраст больных 31,9±1,0 год. Урогенный РеА определялся у 30 больных (триггерная инфекция – Сhlamidya Trachomatis), энтерогенный РеА – у 24 больных (триггерная инфекция – Yersinia enterocolitica). Определение активности ГДА, ГЗДА, ПНФ и ГФ в лизатах лимфоцитов и плазме крови больных и 30 здоровых лиц проводилось по оригинальным методикам. Результаты исследования. По сравнению со здоровыми, у больных РА в плазме выше активность ГДА, ПНФ, ГФ (все р<0,001) и ниже ГЗДА (р<0,01), в лимфоцитах выше активность ГЗДА (р<0,001), ГФ (р<0,01), ниже ГДА (р<0,001) и ПНФ (р<0,05); у больных РеА в плазме выше активность ГДА, ПНФ, ниже ГЗДА и ГФ (все р<0,001), в лимфоцитах статистически зна-чимых энзимных различий не определялось (р<0,05). У больных РеА, по сравнению с больными РА, в плазме ниже активность ГДА, ПНФ, ГФ (все р<0,001) и незначительно выше активность ГЗДА (р>0,05), в лимфоцитах выше активность ГДА (р<0,001), ПНФ (р<0,05), ниже ГЗДА (р<0,001) и ГФ (р<0,01). Заключение. Определение активности ГДА, ГЗДА, ПНФ и ГФ в плазме и лизатах лимфоцитов больных РА и РеА в комплексе с клиническими данными способствует дифференциации этих заболеваний. Мозговая Е.Э., Стажаров М.Ю., Мартемьянов В.Ф, Евдокимова Е.В., Зборовская И.А.ЭНЗИМНЫЕ РАЗЛИЧИЯ В ЛИЗАТАХ ЛИМФОЦИТОВ БОЛЬНЫХ РЕАКТИВНЫМ АРТРИТОМ И ПОДАГРОЙ
ФГБУ «НИИ КиЭР» РАМН, кафедра госпитальной терапии ВолгГМУ Цель исследования. Выявление особенностей активности энзимов гуа-ниндезаминазы (ГДА), гуанозиндезаминазы (ГЗДА), пуриннуклеозидфосфо-рилазы (ПНФ) и гуанозинфосфорилазы (ГФ) в лизатах лимфоцитов больных реактивным артритом (РеА) и подагрой для использования этих энзимных показателей в дифференциации заболеваний. Материалы и методы. Под наблюдением находились 54 больных РеА, из которых 36 (66,7%) мужчин и 18 женщин. Средний возраст (M±m) боль-ных – 31,9±1,0 год. Длительность болезни – 9,39±0,9 месяцев. Урогенный РеА определен у 30 (55,6%), энтерогенный – у 24 больных. Диагноз РеА устанавливался в соответствии с диагностическими критериями IV Международного совещания по РеА в Берлине (1999г.) также в условиях стационара наблюдались 42 больных подагрой, из которых 39 (92,9%) мужчин и 3 женщины. Средний возраст больных 53,1±2,2 года. Интермиттирующая форма отмечалась у 15 (35,7%), хроническая – у 27 больных. Активности ГДА, ГЗДА, ПНФ и ГФ в лизатах лимфоцитов определялись по оригинальным методикам и выража-лись в нмоль/мин/мл, содержащим до лизиса 1х107 клеток. Результаты исследования. По сравнению со здоровыми, в лизатах лимфоцитов больных РеА статистически значимых энзимных различий не определялось: незначительно выше активность ГЗДА, ГФ, ниже ПНФ (все р>0,05); у больных подагрой ниже активность ГДА (р<0,001), ГФ (р<0,01), выше ГЗДА (р<0,05) и ПНФ (р<0,01). Сравнительные исследования показа-ли, что у больных РеА, по сравнению с больными подагрой, в лимфоцитах выше активность ГДА, ГФ (все р<0,001), ниже активность ПНФ (р<0,001) и незначительно ниже ГЗДА (р>0,05). Заключение. Определение активности ГДА, ГЗДА, ПНФ и ГФ в лизатах лимфоцитов в комплексе с клинико-инструментальными данными способ-ствует дифференциации реактивного и подагрического артрита. Ненашева Т.М.ХРОНИЧЕСКИЙ ПОДАГРИЧЕСКИЙ АРТРИТ
ГБОУ ВПО СГМУ им.Разумовского Минздрава России, Саратов Ведущим клиническим проявлением подагры считается артрит, патогно-моничный синдром которого – резчайшая боль с функциональными потерями. В связи с распространенностью подагры и прогностической значимо-стью раннего распознавания и адекватного лечения суставного синдрома Целью исследования явилось изучение контингента болеющих, особенностей течения суставного синдрома и частоты диагностических ошибок при подагре. Материал и методы. В работе использованы материалы результатов обследования 364 больных первичной подагрой. Диагноз подагры ставился на основании клинико-лабораторных проявлений, верифицирован с помо-щью диагностических критериев. И у всех больных (100%) был определен-ным. Среди обследованных больных было 353 мужчины и 11 женщин. Больных подагрой с отягощенной наследственностью было 45 человек. Кон-трольную группу составили 100 больных деформирующим остеоартрозом. Полученные результаты. Изучался профессиональный состав больных: работников умственного труда было 78 человек (21,5%), администра-тивных работников 58 (16,1%), лиц, работающих в организациях общепита 27 (7,4%), работников, труд которых связан со стрессом (испытатель, дис-петчер и др.) 47 (12,8%). 315 пациентов осуществляли трудовую деятель-ность, 82 человека являлись пенсионерами (22,5%,) – остальные 50 – (13,7%) – инвалидами. Рецидивы артрита возникали от 3-4 до 12 и более раз в год. В большин-стве случаев число приступов колебалось от 3 до 7 (у 244 больных), а у 58 пациентов было более 8 обострений в год. Продолжительность приступов была от 2 до 5-6 недель. Больные хроническим подагрическим артритом от-личались большим стажем заболевания, частыми и длительными суставными атаками. Как следствие длительного заболевания подагрой у 54 больных имел место вторичный остеоартроз, главным образом суставов нижних ко-нечностей. Вторичный деформирующий остеоартроз еще более снижал тру-доспособность пациентов и их способность к передвижению. Больные хро-ническим подагрическим полиартритом без развития вторичного тяжелого артроза могли довольно долго сохранять трудоспосбность (20-25 лет). У 33 больных хроническим подагрическим артритом выявлен спондилез различ-ных отделов позвоночника. У 226 пациентов имелись тканевые отложения мочевой кислоты в виде четко ограниченных узлов (тофусов) различной величины и локализации. Длительность промежутка от первой атаки до появления симптомов хрониче-ского полиартрита с формированием тофусов весьма вариабельна и состав-ляет в обследуемой группе больных в среднем 5-10 лет. Всем больным проводилось рентгенологическое исследование поражен-ных суставов в стандартных проекциях. Типичная для подагры деструкция эпифизов: краевые кистовидные просветления с четким внутренним конту-ром, симптом «пробойника» были выявлены у 303 больных. У 313 пациентов определялось утолщение мягких околосуставных тканей. У 192 наблюдав-шихся отмечены неспецифические изменения в виде сужения суставной ще-ли, ремоделирование суставных поверхностей. У 54 больных подагрой наблюдались признаки выраженного остеоартроза и при рентгенологическом исследовании определялось резкое сужение су-ставной щели, выраженные краевые остеофиты и ремоделяция суставных поверхностей. При обследовании больных использовался радиоизотопный метод иссле-дования- сцинтиграфия суставов. Сцинтиграфия суставов выявляла увели-чение интенсивности счета радиофиксирующего препарата, асимметричный, повышенный и неравномерный его захват костной тканью пораженных су-ставов. Анализ морфологических исследований биоптатов синовиальной оболоч-ки пораженного сустава проведен 10 больным. У шести человек в субинти-мальном слое синовиальной оболочки, чаще в ворсинках при микроскопиче-ском исследовании в поляризующем свете отмечено свечение мелких ли-нейных масс мочекислых соединений. Отложения уратов представляли собой узелки, в центре которых находится скопление игольчатых кристаллов аморфных масс. Вокруг отложений формируется клеточный инфильтрат, со-стоящий из макрофагов, лимфоцитов, гигантских клеток, единичных нейтрофилов. Эти образования по своей структуре близки к подагрическим тофусам, но имеют меньшие размеры. Отмечена гиперплазия ворсин проли-ферация синовиоцитов. В синовиальной оболочке в анализированных случа-ях установлен периваскулярный отек, периваскулярная клеточная инфиль-трация с периваскулярным склерозом и продуктивные, а также продуктивно-деструктивные васкулиты. Во всех случаях установлено изменение сосудов: эндотелий сосудов набухший, слабо пролиферирует, стенки сосудов утолще-ны и отечны, имеют место фибриноидные изменения. Обсуждение. Проведенные исследования показали рецидивирующий характер течения артрита, его продолжительность, необходимость проведе-ния дополнительных методов обследования: рентгенографию суставов, сцинтиграфию и в сложных случаях гистологическое исследование биоптата синовиальной оболочки. Диагностика подагры у значительного большинства больных была неудовлетворительной. В первый год болезни правильный диагноз установлен лишь у 31 больного (8,7%). В первые пять лет болезни диагноз подагры установлен у 251 больного (69,1%), а у 81 пациента (22,2%) спустя 10 лет после дебюта подагры. Больные направлялись в кли-нику с разными диагнозами. Так с ревматоиднм артритом поступило – 70 пациентов, реактивным артритом -18, с рожистым воспалением – 10, деформирующим остеоартрозом -24, болезнью Бехтерева – 8, ревматической ли-хорадкой- 5, остеомиелитом – 3, подвывихом голеностопного сустава – 6, остеохондрозом позвоночника -3. В единичных случаях диагностировался тромбофлебит глубоких вен -2, инфекционное заболевание -2, системные поражения соединительной ткани -2, флегмона -2, облитерирующий эндар-териит с развитием гангрены 1 пальца правой стопы-1. Выводы. Диагностика подагрического артрита остается неудовлетвори-тельной. Суставной синдром неоднократно рецидивирующий в течение года требует исследования концентрации мочевой кислоты в сыворотке крови. Необходима информированность врачей о возможных клинических проявле-ниях суставного синдрома при подагре и его «масках». Оранский С.П., Елисеева Л.Н., Давыдова А.Ф., Семизарова И.В.СЫВОРОТОЧНАЯ КОНЦЕНТРАЦИЯ КОРТИЗОЛА ПРИ КУРСОВОМ ПРИМЕНЕНИИ РИТУКСИМАБА У ПАЦИЕНТОВ С РЕВМАТОИДНЫМ АРТРИТОМ
ГБОУ ВПО Кубанский государственный медицинский университет Министер-ства здравоохранения России, Краснодар, Российская Федерация Ревматоидный артрит (РА) является одним из наиболее частых хрониче-ских аутоиммунных заболеваний, как в мире, так и в России. Известно, что течение РА характеризуется неуклонным прогрессированием и высокой ча-стотой тяжелых инвалидизирующих осложнений. В настоящее время приме-нение генно-инженерных биологических агентов является наиболее эффек-тивным вариантом терапии РА и рекомендовано к применению ведущими мировыми профессиональными ассоциациями, в то же время до сих пор от-сутствуют доступные Методы ранней оценки возможной эффективности тако-го лечения. Разработка таких методов при РА является чрезвычайно важной прикладной клинической задачей в связи с высокой стоимостью данного ви-да терапии. В последние годы появились данные об угнетении эндогенной продукции кортизола при РА на фоне высокой активности РА, что расцени-вается как важный прогностический фактор. В то же время динамика про-дукции кортизола на фоне применения базисных препаратов и, в частности, биологических агентов, изучена недостаточно. Целью настоящей работы явилась оценка сывороточной концентрации кортизола при курсовой терапии ритуксимабом при РА. Материалы. Верификация диагноза РА проведена в соответствии с крите-риями ACR (1987) и ACR/EULAR (2010). В основную группу были включены 25 пациентов (3 мужчин и 22 женщины) с серопозитивным РА средней и вы-сокой степени активности в возрасте 44,5 (27,4; 60,2) лет, с длительностью заболевания 6,4 (4,2; 7,9) лет. Ритуксимаб применялся на фоне продолже-ния терапии метотрексатом в дозе 10-15 мг в неделю. Применение ритуксимаба осуществлялось согласно существующим рекомендациям – первый курс – 1000 мг в/в капельно медленно 1 раз в 2 недели и повторный курс – через 6 мес. – 2 инфузии. Полный курс (4 инфузии) выполнен 23 пациентам, 2 пациентам повторное введение препарата не проводилось в связи с наличи-ем вирусных инфекций (в одном случае – респираторная вирусная инфек-ция, в другом – герпервирусная). В качестве контрольной использовалась группа из 25 относительно здоровых лиц, рандомизированная с основной группой по полу и возрасту. Из исследования исключались пациенты РА с сопутствующими инфекционными и онкологическими заболеваниями любой локализации, а также почечной, печеночной, сердечной недостаточностью, а также непереносимостью метотрексата или ритуксимаба. Забор венозной крови выполнялся в исходном состоянии, а также после первого и второго курса лечения ритуксимабом. Методы. Определялся индекс активности заболевания DAS28. Сыворо-точная концентрация С-реактивного белка (СРБ), ревматоидного фактора (РФ) оценивалась с помощью биохимического анализатора Siemens Advia 1800. Сывороточная концентрация кортизола определялась с помощью им-муноферментного анализатора Statfax 2100 с использованием готового набо-ра реактивов производства компании «Алкор-Био» (Россия). Результаты и обсуждение. Нами произведена оценка влияния инфлик-симаба на изучаемые показатели в зависимости от ответа на препарат, опре-делявшийся по рекомендуемым EULAR критериям. Среди пациентов, вклю-ченных в данное исследование, хороший клинический эффект зафиксирован у 16 пациентов (64%), умеренный – у 6 (24%) и отсутствие эффекта – у 1 пациента (4%). Установлено, что до применения препарата исследуемые показатели в группе пациентов с хорошим эффектом статистически значимо не отличались от таковых в группе с умеренным эффектом и его отсутстви-ем. Вне зависимости от ответа на терапию у всех пациентов индекс DAS 28 и показатель СОЭ прогрессивно снижались после первого курса с сохране-нием эффекта ко второму. Показатели сывороточной концентрации СРБ и РФ устойчиво снижались уже после первого курса в группе с хорошим ответом на терапию с сохранением эффекта и после второго курса; в группе же с умеренным эффектом или его отсутствием – не отмечалось значимой дина-мики указанных маркеров. Нами установлена гетерогенность сывороточной концентрации кортизола в зависимости от ответа на препарат. Так, в группе пациентов с хорошим ответом на ритуксимаб исходная концентрация корти-зола – 167,3 (99,2; 278,0) нмоль/л была ниже чем в контрольной группе – 379,8 (232,4; 498,9) нмоль/л, после первого и второго курса терапии отме-чалось статистически значимое увеличение показателей – до 293,3 (203,4; 374,3) и 329,3 (249,2; 410,3) нмоль/л соответственно. В группе же пациен-тов с умеренным эффектом от терапии или его отсутствием не регистрирова-лись отличий показателя концентрации кортизола с контрольной группой, а также динамики на фоне лечения. Механизм изменения продукции кортизо-ла на фоне антицитокиновой терапии детально не исследован, хотя, имеются отдельные указания, что провоспалительные цитокины способны угнетать конвертазы стероидных гормонов в клетках надпочечников. Выводы. Таким образом, установленный нами факт гетерогенности сы-вороточной концентрации кортизола в зависимости от ответа на ритуксимаб, может быть использован для выработки индивидуального плана лечения биологическими агентами, когда целевой группой для их применения могут стать пациенты с исходно сниженной продукцией данного гормона. Осипянц Р.А., Каратеев Д.Е., Панасюк Е.Ю., Лукина Г.В., Смирнов А.В., Глухова С.И., Александрова Е.Н., Волков А.В., Насонов Е.Л.СРАВНИТЕЛЬНЫЙ АНАЛИЗ АРТРОСОНОГРАФИИ КИСТЕЙ У ЗДОРОВЫХ ДОБРОВОЛЬЦЕВ И ПАЦИЕНТОВ С РЕВМАТОИДНЫМ АРТРИТОМ В МОСКОВСКОЙ ПОПУЛЯЦИИ
Центральная клиническая больница №1 ОАО «РЖД», ФГБУ «НИИР» РАМН, Москва, Россия Ревматоидный артрит (РА) остается важнейшей медицинской и социаль-но-экономической проблемой во всем мире. В современной ревматологии имеются достаточное количество исследований, направленных на оценку патологических изменений в суставах при РА с помощью высокочувствитель-ных методов визуализации, в частности, артросонографии. Показано, что комплексный алгоритм обследования больных РА является перспективным направлением в области улучшения качества диагностики и выбора страте-гии терапии. Вместе с тем знания нормы необходимы для правильной интер-претации патологического процесса. Цель исследования. Изучить частоту встречаемости субклинического синовита и костных эрозий в суставах кистей по данным ультразвукового (УЗ) – исследования в популяции здоровых добровольцев и определить диа-гностическую значимость артросонографии у больных РА. Материалы и методы. В исследование были включены 36 практически здоровых лиц (30 – женщин и 6 – мужчин) в возрасте от 20 до 79 лет (медиа-на 36,5 [30,5;49] лет). Основным критерием включения являлось отсутствие в анамнезе воспалительных заболеваний суставов. В качестве группы срав-нения были обследованы 46 больных c диагнозом РА (ACR, 1987), медианой возраста 48,5 [39;55] лет и длительности болезни – 5,3 [2;8] года. Всем участникам осуществлялась артросонография кистей (суставы запястья, I-V пястно-фаланговые суставы) на аппарате LOGIQ 9 с мультичастотным ли-нейным датчиком более 10 MHz в режимах «серой» шкалы и энергетическо-го допплера для верификации синовита согласно OMERACT (the Outcome Measures in Rheumatology Clinical Trials). Оценка деструктивных изменений (костных эрозий) проводилась качественным методом (наличие/отсутствие). Дефект костной ткани, визуализируемый в 2 перпендикулярных срезах, ши-риной более 2 мм и глубиной более 1 мм, указывал в пользу УЗ – эрозии. Результаты исследования. Признаки синовита по данным В-модальной сонографии («серая» шкала) в основной группе наблюдались в 30% (22/72; n=18) в суставах запястья и в 25% (94/360; n=31) – в ПФС, что достоверно реже (p<0,0001), чем у больных РА: 87% (80/92; n=45) и 56% (259/460; n=44), соответственно. В большинстве случаев (86%) у здоровых участников выраженность синовита была минимальной, в то время как при РА преобла-дала умеренная и высокая активность воспалительного процесса (78%, p<0,0001). В целом частота диагностически значимого синовита (2 и 3 сте-пени) в группе здоровых лиц, в сравнении с больными РА, была существенно ниже как в суставах запястья (11 и 76%; p=0,01), так и в ПФС (19 и 74%; p<0,01). По результатам энергетического допплера гиперваскуляризация синовии выявлялась в запястных суставах с частотой 6,9% (5/72; n=5) в основной группе против 46% (42/92; n=42) – в группе сравнения (p<0,0001). Васкуляризации допплера в ПФС у здоровых лиц не наблюда-лось, в отличие от группы РА (0 и 50%; p<0,0001). Не отмечено значимой взаимосвязи возраста участников с наличием синовита по данным соногра-фии. Напротив, здоровые добровольцы с УЗ-признаками синовита были не-достоверно младше, чем лица без таковых (медиана возраста 34,5 [27;42] и 39 [34;59] лет; p=0,09, соответственно). Анализ частоты встречаемости деструктивного процесса позволил уста-новить наличие эрозивных изменений в основной группе – в 8,3% (3/36) случаев в костных структурах запястий и в 0,3% (1/36) – в ПФС, что оказа-лось достоверно реже, чем в группе РА, где УЗ-эрозии выявлялись более чем у 90% пациентов (p<0,0001). Обсуждение/Выводы. Полученные результаты подтверждают тот факт, что изолированные признаки синовита и костных эрозий при УЗИ кистей вы-являются с достаточно высокой частотой в популяции здоровых доброволь-цев. Однако наличие диагностически значимого синовита (2 и 3 степени) и более 1 случая костных эрозий по данным сонографии, по-видимому, могут рассматриваться как патологические изменения наиболее характерные для пациентов с воспалительными артропатиями. Таким образом, артросонография кисти – высокочувствительный и до-ступный неинвазивный метод оценки синовиального воспаления и костных эрозий, который может быть использован в дополнение к стандартным ме-тодам диагностики РА в ежедневной практике ревматолога и в рамках раз-личных клинических исследований. Парамонова О.В., Русанова О.А., Емельянов Н.И., Гонтарь И.ПОЦЕНКА ТИРЕОИДНОЙ ДИСФУНКЦИИ У БОЛЬНЫХ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКОЙ
ФГБУ НИИ КиЭР РАМН; кафедра госпитальной терапии ВолгГМУ, г. Волгоград Ассоциация системной красной волчанки (СКВ) и аутоиммунных заболе-ваний щитовидной железы в настоящее время имеет хорошие подтвержде-ния, в том числе и тем, что оба заболевания ассоциированы с HLA-DR3. По данным недавнего исследования 300 пациентов с СКВ, у 5,7% из них был выявлен аутоиммунный гипотиреоз, у 1,7% – болезнь Грейвса, у 14% – носи-тельство антитиреоидных антител. Суммируя предшествовавшие исследова-ния, в которых изучалась распространенность гипотиреоза при СКВ, автора-ми работ было показано, что этот показатель составил в среднем 3,9 – 23%, а распространенность тиреотоксикоза – до 10,9%. Таким образом, скринин-говая оценка функции щитовидной железы (ЩЖ) у пациентов с СКВ вполне оправдана. По данным исследования 2009 года, проведенного Heba Sayed Assal, па-циенты с СКВ часто имеют изменения в сыворотке уровня тиреоидных гор-монов, что проявляется тиреоидной дифункцией: очень низкая концентра-ция общего и свободного Т3, низко-нормальная концентрация общего Т4, повыщенный уровень свободного Т4. ТТГ же в нормальных или субнормаль-ных значениях. Это состояние носит название ESS – синдром (euthyroid sick syndrome). Цель. Нами был изучен гормональный тиреоидный статус пациентов с СКВ, находящихся на стационарном лечении в ревматологическом отделении ГУЗ ГКБ СМП №25. Материалы и методы. Было обследовано 30 больных системной крас-ной волчанкой. По данным анамнеза средний возраст больных на начало заболевания составил 28,39±10,06 лет. Практически у половины наблюдае-мых (у 43,40%) дебют заболевания приходился на возрастной промежуток от 21 до 30 лет. Средняя длительность заболевания у больных СКВ составила 7,81,34 лет. Активность СКВ оценивалась по шкале SLEDAI. В исследуемой группе высокая (III) степень активности патологического процесса отмеча-лась у 7,3% больных, средняя (II) – у 52,0 %, низкая (I) – у 40,7% пациен-тов. По шкале SLEDAI активность заболевания в среднем составила 22,160,56 баллов. Для оценки кумулятивного повреждения, т.е. поражения орга-нов и систем, накопленного за период болезни, использовали индекс повре-ждения SLICC/ACR DI. Средний показатель индекса повреждения SLICC/ACR DI у обследованных больных составил 2,39±0,16 баллов. У всех обследован-ных выявлены различные свойственные СКВ системные проявления. Практи-чески у всех больных на момент обследования отмечались различные кож-ные проявления, чаще в виде эритемы лица, шеи, груди (54,3%), поражения суставов (у 63,7%), почек (у 68,6%), легких (57,1%), крови (71,4%), конституциональные нарушения (56,1%), синдром Рейно (63,8%). Почти у трети больных имелся антифосфолипидный синдром (27,6%). У пациентов прово-дили определение уровня ТТГ, св. Т4 и св. Т3 с помощью коммерческих RIA kits (AMERLEX-MAB FT) ИФА – наборов. Результаты и обсуждение. У обследованных нами больных с СКВ на основании комплексного клинико-лабораторного обследования какие-либо изменения ЩЖ выявлены у трети пациентов 31,4%, (p=0,0001), что было достоверно выше общепопуляционного значения. Среди тиреоидной патоло-гии у данных пациентов аутоиммунный тиреоидит (АИТ) констатирован в 18,1%; у 15,2% пациентов диагностирован узловой зоб – 1-й и 2 – й степе-ни; в единичных случаях отмечался диффузный зоб – 1 (3,5%), смешанный зоб – 2 (7%). Таким образом, доминирующей патологией ЩЖ при СКВ ожи-даемо оказался АИТ, что подтверждается данными литературы: по данным Biro E. с соавт., 2006 г., распространенность тиреоидита Хашимото при СКВ оказалась в 90 раз выше, чем среди населения в целом. С функциональной точки зрения у больных СКВ с тиреоидной патологией отмечалась преимущественно сниженная (57,6%) и, реже, нормальная функция ЩЖ (42,4%). Гипотиреоз был чаще субклинический (24,2%) и лег-кой степени (18,2%), реже – средней степени тяжести (15,2%). Гиперфунк-ции ЩЖ у наших больных не было выявлено. Снижение функции ЩЖ отме-чалось исключительно у больных с АИТ; все пациенты, имевшие различные формы зоба, были эутиреоидны. Данные о дисфункции щитовидной железы при СКВ не являются оконча-тельными и имеют в литературе противоречивые результаты. Тем не менее, пациенты с большей клинической активностью и тяжестью СКВ имеют суще-ственные изменения в гипоталамо-гипофизарно-тиреоидной системе, даже при отсутствии клинически выраженных заболеваниях щитовидной железы. Так как СКВ является полисистемным аутоиммунным заболеванием, при ко-тором может поражаться любой орган – мишень, некоторые авторы выдвига-ют гипотезу о том, что сочетанная аутотиреоидная патология может являться следствием антитиреоидной активности какой – либо группы АТ, продуциру-емых при СКВ. Не исключено, что аутотиреоидная патология – результат иммунного повреждения щитовидной железы при СКВ, сопровождающегося отложением иммунных комплексов. Выводы. Таким образом, всем больным системной красной волчанкой необходима клиническая оценка поражения щитовидной железы с обязательным определением гормонов щитовидной железы (ТТГ, Т3 и Т4), антити-реоидных антител, а также ультразвуковых параметров органа для своевре-менного выявления тиреоидной патологии и назначения лечения для предотвращения формирования гипотиреоза. Кроме того, клинико-лабораторное и инструментальное обследование щитовидной железы при СКВ необходимо проводить в комплексе в связи с латентностью течения этой патологии, а также в динамике. Петров А.М.РЕЗУЛЬТАТИВНОСТЬ ДЕЯТЕЛЬНОСТИ ГОСУДАРСТВЕННЫХ МЕДИЦИНСКИХ УЧРЕЖДЕНИЙ
Кафедра экономической теории МГМСУ, г. Москва Цель работы: рассмотреть методику оценки результативности деятельно-сти медицинских учреждений. Задачи работы: изучить теоретические основы результативности дея-тельности медицинских учреждений, проанализировать различные виды результативности здравоохранения, рассмотреть некоторые проблемы оцен-ки результативности деятельности государственных медицинских учрежде-ний, проанализировать методику расчета показателей оценки результативности деятельности государственных медицинских учреждений для форми-рования их рейтинга. Методы работы: Проанализированы отраслевые показатели, а также, научные статьи, посвящённые данной проблеме. Исследованы возможные негативные и позитивные факторы, влияющие на оценку результативности деятельности медицинских учреждений. Результаты: Результативность – степень достижения положительных итогов, вне связи с затратами на их осуществление. Медицинская результа-тивность определяется общими показателями исхода (выздоровление; улучшение; без перемен; ухудшение; смерть) и специальными показателями (показатели результативности для отдельных специальностей: участковые врачи, ревматологи, кардиологи, неврологи, хирурги и т.д.). Социальная результативность заключается в микросоциальных (удовле-творенность населения медицинской помощью, которая может быть выявле-на системой контроля внутри учреждения при проведении анкетного опроса пациентов) и макросоциальных показателях (уровень смертности, рождае-мости, средней продолжительности жизни). Экономическая результативность определяется показателями результа-тивности работы здравоохранения в целом (показатели младенческой смерт-ности, показатели материнской смертности и др.); показателями результа-тивности инвестиционных программ; показателями результативности финан-сирования (насколько полно и качественно используются средства). Результативность и эффективность медицинской помощи могут находить-ся как в прямой, так и в обратной зависимости. Это связано с действием двух групп факторов: 1. Влиянием на исход лечения индивидуальных осо-бенностей больного. 2. Отличиями в оценке эффективности на различных уровнях предоставления медицинской помощи. Для формирования рейтинга учреждений Министерства здравоохранения Российской Федерации была создана новая методика расчета показателей оценки результативности их деятельности. Данная система рейтингования предусматривает сведение в едином рейтинге медицинской, социальной и экономической результативности деятельности медицинских учреждений. В то же время эти составляющие могут вносить неравнозначный вклад в фор-мирование общей рейтинговой оценки, и предположительно в ряде случаев их суммация может замаскировать качество медицинской помощи, оказываемой учреждением. Заключение. В связи с вышеизложенным представляется целесообразным рассмотреть возможность разработки отдельных рейтингов для каждого вида результативности с увеличением количества оценочных показателей, а также выделения в отдельный рейтинг учреждений высшего профессиональ-ного образования, клиниками которых оказывается медицинская помощь населению. Полякова Ю.В., Симакова Е.С., Сивордова Л.Е., Заводовский Б.В.ИССЛЕДОВАНИЕ УРОВНЯ АДИПОКИНОВ – СОВРЕМЕННЫЕ АСПЕКТЫ ПАТОГЕНЕЗА ОСТЕОАРТРОЗА
ФГБУ «НИИ КиЭР» РАМН, Волгоград, Россия В последние годы изменился взгляд на патогенез остеоартроза (ОА) – од-ного из наиболее распространенных заболеваний костно-мышечной системы. Наряду с хорошо изученными факторами патогенеза ОА все большее внима-ние ученых привлекают провоспалительные цитокины и адипокины – гормо-ны жировой ткани. В качестве пускового фактора повышения активности адипоцитов рассматривают абдоминальное ожирение, приводящее к разви-тию метаболического синдрома с изменением чувствительности перифериче-ских тканей к инсулину, гиперинсулинемией, нарушением углеводного, ли-пидного и пуринового обмена. Дисбаланс адипокинов может приводить к преждевременному повреждению хрящевой ткани. Адипокин обладает про-тивовоспалительными, антиатерогенными и антидиабетическими свойствами, хондроциты имеют рецепторы к адипонектину. Резистин, лептин и висфатин напротив обладают провоспалительными свойствами и активно влияют на синтез целого ряда цитокинов, отвечающих за развитие острых и хрониче-ских воспалительных реакций, активного ангиогенеза в зоне хронического воспаления и образования недифференцированных клеток. Цель: повышение качества диагностики, лечения, уточнение отдельных звеньев патогенеза остеоартроза (ОА) путем исследования уровня адипонек-тина, резистина, лептина и висфатина в сыворотке крови пациентов. Материалы и методы: обследовано 80 пациентов с ОА и 50 практиче-ски здоровых лиц. Комплекс лабораторных тестов включал общий анализ крови, общий анализ мочи, общего билирубина крови, уровня трансаминаз, креатинина, мочевины, мочевой кислоты, липидов крови, показатели глике-мии натощак и постпрандиальной гликемии, уровень базального и стимулированного С-пептида, общего белка, С-реактивного протеина, иммунологи-ческих показателей (циркулирующих иммунных комплексов, ревматоидного фактора, иммуноглобулинов A, M, G). Уровень адипокинов определялся не-прямым твердофазным иммуноферментным методом с использованием ком-мерческих тест систем (Bio Vendor, cat № RD195023100 для определения уровня адипонектина, Bio Vendor, cat № RD191016100 – уровня резистина, DBC Inc cat № CAN-L-4260 – уровня лептина и RaiBiotech, cat № EIA-VIS-1 – уровня висфатина) до и после лечения. Инструментальные методы обследо-вания включали электрокардиографию, рентгенографию органов грудной клетки, рентгенографию и ультразвуковое исследование пораженных суста-вов, мониторинг артериального давления и пульса. Результаты: пониженный уровень адипонектина был у 28 пациентов, высокий уровень резистина – у 31, лептина – у 26 и висфатина – у 23 паци-ентов, что достоверно чаще, чем у здоровых лиц. Не обнаружено достовер-ной разницы уровней определяемых адипонектинов в зависимости от пола пациентов с ОА. Уровень резистина и лептина у пациентов с метаболическим синдромом (средний ИМТ=36,8±3,3, соответствует ожирению II ст.) был до-стоверно выше, чем у пациентов без метаболического синдрома. Низкий уровень адипонектина, высокий уровень резистина, лептина и висфатина обнаружен у пациентов с ОА и реактивным синовитом, рентгенологической стадией III-IV, функциональной недостаточностью суставов III. Отмечается обратная связь между уровнем адипонектина и уровнем СРБ, СОЭ и индек-сами WOMAC, индексами Лекена для гонартроза и коксартроза, прямая кор-реляция между уровнями, резистина, лептина, висфатина и уровнем СРБ, СОЭ и альгофункциональными индексами. Снижение массы пациентов на 5 кг в течение 3-х месяцев привело к достоверному снижению уровней ре-зистина и лептина, выраженности суставного синдрома, проявлений инсули-норезистентности, было отмечено снижение показателей артериального дав-ления, уменьшение частоты пульса. Выводы: полученные данные свидетельствуют о том, что для пациентов, страдающих ОА с низким уровнем адипонектина и высокими уровнями ре-зистина, лептина и висфатина характерен клинический вариант ОА с нали-чием выраженного воспалительного процесса. На фоне снижения массы тела более чем на 5 килограммов у больных с ОА отмечается уменьшение количества, интенсивности и длительности эпизодов болевого синдрома, сокращается срок временной нетрудоспособности и потребность в нестероидных противовоспалительных препаратах. Так же отмечается меньшая выраженность признаков синовита, в ряде случаев повторные обострения ОА протекают без клинических признаков синовита. Одновременно отмечается значительное положительное влияние на метаболические сдвиги: улучшаются показатели углеводного, липидного обмена, снижается уровень мочевой кислоты крови. Вероятно, на фоне комплексного влияния снижения массы тела, улучшения показателей обмена веществ, уменьшения выраженности воспалительного и болевого синдрома, а так же при уменьшении потребности в нестероидных противовоспалительных препаратах стабилизируются показа-тели артериального давления и пульса. Можно предположить, что разработка новых препаратов, влияющих на обмен адипонектинов, улучшит резуль-таты лечения ОА, снизит риски осложнений, проводимой на современном этапе терапии ОА, уменьшит показатели временной нетрудоспособности населения, позволит отсрочить сроки инвалидизации и потребности в эндо-протезировании суставов. Постникова Г.А., Немцов Б.Ф.ЦИТОСТАТИЧЕСКАЯ ТЕРАПИЯ ВТОРИЧНОГО СИСТЕМНОГО АМИЛОИДОЗА У БОЛЬНЫХ РЕВМАТОЛОГИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ
Кировская государственная медицинская академия, Кафедра госпитальной терапии; Киров, Россия Актуальность. Вторичный системный амилоидоз (ВСА) в половине случа-ев развивается на фоне хронических воспалительных заболеваний ревмато-логического профиля: ревматоидного артрита (РА), анкилозирующего спон-дилоартрита (АС), псориатической артропатии (ПА). Применение цитостати-ческих препаратов патогенетически обосновано, поскольку амилоидогенез связан с повышенным синтезом острофазовых белков-предшественников и активным участием Т- и В-лимфоцитов в процессе полимеризации амилоид-ных фибрилл. Цель: исследование эффективности применения неселективных цитоста-тиков циклофосфамида, азатиоприна и метотрексата у больных с ВСА. Материалы и методы. Исследовались истории болезней и амбулатор-ные карты 12 больных ВСА с поражением почек, средний возраст их состав-лял 52,3 ±7,5 лет. Развитию ВСА в 8 случаях предшествовал РА, в 2 – АС, в 2 – ПА. Продолжительность основного заболевания до развития ВСА состав-ляла в среднем 12,1 ±5,8 лет. 7 больных с РА получали преднизолон в дозах от 5 до 20 мг/сутки и метотрексат 7,5-10 мг/сутки; остальные – НПВС. У всех 12 больных ВСА наблюдался нефротический синдром с массивной протеину-рией, гипопротеинемией. В начале наблюдения азотвыделительная функция почек во всех случаях была сохранной: уровень креатинина сыворотки кро-ви не превышал 110 мкмоль/л. Стадию ХБП определяли согласно рекомен-дациям K/DOQI, 2002: по уровню скорости клубочковой фильтрации, вычис-ленной по формуле Кокрофта-Голта. У 10 больных обнаружена ХБП II стадии с уровнем СКФ 60-89 мл/минуту, у 2 – ХБП III стадии, СКФ 48-52 мл/минуту. Диагноз ВСА подтвержден гистологически у всех больных: в 3 случаях – по данным исследования нефробиоптата, в 9 – биоптата прямой кишки. Период от появления протеинурии до установления диагноза ВСА составил от 1 года до 6,5 лет. После уточнения диагноза ВСА назначались неселективные цито-статики: 5 больных получали ежемесячные «пульсы» циклофосфана в дозе 400-800 мг внутривенно капельно; 6 больных получали азатиоприн 100-150 мг/сутки, 1 – продолжала получать метотрексат 10 мг/неделю. Результаты. Длительность проводимой цитостатической терапии ВСА составила от 1,5 до 4 лет. В 3 случаях (2 больных РА, 1 – ПА) отмечено зна-чительное улучшение: достигнута ремиссия нефротического синдрома (протеинурия снизилась до умеренной, нормализовался общий белок крови, ис-чезли отёки). Азотвыделительная функция почек остается сохранной (пери-од наблюдения составил от 2 до 4,5 лет). Все трое получали «пульс»-терапию циклофосфаном, суммарная доза составила от 4,5 до 8 г. В 3 случа-ях на протяжении от 1 до 2,5 лет сохраняется персистирующий нефротиче-ский синдром с массивной протеинурией от 3 до 9 г/сутки, гипопротеинеми-ей, отеками; однако азотвыделительная функция почек остается нормаль-ной. 2 из них получают пульс-терапию циклофосфаном, 1 – азатиоприн. В 6 случаях цитостатическая терапия (азатиоприн, метотрексат) была отменена в связи с постепенным ухудшением азотвыделительной функции почек, в среднем через 3,5 года от начала терапии ВСА. Обсуждение. Переносимость больными цитостатической терапии была удовлетворительной, тяжелые осложнения отсутствовали. В 2 случаях на фоне лечения циклофосфамидом наблюдалось повышение уровня трансами-наз, преходящее после отмены препарата; в дальнейшем больные принима-ли азатиоприн в дозе 75-100 мг в сутки. При улучшении клинических и ла-бораторных показателей на фоне «пульс»-терапии циклофосфаном отмеча-лась нормализация уровня С-реактивного белка крови. Факторами, ухудша-ющими прогноз и достоверно ассоциирующимися с развитием хронической почечной недостаточностью (ХПН), являлись: более пожилой возраст боль-ных (более 62 лет, p=0,048) и длительный период наличия протеинурии до начала терапии ВСА (более 4 лет, p=0,048). Выводы. У 25% больных ВСА, получавших цитостатическую терапию, отмечено улучшение клинико-лабораторных симптомов. Развитие ХПН до-стоверно ассоциировалось с более пожилым возрастом и поздним началом активной патогенетической терапии ВСА. Романов А.И., Каллистов Д.Ю., Гаврилова Е.С., Романова Е.А., Сипко Г.В.РАСПРОСТРАНЕННОСТЬ И КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ РАССТРОЙСТВ СНА У ПАЦИЕНТОВ С РЕВМАТОИДНЫМ АРТРИТОМ НА ЭТАПЕ РЕАБИЛИТАЦИИ
ФГБУ «Центр реабилитации» Управления делами Президента Российской Федерации Высокая распространенность ревматоидного артрита (РА) и существенное негативное влияние этого заболевания на состояние здоровья и качество жизни людей, экономические потери общества, связанные с длительной потерей трудоспособности работниками, определяют необходимость со-вершенствования системы профилактики и реабилитации. Современные программы медико-психологической реабилитации должны учитывать раз-личные факторы, оказывающие влияние на течение восстановительного процесса; важное место среди этих факторов могут занимать и нарушения сна. Цель исследования: изучить распространенность и оценить клиниче-ское значение отдельных видов расстройств сна – хронической бессонницы, связанных со сном нарушений дыхания, двигательных нарушений сна у па-циентов с ревматоидным артритом на этапе реабилитации. Пациенты и методы: в 2003 – 2012 гг. проведено обследование 64 па-циентов (29 мужчин и 35 женщин, средний возраст – 45,3+11,2 года, ин-декс массы тела 25,2+2,5 кг/м2) с ревматоидным артритом. Пациенты нахо-дились на реабилитации в стадии ремиссии или низкой активности заболе-вания. У 23 пациентов был диагностирован серо-позитивный РА. Выявление симптомов расстройств сна проводилось при клиническом осмотре и мето-дом анкетного опроса. Количественная оценка выраженности хронической бессонницы осуществлялась с использованием Индекса тяжести бессонни-цы – Insomnia Severity Index, анализ выраженности избыточной дневной сонливости проводился в соответствие с Эпфордской шкалой сонливости (ESS). В качестве основного инструментального метода диагностики рас-стройств сна у обследованных пациентов использовалось стандартное поли-сомнографическое исследование (Grass Heritage, Comet PSG, США), ко-торое включало в себя регистрацию центрального и затылочного отведений электроэнцефалограммы, правой и левой электроокулограмм, подбородоч-ной электромиограммы, электрокардиограммы; регистрация ороназального воздушного потока осуществлялась с помощью термопары, грудного и брюшного дыхательных усилий – при помощи пьезокристаллических датчи-ков растяжения; сатурация артериальной крови – при помощи пульсоксимет-ра, двигательная активность – при помощи электромиограммы конечностей с передних большеберцовых мышц. Анализ полисомнографических записей предусматривал подсчет стадий сна, реакций ЭЭГ-активации, эпизодов ап-ноэ и гипопноэ, среднего и минимального уровней сатурации артериальной крови. Верификация диагнозов расстройств сна осуществлялась в соответ-ствие с принципами Международной классификации расстройств сна (ICSD, 2005). Результаты: различные варианты хронической бессонницы были выяв-лены у 38 пациентов, в том числе нарушения засыпания у 14 больных, нарушения поддержания сна – у 24. Индекс тяжести бессонницы в среднем по группе составил 19.3+3.4 балла. У части больных отмечались сочетания расстройств сна, в частности двигательных нарушений и хронической бес-сонницы. Учитывая многообразие изучаемых факторов и возможные внут-ренние взаимосвязи между ними, методом логистической регрессии был про-веден анализ, направленный на выявление взаимосвязи факторов риска нарушений сна и симптомов РА и позволивший количественно оценить зна-чение клинических проявлений нарушений сна. Результаты анализа свиде-тельствуют о том, что наличие нарушения засыпания и / или поддержания сна в 1.7 раза увеличивало вероятность наличия суставной боли. По данным полисомнографического исследования у пациентов с РА и хронической бес-сонницей отмечались изменения структуры сна – снижение эффективности сна и уменьшение % содержания 3 и 4 стадий медленно волнового сна, повышенная фрагментация сна. Синдром обструктивного апноэ сна (опреде-ляемый по наличию индекса апноэ-гипопноэ > 5 событий в час) был выяв-лен у 14 больных, в том числе апноэ средней и тяжелой степени – у 6 пациентов. Двигательные нарушения сна (синдром беспокойных ног, расстрой-ство периодических конечностей) выявлены у 9 пациентов; в симптоматике СБН преобладали болевые проявления. Оценка влияния расстройств сна на основные показатели реабилитации показала, что больные с хронической бессонницей и СОАС, имели большее число сопутствующих заболеваний (в средним на 35%), требовали проведения более длительных лечебно-реабилитационных мероприятий (в среднем на 3,3+2.1 койко-дня), получали больший объем медикаментозной терапии (в средним на 2,0+0,7 препарата) по сравнению с лицами без нарушений сна. На фоне применение психоте-рапевтических методик и небензодиазепиновых гипнотиков для коррекции бессонницы отмечено уменьшение выраженности субъективно оцениваемых болей в суставах у 76% больных. Обсуждение: полученные данные говорят о высокой распространен-ности расстройств сна в неоднородной группе пациентов с РА. Статистиче-ская взаимосвязь тяжести бессонницы и выраженности болевого синдрома могут свидетельствовать о формировании своего рода «порочного круга», когда болевой синдром способствует формированию бессонницы, а наруше-ния и депривация сна, влияя на центральные антиноцицептивные меха-низмы, способствуют поддержанию болевой симптоматики. Выводы: комплексные программы реабилитации пациентов с РА должны предусматривать мероприятия по диагностике и коррекции расстройств сна. Савелова Е.Е., Майко О.Ю.ДИНАМИКА УРОВНЯ С-ТЕРМИНАЛЬНЫХ ТЕЛОПЕПТИДОВ КОЛЛАГЕНА II ТИПА НА ФОНЕ ТЕРАПИИ ХОНДРОИТИНОМ СУЛЬФАТОМ У БОЛЬНЫХ ОСТЕОАРТРОЗОМ
ГБОУ ВПО Оренбургская государственная медицинская академия, Оренбург Цель: оценить в динамике уровень С-терминальных телопептидов, обра-зующихся при деградации коллагена II типа (СТХ-II), на фоне курсового лечения с использованием хондроитина сульфата у больных остеоартрозом (ОА). Материалы и методы: В исследование было включено 20 амбулаторных больных, большинство из которых (90%) составили женщины, с обострени-ем ОА коленных (n=17) и тазобедренных (n=3) суставов (по критериям R. Altman, 1991), среднего возраста 56,5 (53,5; 61,5) лет. Контрольная группа включала 20 человек без клинико-рентгенологических признаков ОА, сопо-ставимая по полу, возрасту, сопутствующим заболеваниям с основной груп-пой. Длительность заболевания составила 5 (3,5; 7,5) лет. По данным рент-генографии суставов преобладала II стадия ОА по Kellgren-Lawrence у 65% больных, реже встречались I – у 25% и III стадия – у 10% пациентов. При проведении ультразвукового исследования (УЗИ) суставов выявлены при-знаки синовита и/или тендинита у 75% больных, а у 25% пациентов отсут-ствовали воспалительные изменения в суставах. Все пациенты принимали хондроитин сульфат (структум) в дозе 500 мг х 2 раза в сутки в течение 3-х месяцев. Альго-функциональный статус боль-ных оценивали согласно интенсивности боли в покое и при ходьбе по визу-ально-аналоговой шкале (ВАШ) и выраженности функциональной недоста-точности по индексу Лекена. Для количественного определения CTX-II (в утренней порции мочи) использовали иммуноферментный тест Urine CartiLapsТМ EIA. Дополнительно определяли креатинин (ммоль/л) в этом же образце мочи. Проводили корректировку результатов с учетом концентрации креатинина по формуле: Скорректированное значение СТХ-II (нг/ммоль) = 1000 ×Urine CartiLaps (мкг/л): Креатинин (ммоль/л). Средние значения пред-ставлены в виде Ме (Q25; Q75). Результаты и обсуждение: Исходные средние значения (до начала ле-чения) CTX-II, скорректированные по креатинину, у больных ОА составили 367,1 (285,7; 420,6) нг/ммоль, которые оказались статистически значимо выше по сравнению с контролем 182,6 (134; 271) нг/ммоль (р<0,01), сопо-ставимым с общепопуляционной нормой. Анализируя исходные данные больных ОА, было выявлено, что 6 (30%) пациентов имели нормальные значения СТХ-II – 266,2 (241,4; 285,7) нг/ммоль, сопоставимые с контрольными значениями. У остальных 14 (70%) больных средний уровень был статистически значимо выше контроля и со-ставил 392,5 (362,6; 493,2) нг/ммоль. Из них 3 больных КА имели более вы-сокие средние значения СТХ-II – 384 (362,6; 783), чем при ГА – 336,3 (285,7; 405,3) нг/ммоль. Больные ОА с повышенными и нормальными значе-ниями были сопоставимы по всем клиническим показателям. Так, выражен-ность боли при ходьбе и в покое по ВАШ составила 50 (25; 67,5) и 15 (0; 30) мм соответственно в целом по группе. Значения функционального индекса Лекена – 9,5 (5; 14,5) баллов. Через 3 месяца от начала лечения у 11 (55%) больных значения СТХ-II повысились по сравнению с исходными, но не статистически значимо и со-ставили 545 (431,4; 597,9) нг/ммоль. У 9 (45%) пациентов уровень СТХ-II снизился и средние значения были 278,7 (253,5; 309,1) нг/ммоль, а у 5 больных из них достигли уровня контрольных значений – 253,5 (142,2; 278,7) нг/ммоль. Причем, пациенты, имеющие повышенные значения, были с более худшими клиническими показателями ОА, чем пациенты с понижен-ным уровнем СТХ-II. Так, боли при ходьбе и в покое по ВАШ были 45 (35; 60) и 10 (10; 40) мм соответственно против 20 (15; 30) и 5 (2; 5) мм (р<0,05). Значения функционального индекса Лекена – 9,5 (5; 14,5) против 6 (5; 7) баллов (р<0,05). Также было определено, что у пациентов с УЗ-признаками синовита и/или тендинита показатели CTX-II были статистически значимо выше, чем у больных, не имеющих признаков воспаления в суставах, и составили 384 (317; 436) против 285 (266,2; 310,7) нг/ммоль (р<0,01). Выводы: 1. У больных остеоартрозом коленных и тазобедренных суста-вов был обнаружен статистически значимо более высокий уровень С-терминальных телопептидов коллагена II типа, особенно с признаками вос-палительных изменений в суставах, по сравнению со здоровыми лицами,что, вероятно, отражает наличие деструктивных процессов в хрящевой ткани суставов. 2. Терапия хондроитином сульфатом в течение 3-х месяцев привела к снижению уровня С-терминальных телопептидов коллагена II типа до нор-мальных значений у 45% пациентов, которые имели менее выраженные боли и функциональные ограничения в суставах, по сравнению с остальными больными (55%), у которых диагностирован повышенный уровень маркера. Северина О.Г., Александров А.В., Черкашина И.В., Александрова Н.В., Ненашева Н.В., Никитин М.В.ДИНАМИКА КЛИНИКО-ЛАБОРАТОРНЫХ ПОКАЗАТЕЛЕЙ ПРИ ИСПОЛЬЗОВАНИИ ХРОНОМАГНИТОТЕРАПИИ В КОМПЛЕКСНОМ ВОССТАНОВИТЕЛЬНОМ ЛЕЧЕНИИ БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ
Санаторно-курортное учреждение Филиал «Санаторно-курортный комплекс «Вулан» ФГБУ «Российский научный центр медицинской реабилитации и курортологии», Геленджик; ФГБУ «Научно-исследовательский институт клинической и экспериментальной ревматологии» РАМН, Волгоград Поиск новых методов комплексного восстановительного лечения ревма-тоидного артрита (РА), рассчитанных на нормализацию естественных про-цессов регуляции гомеостаза, остается актуальным. Вызывает интерес эф-фективность применения метода хрономагнитотерапии на реабилитационных этапах лечения ревматических больных для нормализации естественных процессов регуляции гомеостаза и нивелирования патогенного влияния эн-догенных факторов, способствующих интенсификации свободнорадикально-го окисления и перекисного окисления липидов. Цель работы: изучение влияния метода хрономагнитотерапии на эндо-генные факторы, вызывающие нарушение пуринового метаболизма (ПМ) и антиоксидантной системы (АОС) у больных РА. Материалы и методы. Под нашим наблюдением находилось 120 боль-ных с достоверным (по критериям АCR, 1991 г.) РА (88 женщин и 32 мужчины в возрасте от 18 до 66 лет). Активность РА I степени установлена у 25%, II – у 57,5% и III – у 17,5% больных. Системные проявления заболевания были выявлены у 20 человек (16,7%). Больные РА путем случайного подбо-ра были разделены на две сопоставимые группы: основную (n=80) и кон-трольную (n=40). Пациенты обеих групп получали аналогичное медикаментозное и физиотерапевтическое лечение. Кроме того, больные основной группы получали дополнительно 10-12 ежедневных сеансов хрономагнито-терапии от аппарата «Мультимаг» (Касимовский приборный завод, г. Ря-зань). Клинико-иммунологическая оценка эффективности терапии проводилась с помощью унифицированных критериев OMERACT III и с учетом дина-мики специальных исследований, характеризующих функционирование АОС и ПМ: активность ферментов сыворотки крови – каталазы (Кат), церуло-плазмина (ЦП), ксантиндегидрогеназы (КО), аденозиндезаминазы (АДА), гуаниндезаминазы (ГДА); содержание антител (Ат) к Кат, ЦП, КО, АДА и ГДА. Антитела к ферментам ПМ и АОС выявляли твердофазным иммуноферментным анализом с использованием антигенных наносистем, для получения ко-торых применяли метод эмульсионной полимеризации в потоке газообразно-го азота с включением магнитного материала и соответствующей антигенной матрицы. Результаты. Оценка эффективности терапии по критериям ACR 20 в ос-новной группе была достоверно выше, чем в контрольной (p=0,042). В то же время, у пациентов обеих групп достоверно изменялся DAS 28 (p<0,001), но в основной группе эти изменения соответствовали 1,6 баллам (хороший эф-фект), а в контрольной – 1,2 баллам (умеренный эффект). У значительного числа больных РА при поступлении в стационар отмеча-лось угнетение ферментативной активности Кат (p=0,042), повышение ак-тивности ЦП и КО (p<0,001), практически неизмененная активность АДА (p>0,1) и тенденция к снижению активности ГДА (р=0,068). Повышенные уровни Ат к изучаемым ферментам были отмечены у 59,2% больных (для Ат к КАТ), 64,2% (для Ат к ЦП), 59,2% (для Ат к КО), 43,3% (для Ат к АДА) и 41,7% (для Ат к ГДА) больных РА. После проведенного лечения в основной группе были отмечены положи-тельные изменения практически всех изучаемых показателей (p<0,05), кро-ме (Ат к АДА и активности ГДА, p>0,05). В контрольной группе наблюдалось увеличение активности Кат (p=0,036), снижение активности ЦП (p<0,001) и уровня Ат к ЦП (p<0,001); достоверных положительных изменений других лабораторных показателей отмечено не было (р>0,05). Положительный кли-нико-иммунологический эффект применения хрономагнитотерапии может быть связан с очищением поляризованных мембран от фиксированных на их поверхности иммунных комплексов, способных дезактивировать мембранные рецепторы и затруднять клеточный метаболизм. Выводы. Включение хрономагнитотерапии (комплекс «Мультимаг») в реабилитационные мероприятия способно положительно влиять на течение метаболических реакций и степень выраженности локальных воспалитель-ных процессов у больных РА. Симакова Е. С., Сивордова Л. Е., Ахвердян Ю. Р., Полякова Ю. В., Ковех А. А., Заводовский Б. В.ОЦЕНКА УРОВНЕЙ АНТИТЕЛ К ХОНДРОИТИН СУЛЬФАТУ У ЗДОРОВЫХ ЛИЦ И БОЛЬНЫХ ОСТЕОАРТРОЗОМ В ЗАВИСИМОСТИ ОТ КЛИНИЧЕСКОЙ ФОРМЫ И СТАДИИ ЗАБОЛЕВАНИЯ
ФГБУ «НИИ КиЭР» РАМН Цель работы. Оценить средние уровни антител к хондроитин сульфату (антиХС) у здоровых лиц и больных остеоартрозом в зависимости от стадии и клинической формы заболевания. Материалы и методы. Мы наблюдали 120 больных ОА в возрасте от 21 до 65 лет (71 женщина (59,17%) и 49 мужчин (40,83%)). Группу сравнения составили 40 практически здоровых лиц. Средний возраст женщин с ОА составил 47,28±4,49 лет, мужчин – 49,18±4,73 лет и был сопоставим с группой здоровых лиц (t=0,54, p>0,05; t=0,29, p>0,05 соответственно). Из 120 больных ОА у 51 (42,5%) были клинические проявления синовита. При рентгенологическом исследовании суставов были установлены сле-дующие стадии поражения суставов: I стадия – у 36 (30%) больных, II ста-дия – у 56 (46,67%) больного, III стадия – у 28 (23,33%) больных. АнтиХС определялись непрямым твердофазным иммуноферментным мето-дом на полистироловых планшетах (ELISA-тест) по оригинальной методике с использованием в качестве антигена коммерческого препарата производства компании Sigma (США, Cat. № С-8529). Полученные результаты/обсуждение. У здоровых лиц средний геометрический титр антиХС хряща был равен 39,14+-1,19. При этом средняя оптическая плотность при разведении сыворотки 1:80 составила 0,07+-0,02. Уровень нормальных показателей антиХС, определяемый как М +- 2б, со-ставил по среднему геометрическому титру от 24,09 до 54,19, или по оптиче-ской плотности до 0,32 ед. С учетом среднеквадратичного отклонения этого ряда был сделан вывод о том, что повышенным содержанием антиХС следует считать титр сыворотки выше, чем 1:64 или среднюю оптическую плотность выше, чем 0,32 при разведении сыворотки 1:80, или средний геометриче-ский титр выше 54,19. Такие величины выявлены у 3 здоровых лиц (7,5%) случаев, что составило частоту положительных результатов для данного ряда. Среди больных ОА повышенные титры антиХС обнаружили у 99 пациен-тов (82,5%), что достоверно выше, чем у здоровых лиц (3 пациента (7,5%), (р<0,001)). При этом средний геометрический титр этих антител составил 187,67+-2,16, а средняя оптическая плотность при разведении сыворотки 1:80 – 0,36 +- 0,13. Эти показатели оказались достоверно выше, чем у здоровых лиц (p<0,01). Достоверных различий в уровне антиХС больных остео-артрозом в зависимости от пола и возраста не было. Таким образом, для больных ОА в целом характерна достоверно более высокая частота обнаружения и количественные показатели уровня антиХС суставного хряща. Чаще всего антиХС выявлялись у больных со II (54 паци-ента (96,43%)) и III стадией заболевания (26 больных (92,86%)), чем при I стадии (19 пациентов, (52,78%)), (p<0,001). В группе больных с моно- и олигоартрозом частота положительных ре-зультатов при определении антител составила 73,91%, а их средний геомет-рический титр – 147,72+-2,29. В группе больных с полиостеоартрозом частота положительных результатов составила 94,12%, при среднем геометрическом титре антител – 228,14+-2,77. Разница между представленными величинами была статистически достоверной. Так, частота положительных результатов определения антител у больных с моно- и олигоартрозом была достоверно меньше таковой при множественном поражении суставов (p<0,01). Средний геометрический титр антител к хондроитин сульфату суставного хряща у больных с поражением одного или нескольких суставов был значительно ниже, чем у больных с полиостеоартрозом (p<0,01). При явлениях вторично-го синовита антиХС выявлялись достоверно чаще (50 пациентов (98,04%)), чем без синовита (48 человек (69,57%)), (х2=15,88, р<0,0001). Выводы/заключение. Для больных остеоартрозом, в т. ч. на ранних стадиях, характерно достоверно более частое обнаружение антиХС. В срав-нении со здоровыми лицами, у пациентов с ОА определяется достоверно более высокий средний геометрический титр антиХС. Наиболее высокое со-держание антиХС характерно для больных с выраженной рентгенологиче-ской стадией заболевания (стадии I и II), а также у больных с полиостеоартрозом и синовитом. Симакова Е.С., Сивордова Л.Е., Полякова Ю.В., Кравцов В.И., Заводовский Б.В.ЭФФЕКТИВНОСТЬ НЕОМЫЛЯЕМЫХ СОЕДИНЕНИЙ БОБОВ СОИ И АВОКАДО ПРИ ОСТЕОАРТРОЗЕ В ЗАВИСИМОСТИ ОТ УРОВНЯ ОКИСЛЕННЫХ ЛИПОПРОТЕИНОВ НИЗКОЙ ПЛОТНОСТИ
ФГБУ «НИИ клинической и экспериментальной ревматологии» РАМН, ГБОУ ВПО «Волгоградский государственный медицинский университет», г. Волго-град, Российская Федерация Остеоартроз (ОА) является самым распространенным заболеванием суставов, характеризующимся хроническим прогрессирующим течением, требующим длительного лечения. В последнее годы идет интенсивный поиск новых болезнь-модифицирующих препаратов. Одним из них является экстракт неомыляемых соединений бобов сои и авокадо (Пиаскледин (Avocado and soya unsaponifiables – ASU), Expanscience, Франция). Цель исследования: повысить эффективность терапии ОА за счет уточнения показаний к применению неомыляемых соединений бобов сои и аво-кадо в зависимости от уровня окисленных липопротеинов низкой плотности (оЛПНП) и антител к ним (анти-оЛПНП) в сыворотке крови. Материалы и методы: Под нашим наблюдением находились 130 боль-ных ОА и 45 практически здоровых лиц, сопоставимых по полу и возрасту. оЛПНП и антитела к ним определялись иммуноферментным методом с ис-пользованием тест систем (Oxidised LDL, cat№20042 и OLAB-JgG, cat№20032, Biomedica Gruppe) до и после лечения. Для оценки эффективности лечения ОА оценивали счет боли, общую выраженность боли, индекс WOMAC, аль-гофункциональный индекс Лекена для гонартроза и коксартроза, индекс Драйзера для ОА кистей до и после лечения. Результаты исследования и обсуждение: Средний уровень оЛПНП в сыворотке крови здоровых людей составил 114,3+-4,2 нг/мл, анти-оЛПНП – 324+-14 мЕд/мл (везде M+-m). Уровень нормальных показателей, определяемый как М+-2б, составил для оЛПНП от 60 до 168 нг/мл, для анти-оЛПНП от 244 до 404 мЕд/мл. Частота выявления оЛПНП в сыворотке крови у здоро-вых лиц составила 4,4% (2 человека), анти-оЛПНП – 2,2% (1 человек). По-вышенный уровень оЛПНП в сыворотке крови больных ОА был обнаружен у 78 (60%), анти-оЛПНП – у 38 пациентов (29%), что было достоверно чаще, чем у здоровых лиц (р<0,001, р<0,001 соответственно). Средний уровень оЛПНП у больных ОА составил 252,2+-3,4 нг/мл, анти-оЛПНП – 484,5+-12,5 мЕд/мл, что достоверно превышало показатели здоровых лиц (р=0,0014, р<0,001 соответственно). Средний уровень оЛПНП в сыворотке крови у мужчин составил 257,6+-3,7 нг/мл, у женщин – 251,6+-3,8 нг/мл. Средний уровень анти-оЛПНП в сыворот-ке крови у мужчин составил 472,8+-13,7 мЕд/мл, у женщин – 489,8+-13,8 мЕд/мл (t=0,83, р>0,05). Таким образом, уровень оЛПНП и анти-оЛПНП в сыворотке крови больных ОА не зависит от пола пациентов. В нашем исследовании повышение уровня оЛПНП и анти-оЛПНП происхо-дило при более длительном течении ОА. Это подтверждает данные о том, что с возрастом ослабевают антиоксидантные системы и увеличивается уровень окислительных реакций. Был изучен уровень оЛПНП и анти-оЛПНП в зави-симости от клинической картины ОА. Выявлено, что оЛПНП при ОА были достоверно выше уровня здоровых лиц во всех группах, кроме ОА с рентге-нологической стадией I (р>0,05). У больных с высоким уровнем анти-оЛПНП в сыворотке крови достоверно чаще преобладал полиостеоартроз, с узелко-вой и безузелковой формой заболевания, быстропрогрессирующем течением, вторичным синовитом, с продолжительностью заболевания более 10 лет, рентгенологической стадией III и IV, с III классом функциональной недоста-точности суставов. Для того, чтобы оценить эффективность неомыляемых соединений бобов сои и авокадо при ОА в зависимости от концентрации оЛПНП и анти-оЛПНП в сыворотке крови, мы проанализировали результаты терапии в группах с их высоким и низким уровнем. Было установлено, что наилучший эффект терапии был достигнут в группе пациентов с высоким уровнем оЛПНП в сыворот-ке крови (более 168 нг/мл), где улучшение наступило в 94,8% случаев. У пациентов, имеющих нормальный уровень оЛПНП в сыворотке крови, поло-жительный результат лечения при приеме неомыляемых соединений бобов сои и авокадо был достигнут только в 62% случаев. В группе пациентов с высоким уровнем анти-оЛПНП (более 404 мЕд/мл) в сыворотке крови улучшение наступило в 94,4% случаев. У пациентов, имеющих нормальный уро-вень анти-оЛПНП в сыворотке крови, положительный результат лечения при приеме Пиаскледином был достигнут только в 63,6% случаев. Можно пред-положить, что эти вещества положительно влияют на перекисное окисление липидов, стабилизируют мембраны клеток, уменьшают патогенное действие активных форм кислорода. Наши данные показывают, что при назначении неомыляемых соединений бобов сои и авокадо пациентам с ОА контроль оЛПНП и анти-оЛПНП позволит повысить эффективность лечения этим препаратом с 77,5% до 94,8%. У пациентов с ОА и с высоким уровнем анти-оЛПНП эффективность терапии ASU повышается с 63,6% до 94,4%. Выводы: Таким образом, нарушения липидного обмена могут оказывать негативное влияние на прогрессирование ОА. Неомыляемые соединения бобов сои и авокадо наиболее эффективны у пациентов с высоким уровнем оЛПНП (более 168 нг/мл) и анти-оЛПНП (более 404 мЕд/мл) в сыворотке крови. Следовательно, мониторинг уровня оЛПНП и анти-оЛПНП позволяет повысить эффективность применения ASU при терапии ОА. Синельник Е.А., Ханов А.Г. КЛИНИКО-МОРФОЛОГИЧЕСКИЙ АНАЛИЗ СЛУЧАЯ ПЕРИОДИЧЕСКОЙ БОЛЕЗНИ ГБУ РО «Областная клиническая больница №2»,Клиническая больница №1 ФГБУЗ ЮОМЦ ФМБА России, г. Ростов-на-Дону, Россия Периодическая болезнь (ПБ) или семейная средиземноморская лихорадка — наследственное аутосомно-рецессивное заболевание, связанное с точеч-ной мутацией в гене белка пирина. Этот ген носит название MEFV (MEditerranean FeVer) и имеет порядка 29 выявленных в настоящее время вариантов мутаций. ПБ проявляется возникающими через определенные интервалы времени стереотипными приступами лихорадки, полисерозита, абдоминального и суставного болевых синдромов, лейкоцитозом и ускорен-ным СОЭ в общем анализе крови. При этом в межприступный период боль-ные чувствуют себя удовлетворительно, приспосабливаются к своему забо-леванию, подбирая лекарственные препараты для симптоматического лече-ния. Изучение ПБ актуально, поскольку частота заболевания за последние де-сятилетия растет. При этом, иногда, несмотря на очевидные клинические признаки и современные возможности диагностики, ПБ часто остается не-распознанной или имеет место её поздняя диагностика.В основе приступов ПБ является спонтанная или спровоцированная дегрануляция нейтрофилов с выбросом медиаторов и развитием асептического воспаления преимуще-ственно в серозных и синовиальных оболочках. Из избыточного количества острофазового белка SAA, различными клетками крови и соединительной ткани, синтезируется фибриллярный компонент амилоида. Так как амилоид при ПБ строится из белка SAA, амилоидоз при ПБ носит характер АА – ами-лоидоза. При АА амилоидозе почки поражаются в 100% случаев. У человека выделено несколько типов SAA, и только фрагменты некоторых из них вхо-дят в состав амилоидных фибрилл. Это, возможно, и объясняет развитие амилоидоза, по различным данным у 10–40% больных ПБ. Нами был проведен клинико-морфологический анализ летального случая периодической болезни, осложненной нефропатическим амилоидозом, у мужчины 31 года армянской национальности. Периодическая болезнь была выставлена эмпирически на втором году жизни, колхицин пациент не получал. В 24 года был выявлен нефротический синдром, выставлен диагноз амилоидоза почек и только тогда назначен кол-хицин в дозе 1 мг в сутки. С 28 лет постепенно прогрессировала хрониче-ская почечная недостаточность, на фоне которой через 3 года появилась артериальная гипертензия с эпизодами повышения артериального давления до 200/120 мм рт ст. Госпитализирован пациент был в связи с развитием анасарки, одышки и подъемами артериального давления. При поступлении и на протяжении всей госпитализации состояние оставалось тяжелым за счет рефрактерных к консервативной терапии выраженной гипергидратации, уремического отека легких, гиперкалиемии и артериальной гипертензии, которые стали нивелироваться после проведения гемодиализа. Во время операции наложения артериовенозной фистулы для продленного гемодиали-за у пациента была отмечена остановка сердца, длящаяся 5 минут. После восстановления сердечной деятельности состояние оставалось тяжелым за счет комы, периодически сменяемой оглушением и психомоторным возбуж-дением, нестабильности гемодинамики и необходимости проведения про-дленной ИВЛ, на фоне чего пациент умер от присоединившейся деструктив-ной пневмонии. При патологоанатомическом исследовании вторичный амилоидоз был подтвержден специфическим окрашиванием гистологических препаратов внутренних органов Конго-красным с последующей поляризационной микро-скопией. Макроскопически наиболее выраженные изменения были выявлены в почках – уменьшенные в размерах почки с атрофичной паренхимой с жел-товатыми включениями липидов и сальным блеском, гепатоспленомегалия с уплотнением и наличием сального блеска селезенки и печени, кардиомега-лия за счет выраженной гипертрофии миокарда, утолщение клапанов серд-ца, уплотнение и уменьшение в размерах надпочечников а так же уремиче-ский гастроэнтероколит, уремический диффузный бронхит и тотальная лево-сторонняя деструктивная пневмония. При микроскопическом исследовании так же наиболее массивные отло-жения амилоида были выявлены в почках, затем в желудочно-кишечном тракте и надпочечниках. В почках амилоид был выявлен в базальных мем-бранах канальцев, выносящих протоков, капиллярных петель клубочков, в стенках сосудов и интерстиции. Это привело к развитию вторичного тубуло-интерстициального нефрита и нефросклероза. Вторичный тубуло-интерстициальный нефрит и нефросклероз стали причиной уремии и вторич-ной артериальной гипертензии. В надпочечниках амилоид был найден в строме клубочковой и пучковой зон коры и сосудах. В органах желудочно-кишечного тракта – в стенках сосудов, подслизистой оболочке и базальной мембране покровного эпителия. Данных о наличие синдрома мальадсорбции не было. Так же амилоид был выявлен в сосудах селезенки и печени, в меньшей степени – в их строме, в интиме и медии аорты, в строме и сосудах поджелудочной и щитовидной железы, периневрии, в медии и адвентиции аорты. Поражение миокарда у данного пациента было связано в большей степени с артериальной гипертензией, гипертрофией миокарда и водно-электролитным дисбалансом, так как амилоид в сердце был выявлен лишь в небольшом количестве в сердечных клапанах и стенках мелких артерий. Смертельным осложнением, кроме уремии, у данного больного выступила деструктивная пневмония, которая стала входными воротами для сепсиса. Предложения. На примере данного случая обращает на себя внимание необходимость ранней диагностики и, соответственно, своевременное нача-ло лечения ПБ с целью максимально возможного предотвращения развития смертельного осложнения – амилоидоза. Диагноз ПБ должен быть подтвер-жден генетическим исследованием для определения конкретной мутации у данного пациента, чтобы в дальнейшем была возможность изучить особен-ности течения каждой формы мутации и строить лечебную тактику. Для этого такие пациенты должны браться на диспансерный учет и наблюдаться по схеме диспансерного наблюдения любого ревматологического или нефроло-гического заболевания с поражением почек. Подробное описание клиниче-ского случая, патологоанатомическое заключение, макро – и микропрепара-ты представлены по адресу; http://visualrheumatology.ru/periodicheskaya-bolezn.html Скрябина Е.Н., Александрова О.Л., Шаймарданова Н., Наволокин Н.А.ТУБЕРКУЛЕЗ ПРИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКЕ
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава России Сочетание двух тяжелых заболеваний – системной красной волчанки (СКВ) и туберкулеза – одна из актуальных проблем, представляющих инте-рес для фтизиатров и ревматологов. Значимость ее определяется тем, что распространенность туберкулеза среди больных ревматическими заболева-ниями, в том числе и СКВ значительно выше, чем в популяции. Смертность среди пациентов СКВ от инфекционных осложнений в последние годы зани-мает одно из первых мест в структуре летальности при этой патологии. Целью данного исследования явилось изучение особенностей течения, органной патологии и прогноза СКВ и туберкулеза при их сочетании, а также влияние глюкокортикостероидной (ГКС) терапии на развитие туберкулеза у больных СКВ. Проведен ретроспективный анализ 180 историй болезни: 175 больных с изолированной СКВ и 5 – с сочетанной патологией (СКВ в соче-тании с туберкулезом). Все больные находились на лечении в ревматологическом отделении об-ластной клинической больницы (ОКБ) г. Саратова. Проанализированы кли-нические проявления СКВ, результаты лабораторного, инструментального исследования, а также дозы и продолжительность лечения ГКС, назначавши-еся до постановки диагноза туберкулеза у этих больных. В результате исследования установлено, что среди больных СКВ тубер-кулез был выявлен у 5 из 180 пациентов (2,78%). Туберкулез в анамнезе до развития СКВ выявлялся у 1 из 5 больных с сочетанной патологией и у 3 из 175 (1,71%) с изолированной СКВ. У всех 4 пациентов обеих групп туберку-лез был выявлен на 2-5 лет раньше, чем диагностирована СКВ, что, по-видимому, свидетельствовало о снижении иммунитета у этой категории больных. Пол, возраст дебюта болезни, средний возраст не имели суще-ственного различия в анализируемых нами группах. Продолжительность СКВ также не оказывала влияния на развитие туберкулезного процесса. Следует отметить, что туберкулез при СКВ в 4 из 5 случаев развивался на фоне II-III степени активности, в одном случае – на фоне I степени активно-сти СКВ. У пациентов с изолированной СКВ в 117 случаях была выявле-на I степень активности (66,9% наблюдений), у 63 обследованных – II-III (33,1% наблюдений). Только у одной из 5 больных, находившихся на лечении в ОКБ, был вы-явлен очаговый туберкулез легких, диагностика и лечение которого особой сложности не представляли. У 4 из 5 больных был милиарный туберкулез легких. У 1 из 4 больных с милиарным туберкулезом отмечалось изолиро-ванное поражение легких; у остальных 3 пациентов наблюдалось также ту-беркулезное поражение печени, селезенки, надпочечников, мозговых обо-лочек или кишечника. Массивное поражение легких с вовлечением двух и более долей имелось у всех наших больных с милиарным туберкулезом. При этом необходимо отметить, что верхние отделы легких, поражались всего в четверти случаев. Диагностика милиарного туберкулеза, развившегося у 4 больных с СКВ, представляла большие сложности, так как клиническая кар-тина не отличалась от таковой при высокой степени активности в случаях с изолированной СКВ. В обеих группах отмечалась высокая упорная лихорад-ка, выраженная интоксикация, кожный васкулит, дерматит, артрит, панци-топения, поражение легких (плеврит, пневмонит), высокий титр антител к ДНК. Летальные исходы наблюдались только у больных СКВ, имевших наибо-лее тяжелую форму туберкулеза – милиарный туберкулез, от которого умер-ло 3 больных. У одной пациентки с милиарным туберкулезом, развившемся на фоне СКВ, была достигнута ремиссия специфического процесса, а через несколько лет – СКВ. При анализе доз и продолжительности ГКС терапии в двух рассматрива-емых группах больных получены следующие результаты. По средней про-должительности гормональной терапии существенных различий в двух сравниваемых группах не выявлено. Установлено, что среднесуточная доза ГКС, принимаемых внутрь, у больных с туберкулезом и СКВ в 2 раза пре-вышала таковую у больных с изолированной СКВ, а средняя суммарная доза ГКС, используемых в виде пульс-терапии – в 3 раза. Это свидетельствует о высокой активности и резистентности к лечению СКВ и создает предпосыл-ки для развития инфекционного процесса. Таким образом, у больных СКВ туберкулез встречался значительно чаще, чем в общей популяции. Особенностью туберкулеза, развившегося у боль-ных СКВ, являлось более частое поражение средних и нижних отделов лег-ких, в отличие от изолированного туберкулеза, поражающего, в основном, верхние доли. Туберкулез у больных СКВ развивался при наличии высокой активности, на фоне приема больших доз ГКС, чем при изолированной СКВ. Для милиарного туберкулеза, развившегося у больных СКВ, характерно бурно прогрессирующее течение, трудно отличимое от тяжелых форм изоли-рованной СКВ. При тяжелых формах СКВ, резистентных к терапии, должен вестись целенаправленный поиск для исключения туберкулезного процесса. Смирнова Л.А.. Немцов Б.Ф.СЕНСОРНАЯ НЕЙРОПАТИЯ ПРИ РЕВМАТОИДНОМ АРТРИТЕ. СВЯЗЬ С ПЕРЕКИСНЫМ ОКИСЛЕНИЕМ ЛИПИДОВ
ГБОУ ВПО Кировская ГМА г. Киров, Россия Введение/Цель. Поражение периферической нервной системы – одно из самых частых системных проявлений РА. Свободно-радикальные процессы и ПОЛ играют определенную роль в патогенезе как хрящевой деструкции, так и формировании внесуставных проявлений при РА. Цель: Изучить взаимо-связь вибрационной чувствительности (ВЧ) как проявление сенсорной нейропатии при ревматоидном артрите с перекисным окислением липидов (ПОЛ). Материалы/Методы. Обследовано 84 больных достоверным РА в соот-ветствии с критериями АРА, из них 7 (8,5%) мужчин, 77 (91,5%) женщин. Средний возраст составил 44,25±0,88 при длительности заболевания 7,2±0,69 лет. Изучение ВЧ проводили с помощью электронного биотезиомет-ра “EG-Electronic, США” по предложенной нами методике в трех точках на нижних конечностях. ПОЛ сыворотки крови изучали хемилюминесцентным методом на приборе “Биохемилюминометр БХЛ-04”. Интенсивность ПОЛ определяли по значению светосуммы за 30 сек и выражали в mv. Результаты/Обсуждение. Выявлено, что у больных РА со II и III степе-нями активности заболевания интенсивность ХЛ сыворотки крови были ста-тистически значимо выше, чем при I степени активности (р<0,05). При ана-лизе зависимости ПОЛ от степени тяжести РА установлено нарастание пока-зателей ХЛ от легкой степени к тяжелой, однако достоверные различия об-наружены только между легкой и тяжелой степенями тяжести РА (р<0,05). В группе больных с экстраартикулярными проявлениями показатели ПОЛ были значимо выше по сравнению с больными без признаков системности (р=0,008). Отдельно были проанализированы данные ХЛ у больных РА с наличием нейропатии. При этом установлено, что наличие поражения пери-ферической нервной системы сопровождалось достоверно более высокой интенсивностью ПОЛ по сравнению с группой больных без нейропатии (р=0,004) Выводы/Заключение. Среди внесуставных проявлений перифериче-ская сенсорная нейропатия, выявленная нами по показателям ВЧ, была од-ной из самых частых и обнаружена в 60% случаев, что в целом соответству-ет данным литературы. Интенсивность ПОЛ, оцененная по ХЛ сыворотки крови, связана с активностью заболевания, нарастает при РА с более тяже-лым течением заболевания и при наличии поражения периферической нервной системы. Соколов В.А, Подолинный Г.И.РАСПРОСТРАНЕННОСТЬ СИНДРОМА БОЛИ В НИЖНЕЙ ЧАСТИ СПИНЫ СРЕДИ ПОПУЛЯЦИИ ГОРОДСКИХ ЖИТЕЛЕЙ ПРИДНЕСТРОВСКОГО РЕГИОНА МОЛДОВЫ
Приднестровский государственный университет имени Т.Г. Шевченко, Рес-публика Молдова Социально значимыми из ревматических заболеваний (РЗ) прежде всего являются остеоартроз периферических суставов и позвоночника, ревматоидный артрит и синдромом боли в нижней части спины(синдром БНС), которые представляют серьезную медикосоциальную проблему и. характеризуются оражением лиц трудоспособного возраста и рано возникающей и инвалидизацией больных. Под синдромом БНС (lowback pain) (БНС) понимают симптомокомплекс, сопровождающийся болью, локализующуюся между XII парой рёбёр и ягодичными складками. Доказано, что вторичная вертебральная радикулопатия диагностируется лишь у 7 – 8% больных с люмбалгией. Постепенно сформи-ровалось мнение, что БНС – это междисциплинарная проблема, в которой наряду с неврологическими, травматологическими и ортопедическими нарушениями большое место отводиться ревматологическим аспектам. В проведённом недавно в России и Швеции популяционном исследова-нии спинальных болей среди лиц в возрасте 35-55 лет установлено, что ча-стота возникновения болей составила 65,0-66.3%. Данных о частоте синдрома БНС в Приднестровском регионе республики Молдовы в литературе обнаружено не было, это и послужило поводом для исследования. Целью исследования явилось определение частоты синдрома боли в нижней части спины и ассоциированных с ним признаков наследственной дисплазии соединительной ткани среди выборки взрослых жителей г. Тирасполя. Материалы и методы исследования. Работа является частью программы НИЛ «ИНТЕРН» ПГУ им.Т.Г.Шевченко по изучению частоты РЗ, БНС и ДСТ в Приднестровье. Для анкетирования использовалась скринирующая ан-кета, разработанная в ГУ Институт Ревматологии РАМН, которая заполнялась на каждого из 2000 взрослого жителя с 18 лет и старше, если они предъ-являли спинальные жалобы и анкета №2, разработанная в процессе исследования. Диагноз РЗ, БНС и ДСТ устанавливался по общеизвестным критериям. Проводилось рентгенологическое исследование позвоночника . Статистическая обработка результатов проводилась с использованием про-грамм «Biostat», «Statistika». Результаты и обсуждение. Ответы были получены от 1820 жителей из 2000, что составило 91% взрослых лиц. Средний возраст опрошенных соста-вил 59,56 ± 12,33 лет(женщин- 63,33%, средний возраст- 60,39 ± 14,76 лет. Мужчины составляли 36,67%.- средний возраст- 58,29 ± 14,76 лет. В процессе анкетирования было выявлено, что жалобы на боли в спине предьявляли 67,5 % опрошенных, из них женщин – 66,8%, мужчин – 68,2%( преобдадали лица старше 60 лет- 87,5% женщин и 93,9 % мужчин). Необходимо отметить, что почти у каждого четвертого(25,50%) паци-ентов с БНС определялся клинический метеопатический соединительноткан-ный синдром (КМС-синдром), проявлялсяющийся в виде жалоб общего ха-рактера- головнымим болями, астеническим синдромом, болью в суставах и\или вегето-сосудистыми(гипертоническими) кризами, которые как прави-ло, усиливались на перемену погоды, магнитные бури и\или в полнолуние, а также сопровождались искривлением позвоночника и др. аномалии ске-лета и внутренних органов и отягощенным наследственным анамнезом по заболеваниям суставов и позвоночника. Из расспроса и обследования пациентов было выявлено, что в у 60,1% лиц имел место остеохондроз позвоночника(остеоартроз позвоночника), а у 0,02%-анкилозирующий спон-дилоартрит. Выводы. Проведенное исследование распространенности синдрома боли в нижней части спины среди 2000 чел. организованной и неорганизованной популяций жителей г.Тирасполя показало, что жалобы на боли в спине пре-дьявляли 67,5 % пациентов, из них женщин – 66,8%, мужчин – 68,2%. У 60,1 пациентов имели место остеохондроз позвоночника, а у 0,02% – ан-килозирующий спондилоартрит. Причем признаки наследственной дисплазии соединительной ткани определялись почти у каждого четвертого пациента с БНС, у которых, определялся клинический метеопатический соединительнотканный синдром, проявляющийся в виде – головных болей, астеническим синдромом, артрал-гиями и болью в спине и\или вегетососудистыми(гипертоническими) кри-зами, которые как правило, усиливались на перемену погоды, магнитные бури и\или в полнолуние, а также сопровождались искривлением позвоночника и др. аномалии скелета и внутренних органов, с отягощенным наследственным анамнезом по заболеваниям суставов и позвоночника. У 60,1% пациентов имел место остеохондроз позвоночника, а у 0,02%-анкилозирующий спондилоартрит. Выявлен факт преобладания часто-ты синдрома БНС среди лиц пенсионного возраста (старше 60 лет) в Придне-стровской популяции, по сравнению средними с данными по регионам Рос-сии. Это обьясняется влиянием такого социального фактора, как безрабо-тица, связанного с кризисом и вынужденной миграцией примерно трети мужской и женской трудоспособной части населения Приднестровья на за-работки именно в Россию. Стажаров М.Ю., Бедина С.А., Мозговая Е.Э., Папичев В.А.АКТИВНОСТЬ АМИНООКСИДАЗ В КРОВИ БОЛЬНЫХ СИСТЕМНОЙ СКЛЕРОДЕРМИЕЙ
ФГБУ «НИИ КиЭР» РАМН, ГУЗ “Волгоградский областной клинический хоспис», Волгоград Цель исследования. Повышение качества диагностики активности па-тологического процесса при системной склеродермии (CCД). Материалы и методы. Под наблюдением в условиях стационара нахо-дились 25 больных, из которых 23 (92,1%) женщины. Основная часть боль-ных (68%) в возрасте от 41 до 60 лет. I степень активности патологического процесса установлена у 15 (60%) больных, II – у 10 (40%). При I степени преобладало хроническое течение (80%), при II – подострое (70%) В сыво-ротке крови по оригинальным методикам определялись активности бензила-минооксидазы (БАО), лизиламинооксидазы (ЛАО) и диаминоксидазы (ДАО). Контрольную группу составили 30 практически здоровых людей. Результаты. В сыворотке крови здоровых людей активность ЛАО (в нмоль/мг/час) составила 6,0±0,3; БАО – 5,2±0,3 и ДАО – 4,8±0,2. По срав-нению со здоровыми у больных ССД (всей группы) ниже активность всех ферментов (р<0,001); у больных ССД с I степенью активности процесса ни-же активность БАО и ЛАО (р<0,001), ДАО (р<0,01), у больных ССД с II сте-пенью ниже активность всех ферментов (р<0,001). Сравнительный ааналих показал, что у больных с I степенью, по сравнению со II, выше активность всех изученных ферментов (р<0,001). Заключение. Определение активности ЛАО, БАО и ДАО сыворотке крови больных ССД способствует выявлению минимальной активности «склеродер-мического» процесса и уточнению степени активности процесса. Стажаров М.Ю., Григорьянц С.Р., Пересыпкин В.В., Пересыпкин М.В., Бедина С.А.ЭНЗИМНЫЕ РАЗЛИЧИЯ В ЭРИТРОЦИТАХ БОЛЬНЫХ РЕАКТИВНЫМ АРТРИТОМ И ПОДАГРИЧЕСКИМ АРТРИТОМ
ФГБУ «НИИ КиЭР» РАМН Цель исследования: выявить возможность использования показателей активности гуаниндезаминазы (ГДА), гуанозиндезаминазы (ГЗДА), гуанозин-фосфорилазы (ГФ) и пуриннуклеозидфосфорилазы (ПНФ) в лизатах эритро-цитов больных реактивным артритом (РеА) и подагрическим артритом (ПА) для повышения качества дифференциации этих заболеваний. Материал и методы. Под наблюдением находились 42 больных по-дагрой с наличием артрита, из которых 39 (92,9%) мужчин и 3 (7,1%) жен-щины. Средний возраст больных (М±m) – 53,1±2,2 года, длительность бо-лезни – 11,4±1,9 лет. Интермиттирующая форма определялась у 15 (35,7%), хроническая – у 27 (64,3%) больных, полиартрит – у 23 (54,7%) больных. Группа сравнения была представлена 54 больными РеА, из которых 36 (66,7%) мужчин и 18 женщин. Средний возраст больных – 31,9±1,0 год. Длительность болезни – 9,4±0,9 месяца. Урогенная форма РеА установлена у 30 (55,6%), энтерогенная – у 24 (44,4%) больных. Активность ГДА, ГЗДА, ГФ и ПНФ в лизатах эритроцитов определялась по оригинальным методикам и выражалась в нмоль/мин/мл., содержащем до лизиса 1×109 клеток. Результаты. По сравнению со здоровыми у больных подагрой (ПА) в ли-затах эритроцитов выше активность ГДА (р<0,01), незначительно выше ГЗДА (р>0,05), ГФ (р>0,05) и ниже активность ПНФ (Р<0,001); у больных РеА выше активность ГДА (р<0,001), незначительно выше ПНФ (р>0,05), ниже активность ГЗДА (р<0,001) и ГФ (р<0,01). Сравнительные исследования показали, что у больных ПА по сравнению с больными РеА в эритроцитах выше активность ГЗДА (р<0,05), незначи-тельно выше ГДА, ГФ (все р>0,05) и ниже активность ПНФ (р<0,001). Заключение. Определение активности ПНФ и ГЗДА в лизатах эритроци-тов больных РеА и ПА в комплексе с клинико-инструментальными данными способствует дифференциации этих заболеваний. Сулейманова Г.П.ОСОБЕННОСТИ ФОРМИРОВАНИЯ ПСИХОЛОГИЧЕСКИХ ЗАЩИТНЫХ МЕХАНИЗМОВ У БОЛЬНЫХ ФИБРОМИАЛГИЕЙ ПРИ АСТЕНИЧЕСКОМ СИНДРОМЕ
ФГБУ НИИ Клинической и экспериментальной ревматологии РАМН Цель: изучить особенности формирования психологической защиты у больных фибромиалгией в зависимости от выраженности астенического син-дрома. Материалы и методы. Проведено клинико-психологическое исследова-ние у 100 больных фибромиалгией в возрасте от 24 до 51 года. При прове-дении психологического исследования использовались методики: УНП (Дмитриева Л.Л., 1990), ИЖС (Лаборатория клинической психологии Санкт-Петербургского психоневрологического института им. В.М. Бехтерева, 2005). Результаты. Как показали результаты обследования, доля лиц с клини-чески значимым уровнем астенизации (свыше 6 баллов) составила 68 %. У 28% пациентов регистрировались субклинические показатели астенического синдрома. Подавляющее большинство (65%) в анамнезе отмечали острые или хронические психотравмирующие воздействия, предшествовавшие раз-витию заболевания, либо значительно усугублявшие уже имеющуюся асте-нию. Наряду с этим, практически у всех больных фибромиалгией (92%) от-мечались постоянные психические и физические перегрузки в быту или на работе, сопровождавшиеся чувством усталости (необходимость постоянного сосредоточения внимания, выполнение множества различных дел за корот-кие сроки, вынужденное пребывание длительное время в сидячей позе). Также часто наблюдались различные вегетативные и функциональные рас-стройства: парастезии (77%), частая головная боль (89%), нарушения сна (86%), фукциональные расстройства желудочно-кишечного тракта (42%), нестойкие изменения артериального давления (55%). В целом, средние значения астении у больных фибромиалгией составили 6,72±0,17 балла. Длительность астении коррелировала с ее выраженностью (r=0,38, р=0,017). Между возрастом больных фибромиалгией и уровнем астении корреляционной взаимосвязи не обнаружено. Уровень астении пря-мо коррелировал с психологическими защитами «Вытеснение», «Регрессия», «Проекция» и «Замещение» (p<0,05). Обсуждение. Следует отметить, что изо всего спектра исследуемых пси-хологических защит перечисленный ряд представляет собой наиболее при-митивные и дезадаптивные механизмы, которые не привлекают интеллекту-альные резервы психики, всегда неосознаваемые и поведенчески деструк-тивные. Наблюдаемые фрустрирующие акценты астенического синдрома «подавляются» или «вытесняются» из сферы осознаваемого в зону бессозна-тельной психической активности. При этом выстраиваемые защитно-приспособительные механизмы актуализируют наиболее ранние и успешные в прошлом способы поведения (Регрессия), перенос агрессивных и неприемлемых тенденций на других (Проекция и Замещение). Подавляемые с помо-щью психологической защиты аффективно сильно заряженные психологиче-ские компоненты болезни способствуют дезорганизации подкорковых веге-тативно-соматических структур. Учитывая патогенетические механизмы астенических проявлений, выявленные защитные механизмы могут пред-ставлять собой объективную причину клинической дезадаптации больных с астенией, проявляясь клиническим феноменом раздражительной слабости и аутоагрессией. Таким образом, можно предположить, что астенический синдром пред-ставляет собой доминантный и сильный раздражитель для организма, спо-собный активировать эмоциональный комплекс адаптационных защитных механизмов. Включение психологической защиты направлено на ослабление внутриличностного конфликта и вторичных функциональных наслоений, вызванных соматической патологией. Эмоциональный эквивалент подавляе-мых аффективно заряженных компонентов болезни находит свое выражение в парадоксальном усилении психосоматического напряжения, приводя к по-вторной активизации психологических “защитных” сил организма, действие которых направлено на нейтрализацию эмоционального напряжения. Подоб-ные «психосоматические спирали» всегда будут носить деструктивный ха-рактер для психики, поскольку пополнение ресурсов защиты возможно лишь за счет деформации личности. И вот уже возникает потребность в “защите от защиты” – сохранении личности через преодоление психологической защи-ты. Это, в свою очередь, требует новых энергетических затрат и психологи-ческих жертв, что может ухудшать, в нашем случае, течение астенического процесса. Выводы. У больных фибромиалгией для нормализации эмоционального состояния, действенной переработки психологического конфликта, повыше-ния коммуникативного, интрапсихического и соматического самоконтроля пациентов помимо фармакологических методов лечения необходимо реко-мендовать применение групповой психотерапии, гештальттерапии, релакси-рующих техник, биологической обратной связи. Хабижанова В.Б.МАРКЕРЫ ВОСПАЛЕНИЯ ПРИ ПОДАГРЕ
Казахский национальный медицинский университетимени С.Д.Асфендиярова, Алматы, Республика Казахстан В последние десятилетия все большая роль отводится воспалительным реакциям в развитии атеросклероза. Изучение маркеров воспаления, явля-ющимися предикторами кардиоваскулярных катастроф в популяции, а также отражающими активность хронического воспалительного процесса при рев-матических заболеваниях (в том числе и подагре), является объектом науч-ных исследований. Цель исследования: Изучение связи маркеров воспаления (СОЭ и С-реактивного белка) с проявлениями подагрического артрита и сопутствую-щей патологией у больных подагрой. Материалы и методы: Обследовано 218 больных подагрой с достовер-ным диагнозом по критериям S.L. Wallace (рекомендованных АRA в 2001 го-ду), жители Алматы. Среди больных было 188 (86,2%) мужчин и 30 (13,8%) женщин, сопоста-вимых по возрасту (56,0±0,88 и 60,37±1,53, соответственно). Средняя дли-тельность болезни на момент обращения – 9,97±0,61 лет. Всем больным про-водилось клинико-лабораторное обследование, биохимические исследования крови с определением уровня мочевой кислоты, липидов и глюкозы натощак. С-реактивный белок (СРБ) определялся методом латекс-агглютинацией. Полученные результаты: Средний уровень СОЭ у больных подагрой составил 21,36±0,99 мм/ч, медиана и интерквартильный размах СОЭ – 18 [10; 30,75]. У 51 (23,4%) больных уровень СОЭ был ниже 10 мм/ч, у большинства больных 61 (28,0%) – СОЭ от 10 до 20 мм/ч, у 41 (18,8%) – от 20 до 30 мм/ч, у 33 (15,1%) – от 30 до 40, у 22 (10,1%) – от 40 до 50, у 10 (4,6%) – более 50 мм/ч. Уровень СРБ белка у обследованных больных составил 10,58±1,38 мг/мл, медиана 6 [0; 11,05]. Больных подагрой с отрицательным результатом СРБ (менее 6 мг/мл) было 65 (29,8%). У большинства больных 153 (71,2%) уровень СРБ составил более 6 мг/мл. Нами изучена связь уровня СОЭ и СРБ с характером и течением подагри-ческого артрита. Средние значения СОЭ достоверно были выше при хроническом течении подагры, составляя 25,03±1,44 мм/ч, чем при рецидивирующем – 18,02±1,30 (р<0,05). Также уровень СРБ при хроническом течении подагры был выше, чем при рецидивирующем (11,78±2,33 и 9,49±1,59 мг/мл, соответственно), хотя без существенной разницы (p<0,1). При затяжном варианте артрита значения СОЭ были выше, чем при остром (19,98±1,67 и 14,80±2,02 мм/ч соответственно, р<0,05). Тогда как при остром варианте подагрического артрита концентрация СРБ была сопоставима с затяжным (10,23±2,66 мг/мл и 9,04±2,01, р=0,8). Нами также изучена связь маркеров воспаления с основными клиническими характеристиками подагры. Так, значения СОЭ коррелировали с возрастом больных, количеством пораженных суставов как на момент обследования, так и за время болезни, частотой артрита (R=0,23, р<0,05). СРБ также имел корреляционную связь с этими характеристиками заболевания, хотя слабовыраженную (R=0,06, р<0,1). Влияние сопутствующей патологии у больных подагрой на уровень изучаемых показателей представлено в таблице 1. Как видно из таблицы 1, при наличии ИБС и ХПН уровень СОЭ был достоверно выше, чем у больных без указанной патологии (20 [10; 32], 25 [10; 37,75] напротив 12 [6,5; 24], 17 [9,75; 28,25] соответственно, р<0,05). Особенно существенно отличался уровень СОЭ в зависимости от наличия АГ. У больных с АГ уровень СОЭ в 2 раза был выше, чем при отсутствии – 20 [10;31] и 10 [5; 16,25]. Наличие СД 2 типа у больных подагрой на показатели СОЭ особо не влияли. Таблица 1. Показатели медиаторов воспаления у больных подагрой с сопутствующей патологией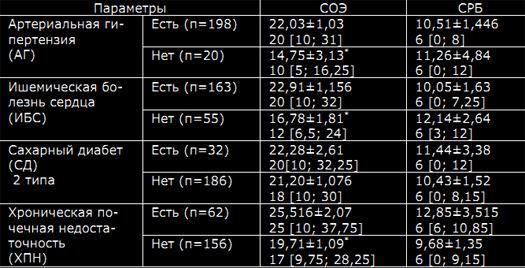 Нами не было выявлено связи уровня СРБ с сопутствующей патологией (АГ, ИБС, СД 2 типа), кроме ХПН. У больных с ХПН концентрация СРБ соста-вила 12,85±3,515 или 6 [6; 10,85] мг/мл, тогда как у больных без нее – 9,68±1,35 или 6 [0; 9,15] (р<0,1).
Обсуждение: Уровни СОЭ и СРБ зависели от характера и течения артрита, т.е. от выраженности воспалительных явлений. При хроническом течении подагры показатели СРБ были незначительно выше (р<0,1), а значения СОЭ достоверно выше (р<0,05), чем при рецидивирующем. Повышение уровня маркеров воспаления связано с увеличением длительности (при хроническом течении) асептического воспаления в суставах, возникающего как реакция на преципитацию микрокристаллов урата. В полученных нами результатах исследования выявлена корреляция изучаемых показателей, особенно СОЭ, с возрастом больных, количеством пораженных суставов как на момент об-следования, так и за время болезни, частотой артрита (R=0,23, р<0,05). При сопутствующей патологии – АГ, ИБС у больных подагрой показатели СОЭ и СРБ были выше, что связано с влиянием хронического иммунного воспале-ния на выраженность атеросклеротического процесса.
Выводы: Показатели СОЭ и СРБ у больных подагрой могут считаться маркерами воспаления. СРБ, а также СОЭ, отражают течение хронического воспалительного процесса при подагре и являются маркерами атеросклероза. Их уровень коррелирует с тяжестью подагры и развитием АГ, ИБС, про-грессированием почечной недостаточности.
Харченко С.А., Грехов Р.А., Бондаренко Е.А.
Нами не было выявлено связи уровня СРБ с сопутствующей патологией (АГ, ИБС, СД 2 типа), кроме ХПН. У больных с ХПН концентрация СРБ соста-вила 12,85±3,515 или 6 [6; 10,85] мг/мл, тогда как у больных без нее – 9,68±1,35 или 6 [0; 9,15] (р<0,1).
Обсуждение: Уровни СОЭ и СРБ зависели от характера и течения артрита, т.е. от выраженности воспалительных явлений. При хроническом течении подагры показатели СРБ были незначительно выше (р<0,1), а значения СОЭ достоверно выше (р<0,05), чем при рецидивирующем. Повышение уровня маркеров воспаления связано с увеличением длительности (при хроническом течении) асептического воспаления в суставах, возникающего как реакция на преципитацию микрокристаллов урата. В полученных нами результатах исследования выявлена корреляция изучаемых показателей, особенно СОЭ, с возрастом больных, количеством пораженных суставов как на момент об-следования, так и за время болезни, частотой артрита (R=0,23, р<0,05). При сопутствующей патологии – АГ, ИБС у больных подагрой показатели СОЭ и СРБ были выше, что связано с влиянием хронического иммунного воспале-ния на выраженность атеросклеротического процесса.
Выводы: Показатели СОЭ и СРБ у больных подагрой могут считаться маркерами воспаления. СРБ, а также СОЭ, отражают течение хронического воспалительного процесса при подагре и являются маркерами атеросклероза. Их уровень коррелирует с тяжестью подагры и развитием АГ, ИБС, про-грессированием почечной недостаточности.
Харченко С.А., Грехов Р.А., Бондаренко Е.А.
ОСОБЕННОСТИ ПСИХОСОМАТИЧЕСКИХ СООТНОШЕНИЙ ПРИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКЕ
ФГБУ «НИИ КиЭР» РАМН, Волгоград Изучение психосоматических соотношений при системной красной вол-чанке (СКВ) относится к актуальным направлениям современной ревматоло-гии. Перспектива исследований в этом направлении связана в первую оче-редь с изучением личностных особенностей и типов реагирования пациентов на болезнь, форм психологической защиты и компенсации. Поскольку тя-жесть заболевания, быстрое снижение функциональных способностей, воз-растание физического дискомфорта, а также необходимость постоянного приема лекарственных препаратов приводит больных СКВ к ощущению по-тери контроля над заболеванием, утрате профессиональной независимости и способности осуществлять важные для пациента виды деятельности, психо-логическим нарушениям: снижению самооценки и уверенности в себе, не-удовлетворенности своим образом жизни, к развитию беспокойства, враж-дебности, агрессивности и депрессии. Этот факт и, как правило, негативная информированность больных о характере болезни и ее прогнозе, делают общение с ними чрезвычайно ответственным и напряженным. Целью работы являлось изучение психосоматических соотношений, ин-тегрирующих отдельные свойства личности больных СКВ, особенностей их личностно-средового взаимодействия и защитно-приспособительных меха-низмов. Под наблюдением находилось 87 пациентов с СКВ, среди которых подав-ляющее большинство составили женщины (82,8%) в возрасте от 16 до 70 лет (средний возраст составил 35,33 ± 1,77 года). С помощью серии психодиа-гностических методик определялись выраженность астении, депрессии, тревоги, ипохондрии, уровень субъективного контроля, типы реагирования на болезнь и напряженность спектра механизмов психологических защит (ПЗ), их взаимосвязи. В результате проведенного статистического анализа массива полученных данных возможно предположить следующую модель психосоматических со-отношений. Исходным моментом является осознание имеющегося внутриличностного конфликта, связанного с фактом заболевания и непринятия ответственности за происходящее на себя (экстернальность в сферах Ио, Ин (3,63 ± 0,34 балла), Ип (3,42 ± 0,21), Им и особенно в Из (3,31 ± 0,32). Депрессия (4,47 балла) и тревога (5,57 баллов), как атрибут психологического конфликта, включает в действие механизмы психологической защиты, действующие «широким фронтом» (за счет их большой напряженности – «блок психологических защит» (H) (86,5 ± 1,9 баллов) – (E) (76,8 ± 2,9) – (C) (64,8 ± 3,2), либо избирательно за счет их ассоциированности с отдельными психологическими характеристиками). Исходом является формирование определенной «внутренней концепции болезни» в составе внутренней картины болезни (ВКБ) в виде недостатков «обученной беспомощности». Регу-лятивная система стабилизации личности, один из уровней которой составляют механизмы психологической защиты, в целях уменьшения невротических проявлений включает другие работающие у индивида защитно-приспособительные механизмы (в нашем случае – «Компенсация», «Замещение»). Итогом их работы должно являться достижение адекватного уровня защитно-приспособительного реагирования во всех сферах отношений лич-ности больных, в том числе и в виде формирования определенных типов отношения к болезни. Конкретный спектр этих типов определяется профилем используемых индивидом ПЗ и их напряженностью, во-первых, и выраженностью определенных систем личностных характеристик, во-вторых. При СКВ определяются дезадаптивные типы отношения к заболеванию. Возможно, что исходные беспокоящие клинико-психологические феномены, связанные с заболеванием и познавательной сферой пациентов, первоначально находят свое отражение в ВКБ в виде эмоциональных (тревога, депрессия, снижение самооценки), мотивационных (уменьшение попыток заниматься повседневной деятельностью) и когнитивных (неэффективность попыток выработать новую адаптивную модель поведения) недостатков «обученной беспомощности», трансформируются под влиянием защитно-приспособительных механизмов и потом отражаются в непосредственном поведении больных СКВ (несоблюдение режима лечения, избыточный прием медикаментов). Таким образом, выявленные нами взаимосвязи во внутренней картине заболевания и в их личностных характеристиках (участвующих определенным образом в формировании механизмов реагирования на болезнь) могут оказаться важными при изучении пато- и психогенеза хронических заболеваний, в частности, внутренних конфликтов личности и механизмов их переработки.



